En Cataluña, el sistema público de sanidad solo financia la vacunación antineumocócica en pediatría a niños con condiciones de riesgo. El objetivo del estudio fue determinar la cobertura de dicha vacunación y su asociación con la edad, factores sociodemográficos y otras variables.
Material y métodoEstudio descriptivo transversal de los niños de 2 meses a 15 años de edad, asignados a los centros de atención primaria de Cataluña, y con enfermedades para las que el programa oficial de vacunas indica la vacunación antineumocócica. La información sobre el estado vacunal y las variables en estudio se recogió a partir de los datos registrados en la historia clínica electrónica de los equipos de atención primaria. Se analizó la asociación de la vacunación antineumocócica con variables demográficas y médicas mediante un análisis bivariado y un modelo de regresión logística múltiple, utilizando como medida de asociación la odds ratio ajustada (ORa), con su intervalo de confianza al 95%.
ResultadosLa cobertura vacunal fue del 47,7%. Las variables asociadas a la vacunación fueron: edad (ORa: 9,2 [7,9-10,7] en niños de 2 meses a 2 años; ORa: 8,1 [7,0-9,3] en niños de 3-5 años; ORa: 4,6 [4,0-5,2] en niños de 6-11 años), nacionalidad española (ORa: 3,9 [3,5-4,3]), inmunización correcta según el calendario de vacunación sistemática (ORa: 2,5 [2,1-3,0]), y número de condiciones de riesgo (ORa: 3,2 [2,5-4,1] en niños con 2 o más condiciones).
ConclusionesLa cobertura vacunal frente a neumococo en niños con condiciones de riesgo es baja en Cataluña. Es necesario implementar estrategias para aumentar la cobertura.
The public health system in Catalonia only funds pneumococcal vaccination in paediatrics for children at-risk. The aim of this study was to determine pneumococcal vaccination coverage and its association with age, sociodemographic factors and other variables.
Material and methodDescriptive cross-sectional study of children aged between 2 months and 15 years old assigned to primary care centres in Catalonia and with diseases that are included for pneumococcal vaccine in the official vaccination program. The information on vaccination status and study variables were obtained from data registered in the electronic medical records in the primary care centres. An analysis was made of the association between pneumococcal vaccination and demographic and medical variables using bivariate analysis and a multiple logistic regression model. The adjusted odds ratio (aOR), with a confidence interval of 95%, was used to measure the relationships.
ResultsPneumococcal vaccination coverage was 47.7%. Variables which predicted pneumococcal vaccination were: age (aOR: 9.2 [7.9-10.7] in children 2 months-2 years old; aOR 8.1 [7.0-9.3] in children 3-5 years; aOR: 4.6 [4.0-5.2] in children 6-10 years), Spanish nationality (aOR: 3.9 [3.5-4.3]), correct immunisation according to systematic immunisation schedule (aOR: 2.5 [2.1-3.0]), and number of risk conditions (aOR: 3.2 [2.5-4.1] in children with 2 or more conditions).
ConclusionsPneumococcal vaccination coverage in children with risk conditions is low in Catalonia. Strategies need to be implemented to increase coverage.
Streptococcus pneumoniae es una causa importante de morbimortalidad. A nivel mundial, se ha estimado que se producen 1,6 millones de muertes anuales por enfermedad neumocócica1, de las cuales 541.000 se dan en niños menores de 5 años2.
La vacunación antineumocócica ha sido clave en la disminución de la morbilidad por esta infección, en especial por enfermedad neumocócica invasiva3–8.
En Estados Unidos, la vacuna antineumocócica conjugada se incluyó en el calendario de vacunación sistemática infantil en el año 2000, y actualmente se recomienda a todos los niños de 2 a 59 meses y a los mayores de esta edad con enfermedades de base9. En Europa10 hay una gran variabilidad en cuanto a las estrategias vacunales: algunos países la han incluido en su calendario vacunal infantil, como Inglaterra11, Alemania12 y Francia13, mientras otros la recomiendan solo en los grupos de riesgo. En España, la vacuna actualmente solo está incluida de forma sistemática en el calendario vacunal infantil de Galicia14. En Cataluña, y desde 200115,16, el programa oficial de vacunaciones restringe la financiación de la vacuna antineumocócica conjugada a los niños con ciertas enfermedades crónicas de base: hemoglobinopatías, asplenia anatómica o funcional, cardiopatías, enfermedad respiratoria crónica, diabetes mellitus, fístula de líquido cefalorraquídeo, inmunodeficiencias congénitas o adquiridas, insuficiencia renal o síndrome nefrótico y en pacientes portadores de implante coclear. La vacuna polisacárida 23-valente también está financiada por el sistema público de salud para los niños con estas enfermedades a partir de los 2 años de edad.
El objetivo de este estudio es determinar la cobertura vacunal frente a neumococo en niños con enfermedades crónicas de riesgo en Cataluña y determinar las variables asociadas a la vacunación.
Material y métodosDiseño y ámbitoEstudio descriptivo transversal de ámbito poblacional. Se incluyen todos los pacientes pediátricos asignados a los Equipos de Atención Primaria (EAP) de Cataluña del Institut Català de la Salut (ICS).
Población y criterios de selecciónSe seleccionaron para su inclusión en el estudio los niños que a fecha de 1 de julio de 2012 tuvieran una edad comprendida entre 2 meses (edad mínima para la administración de la vacuna antineumocócica conjugada) y 15 años, y que presentaran una o más enfermedades crónicas de base para las que la vacunación antineumocócica estuviera financiada15.
Variables estudiadasSe recogió información a partir de la historia clínica electrónica de los centros de atención primaria (AP) sobre las siguientes variables:
- -
Variables demográficas: género, edad (categorizada en los siguientes estratos: 2 meses-2 años; 3-5 años; 6-10 años y≥11 años) y nacionalidad.
- -
Variables médicas: número de visitas al pediatra o al médico de AP en los 6 meses anteriores a la fecha del estudio (1 de julio de 2012), inmunización adecuada según el calendario vacunal de Cataluña, y tipo y número de condiciones de base de riesgo (categorizadas a partir de los diagnósticos CIE-10 en los siguientes grupos: enfermedad respiratoria crónica; cardiopatía; inmunosupresión [tratamiento con corticoides o fármacos inmunosupresores, trastorno inmunológico o neoplasia]; trastorno neuromuscular [incluidas las fistulas de líquido cefalorraquídeo]; diabetes mellitus; síndrome de Down; nefropatía; hepatopatía; asplenia anatómica o funcional; y trastorno de la sangre [hemoglobinopatía, anemia de células falciformes]). Entre los trastornos respiratorios crónicos se ha excluido el asma porque no se incluye en las indicaciones de vacunación antineumocócica infantil financiadas por el sistema público de salud en Cataluña15.
- -
Variables relacionadas con la vacunación antineumocócica: tipo de vacuna (7-valente, 10-valente, 13-valente o 23-valente) y número de dosis recibidas. Se consideraron como vacunados los niños que hubieran recibido al menos una dosis de cualquier vacuna antineumocócica a fecha de 1 de julio de 2012.
Los datos se han obtenido a partir del Sistema de Información para el Desarrollo de la Investigación en Atención Primaria17. Son datos anónimos procedentes de los registros de la historia clínica electrónica. Este registro incluye datos de todos los niños asignados a los EAP de Cataluña del ICS.
Aspectos éticosLos datos a los que se tuvo acceso fueron en todo momento anonimizados, sin datos personales identificativos (nombre y apellidos, dirección, teléfono, centro de salud al que pertenecían, número de tarjeta sanitaria, etc.). Como referencia para cada caso solo se disponía de un número hash encriptado por el Sistema de Información para el Desarrollo de la Investigación en Atención Primaria. Por tanto, se preservó en todo momento la confidencialidad de los datos. En cuanto a los sujetos del estudio, este en ningún momento supuso ningún riesgo ni ninguna molestia para ellos (visitas, pruebas o siquiera una recogida de datos complementarios a los ya obtenidos en la historia clínica). Con todo ello, el Comité Ético de Investigación Clínica competente para evaluar el proyecto, perteneciente al Instituto de Investigación en Atención Primaria Jordi Gol, dio su aprobación al mismo.
Análisis estadísticoSe realizó un análisis descriptivo univariado de las variables en estudio. Las variables cualitativas se definieron para cada categoría con el número absoluto y el porcentaje. Las variables cuantitativas se sometieron a pruebas de normalidad (gráficos P-P y Q-Q, prueba de Kolmogorov-Smirnov); las que seguían una distribución normal se describieron con la media y la desviación estándar, y aquellas que no cumplieran criterios de normalidad, con la mediana y el rango intercuartílico (RIC).
Se realizó un análisis bivariado para la comparación del grupo de niños vacunados con el de los no vacunados y su asociación con las variables en estudio. Para ello se utilizó la prueba de Chi-cuadrado de Pearson (para las variables ordinales con más de 2 categorías se usó la Chi-cuadrado de tendencia lineal, ajustando el valor p con la corrección de Bonferroni); cuando no cumplían los requisitos para la aplicación de la prueba de Chi-cuadrado se usaron las pruebas exactas. Como medida de asociación se calcularon las odds ratio con su intervalo de confianza al 95% (IC 95%); se consideró como variable dependiente la vacunación antineumocócica, y como variables independientes, las variables sociodemográficas y médicas mencionadas.
Posteriormente se realizó un análisis multivariado con modelos de regresión logística múltiple, utilizando como variable dependiente la vacunación antineumocócica y como variables independientes las que hubieran resultado estadísticamente significativas en el análisis bivariado, y se calculó la odds ratio ajustada (ORa). En el modelo de regresión múltiple se investigó la significación estadística de los términos de interacción, y se estimaron modelos específicos para las condiciones de riesgo más prevalentes.
Se consideraron estadísticamente significativos valores de p inferiores a 0,05. Todos los análisis estadísticos se han realizado con el paquete de programas estadísticos SPSS® versión 18.
ResultadosEl total de niños de 2 meses a 15 años registrados en la base de datos de AP era de 904.682, de los cuales se incluyeron 16.405 (1,8%) con enfermedades crónicas de base de riesgo para enfermedad neumocócica.
La mediana de edad de los niños seleccionados para el estudio fue de 7,8 años (RIC 6,8), y el 53,7% eran varones (tabla 1). El 75% eran de nacionalidad española.
Características de la población en estudio (n=16.405)
| n | % | |
|---|---|---|
| Género | ||
| Femenino | 7.588 | 46,3 |
| Masculino | 8.817 | 53,7 |
| Grupos de edad | ||
| 2 meses-2 años | 2.597 | 15,8 |
| 3-5 años | 3.523 | 21,5 |
| 6-10 años | 6.061 | 36,9 |
| ≥11 años | 4.224 | 25,7 |
| Nacionalidada | ||
| Española | 7.964 | 75,0 |
| Otras | 2.649 | 25,0 |
| Vacunación antineumocócica | ||
| Sí | 7.831 | 47,7 |
| No | 8.574 | 52,3 |
| Número de dosis recibidas (el porcentaje es sobre los vacunados) | ||
| 1 | 1.196 | 15,3 |
| 2 | 1.450 | 18,5 |
| 3 | 1.810 | 23,1 |
| 4 | 2.961 | 37,8 |
| 5 o más | 414 | 5,3 |
| Tipo de vacuna (el porcentaje es sobre los vacunados) | ||
| 7-valente | 5.875 | 75,0 |
| 10-valente | 152 | 1,9 |
| 13-valente | 2.160 | 27,6 |
| 23-valenteb | 805 | 11,8 |
| Inmunización correcta según el calendario sistemáticoc | ||
| Sí | 14.639 | 92,3 |
| No | 1.227 | 7,7 |
| Número de visitas al médico de AP | ||
| 0 | 3.642 | 22,2 |
| 1 | 2.738 | 16,7 |
| 2 | 2.368 | 14,4 |
| 3 o 4 | 3.396 | 20,7 |
| 5 o más | 4.261 | 26,0 |
| Número de condiciones de riesgo | ||
| 1 | 15.834 | 96,5 |
| 2 o más | 571 | 3,5 |
| Condiciones de riesgo | ||
| Cardiopatía | 6.121 | 37,3 |
| Inmunosupresión de cualquier tipo | 2.825 | 17,2 |
| Trastorno neuromuscular (incluida fístula LCR) | 2.237 | 13,6 |
| Enfermedad respiratoria crónica | 1.807 | 11,0 |
| Hemoglobinopatía o anemia | 1.606 | 9,8 |
| Diabetes | 1.247 | 7,6 |
| Síndrome de Down | 495 | 3,0 |
| Nefropatía | 355 | 2,2 |
| Hepatopatía | 302 | 1,8 |
| Asplenia | 6 | 0,0 |
Para la variable «Nacionalidad» no se dispone de información en 5.792 niños (35,3% del total de niños incluidos en el estudio).
El 96,5% de los niños (n=15.834) padecían solo una de las enfermedades de base de riesgo consideradas en el estudio, y la cardiopatía era la más frecuente (6.121 niños; 37,3%), seguida por la inmunosupresión (2.825 niños; 17,2%) (tabla 1). Estaban correctamente inmunizados por edad, según el calendario de vacunación sistemática, 14.639 niños (92,3%).
Habían recibido alguna dosis de vacuna antineumocócica 7.831 niños (cobertura vacunal del 47,7%). La mediana de dosis recibidas fue de 3 (RIC 2). En cuanto al tipo de vacuna, el 75% de los niños vacunados (n=5.875) había recibido al menos una dosis de la vacuna 7-valente, el 1,9% (n=152) había recibido alguna dosis de la vacuna 10-valente, el 27,6% (n=2.160) había recibido alguna dosis de la vacuna 13-valente, y el 11,8% de los niños vacunados mayores de 2 años (n=805) había recibido al menos una dosis de vacuna 23-valente. La vacuna 7-valente se administró mayoritariamente (85,2%) en los niños de edades comprendidas entre los 3 y los 10 años, las vacunas 10-valente y 13-valente en aquellos de 2 meses a 5 años (93,4 y 97,7%, respectivamente), y la vacuna 23-valente en los de 6 o más años (90,9%).
En los 6 meses anteriores, la mediana de visitas realizadas por los niños del estudio al médico de AP (pediatra o médico de cabecera) fue de 2 (RIC 4), y 12.763 niños (77,8%) se habían visitado al menos una vez.
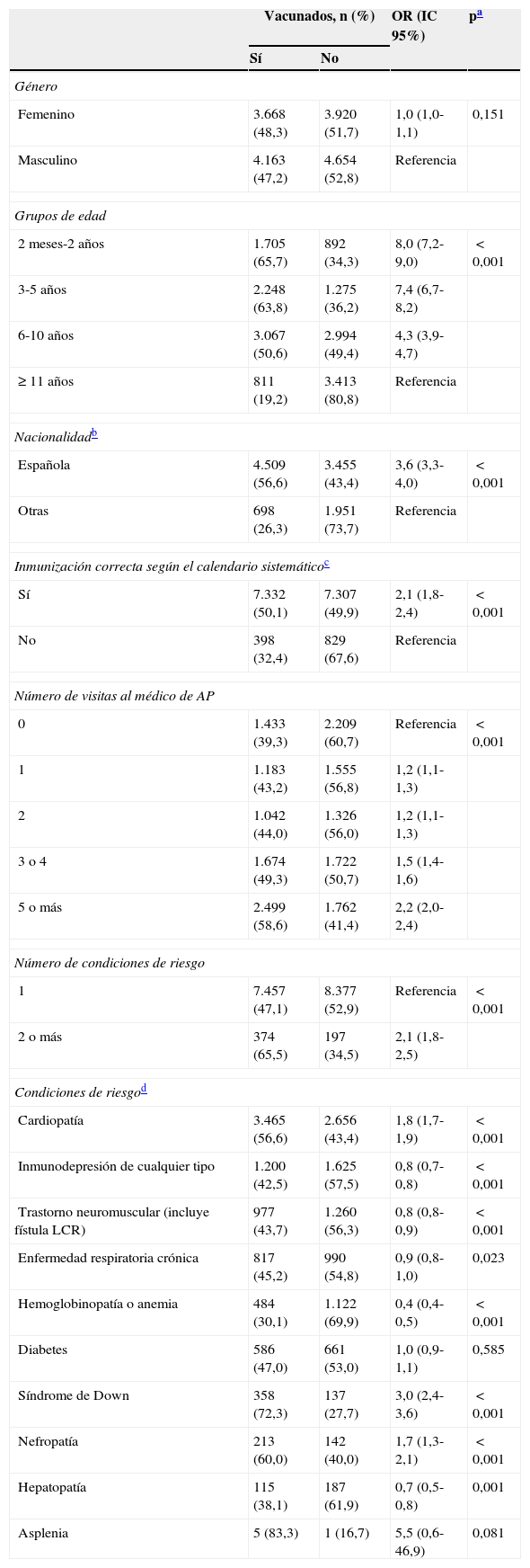
En la tabla 2 se muestran los resultados correspondientes al análisis bivariado. Las variables grupo de edad, nacionalidad, inmunización correcta según el calendario sistemático, número de visitas al médico de AP, número y tipo de condiciones de riesgo se asociaron de forma estadísticamente significativa con la vacunación antineumocócica.
Variables asociadas a la vacunación antineumocócica. Análisis bivariado (n=16.405)
| Vacunados, n (%) | OR (IC 95%) | pa | ||
|---|---|---|---|---|
| Sí | No | |||
| Género | ||||
| Femenino | 3.668 (48,3) | 3.920 (51,7) | 1,0 (1,0-1,1) | 0,151 |
| Masculino | 4.163 (47,2) | 4.654 (52,8) | Referencia | |
| Grupos de edad | ||||
| 2 meses-2 años | 1.705 (65,7) | 892 (34,3) | 8,0 (7,2-9,0) | <0,001 |
| 3-5 años | 2.248 (63,8) | 1.275 (36,2) | 7,4 (6,7-8,2) | |
| 6-10 años | 3.067 (50,6) | 2.994 (49,4) | 4,3 (3,9-4,7) | |
| ≥11 años | 811 (19,2) | 3.413 (80,8) | Referencia | |
| Nacionalidadb | ||||
| Española | 4.509 (56,6) | 3.455 (43,4) | 3,6 (3,3-4,0) | <0,001 |
| Otras | 698 (26,3) | 1.951 (73,7) | Referencia | |
| Inmunización correcta según el calendario sistemáticoc | ||||
| Sí | 7.332 (50,1) | 7.307 (49,9) | 2,1 (1,8-2,4) | <0,001 |
| No | 398 (32,4) | 829 (67,6) | Referencia | |
| Número de visitas al médico de AP | ||||
| 0 | 1.433 (39,3) | 2.209 (60,7) | Referencia | <0,001 |
| 1 | 1.183 (43,2) | 1.555 (56,8) | 1,2 (1,1-1,3) | |
| 2 | 1.042 (44,0) | 1.326 (56,0) | 1,2 (1,1-1,3) | |
| 3 o 4 | 1.674 (49,3) | 1.722 (50,7) | 1,5 (1,4-1,6) | |
| 5 o más | 2.499 (58,6) | 1.762 (41,4) | 2,2 (2,0-2,4) | |
| Número de condiciones de riesgo | ||||
| 1 | 7.457 (47,1) | 8.377 (52,9) | Referencia | <0,001 |
| 2 o más | 374 (65,5) | 197 (34,5) | 2,1 (1,8-2,5) | |
| Condiciones de riesgod | ||||
| Cardiopatía | 3.465 (56,6) | 2.656 (43,4) | 1,8 (1,7-1,9) | <0,001 |
| Inmunodepresión de cualquier tipo | 1.200 (42,5) | 1.625 (57,5) | 0,8 (0,7-0,8) | <0,001 |
| Trastorno neuromuscular (incluye fístula LCR) | 977 (43,7) | 1.260 (56,3) | 0,8 (0,8-0,9) | <0,001 |
| Enfermedad respiratoria crónica | 817 (45,2) | 990 (54,8) | 0,9 (0,8-1,0) | 0,023 |
| Hemoglobinopatía o anemia | 484 (30,1) | 1.122 (69,9) | 0,4 (0,4-0,5) | <0,001 |
| Diabetes | 586 (47,0) | 661 (53,0) | 1,0 (0,9-1,1) | 0,585 |
| Síndrome de Down | 358 (72,3) | 137 (27,7) | 3,0 (2,4-3,6) | <0,001 |
| Nefropatía | 213 (60,0) | 142 (40,0) | 1,7 (1,3-2,1) | <0,001 |
| Hepatopatía | 115 (38,1) | 187 (61,9) | 0,7 (0,5-0,8) | 0,001 |
| Asplenia | 5 (83,3) | 1 (16,7) | 5,5 (0,6-46,9) | 0,081 |
El valor p corresponde a la prueba de Chi-cuadrado de Pearson (para aquellas con más de 2 categorías, la Chi-cuadrado de tendencia lineal, ajustada por la corrección de Bonferroni), excepto en la variable «Asplenia», en la que ha sido necesario por razones de tamaño utilizar el test exacto de Fisher.
Para la variable «Nacionalidad» no se dispone de información en 5.792 niños (el 35,3% del total de niños incluidos en el estudio).
Se realizó un modelo de regresión logística global y uno para las 2 condiciones de riesgo más prevalentes (cardiopatía e inmunosupresión). No se encontraron desviaciones importantes entre las OR del análisis bivariado y las obtenidas en los diferentes modelos generados. Por este motivo, solo se presenta el modelo global de regresión logística.
El número de visitas médicas al centro de AP realizadas en los 6 meses previos al momento del estudio se asoció significativamente a la vacunación antineumocócica en el análisis bivariado, pero no en los modelos de regresión logística para las distintas condiciones de riesgo. Teniendo en cuenta que algunas de estas condiciones se atienden más en el hospital que en AP, se consideró que la relevancia de esta variable no era suficiente como para introducirla en el modelo de regresión logística global.
En la tabla 3 se muestran los resultados del análisis multivariado. La nacionalidad española (ORa: 3,9; IC 95%: 3,5-4,3) y la inmunización correcta según el calendario sistemático (ORa: 2,5; IC 95%: 2,1-3,0) se asociaron de forma independiente a la vacunación antineumocócica; la edad se asoció de forma inversa: ORa de 9,2 (IC 95%: 7,9-10,7) en los niños de 2 meses a 2 años (respecto a los mayores de 10 años); de 8,1 (IC 95%: 7,0-9,3) de 3-5 años, y de 4,6 (IC 95%: 4,0-5,2) en los de 6-10 años. La probabilidad de estar vacunado se asoció de forma directa con el número de enfermedades de base: ORa de 3,2 (IC 95%: 2,5-4,1) para los niños con 2 o más condiciones de riesgo.
Factores asociados a vacunación antineumocócica. Análisis multivariable
| ORa (IC 95%) | p | |
|---|---|---|
| Grupos de edad | ||
| 2 meses-2 años | 9,2 (7,9-10,7) | <0,001 |
| 3-5 años | 8,1 (7,0-9,3) | <0,001 |
| 6-10 años | 4,6 (4,0-5,2) | <0,001 |
| ≥11 años | Referencia | |
| Nacionalidada | ||
| Española | 3,9 (3,5-4,3) | <0,001 |
| Otras | Referencia | |
| Inmunización correcta según el calendario sistemáticob | ||
| Sí | 2,5 (2,1-3,0) | <0,001 |
| No | Referencia | |
| Número de condiciones de riesgo | ||
| 1 | Referencia | |
| 2 o más | 3,2 (2,5-4,1) | <0,001 |
Se han introducido en el modelo aquellas variables que en el análisis bivariado han demostrado tener una asociación estadísticamente significativa con la vacunación antineumocócica.
La cobertura vacunal frente a neumococo en los niños entre 2 meses y 15 años con condiciones de riesgo en Cataluña fue del 47,7%. Esta cifra es inferior a la descrita en la literatura; en un estudio realizado en Tarragona, Effectiveness of Pneumococcal and Influenza Vaccines (EPIVAC), del Instituto de Investigación en Atención Primaria Jordi Gol, que incluyó a 521 niños, de los cuales 59 presentaban factores de riesgo de infección neumocócica, la cobertura observada fue del 64,4%18. Esta diferencia podría explicarse por el hecho de que en el estudio EPIVAC los criterios de selección se centraban en niños hasta 10 años y que habían sido visitados en AP; si en nuestro estudio se seleccionan los niños que cumplen estos criterios, la cobertura vacunal obtenida es del 59,4%, más similar a la del estudio EPIVAC.
En el estudio italiano Indagine di COpertura vaccinale NAzionale nei bambini e negli adolescenti –ICONA– de 2008, la cobertura de vacunación antineumocócica en niños con factores de riesgo entre 12 y 24 meses fue de 48,9% (IC 95%: 42,3-55,4), algo inferior a la obtenida en el presente estudio para los niños de 2 meses a 2 años (65,7%). En los adolescentes de 15 años con factores de riesgo la cobertura vacunal fue de un 0,3% (IC 95%: 0-1,0), bastante inferior al 19,2% de cobertura obtenido en este estudio para los niños de 11 a 15 años19.
Un aspecto a considerar es que se ha escogido como criterio de vacunación antineumocócica el que se haya recibido al menos una dosis de cualquiera de las vacunas. Los motivos que justifican esta decisión se basan en que el número de dosis indicadas depende no solo de la edad del niño, sino también del momento en el que se le diagnostique la condición de riesgo, del tipo de vacuna administrada, y de las pautas de adaptación entre la vacuna 7-valente y la 10 o la 13-valentes. Sorprende que a pesar de que esta opción pueda sobrestimar el número de niños correctamente vacunados (ya que en esta categoría se han incluido también los niños con pautas incompletas de vacunación), la cobertura obtenida en este estudio sea tan baja, sobre todo teniendo en cuenta que en Cataluña esta vacuna está financiada por el sistema público de salud en los niños con condiciones de riesgo. Otro dato a tener en cuenta es que la cobertura para la vacuna antineumocócica polisacarídica 23-valente en el presente estudio ha sido solo del 11,8%, bastante más baja que la cobertura de la vacuna conjugada 7-valente (75%) y que la más reciente vacuna conjugada 13-valente (27,6%). En cuanto a la distribución de las vacunas por edades, la 23-valente (que solo está indicada a partir de los 2 años de edad) se administra sobre todo en los niños mayores, y la 7-valente principalmente en niños a partir de 3 años, lo cual se explica porque estos últimos años esta vacuna ha ido sustituyéndose por la 10 y la 13-valentes, que, por tanto, se dan sobre todo en los niños más pequeños.
En el presente estudio se observó que la gran mayoría de los niños que presentan condiciones de riesgo estaban correctamente inmunizados según el calendario sistemático de Cataluña. Entre los que habían visitado a su médico de AP al menos una vez en los 6 meses anteriores (n=12.763), no se aprovechó la oportunidad para la inmunización antineumocócica en casi el 50% de los casos. Aunque la enfermedad de riesgo más frecuente fue la cardiopatía, las coberturas vacunales frente a neumococo más elevadas se observaron en los pacientes con asplenia (83,3%, aunque cabe mencionar que el número de niños con esta condición era de solo 6), síndrome de Down (72,3%) y nefropatía (60%).
Según el grupo de edad, se ha observado una tendencia decreciente de la cobertura vacunal a medida que la edad aumentaba, hecho que no se detectó en el estudio EPIVAC, aunque sí se observaron diferencias estadísticamente significativas entre las distintas cohortes de nacimiento18.
La inmunización correcta según el calendario sistemático de Cataluña fue un predictor asociado a la vacunación antineumocócica. Esto implicaría que profesionales que prestan más atención a la correcta vacunación de sus pacientes pediátricos lo hacen no solo con las vacunas incluidas en el calendario sistemático, sino también con la del neumococo.
Entre las posibles limitaciones de nuestro estudio cabe mencionar que solo incluye a los niños asignados a los EAP del ICS, por lo que no se dispone de información de aquellos que son atendidos exclusivamente por otros proveedores de salud o bien en el ámbito privado. Sin embargo, se estima que el ICS da cobertura al 78% de la población catalana (5,8 millones de ciudadanos), y que el 70% se visita por su EAP al menos una vez al año y el 85% al menos una vez en 3 años20. Para estimar las posibles diferencias entre población asignada y atendida, se ha calculado que el porcentaje de niños menores de 15 años atendidos sobre el total de asignados es del 81,2%, y es esperable que en la población de nuestro estudio sea aún más elevada, al tratarse de niños con condiciones de riesgo que son atendidos mayoritariamente en sus EAP. Por ello, creemos que los niños incluidos en el estudio constituyen una muestra muy amplia, mayor que la de cualquier otro estudio publicado hasta ahora sobre este tema, y que probablemente los resultados obtenidos son representativos de la situación real de los niños con condiciones de riesgo de Cataluña.
Otra limitación del estudio hace referencia a los niños con implantes cocleares: esta es una de las indicaciones para las que se recomienda la vacunación antineumocócica, pero no dispone de código CIE-10 porque es un procedimiento y no un diagnóstico médico. Por tanto, los niños con estos dispositivos no se han podido incluir en este estudio, lo cual puede implicar una infraestimación de la cobertura vacunal.
Como en todo estudio que utiliza como fuente de información la historia clínica informatizada, se deben tener en cuenta los posibles errores de registro por parte de los sanitarios de AP en el eCAP, aunque desde hace años se está realizando un constante trabajo a todos los niveles para obtener una información lo más depurada y correcta posible21.
En este estudio se presentan datos de coberturas vacunales para la vacuna antineumocócica teniendo en cuenta datos sociodemográficos y médicos. Esto es útil a la hora de planificar futuras estrategias encaminadas a aumentar dichas coberturas. En este sentido habría que incidir especialmente en los niños con trastornos hematológicos o hepatopatías, mayores de 10 años y de nacionalidad no española.
En conclusión, el presente estudio muestra que la cobertura vacunal antineumocócica (siendo esta una vacuna administrada en el marco de un programa de vacunación selectiva) en población pediátrica con condiciones de riesgo es baja en Cataluña, y señala la necesidad de diseñar e implementar planes de actuación dirigidos a mejorar esta cobertura.
Conflicto de interesesLos autores declaran tener los siguientes conflictos de interés: la Dra. Magda Campins ha sido ponente de simposios esponsorizados por Pfizer y ha formado parte de comités de expertos de este mismo laboratorio.
Los autores desean expresar su agradecimiento al Sistema de Información para el Desarrollo de la Investigación en Atención Primaria, especialmente a los doctores Leonardo Méndez y Ermengol Coma, por su valiosa colaboración en el proyecto.
Este trabajo ha sido realizado en el marco del Programa de Doctorado en Ciencias de la Salud de la Universidad Autónoma de Barcelona.