La anaplasmosis humana (AH) es una zoonosis emergente, transmitida en nuestro medio por la picadura de Ixodes ricinus (garrapata Ixodidae) y producida por Anaplasma phagocytophilum1. Desde su primera descripción en EE.UU. en 1994, se han comunicado múltiples casos en ese país y pequeñas series y casos diseminados por Europa1-3. En España existen estudios que han demostrado la presencia de esta infección en I.ricinus y en individuos expuestos a garrapatas (tabla 1), pero solo se han publicado 2 casos autóctonos y uno importado4-6. Una posible explicación de la escasa incidencia de AH puede deberse a que la mayoría de los ejemplares de I.ricinus en España están infectados por cepas no patógenas de A.phagocytophilum7, aunque también puede que esté infradiagnosticada, por la inespecificidad de su presentación clínica y falta de concienciación por parte de los profesionales.
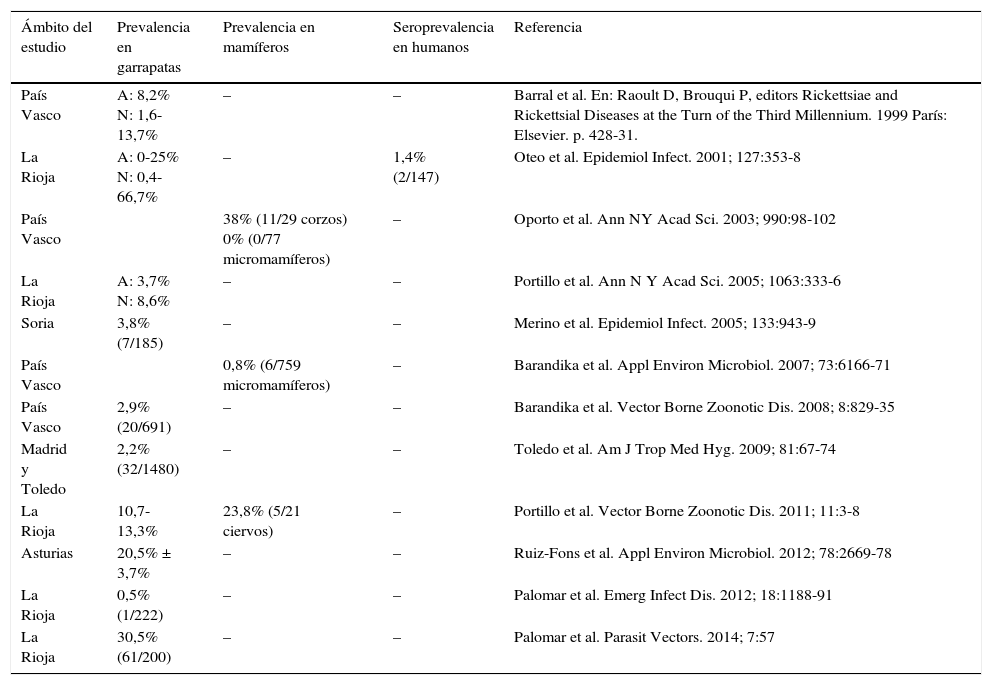
Estudios realizados en España sobre prevalencia de infección por Anaplasma phagocytophilum en garrapatas, mamíferos y humanos expuestos
| Ámbito del estudio | Prevalencia en garrapatas | Prevalencia en mamíferos | Seroprevalencia en humanos | Referencia |
|---|---|---|---|---|
| País Vasco | A: 8,2% N: 1,6-13,7% | – | – | Barral et al. En: Raoult D, Brouqui P, editors Rickettsiae and Rickettsial Diseases at the Turn of the Third Millennium. 1999 París: Elsevier. p. 428-31. |
| La Rioja | A: 0-25% N: 0,4-66,7% | – | 1,4% (2/147) | Oteo et al. Epidemiol Infect. 2001; 127:353-8 |
| País Vasco | 38% (11/29 corzos) 0% (0/77 micromamíferos) | – | Oporto et al. Ann NY Acad Sci. 2003; 990:98-102 | |
| La Rioja | A: 3,7% N: 8,6% | – | – | Portillo et al. Ann N Y Acad Sci. 2005; 1063:333-6 |
| Soria | 3,8% (7/185) | – | – | Merino et al. Epidemiol Infect. 2005; 133:943-9 |
| País Vasco | 0,8% (6/759 micromamíferos) | – | Barandika et al. Appl Environ Microbiol. 2007; 73:6166-71 | |
| País Vasco | 2,9% (20/691) | – | – | Barandika et al. Vector Borne Zoonotic Dis. 2008; 8:829-35 |
| Madrid y Toledo | 2,2% (32/1480) | – | – | Toledo et al. Am J Trop Med Hyg. 2009; 81:67-74 |
| La Rioja | 10,7-13,3% | 23,8% (5/21 ciervos) | – | Portillo et al. Vector Borne Zoonotic Dis. 2011; 11:3-8 |
| Asturias | 20,5% ± 3,7% | – | – | Ruiz-Fons et al. Appl Environ Microbiol. 2012; 78:2669-78 |
| La Rioja | 0,5% (1/222) | – | – | Palomar et al. Emerg Infect Dis. 2012; 18:1188-91 |
| La Rioja | 30,5% (61/200) | – | – | Palomar et al. Parasit Vectors. 2014; 7:57 |
A: adultos; N: ninfas.
Presentamos 2 casos de AH (uno confirmado y otro probable) diagnosticados en Galicia, comentando algunos aspectos de interés.
Caso 1. Mujer de 43años con fiebre, cefalea, mialgias y malestar general de 4días de evolución. Antecedentes de glomerulonefritis membranosa con síndrome nefrótico. Vivía en hábitat rural y tenía contacto con perros. Presentaba fiebre (39°C) con resto de exploración normal. En los análisis destacaban: leucocitos 6.800/mm3 (80% neutrófilos); VSG 137mm; PC reactiva 39mg/l; urea 86mg/dl, creatinina 1,3mg/dl, proteínas totales 5,8g/dl y albúmina 2,6g/dl, resto normal. Una radiografía de tórax y ecografía abdominal no mostraron alteraciones. Tras extraer hemocultivos, se inició tratamiento con ciprofloxacino i.v. La paciente quedó afebril en 24h, desarrollando leucopenia (3.900/mm3) y trombocitopenia (119.000/mm3) a las 48h de ingreso. El frotis de sangre periférica no mostró alteraciones. Los hemocultivos y estudios de PCR en sangre para Rickettsia spp. y A.phagocytophilum fueron negativos. Las serologías de Coxiella burnetii, Borrelia burgdorferi, A.phagocytophilum y Rickettsia spp. resultaron negativas en fase aguda. La paciente fue dada de alta con ciprofloxacino oral hasta completar 14días. El estudio serológico de convalecencia mostró seroconversión (título de IgG 128) frente a A.phagocytophilum (Focus Diagnostics, Cypress, CA, EE.UU.). La paciente se encontraba asintomática y con análisis normalizados.
Caso 2. Varón de 33años que ingresa por fiebre y cefalea de 7días de evolución. El sedimento urinario, radiografía de tórax, TAC cerebral y una punción lumbar fueron normales. Vivía en hábitat rural y poseía un perro. En la exploración presentaba temperatura de 39,6°C, sin otros datos reseñables. En la analítica destacaba: leucocitos 2.100/mm3 con fórmula normal, VSG 23mm y PC reactiva 52mg/l. El frotis de sangre periférica mostró linfocitos de aspecto activado. La radiografía de tórax fue normal, y la ecografía abdominal mostró esplenomegalia leve sin lesiones focales. Se extrajeron hemocultivos y se inició ciprofloxacino i.v. Tras 5días, la fiebre y la leucopenia persistían y se elevaron las transaminasas. Se inició tratamiento con doxiciclina oral y la fiebre desapareció en 48h. El quinto día, los leucocitos se habían normalizado y las transaminasas habían disminuido. Los hemocultivos y la PCR de A.phagocytophilum en sangre fueron negativos. Las serologías de virus de hepatitisA, B y C, VIH, VEB, CMV, sífilis, Mycoplasma pneumoniae, Chlamydia pneumoniae, Brucella sp., C.burnetii, B.burgdorferi sensu lato, Bartonella henselae y R.conorii, fueron negativas. La serología de A.phagocytophilum fue positiva con títulos de 1024 en fase aguda y de convalecencia. Al paciente se le dio de alta para completar 14días de tratamiento. Un mes después estaba asintomático.
La AH se presenta como un síndrome febril inespecífico asociado con frecuencia a leucopenia y/o trombocitopenia y a un moderado aumento de las transaminasas en personas expuestas a garrapatas. Una respuesta precoz (24-48h) de la fiebre a la doxiciclina refuerza la sospecha diagnóstica1,3. El diagnóstico se basa en técnicas de laboratorio (detección de mórulas en neutrófilos, detección de Ac y PCR), cuyos resultados definen los casos como probables o confirmados según los criterios del ESCMID8. La rentabilidad de dichas técnicas disminuye con el tiempo de evolución y el tratamiento previo con antibióticos. Por ello, se recomienda la toma de muestras de forma precoz1,3,9,10. La mayoría de casos se diagnostican por serología, dado que los cultivos tienen mínima rentabilidad. La PCR solo es rentable durante la primera semana y se realiza en centros de referencia. La visualización de mórulas es excepcional en Europa1,4,5,9. La doxiciclina es el tratamiento de elección (salvo en embarazadas), recomendándose el inicio ante la sospecha1,3,10.
Nuestros pacientes presentaron una historia clínico-epidemiológica compatible y fueron diagnosticados por serología. En el caso1, el diagnóstico se confirmó mediante seroconversión, y el caso2 fue un caso probable de acuerdo a títulos serológicos altos sin aumento en convalecencia, reforzado por la respuesta a doxiciclina. En ambos casos la búsqueda de mórulas y la PCR fueron negativas, probablemente porque las muestras fueron tomadas de forma tardía y por la toma previa de antibióticos. En el caso1, el tratamiento con ciprofloxacino se mantuvo debido a la buena respuesta, aunque su uso no es de elección3,10.