El presente estudio pretende revisar el absceso del músculo iliopsoas (AMI) desde una perspectiva contemporánea, partiendo de la experiencia acumulada en dos centros de tercer nivel.
Material y MétodosAnálisis retrospectivo de 35 pacientes con diagnóstico de AMI entre 1998 y 2009. Revisamos sus variables clínico-microbiológicas y su evolución en función del tipo de tratamiento definitivo: médico [antibioterapia (10 pacientes)] o intervencionista [antibioterapia más drenaje percutáneo y/o quirúrgico (25 pacientes)].
ResultadosEl absceso fue de naturaleza primaria en 8 casos y secundaria en los restantes, con predominio de las formas asociadas a espondilodiscitis. La tríada clínica clásica (fiebre, dolor y dificultad para la deambulación) estuvo presente en 10 pacientes, con una mediana de duración de los síntomas hasta el diagnóstico de 12 días. Staphylococcus aureus fue el microorganismo más frecuente. Tras una mediana de seguimiento de 454 días, el riesgo de evolución desfavorable (muerte relacionada y/o recidiva) fue mayor en pacientes con diabetes mellitus (44,4 vs. 7,7%; p=0,027), sin diferencias significativas entre los grupos sometidos a tratamiento médico o intervencionista (20,0 vs. 28,0%).
ConclusionesEn nuestra serie predominaron las formas de AMI por S. aureus secundarias a un foco osteoarticular. El tratamiento exclusivamente médico parece eficaz a largo plazo, si bien los pacientes diabéticos presentaron mayor riesgo de recidiva.
The present study was aimed at reviewing the iliopsoas abscess (IPA) from a contemporary perspective, on the basis of experience from two tertiary referral centres.
Material and methodsWe performed a retrospective analysis of 35 cases of IPA diagnosed between 1998 and 2009. Their clinical and microbiological features were recorded, as well as their long-term outcome according to the type of treatment: antibiotics alone (10 patients), or antibiotics plus percutaneous drainage or surgery (25 patients).
ResultsPrimary abscess occurred in 8 patients. The most frequent source of secondary abscesses was spondylodiscitis. The classic clinical triad (fever, pain and functional impairment) was present in 10 patients, with a median duration of symptoms before diagnosis of 12 days. Staphylococcus aureus was the most frequently isolated microorganism. At the end of a median follow-up of 454 days, the risk of poor outcome (related death and/or relapse) was higher among patients with diabetes mellitus (44.4% vs. 7.7%; P=.027), with no significant differences according to the therapeutic approach (20.0% in the group of antibiotics alone vs. 28.0% in the group with drainage or surgery).
ConclusionsIn our series, most cases of IPA were due to S. aureus and secondary to a skeletal source. Antibiotic therapy seems effective in the long-term, although diabetic patients had a higher risk of relapse.
Aunque descrito por primera vez por Mynter hace ahora 130 años1, el absceso del músculo iliopsoas sigue constituyendo una entidad infrecuente y pobremente caracterizada en su etiología, asociaciones clínicas y, particularmente, abordaje terapéutico más adecuado2. Gran parte de la literatura previa se basa en la comunicación de casos aislados o en estudios retrospectivos con un reducido número de pacientes y prolongados periodos de inclusión3–5. Así, la serie más amplia publicada hasta la fecha comprende un total de 124 casos diagnosticados a lo largo de 14 años en 11 hospitales españoles6. La ausencia de homogeneidad en su aproximación diagnóstica y tratamiento puede condicionar la validez de sus conclusiones en la práctica clínica actual. Por otra parte, en el curso de las últimas décadas hemos asistido a un cambio progresivo en la epidemiología del absceso del músculo iliopsoas, con un descenso de los casos de etiología tuberculosa y una mayor incidencia de los secundarios a una infección hematógena por Staphylococcus aureus, frecuentemente asociada a la administración de cuidados sanitarios2,5. La moderna universalización de las técnicas de imagen abdominal ha facilitado el diagnóstico en fases tempranas de su historia natural, en contraste con la presentación insidiosa y elevada mortalidad descrita en las series clásicas, además de ofrecer nuevas posibilidades de drenaje percutáneo no quirúrgico5,7. El presente estudio pretende analizar el absceso del músculo iliopsoas desde una perspectiva contemporánea, particularmente en lo que respecta a su abordaje terapéutico y riesgo de recidiva a largo plazo, a partir de la experiencia acumulada en dos centros de tercer nivel.
Material y métodosRealizamos un análisis retrospectivo de todos los casos de absceso del músculo iliopsoas diagnosticados en dos hospitales universitarios de tercer nivel de la Comunidad de Madrid entre enero de 1998 y diciembre de 2009. Los centros participantes fueron el Hospital Universitario 12 de Octubre (dotado de 1.330 camas y con una población de referencia de 590.000 habitantes en el año 2007) y el Hospital Universitario La Paz (con 1.320 camas y una población de 787.000 habitantes). La definición de caso fue establecida en un contexto clínico compatible a partir de la presencia de hallazgos radiológicos sugerentes de colección o absceso en el compartimento iliopsoas (por ultrasonografía [US], tomografía computarizada [TC] o resonancia magnética nuclear [RMN]) y la resolución de los mismos mediante drenaje quirúrgico o percutáneo, o bien tras la administración de tratamiento antibiótico6,8. Por medio de un cuestionario estandarizado se recogieron de cada caso sus variables demográficas; enfermedades subyacentes; presentación clínica; hallazgos de laboratorio, microbiológicos y radiológicos; modalidad de tratamiento (incluyendo la duración total del tratamiento antibiótico), y evolución. En caso de que se realizara drenaje del contenido del absceso se procedió a su procesamiento en medios de cultivo aerobio y anaerobio, según la práctica habitual en cada centro, en tanto que el cultivo en medio de Löwenstein fue realizado ante la sospecha de etiología tuberculosa según criterio del médico responsable. El diagnóstico etiológico fue establecido por el aislamiento del microorganismo en hemocultivo o cultivo del material drenado del absceso, o bien por la combinación de hallazgos clínicos e histológicos compatibles con etiología tuberculosa y respuesta al tratamiento antituberculoso6. Diferenciamos entre absceso secundario (si pudo documentarse algún foco de infección contiguo al músculo iliopsoas) y primario (en ausencia del mismo)6. Definimos evolución desfavorable como recidiva del absceso y/o muerte directamente relacionada. Establecimos dos grupos de pacientes según su abordaje terapéutico definitivo: médico (exclusivamente tratamiento antibiótico) o intervencionista (tratamiento antibiótico asociado a drenaje percutáneo y/o quirúrgico del absceso). Las variables cualitativas aparecen descritas con sus frecuencias absolutas y relativas; las variables cuantitativas se ofrecen por su media o mediana±desviación estándar (DE) o rango. La comparación entre grupos fue realizada mediante el test exacto de Fisher, t de Student, U de Mann-Whitney o ANOVA, con un nivel de significación fijado en un valor de p<0,05. Empleamos la aplicación estadística SPSS versión 13.0 (SPSS Inc., Chicago, IL).
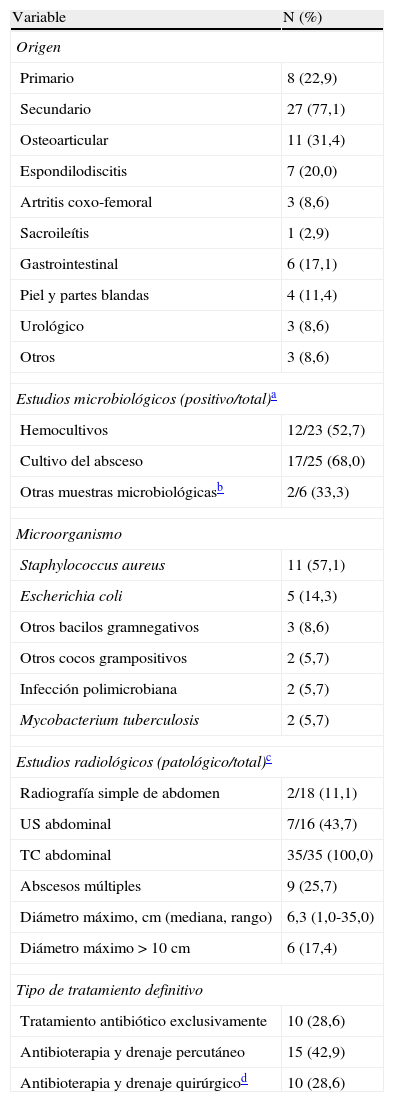
ResultadosLa serie analizada incluyó un total de 35 pacientes cuyas características epidemiológicas y clínicas aparecen detalladas en la tabla 1, sin diferencias significativas entre los dos centros participantes en el estudio. La diabetes mellitus (DM) y la hepatopatía crónica en estadio cirrótico representaron las enfermedades subyacentes más frecuentes. En 10 casos (28,6%) se documentó la presencia de alguna forma de inmunosupresión. La mediana de duración de los síntomas hasta el diagnóstico fue de 12 días (rango: 1-350). La tríada clínica (fiebre, dolor y dificultad para la deambulación) estuvo presente en tan solo 10 casos (28,6%), si bien 34 pacientes (97,1%) refirieron al menos uno de sus componentes en la evaluación inicial. La tabla 2 muestra el origen del absceso, los hallazgos microbiológicos y radiológicos, y su abordaje terapéutico. El absceso fue considerado primario en 8 casos (22,9%). Entre las formas secundarias, por su parte, la espondilodiscitis lumbar fue el origen más frecuente (7 casos). En 25 pacientes (71,4%) se identificó el agente etiológico del absceso, con predominio de S. aureus (11 casos), Escherichia coli (5 casos) y Proteus mirabilis (dos casos). El aislamiento de S. aureus fue más frecuente en los abscesos de origen osteoarticular en relación con el resto de la serie (54,5 vs. 20,8%; p=0,046). Solo dos casos fueron considerados de etiología tuberculosa, incluyendo un paciente que respondió al tratamiento antituberculoso empírico en ausencia de confirmación microbiológica. Se practicó un ecocardiograma (transtorácico o transesofágico) en 9 de los 12 pacientes con absceso por S. aureus (34,3%), que reveló hallazgos sugerentes de endocarditis infecciosa (EI) en uno de ellos.
Características epidemiológicas y clínicas de los 35 casos de absceso de músculo iliopsoas incluidos en el presente estudio
| Variable | N (%) |
| Edad, años (media±DE) | 54,8±18,2 |
| Edad >70 años | 9 (25,7) |
| Género masculino | 18 (51,4) |
| Enfermedades subyacentes | |
| Diabetes mellitus | 6 (17,1) |
| Cirrosis hepática | 5 (14,3) |
| Neoplasia | 4 (11,4) |
| Enfermedad inflamatoria intestinal | 3 (8,6) |
| Infección por VIH | 2 (5,7) |
| Otra causa de inmunosupresióna | 3 (8,6) |
| Duración de los síntomasb, días (mediana, rango) | 12 (1-350) |
| Manifestaciones clínicas | |
| Dolor en reposo | 28 (80,0) |
| Dolor a la deambulación | 19 (54,3) |
| Fiebre | 21 (60,0) |
| Síntomas gastrointestinales | 5 (14,3) |
| Tríada clásica | 10 (28,6) |
| Hallazgos a la exploración física | |
| Dolor a la palpación abdominal | 20 (57,1) |
| Signo del psoas | 13 (37,1) |
| Masa palpable | 9 (25,7) |
| Edema en miembro inferior | 3 (8,6) |
| Hemoglobina, g/dL (media±DE) | 11,8±2,1 |
| Hemoglobina <11g/dL | 10 (28,6) |
| Leucocitos, x 109/L (mediana, rango) | 13,0 (1,7-219,0) |
| Leucocitos >15×109/L | 9 (25,7) |
| Neutrófilos, x109/L (mediana, rango) | 10,4 (0,03-23,8) |
| Neutrófilos >12×109/L | 10 (28,6) |
| Plaquetas, x109/L (mediana, rango) | 358 (81,0-777,0) |
| Plaquetas >450×109/L | 8 (22,9) |
| VSG en primera hora, mm (media±DE)c | 77,5±26,6 |
| VSG en primera hora >100mm | 5 (14,3) |
DE: desviación estándar; VIH: virus de la inmunodeficiencia humana; VSG: velocidad de sedimentación globular.
Origen de los 35 casos de absceso de músculo iliopsoas, etiología y tratamiento
| Variable | N (%) |
| Origen | |
| Primario | 8 (22,9) |
| Secundario | 27 (77,1) |
| Osteoarticular | 11 (31,4) |
| Espondilodiscitis | 7 (20,0) |
| Artritis coxo-femoral | 3 (8,6) |
| Sacroileítis | 1 (2,9) |
| Gastrointestinal | 6 (17,1) |
| Piel y partes blandas | 4 (11,4) |
| Urológico | 3 (8,6) |
| Otros | 3 (8,6) |
| Estudios microbiológicos (positivo/total)a | |
| Hemocultivos | 12/23 (52,7) |
| Cultivo del absceso | 17/25 (68,0) |
| Otras muestras microbiológicasb | 2/6 (33,3) |
| Microorganismo | |
| Staphylococcus aureus | 11 (57,1) |
| Escherichia coli | 5 (14,3) |
| Otros bacilos gramnegativos | 3 (8,6) |
| Otros cocos grampositivos | 2 (5,7) |
| Infección polimicrobiana | 2 (5,7) |
| Mycobacterium tuberculosis | 2 (5,7) |
| Estudios radiológicos (patológico/total)c | |
| Radiografía simple de abdomen | 2/18 (11,1) |
| US abdominal | 7/16 (43,7) |
| TC abdominal | 35/35 (100,0) |
| Abscesos múltiples | 9 (25,7) |
| Diámetro máximo, cm (mediana, rango) | 6,3 (1,0-35,0) |
| Diámetro máximo >10cm | 6 (17,4) |
| Tipo de tratamiento definitivo | |
| Tratamiento antibiótico exclusivamente | 10 (28,6) |
| Antibioterapia y drenaje percutáneo | 15 (42,9) |
| Antibioterapia y drenaje quirúrgicod | 10 (28,6) |
DE: desviación estándar; TC: tomografía computarizada; US: ultrasonografía.
Número de pacientes con resultado microbiológico positivo en relación con el número total en los que fue realizado el cultivo.
Incluye un cultivo de líquido sinovial y un cultivo de material drenado a través de una fístula cutánea.
Diez pacientes (28,6%) recibieron exclusivamente antibioterapia como abordaje terapéutico. Esta opción de tratamiento fue más frecuente en los casos de origen osteoarticular (50,0 vs. 17,4%; p=0,053). Se realizó drenaje percutáneo como abordaje terapéutico inicial en 20 pacientes (57,1%) al cabo de una mediana de 9,5 días desde el diagnóstico (rango: 1-44), obteniéndose una media de 249mL de material. Por último, 10 pacientes (28,6%) fueron sometidos al drenaje quirúrgico de la colección (incluyendo cinco casos previamente drenados de forma percutánea), que supuso la realización de nefrectomía (dos casos), resección ileocecal y corporectomía parcial lumbar (un caso en cada procedimiento). El tamaño máximo de los abscesos tratados mediante drenaje quirúrgico (17,8±10,9cm) fue mayor en comparación con el de los sometidos a drenaje percutáneo (6,2±3,9cm) o a tratamiento exclusivamente médico (5,4±3,0cm; p=0,002).
La mediana de seguimiento de la serie fue de 454 días (rango: 54-3.640). Se documentó la recidiva del absceso en 8 casos (22,9%), con un intervalo mediano desde el primer diagnóstico de 252,5 días. El tratamiento de la recidiva consistió en la administración exclusiva de tratamiento antibiótico en cuatro pacientes, y en el drenaje quirúrgico asociado a antibioterapia en los restantes. Un paciente falleció durante el primer ingreso hospitalario, en tanto que al final del periodo de seguimiento habían fallecido otros cuatro pacientes, resultando en una mortalidad global del 14,3%. Una de las muertes tuvo lugar en el periodo post-operatorio de una recidiva, otra fue secundaria a shock séptico, y las dos restantes no se consideraron relacionadas con el absceso del músculo iliopsoas. De este modo 9 pacientes (25,7%) presentaron una evolución desfavorable, bien fuera por recidiva del absceso en 8 casos, o por muerte relacionada en tres (dos de ellos con una recidiva previa).
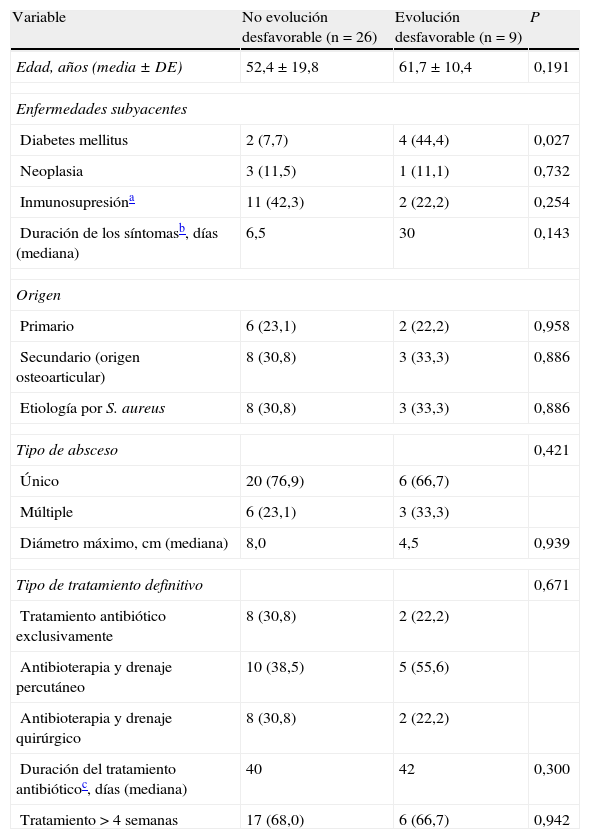
Tal y como se detalla en la tabla 3, el riesgo de evolución desfavorable fue mayor en los pacientes con DM (p=0,027), sin que encontráramos diferencias en relación con el resto de las variables analizadas (otras comorbilidades, etiología, origen, número de abscesos o duración total del tratamiento antibiótico). Tampoco observamos diferencias significativas al comparar la probabilidad de evolución desfavorable en los pacientes sometidos a tratamiento médico (dos de 10 [20,0%]) o intervencionista (7 de 25 [28,0%]; p=0,488). Al analizar de forma específica el subgrupo que recibió tan solo tratamiento médico comprobamos que la duración media de la antibioterapia fue menor en los dos pacientes con evolución desfavorable (26,5 días) en relación con los 8 restantes (57,3 días), sin que esta diferencia alcanzara la significación estadística (p=0,444). Tampoco demostramos diferencias en el tamaño del absceso (2,7±0,4cm vs. 6,2±3,0cm, respectivamente; p=0,160).
Comparación de los variables asociadas a evolución desfavorable (recidiva del absceso y/o muerte directamente relacionada)
| Variable | No evolución desfavorable (n=26) | Evolución desfavorable (n=9) | P |
| Edad, años (media±DE) | 52,4±19,8 | 61,7±10,4 | 0,191 |
| Enfermedades subyacentes | |||
| Diabetes mellitus | 2 (7,7) | 4 (44,4) | 0,027 |
| Neoplasia | 3 (11,5) | 1 (11,1) | 0,732 |
| Inmunosupresióna | 11 (42,3) | 2 (22,2) | 0,254 |
| Duración de los síntomasb, días (mediana) | 6,5 | 30 | 0,143 |
| Origen | |||
| Primario | 6 (23,1) | 2 (22,2) | 0,958 |
| Secundario (origen osteoarticular) | 8 (30,8) | 3 (33,3) | 0,886 |
| Etiología por S. aureus | 8 (30,8) | 3 (33,3) | 0,886 |
| Tipo de absceso | 0,421 | ||
| Único | 20 (76,9) | 6 (66,7) | |
| Múltiple | 6 (23,1) | 3 (33,3) | |
| Diámetro máximo, cm (mediana) | 8,0 | 4,5 | 0,939 |
| Tipo de tratamiento definitivo | 0,671 | ||
| Tratamiento antibiótico exclusivamente | 8 (30,8) | 2 (22,2) | |
| Antibioterapia y drenaje percutáneo | 10 (38,5) | 5 (55,6) | |
| Antibioterapia y drenaje quirúrgico | 8 (30,8) | 2 (22,2) | |
| Duración del tratamiento antibióticoc, días (mediana) | 40 | 42 | 0,300 |
| Tratamiento >4 semanas | 17 (68,0) | 6 (66,7) | 0,942 |
DE: desviación estándar.
Gracias a su amplia vascularización y pH local ácido el tejido muscular parece exhibir cierta resistencia intrínseca a la infección bacteriana. Tal circunstancia, asociada a su localización anatómica retroperitoneal, justifica el carácter excepcional de los procesos piógenos limitados al compartimento iliopsoas8. Además esta infrecuente forma de miositis se caracteriza por su presentación clínica inespecífica y amplio espectro etiológico, como demuestra el presente estudio. Así, en línea con otros trabajos3,8 encontramos la clásica tríada clínica1 en menos de la tercera parte de nuestros pacientes. La demora desde el inicio de los síntomas hasta el diagnóstico excedió de 21 días en el 25,7% de los casos, proporción similar a la descrita por Navarro López et al.6. No obstante, la duración media de la sintomatología fue notablemente menor (31 días) en comparación con otras series más antiguas, como la de Pérez-Fernández et al. (62 días)7, sugiriendo un protagonismo creciente de las pruebas de imagen abdominal (TC o RMN) en el diagnóstico actual de esta entidad. En cuanto a sus factores predisponentes, la DM destaca como la condición común en la mayor parte de las series modernas3–6,9, incluida la nuestra, y se ha descrito que puede facilitar la evolución hacia formas de mionecrosis con formación de gas tisular y elevada mortalidad8.
Staphylococcus aureus fue el microorganismo más frecuentemente identificado, hallazgo común a otras series occidentales3-6 y que contrasta con la mayor incidencia de abscesos producidos por bacilos gram-negativos comunicada por autores asiáticos, con especial relevancia de Klebsiella pneumoniae8,9. Incluso en el contexto ya comentado de evolución en su epidemiología, resulta llamativa la escasa representación que hemos observado de casos producidos por Mycobacterium tuberculosis (5,7%), inferior a la obtenida en estudios previos realizados en nuestro país cuyos periodos de inclusión comprendieron la década de los noventa, como el de Pérez-Fernández et al. (35,7% de casos de etiología tuberculosa)7 o el de Navarro López et al. (12,1%)6. No obstante el diseño retrospectivo de nuestro trabajo y los cambios acontecidos en la incidencia de la tuberculosis extrapulmonar a lo largo del periodo analizado impiden extraer conclusiones definitivas al respecto. La proporción de abscesos primarios (22,9%) fue comparable a la descrita en otras series occidentales3,4,6, en tanto que la espondilodiscitis constituyó el origen más frecuentemente documentado en las formas secundarias. Podemos destacar la notable rentabilidad diagnóstica que obtuvimos tanto del hemocultivo (52,7%) como, en especial, del cultivo del material drenado del absceso (68%), similar a la de estudios previos6,7. Es posible que la sensibilidad de los hemocultivos en nuestra serie, superior a la comunicada previamente6, esté condicionada por la elevada frecuencia de bacteriemia por S. aureus (aislado en 8 de los 12 hemocultivos positivos). En ese sentido, uno de los 11 pacientes (9,1%) con absceso por S. aureus presentó criterios de EI posible, asociación infrecuentemente descrita en la literatura. Hasta el 24% de los casos de espondilodiscitis por S. aureus (el foco secundario más frecuente en nuestra experiencia) se ven precedidos por una bacteriemia en el año previo a su diagnóstico10. Por otra parte, la presencia de una infección del esqueleto axial actúa como un potente predictor clínico de endocarditis en el contexto de una bacteriemia nosocomial por S. aureus11. A partir de estas observaciones, y en vista de la potencial gravedad de esta complicación, sugerimos plantear la realización de un ecocardiograma en todos los pacientes en los que se aísle S. aureus en el material de drenaje del absceso asumiendo la posibilidad de una bacteriemia oculta precedente. En la revisión exhaustiva realizada por Ricci et al. hace más de dos décadas, con 367 casos recogidos hasta ese momento en la literatura, los abscesos primarios fueron propios de pacientes jóvenes, sin comorbilidad asociada y originarios de países en vías de desarrollo12. Por otra parte, el origen urológico aparece con más frecuencia en series asiáticas, tal y como describe Huang et al. en su estudio de 25 casos de absceso del músculo iliopsoas procedentes de Taiwán, la mitad de los cuales fueron secundarios a una infección de tracto urinario9.
En nuestra serie el tratamiento exclusivamente médico fue elegido con más frecuencia en las formas de origen osteoarticular, en línea con estudios previos6. Hemos observado un riesgo de recidiva (22,9%) algo superior al comunicado por otros autores (15,8% en la serie de Navarro López et al.6 o 13% en la de Penado et al.3). No hemos podido demostrar el impacto de la modalidad terapéutica empleada (médica o intervencionista) en el riesgo de evolución desfavorable del absceso, definida por mortalidad de causa relacionada o recidiva. Tan solo la presencia de DM fue identificada en el análisis univariante como factor de mal pronóstico. Si bien se ha comunicado una mayor mortalidad intrahospitalaria en pacientes diabéticos con absceso hepático piógeno13, el presente estudio es el primero en demostrar un mayor riesgo de recidiva asociado a esta condición en el absceso del músculo iliopsoas. No obstante, la literatura recoge escasos trabajos que hayan analizado los factores pronósticos a largo plazo en esta entidad, debido probablemente al reducido tamaño muestral de la mayor parte de las series4,5,7,8. Navarro López et al. identificaron que la edad superior a 65 años, la presencia de bacteriemia y el aislamiento de E. coli actuaban como predictores independientes de mortalidad en su serie multicéntrica6. A pesar de su notable tamaño muestral, estos autores tampoco observaron diferencias significativas en el riesgo de recidiva del absceso en función de su origen o del tipo de tratamiento. Por tanto, y en ausencia de estudios de mayor calidad metodológica, parece razonable reservar el tratamiento médico a los abscesos de menor tamaño secundarios a una diseminación hematógena, y plantear el drenaje en las formas asociadas a un foco de infección gastrointestinal o urológica, particularmente en pacientes diabéticos.
La presente serie de abscesos del músculo iliopsoas es una de las más amplias comunicadas hasta la fecha en nuestro país, y presenta la ventaja de incluir casos diagnosticados en un periodo de 11 años en dos centros comparables de tercer nivel, lo que permite asumir un abordaje clínico relativamente homogéneo. Además, su periodo de seguimiento (mediana de 64,8 semanas) duplica al recogido por Navarro López et al. en su cohorte multicéntrica (32 semanas)6. No obstante, comparte con otros estudios que han analizado esta entidad las limitaciones derivadas de su diseño retrospectivo y tamaño muestral relativamente pequeño, circunstancia que dificulta la demostración de diferencias entre subgrupos de pacientes.
En conclusión, en la presentación contemporánea del absceso del músculo iliopsoas predominan las formas secundarias a un foco osteoarticular, con S. aureus como agente más frecuente, y destaca la elevada rentabilidad diagnóstica tanto del hemocultivo como del cultivo del material de drenaje a la hora de establecer su documentación microbiológica. El riesgo de recidiva supera el 20% y es mayor en los pacientes con DM, sin que hayamos podido demostrar diferencias significativas en función del tipo de abordaje terapéutico o la duración de la antibioterapia. Por tanto, y en vista de los hallazgos de nuestra serie, el tratamiento médico basado en la administración de antibioterapia parece una opción eficaz a largo plazo en el absceso del músculo iliopsoas, si bien en pacientes diabéticos se debería considerar la existencia de un mayor riesgo de recidiva.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Mario Fernández-Ruiz ha recibido una beca de la Fundación para la Investigación Biomédica del Hospital Universitario 12 de Octubre. Francisco López-Medrano ha recibido una beca de la Fundación Mutua Madrileña (FMM).