Caracterizar los pacientes con diabetes que iniciaron terapia con bomba de insulina y monitorización continua de glucosa en tiempo real (CSII-rtCGM) en un centro especializado de Medellín, Colombia.
Materiales y métodosSe evaluaron los pacientes con diabetes que recibieron entrenamiento e instalación del dispositivo en el centro entre febrero de 2010 y mayo de 2014. Se realizó un análisis descriptivo de las variables sociodemográficas y clínicas.
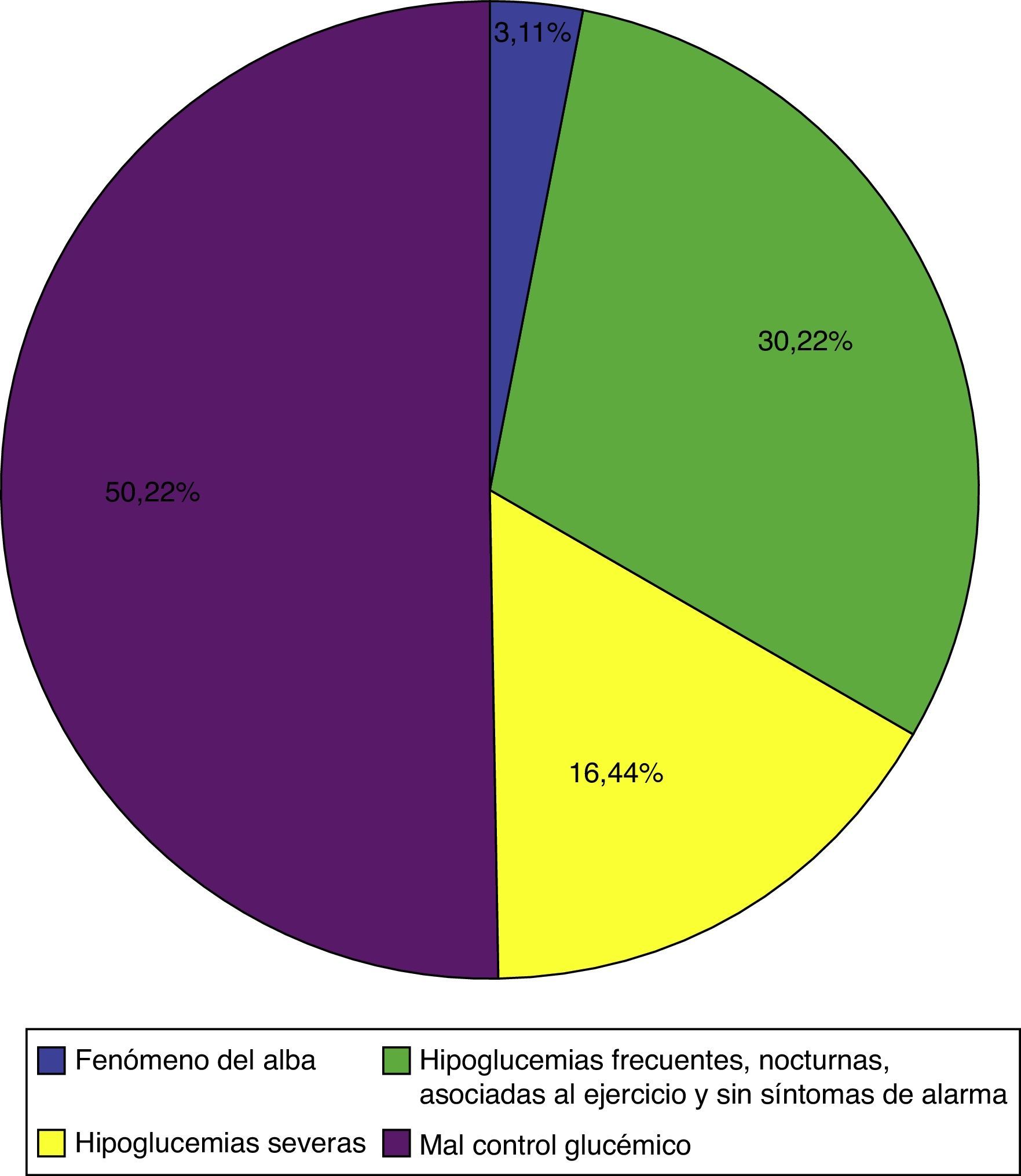
ResultadosSe incluyeron 141 pacientes de los 174 pertenecientes al programa. El 90,1% tenía diabetes tipo 1 (DT1), siendo la edad promedio al inicio de la terapia de 31,4 años (SD: 14,1). El 75,8% de los pacientes tenía peso normal (IMC<25), el 21,0% sobrepeso (IMC=25-30) y el 2,3% era obeso (IMC≥30). La mediana de duración de la enfermedad fue de 13 años (P25-P75=10,7-22,0). El 14,2% de los pacientes fueron hospitalizados al menos una vez en el año previo al inicio de la terapia con CSII-rtCGM por causas relacionadas con la diabetes. El promedio de hemoglobina glucosilada era de 8,6%±1,46%. Las principales indicaciones para la formulación de CSII-rtCGM fueron: mal control glucémico (50,2%); hipoglucemias frecuentes, nocturnas o asociadas al ejercicio y sin síntomas de alarma (30,2%); hipoglucemias severas (16,44%) y fenómeno del alba (3,1%).
ConclusiónLas características de los pacientes que inician terapia con CSII-rtCGM son similares a las reportadas en la literatura. Los resultados muestran que el centro especializado inicia esta terapia principalmente en pacientes con DT1 con mal control glucémico a pesar de la terapia intensiva, hipoglucemias leves persistentes o hipoglucemias severas.
To describe baseline characteristics of diabetic patients who were started on insulin pump and real time continuous glucose monitor (CSII-rtCGM) in a specialized center in Medellin, Colombia.
Materials and methodsAll patients with diabetes with complete data who were started on CSII-rtCGM between February 2010 and May 2014 were included. This is a descriptive analysis of the sociodemographic and clinical characteristics.
Results141 of 174 patients attending the clinic were included. 90,1% had type 1diabetes (T1D). The average age of T1D patients at the beginning of therapy was 31,4 years (SD 14,1). 75.8% of patients had normal weight (BMI<25), 21.0% were overweight (BMI 25-30) and 2,3% were obese (BMI>30). The median duration of T1D was 13 years (P25-P75=10.7-22.0). 14,2% of the patients were admitted at least once in the year preceding the start of CSII-rtCGM because of diabetes related complications. Mean A1c was 8.6%±1.46%. The main reasons for starting CSII-rtCGM were: poor glycemic control (50.2%); frequent hypoglycemia, nocturnal hypoglycemia, hypoglycemia related to exercise, asymptomatic hypoglycemia (30.2%); severe hypoglycemia (16.44%) and dawn phenomena (3.1%).
ConclusionBaseline characteristics of patients included in this study who were started on CSII-rtCGM are similar to those reported in the literature. The Clinic starts CSII-rtCGM mainly in T1D patients with poor glycemic control, frequent or severe hypoglycemia despite being on basal/bolus therapy.
La diabetes es una enfermedad en la cual el páncreas no logra suplir adecuadamente las demandas de insulina, generando una elevación de los niveles sanguíneos de glucosa que conlleva la aparición de consecuencias agudas (crisis hiperglucémicas) y complicaciones crónicas1. La prevalencia mundial actual de la enfermedad es del 6,4%1, siendo el tipo 2 (DT2) la forma predominante2,3. Se predice que el aumento de su incidencia y prevalencia será mayor en países en vías de desarrollo en relación con el sedentarismo y la obesidad.
Aunque no hay terapia curativa para esta enfermedad, es bien sabido que el control glucémico estricto reduce las complicaciones asociadas4–6, por esto se han utilizado esquemas intensivos de insulina basados en los valores de la glucemia y de acuerdo con la cantidad de hidratos de carbono a ingerir que implican múltiples inyecciones al día4,7,8. La terapia con infusión subcutánea continua de insulina con monitorización continua de glucosa en tiempo real (CSII-rtCGM), como un nuevo dispositivo que simula la fisiología del páncreas, proporciona análogos de insulina de acción rápida en forma de suministros basales las 24h del día, con administraciones de dosis mayores precediendo las comidas, y permite conocer los valores de glucosa en el tejido intersticial como reflejo de la glucemia en tiempo real, sugiriendo al paciente la necesidad de tomar conductas4,9. Su uso ha permitido lograr un mejor control glucémico y contar con una herramienta de aporte continuo de insulina con monitorización continua de glucosa. Actualmente no hay consenso en cuanto a la selección de los pacientes que se beneficiarían de esta terapia, aunque se reconocen algunas indicaciones médicas, como el mal control glucémico, el fenómeno del alba, las hipoglucemias severas, inadvertidas, nocturnas y asociadas al ejercicio; la adherencia del paciente y el empoderamiento acerca de su enfermedad son claves9,10.
Cerca de 400.000 pacientes con diabetes en los Estados Unidos reciben terapia con infusión subcutánea continua de insulina11, entre los que se incluyen niños, adultos, ancianos y mujeres embarazadas; esto hace que exista una alta posibilidad de enfrentarse en la práctica clínica a pacientes que tienen este dispositivo12,13. En Colombia existen pocos centros especializados en entrenamiento, capacitación, instalación y seguimiento de pacientes en terapia con CSII-rtCGM. El objetivo de este estudio es presentar las características epidemiológicas de los pacientes diabéticos que iniciaron esta terapia en uno de los centros especializados en la ciudad de Medellín, Colombia.
Materiales y métodosSe realizó un estudio observacional retrospectivo en un centro especializado en endocrinología en Medellín, Colombia. Se incluyeron consecutivamente todos los pacientes, niños y adultos, con diabetes tipo 1 y 2 vinculados al programa de CSII-rtCGM que recibieron entrenamiento e instalación del dispositivo en la institución entre el 1 de febrero de 2010 y el 31 de mayo de 2014. Se excluyeron pacientes con dispositivos instalados en otras instituciones, o con registros incompletos de los parámetros de formulación de la bomba de insulina.
Se midieron las variables sociodemográficas, antropométricas, clínicas y de laboratorio. La historia clínica se consideró como la fuente de información primaria para el estudio. Un investigador revisó los criterios de elegibilidad de los pacientes y diligenció la información de las variables de interés en un instrumento diseñado para tal fin; posteriormente incluyó la información en una base de datos de Microsoft Access®. El análisis de los datos se realizó en el software estadístico IBM SPSS Statistics 22®.
Para minimizar potenciales sesgos de información un investigador revisó las inconsistencias entre la información de la historia clínica y la registrada en el instrumento de recolección y bases de datos.
Se realizó un análisis descriptivo de las variables del estudio mediante medidas de resumen como frecuencias absolutas y relativas para las variables cualitativas (sexo, afiliación al sistema de salud, nivel educativo, comorbilidades, tipo de diabetes mellitus, episodios de hipoglucemia severa y no severa, antecedentes de hospitalizaciones por complicaciones y/o descompensación aguda asociadas a la enfermedad, tratamiento recibido previo a la instalación del dispositivo, complicaciones micro y macrovasculares por la diabetes en el momento del inicio de la terapia con bomba de insulina).
Para las variables cuantitativas de edad, índice de masa corporal, hemoglobina glucosilada (HbA1C) en el momento de la instalación del dispositivo, número de hospitalizaciones al año por causas relacionadas con la diabetes, tiempo entre el diagnóstico de diabetes y el inicio de la terapia con CSII-rtCGM, tiempo entre el inicio de la terapia con CSII y la instalación del sensor de monitorización continua de glucosa en tiempo real (rtCGM), se obtuvieron las medidas de tendencia central (promedio o mediana) y de dispersión (desviación estándar rango intercuartílico: percentil 25-percentil 75) según la distribución normal de la variable evaluada con la prueba Kolmogorv-Smirnov. No se realizaron comparaciones ni se establecieron medidas de asociación en el estudio.
Las hipoglucemias severas fueron definidas como eventos que requerían asistencia de otra persona para administrar activamente hidratos de carbono, glucagón o hacer cualquier otra medida correctiva. Aunque las mediciones plasmáticas pueden no estar disponibles durante el evento, la recuperación neurológica que sigue a la normalización de los valores de glucosa se consideró suficiente evidencia de la hipoglucemia. Consideramos hipoglucemia sintomática todo episodio de glucosa menor de 70mg/dl en un paciente diabético asociado a síntomas y signos de neuroglucopenia y autonómicos que se resuelve con la ingesta de hidratos de carbono (tríada de Whipple). Por su parte, las hipoglucemias asintomáticas o sin síntomas de alarma se definieron como todo episodio de glucosa menor de 70mg/dl en un paciente diabético no asociado a síntomas. Las hipoglucemias sintomáticas y asintomáticas que no cumplen criterios de severas fueron consideradas como no severas, y podían o no ser nocturnas y/o asociadas al ejercicio.
Todos los pacientes recibieron entrenamiento por un grupo multidisciplinario que incluía una educadora en diabetes, un nutricionista y un médico endocrinólogo. El sistema utilizado en todos los casos fue Paradigm VEO de Medtronic.
El protocolo de investigación fue evaluado y avalado por el comité de ética universitario adscrito al centro especializado en endocrinología.
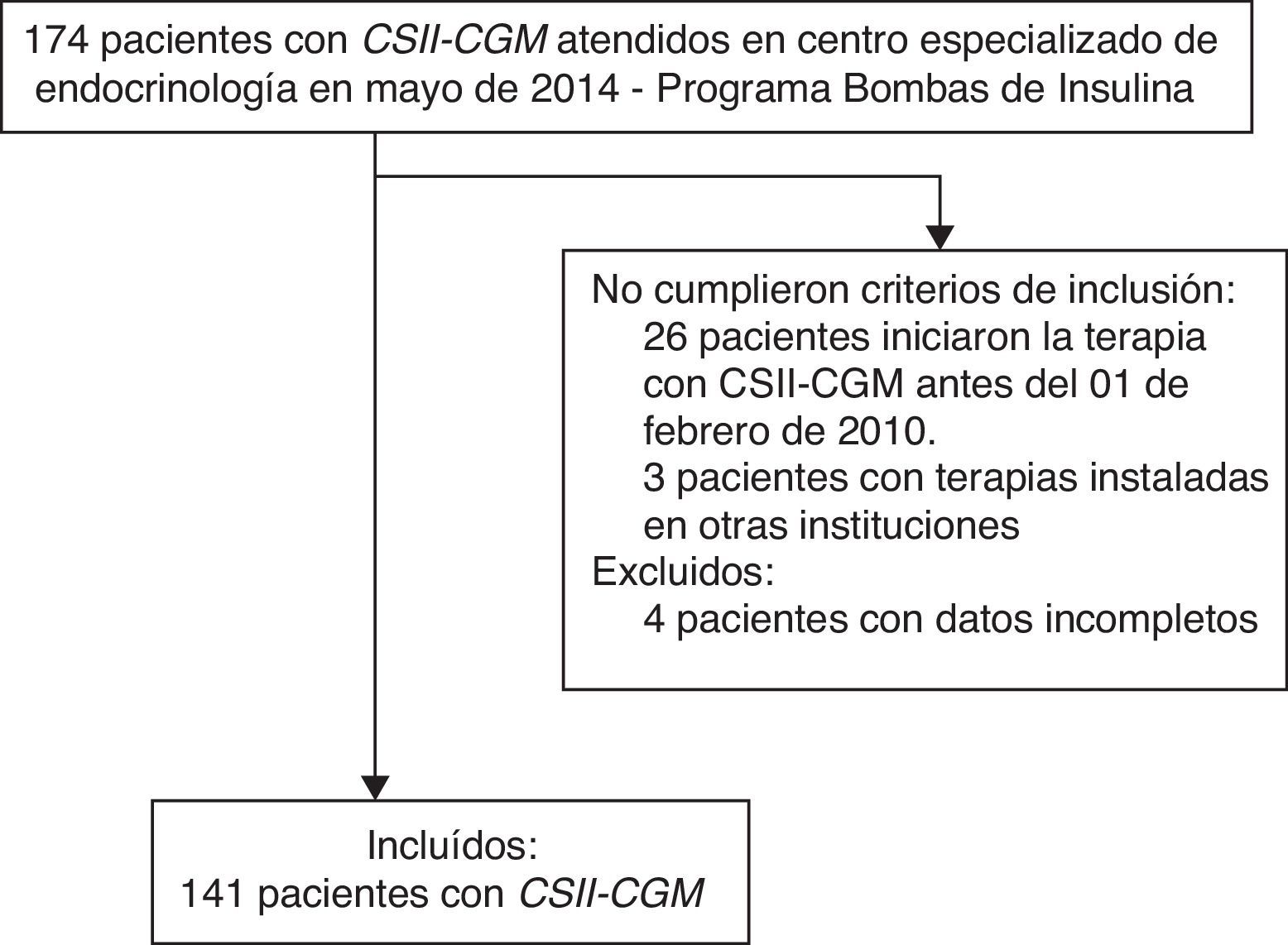
ResultadosSe identificaron 174 pacientes en terapia con CSII-rtCGM atendidos en la institución hasta mayo de 2014. Se incluyeron 141 pacientes diabéticos que cumplieron los criterios de elegibilidad y se excluyeron 4 pacientes por registros incompletos (fig. 1). Un 90,1% (127/141) de los pacientes tenía DT1, 3 pacientes se encontraban en estado de gestación en el momento de la instalación de la terapia y el 9,9% (14/141) tenía DT2.
La edad de los pacientes fue en promedio 33,6±15 años, 54,0±13,7 años en pacientes con DT2 y 31,4±14,1 años en DT1; 20,6% eran menores de 18 años. Un 70,2% de los pacientes eran de sexo femenino; 56,0% tenían formación secundaria, 30,5% profesional, 12,1% primaria y 1,4% de posgrado. Todos los pacientes del estudio estaban afiliados al régimen contributivo del sistema de salud colombiano. En el momento de la instalación del dispositivo el 4,3% de los pacientes tenía tabaquismo activo y el 6,4% reportó ser exfumador. El 41,1% de los pacientes reportó en la historia clínica la realización de ejercicio.
La mediana del índice de masa corporal (IMC) fue de 23,3 (P25-P75=20,7-24,8); el 75,8% de los pacientes tenía peso normal (IMC<25), el 21,0% tenía sobrepeso (IMC >25 y <30) y el 2,3% era obeso (IMC≥30). Si consideramos solamente los pacientes diabéticos tipo 1 la mediana del IMC fue de 22,0 (P25-P75=20,0-24,0) y en los pacientes con DT2 la mediana fue de 28,0 (P25-P75=23,0-29,0).
La mediana de duración de la diabetes en los pacientes evaluados fue de 13,0 años (P25-P75=10,7-22,0). En cuanto a las complicaciones microvasculares asociadas a la diabetes el 9,9% de los pacientes presentaban retinopatía diabética, siendo proliferativa en la mayoría de los casos (12/14). La nefropatía se encontró en el 15,6% de los individuos diabéticos; a uno de ellos además se le realizó trasplante renal por esta causa. La neuropatía se observó en el 14,2% de los casos, siendo la neuropatía sensitiva la más frecuente (17/20), seguida de disfunción eréctil (2/20) y gastroparesia (1/20). Solo un paciente presentó pie diabético. Se identificaron 3 pacientes con al menos una complicación macrovascular como enfermedad cerebrovascular, fallo cardíaco secundario a enfermedad coronaria, enfermedad arterial oclusiva crónica y claudicación intermitente.
En el 31,2% de los casos se identificó además de la diabetes enfermedad tiroidea (disfunción tiroidea autoinmune tributaria de tratamiento), el 27,0% de los pacientes padecía además dislipidemia, el 20,6% hipertensión arterial y el 6,4% otra enfermedad autoinmune asociada diferente a enfermedad tiroidea.
El 14,2% de los pacientes fue hospitalizado al menos una vez en el año previo al inicio de la terapia con CSII-rtCGM por causas relacionadas con la diabetes. La frecuencia de hospitalización observada fue de 0,3 hospitalizaciones/paciente/año (rango=0-13).
La mediana de glucometrías al día fue de 6,0 (P25-P75=4,0-6,0). Antes de la instalación de la terapia con CSII-rtCGM el 95,0% de los pacientes reportó al menos un episodio de hipoglucemia en el último año y el 39,0% de los pacientes reportó al menos un episodio de hipoglucemia severa. La tasa de hipoglucemia severa fue de 14,7 episodios/paciente/año. Las hipoglucemias no severas fueron reportadas como sintomáticas en el 49,6% de los casos, sin clasificar el 40,6% y finalmente asintomáticas en el 9,8%, determinadas estas últimas por el hallazgo de un valor por debajo de 70mg/dl en el registro de automonitorización y la ausencia de síntomas neuroglucopénicos informados por el paciente.
Todos los pacientes recibían insulina en esquema basal/bolo con análogos de insulina como tratamiento de la enfermedad antes del inicio de la terapia con CSII-rtCGM. Un 7,8% de los pacientes recibía conjuntamente esquemas de insulina con hipoglucemiantes orales, principalmente metformina.
Al inicio de la terapia el promedio de HbA1C era de 8,6%±1,4, siendo de 8,5±0,1 en pacientes con DT1 y de 9,1±0,3 en DT2.
Las principales indicaciones halladas para la formulación de la infusión continua de insulina con monitorización continua de glucosa se presentan en la figura 2. Un 59,5% de los pacientes tenía más de una indicación para la bomba, siendo el mal control glucémico y las hipoglucemias severas la combinación más frecuente.
En cuanto a los parámetros de formulación del infusor subcutáneo continuo de insulina, conforme a las normas generales de inicio de terapia con SCII-rtCGM, la mediana de basales (número de tasas basales a lo largo del día programadas para cada paciente) al inicio fue de 1,0 (P25-P75=1,0-1,0) y la de la sensibilidad (factor de sensibilidad insulínica) de 50,0 (P25-P75=50,0-50,0), la cual fue calculada con la fórmula 1.700/dosis total de insulina diaria.
En 4 de los pacientes analizados el sensor fue instalado días antes del dispositivo; en la mayoría de los pacientes (61,0%) la instalación fue simultánea. Por su parte, en 49 pacientes (34,7%) la instalación del sensor fue en los 3 meses siguientes a la instalación del infusor, y en 2 pacientes fue posterior a un año (457 y 744 días); la educación del paciente fue el criterio fundamental para elegir el momento de la instalación del sensor.
DiscusiónLas terapias intensivas de insulina tradicionalmente implican múltiples inyecciones diarias5, y así como mejoran el control glucémico, la frecuencia de los episodios de hipoglucemia también tiende a aumentar4, por lo que se requieren esquemas que permitan el aporte suficiente de insulina y minimicen los riesgos de hipoglucemias mediante la monitorización frecuente de la glucemia. Innovaciones en la administración de insulina y la monitorización de glucosa han sido diseñadas en un afán por mejorar el control glucémico y la calidad de vida de los pacientes. Estos avances incluyen las terapias con CSII-rtCGM, que permiten realizar infusiones subcutáneas continuas y la monitorización continua de glucosa en tiempo real5,7.
La edad de los pacientes en el momento del inicio de la terapia con CSII-rtCGM es variable si consideramos pacientes con DT1, DT2 o ambos; la edad de los pacientes fue en promedio 33,6±15 años en nuestro estudio (90,1% con DT1), muy similar a lo reportado previamente en otro trabajo, que describió una cohorte con el 91,7% de sus pacientes diabéticos tipo 1 (34,1±17,1 años)14; si consideramos solamente a los pacientes tipo 1 el promedio de edad fue de 31,4±14,0, lo cual está acorde con la mayoría de los estudios reportados en la literatura15–24, siendo este promedio mayor en los pacientes diabéticos tipo 2 (54,0±13,7), como también ha sido descrito25–27. La eficacia y seguridad de las terapias con CSII-rtCGM ha sido probada en pacientes ancianos con DM226 y en pacientes mayores de 50 años con DT128.
Al considerar las mujeres gestantes que usan este tipo de terapias los datos son escasos, pero parecen ser promisorios en este grupo de pacientes12; en nuestro estudio 3 pacientes con DT1 se encontraban en estado de gestación. El IMC de la población analizada es similar al reportado en otros estudios que evalúan pacientes diabéticos que iniciaron la terapia con CSII-rtCGM14,15,17,18,20–23; los estudios que incluyen solo pacientes diabéticos tipo 2 reportan un IMC superior25–27.
El porcentaje de pacientes diabéticos con tabaquismo activo que inician terapia con CSII-rtCGM ha sido reportado entre el 4,0% y el 22,8%17,21,25,26.
Aunque el tiempo de duración de la enfermedad o años transcurridos entre el diagnóstico de la diabetes y la instalación del dispositivo es de alrededor de 13,0 años14,17–23,25–27, existen trabajos en pacientes DT1 que inician la terapia con CSII-rtCGM en el momento del diagnóstico o poco tiempo después (3,3±3,0 años)16.
Las complicaciones crónicas asociadas a la diabetes son comunes; la retinopatía en pacientes diabéticos se reporta del 21,0% al 77,0%14,15,20,25–27, porcentaje variable considerando que este dependerá del tipo de diabetes y del tiempo transcurrido de la enfermedad; sin embargo, en nuestra cohorte el porcentaje encontrado fue mucho menor. La frecuencia de nefropatía y neuropatía coincide con la reportada en otros estudios15,20,25–27. Es llamativo que la frecuencia de retinopatía sea inferior a la de nefropatía en nuestra cohorte, lo cual pudiera explicarse por no contar con los reportes de las valoraciones de oftalmología en todos los casos o por la tendencia a iniciar terapias con CSII-rtCGM en pacientes con diabetes mal controlada y evidencia de nefropatía diabética, lo cual constituiría un sesgo de selección.
Asimismo, el porcentaje de complicaciones macrovasculares de nuestro estudio coincide con el reportado en pacientes DT114,15, pero es muy inferior si se compara con los datos reportados en DT225,26.
Se han reportado en la literatura frecuencias de hospitalización de los pacientes diabéticos antes de iniciar la terapia con CSII-rtCGM de 8,5 días/paciente/año20. En nuestro caso no fue posible cuantificar los días de hospitalización por paciente, sin embargo se pudo establecer que el 14,2% de nuestros pacientes tuvo al menos un episodio de hospitalización por causas relacionadas con la diabetes en el año previo al inicio del tratamiento nuevo; con una frecuencia de hospitalización de 0,3 hospitalizaciones (eventos)/paciente/año no descartamos que haya subestimación en esta variable por problemas de reporte.
Los pacientes incluidos en este estudio tuvieron una mediana de 6,0 glucometrías al día. Esta medición se hizo posterior al inicio del programa educativo justo antes de la instalación del dispositivo, lo cual sugiere que los pacientes se adherían al tratamiento y que probablemente la educación brindada por nuestro grupo influyó en este resultado. En nuestro estudio el 95,0% de los pacientes antes de la terapia reportó hipoglucemias, y esta fue la indicación para el uso del dispositivo en casi la mitad de los casos. Una nueva herramienta de las bombas de insulina con sensor de monitorización continua de glucosa permite fijar un valor umbral de glucosa de referencia por debajo del cual se suspende la infusión de insulina evitando los episodios de hipoglucemia severa. Estudios recientes que evaluaron esta estrategia demuestran que se reducen los episodios de hipoglucemia nocturna sin alterar el control glucémico18. Hasta el 10,6% de los pacientes diabéticos en terapia con múltiples dosis de insulina reporta al menos un episodio de hipoglucemia severa en el último mes, y la frecuencia de hipoglucemias reportadas al mes (considerando severas y no severas) es de 3,3+3,5 (media+SD)17. El 39,0% de los pacientes de la población evaluada reportó al menos un episodio de hipoglucemia severa en el último año, y la tasa de hipoglucemia severa fue de 14,7 episodios/paciente/año. En otro estudio el 13,6% de los pacientes reportó haber experimentado hipoglucemias severas el año anterior al inicio del nuevo tratamiento con el dispositivo19.
Pacientes diabéticos tipo 1 con hipoglucemias inadvertidas y/o marcado aumento de los valores de glucosa en el alba, a pesar de ajustes en la terapia intensiva con regímenes de múltiples inyecciones diarias de insulina, son buenos candidatos a la terapia con CSII-rtCGM24. La mayoría de los estudios que evalúan la eficacia y seguridad de la terapia con CSII-rtCGM tienen como principal indicación el mal control glucémico a pesar de la implementación de las terapias intensivas convencionales14–17,19–28; otros estudios, por su parte, consideran el uso de estos dispositivos en casos de hipoglucemias severas, inadvertidas o nocturnas14,18.
La hemoglobina glucosilada media reportada en la literatura en el momento de iniciar la terapia con bomba de insulina en los ensayos clínicos en pacientes diabéticos tipo 1, que comparan su eficacia y seguridad con los esquemas convencionales intensivos, es de 8,3±0,5 y de 8,4±0,9 (media±SD), los cuales se acercan mucho a nuestra experiencia19,21. Evaluaciones retrospectivas encuentran niveles de HbA1C medias de 8,0%±0,9 y 8,9±1,9 al inicio de la terapia con este dispositivo14. Los niveles de HbA1C son mucho menores (7,2%+0,7) en pacientes con inicio del tratamiento relacionado con hipoglucemias nocturnas18.
Cerca del 30,0% de los pacientes diabéticos tipo 2 tienen pobre control glucémico a pesar de instaurar las guías de práctica clínica, y tienen niveles de HbA1C mayores a 8,0%25. La terapia con CSII-rtCGM pudiera ser una alternativa en este contexto, dado que los pacientes con DT2 pueden ser entrenados para el uso de esta, y pudiera considerarse cuando estén indicados regímenes intensivos de insulina26,27. Un estudio reportó el uso de la terapia CSII-rtCGM asociada a hipoglucemiantes orales en un grupo de pacientes diabéticos tipo 2, con HbA1C media de 9,4±0,8%25. Valores iniciales de HbA1C de 8,2%±1,3% y de 8,4±1,1% (media±SD) también han sido reportados en la literatura para el inicio de la terapia con CSII-rtCGM en diabéticos tipo 226,27.
La tercera parte (31,2%) de nuestros pacientes tiene disfunción tiroidea autoinmune tributaria de tratamiento, además de la diabetes, lo cual constituye un hallazgo importante, y dado que el 90,1% de los pacientes son DT1 se justifica entonces la tamización con pruebas de función tiroidea en este grupo poblacional acorde a las guías. Otras comorbilidades, como la hipertensión arterial, reportada hasta en el 76,4%25 de los pacientes con DT2, se encontró en un porcentaje menor en nuestra cohorte, probablemente explicado por la mayor cantidad de pacientes con DT1, pero el porcentaje de dislipidemia fue cercano a los datos reportados previamente25,26. Aunque el 6,4% de los pacientes estudiados reportó al menos otra enfermedad autoinmune diferente a la enfermedad tiroidea, no se encontraron datos reportados en la literatura de la frecuencia de otras enfermedades autoinmunes en pacientes diabéticos que inician terapia con CSII-rtCGM.
Todas las terapias con CSII-rtCGM de nuestro centro se iniciaron utilizando análogos de la insulina. Los análogos de la insulina resultan en una reducción significativa (0,2%) en la HbA1C comparado con la insulina cristalina cuando se usa en los dispositivos de infusión continua subcutánea de glucosa, y tienen una mayor preferencia por el paciente29. Algunos estudios reportan menos episodios de hipoglucemia con los análogos de insulina, pero esto es variable de acuerdo a la definición usada; no se encuentran diferencias en la dosis de insulina ni en el peso al compararlos con la insulina cristalina29.
El inicio de la monitorización continua de glucosa en forma simultánea o muy cercano a la instalación del sistema de infusión continua subcutánea de insulina pudiera favorecer la adherencia al mismo; dado que su eficacia está directamente relacionada con los días de uso, nuestro centro realiza la instalación de ambos sistemas de forma simultánea o en los 3 meses siguientes a la instalación del infusor, lo cual es autorizado por el sistema de salud colombiano. Se encuentra actualmente en curso un ensayo clínico controlado en niños y adolescentes (5,0-18,0 años) diabéticos tipo 1 que iniciarán terapia con CSII-CGM comparando el inicio de ambos sistemas de forma simultánea o iniciando con el infusor y la instalación del sensor 6 meses después, teniendo como objetivo determinar si esto tiene implicaciones en la eficacia y seguridad del tratamiento en este grupo poblacional16 que se ha reconocido como uno de los menos adherentes30.
En cuanto a las limitaciones de nuestro estudio, es de reconocer su naturaleza retrospectiva y el posible sesgo de selección, dado que se trata de pacientes atendidos en un centro especializado en endocrinología de la ciudad de Medellín (Colombia), pero considerando que se trata de una terapia novedosa se justifica la descripción de estos individuos. Hay que resaltar, sin embargo, que del total de los pacientes que cumplían los criterios de inclusión para el estudio solo fueron excluidos 4 pacientes por datos incompletos, lo que sugiere que el diligenciamiento de las historias era completo.
Las características de los pacientes que inician terapia con CSII-rtCGM en nuestra experiencia son similares a las reportadas en la literatura. Los resultados muestran que el centro especializado inicia esta terapia principalmente en pacientes con DT1 con mal control glucémico a pesar de la terapia intensiva, hipoglucemias leves persistentes o hipoglucemias severas.
Conflicto de interesesDeclaramos que ninguno de los investigadores tiene conflicto de intereses.