Durante la gestación, las alteraciones de la función tiroidea se asocian a múltiples complicaciones, tanto maternas como fetales. En los últimos años se han elaborado numerosas guías de práctica clínica para facilitar la identificación y correcto manejo de la patología tiroidea en la gestante. Esta proliferación de guías ha causado confusión al proponer distintos puntos de corte de valores de normalidad y distintas recomendaciones ante situaciones similares. Por ello, la Sociedad Española de Endocrinología y Nutrición y la Sociedad Española de Ginecología y Obstetricia han elaborado el presente Documento de Consenso, con el objetivo de crear un marco de actuación conjunto que unifique criterios de diagnóstico y tratamiento de la disfunción tiroidea en estas pacientes. El documento se estructura respondiendo a las preguntas más frecuentes que se plantean en la práctica clínica, agrupándose en 5 apartados: 1/Valores de referencia de pruebas de función tiroidea y cribado durante la gestación, 2/Nutrición de yodo, 3/Hipotiroidismo y gestación, 4/Hipertiroidismo y gestación y 5/ Autoinmunidad tiroidea.
During pregnancy, thyroid function disorders are associated with multiple complications, both maternal and foetal. In recent years, numerous Clinical Practice Guidelines have been developed to facilitate the identification and correct management of thyroid disease in pregnant women. However, this proliferation of guidelines has led to confusion by proposing different cut-off points for reference values and different recommendations for similar situations. For this reason, the Sociedad Española de Endocrinología y Nutrición and the Sociedad Española de Ginecología y Obstetricia have prepared this Consensus Document, with the aim of creating a framework for joint action to unify criteria for the diagnosis and treatment of thyroid dysfunction in these patients. The document is structured to answer the most frequently asked questions in clinical practice, grouped into five sections: 1/Reference values for thyroid function tests and screening during pregnancy 2/Iodine nutrition 3/Hypothyroidism and pregnancy 4/Hyperthyroidism and pregnancy 5/ Thyroid autoimmunity.
Las alteraciones de la función tiroidea son muy frecuentes en las mujeres en edad fértil. Dada su asociación durante la gestación con múltiples complicaciones, tanto maternas como fetales, se han elaborado diversas guías de práctica clínica para orientar en la identificación y correcto manejo de la patología tiroidea en la gestante. Durante la última década las sociedades científicas más relevantes han elaborado diferentes guías: American Thyroid Association (ATA) 2011, Endocrine Society 2012, European Thyroid Association (ETA) 2014, ATA 20171 y American College of Obstetricians and Gynecologists (ACOG) 2020. Esta proliferación de guías ha contribuido a aumentar la confusión al proponer diferentes puntos de corte de valores de normalidad y distintas recomendaciones ante situaciones similares.
Por este motivo, las Juntas Directivas de la Sociedad Española de Endocrinología y Nutrición (SEEN) y la Sociedad Española de Ginecología y Obstetricia (SEGO) han impulsado la redacción de un Documento común de Consenso, para que los facultativos de ambas especialidades tengan un marco de actuación conjunto, con los mismos criterios de diagnóstico y tratamiento de estas pacientes.
Se propusieron 3 expertos por cada especialidad quienes diseñaron un panel de 21 preguntas, agrupadas en 5 temas:
- -
Valores de referencia de pruebas de función tiroidea, clasificación de las disfunciones y cribado durante la gestación.
- -
Nutrición de yodo.
- -
Hipotiroidismo y gestación.
- -
Hipertiroidismo y gestación.
- -
Autoinmunidad tiroidea en gestación y posparto.
El objetivo ha sido dar respuesta a las preguntas planteadas mediante un enfoque eminentemente práctico, pretendiendo sentar las bases de un abordaje terapéutico consensuado. Los niveles de evidencia de las recomendaciones se han establecido siguiendo los de las guías clínicas precedentes.
Valores de referencia, clasificación de las disfunciones y cribado¿Cuáles son los valores normales de las pruebas de función tiroidea durante el embarazo?De acuerdo con la Guía ATA 2017, siempre que sea posible, deben definirse rangos de referencia de TSH basados en la población de referencia y específicos para cada trimestre. (Recomendación fuerte, evidencia moderada)1.
En caso de no disponer de rangos de referencia propios, la guía ATA sitúa el límite superior de TSH en el primer trimestre en 4mU/L.
¿Cuál es el momento adecuado para hacer el cribado de disfunción tiroidea en la mujer gestante?Este punto de corte es válido cuando la determinación de TSH se realiza entre las semanas 7-12 de gestación. En España, dado que el análisis bioquímico del programa de Detección Precoz de Aneuploidías tiene lugar entre las 9-11 semanas, la recomendación más práctica es unificar ambos programas de cribado (tabla 1).
Esquema de valores de referencia de TSH en primer trimestre
| CON rangos de referencia propios | SIN rangos de referencia propios |
|---|---|
| Elaborados en CADA laboratorio a partir de una muestra representativa de: | Límite superior: 4,0mU/La |
| Mujeres sin patología tiroidea | Límite inferior: 0,1mU/La |
| Con buena nutrición yódica | |
| Anticuerpos antitiroideos negativos | |
| Serán específicos para cada Plataforma de laboratorio, dependiendo de la marca de sus reactivos o especificaciones técnicas | Pueden usarse en cualquier ámbito asistencial |
| Tiempo de realización: 9-11 semanas, conjuntamente con cribado bioquímico de aneuploidías |
La evaluación inicial de la función tiroidea se realiza mediante la determinación de TSH. Las distintas posibilidades de disfunción tiroidea se recogen en la tabla 2.
Resumen de las posibles combinaciones que incluye la disfunción tiroidea
| TSH | T4 y/o T3 | ||
|---|---|---|---|
| Hipotiroidismo | TSH>percentil 95RR o | Clínicoa | ↓ |
| TSH>4mU/L | Subclínico | Normal | |
| Hipertiroidismo | TSH<percentil 5RR o | Clínico | ↑ |
| TSH<0,1mU/L | Subclínico | Normal |
RR: rangos de referencia propios (ajustados para cada población y trimestre).
Otras alteraciones tiroideas:
- a)
Hipotiroxinemia materna aislada: Descenso de los niveles plasmáticos de T4, con una TSH normal. La causa más frecuente en nuestro medio es la deficiencia nutricional de yodo.
- b)
Autoinmunidad tiroidea: Presencia de anticuerpos (Ac) antitiroideos, principalmente antiperoxidasa tiroidea (anti-TPO) y antitiroglobulina. Su positividad implica una mayor susceptibilidad tanto al hipo como al hipertiroidismo y se asocia con un peor pronóstico reproductivo.
Un debate reiterado es la necesidad de realizar un cribado universal de la función tiroidea durante el embarazo (a todas las gestantes) o de manera selectiva (solo en pacientes consideradas de riesgo).
Desde la SEEN-SEGO, fuimos pioneros a la hora de argumentar las razones a favor de un cribado universal de patología tiroidea en primer trimestre de gestación2. Las estrategias de cribado recomendadas están recogidas en la tabla 3.
Estrategias de cribado de disfunción tiroidea
| Momento de realización | Prueba solicitada | Actitud a seguir | |
|---|---|---|---|
| Gestantes sanas | 9-11 semanas | TSH | -- TSH> 10 mU/L: Tto con Levotiroxina (LT4)-- TSH> 2,5 Valorar pedir anti-TPO*-- TSH <0,1 Pedir TSI y valorar βhCG |
| Pacientes de alto riesgo obstétrico: | |||
| -- Infertilidad previa.-- Abortos de repetición.-- Muerte intraútero.-- Parto pretérmino | Idealmente, preconcepcionalo en el momento de confirmar embarazo (test de gestación positivo) | TSHT4LAnti-TPO | -- Si TPO Positivo: Tto con LT4 a partir de TSH> 2,5 mU/L.-- Si TPO Negativo: Tto con LT4 a partir de TSH>4,0 mU/L |
| Pacientes con patología tiroidea previa: | |||
| Hipotirodismo | Idealmente, preconcepcionalo en el momento de confirmar embarazo (test de gestación positivo) | TSHT4LAnti-TPO** | De entrada, aumentar un 30% la dosis preconcepcional de LT4. |
| Hipertirodismo | Idealmente, preconcepcionalo en el momento de confirmar embarazo (test de gestación positivo) | TSHT4L, T3TSI*** | Si hipertiroidismo activo o en tratamiento antes de la gestación, derivar a Endocrinología-- Si TSI positivos: Compatible con enfermedad de Graves.-- Si TSI negativos: Considerar otras posibles causas (nódulo tóxico, tiroiditis). |
Valorar solicitar anti-TPO especialmente en casos con historia personal o familiar de enfermedad autoinmune
El yodo es un micronutriente esencial imprescindible para la síntesis de las hormonas tiroideas, estando aumentadas sus necesidades nutricionales durante el embarazo3.
La ingesta de yodo recomendada por la OMS es de 250μg/día. Asimismo, establece un umbral de 500μg/día por encima del cual no se consiguen beneficios adicionales e incluso podría inducir alteraciones de la función tiroidea. Por otra parte, el Institute of Medicine en EE. UU. fija las necesidades en 220μg/día durante el embarazo y 290μg/día durante la lactancia4.
¿Se recomienda su suplementación farmacológica durante el mismo?Las fuentes nutricionales de yodo son:
- a)
Sal yodada: constituye el mejor vehículo dietético para garantizar un aporte adecuado de yodo.
- b)
Leche y derivados lácteos:: es una fuente emergente de ingesta de yodo, especialmente en los niños de edad escolar.
- c)
Pescado: aunque su contenido en yodo puede ser elevado, se considera insuficiente para garantizar los requerimientos diarios de la gestación.
Para aportar 250μg/día de yodo, deben ingerirse 3 raciones de leche o derivados y 2g de sal yodada a diario. Es necesario llegar a la gestación con una adecuada repleción de los depósitos, lo que obliga a un consumo de sal yodada durante al menos 2 años previos al embarazo.
Los métodos para garantizar una adecuada ingesta de yodo serían:
- a)
Alimentos ricos en yodo: Los referidos en el punto anterior.
- b)
Suplementos farmacológicos: Tienen un contenido en yodo entre 150 y 300μg por comprimido y se comercializan solos o asociados con ácido fólico y vitamina B12. Están recomendados cuando no existen garantías de una ingesta de yodo adecuada. (Recomendación fuerte, evidencia moderada)1.
- c)
Complejos polivitamínicos que contienen yodo: Aunque en ficha técnica su contenido en yodo oscila entre los 150-225μg, su contenido real es muy variable y no siempre ajustado al indicado en la etiqueta.
Cuando no hay seguridad de una ingesta adecuada de yodo, se recomienda el uso de suplementos de yoduro potásico, que se deben iniciar de manera preconcepcional, al menos 2 meses antes, para conseguir unos depósitos de yodo adecuados al inicio del embarazo y mantenerlos hasta la finalización de la lactancia materna exclusiva.
En los casos de hipertiroidismo por enfermedad de Graves-Basedow se aconseja suspender la sal yodada y evitar la suplementación con yodo. La actitud frente a un bocio multinodular es similar. Las mujeres hipotiroideas, aunque estén en tratamiento con levotiroxina, deben realizar una ingesta adecuada de yodo.
¿Se recomienda su suplementación farmacológica durante el posparto y la lactancia?La indicación de mantener suplementos farmacológicos de yodo tras el parto vendrá condicionada por el tipo de lactancia:
- -
En las madres que optan por una lactancia artificial no son necesarios, dado que estas leches ya contienen yodo.
- -
En los casos de lactancia mixta (materna-artificial) dependerá de la proporción de ambas. Cuanta más lactancia materna, mayores serán las necesidades de yodo de la madre.
- -
En caso de lactancia materna exclusiva, los suplementos yodados deben mantenerse durante toda la lactancia.
Las mujeres con un hipotiroidismo conocido deben planificar su embarazo para reducir la tasa de complicaciones. Se recomienda una concentración de TSH<2,5mU/L. (Recomendación fuerte, evidencia moderada)1.
¿Por qué un límite de 2,5mU/L en la pregestación de las mujeres hipotiroideas, cuando el punto de corte en las gestantes eutiroideas es de 4,0mU/L? Porque así se garantiza que se pueda hacer frente al aumento de requerimientos hormonales de la gestación.
¿Cómo debería ser el manejo de las gestantes con hipotiroidismo clínico? (Incluyendo las diagnosticadas previamente al embarazo)El hipotiroidismo clínico se asocia a múltiples complicaciones maternas (aborto, anemia, hipertensión y preeclampsia, abruptio placentae, amenaza y parto pretérmino, hemorragia posparto…) y fetales o neonatales (muerte intraútero, bajo peso al nacer, distrés respiratorio neonatal..)5.
El manejo de las gestantes con hipotiroidismo clínico previo al embarazo difiere del de las diagnosticadas durante el mismo y está recogido en la tabla 4.
Manejo del hipotiroidismo clínico
| Hipotiroidismo clínico TSH>10mU/LTSH>4mU/l con T4 bajaTSH>95thRR con T4 baja | |||
|---|---|---|---|
| Conocido antes de la gestación | Diagnosticado en la gestación | ||
| Bien controlado | Mal controlado | ||
| En preconcepción | Evitar embarazo hasta alcanzar una TSH<2,5mU/L | No control preconcepcionalNo cumplidoras de tratamiento oEscasa respuesta al incremento de dosis | No hay suficiente evidencia para establecer un cribado de disfunción tiroidea preconcepcional a excepción de las mujeres con historia de infertilidad |
| Iniciada gestación | Los requerimientos de tiroxina aumentan desde las 4-6 semanas | El incremento de dosis en mujeres con hipotiroidismo no controlado en el primer trimestre disminuye el riesgo de pérdida fetal | Aproximadamente el 0,65% de las embarazadas teóricamente sanas presentan un hipotiroidismo clínico no conocido, que solo puede detectarse mediante cribado |
| Premisas | Aunque la ATA recomienda aumentar la dosis de LT4 en un 20-30% en el momento de la confirmación de embarazo, el incremento de dosis tendrá mucho que ver con la etiología del hipotiroidismo y con el nivel de TSH preconcepcionalPacientes con una tiroidectomía o ablación tiroidea requerirán dosis más altas que las de un hipotiroidismo autoinmune | No existe una recomendación estándar para este grupo de pacientes | Los factores que determinan la dosis apropiada al inicio son:Edad gestacional en el momento del diagnósticoEtiología y severidad del hipotiroidismo |
| Plan | Si antes de la gestación la TSH está entre 2,5 y 4mU/L o entre 2,5mU/L y 95thRR aumentar dosis de LT4 en:Hipotiroidismo primario autoinmune: ꝉ25-30% (doblar dosis 2 días por semana)Hipotiroidismo por ablación: ꝉ 40-45% (doblar dosis 3 días por semana)Si antes de la gestación la TSH está entre 5thRR/<1,2mU/L, no modificar la dosisControl cada 4 semanas hasta alcanzar TSH<2,5mU/L | Algunos autores proponen duplicar la dosis habitual de LT4 3 días a la semana (aumento alrededor del 40%) y titular cada 4 semanas hasta alcanzar la TSH<2,5mU/L | Empezar con una dosis calculada, a razón de 2,3μg/kg/día de LT4En pacientes con hipotiroidismo clínico severo (TSH>10mU/L) puede administrarse al inicio una dosis superior (hasta el doble) de lo calculado, con objeto de normalizar cuanto antes el depósito extratiroideo de tiroxina |
- -
Se realizará mediante determinaciones seriadas de TSH. La primera determinación debe hacerse en el momento en que se confirme el embarazo.
- -
El control se realizará cada 4 semanas. Periodos más cortos pueden inducir sobretratamiento.
- -
Alcanzado el objetivo terapéutico de TSH<2,5mU/L, los controles de TSH pueden hacerse cada 4 semanas, hasta llegar a la semana 20 y, al menos otra vez, antes de la semana 30. (Recomendación fuerte, evidencia alta)1.
- -
En caso de suplementación con hierro, debido a su interferencia sobre la absorción de la LT4, se debe establecer una separación mínima de 4h entre la toma del hierro y de LT4.
- -
Confirmar que la ingesta de LT4 sea 30min antes del desayuno para evitar una disminución de su absorción. En caso de vómitos matinales frecuentes, aconsejar la toma de LT4 después de cada episodio.
La asociación del hipotiroidismo subclínico (HSC) con complicaciones maternofetales y la recomendación o no de tratamiento es muy controvertida6 al no haber clara evidencia de que la intervención con LT4 pueda prevenir eventos perinatales adversos.
Por ello, las recomendaciones a favor y en contra del tratamiento debieran aplicarse de una forma individualizada, valorando los pros y los contras del tratamiento. Los distintos escenarios posibles y las recomendaciones de tratamiento están recogidos en la tabla 5.
Indicaciones de tratamiento con levotiroxina (LT4) durante el embarazo, teniendo en cuenta los principales resultados (maternos y neonatales)
| Recomendación | Pros | Contras | |
|---|---|---|---|
| Resultados maternos | |||
| TPO positivos | |||
| TSH>10mU/L | LT4 está fuertemente recomendada | El tratamiento del hipotiroidismo clínico reduce el riesgo de complicaciones obstétricas | Ninguno |
| TSH 4,0-10,0mU/L | LT4 está recomendada | El tratamiento de este grupo reduce las complicaciones y evita la progresión a hipotiroidismo clínico | La terapia con LT4 debe ser monitorizada para evitar sub/hipertratamiento |
| TSH 2,5-4,0mU/L | Puede considerarse el tratamiento con LT4 | El tratamiento debe restringirse a situaciones de alto riesgo como infertilidad o aborto recurrente (evidencia débil para parto pretérmino) | La recomendación de tratamiento es débilAlto riesgo de sobretratamientoNo evidencia de efectividad para: diabetes gestacional, enfermedad hipertensiva o restricción de crecimiento fetal |
| TSH<2,5mU/L | LT4 no está recomendada | El tratamiento debe restringirse a situaciones de alto riesgo como infertilidad, reproducción asistida o aborto recurrente y considerado de forma individualizada | No hay evidencia de que el tratamiento con LT4 mejore la tasa de fertilidad y no ha demostrado reducir la tasa de abortos en este grupo |
| TPO negativos | |||
| TSH>10mU/L | LT4 está fuertemente recomendada | Es considerado un hipotiroidismo clínico | La calidad de la evidencia es baja |
| TSH 4,0-10,0mU/L | LT4 está recomendada | El riesgo es similar al del HSC con TPO positivos cuando la TSH está entre 5-10mU/L | Recomendación débilLa calidad de la evidencia es bajaEl tratamiento debe ser considerado con cautela en ausencia de rangos de referencia propios |
| TSH 2,5-4,0mU/L | El tratamiento con LT4 no debe usarse | Pueden usarse bajas dosis de LT4 en mujeres sometidas a FIV o ICSI, con objeto de conseguir una TSH<2,5mU/L | No hay evidencia de que el tratamiento con LT4 mejore la tasa de fertilidad en mujeres eutiroideas y anti-TPO negativas |
| TSH<2,5mU/L | No se recomienda tratamiento con LT4 | Ninguna | Fuerte recomendación en contra del uso de LT4 en esta situación |
| Potenciales riesgos de uso yatrogénico de LT4 en el embarazo: | |||
| -Restricción de crecimiento | |||
| -Morfología anormal del cerebro en niños | |||
| Función cognitiva de la descendencia | |||
| TSH>10mU/L | LT4 está fuertemente recomendada | Niveles altos de TSH materna no tratados se asocian a bajo cociente intelectual, independiente del test | La efectividad del tratamiento con LT4 está limitada a una intervención precoz (durante primer trimestre) |
| TSH4,0-10,0mU/L | LT4 está recomendada | El tratamiento precoz con LT4 puede mejorar la función cognitiva en la descendencia | La efectividad del tratamiento con LT4 no se ha demostrado de manera concluyente en términos de resultados cognitivos |
| TSH2,5-4,0mU/L | El tratamiento con LT4 no debe usarse | Ninguna | Alto riesgo de sobretratamientoNo evidencia de efectividad en resultados cognitivos |
| TSH<2,5mU/L | No se recomienda tratamiento con LT4 | Ninguna | Fuerte recomendación en contra del uso de LT4 en esta situación |
| Potenciales riesgos de sobretratamiento con LT4 en el embarazo: | |||
| Restricción de crecimiento fetal | |||
| Morfología anormal del cerebro en niños | |||
Fuente: Velasco y Taylor6.
En caso de decidir tratar el HSC, se recomienda iniciar tratamiento con 50μg de LT4 en la mayoría de los casos.
La monitorización se realizará mediante determinaciones seriadas de TSH, estando indicada en todas las pacientes que:
- -
Reciben tratamiento sustitutivo con LT4.
- -
Presentan riesgo de desarrollar un hipotiroidismo clínico: hemitiroidectomía previa o pacientes con anti-TPO positivos. (Recomendación fuerte, evidencia alta)1.
Las mujeres con un hipotiroidismo, clínico o subclínico, adecuadamente tratado no tienen un aumento de complicaciones obstétricas, por lo que no hay indicación de estudios adicionales. (Recomendación fuerte, evidencia moderada)1.
¿Cuál sería la actitud después del parto en el control y tratamiento del hipotiroidismo?Es preciso garantizar un control de la función tiroidea después del parto para lo que proponemos el plan de seguimiento de Stagnaro-Green7 recogido en la tabla 6.
Tratamiento del hipotiroidismo en el posparto
| Diagnóstico | Recomendación posparto | Control posparto |
|---|---|---|
| Hipotiroidismo clínico | Dos tercios de la dosis final de LT4 alcanzada en el embarazo | |
| En caso de tiroiditis de Hashimoto, valorar mantener en un 20% más de LT4 respecto a la dosis pregestacional | 6 semanas | |
| Hipotiroidismo subclínico | Mitad de la dosis final de LT4 alcanzada en el embarazo | |
| Anticuerpos positivos | Si la última dosis era: | 6 semanas |
| Hipotiroidismo subclínico | -- 25μg/día: suspender | 6 semanas |
| Anticuerpos negativos | -- 50μg/día: reducir a 25μg/día | 6 semanas |
| -- 75-100μg/día: reducir a 50μg/día | Cada 6 semanas hasta control | |
| -- >100μg/día: reducir 25μg cada semana hasta llegar a 50μg/día como dosis final |
Fuente: Stagnaro-Green7.
La hipotiroxinemia materna en el primer trimestre de gestación compromete el aporte de tiroxina necesario para un correcto desarrollo neurológico fetal. Sin embargo, ningún estudio publicado ha demostrado que el tratamiento con LT4 mejore el cociente intelectual en la descendencia. Dado que, en nuestro medio, la causa más frecuente de hipotiroxinemia materna es la deficiencia nutricional de yodo, recomendamos suplementarlo precozmente como primera medida de prevención de la hipotiroxinemia materna.
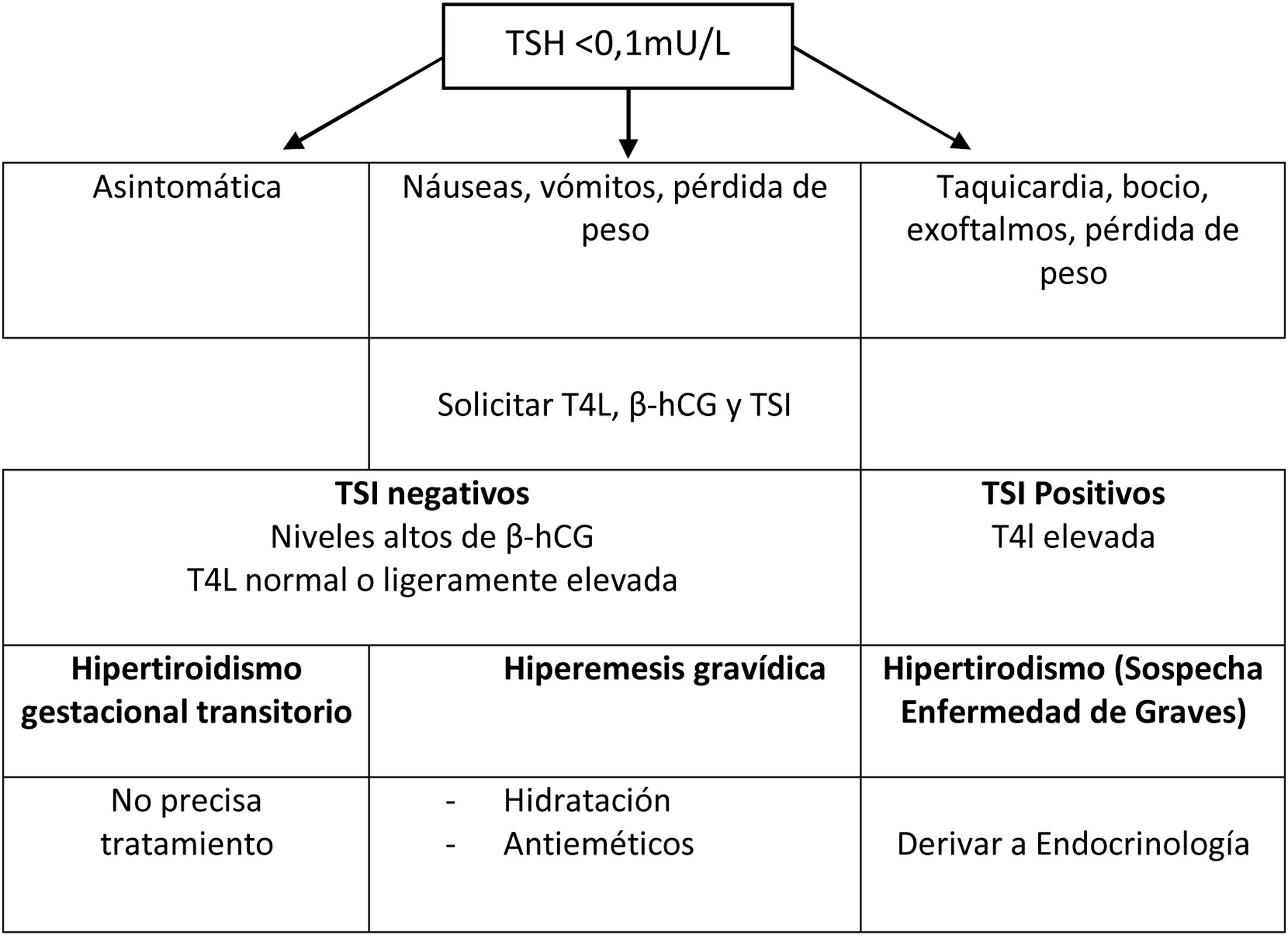
Hipertiroidismo¿Cómo distinguir la hiperemesis gravídica/hipertiroidismo transitorio gestacional de la enfermedad de Graves?Las náuseas y vómitos son muy frecuentes durante el primer trimestre de gestación, pero suelen ser esporádicos, de poca relevancia y solo un porcentaje reducido de mujeres desarrollará una hiperemesis gravídica. Dado que presentan una TSH baja, al estar relacionado su origen con un mayor aumento de la β-hCG, es preciso distinguirlo del hipertiroidismo por enfermedad de Graves (EG). Las características clínicas que ayudan a distinguir ambas entidades están recogidas en la tabla 7.
Diagnóstico diferencial entre hipertiroidismo gestacional y enfermedad de Graves
| Hipertiroidismo gestacional | Enfermedad de Graves |
|---|---|
| TSI negativos | TSI positivos |
| Hiperemesis. Más frecuente en embarazo múltiple | Con frecuencia bocio y puede haber síntomas oculares |
| No síntomas antes del embarazo | Probablemente, ya con síntomas antes del embarazo |
| No historia familiar de enfermedad autoinmune | Historia familiar de enfermedad autoinmune |
| No necesidad de fármacos antitiroideos | Necesidad de tratamiento con antitiroideos |
| Usualmente autolimitados a partir del segundo trimestre | Curso clínico variable, aunque suele mejorar durante el embarazo |
El hipertiroidismo gestacional transitorio es más frecuente en pacientes con títulos altos de β-hCG (embarazo múltiple, técnicas de reproducción asistida, primigestas…) y no se suele acompañar de ninguna sintomatología, no requiriendo tratamiento ni controles adicionales de función tiroidea. La alteración analítica se autolimita cuando descienden los títulos de β-hCG, a partir del segundo trimestre.
En el caso de la hiperemesis gravídica, el tratamiento debe contemplar la hidratación, reposición de electrólitos y uso de fármacos antieméticos. Un esquema del diagnóstico diferencial y manejo clínico de una TSH baja en el primer trimestre está recogido en la figura 1.
¿Cómo se maneja el hipertiroidismo por enfermedad de Graves durante el embarazo?El hipertiroidismo por EG representa una situación de riesgo obstétrico elevado:
- -
Presentan con mayor frecuencia complicaciones tanto maternas (preeclampsia, insuficiencia cardíaca) como fetales (desprendimiento de placenta, hipertiroidismo fetal y neonatal).
- -
El uso de fármacos antitiroideos puede tener efectos teratogénicos.
Los principios generales del tratamiento del hipertiroidismo son8:
- -
Cuando se indique tratamiento antitiroideo deberá utilizarse con la mínima dosis posible de fármaco que permita mantener los niveles de T4L en el límite alto de la normalidad. (Recomendación fuerte, evidencia muy alta)1.
- -
El fármaco de elección en primer trimestre es el propiltiouracilo. Posteriormente, es preferible pasar a metimazol por el riesgo de hepatotoxicidad del propiltiouracilo.
- -
La máxima dosis diaria recomendada de propiltiouracilo es de 200-400mg y de metimazol de 10-20mg.
- -
Los fármacos antitiroideos se han asociado a una larga lista de defectos congénitos. Por ello, debería considerarse retirarlos en mujeres con deseo gestacional o al inicio del embarazo, especialmente si los anticuerpos antirreceptor de TSH (TSI) son bajos o indetectables, y cuando se utilizan dosis bajas.
- -
La función tiroidea debe evaluarse cada 4 semanas, para ajustar el tratamiento. (Recomendación fuerte, evidencia alta.)1
- -
El hipertiroidismo subclínico no precisa tratamiento ya que no se asocia a una mayor morbilidad obstétrica ni fetal.
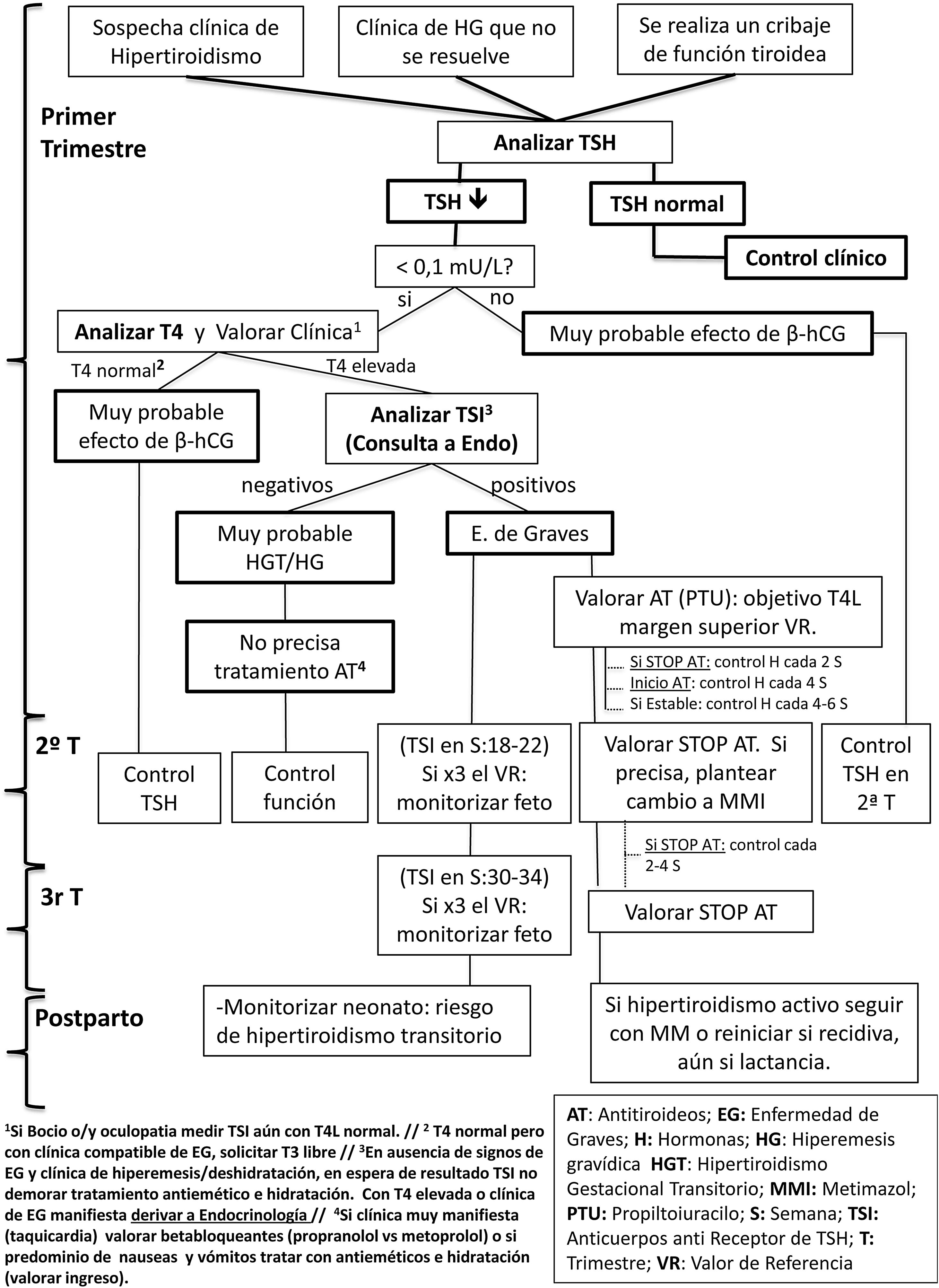
El esquema del diagnóstico y tratamiento del hipertiroidismo por EG están recogidos en la figura 2.
Diagnóstico y manejo del hipertiroidismo durante la gestación (basado en Alexander et al.1.
Tanto los anticuerpos TSI presentes en la circulación materna como los fármacos antitiroideos pueden atravesar la placenta, por lo que el feto puede presentar tanto un hiper como un hipotiroidismo.
Las mujeres a quienes se ha realizado tratamiento definitivo de una EG pueden mantener títulos elevados de TSI circulantes, por lo que existe el riesgo de hipertiroidismo fetal en ausencia de hipertiroidismo en la madre.
Controles de anticuerpos TSI durante el embarazoEl control y seguimiento de los TSI según su concentración y trimestre de gestación se recogen en la tabla 8.
Control de los niveles plasmáticos de TSI durante la gestación
| Trimestre | Niveles de TSI | Acción |
|---|---|---|
| Primero | Están bajos o indetectables | Riesgo de hipertiroidismo fetal muy bajo |
| Si T4L normalizada, valorar reducir o suspender AT. No es preciso realizar más controles de TSI | ||
| Están elevados | Si además T4L elevada, incrementar AT. Realizar nuevo control a la semana 18-22 | |
| Segundo | Se negativizan | Si T4L normalizada, valorar reducir o suspender AT |
| Control mensual de la función tiroidea | ||
| Persisten elevados | Si además T4L elevada, incrementar AT | |
| Realizar nuevo control a la semana 30-34 | ||
| Están elevados x3 el límite superior del valor referencia | Si además T4L elevada incrementar AT | |
| Monitorizar feto a partir de la 20-22 semanas (elevado riesgo de hipertiroidismo fetal) | ||
| Tercero | Están elevados x3 el límite superior del valor referencia: | Monitorización ecográfica del feto (elevado riesgo de hipertiroidismo fetal) |
| Monitorización recién nacido (riesgo muy alto de hipertiroidismo neonatal) |
AT: antitiroideos.
Si en el segundo o tercer trimestres los TSI están elevados 3 veces el valor de referencia, existe un elevado riesgo de hipertiroidismo fetal, siendo preciso realizar una monitorización ecográfica.
Control neonatal del hijo de madre con enfermedad de GravesSiempre que haya una historia de enfermedad tiroidea materna, uso de antitiroideos durante el embarazo o positividad de los TSI, debe comunicarse esta información al neonatólogo o pediatra del recién nacido. (Recomendación fuerte, evidencia moderada)1.
Debe realizarse determinación de TSI en sangre de cordón o lo más precozmente posible tras el parto. En los recién nacidos con TSI positivos en sangre de cordón, se recomienda realizar estudio de función tiroidea en los días 3-5 de vida.
¿Cómo se controla la enfermedad de Graves en el posparto y durante la lactancia?Existe un riesgo de reactivación de la EG en la madre tras el parto, especialmente entre los 4-12 meses posparto. En caso de reactivación, el fármaco de elección es el metimazol.
El paso a la leche de los fármacos antitiroideos es muy bajo y no contraindica la lactancia. No se recomienda el control de función tiroidea en estos lactantes. (Recomendación débil, evidencia moderada)1.
Deseo gestacional e hipertiroidismo, ¿una contraindicación?No es una contraindicación absoluta, pero la dificultad del manejo del hipertiroidismo durante la gestación y el riesgo que supone para el feto y el neonato lo desaconsejan, al menos hasta que la situación de hipertiroidismo esté controlada1. Las actitudes recomendadas ante estas distintas situaciones están recogidas en la tabla 9.
Posibles escenarios en los casos con historia de hipertiroidismo por enfermedad de Graves con deseo gestacional
| En pregestación | Hipertiroidismo controlado | Hipertiroidismo no controlado |
|---|---|---|
| Perfil de paciente | Pacientes en remisión que no precisan tratamiento o que están estables con tratamiento antitiroideo (MMI/PTU) desde hace mínimo de 2 meses | Pacientes que tienen mal control a pesar del tratamiento con antitiroideos o que requieren dosis muy elevadas de fármacos antitiroideos |
| Hallazgo analítico | TSH, T4L y T3L en rangos normales o alterados mínimamente | TSH muy frenada |
| TSI negativos o con títulos bajos | T4L y/o T3L elevadas | |
| TSI a títulos altos | ||
| Actitud a seguir | Confirmar eutiroidismo a los 2 meses | Instaurar método anticonceptivo |
| Ajustar tratamiento: | ||
| Si toma MMI valorar cambio a PTU | ||
| Incremento de dosis hasta lograr eutiroidismo | ||
| Recomendación | Puede planificarse el embarazo | No se recomienda embarazo |
| Valorar retirada de tratamiento con antitiroideos antes del embarazo o substituir MMI por PTU | En caso de precisar dosis muy altas de antitiroideos, valorar tratamiento definitivo (tiroidectomía o ablación con 131 I) | |
| En caso de embarazo | Valorar retirada de tratamiento en primer trimestre. En caso de tratamiento substituir MMI por PTU | Embarazo de alto riesgo |
| Mantener un control estricto ante posible reagudización (solicitar TSH, T4, T3 y TSI en el momento que se confirme el embarazo.) | Cambiar inmediatamente el tratamiento con MMI por PTU | |
| No recomendada la suplementación con yodo | Monitorizar estrechamente al feto por: riesgo de anomalías congénitas asociadas a fármacos antitiroideos y por riesgo de hipo/hipertiroidismo fetal | |
| No recomendada la suplementación con yodo |
MMI: metimazol; PTU: propiltiouracilo.
Se ha considerado que la presencia de autoinmunidad tiroidea es un factor independiente de riesgo de aborto9 existiendo un debate sobre si deben tratarse con LT4 las mujeres gestantes eutiroideas con anti-TPO positivos. En la tabla 5 se resumen las posibles opciones.
Autoinmunidad tiroidea y parto pretérminoLa asociación entre autoinmunidad tiroidea y riesgo de parto pretérmino se ha evidenciado en diferentes metaanálisis. Sin embargo, la guía ATA considera que no hay suficiente evidencia para recomendar tratar con LT4 a gestantes eutiroideas, con anti-TPO positivos, para prevenir el parto pretérmino. (No recomendación, evidencia insuficiente.)1
¿En qué situaciones se recomienda la determinación de Ac anti-TPO?En la gestante, se recomienda la determinación de Ac anti-TPO cuando la TSH sea superior a 2,5mU/L al inicio del embarazo1.
Cada vez está adquiriendo más importancia los Ac antitiroglobulina como causa de infertilidad/subfertilidad10. Por este motivo, se recomienda su determinación en las mujeres que consultan por infertilidad. (Recomendación fuerte, evidencia moderada.)10
¿Cuándo sospechar una tiroiditis posparto y cómo se controla?La tiroiditis posparto (TPP) es la aparición de una enfermedad tiroidea autoimmune en el primer año posparto. Su prevalencia es alrededor del 5%.
Son factores de riesgo para su aparición la presencia de autoinmunidad tiroidea u otras enfermedades autoinmunes, así como antecedentes previos de TPP.
Presentación de la tiroiditis pospartoLa forma clínica de presentación es variable:
- -
Forma clásica: Fase transitoria de hipertiroidismo, seguida de fase transitoria de hipotiroidismo, con retorno al eutiroidismo hacia el final del primer año posparto. Supone alrededor del 20% de las formas de TPP.
- -
Hipertiroidismo aislado: Síntomas de tirotoxicosis, que requieren diagnóstico diferencial con la EG. Supone alrededor del 30% de las TPP.
- -
Hipotiroidismo aislado: Casi la mitad de las TPP se presentan como un hipotiroidismo, que aparece entre los 3-8 meses posparto. En un porcentaje significativo (10-50%) el hipotiroidismo será permanente.
- -
Durante la fase tirotóxica de la TPP, las mujeres sintomáticas pueden ser tratadas con betabloqueantes seguros en la lactancia, como propranolol o metoprolol, a las dosis más bajas que consigan aliviar los síntomas. (Recomendación fuerte, evidencia moderada)1.
- -
Debe considerarse el tratamiento con LT4 en las mujeres sintomáticas en la fase hipotiroidea de la TPP. Si no se inicia tratamiento, deben repetirse los niveles de TSH cada 4-8 semanas hasta que la función tiroidea se normalice. También debe iniciarse tratamiento con LT4 si la mujer busca embarazo o está lactando. (Recomendación débil, evidencia moderada)1.
- -
Si se inicia tratamiento con LT4, debe intentarse su suspensión después de 6-12 meses. Deben evitarse reducciones de dosis si deseo gestacional o embarazo. (Recomendación débil, evidencia baja)1.
Los autores declaran no tener ningún conflicto de intereses.
Los autores desean agradecer a los Dres. Elena Navarro, Juan Carlos Galofré, Mercè Albareda y Piedad Santiago su contribución en la revisión de este manuscrito.
El Documento de Consenso completo está disponible en: https://www.seen.es/ModulGEX/workspace/publico/modulos/web/docs/apartados/3356/100322_120046_3574428481.pdf.