El hidrotórax fetal es una condición rara con una incidencia reportada de uno en cada 10.000-15.000 embarazos, y consiste en una acumulación severa de líquido en el espacio pleural.
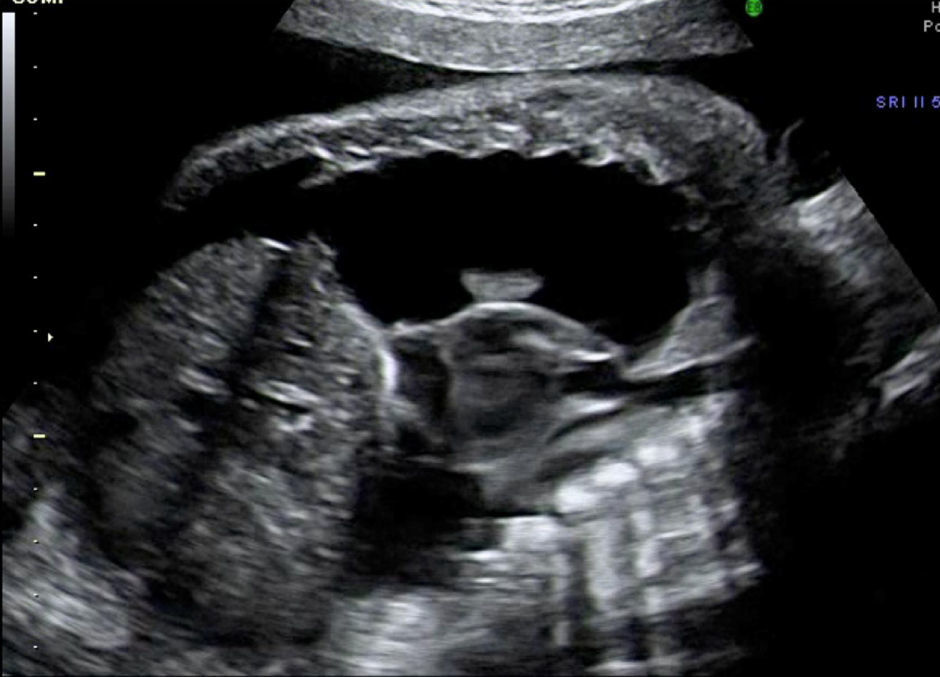
En la ecografía prenatal el derrame pleural se aprecia como un área anecoica uni- o bilateral en el tórax que rodea los pulmones fetales. La evolución varía desde su resolución espontánea hasta su aumento progresivo y el posterior desarrollo de hidrops fetal y polihidramnios con un alto riesgo de parto pretérmino y muerte intrauterina o neonatal debido a que el efecto masa que produce puede causar hipoplasia pulmonar.
El enfoque óptimo del manejo prenatal está todavía en debate ya que el curso natural de la enfermedad puede variar, pero es una condición seria con tasas de morbimortalidad elevadas y la terapia prenatal puede estar indicada en casos seleccionados.
El propósito de este artículo es revisar tanto los aspectos básicos como el estado actual de esta condición, incidiendo principalmente en el diagnóstico, opciones de manejo, alternativas de tratamiento invasivo prenatal, y ofrecer la revisión de nuestra experiencia.
Fetal hydrothorax is a rare condition with a reported incidence of one in 10,000-15,000 pregnancies, and it is a severe accumulation of fluid in the pleural space.
Pleural effusion is seen in prenatal ultrasound as a unilateral or bilateral non-echogenic area in the chest around the fetal lungs. The outcome varies from spontaneous resolution to its gradual increase and the subsequent development of fetal hydrops and polyhydramnios with a high risk of preterm delivery, stillbirth or neonatal death due to pulmonary hypoplasia.
The optimal prenatal management is still unclear, since the natural course of the disease can vary, but it is a serious condition with a high morbidity and mortality and prenatal therapy may be indicated in selected cases.
The purpose of this paper is to review both the basic aspects of the condition and the current status, focusing primarily on the diagnosis, management options, prenatal therapy alternatives, and provide a review of our experience.
La incidencia estimada de hidrotórax fetal es de 1/10.000-15.000 embarazos1. Si es aislado la causa más frecuente es el quilotórax congénito, una anomalía primaria del sistema linfático.
El acúmulo de líquido en el espacio pleural puede conducir a hipoplasia pulmonar (más severa si el cuadro comienza antes de la semana 24 de gestación), compresión cardiaca y obstrucción a nivel del sistema venoso de retorno, que provocará en última instancia hidrops fetal. La compresión mantenida del esófago producirá polihidramnios.
Sin tratamiento, la mortalidad perinatal es del 22-55%2. Las anomalías asociadas y las aneuplodías están presentes en un 25 y 7% respectivamente y empeoran el pronóstico. El hidrotórax fetal primario puede desaparecer, estabilizarse o empeorar.
El hidrotórax secundario normalmente forma parte de un cuadro de hidrops no inmune y el pronóstico dependerá de la causa subyacente.
Fisiopatología, diagnóstico y etiologíaEn condiciones normales, existe fluido en movimiento entre las células mesoteliales de la pleura parietal. Este fluido se comunica con los canales linfáticos y drena en los nódulos linfáticos del mediastino. Si existe una disrupción en el transporte del fluido linfático, este se acumula en el espacio pleural.
El hidrotórax primario, llamado quilotórax en el periodo neonatal, puede ser debido a una malformación congénita en el conducto torácico, o en el sistema linfático pulmonar, como en la linfangiectasia pulmonar primaria3.
La linfangiectasia pulmonar primaria es una rara anomalía caracterizada por la dilatación de los canales linfáticos del tejido broncopulmonar y de la pleura; su etiología es desconocida. Se han descrito casos asociados a herencia autosómica recesiva, mutaciones genéticas y al síndrome linfedema-linfangiectasia-retardo mental (Hennekam)4. La presentación clínica es variable; generalmente se acompaña de hidrops, linfedema y a veces linfangiectasia en otras vísceras. El pronóstico es reservado; la mayoría de los recién nacidos fallecen por dificultad respiratoria severa; su diagnóstico solo puede realizarse postnatalmente. Esta entidad, aunque rara, conviene tenerla en mente en el diagnóstico diferencial del hidrotórax fetal primario.
El hidrotórax fetal secundario puede formar parte de un cuadro de hidrops fetal generalizado. En un 25% de los casos, encontramos anomalías asociadas: malformación adenomatoidea quística, secuestro pulmonar, hernia diafragmática, cardiopatías (estructurales y arritmias), tumores mediastínicos (teratoma tiroideo, bocio congénito). En un 7% de los casos aproximadamente, puede haber cromosomopatías (trisomía 21 y monosomía X principalmente). A veces el hidrotórax fetal se observa en fetos con higroma quístico, infecciones congénitas (adenovirus, parvovirus B19, herpes simple). Finalmente puede formar parte de síndromes genéticos (Noonan, Opitz Frias, hipertelorismo, hipospadias)5 y metabólicos.
Cuando el hidrops fetal está presente, la etiología es muy heterogénea y el diagnóstico prenatal de la causa no siempre será posible.
El diagnóstico ecográfico del hidrotórax se basa en la presencia de líquido en el tórax fetal, uni o bilateral. El primer paso en la evaluación del mismo es determinar si es primario o secundario. El hidrotórax primario es un diagnóstico de exclusión. Dado que son múltiples las posibles causas hay que realizar un protocolo de estudio lo más completo posible valorando la solicitud de las siguientes pruebas:
- –
Cariotipo fetal: mediante amniocentesis, biopsia corial o cordocentesis, dependiendo de la edad gestacional. También puede realizarse en el líquido pleural. En este caso una citología del líquido pleural puede orientarnos en la etiología, pues una proporción mayor del 80% de linfocitos es diagnóstico de quilotórax. La concentración de proteínas y colesterol es menor que en la sangre6.
- –
Serologías maternas para excluir infecciones congénitas: toxoplasmosis, rubéola, citomegalovirus, parvovirus B19, sífilis y herpes.
- –
Grupo sanguíneo materno y test de Coombs indirecto, para descartar hidrops fetal inmune por anemia.
- –
Doppler fetal, especialmente hay que medir la velocidad del pico sistólico de la arteria cerebral media, pues está elevada cuando existe anemia fetal, bien por anticuerpos maternos causantes de isoinmunización eritrocitaria o por infecciones congénitas.
- –
Ecografía fetal detallada para evaluar la magnitud del hidrotórax y descartar enfermedad en el tórax y en el mediastino: malformación adenomatoidea quística, secuestro broncopulmonar y hernia diafragmática.
Una hernia diafragmática derecha puede presentarse como hidrotórax si el saco herniario se llena de fluido y envuelve el pulmón; la etiología del hidrotórax en casos de hernia diafragmática no está clara; algunos estudios señalan que puede ser debida a la congestión de los vasos hepáticos, otros estudios sugieren que hay una relación entre la hernia diafragmática y el quilotórax: el conducto torácico y el diafragma están muy próximos entre sí; un insulto en el periodo embriológico a nivel del diafragma podría alterar el conducto torácico y producir quilotórax7.
- –
Ecocardiografía fetal, para excluir anomalías cardiacas estructurales y arritmias, que se encuentran hasta en el 53% de los casos de hidrops fetal no inmune8. Un estudio reciente describe los resultados obtenidos en la evaluación hemodinámica cardiaca y de la relación área del derrame/área torácica. Señalan que cuanto mayor es esta relación mayor es la presión intratorácica, esto implica mayor compresión cardiaca con disminución en el tamaño de las cavidades del corazón y de la distensibilidad del mismo. También encontraron cambios hemodinámicos con aumento en la velocidad de la arteria pulmonar y disminución en la velocidad de la aorta. Estos parámetros junto con el tamaño del derrame podrían ser útiles para evaluar el pronóstico del hidrotórax fetal aunque se necesitan más estudios al respecto9.
Como hemos indicado anteriormente, la diferenciación entre un hidrotórax primario y uno secundario es difícil. Si el derrame es aislado, es más probable que sea primario, pero puede evolucionar incrementando el volumen y convertirse en bilateral; puede aparecer posteriormente edema subcutáneo, y finalmente ascitis. Algunos fetos se presentarán en la primera valoración ecográfica con un cuadro de hidrops fetal debido a un diagnóstico tardío, pero si el derrame es más significativo en el tórax y el edema predomina en la parte superior del cuerpo, es más probable que el hidrotórax sea primario10.
Cualquiera que sea la etiología, el hidrotórax fetal tiene una evolución variable. Puede desaparecer en aproximadamente un 22% de los casos, incluso cuando son grandes, aunque raramente si hay hidrops11. Más comúnmente el empeoramiento se manifestará con aumento del derrame pleural y extensión del mismo al lado contralateral. Grandes derrames pueden causar compresión esofágica, impidiendo o dificultando la deglución fetal lo que conduce a polihidramnios. El aumento de la presión intratorácica puede comprimir la vena cava superior y disminuir el retorno venoso y la compresión cardiaca puede producir fallo cardiaco e hidrops9. Los factores que más empeoran el pronóstico son la presencia de hidrops y el parto pretérmino.
Manejo y opciones de terapia fetalDesde hace tiempo, la rareza del hidrotórax fetal y la variabilidad en el curso clínico implican que no exista un enfoque claro respecto a la utilidad de la terapia fetal. El objetivo del tratamiento prenatal es disminuir la hipoplasia pulmonar producida por la compresión mantenida en el tórax, y el parto pretérmino asociado al hidramnios. Las opciones son: manejo conservador, toracocentesis, shunt toracoamniótico y pleurodesis.
Manejo conservadorCuando el hidrotórax es leve, sin hidrops ni polihidramnios, el manejo conservador es adecuado porque puede haber regresión espontánea. El pronóstico fetal es bueno, con tasas de supervivencia del 73 al 100%2,11, mientras que la supervivencia media general del hidrotórax fetal es del 46 al 59% (fetos con y sin hidrops)5,12.
ToracocentesisEste procedimiento fue propuesto por primera vez como tratamiento del hidrotórax fetal primario por Peters et al.13 en 1982. La técnica consiste en la introducción guiada por ecografía de una aguja de 20 G para aspirar el líquido pleural. El drenaje pleural, además de descomprimir el tórax y permitir el desarrollo pulmonar, puede ayudar a diagnosticar anomalías cardiacas e intratorácicas «ocultas» por el derrame.
El análisis citológico y bioquímico del líquido pleural es útil para el diagnóstico del hidrotórax primario. La no reexpansión de los pulmones tras la toracocentesis y la no regresión del hidrops cuando está presente ayudan a distinguir el hidrops secundario al hidrotórax, del hidrops asociado a otras causas. Sin embargo, en la mayoría de los casos, el líquido pleural se reacumula en 24-48 h, necesitando la repetición del procedimiento.
En hidrotórax diagnosticados en gestaciones a término, la toracocentesis antes del parto facilita la reanimación neonatal.
Desde 1982 se han publicado varias series mostrando los resultados de supervivencia neonatal en casos tratados mediante toracocentesis.
Aubard et al. revisaron 29 casos (de 21 artículos publicados) de toracocentesis realizadas entre las semana 17 y 37 de gestación; la supervivencia fue del 10% en fetos con hidrops y del 60% en fetos sin hidrops11. Rustico et al., en su revisión de la literatura, reportan una supervivencia del 50% en fetos con hidrops (11/22 casos) y del 77% en fetos sin hidrops (10/13 casos) con una supervivencia global del 60% (21/35 casos) para la toracocentesis5. Una de las revisiones más completas es la publicada por Deurloo et al. en 200714, que presenta una recopilación de 44 artículos seleccionados de series observacionales y casos clínicos desde 1982 a 2006; en total se presentan resultados de 172 fetos con hidrops tratados prenatalmente con diferentes técnicas, reportando una supervivencia del 54% para la toracocentesis simple (7/13 casos) y del 67% para la toracocentesis múltiple (12/18 casos).
El riesgo de rotura prematura de membranas en la toracocentesis es similar al de la amniocentesis: 1-1,6%.
Shunt pleuroamnióticoDebido a la rápida reacumulación de líquido pleural después de la toracocentesis, se ha propuesto un sistema que permita el drenaje continuo del derrame pleural. Esta técnica fue descrita por primera vez en 1986 por Seeds y Bowes15, aunque estos shunts fueron originariamente ideados para el drenaje de la vejiga fetal. El shunt más utilizado es el catéter de silicona doble pigtail de Rocket (Rocket of London Ltd. Watford, U.K.), con orificios laterales y en los extremos del mismo.
La inserción se realiza mediante control ecográfico, se introduce transabdominalmente a la cavidad amniótica un trocar de 9Fr (3mm) con la cánula. Idealmente el trocar es insertado perpendicularmente a la pared torácica fetal hasta llegar al derrame pleural, (visualizando el corte cardiaco de las 4 cámaras), lo más cerca posible de la línea media axilar a nivel de la base de la escápula. Es importante que la punta del trocar avance correctamente en el derrame. Se retira el trocar y se inserta el catéter acoplándolo a la cánula; con la ayuda de una barra empujamos el catéter hasta que la mitad del mismo y el bucle distal queden en el tórax fetal. La cánula es retirada suavemente del tórax fetal y con una barra más larga que la primera, se deposita el resto del catéter con el bucle proximal en la cavidad amniótica. Siempre debe evitarse atravesar la placenta. Una vez terminado el procedimiento, el catéter crea una comunicación permanente entre el espacio pleural y la cavidad amniótica. Cuando el hidrotórax es bilateral, podemos rotar el feto con el extremo romo de la cánula para permitir la colocación de un segundo shunt en el espacio pleural contralateral10.
Las complicaciones del shunt incluyen: migración del catéter al espacio pleural, a la cavidad amniótica y a la cavidad peritoneal materna10,16. A veces puede obstruirse. Aproximadamente en un 10-20% de los casos hay que repetir el procedimiento. También se ha descrito la reversión del shunt, entrando líquido amniótico al tórax fetal. La inserción del shunt se asocia a rotura prematura de membranas en un 17% de los casos10, corioamnionitis y parto pretérmino. Se recomienda administrar profilaxis antibiótica e indometacina y/o nifedipina oral.
Tras el nacimiento se aconseja pinzar inmediatamente el catéter para evitar la formación de un neumotórax.
Los resultados en cuanto a supervivencia neonatal en fetos tratados con shunt toraco-amniótico, reportados en la literatura, son de aproximadamente el 50% en fetos hidrópicos, y el 70-100% en fetos sin hidrops. Rustico et al., en su revisión de la literatura, reportan una supervivencia del 62% en fetos con hidrops (77/125 casos) y del 82% en fetos sin hidrops (27/33 casos) con una supervivencia global del 66% (104/158 casos) para el shunt pleuroamniótico5 y Deurloo et al.14 en su recopilación de 44 artículos en la que presentan resultados de 172 fetos con hidrops tratados prenatalmente con las diferentes técnicas, reportan una supervivencia del 61% para el shunt pleuroamniótico (61/100 casos) y del 67% para la realización de una toracocentesis simple previa a la colocación de shunt pleuroamniótico (24/36 casos).
En la tabla 1 se muestran los hallazgos ecográficos, y el resultado de las series recientes publicadas en la literatura con más de 15 casos de hidrotórax tratados prenatalmente mediante inserción de shunt pleuroamniótico.
Hallazgos ecográficos, y resultado de las series publicadas en la literatura con más de 15 casos de hidrotórax tratados prenatalmente mediante inserción de shunt pleuroamniótico
| Referencia | Número de casos (%) | EG shunt | EG parto | Sobrevida perinatal n (%) | ||
| Hidrops | No Hidrops | Hidrops | No hidrops | |||
| Nicolaides y Azar12 | 28 | 18 | NA | NA | 50% | 100% |
| Pettersen y Nicolaides17 | 41 (59) | 28 (41) | 29 (20-33) | 36 (23-41) | 19 (46) | 28 (100) |
| Mussat et al.18 | 20 | – | 31 (27-35) | 34 (29-40) | 13 (65) | – |
| Picone et al.16 | 54 | – | 30,5 (19-36) | 34 (22-40) | 28 (51,4) | – |
| Smith et al.19 | 12 (70) | 5 (30) | 24 (20-36) | 32 (22-40) | 7 (58) | 3 (60) |
| Rustico et al.5 | 43 (81,1) | 10 (18,9) | NA | NA | 25 (58,1) | 9 (90) |
| Yinon et al.20 | 59 (67) | 29 (33) | 28 (18-37) | 34 (19-42) | 31 (52,5) | 21 (72,4) |
EG: edad gestacional; NA: no aclarado en el texto.
Una forma alternativa de tratamiento prenatal del hidrotórax fetal es la inyección intrapleural de OK-432, una sustancia liofilizada derivada del Streptococus piogenes del grupo A, de origen humano, que ha sido usada como agente esclerosante para el tratamiento del linfangioma en pacientes adultos y pediátricos. El mecanismo de acción es promover la producción de adherencias esclerosantes entre la pleura parietal y visceral mediante una reacción inflamatoria mediada por células, principalmente linfocitos T21.
El primer trabajo publicado con esta terapia fue por Okawa et al.22 en 2001, en un caso de hidrotótax aislado severo en la semana 25 de gestación. Tras realizar 2 toracocentesis previas, el líquido pleural volvió a acumularse, por lo que decidieron inyectar en la semana 31 de embarazo 0,01 mg de OK-432 intrapleural con una aguja de 20 G, drenando previamente el líquido pleural. En el seguimiento observaron que el líquido pleural no volvió a acumularse. La gestación llegó a término y el recién nacido no requirió soporte respiratorio.
Desde 2001 se han publicado varios casos clínicos de fetos con hidrotórax tratados con pleurodesis23–26. Leung VK et al.27 publicaron un caso y presentan una revisión de la literatura con un total de 16 fetos tratados con pleurodesis como primera o segunda línea de tratamiento (después de toracocentesis). El procedimiento tuvo éxito en 13 casos. Concluyeron que es una técnica más fácil de realizar y con menor morbilidad que el shunt pleuroamniótico, que la localización placentaria no es un obstáculo y que los resultados son buenos en cuanto a la supervivencia neonatal (que fue del 81%, 13/16 casos, un niño afecto por síndrome de Down murió al año de vida). No hubo evidencia de teratogenicidad fetal. La dosis no está estandarizada, en general administran de 0,1 a 1 mg.
Chen et al. en el 2007 reportan los resultados de 17 fetos con hidrotórax (no incluidos en la revisión de Leung VK del 2012), 15 de los cuales eran bilaterales (5 de estos presentaban hidrops fetal) y 2 unilaterales, con una edad gestacional media de 23 semanas (17-29), manejados con: modificación de la dieta materna (5 casos), modificación de la dieta más pleurodesis con OK-432 (9 casos) y modificación de la dieta más pleurodesis con colocación de shunt pleuroamniótico en casos en los que el hidrotórax no se resolvió (3 casos), a todos se les realizó toracocentesis para estudio del líquido pleural. Siete de los 12 fetos (58%) tratados invasivamente sobrevivieron, todos los fetos con hidrops presentaron muerte intrauterina28.
Yang et al.29 reportaron también en el año 2012 una serie propia de 45 casos de fetos con hidrotórax bilateral (con y sin hidrops) manejados con inyección intrapleural de 0,1 mg de OK-432 en 10ml de suero salino, entre 16-29 semanas de gestación, posteriormente se realizó colocación de shunt pleuroamniótico en 6 casos con hidrops como procedimiento de rescate por no mejoría con pleurodesis, pero ninguno sobrevivió.
La sobrevida fue del 66,7% en fetos sin hidrops (12/18) y del 14,8% en fetos con hidrops (4/27).
En el 30% de los fetos hidrópicos que no respondieron a la terapia encontraron mutaciones en genes relacionados con linfedema. Los autores concluyeron que el tratamiento con OK-432 aparentemente no es eficaz en fetos con hidrops y que es menos efectivo que el shunt toracoamniótico.
Finalmente, Parra et al. en el 200330 publican 2 casos de hidrotórax fetal tratados con inyección intrapleural de sangre materna, después de toracocentesis. El mecanismo de acción para la pleurodesis parece ser la adhesión de fibrina liberada por las células sanguíneas a la pleura. No definen la dosis ideal de sangre; ellos administraron 7 y 9ml. Los 2 casos tuvieron buena evolución.
La completa aspiración del líquido pleural previa a la inyección de la sustancia esclerosante y la demostración de la adhesión pleural mediante ecografía son 2 requisitos para considerar que la técnica se realizó de forma exitosa.
Nuestra experienciaEn los últimos 4 años desde enero 2008 hasta abril del 2012, hemos atendido 9 casos de hidrotórax primario. Siete fetos tenían hidrops asociado en el momento del diagnóstico. En 2 casos el hidrotórax fue aislado y se manejaron con una única toracocentesis, uno de los casos se diagnosticó en la semana 37, con derrame pleural bilateral y polihidramnios y realizamos una toracocentesis extrayendo 40cc de líquido claro antes de la inducción del parto. El recién nacido pesó 3.600g, y no precisó toracocentesis postnatal. Se confirmó el diagnóstico de quilotórax primario. La evolución fue favorable; se instauró alimentación parenteral y enteral con ácidos grasos de cadena media. En el segundo caso se realizó toracocentesis en la semana 30, en la siguiente revisión el hidrotórax se había resuelto y no requirió otro tipo de tratamiento; su evolución fue favorable, con parto de un recién nacido sano a término.
En el resto de los casos se colocó un shunt pleuroamniótico, previa información y consentimiento informado de los padres. En 3 casos persistieron el hidrotórax y el hidrops tras la colocación correcta del drenaje, produciéndose en 2 casos la muerte fetal anteparto y en el tercero el recién nacido falleció pocos minutos después del nacimiento por hipoplasia pulmonar. El resto de los casos mejoraron con la inserción del shunt pleuroamniótico y tuvieron una evolución postnatal favorable.
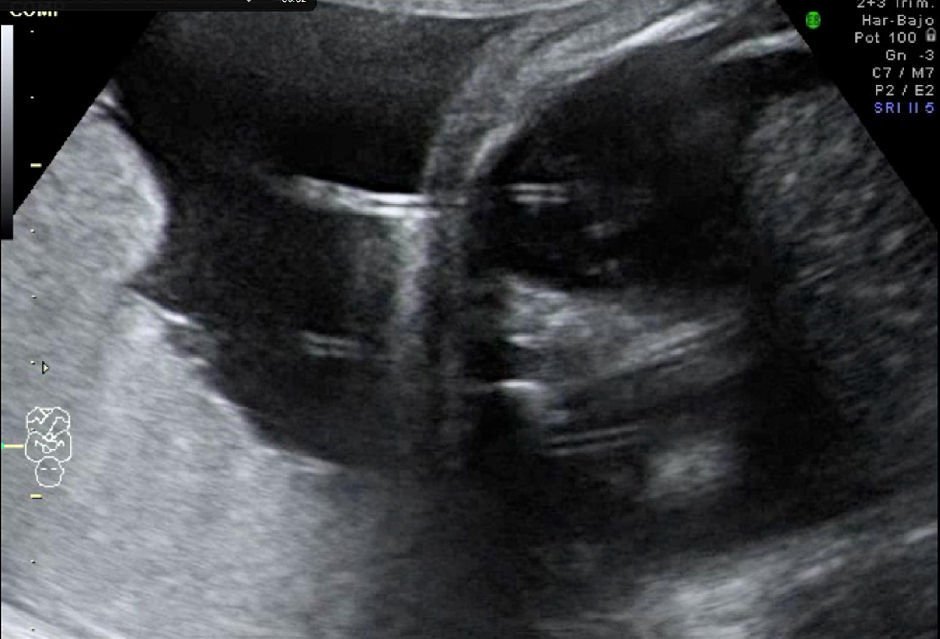
En la tabla 2 desglosamos los datos clínicos, el manejo realizado en cada caso y el resultado del embarazo. La supervivencia global de los fetos con hidrotórax de causa desconocida en nuestra serie fue del 66%. Las figuras 1 y 2 demuestran la imagen ecográfica del hidrotórax bilateral en uno de los casos y la imagen ecográfica tras la colocación del shunt pleuroamniótico bilateral.
Descripción de los datos ecográficos, manejo y resultado de los casos con hidrotórax fetal evaluados en nuestra área de referencia
| Caso 1 | Caso 2 | Caso 3 | Caso 4 | Caso 5 | Caso 6 | Caso 7 | Caso 8 | Caso 9 | |
| EG al diagnóstico (semanas) | 32,4 | 19,4 | 19,6 | 27,6 | 32,6 | 30,5 | 37,0 | 16,4 | 28,3 |
| Cariotipo | 46XY | 46XX | 46XX | 46XY | 46XY | 46XY | 46XX | 46XX | 46X* |
| EG al tratamiento (semanas) | 32,4 | 22,2 | 23,5 | 27,6 | 32,6 | 30,5 | 37,0 | 17,4 | 28,4 |
| Hallazgos ecográficos | HTX-B hidrops | HTX-I hidrops | HTX-B hidrops PH | HTX-I Hidrops PH | HTX-B hidrops PH | HTX-D | HTX-B | HTX-B hidrops | HTX-D hidrops |
| Tratamiento | ST-B | TRC ST-I | ST-B | ST-I | ST-B | TRC | TRC | ST-B | ST-I |
| Resolución | Sí | Sí | No | No | Sí | Sí | Sí | No | Sí |
| Intervalo tratamiento - parto (días) | 23 | 108 | 49 | 1 | 42 | 51 | 1 | 66 | 38 |
| EG al parto (semanas) | 35,6 | 37,5 | 30,5 | 27,7 | 38,6 | 38 | 37,1 | 27,0 | 34,0 |
| Resultado | Vive sano | Vive v | MIU | MIU | Vive sano | Vive sano | Vive sano | Muerte neonatal | Vive sano |
EG: edad gestacional; HTX-B: hidrotórax bilateral; HTX-D: hidrotórax derecho; HTX-I: hidrotórax izquierdo; MIU: muerte intrauterina; MNN: muerte neonatal; PH: polihidramnios; ST-B: shunt pleuroamniótico bilateral; ST-D: shunt pleuroamniótico derecho; ST-I: shunt pleuroamniótico izquierdo; TRC: toracocentesis.
El hidrotórax fetal es una enfermedad poco frecuente y grave. La supervivencia va a depender de la severidad del derrame pleural, de la presencia de hidrops asociado, de la edad gestacional en que debute y de la prematuridad asociada causada principalmente por el polihidramnios. Cuando el diagnóstico se realiza antes de la semana 24, el riesgo de hipoplasia pulmonar es muy elevado.
La causa más frecuente de hidrotórax primario es el quilotórax, y es también el que tiene mejor pronóstico. El hidrotórax secundario asociado a hidrops presenta una evolución más incierta por las anomalías subyacentes que puede haber. Es difícil diferenciar prenatalmente entre ambos tipos. A veces el diagnóstico solo podrá completarse en el periodo neonatal y es importante informar a los padres de ello.
En cuanto al tratamiento prenatal, la opción estándar actualmente es el shunt de derivación pleuroamniótico en fetos con hidrotórax severo con y sin hidrops que debutan en el segundo trimestre, con una supervivencia del 33-66% en fetos con hidrops y del 70-100% en fetos sin hidrops.
En casos de hidrotórax leve-moderado sin hidrops es preferible el manejo expectante con control ecográfico semanal o quincenal, ya que pueden desaparecer intraútero o permanecer estables, evitando realizar una técnica invasiva no exenta de riesgos.
Si el diagnóstico se realiza en el tercer trimestre, puede considerarse la realización de una o más toracocentesis. Incluso si debuta a partir de la semana 36, la toracocentesis facilita la reanimación neonatal.
La pleurodesis es una técnica alternativa de tratamiento. Las series publicadas muestran tasas de supervivencia del 0-14,8% en fetos con hidrops y del 66-100% en fetos sin hidrops, pero no hay estudios suficientes para validar su uso. Tiene la ventaja de requerir un instrumento más fino que el shunt (una aguja de 20 G), lo que disminuye la morbilidad.
La valoración del hidrotórax fetal debe realizarse por un equipo multidisciplinar para optimizar los resultados. Tras el nacimiento, hay que prestar soporte respiratorio, y si se trata de un quilotórax, alimentación parenteral o enteral con ácidos grasos de cadena media.
Son necesarios estudios que muestren los resultados a largo plazo en cuanto a la morbilidad en fetos tratados y no tratados.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.