Las fosfodiesterasas de nucleótidos cíclicos (PDEs) de la subfamilia 4 (PDE4) son responsables de la hidrólisis y compartimentalización subcelular del adenosín monofosfato cíclico (AMPc), segundo mensajero que modula la funcionalidad vascular. Habíamos demostrado que la isoforma B de la PDE4 (PDE4B) se induce en el aneurisma de aorta abdominal (AAA) y que la inhibición de la actividad PDE4 mediante rolipram limita la formación de aneurismas experimentales. En este estudio hemos profundizado en los mecanismos que subyacen al efecto beneficioso del rolipram sobre el AAA.
MétodosSe ha utilizado el modelo de inducción de AAA por infusión de angiotensina II (Ang II) en ratones con apolipoproteína E ApoE-/−. La formación de aneurismas se ha evaluado mediante ultrasonografía. La expresión de enzimas implicados en el control de la homeostasis rédox se ha analizado por reacción en cadena de la polimerasa con transcriptasa reversa (RT-PCR) en tiempo real y la activación de vías de señalización mediante Western blot.
ResultadosSe ha confirmado la inducción de la PDE4B en el AAA humano en otra cohorte de pacientes. En ratones ApoE-/- infundidos con Ang II el rolipram incrementó el porcentaje de animales libres de aneurisma sin afectar al de rotura aórtica. Análisis cuantitativos determinaron que este fármaco atenuó significativamente la deposición de colágeno en la aorta. Además, el rolipram redujo el incremento en la expresión de Nox2 en respuesta a la Ang II, promovió una mayor inducción del nivel de ARNm de Sod1 y normalizó la expresión de Sod3. Asimismo, la inhibición de PDE4 disminuyó la activación de la Extracellular Signal-Regulated Kinase 1/2 (ERK1/2) y de la vía canónica de Wnt, mientras la actividad de la proteína cinasa B (AKT) no se vio alterada.
ConclusionesLa inhibición de la actividad PDE4 modula la expresión de enzimas implicados en la homeostasis rédox y afecta a vías de señalización celular implicadas en el desarrollo de la patología aneurismática.
Cyclic nucleotide phosphodiesterases (PDEs) of the PDE4 subfamily are responsible for the hydrolysis and subcellular compartmentalization of cAMP, a second messenger that modulates vascular functionality. We had shown that PDE4B is induced in abdominal aortic aneurysms (AAA) and that PDE4 inhibition by rolipram limits experimental aneurysms. In this study we have delved into the mechanisms underlying the beneficial effect of rolipram on AAA.
MethodsAAA were induced in ApoE-/− mice by angiotensin II (Ang II) infusion. Aneurysm formation was evaluated by ultrasonography. The expression of enzymes involved in rédox homeostasis was analyzed by real-time RT-PCR and the activation of signaling pathways by Western blot.
ResultsInduction of PDE4B in human AAA has been confirmed in a second cohort of patients. In Ang II-infused ApoE-/− mice, rolipram increased the percentage of animals free of aneurysms without affecting the percentage of aortic ruptures. Quantitative analyses determined that this drug significantly attenuated aortic collagen deposition. Additionally, rolipram reduced the increased Nox2 expression triggered by Ang II, exacerbated Sod1 induction, and normalized Sod3 expression. Likewise, PDE4 inhibition decreased the activation of both ERK1/2 and the canonical Wnt pathway, while AKT activity was not altered.
ConclusionsThe inhibition of PDE4 activity modulates the expression of enzymes involved in rédox homeostasis and affects cell signaling pathways involved in the development of AAA.
Las fosfodiesterasas de nucleótidos cíclicos (PDEs) constituyen una gran superfamilia de enzimas altamente conservadas que regulan los niveles celulares de adenosín monofosfato cíclico (AMPc) y guanosín monofosfato cíclico (GMPc), segundos mensajeros que juegan un papel fundamental en la señalización intracelular1–3. Estas enzimas son fosfohidrolasas que selectivamente catalizan la hidrólisis e inactivación del AMPc y el GMPc, por lo que regulan la magnitud y duración de su señalización, así como múltiples procesos fisiológicos y metabólicos, desde la inflamación, la señalización dependiente de canales iónicos, la diferenciación y apoptosis celular, la contracción muscular, la lipogénesis, la síntesis de glucógeno y la gluconeogénesis4. La alteración en la actividad o expresión de estas enzimas se ha vinculado con diversas patologías entre ellas enfermedades cardiovasculares.
Existen 11 familias de PDEs (PDE1 a PDE11) que muestran diferente selectividad hacia sus sustratos5,6. De entre ellas, los miembros de la subfamilia PDE4, constituyen la mayor parte de las PDEs selectivas para AMPc en diferentes órganos y tipos celulares y se caracterizan por ser enzimas sensibles a la inhibición por rolipram7–10. Esta subfamilia está constituida por cuatro miembros (PDE4A-D) con múltiples variantes que se expresan en un gran número de tejidos y se han implicado en numerosos procesos fisiopatológicos. A través del control de la tasa de degradación del AMPc estas enzimas son clave en la regulación de la función vascular modulando la permeabilidad endotelial, la angiogénesis, la activación del monocito/macrófago y la regulación de la proliferación, migración, diferenciación y contracción de las células de músculo liso vascular (CMLV)7,8.
El aneurisma de aorta abdominal (AAA) es una enfermedad degenerativa crónica que consiste en la dilatación focal de la aorta derivada del debilitamiento de la pared vascular11,12. Se trata de una alteración vascular con frecuencia asintomática pero cuya ruptura desemboca en graves hemorragias internas que se asocian a una elevada morbimortalidad. El manejo clínico de los pacientes con AAA se limita a la intervención quirúrgica de los aneurismas de alto riesgo, cirugía no exenta de complicaciones que conlleva un elevado coste sanitario13. Sin embargo, no se dispone de estrategias farmacológicas que limiten la progresión y reduzcan el riesgo de ruptura del aneurisma14, por lo que es fundamental profundizar en la fisiopatología de estas enfermedades para identificar nuevas dianas terapéuticas que mejoren el tratamiento de estos pacientes14,15.
Nuestros estudios previos en muestras de aorta aneurismática tanto humanas como de modelos experimentales ponen de manifiesto el incremento en la expresión vascular de PDE4B y cómo la inhibición de la actividad PDE4 mediante rolipram atenúa el desarrollo del AAA en un modelo preclínico16. En el presente trabajo ratificamos la inducción de PDE4B en el aneurisma humano en una segunda cohorte de pacientes y profundizamos en los mecanismos implicados en el efecto beneficioso del rolipram sobre el AAA en un modelo experimental, demostrando cómo este fármaco modula la expresión de enzimas implicados en la homeostasis rédox y afecta a vías de señalización celular.
Material y métodosEstudios en muestras humanasLas muestras humanas correspondientes a lesiones aneurismáticas se obtuvieron a partir de pacientes sometidos a reparación quirúrgica de AAA por cirugía abierta en el Hospital de la Santa Creu i Sant Pau (HSCSP), Barcelona; n=27). Asimismo, en el estudio se incluyeron muestras de aorta abdominal sana procedentes de donantes multiorgánicos que no mostraron signos de patología aneurismática o aterosclerótica, tal y como se describió previamente (n=15)16–18. Los pacientes con AAA eran hombres, 85,1% de ellos fumadores17. El uso de estas muestras fue aprobado por el Comité Ético del HSCSP (12/031/1316) y se realizó siguiendo las directrices marcadas por la Declaración de Helsinki. Se obtuvo un consentimiento informado por escrito de los pacientes e individuos control o de sus representantes legales. Las muestras de aorta se almacenaron rápidamente a -80°C para la extracción del ácido ribonucleico (RNA) o se procesaron adecuadamente para los análisis inmunohistoquímicos.
Modelo animalLos estudios se realizaron en ratones deficientes en apolipoproteína E (ApoE-/-; B6.129P2-Apoetm1Unc/J) que se mantuvieron en un ambiente libre de patógenos bajo condiciones estándar de iluminación (ciclos de 12horas de luz/oscuridad) y temperatura (21±1°C) en la unidad de experimentación animal del Institut de Recerca del Hospital de la Santa Creu i Sant Pau (IRHSCSP), Barcelona, España, con acceso ad libitum a bebida y alimento durante todo el procedimiento. El estudio se realizó en machos debido al dimorfismo sexual que caracteriza esta enfermedad con una mayor prevalencia en machos tanto en humanos como en modelos animales. El AAA se indujo mediante la infusión de angiotensina II (Ang II); 1000 ng/kg/min) con minibombas osmóticas (modelo 1004, Alzet; Durect Corporation) implantadas subcutáneamente16,17,19. Los animales se aleatorizaron en tres grupos: ratones que se infundieron con suero salino, animales infundidos con Ang II y ratones infundidos con Ang II tratados con rolipram diariamente (3mg/kg; i.p.; SelleckChem) desde el día anterior a la implantación de las minibombas. Como vehículo se utilizó solución salina+1% dimetilsulfóxido (DMSO) y tanto los animales control como el grupo de ratones infundido con Ang II recibió un volumen equivalente del vehículo. Al cabo de cuatro semanas, los animales fueron anestesiados con ketamina (150mg/kg) y medetomidina (1mg/kg), se sacrificaron por toracotomía y las aortas se extrajeron y procesaron adecuadamente en función de los estudios posteriores.
La investigación fue realizada conforme a la normativa de Política Española de Protección de Animales RD53/2013, que cumple con la normativa Animal Research: Reporting of in Vivo Experiments (ARRIVE) y la Directiva de la Unión Europea 2010/63/UE relativa a la protección de animales de experimentación. Todos los procedimientos fueron aprobados por el Comité Ético del IRHSCSP y el Departament d’Acció Climàtica, Alimentació i Agenda Rural de la Generalitat de Catalunya (proyecto 11483).
Medida del diámetro aórticoEl diámetro de la aorta abdominal se determinó mediante ultrasonografía el día anterior a la implantación de las minibombas y semanalmente tras la infusión de Ang II. Para ello los animales se anestesiaron con isofluorano al 2% y se colocaron sobre una plataforma calefactada en posición de decúbito supino. A continuación se afeitó el precordio y se realizó una ecografía abdominal mediante el equipo de ultrasonidos Vevo 2100 con un transductor de 30MHz para registrar la aorta abdominal, tal y como se describió anteriormente16,17,19,20. Se consideró aneurisma diámetros superiores a 1,5mm. Se estableció el porcentaje de animales libres de aneurisma a lo largo del procedimiento y el porcentaje libre de rotura aórtica.
Análisis de expresión por PCR a tiempo realEl ARN total se aisló mediante el reactivo TriPure Isolation Reagent (Roche Diagnostics) y se realizó una transcripción reversa utilizando el High Capacity cDNA Reverse Transcription kit (Applied Biosystems) y hexámeros aleatorios. El nivel de ARNm se cuantificó mediante el equipo ABI PRISM 7900HT sequence detection system y oligonucleótidos y sondas específicos proporcionados por Integrated DNA Technologies o el sistema TaqMan™ gene expression assays-on-demand (Applied Biosystems) para la detección de los niveles de ARNm en muestras humanas de PDE4B (Hs00277080_m1) y PDE4D (Hs01579625_m1). En muestras de ratón se analizó la expresión de la nicotinamida adenina dinucleótido fosfato (NADPH) oxidasa 1 (Nox1; Mm00549170_m1), la Nox2 (Mm01287743_m1), la Nox4 (Mm00479246_m1) y las superóxido dismutasas Sod1; Mm.PT.58.12368303), Sod2 (Mm.PT.58.14276358) y Sod3 (Mm.PT.58.12048855). La β-actina humana ACTB (ß-actin; HS99999903_m1) y la TATA-binding protein (Tbp; Mm00446973_m1) se utilizaron como genes de normalización en muestras humanas y murinas, respectivamente. Las amplificaciones se realizaron por duplicado y el nivel relativo de ARNm se determinó usando el método de 2-ΔΔCT.
Western blotLos lisados proteicos se sometieron a electroforesis en geles de poliacrilamida (SDS-PAGE) en condiciones desnaturalizantes y se transfirieron a membranas de difluoruro de polivinilideno (IPVH00010; Immobilon, Merck-Millipore). Estas membranas se bloquearon en una solución que contenía 5% de leche desnatada en tampón Tris-HCl con 0,05% Tween 20 (TBST) a temperatura ambiente durante una hora. A continuación, las membranas se incubaron toda la noche a 4°C y con agitación con anticuerpos contra la β-catenina activa (#88145; Cell Signaling), la Extracellular Signal-Regulated Kinase 1/2 (ERK1/2) total (#9102; Cell Signaling) y fosforilada (#9106; Cell Signaling) y la forma fosforilada en la Ser473 de la proteína cinasa B o AKT (#9271; Cell Signaling). Tras realizar varios lavados con TBST, las membranas se incubaron con un anticuerpo secundario conjugado con peroxidasa de rábano (Dako Products, Agilent) y posteriormente los anticuerpos unidos se detectaron gracias a la adición del reactivo Luminata™ Western horseradish peroxidase (HRP) Substrate (Immobilon, Merck-Millipore). La señal quimioluminiscente se detectó mediante películas autorradiográficas (CURIX RP2 plus, Agfa). El tamaño de las proteínas detectadas se estimó usando un marcador de peso molecular (Hyperpage Prestained Protein Marker; Bioline) y los niveles de gliceraldehído-3-fosfato deshidrogenasa (GAPDH); MAB374 permitieron verificar la homogeneidad de carga en cada carril. Las películas se escaneraron en el densitómetro GS-800 (BIO-RAD) y la cuantificación relativa de las bandas mediante el programa Quantity One (BIO-RAD).
InmunohistoquímicaLas muestras humanas y murinas se fijaron en paraformaldehído al 4% durante 24horas y se embebieron en parafina. Se prepararon secciones (5μm) con el micrótomo Jung RM2055 (Leica Microsistemas S.L.U). Las muestras se desparafinaron y rehidrataron en un gradiente de soluciones de etanol. Tras el desenmascaramiento de antígeno en tampón citrato (10mM pH 2,5), la actividad peroxidasa endógena se bloqueó con una solución de peróxido de hidrógeno al 3% en metanol. A continuación, las muestras se incubaron con 10% de suero, se bloqueó la avidina/biotina endógena (Vector Laboratories) y se incubaron toda la noche a 4°C con un anticuerpo específico para la PDE4B (NBP2-01171, Novus Biologicals). Se realizaron tinciones convencionales por hematoxilina-eosina y Tricrómico de Mason.
Análisis estadísticosLos resultados se muestran como media±error estándar de la media (SEM). Las diferencias significativas (para p<0,05) se establecieron mediante ANOVA de una vía (análisis post hoc de Sidak). Cuando la distribución de los datos no siguió el test de normalidad de Agostino-Pearson se utilizó la prueba de U de Mann-Whitney o el test de Kruskal-Wallis. Se utilizó el test de Mantel-Cox para el análisis de la ocurrencia de un evento (porcentaje libre de aneurisma y libre de rotura) entre dos poblaciones. Los datos se analizaron con el programa GraphPad Prism version 6.01 (GraphPad by Dotmatics).
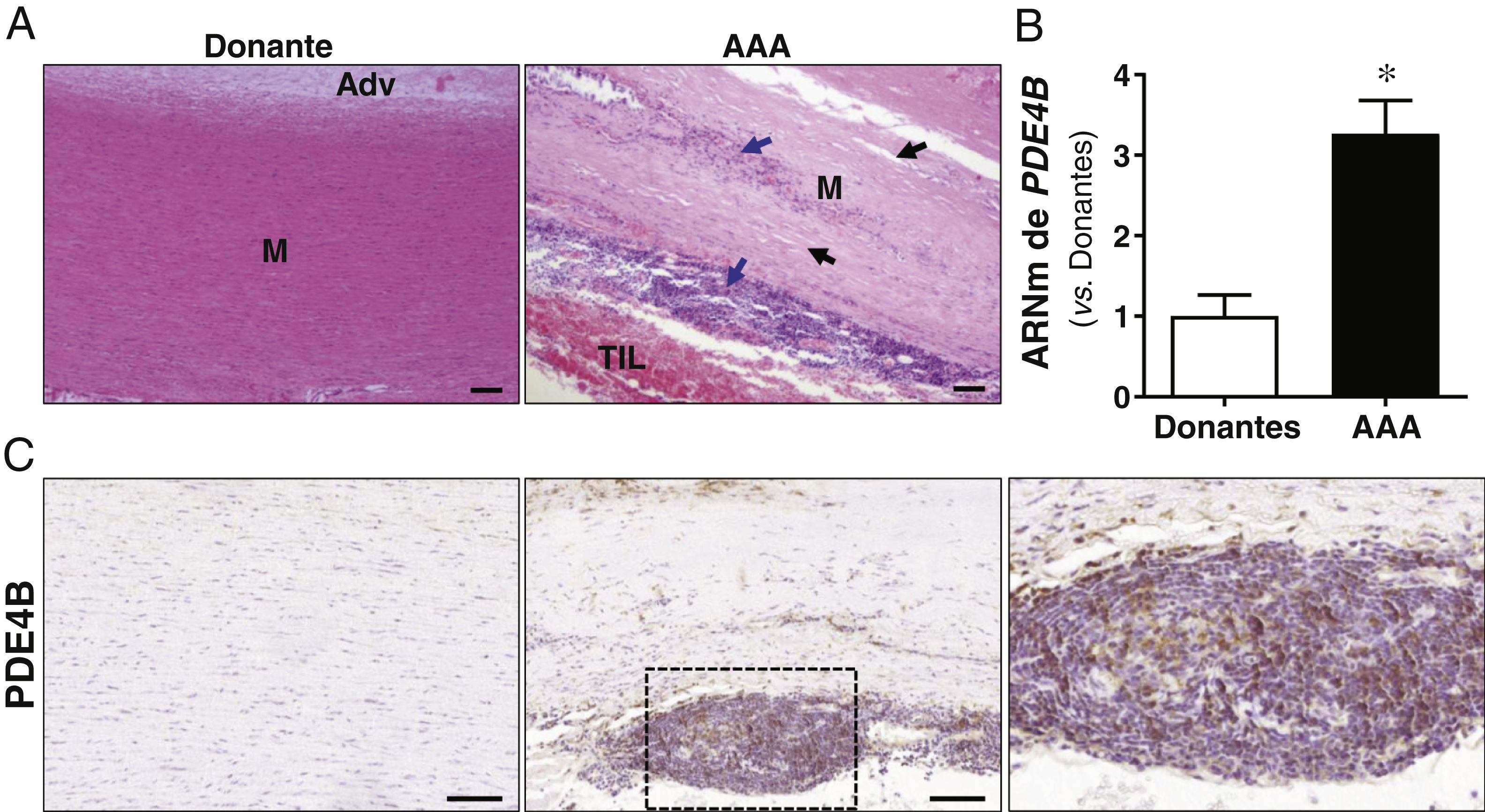
ResultadosExpresión de PDE4B en el aneurisma de aortaNuestro grupo había demostrado previamente que la expresión de la PDE4B está incrementada en el AAA humano16. Estos resultados se han confirmado en una segunda cohorte de pacientes. En comparación con la aorta sana, que muestra una estructura compacta en la que las CMLV se disponen de manera ordenada, la pared vascular de los pacientes con AAA está parcialmente desorganizada y presenta un importante infiltrado inflamatorio, así como una pérdida de CMLV (fig. 1A). En estas muestras, el análisis por RT-PCR a tiempo real constató un incremento significativo del nivel de mRNA de la PDE4B en las lesiones aneurismáticas en comparación con aortas sanas procedentes de donantes de órganos (fig. 1B). Los estudios inmunohistoquímicos confirmaron la inducción de la expresión de PDE4B en el AAA, en el que este enzima se localiza principalmente en células inflamatorias (fig. 1C). La expresión en la aorta de donantes fue prácticamente inapreciable (fig. 1C).
La expresión de PDE4B está aumentada en el AAA humano. A) Imágenes representativas de las tinciones de hematoxilina-eosina de muestras de aorta abdominal procedentes de donantes sanos (Donante) y pacientes con AAA (AAA) en la que se puede observar la desorganización de la pared vascular en esta enfermedad caracterizada por un importante infiltrado inflamatorio (flechas azules) y la pérdida de contenido en CMLV (flechas negras). Se indica la posición de la media (M), la adventicia (Adv) y el trombo intraluminal (TIL) que se detecta en la lesión aneurismática (Barras: 100μm). B) Cuantificación del nivel de mRNA de PDE4B en la aorta abdominal de donantes (n=15) y pacientes con AAA (n=27). Los resultados se muestran como media±SEM. *p<0,001 vs. donantes. C) Análisis inmunohistoquímico para PDE4B en dichas muestras. Se indica con un recuadro la región magnificada correspondiente al infiltrado inflamatorio positivo para PDE4B (Barras: 100μm).
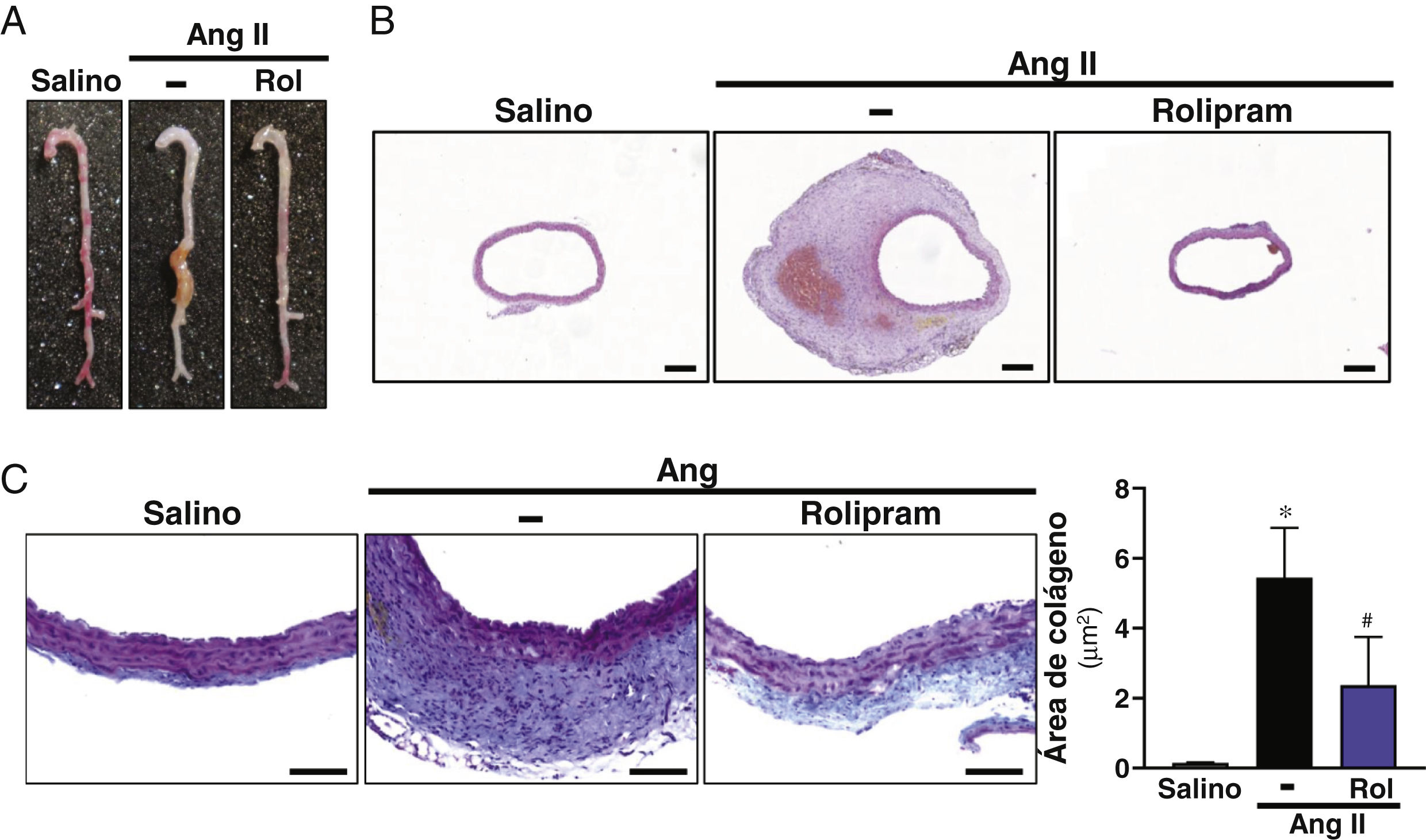
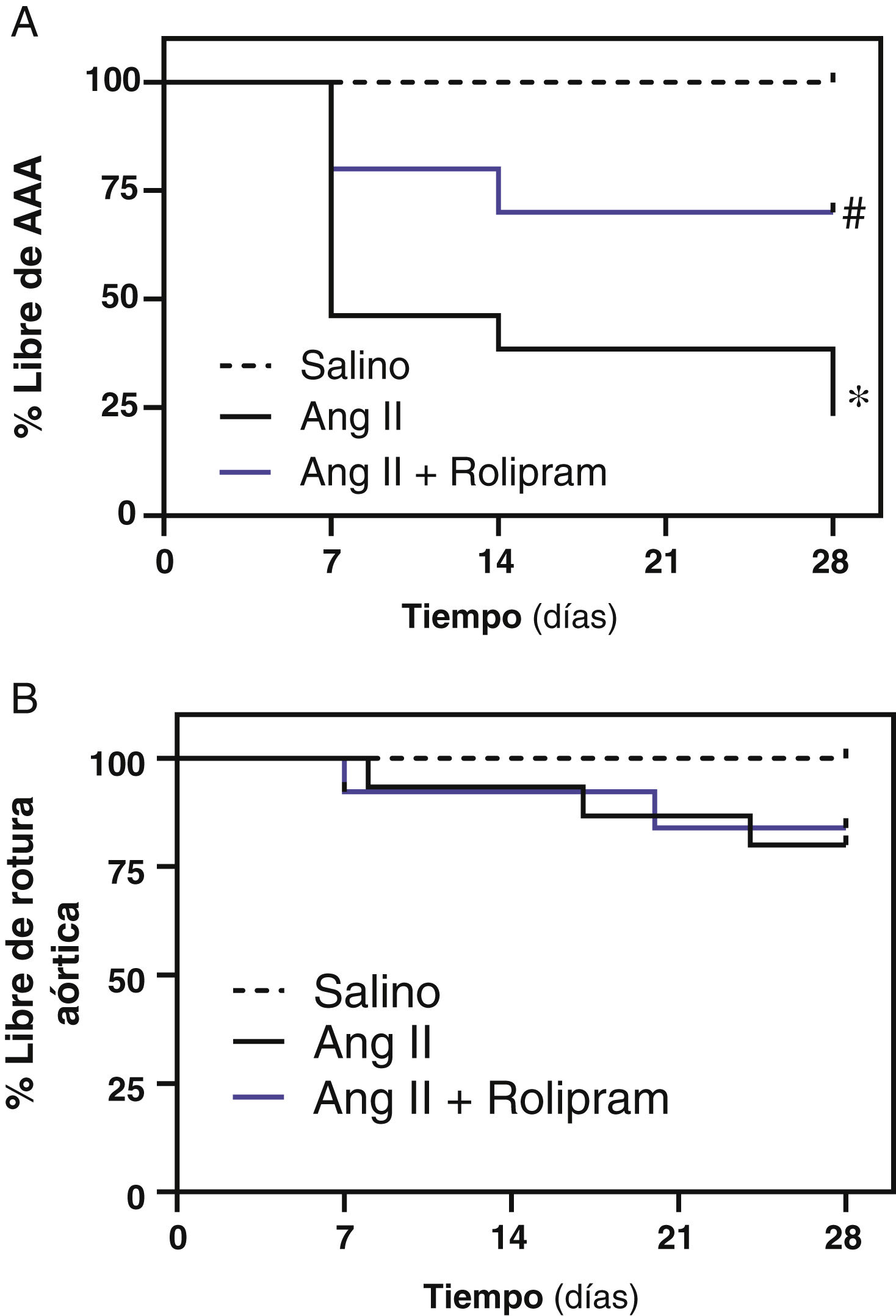
La administración de rolipram en el modelo de inducción de AAA por infusión de Ang II en ratón ApoE-/− atenuó la formación de aneurismas (fig. 2A)16. De hecho, los análisis histológicos mostraron que este fármaco limitó de forma patente el remodelado vascular (fig. 2B) y redujo significativamente la deposición de colágeno inducida por la Ang II evaluado mediante la tinción de tricrómico de Mason (fig. 2C). Tras la administración de Ang II, el porcentaje de animales libres de aneurisma fue reduciéndose progresivamente a lo largo del procedimiento experimental, y al finalizar el tratamiento se situó en torno a 25% de los animales (fig. 3A). El tratamiento con rolipram atenuó esta respuesta. En efecto, el patrón temporal en el grupo de animales en los que se inhibió la actividad PDE4 difirió del mostrado por el grupo infundido con Ang II, y al cabo de 28 días este porcentaje fue de 75%, significativamente superior al de los animales que recibieron únicamente Ang II (fig. 3A). Por el contrario, no se observaron diferencias significativas en el porcentaje de animales libres de rotura aórtica (fig. 3B).
El tratamiento con rolipram atenúa la formación de AAA en ratones ApoE-/− infundidos con Ang II. Los ratones ApoE-/− se infundieron con solución salina (salino) o Ang II (1000 ng/kg/min) durante 28 días y se trataron o no con rolipram (Rol; 3mg/kg/día; i.p.). A) Imágenes macroscópicas de las aortas de cada uno de los grupos experimentales. B) Imágenes representativas de tinciones de hematoxilina-eosina de cortes de muestras de los grupos indicados en A (Barras: 200μm). C) Imágenes representativas de tinciones de tricrómico de Mason de cortes de muestras de los grupos indicados en A (Barras: 100μm). El histograma muestra la cuantificación del área positiva para colágeno. Los resultados se muestran como media±SEM p<0,05: * vs. salino; # vs. Ang II. (salino, n=5; Ang II, n=10; rolipram, n=6).
El rolipram atenúa el desarrollo de AAA en ratones ApoE-/− infundidos con Ang II. Los ratones ApoE-/− se infundieron con solución salina (salino) o Ang II (1.000 ng/kg/min) durante 28 días y se trataron o no con rolipram (3mg/kg/día; i.p.). A) Se muestra el porcentaje de animales libre de AAA a lo largo del periodo experimental en cada grupo p<0,05: * vs. salino; # vs. Ang II. B) Porcentaje de animales libre de roturas aórticas (salino, n=9; Ang II, n=15; rolipram, n=13).
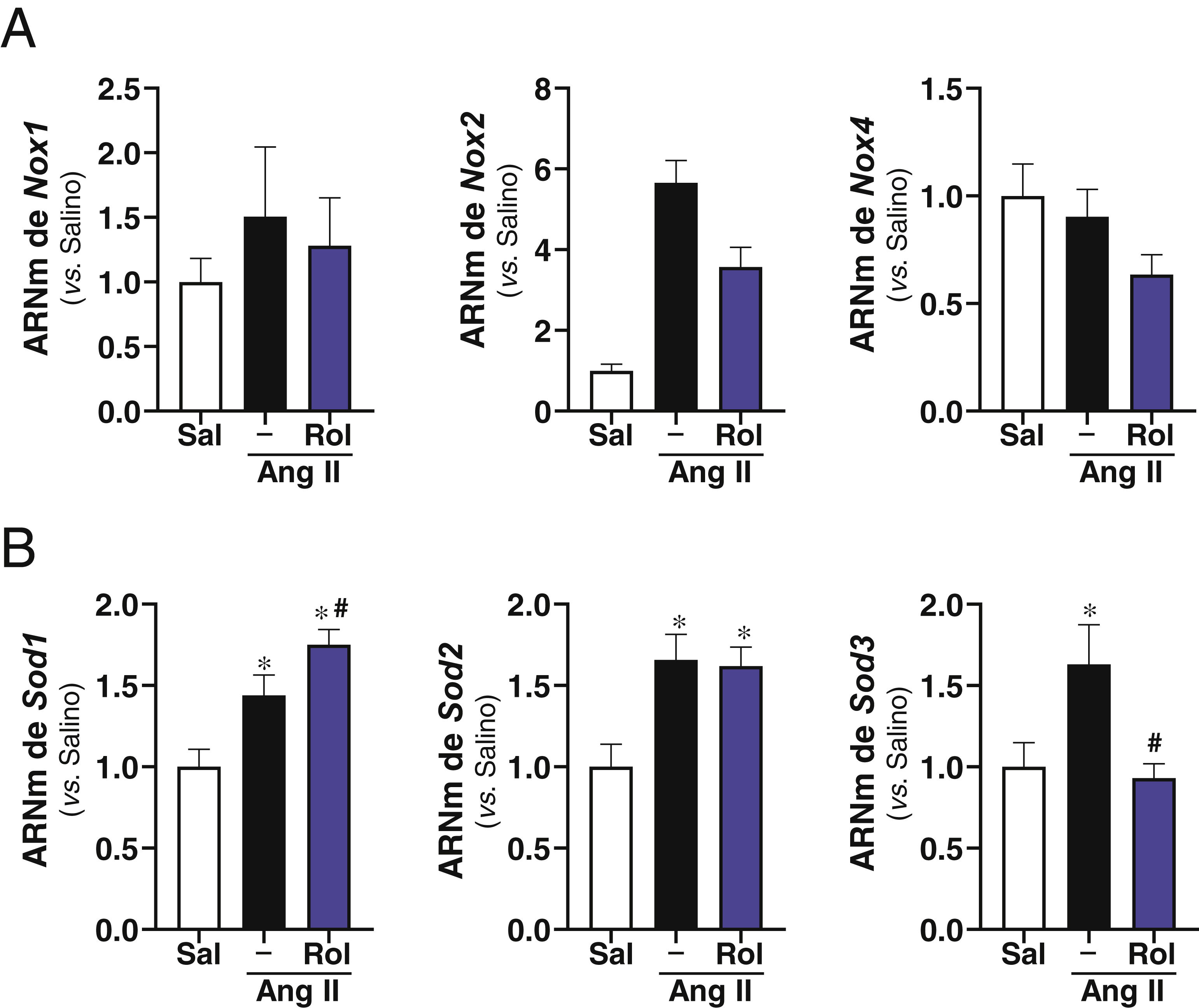
Nuestros estudios previos habían demostrado que el rolipram disminuye la producción de radical superóxido en la aorta abdominal del ratón ApoE-/− infundido con Ang II16. Por ello, caracterizamos la expresión de dos de los sistemas enzimáticos que contribuyen a la homeostasis rédox en la vasculatura. Concretamente analizamos la expresión de distintas isoformas de la NADPH oxidasa y de enzimas de la familia de Sod. En nuestro modelo experimental la Ang II no modificó el nivel de mRNA de Nox1 y Nox4 pero indujo significativamente la expresión de Nox2, un incremento que disminuyó parcialmente por la administración de rolipram (fig. 4A). A su vez, la Ang II indujo la expresión vascular de Sod1, Sod2 y Sod3 (fig. 4B). La inhibición de la actividad PDE4 con rolipram exacerbó el incremento en el nivel de mRNA de Sod1 y normalizó la expresión de Sod3 sin que se viera afectado el aumento en la expresión de Sod2 (fig. 4B).
Efecto del tratamiento con rolipram sobre la expresión de enzimas implicados en la homeostasis rédox en ratones ApoE-/− infundidos con Ang II. Los ratones ApoE-/− se infundieron con solución salina (Sal) o Ang II (1.000 ng/kg/min) durante 28 días y se trataron o no con rolipram (Rol; 3mg/kg/día; i.p.). A) Se muestran los niveles de expresión para Nox1, Nox2 y Nox4 evaluados mediante RT-PCR en la aorta abdominal de cada grupo experimental B) Nivel de mRNA para la Sod1, Sod2 y Sod3. Los resultados se muestran como media±SEM. *p<0,05 vs. salino. #p<0,05 vs. Ang II sola (salino, n=10; Ang II, n=8; rolipram, n=12).
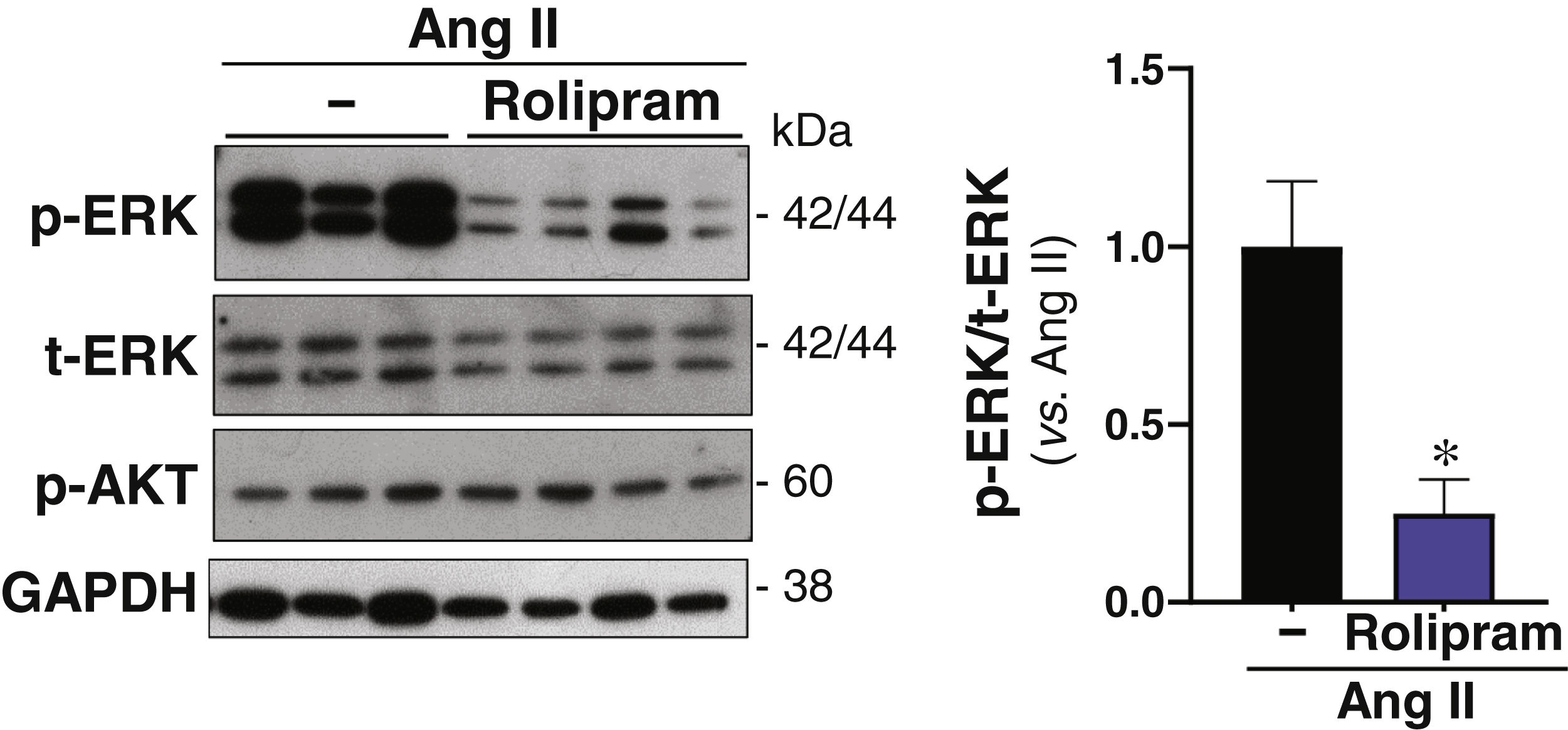
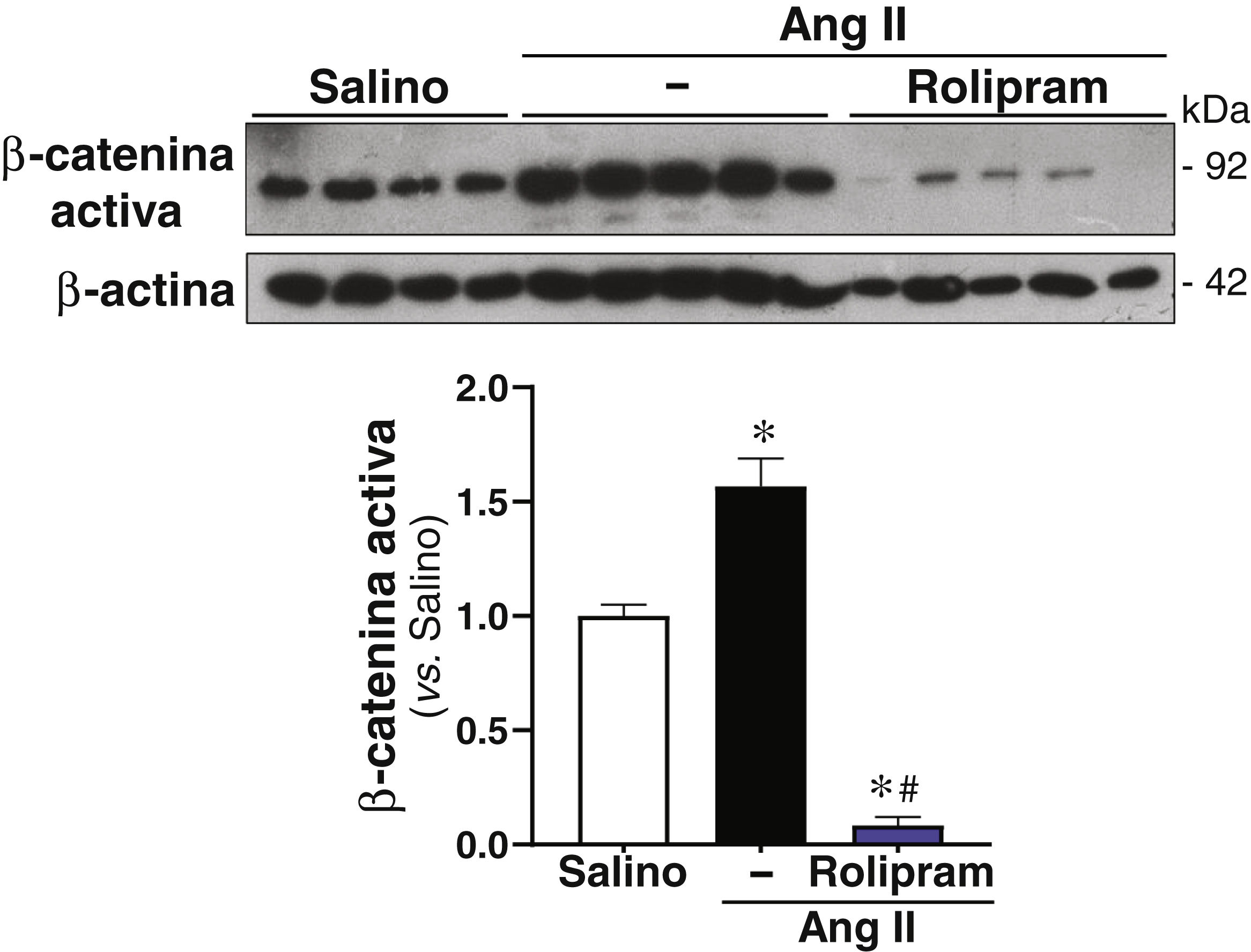
La vía de señalización de ERK1/2 juega un papel fundamental en la inflamación vascular y en la activación de metaloproteasas (MMPs), procesos clave en el desarrollo del AAA. Nuestros análisis demuestran que la actividad ERK1/2 detectada en las lesiones aneurismáticas de los ratones ApoE-/− infundidos con Ang II disminuye significativamente en los animales tratados con rolipram (fig. 5). Por el contrario, no observamos diferencias significativas en lo referente a la activación de la AKT, que no se vio afectada por el tratamiento con este fármaco. A su vez la activación de la ruta canónica de Wnt o dependiente de β-catenina en el AAA, previamente descrita por nuestro grupo21, se redujo significativamente por el tratamiento con rolipram (Fig. 6).
Efecto del tratamiento con rolipram sobre la activación de ERK1/2 y AKT en ratones ApoE-/− infundidos con Ang II. Los ratones ApoE-/− se infundieron con Ang II (1.000 ng/kg/min) durante 28 días y se trataron o no con rolipram (Rol; 3mg/kg/día; i.p.). Se muestran imágenes representativas del análisis por Western blot correspondientes a los niveles de la forma fosforilada de ERK1/2 (p-ERK1/2), ERK total (t-ERK), y la forma fosforilada de AKT (p-AKT). Los niveles de GAPDH se muestran como control de carga. El histograma corresponde a la cuantificación relativa del nivel de fosforilación de AKT en cada grupo experimental. Los resultados se muestran como media±SEM (salino, n=4; Ang II, n=6; rolipram, n=4). *p<0,05 vs. Ang II sola.
El rolipram atenúa la activación de la vía canónica de Wnt en ratones ApoE-/− infundidos con Ang II. Los ratones ApoE-/− se infundieron solución salina (salino) o con Ang II (1.000 ng/kg/min) durante 28 días y se trataron o no con rolipram (Rol; 3mg/kg/día; i.p.). Se muestran imágenes representativas del análisis por Western blot correspondientes a los niveles de la β-catenina activa en cada grupo experimental. Los niveles de β-actina se muestran como control de carga. El histograma corresponde a la cuantificación del nivel de β-catenina activa en cada grupo experimental. Los resultados se muestran como media±SEM. p<0,001: * vs. salino; # vs. Ang II sola. (salino, n=4; Ang II, n=5; rolipram, n=5).
Actualmente no existen estrategias farmacológicas para limitar el desarrollo del AAA. La única medida terapéutica disponible es la intervención quirúrgica (cirugía abierta o endovascular) de aquellos aneurismas con alto riesgo de rotura (diámetro aórtico>5-5,5cm)13,14. Aunque se ha sugerido que las estatinas, la doxiciclina, los inhibidores de la ciclooxigenasa 2 (COX-2) o de la enzima convertidora de angiotensina, entre otros, podrían reducir la progresión del AAA, ninguno de ellos ha demostrado un beneficio clínico concluyente14. La ausencia de fármacos útiles en el tratamiento del AAA es un gran obstáculo a la hora de afrontar el manejo clínico de estos pacientes y por tanto es evidente la necesidad de identificar y desarrollar nuevas herramientas farmacológicas para el tratamiento y prevención de esta patología.
La alteración del nivel de AMPc en la pared vascular podría afectar a procesos clave implicados en la patología aneurismática. De hecho, se ha demostrado que en el AAA humano se produce una disminución de la expresión de la subunidad alfa Gs (GSα), lo que reduce la producción de AMPc y agrava el desarrollo de aneurismas inducidos por la Ang II22. En este contexto, la subfamilia de enzimas PDE4 podría desempeñar también un importante papel en el desarrollo de esta enfermedad debido a su capacidad para regular los niveles de AMPc. PDE4 se considera una de las principales dianas terapéuticas en enfermedades inflamatorias, si bien su posible utilidad en el aneurisma no se había explorado en profundidad hasta el desarrollo de nuestras investigaciones que demostraron la inducción de PDE4B tanto en el AAA humano como experimental16.
Este estudio ha corroborado el aumento de la expresión de PDE4B en las lesiones aneurismáticas en una segunda cohorte de pacientes. En estas lesiones, PDE4B se localizó principalmente en el infiltrado inflamatorio, en concordancia con el hecho de que esta isoforma es la principal enzima PDE4 expresada en células inflamatorias7. Nuestros estudios previos habían descartado un papel relevante en la patología aneurismática de la isoforma PDE4D, si bien posteriormente otros autores detectaron un aumento en la expresión de PDE4D en las CMLV en pacientes con AAA y en lesiones aneurismáticas murinas, sin alteración de PDE4B23. Las discrepancias entre ambos estudios podrían estar relacionadas con el bajo número de muestras humanas analizadas por Gao y colaboradores23 y su heterogeneidad así como a las diferencias en los modelos animales de AAA. En cualquier caso, ambos estudios previos y el presente demuestran que la inhibición de la actividad PDE4 mediante rolipram atenúa el desarrollo del AAA16,23. En efecto, el rolipram aumentó el porcentaje de animales libres de AAA. Por el contrario, no observamos diferencias significativas en la incidencia de rotura aórtica, principal responsable de la mortalidad en este modelo animal. la activación simpática se ha vinculado con la disección aórtica. La activación simpática se ha vinculado con la disección aórtica19 y puesto que el rolipram podría incrementar la síntesis y liberación de noradrenalina24 este fenómeno podría estar involucrado en la ausencia de beneficio de este fármaco sobre la rotura aórtica.
Habíamos descrito que el rolipram ejerce un efecto beneficioso sobre el remodelado vascular en el AAA ya que preserva la integridad de la elastina, disminuye la actividad MMP y atenúa el incremento en el nivel de mRNA del colágeno 1A116. El presente estudio constata el beneficio del rolipram sobre el remodelado de la matriz extracelular, ya que la inhibición de la PDE4 disminuyó el aumento del colágeno en la lesión aneurismática, una respuesta adaptativa y compensatoria dirigida a mantener la estabilidad mecánica de la pared aneurismática que se produce en estadios avanzados de esta enfermedad25.
Asimismo, habíamos determinado que el rolipram reduce el infiltrado inflamatorio y atenúa el estrés oxidativo vascular. Múltiples estudios han demostrado el marcado desequilibrio rédox en la pared vascular de los pacientes con AAA y la asociación del estrés oxidativo con la patogénesis del AAA26,27. La fuente principal de especies reactivas de oxígeno (ROS) en el sistema cardiovascular es la familia de enzimas NOX. En las lesiones aneurismáticas de nuestro modelo experimental detectamos la inducción específica y significativa de la Nox2, una respuesta que se atenuó en presencia de rolipram. Puesto que la deleción de Nox2 es capaz de limitar el desarrollo de AAA en modelos experimentales28, este efecto podría estar implicado en el beneficio que ejerce el rolipram sobre el desarrollo del AAA. Por su parte, las enzimas Sod constituyen uno de los principales mecanismos de defensa antioxidante. Estudios en modelos experimentales de AAA han descrito la inducción temprana de la actividad Sod29 y de la expresión de la Sod230, lo que se ha propuesto como una respuesta compensatoria frente al aumento de ROS en el aneurisma31. Análogamente, determinamos que la expresión de las tres enzimas Sod analizadas (Sod1, Sod2 y Sod3) aumenta en las lesiones aneurismáticas en el ratón ApoE-/− infundido con Ang II. Cabe destacar que el rolipram exacerbó el aumento del nivel de mRNA de Sod1 (isoforma citoplasmática) en la aorta abdominal, lo que podría contribuir a su efecto protector frente a la formación del AAA. Este fármaco no alteró el nivel de mRNA de la Sod2 (isoforma mitocondrial) en respuesta a la Ang II; sin embargo, el rolipram atenuó la inducción de Sod3 (isoforma extracelular) detectada en las lesiones aneurismáticas, una respuesta que tendría una escasa repercusión final ya que, pese a ello, el rolipram reduce el incremento del estrés oxidativo vascular en nuestro modelo experimental16.
El desarrollo del AAA se asocia con la alteración de numerosas vías de transducción de señales, entre ellas la inducción por fosforilación de la ERK1/232,33 y de la AKT34–36 que juegan un papel clave en la activación de las MMPs durante el desarrollo del AAA33,34. A diferencia de lo observado en el caso de la AKT, el rolipram fue capaz de limitar la inducción de la ERK1/2 en nuestro modelo experimental de aneurisma, en concordancia con estudios previos en otros escenarios patológicos que han mostrado la eficacia de este fármaco atenuando la inducción de ERK1/2 y limitando así la apoptosis y la fibrosis, procesos que participan en la fisiopatología del AAA37,38.
En las últimas décadas, la señalización de Wnt ha captado la atención de la comunidad científica debido a su alto potencial terapéutico. En adultos, esta vía se reactiva en varios escenarios patológicos, incluidas las enfermedades cardiovasculares, y, en relación con el sistema cardiovascular, se considera que la activación excesiva de la señalización de Wnt tiene consecuencias perjudiciales39. Nuestros estudios previos demostraron que la activación de la vía de Wnt es característica de la patología aneurismática21. Específicamente, observamos que en el AAA humano y experimental se produce una alteración de múltiples componentes de la señalización mediada por Wnt asociada a la activación de la vía canónica o dependiente de β-catenina21. Destacar que en los animales infundidos con Ang II el rolipram fue capaz de reducir muy significativamente el nivel de β-catenina activa, un efecto similar al descrito para otros inhibidores PDE4 específicos en modelos de leucemia mieloide aguda40. La inhibición de esta vía podría estar relacionada con una supresión de la osteoclastogénesis en macrófagos, un fenómeno que contribuiría al desarrollo del AAA41, postulando su contribución a la respuesta beneficiosa ejercida por el rolipram.
En conclusión, este trabajo caracteriza los mecanismos moleculares modulados por el rolipram en la patología aneurismática, determinando el impacto de este fármaco sobre dos de los sistemas enzimáticos que contribuyen a la homeostasis rédox en la vasculatura (isoformas de NOX y Sod) y sobre vías de señalización claves en la patología aneurismática como la ERK1/2 y la vía de Wnt. Estos mecanismos podrían contribuir al efecto beneficioso de la inhibición de la actividad PDE4 sobre el AAA.
FinanciaciónEste trabajo ha sido realizado gracias a la financiación obtenida a través de la Fundación Española de Arteriosclerosis (Beca FEA 2020-Investigación Básica III). Además, el estudio ha contado con financiación del Instituto de Salud Carlos III (ISCIII; PI21/01048) y el Ministerio de Ciencia e Innovación (PID2021-122509OB-I00 financiado por MCIN/ AEI/10.13039/501100011033 y por «FEDER Una manera de hacer Europa». L.P-U fue financiada a través de un contrato PFIS (ISCIII).
Conflicto de interesesAlicia Santamaría-Orleans es empleada de Laboratorios Ordesa S.L.