La enfermedad cardiovascular sigue siendo la primera causa de mortalidad en los países occidentales. Se necesitan nuevas estrategias para la prevención y el control de esta enfermedad. Al mismo tiempo, la incidencia de factores de riesgo que conducen al desarrollo de esta afección, como la obesidad, la hipertensión y la diabetes, sigue aumentando. Por lo tanto, la búsqueda de nuevos marcadores o mediadores es una prioridad en la mayoría de los programas de prevención cardiovascular. El estudio de la microbiota intestinal está surgiendo porque se sabe que los microorganismos intestinales actúan colectivamente como un órgano integrado, regulando múltiples funciones biológicas que pueden modular los factores de riesgo cardiovascular y los mecanismos patógenos de este proceso. Esta revisión considera la situación actual con respecto a la influencia de la microbiota intestinal en la enfermedad cardiovascular y, en particular, su influencia en los principales factores de riesgo tradicionales que conducen a la enfermedad cardiovascular, como la obesidad, la diabetes, la hipertensión y los lípidos.
Cardiovascular disease remains the first cause of mortality in Western countries. New strategies for prevention and control of cardiovascular disease are needed. At the same time, the incidence of risk factors that lead to the development of this disease, such as obesity, hypertension and diabetes, continues to rise. Therefore, the search for new markers or mediators is a priority in most cardiovascular prevention programs. The study of the intestinal microbiota is emerging because it is known that intestinal microorganisms act collectively as an integrated organ, regulating multiple biological functions that can modulate cardiovascular risk factors and the pathogenic mechanisms of this process. This review considers the current situation regarding the influence of gut microbiota on cardiovascular disease and particularly, its influence on the main traditional risk factors that lead to cardiovascular disease, such as obesity, diabetes, hypertension and lipids.
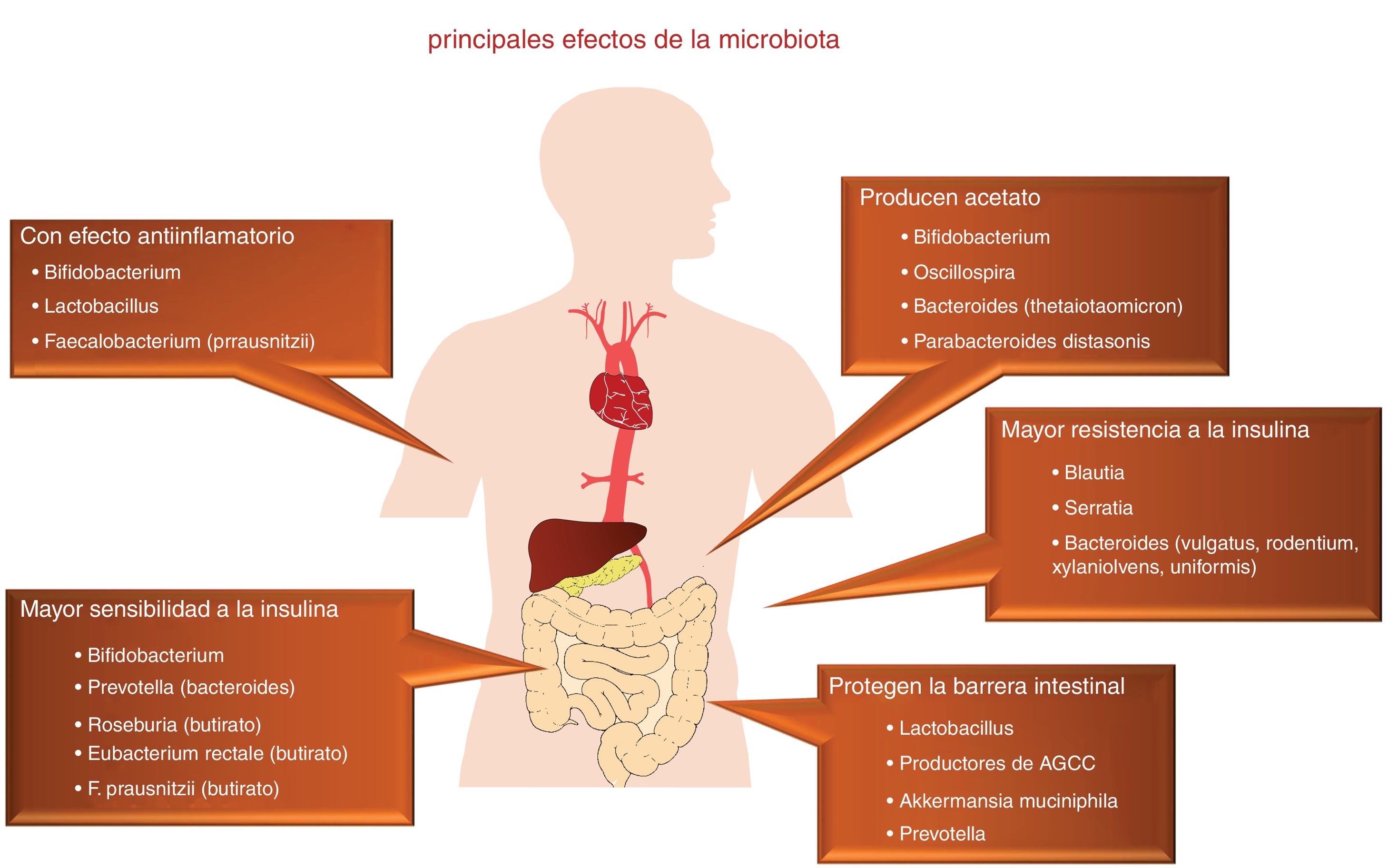
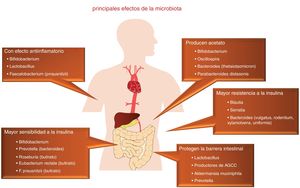
A finales de los años 80 se divulgó con una gran fuerza y expectativa la etiología infecciosa de la arteriosclerosis, en relación con la infección por varios agentes patógenos específicos1. Esta hipótesis se abandonó ante el resultado negativo de varios ensayos clínicos con antibióticos, que ahora consideramos de diseño no siempre afortunado. En este contexto, actualmente está volviendo a replantearse dicha patogenia, aunque desde un punto de vista muy diferente, ya que ahora no se centra en microorganismos concretos, sino en el protagonismo de la rica flora saprofita presente en el ser humano, incluyendo la amplia población bacteriana comensal que reside en nuestro intestino2. En este sentido, el tracto gastrointestinal humano se ha considerado tradicionalmente como un órgano pasivo que recibe componentes de la dieta, donde son absorbidos o metabolizados. Sin embargo, hoy sabemos que nuestro intestino es el hogar de billones de microorganismos, denominados de forma colectiva microbiota intestinal, que desempeñan un papel clave como órgano endocrino, metabólico e inmunológico, generando múltiples señalizaciones que actúan localmente sobre múltiples sistemas orgánicos, por su interacción con los componentes de la dieta (fig. 1).
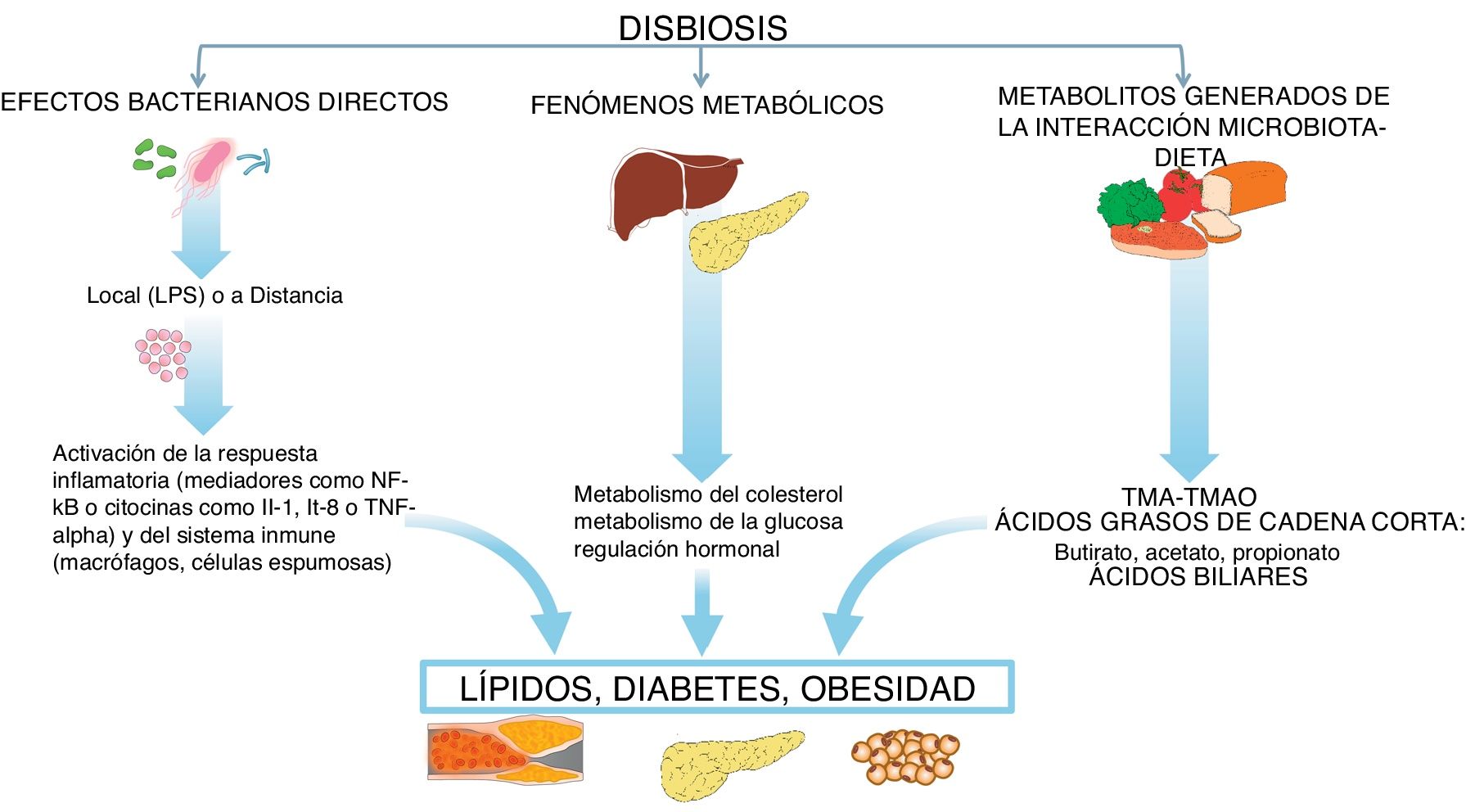
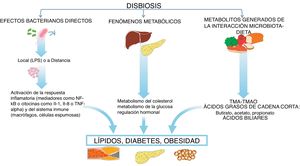
En esta interacción microbiota-intestino-órganos sistémicos pueden activarse mecanismos que pueden influir en la expresión de los principales factores de riesgo, como la diabetes, la hipertensión, la obesidad y las dislipidemias, así como influir directamente en diferentes mecanismos biológicos que participan en la arteriosclerosis3–5, como seguidamente veremos (fig. 2).
Mecanismos biológicos por los que la microflora influye en el desarrollo de arteriosclerosisEntre los mecanismos por los que la microflora influye en el desarrollo de arteriosclerosis, encontramos:
- -
Ciertos productos derivados de la interacción de la dieta con la flora intestinal pueden alterar la respuesta inflamatoria e inmune que influye en el proceso aterosclerótico6–8, lo que conlleva la producción de factores circulantes proaterogénicos que pueden influir en el riesgo cardiovascular9,10. Así, es conocido que la microbiota produce trimetilamina, utilizando la fosfatidilcolina procedente de la carne roja, el marisco y los huevos, o bien la L-carnitina, abundante también en la carne roja pero que además se encuentra en bebidas energéticas o en ciertos nutracéuticos. Esta trimetilamina es oxidada en el hígado, por enzimas flavin monooxigenasas, produciéndose de esta reacción trimetilamina N-óxido (TMAO), la cual actúa como producto aterogénico11. Esta evidencia, que pone como eje central el papel de la microbiota, fue confirmada a través de un estudio que midió los niveles de TMAO tras el consumo de fosfatidilcolina marcada, con y sin antibióticos, evidenciándose que los antibióticos suprimían el incremento del TMAO plasmático12. En este sentido, Wang et al. también demostraron que el metabolismo microbiano de la fosfatidilcolina promueve el desarrollo de enfermedad cardiovascular (ECV). En este estudio, los autores identificaron la TMAO como posible factor de riesgo modificable para las ECV6. Posteriormente, un estudio clínico con más de 4.000 participantes confirmó que los niveles séricos de TMAO predecían la incidencia de riesgo cardiovascular de manera dependiente de la dosis7. Estudios muy recientes han confirmado que la microbiota influye en los niveles plasmáticos de TMAO y, al mismo tiempo, evidencian que este hecho implica la activación plaquetaria13. Sin embargo, actualmente persiste el debate de si el incremento de las concentraciones de TMAO es la consecuencia o el resultado del desarrollo de ECV14.
- -
Otro posible mecanismo está mediado por los ácidos grasos de cadena corta (AGCC), como el acético, el butírico, el propiónico y el valérico, que son metabolitos derivados de la microbiota intestinal con propiedades hormonales y que proceden de la fermentación de la fibra a través de un subconjunto de bacterias con actividad sacarolítica15–17. Estos AGCC influyen de manera directa sobre el riesgo de desarrollar ECV, ya que modulan la acción de la insulina, la respuesta inmune y el metabolismo energético18–20. Específicamente, los AGCC procedentes de la fermentación bacteriana estimulan la liberación de péptido similar al glucagón tipo 1 por parte de las células L del intestino, lo que conlleva un aumento de la secreción de insulina pancreática, una supresión del glucagón y un aumento de la sensibilidad a la misma21. Al mismo tiempo, se ha demostrado que los AGCC estimulan la secreción de péptido YY, una hormona implicada en la regulación del apetito, concretamente reduciéndolo, y que, al mismo tiempo, inhibe la motilidad del intestino y disminuye la obtención de energía procedente de la dieta22. Finalmente, estudios in vitro han demostrado que los AGCC pueden influir en el desarrollo de dislipidemia ya que inhiben la lipolisis y la concentración final de ácidos grasos libres a través de la activación del receptor de ácidos grasos libres 221.
- -
Por otro lado, la microbiota intestinal puede ejercer un papel modulador del metabolismo lipídico, influyendo en el desarrollo de aterosclerosis, a través del metabolismo de los ácidos biliares23,24. Los ácidos biliares primarios, ácido cólico y ácido quenodesoxicólico, son sintetizados en el hígado a partir del colesterol y resultan esenciales para la absorción de este y de las vitaminas liposolubles. La microbiota intestinal tiene la capacidad de desconjugar estos ácidos biliares y transformarlos en secundarios (principalmente desoxicólico), influyendo por tanto en el metabolismo del colesterol, ya que, como es conocido, esta síntesis de ácidos biliares es la principal vía catabólica del colesterol. Al mismo tiempo, ciertas bacterias intestinales son capaces de metabolizar los ácidos biliares primarios y estos tienen múltiples funciones por su capacidad para acoplarse a receptores tales como el X farnesoide (principalmente activado por los ácidos biliares primarios) o el receptor de ácidos biliares acoplado a la proteína G 5, principalmente los secundarios25,26. En resumen, la microbiota intestinal interviene y modula el metabolismo de los ácidos biliares, elementos, estos, clave en la homeostasis lipídica.
- -
Otro potencial mecanismo aterogénico de la microbiota es a través del papel que juega en el mantenimiento de la integridad de la barrera intestinal, que evita la absorción de componentes bacterianos proinflamatorios como componentes de la pared celular bacteriana, principalmente los lipopolisacáridos (LPS). Estos LPS son reconocidos por los receptores tipo Toll (TLR), por lo que tienen potencial de activar la vía inflamatoria a través de la activación a su vez de NF-κB, que ha demostrado que produce citocinas inflamatorias como IL-1, IL-8 o TNF-α27.
- -
Finalmente, es conocido que la microbiota intestinal puede influir sobre el sistema endocrino del huésped alterando el metabolismo funcional de hormonas importantes como la leptina, la grelina y el cortisol28–30. Ello apunta a que existe un diálogo entre nuestro sistema intestinal y nuestro cerebro en cuanto a la producción hormonal, donde la microbiota juega un papel clave en la regulación de dicho eje.
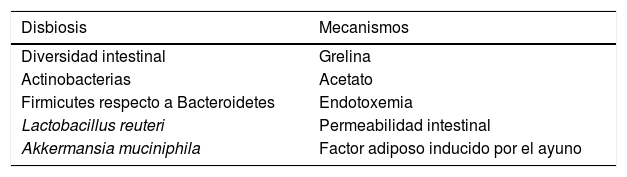
La prevalencia y la incidencia de la obesidad están en continuo crecimiento, al igual que pasa con el resto de los factores de riesgo cardiovascular, probablemente de la mano de estilos de vida inadecuados en los que los malos hábitos dietéticos y el sedentarismo juegan un papel relevante31. La patogenia de la obesidad es muy compleja y se ha demostrado que la microbiota intestinal es también uno de los mecanismos reguladores metabólicos más importantes32,33 (tabla 1). En estudios animales se ha demostrado que el fenotipo de obesidad se acompaña de una disminución de la diversidad bacteriana y un aumento del cociente Firmicutes/Bacteroidetes, 2 de los principales filos bacterianos34. Además, se ha visto que cambios en la alimentación de ratones, sometiéndolos a dietas obesogénicas, indujeron modificaciones en la microbiota que fueron independiente de la ganancia de peso35, y que el trasplante de heces de ratones obesos a ratones delgados induce un aumento del peso en estos últimos36.
Principales mecanismos relacionados con la disbiosis de pacientes con obesidad
| Disbiosis | Mecanismos |
|---|---|
| Diversidad intestinal | Grelina |
| Actinobacterias | Acetato |
| Firmicutes respecto a Bacteroidetes | Endotoxemia |
| Lactobacillus reuteri | Permeabilidad intestinal |
| Akkermansia muciniphila | Factor adiposo inducido por el ayuno |
Las observaciones llevadas a cabo en animales de experimentación se han podido trasladar parcialmente a estudios en humanos, donde los resultados son más inconsistentes y variables. Este hecho probablemente se debe a la mayor complejidad de los humanos, a la heterogeneidad de las poblaciones, así como al difícil control del entorno en el que nos movemos. En humanos con obesidad, algunos estudios han confirmado el incremento del cociente Firmicutes/Bacteroidetes, mientras que en otras los resultados han sido más imprecisos o bien se ha detectado un incremento de Actinobacterias37,38. Por otra parte, se ha observado que géneros que pertenecen a las mismas familias pueden tener funcionalidades similares, lo que le da un limitado valor al hecho de que haya cambios en la proporción de ciertas familias, debido a la heterogeneidad funcional de sus componentes. Un ejemplo lo constituyen los lactobacilos y las bifidobacterias, que son géneros muy frecuentes en la población intestinal y muy utilizados como probióticos, que pueden tener características variables según la especie concreta. Así, Lactobacillus plantarum y Lactobacillusparacasei se asocian a un peso normal, mientras que Lactobacillus reuteri se ha descrito asociado a obesidad39.
Aún no disponemos de estudios clínicos suficientes que hayan investigado la influencia de la microbiota sobre la obesidad en seres humanos. En uno de ellos, nuestro grupo demostró que el 31% de la variación interindividual en el índice de masa corporal (IMC) depende de la composición de la flora intestinal. En él se analizaron 39 hombres y 36 mujeres posmenopáusicas, demostrando que la abundancia del género Bacteroides fue menor en hombres que en mujeres cuando el IMC fue mayor de 33kg/m2, pero no en grados de obesidad menor. Por el contrario, este hallazgo no se confirmó en mujeres en diferentes rangos de IMC. Además, se encontraron otras diferencias a nivel de sexo, como es la mayor presencia de los géneros Veillonella y Methanobrevibacter en hombres, lo que ejemplifica que este es uno de los factores que impide extrapolar las evidencias en este campo a otras poblaciones40. Por otro lado, nuestro grupo ha demostrado que el consumo crónico de una dieta cardiosaludable constituye una potente herramienta para mejorar la disbiosis intestinal observada en pacientes obesos con ECV41,42.
En cuanto a la patogenia de la obesidad, aunque específicamente es desconocida, sí se sabe que en ella existe una inflamación de bajo grado que sin duda influye en su desarrollo y en la que la microbiota ejerce un papel fundamental. Así, se ha demostrado que ciertos componentes generados por las bacterias gramnegativas tienen un efecto proinflamatorio43. Asimismo, sobre animales de experimentación se ha observado que la infusión crónica de LPS produce un estado de endotoxemia crónica que induce una inflamación, acompañada de un aumento de peso. Además, en los ratones alimentados 4 semanas con LPS se incrementa la inflamación del tejido adiposo y se induce resistencia a la insulina44. Finalmente, es conocido que el estado de la microbiota determinará la permeabilidad de la barrera intestinal y esto, a su vez, condicionará el paso a su través de las toxinas, los antígenos y las bacterias presentes en la luz intestinal, iniciando la inflamación y conduciendo al desarrollo de obesidad45.
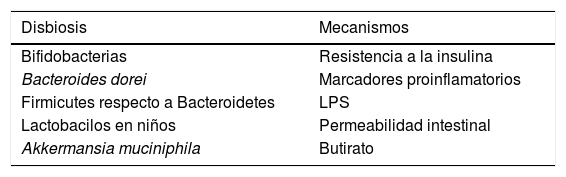
Influencia de la microbiota sobre la diabetesVivimos un momento en que se están incrementando las medidas terapéuticas para combatir esta enfermedad, aunque su control está aún lejos de alcanzarse y se precisará seguir investigando sobre su patogenia. En los últimos años, la evidencia de que la microbiota intestinal influye sobre la diabetes está en alza46 (tabla 2). Un ejemplo que demuestra este nexo de unión es que los hijos nacidos por cesárea tienen mayor riesgo de desarrollar diabetes mellitus tipo 1 que los nacidos de parto vaginal y que la colonización del intestino es diferente en ambos. Así, se ha demostrado que la presencia de Bacteroides dorei en niños predispuestos genéticamente a padecer diabetes mellitus tipo 1 puede ser útil para predecir el desarrollo de la enfermedad47. También se ha descrito una menor presencia de clostridios y de bifidobacterias, con mayor presencia de lactobacilos en niños con diabetes tipo 1, con el hallazgo interesante de que la abundancia de bacterias implicadas en el mantenimiento de la integridad de la pared intestinal era menor en comparación con los controles sanos48. Esto tiene una enorme relevancia científica, dado que se ha demostrado que el aumento de la abundancia de bifidobacterias en el intestino de ratones se acompaña de un efecto antiinflamatorio, a través de la producción de péptido similar al glucagón tipo 2, con reducción de la permeabilidad intestinal49.
Principales mecanismos relacionados con la disbiosis de pacientes con diabetes
| Disbiosis | Mecanismos |
|---|---|
| Bifidobacterias | Resistencia a la insulina |
| Bacteroides dorei | Marcadores proinflamatorios |
| Firmicutes respecto a Bacteroidetes | LPS |
| Lactobacilos en niños | Permeabilidad intestinal |
| Akkermansia muciniphila | Butirato |
Con respecto a la diabetes tipo 2, se ha observado una disbiosis con un aumento del filo Firmicutes con descenso de Bacteroidetes. Es necesario resaltar que la funcionalidad de las bacterias es crítica en su relación con la presencia de diabetes, al margen de su filo o familia de pertenencia, como antes comentamos. Este es el caso de las denominadas Roseburia y Faecalibacterium prausnitzii, que producen butirato y su abundancia es menor en la microbiota de pacientes diabéticos tipo 2, mientras que se incrementan otras clostridiales que no producen butirato. Dado que el butirato es capaz de aumentar la sensibilidad a la insulina, la presencia o no de este tipo de bacterias puede tener importancia patogénica en el riesgo o gravedad de la alteración metabólica. Al mismo tiempo, resulta paradójico que las especies de clostridiales no se correlacionen con indicadores de sobrepeso, como el IMC o el perímetro de cintura50.
Algunos de los mecanismos protectores de la microbiota sobre el desarrollo de la diabetes están relacionados con su acción antiinflamatoria y por su capacidad para modificar la resistencia a la insulina. Un ejemplo lo encontramos en la fermentación de los polisacáridos no digeribles de la fibra dietética, que lleva a la producción de AGCC, con un papel relevante en la acción de la insulina, la regulación de la ingesta energética y de la inflamación. De hecho, es conocido que los AGCC actúan regulando la secreción hormonal, activando los receptores de los adipocitos, suprimiendo la señalización de la insulina y evitando la acumulación de grasa. Incluso, como hemos comentado previamente, pueden aumentar la sensibilidad a la insulina estimulando la secreción de péptido similar al glucagón tipo 151,52. Por otra parte, la microbiota puede estar implicada en la inflamación propia de la diabetes, a través de la translocación intestinal de LPS y peptidoglicanos. Es conocido que los niveles plasmáticos de LPS en pacientes con diabetes tipo 2 están aumentados53, lo que podría desembocar en la activación de los TLR que inducen la trascripción de NF-κB, que regula los genes implicados en la síntesis de mediadores inflamatorios, incluyendo las citocinas TNF-α, IL-6 e IL-1β. Aunque estos estudios están basados fundamentalmente en animales de experimentación, puede que en la especie humana su papel sea también relevante.
Finalmente, otro ejemplo clínico de la conexión de microbiota-diabetes es el del trasplante de heces de donadores sanos a enfermos con síndrome metabólico, con una mejora de la sensibilidad a la insulina, reducción de peso, aumento de la diversidad microbiana, incremento de butirato fecal y aumento de la bacteria productora de butirato, Roseburia intestinalis, aunque los efectos fueron discretos y temporales54. Estos resultados nos llevan a pensar que tendríamos que buscar herramientas o alternativas terapéuticas que ayudaran a colonizar el colon con bacterias «saludables» desde el punto de vista metabólico, que se integren de forma estable y duradera en la comunidad microbiana del individuo.
Influencia de la microbiota sobre la hipertensiónLa Organización Mundial de la Salud califica la hipertensión como una de las causas más importantes de muerte prematura en todo el mundo. El control de la presión arterial en la práctica clínica habitual constituye todo un reto difícil de abordar, probablemente debido a que es el resultado de la alteración de múltiples sistemas como el cardiovascular, el nervioso, el renal y el endocrino. En este sentido, no hay duda de que la dieta juega un papel clave en su control. Por lo tanto, dado que en el intestino interacciona con la dieta, no parece inverosímil que la microbiota pueda participar en su regulación. Esta conexión ha quedado demostrada en trabajos llevados a cabo en animales de experimentación con hipertensión en los que se ha demostrado un aumento del cociente Firmicutes/Bacteroidetes y una disminución de la riqueza y diversidad bacteriana55. En un reciente metaanálisis se ha relacionado el consumo de probióticos con una reducción de la hipertensión, aunque el efecto obtenido fue muy modesto y especialmente más relevante cuando los pacientes partían de una presión arterial elevada56. A pesar de los efectos prometedores de los probióticos en este campo, el nivel de evidencia es bajo y son necesarias más evidencias que confirmen o no su utilidad.
Mucho falta aún por demostrar respecto a los posibles mecanismos implicados en explicar este nexo, aunque se postula que uno de ellos podría ser que el aumento de la actividad simpática en el intestino se asocia a una disbiosis, lo que conllevaría un aumento de la permeabilidad de la pared y, a su vez, a la puesta en marcha de mecanismos inflamatorios que contribuyen al desarrollo de hipertensión57,58. Se necesitarán ulteriores estudios para confirmar la relevancia de estos hechos.
Influencia de la microbiota sobre el metabolismo lipídicoAl igual que con el resto de los factores de riesgo cardiovascular discutidos anteriormente, se ha demostrado que el microbioma del intestino influye en el metabolismo lipídico, en especial por su importancia en el metabolismo de los ácidos biliares y de su receptor X farnesoide, implicado en la producción de VLDL y en la protección de la esteatosis hepática59. No obstante, resulta peculiar esta teoría, ya que es conocido que los mismos receptores actúan en el intestino de manera contraria, es decir, favoreciendo la esteatosis hepática y la obesidad60. Nuestro grupo ha demostrado que en pacientes con sobrepeso y obesidad existen 66 taxones que explican el 29% de la variación interindividual en triglicéridos, el 33% en la de colesterol HDL y el 46% en la de colesterol LDL40. Aunque con menos influencia cuantitativamente, Fu et al. demostraron que la microbiota intestinal puede explicar hasta un 4,5% de las variaciones encontradas en el IMC, hasta el 6% en los triglicéridos y hasta un 4% en el colesterol HDL, independientemente de la edad, el género y los factores genéticos61.
La relación entre microbiota y metabolismo lipídico es muy compleja, existiendo varios mecanismos de interrelación que comentaremos someramente. Por una parte, la señalización de los TLR modula el metabolismo del colesterol62 y a través de dicho mecanismo la microbiota intestinal puede ser un factor importante para modificar los niveles de lípidos plasmáticos63. Asimismo, los receptores nucleares hepáticos X controlan el metabolismo del colesterol y se activan mediante oxiesteroles endógenos. De este modo, se ha demostrado que los agonistas de receptores nucleares hepáticos X aumentan la expresión de los transportadores ABCA1 y ABCG1, lo que da como resultado un incremento del transporte reverso de colesterol64. Además, TLR4 inhibe la activación de los receptores nucleares hepáticos X y, por tanto, presenta una gran influencia en el transporte inverso de colesterol, así como en la inflamación y en el metabolismo de la glucosa62. Otro mecanismo potencial sería a través de moléculas como el ácido acético, el ácido butírico, el ácido propiónico y el ácido valérico, metabolitos con una acción local, que sirven como fuente de energía pero que también pueden ser absorbidos y estimular la gluconeogénesis19 o influir en la sensibilidad a la insulina65. Finalmente, se ha demostrado que altos niveles de TMAO modifican el metabolismo lipídico a través de cambios en TRC, a través del metabolismo de esteroles y modificando la calidad y la cantidad de los ácidos biliares66,67.
ConclusionesLa microbiota intestinal es un determinante importante de muchos mecanismos relacionados con la arteriosclerosis, aunque la mayoría de los estudios tienen un carácter experimental y queda por demostrar aún su dimensión real en la enfermedad humana. Estos mecanismos son vehiculizados a través de la producción de factores proaterogénicos; a través de los ácidos grasos de cadena corta que participan en la regulación de la acción de la insulina, la respuesta inmune y el metabolismo energético; a través de los ácidos biliares, claves en el metabolismo del colesterol; o bien modulando la permeabilidad de la barrera intestinal y, por tanto, la absorción de componentes de la pared celular bacteriana, principalmente los lipopolisacáridos y los peptidoglicanos, que resultan esenciales en la respuesta inflamatoria y en el metabolismo de la glucosa. Ahora es el momento de consolidar esta evidencia profundizando en dichos mecanismos con la idea de identificar a los subgrupos de riesgo y aplicar medidas preventivas o intervenciones personalizadas y adecuadas.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
AgradecimientosQueremos agradecer a D. Esteban Tarradas Merino, del Servicio de Imagen de Apoyo a la Docencia e Investigación (SIADI) de la Facultad de Medicina y Enfermería de la Universidad de Córdoba, por su colaboración en el diseño gráfico de las imágenes.