Los tumores del estroma gastrointestinal (GIST) son los tumores mesenquimales más frecuentes en el tracto digestivo. La mayoría poseen una mutación característica con ganancia de función del gen c-KIT, que codifica el receptor KIT (CD117)1. La disponibilidad de un inhibidor para dicho receptor, mesilato de imatinib, tiene un papel importante en el tratamiento quimioterápico de los GIST de alto riesgo, metastásicos y/o irresecables2–4. Para el diagnóstico anatomopatológico de los GIST se realizan tinciones inmunohistoquímicas. El 95% expresan CD117 y DOG1, además de otros marcadores como CD34 (60-70%), actina de músculo liso (15-60%), proteína S100 (10%) y desmina (rara vez)5. Sin embargo, aunque la expresión de CD117, ante una alta sospecha, es por lo general diagnóstico de GIST, existen otros tumores que se parecen morfológicamente y expresan CD117, entre los que se encuentra el sarcoma de Ewing6,7.
Presentamos el caso de un varón de 35 años, sin antecedentes de interés, que ingresa para estudio por edema en el miembro inferior derecho y masa abdominal palpable. En la tomografía computarizada se evidencia una gran masa pélvica de 20×13×18cm con sospecha de tumor mesenquimal. La biopsia percutánea muestra una proliferación mesenquimal formada por células de hábito epitelioide con leve pleomorfismo nuclear y un pequeño nucléolo, que se disponen en un patrón difuso. Se observan áreas de necrosis que ocupan un 50% del volumen del tejido tumoral biopsiado. El estudio inmunohistoquímico muestra expresión por las células neoplásicas de CD117 (KIT) y negatividad para DOG1, CD34, actina de músculo liso, desmina, proteína S100, citoqueratinas y EMA. En función de la morfología, la expresión inmunohistoquímica de KIT y la localización intraabdominal se interpreta como un GIST epitelioide, iniciándose, por tanto, tratamiento neoadyuvante con imatinib.
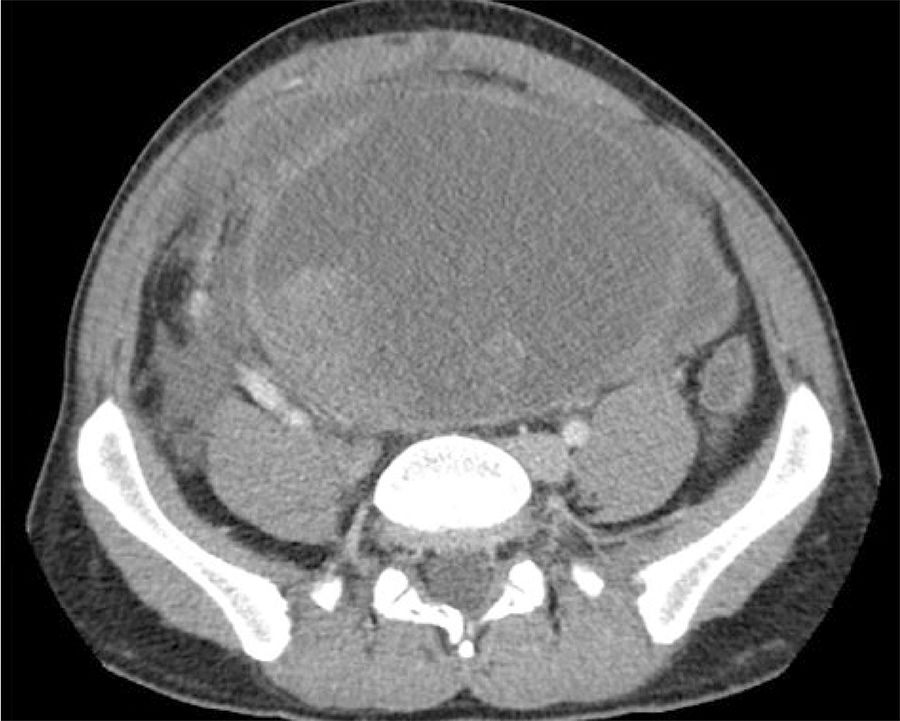
Tras un mes de tratamiento, y sin respuesta clínica, acude a urgencias por dolor intenso y continuo en la fosa iliaca derecha y estreñimiento pertinaz. A la exploración se evidencia una gran masa abdominal palpable, con distensión, dolor y signos de irritación peritoneal. Se realiza tomografía computarizada donde se observa la gran masa sólido-quística sin cambios significativos, sin poder descartar sangrado tumoral, con líquido libre, hidronefrosis grado ii derecha por atrapamiento ureteral (fig. 1) y deterioro secundario de la función renal.
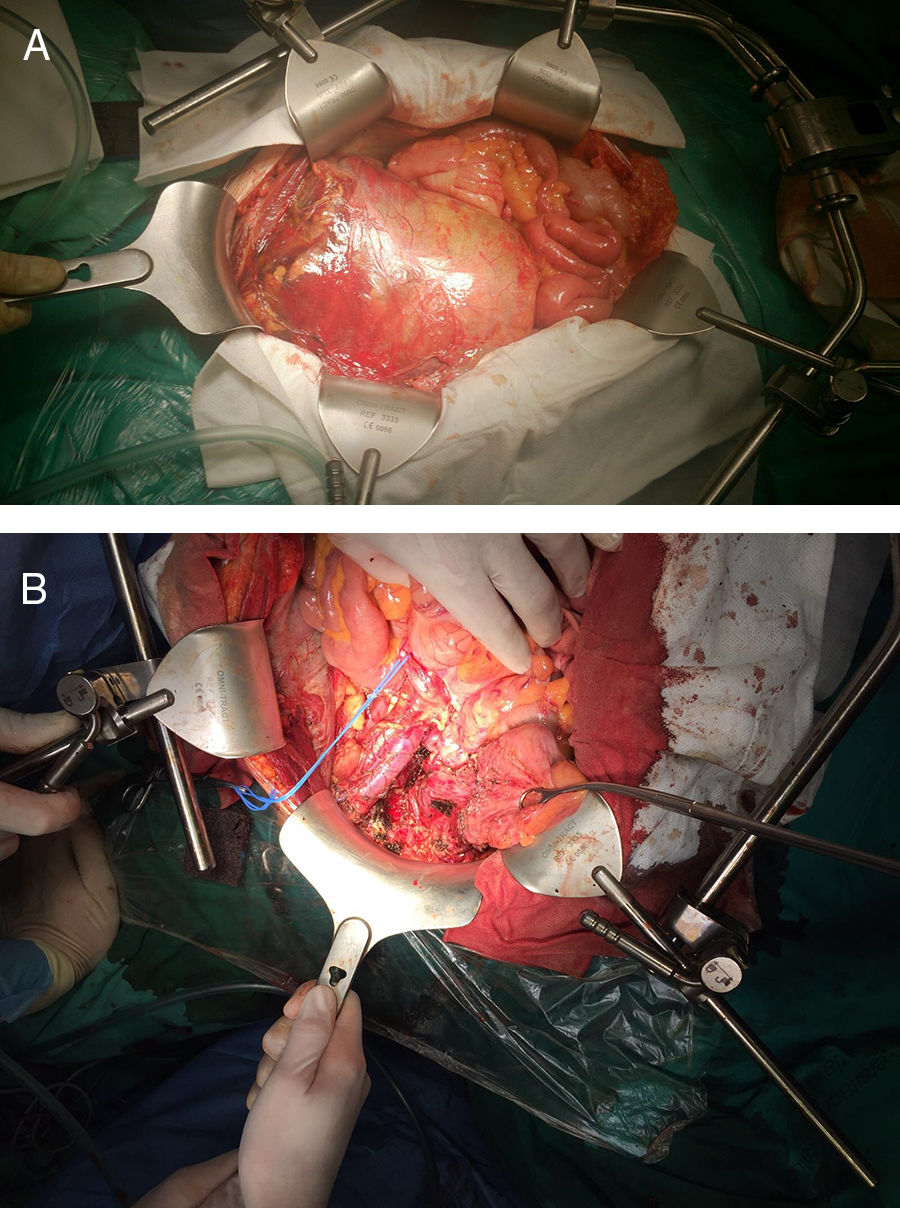
Se realiza cirugía urgente, hallando una masa en localización preperitoneal, adherida a la vena y a la arteria iliaca externa derecha y al uréter con desplazamiento de la vejiga a la fosa iliaca izquierda (fig. 2A). Se reseca el tumor, disecando hasta el orificio obturatriz derecho y la espina iliaca derecha, con sección muscular parcial del músculo pectíneo y apertura del tumor a dicho nivel. Se amplía posteriormente el margen hasta el periostio (fig. 2B). Fue dado de alta al octavo día postoperatorio. Como complicación presentó una neuropatía del nervio obturador derecho posquirúrgica (Clavien ii). En el estudio histopatológico se identifican, además de las áreas de células epiteloides halladas en la biopsia, zonas minoritarias de células pequeñas redondas, así como focos de células claras y células de morfología rabdoide. Se amplía el estudio inmunohistoquímico que, junto a la ya conocida expresión de KIT, muestra una positividad membranosa, fuerte y difusa de CD99. Se realiza estudio de hibridación in situ con fluorescencia utilizando una sonda break apart que evidencia traslocación de EWSR1, y amplificación mediante RT-PCR y secuenciación Sanger que evidencia una fusión EWSR1 (exón 7)-FLI1 (exón 6). El estudio mediante amplificación por PCR de los exones 9, 11, 13 y 17 del gen C-KIT y de los exones 12, 14 y 18 del gen PDGFRA con secuenciación Sanger no detectó mutaciones en estos genes. En función de la histopatología, el inmunofenotipo y los hallazgos moleculares, el diagnóstico patológico final fue sarcoma de Ewing atípico (pT4 L0 V0 R1). La citología del líquido ascítico fue negativa para células malignas.
El paciente ha completado, dentro de un ensayo clínico, 15 ciclos de tratamiento quimioterápico sin evidencia de recidiva a los 15 meses de la intervención.
Una de las teorías aceptadas acerca del origen de los Tumores de la Familia del Sarcoma de Ewing (TFSE) es que surgen de células madre mesenquimales, presentes en el organismo y con capacidad de transformarse en distintos tipos de tejido. Los TFSE son neoplasias indiferenciadas en grado variable y con expresión fenotípica múltiple, compartiendo todas ellas una alteración génica en el gen EWSR1 (cromosoma 22q12) y la tinción inmunohistoquímica positiva para CD99 en la mayor parte de los casos. En el 65% también puede ser positivos para CD117, al igual que los GIST8,9.
Los TFSE son muy poco frecuentes, tienen una incidencia de 3 casos por cada millón de personas y el 90% se presentan entre los 5 y los 25 años. Dentro de los TFSE se encuentra el sarcoma de Ewing extraesquelético, menos frecuente que el óseo, con una prevalencia del 15-20% de todos los sarcomas de Ewing. Su localización más frecuente es la región paravertebral (32%) y los miembros inferiores (26%), y con menor frecuencia la pared torácica (18%), el retroperitoneo (11%), como en nuestro caso, la pelvis (11%) y los miembros superiores (3%). Su forma de presentación es una masa de partes blandas que no afecta a la médula ósea en las imágenes de resonancia magnética10.
La histopatología del tumor, su ubicación y el estudio inmunohistoquímico y molecular son fundamentales para hacer un diagnóstico correcto. Sin embargo, el caso clínico y las pruebas de imagen también desempeñan un papel fundamental en la orientación diagnóstica.
En el caso presentado la morfología epitelioide de las células, la expresión inmunohistoquímica de CD117 y el tratarse de un varón de 35 años con una masa intraabdominal asintomática hizo orientar el diagnóstico a GIST, lo que condicionaba iniciar tratamiento con imatinib para reducir la masa tumoral y poder plantear una resección quirúrgica R0. La falta de respuesta clínica y el hallazgo intraoperatorio de adherencia a la rama isquiopubiana derecha se explican tras el diagnóstico definitivo de sarcoma de Ewing atípico.
Como conclusión, y a tener en consideración en casos futuros, sería adecuado incluir el sarcoma de Ewing atípico de localización intraabdominal entre los diagnósticos diferenciales de los GIST para poder indicar el tratamiento correcto desde el inicio.
El caso clínico fue presentado como póster en el xxi Congreso Nacional de Cirugía celebrado en Málaga del 18 al 20 de octubre de 2017.