El objetivo del estudio es presentar nuestra experiencia en el tratamiento de la incontinencia fecal grave mediante neuromodulación sacra tras los primeros 10 años de utilización de la técnica.
Material y métodosCuarenta y nueve pacientes con incontinencia fecal grave se trataron con neuromodulación sacra durante el periodo 2001-2011. Se practicó manometría anorrectal, ecografía endoanal y estudio de latencia pudenda. Se evaluaron diario evacuatorio, escalas de gravedad y calidad de vida de incontinencia fecal en el preoperatorio y al final del seguimiento.
ResultadosUn tercio de los pacientes presentó morbilidad, la mayoría leve. Se explantaron 4 dispositivos definitivos. Con una mediana de seguimiento de 37 meses, la gravedad de la incontinencia fecal, urgencia e incontinencia mejoraron significativamente al cierre del estudio. El subgrupo de pacientes con seguimiento mayor de 5 años mejoró significativamente la gravedad de la incontinencia pero no los parámetros del diario evacuatorio. No hubo diferencias significativas en la calidad de vida. Los datos descriptivos en pacientes con defectos esfinterianos no muestran peores resultados que en la integridad esfinteriana.
ConclusionesLa neuromodulación sacra es una técnica segura para la incontinencia fecal grave con buenos resultados funcionales a medio plazo. A largo plazo, existe también mejoría de la gravedad de la misma pero son necesarios estudios con mayor muestra para objetivar si otros parámetros clínicos y la calidad de vida avalan este dato. Los resultados preliminares en pacientes con defectos esfinterianos sugieren que la técnica puede ser eficaz en este grupo pero futuros estudios deberán confirmar estos hallazgos.
The objective of this study is to report our experience with sacral nerve stimulation for the treatment of severe faecal incontinence after the first 10 years with this technique.
Material and methodsBetween 2001 and 2011, 49 patients with severe faecal incontinence underwent sacral nerve stimulation. Anorectal manometry, endoanal ultrasound and pudendal nerve latency were performed. Bowel habit diary, severity of faecal incontinence and quality of life scales were evaluated preoperatively and at the end of follow-up.
ResultsMorbidity occurred in a third of patients, mostly minor. Four definitive devices were explanted. With a median follow-up of 37 months, severity of faecal incontinence, urge and incontinence episodes significantly improved at the end of follow-up. Patients’ subgroup with major follow-up of 5 years significantly improved the severity of faecal incontinence but not the parameters of the bowel habit diary. Quality of life showed no significant improvement. Descriptive data in patients with sphincter defects did not show worse results than with sphincter integrity.
ConclusionSacral nerve stimulation is a safe technique for severe faecal incontinence with good functional medium-term results. In the long term, severity of the faecal incontinence also improves but studies with larger sample are necessary to show if other clinical parameters and the quality of life support this information. Preliminary results in patients with sphincter defects suggest that this technique could be effective in this group but future studies will have to confirm these findings.
El tratamiento de elección de la incontinencia fecal (IF) por defecto esfinteriano ha sido clásicamente la esfinteroplastia del esfínter anal externo (EAE)1. Asimismo, hasta hace unos años las alternativas para el manejo de la IF grave eran fundamentalmente la graciloplastia dinámica (GD), el implante de un esfínter anal artificial (EAA) o el estoma definitivo2. Actualmente la neuromodulación sacra (NMS) se considera una nueva opción. Inicialmente se realizó solo en pacientes con integridad esfinteriana pero sus indicaciones se han ampliado con el tiempo3.
El objetivo de este estudio es presentar nuestra experiencia en el tratamiento de la IF grave mediante NMS tras 10 años de utilización de la técnica.
Material y métodoEstudio prospectivo transversal en 49 pacientes con IF grave (43 mujeres y 6 hombres) con una mediana de edad de 63 años (rango [r]: 22-80) tratados mediante NMS en nuestro centro entre febrero de 2001 y marzo de 2011.
Los criterios iniciales de inclusión fueron: IF grave (urgencia evacuatoria, incontinencia de urgencia o incontinencia pasiva/ensuciamiento, al menos una vez por semana durante 2 meses consecutivos asociados a afectación social), EAE intacto mediante ecografía endoanal (EEA) y existencia de conducción nerviosa en al menos una rama pudenda mediante electroestimulación. Desde el año 2006 se incluyó a pacientes con defectos de ambos esfínteres anales sin limitación en el tamaño de los mismos.
Se consideraron criterios de exclusión: cardiopatía que requiriera marcapasos o desfibrilador, embarazo, prolapso rectal y enfermedades que cursaran con diarrea.
Para la inclusión en el estudio se evaluó preoperatoriamente en todos los pacientes la función intestinal con diario evacuatorio de 21 días, la gravedad de la IF y la calidad de vida (CV) con las escalas de Jorge y Wexne4 y FIQLS5, y se realizó estudio funcional mediante manometría anorrectal, EEA (B & K Medical, Gentofte, Dinamarca) y estudio de latencia motora terminal de nervios pudendos.
Durante la evaluación del sistema nervioso periférico (ESNP) se cumplimentó el diario evacuatorio (21 días) para seleccionar a aquellos pacientes subsidiarios de implante definitivo. Al cierre del estudio se evaluaron la función intestinal, la gravedad de la IF y la CV.
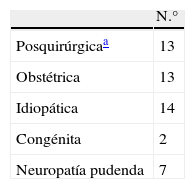
La etilogía de la IF se refleja en la tabla 1. Todos los pacientes se manejaron con tratamiento médico y en 31 casos (63%) se realizó biofeedback, sin mejoría. Los pacientes fueron informados y se obtuvo su consentimiento para realizar la técnica quirúrgica y las diferentes exploraciones. La realización de este estudio fue aprobada por el Comité Ético de Investigación Clínica de nuestro hospital.
Etiología de la incontinencia fecal
| N.° | |
| Posquirúrgicaa | 13 |
| Obstétrica | 13 |
| Idiopática | 14 |
| Congénita | 2 |
| Neuropatía pudenda | 7 |
Hemorroidectomía (2), hemorroidectomía y esfinterotomía interna (2), hemorroidectomía y fistulotomía (1), esfinterotomía interna (1), anopexia grapada (1), resección anterior de recto (4), colectomía derecha (1) y resección transanal de adenoma de recto (1). Atresia anal (1), espina bífida y mielomeningocele (1).
La NMS consta de 2 etapas realizadas de forma ambulatoria bajo anestesia local: la ESNP y la estimulación permanente.
Durante la primera se selecciona la raíz sacra S2, S3 o S4 que presente mejor respuesta sensitiva o motora con el menor umbral de estimulación. Posteriormente, se implanta un electrodo conectado a un generador externo (parámetros de estimulación: anchura de pulso 210 μs, frecuencia 25 Hz y amplitud variable entre 1 y 10 V). Durante los 2 primeros años utilizamos para esta fase un electrodo monopolar de implantación percutánea (Medtronic Interstim® 3065, Medtronic Inc, Minneapolis, EE. UU.) y desde el año 2003 se sustituyó por un electrodo tetrapolar con autoanclaje (Medtronic Interstim® 3889, Medtronic Inc, Minneapolis, EE. UU.). El paciente retorna a sus actividades para rellenar el diario evacuatorio. La puntuación final del mismo se calcula mediante la suma del número de episodios de IF o urgencia, indistintamente. Si presenta mejoría de su función evacuatoria definida como una disminución mínima de un 50% en la puntuación del diario respecto al basal se propone la estimulación permanente3.
En el implante definitivo el generador de impulsos se aloja en un bolsillo subcutáneo en el glúteo homolateral y se activa. Durante el seguimiento pueden variarse los parámetros de estimulación mediante telemetría. Los criterios de mejoría clínica durante el seguimiento son los mismos definidos anteriormente para la ESNP.
Método estadísticoLos datos se han procesado con el programa informático SPSS® 13.0 (SPSS Inc. Chicago, Illinois, EE. UU.).
Los resultados se expresan como media, desviación estándar (DE) y rango (mínimo y máximo) o mediana y rango intercuartil (RIQ). Se ha utilizado la prueba de Kolmogorov-Smirnov para constatar la bondad de ajuste de las muestras a una distribución normal. El análisis estadístico se ha realizado con la prueba t de Student de comparación de 2 medias para grupos apareados o la prueba t de Wilcoxon para las muestras no paramétricas, con un nivel de significación de 0,05.
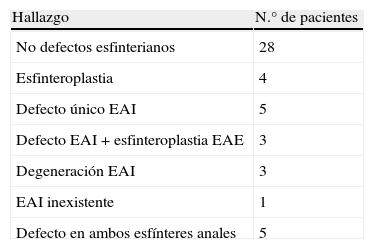
ResultadosLa duración media de los síntomas fue de 90 meses (r: 3-492). En 7 casos la causa de la IF fue la neuropatía pudenda y otros 13 pacientes (26%) con diferentes etiologías la asociaban. Trece pacientes presentaban incontinencia urinaria. Los hallazgos de la EEA preoperatoria se describen en la tabla 2.
Hallazgos de EEA preoperatoria
| Hallazgo | N.° de pacientes |
| No defectos esfinterianos | 28 |
| Esfinteroplastia | 4 |
| Defecto único EAI | 5 |
| Defecto EAI+esfinteroplastia EAE | 3 |
| Degeneración EAI | 3 |
| EAI inexistente | 1 |
| Defecto en ambos esfínteres anales | 5 |
EAE: esfínter anal externo; EAI: esfínter anal interno; EEA: ecografía endoanal.
Quince pacientes (31%) presentaron morbilidad. En la fase de ESNP existió una infección (traumatismo) que obligó a retirarlo y a una nueva estimulación. En la fase de estimulación permanente, la morbilidad consistió en una sección de electrodo durante el implante definitivo que llevó a realizar una segunda prueba, 3 hematomas, dolor o parestesias en 14 casos (28,5%) (región anal: 3, extremidades: 4 y localización del generador: 7) que en 10 casos se resolvieron con analgesia o disminuyendo la amplitud del estímulo, en 3 obligaron al explante y en uno a la reubicación del generador con mejoría; hubo un caso de estreñimiento tratado con enemas.
Resultado funcionalUn total de 33 pacientes (67%) presentaron mejoría clínica mayor del 50% durante la fase de ESNP y recibieron un implante definitivo. De estos, 17 (51%) alcanzaron una continencia completa (CC) durante la ESNP. En otros 3 con mejoría insuficiente se indicó una nueva ESNP: en uno se estimuló otra raíz y en otro se realizaron 2 nuevas pruebas (diferente raíz y bilateral, respectivamente) sin mejoría clínica en ningún caso. El tercero rehusó la reintervención. Un último paciente mostró una respuesta dudosa, mejorando la urgencia pero manteniendo los escapes, por lo que se mantuvo la ESNP 2 semanas más con mejoría e implante definitivo.
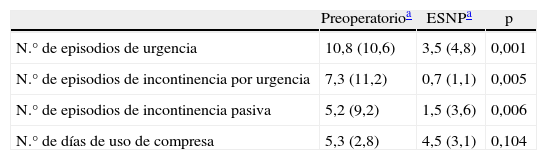
Tras el implante temporal, disminuyeron de forma significativa el número de episodios semanales de urgencia evacuatoria, los escapes por urgencia y los episodios de IF pasiva respecto a la situación basal (tabla 3).
Variación de diario evacuatorio semanal
| Preoperatorioa | ESNPa | p | |
| N.° de episodios de urgencia | 10,8 (10,6) | 3,5 (4,8) | 0,001 |
| N.° de episodios de incontinencia por urgencia | 7,3 (11,2) | 0,7 (1,1) | 0,005 |
| N.° de episodios de incontinencia pasiva | 5,2 (9,2) | 1,5 (3,6) | 0,006 |
| N.° de días de uso de compresa | 5,3 (2,8) | 4,5 (3,1) | 0,104 |
El implante definitivo se realizó en S3 en 26 pacientes, S4 en 6 y S2 en uno. La mediana (RIQ) de seguimiento tras el implante definitivo fue de 37 (52) meses (r: 6-118).
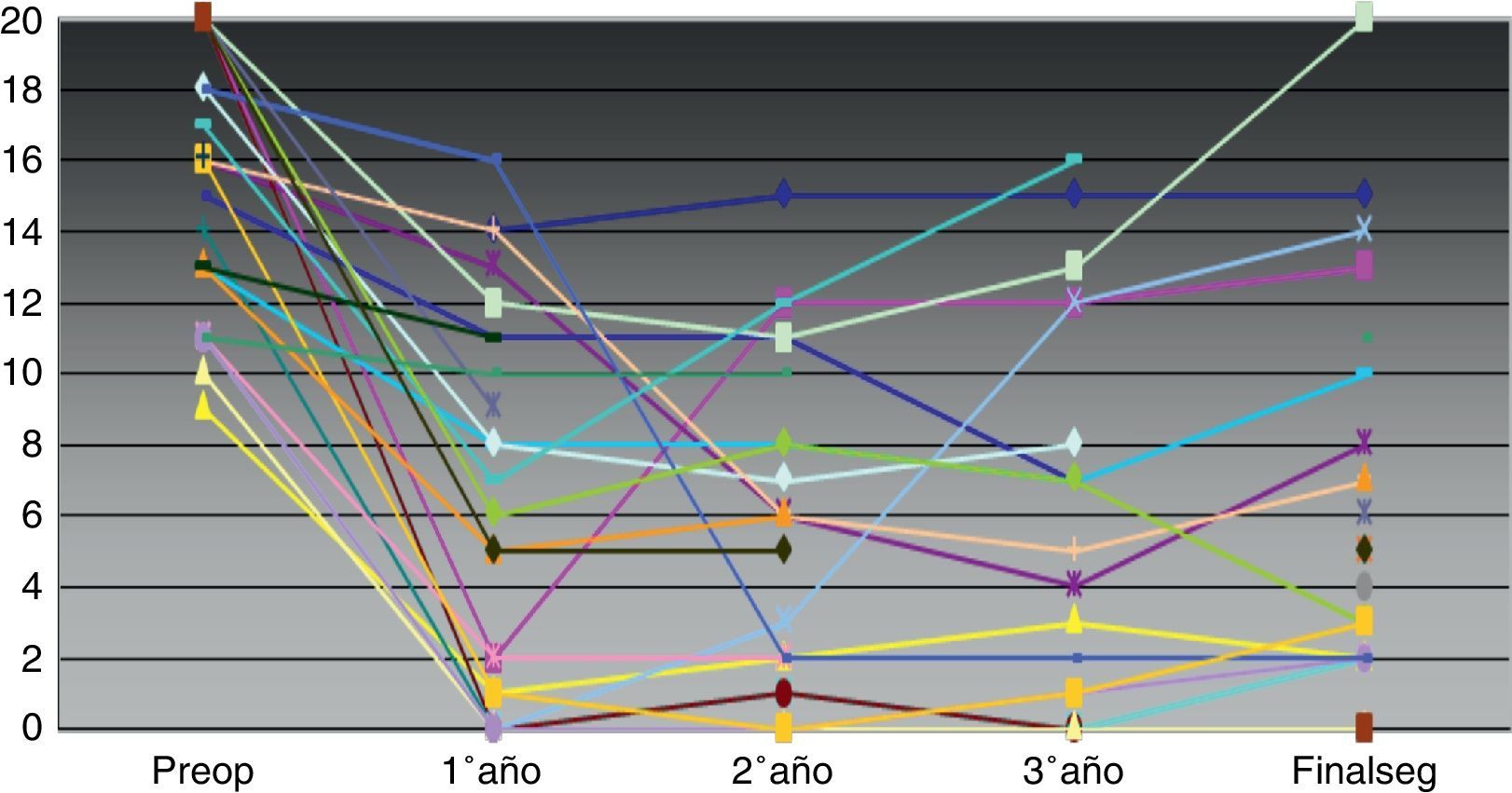
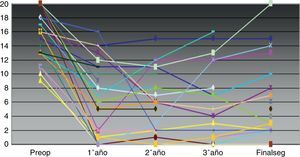
Globalmente, la gravedad de la IF mejoró desde una puntuación media preoperatoria (DE) de 16,04 (3,9) a 5,6 (5,4) (p<0,001) al final del seguimiento. Existió mejoría significativa entre el número de episodios de urgencia evacuatoria, escapes por urgencia e IF pasiva preoperatorio y al final del seguimiento, pero el número de días semanales con utilización de compresa no varió (tabla 3). La variación individual en la escala de gravedad a lo largo del seguimiento se refleja en la figura 1.
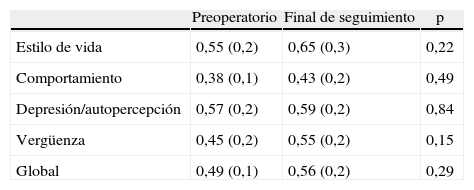
La escala de CV fue cumplimentada al cierre del estudio por 13 de los 29 pacientes que mantenían el implante definitivo y, aunque existió mejoría en todos los parámetros, no se alcanzó la significación estadística respecto al preoperatorio (tabla 4).
Variación en la calidad de vida
| Preoperatorio | Final de seguimiento | p | |
| Estilo de vida | 0,55 (0,2) | 0,65 (0,3) | 0,22 |
| Comportamiento | 0,38 (0,1) | 0,43 (0,2) | 0,49 |
| Depresión/autopercepción | 0,57 (0,2) | 0,59 (0,2) | 0,84 |
| Vergüenza | 0,45 (0,2) | 0,55 (0,2) | 0,15 |
| Global | 0,49 (0,1) | 0,56 (0,2) | 0,29 |
T de Student preoperatorio-final de seguimiento (n=13).
En el subgrupo de pacientes con seguimiento mayor de 5 años (n=8; mediana [RIQ] de seguimiento 75 [27,5] meses; r: 70-118), la gravedad de la IF mejoró desde una puntuación media preoperatoria (DE) de 15,14 (3,8) a 6,7 (5,7) (p=0,025) al final del seguimiento. No hubo mejoría significativa en ninguno de los parámetros del diario evacuatorio ni en la CV entre el periodo preoperatorio y el cierre del estudio.
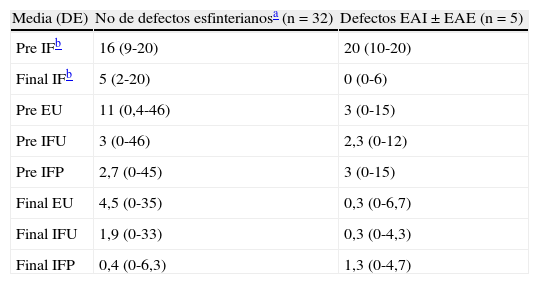
Los datos del subgrupo de pacientes con defectos esfinterianos (n = 5) se detallan en la tabla 5. De forma descriptiva se observa que el resultado clínico no es peor que el mostrado por el grupo de pacientes con integridad esfinteriana.
Descripción de datos en grupos de pacientes con/sin defectos esfinterianos
| Media (DE) | No de defectos esfinterianosa (n=32) | Defectos EAI±EAE (n=5) |
| Pre IFb | 16 (9-20) | 20 (10-20) |
| Final IFb | 5 (2-20) | 0 (0-6) |
| Pre EU | 11 (0,4-46) | 3 (0-15) |
| Pre IFU | 3 (0-46) | 2,3 (0-12) |
| Pre IFP | 2,7 (0-45) | 3 (0-15) |
| Final EU | 4,5 (0-35) | 0,3 (0-6,7) |
| Final IFU | 1,9 (0-33) | 0,3 (0-4,3) |
| Final IFP | 0,4 (0-6,3) | 1,3 (0-4,7) |
EAE: esfínter anal externo; EAI: esfínter anal interno; EU: episodios semanales urgencia; IF: incontinencia fecal; IFP: episodios semanales IF pasiva; IFU: episodios semanales IF por urgencia; Pre: preoperatorio.
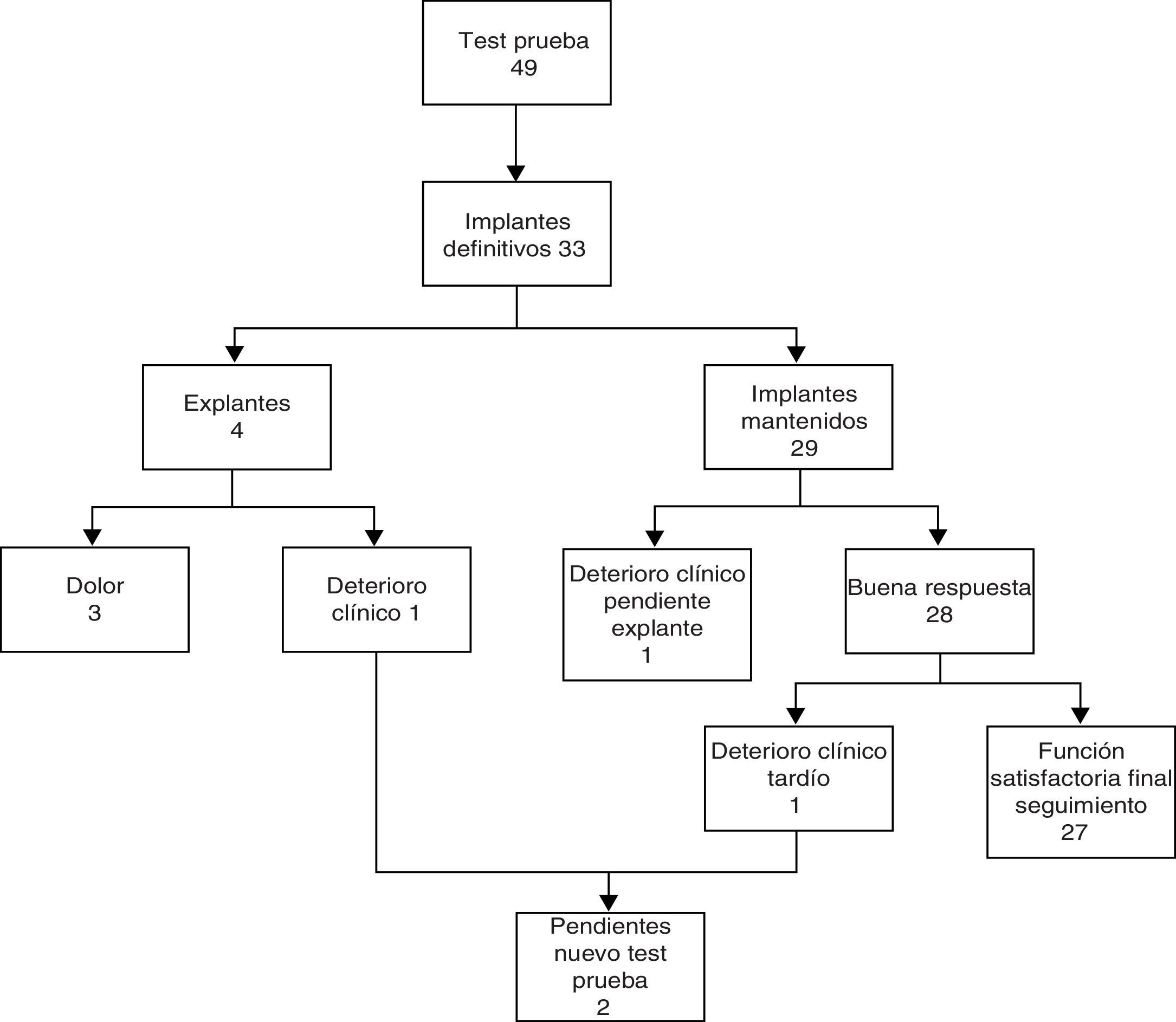
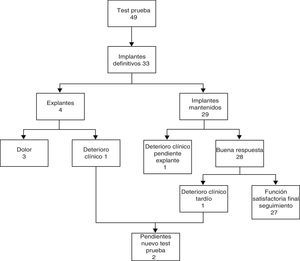
En 4 de los 33 implantes definitivos (12%) se precisó explante (3 por dolor y otro por deterioro clínico). Otro paciente está pendiente de explante por deterioro clínico y ha rehusado nueva estimulación. En 2 casos con deterioro clínico tardío (el ya explantado y otro pendiente) se realizará una nueva estimulación (fig. 2). Siete pacientes con buen resultado clínico necesitaron el recambio del generador (vida media: 56 meses) por agotamiento de la batería. Veinte de los 33 implantes definitivos (61%) necesitaron reprogramar los parámetros de estimulación (media: 3,5 reprogramaciones por paciente). El ajuste más frecuente ha sido la variación de la amplitud del estímulo con un rango entre 0,8 y 6,4 V para mantener la continencia.
DiscusiónLa NMS es una técnica sencilla y segura. En nuestro estudio, ocurrió morbilidad en un tercio de los pacientes, la mayoría leve y sin repercusión sobre el implante. La infección se produjo en un paciente (2%) lo que concuerda con otras series6,7, y no comprometió el implante definitivo. Como Michelsen et al.8 destacamos que las alternativas disponibles para la IF grave hasta la NMS han sido la GD y el EAA, ambas con tasas de infección altas y que pueden ocasionar el fallo definitivo de la técnica9,10. En un implante definitivo se produjo una sección del electrodo. Esto nos ha servido para extremar el cuidado durante el procedimiento que, aunque técnicamente sencillo, tiene unos costes económicos elevados11.
El fallo definitivo de la técnica por morbilidad ocurrió en 3 pacientes (9%), en los que el dolor o las parestesias obligaron al explante. En el resto, el dolor se controló con analgesia convencional y, para tratar las parestesias, disminuímos la amplitud del estímulo. Como Brouwer et al.3, desde hace un año implantamos el generador más alto y lateral en el glúteo para evitar las molestias con la sedestación por una ubicación más medial y baja.
El 67% de pacientes presentaron una respuesta satisfactoria durante la ESNP y recibieron el implante definitivo, lo que concuerda con la literatura12,13. Durante la ESNP el 50% de los pacientes alcanzó la CC.
Al cierre del estudio tras el implante definitivo, el global de la serie (mediana de seguimiento: 37 meses) presentó una mejoría significativa en la gravedad de la IF y en el número de episodios de urgencia y escapes respecto al preoperatorio y únicamente 5 pacientes presentaban CC (17%), y otros 7 (24%) con solo algún escape ocasional. Esto supone un 41% de los 29 pacientes que mantenían el implante al final del seguimiento. En este momento, el subgrupo de pacientes con seguimiento mayor de 5 años mantuvo la mejoría significativa en la gravedad de la IF pero no en los parámetros del diario. Pensamos que el no hallar diferencias significativas en este último se debe a la escasa muestra con seguimiento mayor de 5 años (n=8) aunque también puede que el resultado clínico, aun siendo bueno, se deteriore relativamente con el tiempo. Otra explicación sería que el deseo de ser implantados y obtener una buena respuesta lleve a los pacientes, durante la ESNP y los primeros años tras el implante definitivo, a minimizar escapes que no reflejan en el diario. Con el paso del tiempo podrían tornarse más exigentes y considerar como escapes lo que anteriormente habrían obviado. Ello explicaría también las diferencias respecto a las cifras de CC alcanzadas en las diferentes fases del estudio.
No hemos confirmado la disminución en la utilización de compresa que obtienen algunas series14,15. Una explicación sería que su uso responda a un hábito adquirido o al temor a sufrir escapes y que no refleje una situación actual, sino la necesidad de seguridad. Además, muchos pacientes asocian incontinencia urinaria y no diferencian por qué motivo sigue utilizándola.
En los 13 pacientes que respondieron la encuesta de CV al cierre del estudio no hallamos mejoría significativa. Esto no concuerda con otras series16,17 y puede deberse a la baja cumplimentación al final del seguimiento. La encuesta fue entregada para cumplimentarse y remitirse por correo. Cuando no fue recibida, enviamos una segunda encuesta. Aun así, solo 13 pacientes con implante definitivo (44%) respondieron al requerimiento. Posteriores estudios con un mayor reclutamiento de pacientes confirmarán si nuestros resultados respecto a la CV son o no reales.
En nuestro estudio, un 61% de los pacientes necesitó alguna reprogramación. Coincidimos con Govaert et al.18 en que estos deben ser informados y fijar un seguimiento para realizar los ajustes necesarios. Nosotros disponemos actualmente de un técnico de Medtronic que, regularmente, visita a nuestros pacientes para controlar los parámetros y realizar los cambios necesarios.
Las indicaciones para la NMS se han ido ampliado con el tiempo por diversos motivos. Es una técnica sin manipulación perianal, por lo que su realización no debe deteriorar la continencia preoperatoria. Además, las alternativas quirúrgicas (GD e implante de EAA) son más agresivas con morbilidad elevada y, en ocasiones grave19,20, lo que ha llevado a expandir las indicaciones de la NMS para obtener resultados que permitieran eludir estas otras cirugías. Por último, la NMS tiene su propio «proceso de selección de pacientes» (ESNP) y se ha ensayado en grupos con determinadas características. Cuando mostró buenos resultados, se realizaron implantes definitivos. Poco a poco, esas nuevas indicaciones son hoy una realidad.
Inicialmente, los criterios de exclusión para la NMS incluían las malformaciones congénitas anorrectales, la neuropatía pudenda grave, el síndrome de resección anterior tras proctectomía o los defectos esfinterianos21–24 pero actualmente ninguno lo es. En nuestra serie existen pacientes con todas estas características y, en concreto, existe un grupo con defectos esfinterianos. Debido a su reducido número no hemos podido realizar comparaciones y presentamos los datos de forma descriptiva pero destacamos que el resultado obtenido en este grupo no parece ser peor que el de pacientes con integridad esfinteriana.
Diversos estudios han realizado NMS en pacientes con defectos esfinterianos con buen resultado clínico3,25,26 sin diferencias respecto al de la esfinteroplastia27,28. Se ha publicado el deterioro de la continencia a largo plazo tras esfinteroplastia29 pero otros autores30 no han observado diferencias entre seguimientos mayores o menores de 5 años. Nuestro grupo tiene pendiente de publicación un estudio en el que, con una mediana de seguimiento de 110 meses tras esfinteroplastia, la gravedad de la IF no empeora significativamente respecto a seguimientos menores. A pesar de ello, la mayoría de los autores publica que la efectividad inicial de esta técnica se deteriora con el tiempo31–33.
Actualmente estamos iniciando un estudio aleatorizado en el que pacientes con defectos esfinterianos son asignados para realizar NMS vs. esfinteroplastia. Creemos que este estudio ayudará a obtener conclusiones respecto a estas 2 técnicas en la IF por defectos esfinterianos.
ConclusiónLa NMS es una técnica segura y con baja morbilidad. La mayoría de los pacientes con una estimulación de prueba satisfactoria alcanza un buen resultado funcional tras el implante definitivo aunque son necesarios estudios con mayor número de pacientes con seguimiento a largo plazo para confirmar si este es estable con el paso del tiempo. No hemos encontrado diferencias significativas en la CV de nuestros pacientes. La NMS podría considerarse una alternativa en la IF por defecto esfinteriano si los resultados preliminares obtenidos aquí se confirman en series con un mayor número de pacientes. Consideramos conveniente el diseño de estudios prospectivos aleatorizados que comparen la NMS con la esfinteroplastia para definir las indicaciones de la NMS y su lugar en el manejo de los diferentes tipos de IF.
FinanciaciónEl estudio no ha recibido ningún apoyo en forma de beca ni ha sido presentado previamente en ningún congreso.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.