Bevacizumab™ es un anticuerpo monoclonal que bloquea el factor de crecimiento del endotelio vascular. Este es un potente inductor de la angiogénesis y un factor crítico para la supervivencia de las células endoteliales. El proceso de neovascularización que soporta el crecimiento vascular tumoral es muy similar al implicado en la reparación de las heridas, por lo que una alteración del mismo podría alterar también las heridas quirúrgicas. La reducción de la densidad vascular, por formación de coágulos y apoptosis endotelial, alteraría la membrana basal de los pericitos1.
Se han descrito perforaciones intestinales hasta en el 2% de pacientes en tratamiento con Bevacizumab™, así como complicaciones anastomóticas2–4. Presentamos 2 pacientes con complicaciones anastomóticas tardías asociadas a este fármaco.
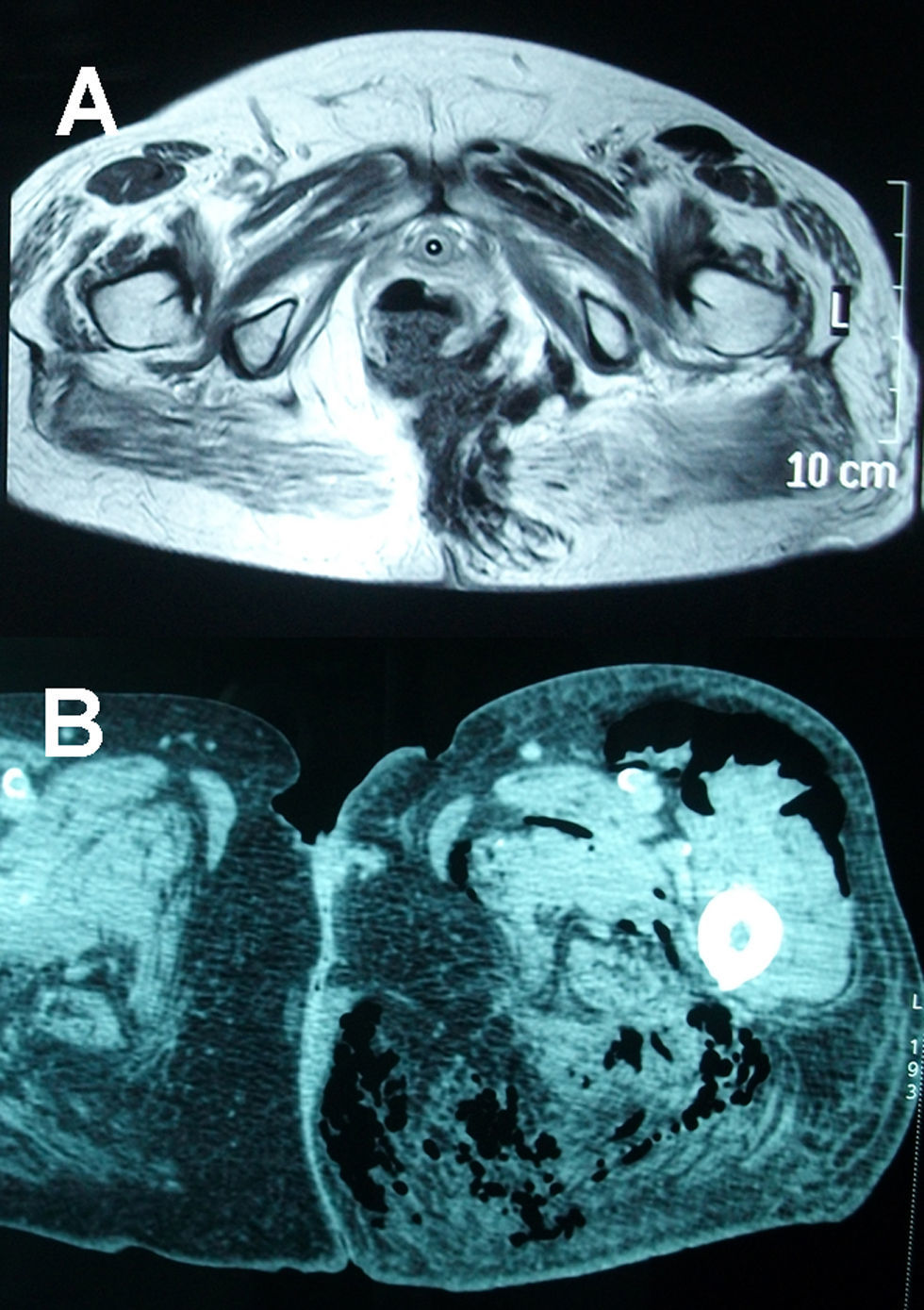
El primer paciente, varón de 71 años, fue diagnosticado de adenocarcinoma de recto, a 10cm del márgen anal. El estudio preoperatorio evidenció un T3 avanzado N1 M0. Se realizó neoadyuvancia con radioterapia (RT) de 45Gy en 5 semanas y quimioterapia (QT) con 5-FU al inicio y final del tratamiento. Tras 8 semanas se realizó una resección anterior baja asistida por laparoscopia, con exéresis mesorrectal total, reservorio colónico en J e ileostomía de protección (que se cerró previo enema opaco sin complicaciones). Al final del primer año el paciente presentó cuadro de urgencia rectal por los que se realizó una colonoscopia de control, apreciándose una ulceración en la línea de sutura con biopsias negativas para tumor. La RNM y la PET también dieron resultados negativos para recidiva neoplásica. Al tercer año de seguimiento se detectaron metástasis pulmonares. Se inició tratamiento con Bevacizumab™ y FOLFIRI y coinciendo con el tercer ciclo desarrolló un cuadro de dolor anal agudo, tenesmo y urgencia rectal. La exploración detectó un defecto de toda la cara posterior de la anastomosis a 5cm del márgen anal. La RNM (fig. 1A) mostró una colección perianastomótica. Se suspendió la QT y se iniciaron antibióticos con buena respuesta clínica local. Posteriormente el paciente desarrolló un síndrome de cava superior, con un ingreso prolongado y se trasladó a Cuidados Paliativos.
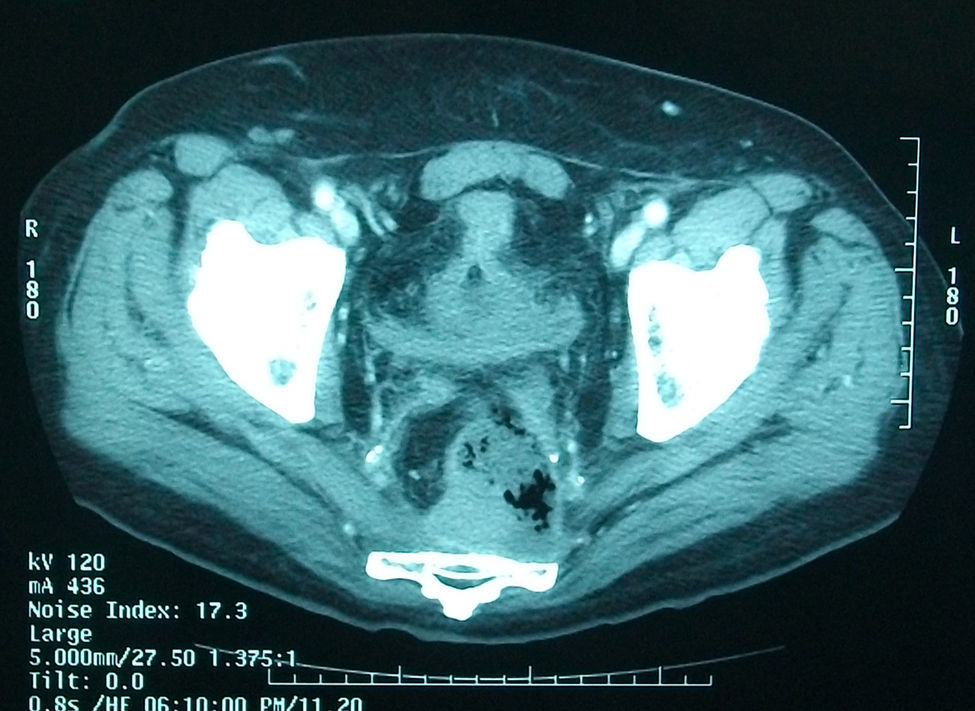
La segunda paciente, una mujer de 68 años diagnosticada de adenocarcinoma de recto a 7cm del márgen anal, con un estudio compatible con T3N1M1 (metástasis hepáticas). Se realizó RT de ciclo corto con 25Gy durante 5 días y tras un intervalo de 8 días una resección anterior baja asistida por laparoscopia, con exéresis mesorrectal total y anastomosis colorrectal LT. Al tercer mes se inició adyuvancia con Bevacizumab™ y FOLFIRI. Al completar el 4.° ciclo acude a urgencias por dolor anal y lumbosacro y empastamiento perineal y glúteo izquierdo. La RNM (fig. 2A) evidenció una disrupción anastomótica, de media circunferencia con absceso pélvico profundo y extensión a la raíz del muslo izquierdo. Se realizó una colostomía y desbridamientos locales con terapia Vacuum. La paciente fue dada de alta a Cuidados Paliativos.
Resultados de varios estudios en fase III han demostrado mejoría en la supervivencia de pacientes con enfermedad neoplásica colorrectal avanzada, que reciben Bevacizumab™ en combinación con QT de 1.a o 2.a líneas basadas en 5-FU2,5. Scappatici et al5 en un ensayo controlado con 424 pacientes detectaron un aumento de complicaciones anastomóticas, pero sin significación estadística. Otros estudios han sido más claros. En la serie de Sugrue et al4 con 1.968 pacientes, se detectaron perforaciones en 1,7% y se establecieron algunos factores de riesgo: AINES, diverticulosis, úlcera péptica, tumor primario intacto, cirugía y/o RT previas, complicaciones anastomóticas postoperatorias, carcinomatosis y obstrucción intestinal. Estos factores de riesgo han sido confirmados en otras series1,4; sin embargo, Badgwell et al, con 1.442, no encontraron factores de riesgo con la misma tasa de complicaciones6. En el cáncer de recto la RT preoperatoria produce cambios isquémicos evolutivos que podrían sumarse a los inducidos por el Bevacizumab™7.
El carácter isquémico de las lesiones se traduce, como en nuestros casos, en la aparición de dolor intenso en la zona perineal y anal previo a las complicaciones sépticas8. Aunque en la mayoría de los casos comunicados las complicaciones aparecen entre 8 y 10 semanas de iniciado el tratamiento4,6 otras series han encontrado complicaciones alejadas de la cirugía como en nuestros casos8,9. Además, más frecuentes en pacientes con antecedentes de complicaciones anastomóticas —como en nuestro primer caso—.
A la vista de los casos publicados se debería tener en cuenta algunas recomendaciones cuando se emplea el Bevacizumab™ en pacientes intervenidos de neoplasias colorrectales. En cirugía programada esperar entre 40 y 60 días tras el tratamiento con Bevacizumab™ y tras la cirugía no iniciarlo antes de 30 a 60 días 1,5,10. Además, evitar el cierre de estomas si se piensa en iniciar Bevacizumab™1. En caso de cierre de estomas realizar de forma previa y rutinaria enema opaco y/o colonoscopia y valorar TAC. Por otra parte, en cirugía de urgencia valorar la creación de estomas, extremar las indicaciones de anastomosis no protegidas y valorar el empleo de mallas o sistemas de refuerzo en las heridas de laparotomía1,8.