La resección pancreática supone un riesgo teórico de desarrollo de diabetes; no obstante, son escasos los estudios que han mostrado el efecto de la duodenopancreatectomía cefálica en el control glucémico postoperatorio.
Material y métodosSe revisó el seguimiento clínico postoperatorio de 70 pacientes sometidos a duodenopancreatectomía cefálica entre marzo de 1993 y noviembre de 2009 en nuestro hospital. La indicación quirúrgica se debió a enfermedad primaria pancreática en 30 casos (21 adenocarcinomas de páncreas, 6 pancreatitis crónicas, 1 carcinoma endocrino, 1 cistoadenoma y 1 seudoquiste complicado). En los restantes 40 pacientes el páncreas no estaba afectado (24 carcinomas ampulares, 11 colangiocarcinomas, 3 carcinomas duodenales, 1 adenoma de la papila y 1 hiperplasia adenomiomatosa de la vía biliar). Se recogieron los datos del estado diabetológico pre y postoperatorio.
ResultadosAntes de la resección, 49 pacientes (70,0%) eran normoglucémicos sin necesidad de tratamiento. Diecisiete pacientes requerían tratamiento antidiabético oral, 3 insulina subcutánea y sólo uno era tratado mediante dieta. La duodenopancreatectomía deterioró el control glucémico en el 47,1% de los pacientes (23 de los previamente no diabéticos y 10 de los tratados con antidiabéticos orales). El control glucémico fue peor cuando la indicación quirúrgica se debió a una afección primaria de la glándula (progresión del 63,3%) en comparación con los pacientes con patología (progresión del 35,0) (p<0,05).
ConclusionesNuestro estudio revela que la resección de la cabeza pancreática favorece la aparición de diabetes postoperatoria, especialmente cuando la indicación quirúrgica se debe a una afección primaria del páncreas.
Pancreatic resection carries a theoretical risk of developing diabetes; however few studies have demonstrated the effect of a cephalic duodenopancreatectomy on post-operative blood glucose control.
Material and methodsAn analysis was made of the post-operative clinical follow up of 70 patients subjected to a cephalic duodenopancreatectomy in our Hospital between March 1993 and November 2009. The surgical indication was due to primary pancreatic disease in 30 patients (21 adenocarcinoma of the pancreas, 6 chronic pancreatitis, 1 endocrine carcinoma, 1 cystadenoma and 1 complicated pseudocyst). The pancreas was not affected in the other 40 patients (24 ampullary carcinomas, 11 cholangiocarcinomas, 3 duodenal carcinomas, 1 papillary adenoma and 1 adenomatous hyperplasia of the bile duct). Data on the pre- and post-operative diabetic state were collected.
ResultsBefore resection, 49 patients (70.0%) had a normal glucose without the need for treatment. Seventeen patients required oral diabetic treatment, 3 subcutaneous insulin, and only one was treated by diet. The duodenopancreatectomy worsened glucose control in 47.1% of the patients (23 of the previously non-diabetics and 10 of those treated with oral diabetics). Glucose control was worse when the surgical indication was due to primary involvement of the gland (progression of 63.3%) compared with patients with disease (progression of 35.0%) (P<.05).
ConclusionsOur results show that resection of the head of the pancreas favours the appearance of post-operative diabetes, particularly when the surgical indication is due to primary pancreatic involvement.
A pesar de que la agresividad de la duodenopancreatectomía cefálica esta bien demostrada, las cifras de morbilidad y mortalidad se han reducido notablemente desde que el procedimiento fuera descrito por Whipple1 y Kausch2. Las complicaciones postoperatorias inmediatas son bien conocidas y han sido bien documentadas3-6; sin embargo, aunque parece lógico que la cirugía de la glándula pancreática pueda también afectar a su función endocrina, existen escasos datos acerca del efecto que tiene la resección de la cabeza pancreática en el control glucémico a largo plazo. La mayoría de las células beta de los islotes de Langerhans se localizan en la cola pancreática, por lo que la aparición de una diabetes mellitus pancreatopriva es esperable tras una resección corporocaudal. No obstante, se conoce poco acerca de cómo el procedimiento de Whipple puede afectar al control glucémico y si este efecto puede ser diferente en función de si la indicación para la resección de la cabeza pancreática se realiza por causa de una enfermedad primaria de la glándula o no. El riesgo de desarrollar una diabetes tras esta cirugía y de necesitar tratamiento insulínico de por vida es una de las dudas que con frecuencia plantean los pacientes antes de la intervención, debido a ello el cirujano debe conocer el riesgo de aparición de intolerancia hidrocarbonada. En este estudio analizamos la probabilidad de aparición de diabetes mellitus y de progresión en la necesidad de tratamiento hipoglucemiante tras someter a los pacientes a una DPC.
Material y métodosSe revisaron retrospectivamente los datos del seguimiento de los pacientes que fueron sometidos a DPC en nuestro hospital desde marzo de 1993 a noviembre del 2009. Los pacientes que fallecieron en el postoperatorio inmediato o se perdieron de seguimiento fueron excluidos. Se recogieron datos de 70 pacientes con una edad media±desviación estándar de 60,4±11 años (rango de 31 a 84 años). Se intervinieron 30 varones y 40 mujeres. La DPC se efectuó tras un diagnóstico de enfermedad pancreática primaria en 30 pacientes (21 adenocarcinomas pancreáticos, 6 pancreatitis crónicas, un carcinoma endocrino, un cistoadenoma mucinoso de cabeza pancreática y un paciente intervenido debido a un seudoquiste complicado con una hemorragia intraquística masiva). En los restantes 40 casos la glándula pancreática no se vio primariamente afectada y la neoplasia que motivó la DPC se localizó en otras estructuras de la encrucijada bilio-pancreática (24 adenocarcinomas ampulares, 11 colangiocarcinomas de la vía biliar distal, 3 adenocarcinomas duodenales, un adenoma velloso de la ampolla de Vater y una hiperplasia adenomiomatosa de la vía biliar). Se realizó una DPC estándar tipo Whipple en 58 pacientes (82,9%), mientras que 12 pacientes fueron sometidos a una DPC con preservación pilórica. Se recogió el estado diabetológico de los pacientes en el período preoperatorio y durante su seguimiento clínico postoperatorio en consultas externas. Durante la evaluación preoperatoria de los pacientes se analizó su historial médico y se determinó si existía un diagnóstico previo de diabetes mellitus realizado por su médico de familia, endocrinólogo o internista, recogiendo en tal caso el tipo de tratamiento que recibían para el control glucémico. Los pacientes que no habían presentado antecedentes de cifras anormales de glucemia y que, por tanto, no habían requerido tratamiento fueron considerados no diabéticos. La insuficiencia pancreática endocrina se dividió en aquellos pacientes que sólo habían requerido dieta para su control glucémico, los que estaban recibiendo tratamiento con hipoglucemiantes por vía oral y los que necesitaban aporte de insulina subcutánea para alcanzar cifras normales de glucemia. Tras la cirugía, todos aquellos pacientes que presentaron cifras anormales de glucemia de forma mantenida durante su ingreso fueron evaluados antes de su alta hospitalaria por un endocrinólogo para plantear la actitud terapéutica. El control glucémico ambulatorio posterior fue realizado por su médico de familia. El seguimiento postoperatorio medio en las consultas externas de cirugía fue de 47,27 meses, aunque la progresión del estado diabetológico sólo se analizó si éste apareció durante el primer año postoperatorio para no incluir causas no quirúrgicas como causantes del deterioro del control de la glucemia. Todos los pacientes analizados fueron seguidos al menos durante 1 año, a excepción de 9 pacientes que fallecieron por recidiva tumoral antes de completar los 12 meses de seguimiento. En el caso de estos pacientes, se analizó el último estado de control glucémico conocido previo a su fallecimiento. La progresión del estado diabetológico se definió como la necesidad de introducir algún tratamiento o medida para el control glucémico durante el seguimiento clínico postoperatorio en aquellos pacientes que no eran diabéticos previamente, o bien cuando se requirió ascender un peldaño terapéutico (dieta/hipoglucemiantes orales/insulina) en aquellos pacientes que ya presentaban algún grado de intolerancia hidrocarbonada preoperatoria. La decisión de la introducción de un tratamiento para el control glucémico o de la modificación del mismo se llevó a cabo por su médico de familia o endocrinólogo de zona. La significación estadística de las diferencias encontradas se analizó mediante una prueba del chi-cuadrado para las variables cualitativas y una prueba no paramétrica de Mann-Whitney para las variables cuantitativas.
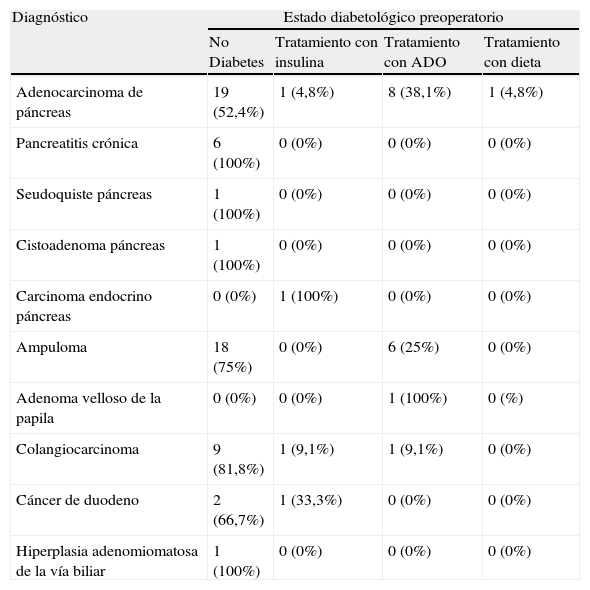
ResultadosAntes de la cirugía, 49 pacientes (70,0%) presentaban un correcto control glucémico, sin necesidad de tratamiento. Entre los pacientes con diagnóstico de diabetes antes de la intervención, sólo uno (1,4%) presentaba intolerancia hidrocarbonada, tratada con dieta y 3 pacientes (4,3%) ya eran tratados con insulina a causa de una diabetes mellitus tipo 1. Los 17 pacientes (24,3%) restantes recibían tratamiento habitual con agentes antidiabéticos orales para mantener un estado normoglucémico. La función endocrina preoperatoria se recoge en la tabla 1.
Estado diabetológico preoperatorio según diagnóstico e indicación quirúrgica
| Diagnóstico | Estado diabetológico preoperatorio | |||
| No Diabetes | Tratamiento con insulina | Tratamiento con ADO | Tratamiento con dieta | |
| Adenocarcinoma de páncreas | 19 (52,4%) | 1 (4,8%) | 8 (38,1%) | 1 (4,8%) |
| Pancreatitis crónica | 6 (100%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Seudoquiste páncreas | 1 (100%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Cistoadenoma páncreas | 1 (100%) | 0 (0%) | 0 (0%) | 0 (0%) |
| Carcinoma endocrino páncreas | 0 (0%) | 1 (100%) | 0 (0%) | 0 (0%) |
| Ampuloma | 18 (75%) | 0 (0%) | 6 (25%) | 0 (0%) |
| Adenoma velloso de la papila | 0 (0%) | 0 (0%) | 1 (100%) | 0 (%) |
| Colangiocarcinoma | 9 (81,8%) | 1 (9,1%) | 1 (9,1%) | 0 (0%) |
| Cáncer de duodeno | 2 (66,7%) | 1 (33,3%) | 0 (0%) | 0 (0%) |
| Hiperplasia adenomiomatosa de la vía biliar | 1 (100%) | 0 (0%) | 0 (0%) | 0 (0%) |
ADO: antidiabéticos orales.
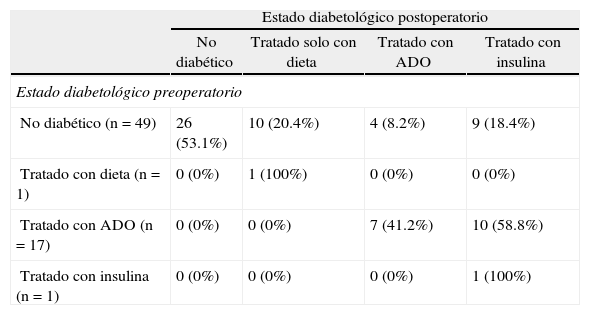
La pancreatectomía indujo una progresión del estado diabetológico en 33 pacientes (47,1% del total). En 23 pacientes previamente no diabéticos (46,9% de los no diabéticos) y en 10 pacientes que eran previamente tratados con hipoglucemiantes por vía oral (58,8% de los tratados con antidiabéticos) se detectó una progresión del estado diabetológico, aunque las diferencias no alcanzaron significación estadística. Entre los pacientes que antes de la intervención tenían cifras normales de glucosa, un 20,4% del total requirió tratamiento con insulina tras la cirugía, un 8,2% antidiabéticos orales y otro 18,4% fue tratado con restricciones dietéticas (tabla 2).
Estado diabetológico pre y postoperatorio
| Estado diabetológico postoperatorio | ||||
| No diabético | Tratado solo con dieta | Tratado con ADO | Tratado con insulina | |
| Estado diabetológico preoperatorio | ||||
| No diabético (n=49) | 26 (53.1%) | 10 (20.4%) | 4 (8.2%) | 9 (18.4%) |
| Tratado con dieta (n=1) | 0 (0%) | 1 (100%) | 0 (0%) | 0 (0%) |
| Tratado con ADO (n=17) | 0 (0%) | 0 (0%) | 7 (41.2%) | 10 (58.8%) |
| Tratado con insulina (n=1) | 0 (0%) | 0 (0%) | 0 (0%) | 1 (100%) |
ADO: antidiabéticos orales.
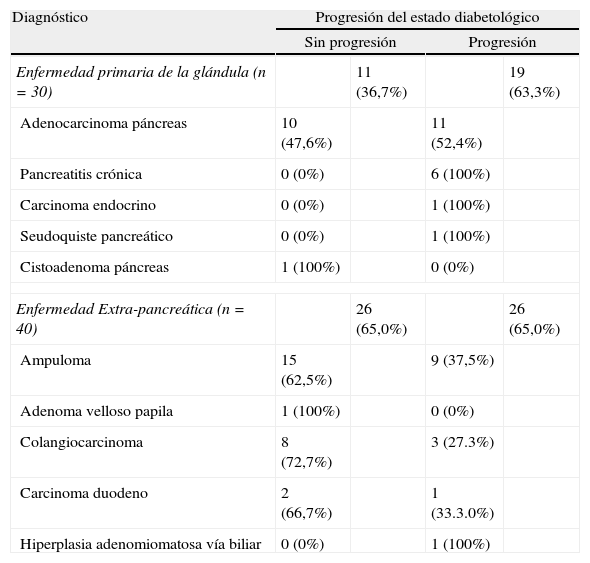
El control glucémico empeoró con mayor frecuencia en aquellos paciente en los que la resección pancreática se realizó debido a una enfermedad primaria de la glándula (63,3% de progresión del estado diabetológico) en comparación con aquellos que fueron sometidos a DPC a causa de una neoplasia extrapancreática (35,0% de progresión) alcanzando significación estadística (p<0,05). Todos los pacientes con pancreatitis crónica empeoraron su control glucémico y aquellos con adenocarcinoma de páncreas progresaron en su insuficiencia endocrina en un 52,4% (tabla 3).
Progresión del estado diabetológico según diagnóstico
| Diagnóstico | Progresión del estado diabetológico | |||
| Sin progresión | Progresión | |||
| Enfermedad primaria de la glándula (n=30) | 11 (36,7%) | 19 (63,3%) | ||
| Adenocarcinoma páncreas | 10 (47,6%) | 11 (52,4%) | ||
| Pancreatitis crónica | 0 (0%) | 6 (100%) | ||
| Carcinoma endocrino | 0 (0%) | 1 (100%) | ||
| Seudoquiste pancreático | 0 (0%) | 1 (100%) | ||
| Cistoadenoma páncreas | 1 (100%) | 0 (0%) | ||
| Enfermedad Extra-pancreática (n=40) | 26 (65,0%) | 26 (65,0%) | ||
| Ampuloma | 15 (62,5%) | 9 (37,5%) | ||
| Adenoma velloso papila | 1 (100%) | 0 (0%) | ||
| Colangiocarcinoma | 8 (72,7%) | 3 (27.3%) | ||
| Carcinoma duodeno | 2 (66,7%) | 1 (33.3.0%) | ||
| Hiperplasia adenomiomatosa vía biliar | 0 (0%) | 1 (100%) | ||
No existieron diferencias en cuanto a la progresión del estado diabetológico en función de la técnica quirúrgica empleada (48.3% tras DPC tipo Whipple y 41,7% tras DPC con preservación pilórica). La aparición de diabetes pancreatopriva no se relacionó con la edad en el momento de la intervención (p>0,05).
DiscusiónLa DPC es una intervención agresiva que aún está gravada con cifras de morbilidad y mortalidad elevadas. Puesto que son las complicaciones postoperatorias inmediatas las que determinan en gran medida las posibilidades de supervivencia a corto y largo plazo, la mayoría de los estudios sólo se centran en el análisis de la morbilidad precoz. Sin embargo, existen pocos estudios que analicen la insuficiencia endocrina que puede aparecer tras la cirugía y que condicionan de forma importante la calidad de vida. La revisión de la literatura científica muestra que la extensión de la resección pancreática es el principal factor implicado en la insuficiencia pancreática endocrina postoperatoria7, lo que demuestra que la pancreatectomía distal conlleva un riesgo mayor de alteraciones del metabolismo hidrocarbonado8,9. A pesar de ello, nuestro estudio revela que la resección de la cabeza pancreática también puede favorecer el desarrollo de una diabetes mellitus pancreatopriva. La mayoría de los estudios que analizan el control glucémico tras la realización de una pancreatectomía han sido realizados en pacientes diagnosticados de pancreatitis crónica10,11, por lo que podría aducirse que el deterioro del control glucémico y la aparición de una diabetes mellitus no estarían relacionados de manera exclusiva con la resección de células productoras de insulina durante la pancreatectomía, sino también en parte con la destrucción previa de éstas por el proceso inflamatorio crónico, limitando la reserva pancreática posquirúrgica. En este sentido, nuestro estudio muestra datos acordes con lo publicado, ya que todos los pacientes que presentaban una pancreatitis crónica eran normoglucémicos previamente a la cirugía, pero requirieron algún tipo de tratamiento para controlar su hiperglucemia después de la intervención.
La asociación de diabetes mellitus y cáncer pancreático ha sido un tema de discusión durante años. El mecanismo según el cual el cáncer pancreático puede estar implicado en la hiperglucemia no es bien conocido. Entre otros factores, se ha sugerido un incremento de la resistencia periférica a la insulina, la supresión de la secreción insulínica, la alteración de la conversión de proinsulina a insulina e incluso la existencia de una alteración de los hábitos nutricionales y del metabolismo hidrocarbonado12. Nuestras resultados revelan que un 47,6% de los pacientes diagnosticados de adenocarcinoma de páncreas presentaban algún tipo de alteración del metabolismo hidrocarbonado antes de la cirugía. Esto supone la mayor incidencia, con mucha diferencia, entre todos los pacientes sometidos a DPC, aunque no todos ellos presentaban hiperglucemias de reciente comienzo. En nuestro estudio no hallamos una mejoría del control glucémico tras la pancreatectomía por cáncer de páncreas, como otros autores han sugerido13. Por el contrario, el grupo de pacientes con enfermedad pancreática maligna mostró el segundo mayor porcentaje de progresión de la insuficiencia pancreática endocrina postoperatoria, con un 52,4% de pacientes afectados. No resulta sorprendente que los pacientes con una afección propia de la glándula pancreática, ya sea maligna o inflamatoria crónica, tuvieran una mayor tendencia a presentar un insuficiente control de la glucemia durante el seguimiento clínico postoperatorio en comparación con los pacientes que presentaban afecciones extrapancreáticas como motivo de la cirugía. La resección de parte del páncreas puede ser suficiente para el desarrollo de una diabetes pancreatopriva cuando las reservas de células beta son limitadas. Sin embargo, más de un tercio de estos pacientes desarrolló hiperglucemia postoperatoria requiriendo tratamiento, lo que pone de manifiesto el riesgo de aparición de diabetes tras la DPC aún en pacientes con páncreas sano.
Se ha descrito que la función endocrina postoperatoria podría verse menos afectada tras una DPC con preservación pilórica, lo que ha añadido argumentos a los que defienden que esta debe ser la técnica de elección cuando se considere una resección de la cabeza pancreática14-16. No obstante, una vez más, estos estudios se han desarrollado en pacientes con pancreatitis crónica, por lo que los resultados podrían estar influenciados por un estado de la glándula ya proclive a la diabetes. En nuestra experiencia, la técnica de resección no tuvo influencia en la función endocrina postoperatoria.
Se ha afirmado que resecciones de menos del 80% de la parte distal del páncreas, donde se localiza la mayor densidad de células beta, suponen un riesgo reducido de aparición de diabetes17 nuestros resultados demuestran como resecciones de menor extensión, las de la cabeza pancreática, donde la densidad de células productoras de insulina se considera menor, conlleva un riesgo importante de aparición de hiperglucemia postoperatoria con necesidad de alguna modalidad de tratamiento. Mas allá de los estudios bioquímicos específicos que analizan la modificación de parámetros concretos de la función endocrina durante el postoperatorio de una DPC, como el péptido C o la hemoglobina glucosilada, nuestro estudio presenta datos pragmáticos sobre la necesidad real de tratamiento hipoglucemiante, insulínico u oral, tras la cirugía, ya que para el paciente que medita sobre si quiere ser sometido a una resección pancreática ante un diagnóstico a menudo incierto el conocer el riesgo real de desarrollar una diabetes cobra una gran importancia. Si bien la literatura admite hasta más de un 20% de enfermedad no tumoral en las piezas de resección de pacientes sometidos a DPC por sospecha de malignidad18, nuestra serie mostró un 14,3%. No obstante, hasta una cuarta parte de los pacientes que empeoraron su control glucémico tras la cirugía presentaban una enfermedad benigna y requirieron de por vida un tratamiento que previamente no necesitaban. Nuestro estudio es retrospectivo por lo que puede aducirse que, tal vez, las indicaciones de progresión en el tratamiento para el control glucémico no fueron homogéneas para todos los pacientes, e incluso que, como sucede en la práctica clínica habitual, los pacientes han podido ser infratratados con antidiabéticos por vía oral cuando en realidad requerían insulina. No obstante, precisamente por ello, los resultados de nuestro estudio son extrapolables a la práctica clínica habitual en la que el cirujano habitualmente no es responsable del control glucémico ambulatorio de los pacientes, por lo que no participa en la decisión de su insulinización, pero sí en la información al paciente en la fase preoperatoria y en el establecimiento de la indicación de resecar. La información que realmente demandan los pacientes es saber si van a desarrollar una diabetes tras la cirugía y si requerirán tratamiento con insulina de por vida. El cirujano pancreático debe conocer el riesgo real de necesidad de tratamiento crónico postoperatorio para el control glucémico en aquellos pacientes que serán sometidos a una DPC para poder informar acerca de todas las consecuencias, postoperatorias inmediatas y a largo plazo, que la aceptación del procedimiento puede conllevar, analizando no sólo los beneficios del procedimiento, sino también sus consecuencias a menudo irreversibles.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.