Aunque la sustitución valvular convencional sigue siendo el tratamiento de elección en la enfermedad valvular aórtica, se han desarrollado en los últimos años procedimientos transcatéter con el objeto de disminuir la mortalidad en los grupos de alto riesgo. Las indicaciones de la implantación de estas prótesis por vía transfemoral y transapical se han basado fundamentalmente en una puntuación elevada en los modelos de estratificación de riesgo. Los resultados a corto plazo para ambas técnicas han mostrado un porcentaje de éxito en el procedimiento superior al 90% y una mortalidad observada inferior a la predicha. Sin embargo queda por conocer la durabilidad a largo plazo de este tipo de prótesis y demostrar su superioridad frente a las técnicas convencionales.
Conventional aortic valve replacement is the reference treatment for the aortic valve pathology. Transcatheter aortic valve implantation has emerged in recent years as alternative for high-risk patients with symptomatic aortic stenosis. The indications of these procedures through the transfemoral or transapical routes are based on a high rating on the different risk scores. Short-term results have shown a periprocedrual success over 90% and hospital mortality lower than the predicted by the scores. However, many questions must be answered about these techniques during the next years like long-term durability and their superiority compared with conventional treatment.
El tratamiento de elección de la enfermedad valvular aórtica sigue siendo la sustitución valvular aórtica convencional1. Sin embargo, existen motivos para buscar tratamientos alternativos. El registro europeo sobre enfermedad valvular (The Euro Heart Survey on Valvular Heart Disease) muestra que un 30–60% de los pacientes con estenosis aórtica (EAo) grave sintomática no son tratados con cirugía, fundamentalmente por la edad avanzada y las comorbilidades asociadas2. Un estudio recientemente publicado sobre una serie de pacientes diagnosticados de EAo de edad avanzada en la ciudad de San Francisco3 mostró resultados similares. Un 55,8% (140/251) de esta población de veteranos con EAo grave sintomática recibió sólo tratamiento médico, y es de destacar como 85 de esos 140 pacientes no fueron evaluados por un especialista en cirugía cardíaca, y que sólo en 23 de ellos la intervención fue desaconsejada por un cirujano.
Ante este hecho se plantea la cuestión de por qué estos pacientes no son remitidos para realizar una inter-vención convencional, cuyos resultados han mejorado en los últimos años de forma notable en estos grupos de riesgo, o si por el contrario, se debieran buscar tratamientos alternativos como las técnicas transcatéter.
En este artículo hemos tratado de dar una visión actual y objetiva sobre los resultados e indicaciones de las técnicas alternativas al reemplazo valvular aórtico convencional, así como valorar las perspectivas futuras de estas técnicas. Fundamentalmente, nos centraremos en el tratamiento de la EAo, dado que es la enfermedad para la cual se han diseñado inicialmente estos procedimientos.
Prevalencia y pronóstico de la estenosis aórtica. justificación de las técnicas alternativasLa enfermedad valvular aórtica, y dentro de ésta la EAo, es una enfermedad muy prevalente en la población general, especialmente en los grupos de edad avanzada. Un 25% de los pacientes mayores de 65 años tiene algún grado de esclerosis aórtica, mientras que la prevalencia de la EAo en los mayores de 75 años se sitúa alrededor del 4%4,5. Los estudios de seguimiento de los pacientes con esclerosis aórtica muestran que uno de cada seis evoluciona hacia una EAo ligera-moderada, y de éstos, un 25% hacia una EAo grave6,7. Por lo tanto, nos enfrentamos a un problema de primera magnitud a nivel sociosanitario, que consumirá muchos recursos en los próximos años con el envejecimiento previsible de la población. Este envejecimiento ya es particularmente llamativo en nuestro país en la actualidad; según datos del Instituto Nacional de Estadística basados en el padrón municipal de enero de 2009, un 8,4% de la población (3.952.363 habitantes) es mayor de 75 años8. Los datos recogidos en nuestro país en el registro PEGASO9, que incluye pacientes con EAo grave mayores de 80 años, aportarán sin duda información muy importante sobre el pronóstico y el tratamiento óptimo de este grupo de enfermos.
El estudio clásico de Ross y Braunwald10 sobre la historia natural de la EAo sintomática determinó que la supervivencia media de los pacientes con angina y/o síncope era de 3 años, y 2 y 1,5 años para los que presentaban disnea e insuficiencia cardíaca avanzada, respectivamente. Sin embargo, esta serie sobre un total de 1.968 pacientes incluyó un grupo de enfermos con una edad media (46 años) y una etiología heterogénea (reumática, bicúspide) que difieren sustancialmente de las características actuales de los pacientes con EAo. Otros estudios retrospectivos11,12 y prospectivos13,14 han evaluado el pronóstico de los pacientes con EAo grave asintomática. Es importante remarcar que dichos estudios no son homogéneos en su diseño (edad, criterios de exclusión, gradiente valvular medio, enfermedad coronaria asociada…). A pesar de estas limitaciones, se observa como un tercio de los pacientes asintomáticos con EAo presentan síntomas a los 2 años de seguimiento11, y dos tercios precisarán sustitución valvular aórtica o fallecerán durante los 4–5 años siguientes11–14. Además, los pacientes con EAo grave asintomática presentan una incidencia anual de muerte súbita del 3–4%10. A pesar de todos estos datos, las guías clínicas siguen recomendando en la actualidad la sustitución valvular aórtica en los pacientes sintomáticos (indicación clase IB), y sólo en determinadas situaciones (disfunción ventrículo izquierdo [VI]) se recomienda la cirugía en pacientes asintomáticos (indicación IC)1. Probablemente existan otros factores pronósticos en los pacientes asintomáticos como son la velocidad pico en la válvula aórtica medida por ecografía-Doppler, la calcificación valvular o los niveles plasmáticos de propéptido natriurético cerebral (BNP) que nos puedan ayudar a determinar la evolución de este subgrupo de enfermos15–17. Sin duda las indicaciones de la cirugía en estos pacientes asintomáticos van a ser revisadas en los próximos años.
Por todo lo anteriormente mencionado, es previsible que el número de pacientes que precisarán una sustitución valvular aórtica va ir aumentando en los próximos años, así como su complejidad y riesgo (mayor edad, reintervenciones, aorta de porcelana…), motivo por el cual se plantea la necesidad de buscar procedimientos alternativos.
Resultados y estimación del riesgo de la cirugía convencionalResultadosComo indicábamos anteriormente, la cirugía de sustitución valvular aórtica es el tratamiento de elección en la EAo grave sintomática1. Ofrece una morbimortalidad hospitalaria baja y unos excelentes resultados a largo plazo en términos de supervivencia y calidad de vida del paciente, así como en lo referente a la regresión de la hipertrofia, recuperación de la función ventricular, funcionamiento de la prótesis y necesidad de reoperación18–20.
Se estima que en el mundo se realizan unas 200.000 sustituciones valvulares aórticas cada año, con una mortalidad hospitalaria menor del 3% y una incidencia de accidente cerebrovascular (ACV) menor del 2%19–22. La base de datos de la Society of Thoracic Surgeons (STS) muestra además, que a pesar de un perfil de riesgo cada vez mayor, la mortalidad ha ido en descenso en los últimos 10 años19.
Así, en esta serie sobre la base de datos de la STS19, al comparar la población operada en 1997 con la operada en 2006, se comprueba como esta última tiene mayor edad, y una mayor prevalencia de obesidad, diabetes, hipertensión, enfermedad pulmonar obstructiva crónica (EPOC), enfermedad cerebrovascular e insuficiencia renal. A pesar de un significativo aumento de la mortalidad esperada (de 2,8 a 3,2%), la mortalidad observada y la ajustada al riesgo han disminuido de manera significativa (3,4 a 2,6%, y 3,5 a 2,3%, respectivamente). Este descenso en la mortalidad se mantiene en cada uno de los subgrupos de alto riesgo anteriormente mencionados. Algo similar sucede con la incidencia de ACV, que ha pasado de 1,7 al 1,3%. La mortalidad fue significativamente mayor en mujeres, pacientes de raza no blanca, mayores de 70 años, diabéticos, enfermedad vascular periférica, fracción de eyección (FE) menor del 30% e índice de masa corporal mayor de 30kg/m2.
Disponemos de abundante información sobre los resultados de esta cirugía a largo plazo20–30. Los principales predictores de mortalidad en el seguimiento son: la edad, la clase funcional, la función ventricular y la coexistencia de enfermedad coronaria. En general, los pacientes de mayor riesgo son los pacientes que obtienen mayor beneficio de la cirugía21. En el subgrupo de los pacientes de mayor edad se consiguen supervivencias a medio y largo plazo superponibles a los de la población general de la misma edad y sexo21. El tipo de prótesis no influye en la supervivencia a largo plazo, aunque la necesidad de reintervención es mayor en las bioprótesis, y la incidencia de complicaciones hemorrágicas y tromboembólicas son mayores en las mecánicas23. En cuanto al gradiente residual de la prótesis, aunque todavía hay discusión al respecto, parece que sólo tiene impacto en la supervivencia en los pacientes con disfunción ventricular28–30.
Estimación del riesgoSon muchas las publicaciones en los últimos años que señalan los buenos resultados de la cirugía en distintos subgrupos de pacientes catalogados como de alto riesgo, fundamentalmente en pacientes de edad avanzada31–37. El principal problema, como se discutirá más adelante, es que se trata de un grupo muy heterogéneo de pacientes, y las puntuaciones de riesgo habituales son menos aplicables, y de entrada es difícil definir de forma correcta la mortalidad esperada. Sabemos que en muchos de esos pacientes de riesgo la cirugía obtiene excelentes resultados, mientras que en otros pacientes también sabemos que los resultados de la cirugía son subóptimos, incluso a veces con puntuaciones de riesgo menores.
El resultado de la cirugía depende de tres factores: las características del paciente (gravedad de la enfermedad cardiovascular, comorbilidad, situación general, etc.), la eficacia del procedimiento (indicación quirúrgica adecuada, técnica quirúrgica, manejo anestésico y postoperatorio, infraestructura del hospital, recursos disponibles, personal, etc.) y, por último, del azar38. Los modelos de riesgo cuantifican solamente el primer punto, por lo que, a igual perfil de riesgo, las diferencias en los resultados se deberán a la eficacia del tratamiento aplicado o al azar. Con la aparición de las técnicas de implante valvular aórtico transcatéter, se han utilizado valores elevados de determinados sistemas de estratificación de riesgo (fundamentalmente EuroSCORE y STS)39,40 como criterio mayor de contraindicación de la cirugía convencional y criterio de indicación del uso de estas técnicas alternativas. Sin embargo esta política puede ser errónea debido al bajo poder discriminativo y a la mala calibración de estos modelos en los pacientes valvulares de alto riesgo41,42. La mayoría de los modelos utilizados son capaces de predecir de manera ajustada el porcentaje de pacientes que van a fallecer, pero no de identificar a los casos concretos en los que se producirá la muerte. Dentro de estos modelos predictivos, el EuroSCORE logístico sobrestima el riesgo quirúrgico en la cirugía valvular, y esta sobrestimación es aún mayor en los subgrupos de riesgo alto y conforme las series son más recientes33,42–45. Además, el EuroSCORE es un modelo desarrollado para aplicarse a series completas, por lo que su uso en el paciente individual sólo debe tener un valor orientativo.
Los pacientes de alto riesgo con frecuencia presentan factores de riesgo no incluidos en estos modelos, por su escasa prevalencia, pero con un peso muy importante en el paciente individual (aorta de porcelana, caquexia, situación cognitiva, radiación torácica previa, etc.). Por todo ello, para la aplicación a un individuo aislado deberían utilizarse modelos que incluyan el mayor número de variables posibles, incluso desarrollados para grupos patológicos concretos, en este caso para la cirugía valvular46–51. Siempre debe considerarse como un factor más a tener en cuenta, y nunca establecerse la indicación o contraindicación de un procedimiento a partir de una cifra determinada de una puntuación de riesgo.
A pesar de los buenos resultados publicados en subgrupos de alto riesgo, un porcentaje importante de estos pacientes no son sometidos a cirugía, como reflejábamos anteriormente. En la mayoría de los pacientes de alto riesgo, la operabilidad o no operabilidad viene definida por el sentido clínico, que incluye variables muchas veces no contempladas por los modelos de riesgo habituales. En cualquier caso, el etéreo concepto de operabilidad es un excelente predictor de los resultados a largo plazo36,37. La clave está en hacerlo cuantificable, para ser capaces de discernir cuáles de esos pacientes con alto riesgo se pueden operar mediante cirugía convencional, cuáles se pueden beneficiar de las técnicas alternativas, y en qué pacientes no vamos a modificar su pronóstico. Como muy acertadamente señala Sundt52, de la Clínica Mayo, en un reciente editorial, «para el paciente inoperable, las técnicas transcatéter son una bendición, pero para el paciente operable, una maldición».
Técnicas transcatéter para el tratamiento de la estenosis aórticaEl primer implante de válvula percutánea en posición aórtica lo realizó Cribier53 en el año 2002. El procedimiento se llevó a cabo en un paciente con múltiples comorbilidades y en shock cardiogénico que había sido rechazado para sustitución valvular aórtica quirúrgica. La implantación de prótesis aórticas mediante técnicas transcatéter ha sufrido desde entonces un crecimiento exponencial, y actualmente ya se han implantado más de 6.00054–69. Actualmente existen en el mercado dos tipos de prótesis: SapienTM (Edwards Lifesciences Inc, Irvine, California, USA) y CoreValveTM (CoreValve, París, Francia; Medtronic Inc, Minneapolis, Minnesota, USA), con unas características específicas para cada modelo. La válvula Edwards SapienTM está constituida por tres velos de pericardio bovino, está suturada en el interior de una estructura metálica de acero inoxidable, y está disponible en diámetros de 23 y 26mm para uso transfemoral y transapical, y se va a incorporar el modelo XT con el número 29mm. La válvula CoreValveTM está constituida por tres velos de pericardio porcino suturados en el interior de una estructura metálica autoexpandible de nitinol. La válvula está disponible en diámetros de 26 y 29 m. Los criterios de indicación de estas técnicas se han basado fundamentalmente en un riesgo operatorio elevado según dos sistemas de puntuación de riesgo quirúrgico (EuroSCORE y STS).
En líneas generales podemos concluir que ambos procedimientos han demostrado ser eficaces a corto plazo, y la mortalidad global observada es inferior a la predicha por el EuroSCORE y el STS, por lo que se ha planteado su uso como una alternativa válida, a la espera de conocer los resultados a medio plazo. Sin embargo este hecho no nos ha de llevar a la conclusión de que estos procedimientos son superiores a la cirugía convencional, ya que los modelos de riesgo tienden a sobrestimar la mortalidad en este grupo de pacientes y no existen estudios aleatorizados comparativos entre la cirugía convencional y los procedimientos transcatéter.
Tampoco existen estudios aleatorizados publicados que comparen ambas técnicas, y sólo existen registros descriptivos que han mostrado resultados similares con una tendencia a presentar mayor riesgo preoperatorio y mortalidad en el grupo transapical, como comentaremos más adelante.
A pesar de los buenos resultados iniciales, quedan muchas preguntas sin responder. En primer lugar, la durabilidad de este nuevo tipo de prótesis es desconocida; aunque los resultados iniciales muestran una hemodinámica excelente y los estudios in vitro pronostican una adecuada durabilidad54–56, estos resultados han de ser confirmados durante el seguimiento. Las lecciones aprendidas con el uso de las prótesis sin soporte en cirugía, cuyo tiempo libre de fallo estructural primario ha sido inferior al esperado, nos deben llevar a tomar una actitud prudente26. También queda por determinar la evolución y pronóstico de las insuficiencias valvulares periprotésicas y centrales residuales que se han observado en ambos procedimientos. Recordemos que suponen una fuente de reintervención, recurrencia de insuficiencia cardíaca o hemólisis en la cirugía convencional.
Por otra parte, aún desconocemos exactamente qué grupo de pacientes se benefician de este tipo de tratamientos menos agresivos y cuál es el abordaje más adecuado (transfemoral o transapical). Además, las indicaciones no se han de basar únicamente en los modelos de riesgo, y probablemente se han de tener en cuenta otros factores de comorbilidad y de enfoque técnico.
Por último y no menos importante, no ha quedado definido claramente el modo de abordaje de esta enfermedad en las diferentes instituciones, y creemos que la mejor forma es crear grupos de trabajo multidisciplinario con la participación activa del cirujano cardíaco en la toma de decisiones. Recordemos que el cirujano realiza dos de las cuatro posibles opciones terapéuticas en la EAo. Hemos de realizar este esfuerzo si no queremos que se repitan experiencias pasadas, como ocurrió en el tratamiento de la cardiopatía isquémica.
Resultados de la técnica transfemoralSon dos los estudios multicéntricos más importantes publicados sobre los resultados de la técnica transfemoral: el Partner y el Source57–59,61. El Partner es un estudio prospectivo, multicéntrico, no aleatorizado, observacional, donde participaron varios centros europeos, y se incluyeron un total de 130 pacientes, 69 en la técnica transapical y 61 en la transfemoral.
El Source es un registro que describe los resultados de un grupo de pacientes tratados de forma consecutiva en 34 centros europeos (entre los que se incluye el Hospital Clínico San Carlos), durante el primer año de comercialización de la prótesis SapienTM de Edwards. Se incluyeron 1.038 pacientes, 575 en la técnica transapical y 463 en la técnica transfemoral. En ambos estudios la indicación de vía transfemoral o transapical quedaba a juicio de cada grupo.
Las tablas I y II muestran los resultados más relevantes de la técnica transfemoral, mostrando los resultados de los registros del Source y el Partner, así como la experiencia de varios centros en Canadá y los del grupo de Vahanian en París60. Todos los anteriores estudios se realizaron con la prótesis SapienTM de Edwards. También se muestran los resultados de varios centros en España con la otra prótesis comercializada para uso transfemoral, la CoreValveTM62.
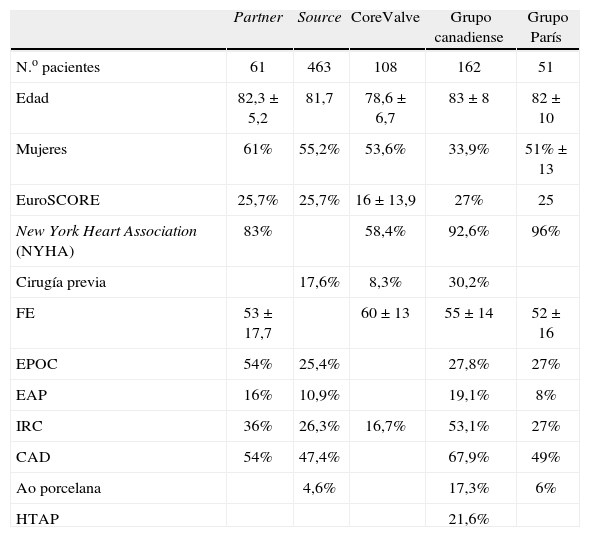
Características demográficas. técnica transfemoral
| Partner | Source | CoreValve | Grupo canadiense | Grupo París | |
| N.o pacientes | 61 | 463 | 108 | 162 | 51 |
| Edad | 82,3±5,2 | 81,7 | 78,6±6,7 | 83±8 | 82±10 |
| Mujeres | 61% | 55,2% | 53,6% | 33,9% | 51%±13 |
| EuroSCORE | 25,7% | 25,7% | 16±13,9 | 27% | 25 |
| New York Heart Association (NYHA) | 83% | 58,4% | 92,6% | 96% | |
| Cirugía previa | 17,6% | 8,3% | 30,2% | ||
| FE | 53±17,7 | 60±13 | 55±14 | 52±16 | |
| EPOC | 54% | 25,4% | 27,8% | 27% | |
| EAP | 16% | 10,9% | 19,1% | 8% | |
| IRC | 36% | 26,3% | 16,7% | 53,1% | 27% |
| CAD | 54% | 47,4% | 67,9% | 49% | |
| Ao porcelana | 4,6% | 17,3% | 6% | ||
| HTAP | 21,6% |
FE: fracción de eyección; EPOC: enfermedad pulmonar obstructiva crónica; EAP: edema agudo de pulmón; IRC: insuficiencia renal crónica; CAD: enfermedad coronaria asociada; HTAP: hipertensión pulmonar.
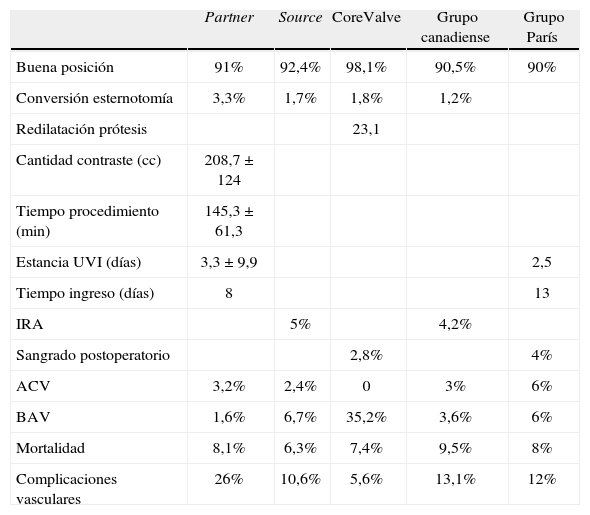
Resultados postoperatorios. técnica transfemoral
| Partner | Source | CoreValve | Grupo canadiense | Grupo París | |
| Buena posición | 91% | 92,4% | 98,1% | 90,5% | 90% |
| Conversión esternotomía | 3,3% | 1,7% | 1,8% | 1,2% | |
| Redilatación prótesis | 23,1 | ||||
| Cantidad contraste (cc) | 208,7±124 | ||||
| Tiempo procedimiento (min) | 145,3±61,3 | ||||
| Estancia UVI (días) | 3,3±9,9 | 2,5 | |||
| Tiempo ingreso (días) | 8 | 13 | |||
| IRA | 5% | 4,2% | |||
| Sangrado postoperatorio | 2,8% | 4% | |||
| ACV | 3,2% | 2,4% | 0 | 3% | 6% |
| BAV | 1,6% | 6,7% | 35,2% | 3,6% | 6% |
| Mortalidad | 8,1% | 6,3% | 7,4% | 9,5% | 8% |
| Complicaciones vasculares | 26% | 10,6% | 5,6% | 13,1% | 12% |
IRA: insuficiencia renal aguda; ACV: accidente cerebrovascular; BAV: bloqueo auriculoventricular.
Las características demográficas son bastante similares entre los diferentes grupos; la puntuación media del EuroSCORE y STS se situaron alrededor del 25 y 16%, respectivamente. Con respecto a los resultados perioperatorios, son bastante homogéneos entre los diferentes grupos; se observa un porcentaje de éxito del procedimiento entre 91–97%, con una mortalidad alrededor del 8%. Por otro lado, los pacientes operados por vía transfemoral presentaron un número elevado de complicaciones vasculares (5,6–26%).
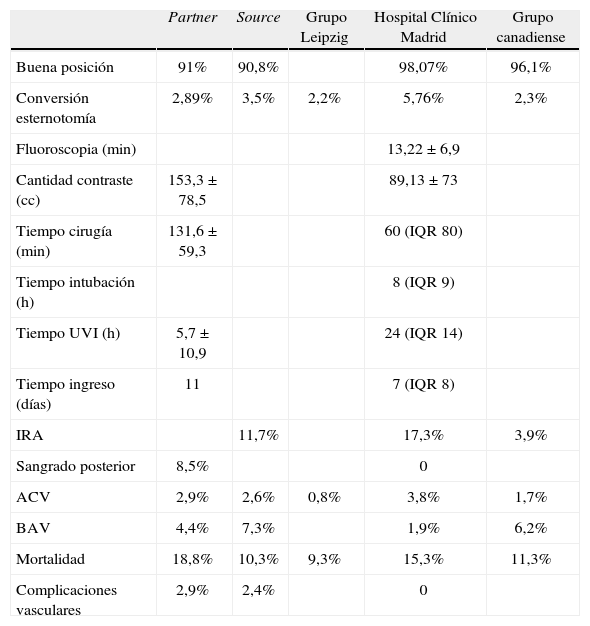
Resultados de la técnica transapicalEn las tablas III y IV presentamos resultados de la técnica transapical de los dos registros más importantes publicados, el Source y el Partner, así como los del grupo de Leipzig, que ha presentado la serie más amplia de implantación de prótesis aórticas vía transapical (n=266) y la experiencia conjunta de varios centros en Canadá, donde se incluyen 396 pacientes, 167 para vía transfemoral y 172 para vía transapical63–69. En este caso la elección de la vía de acceso se hace por un grupo multidisciplinario, donde el criterio principal es el tamaño y la calidad de las arterias femorales. También presentamos nuestros resultados sobre una serie de 52 pacientes.
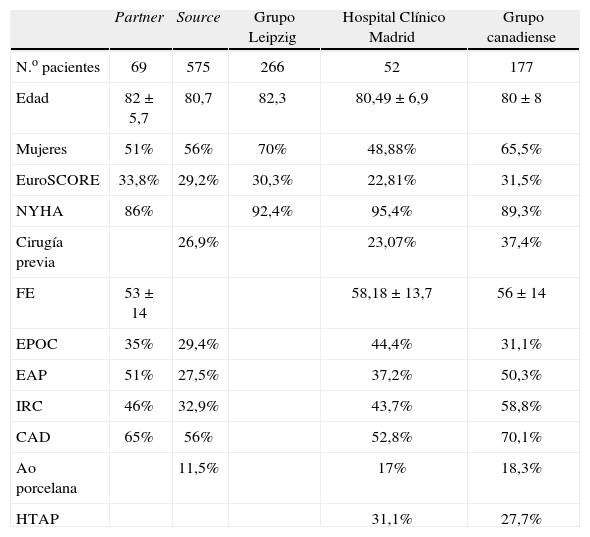
Características demográficas. técnica transapical
| Partner | Source | Grupo Leipzig | Hospital Clínico Madrid | Grupo canadiense | |
| N.o pacientes | 69 | 575 | 266 | 52 | 177 |
| Edad | 82±5,7 | 80,7 | 82,3 | 80,49±6,9 | 80±8 |
| Mujeres | 51% | 56% | 70% | 48,88% | 65,5% |
| EuroSCORE | 33,8% | 29,2% | 30,3% | 22,81% | 31,5% |
| NYHA | 86% | 92,4% | 95,4% | 89,3% | |
| Cirugía previa | 26,9% | 23,07% | 37,4% | ||
| FE | 53±14 | 58,18±13,7 | 56±14 | ||
| EPOC | 35% | 29,4% | 44,4% | 31,1% | |
| EAP | 51% | 27,5% | 37,2% | 50,3% | |
| IRC | 46% | 32,9% | 43,7% | 58,8% | |
| CAD | 65% | 56% | 52,8% | 70,1% | |
| Ao porcelana | 11,5% | 17% | 18,3% | ||
| HTAP | 31,1% | 27,7% |
FE: fracción de eyección; EPOC: enfermedad pulmonar obstructiva crónica; EAP: edema agudo de pulmón; IRC: insuficiencia renal crónica; CAD: enfermedad coronaria asociada; HTAP: hipertensión pulmonar.
Resultados postoperatorios. técnica transapical
| Partner | Source | Grupo Leipzig | Hospital Clínico Madrid | Grupo canadiense | |
| Buena posición | 91% | 90,8% | 98,07% | 96,1% | |
| Conversión esternotomía | 2,89% | 3,5% | 2,2% | 5,76% | 2,3% |
| Fluoroscopia (min) | 13,22±6,9 | ||||
| Cantidad contraste (cc) | 153,3±78,5 | 89,13±73 | |||
| Tiempo cirugía (min) | 131,6±59,3 | 60 (IQR 80) | |||
| Tiempo intubación (h) | 8 (IQR 9) | ||||
| Tiempo UVI (h) | 5,7±10,9 | 24 (IQR 14) | |||
| Tiempo ingreso (días) | 11 | 7 (IQR 8) | |||
| IRA | 11,7% | 17,3% | 3,9% | ||
| Sangrado posterior | 8,5% | 0 | |||
| ACV | 2,9% | 2,6% | 0,8% | 3,8% | 1,7% |
| BAV | 4,4% | 7,3% | 1,9% | 6,2% | |
| Mortalidad | 18,8% | 10,3% | 9,3% | 15,3% | 11,3% |
| Complicaciones vasculares | 2,9% | 2,4% | 0 |
IRA: insuficiencia renal aguda; ACV: accidente cerebrovascular; BAV: bloqueo auriculoventricular.
En estas tablas se puede observar que tanto las características de los pacientes como los resultados perioperatorios son bastante similares, en general pocas complicaciones y mortalidad por debajo de la puntuación de riesgo (9,3–18,8%), estando más relacionado con la comorbilidad de los pacientes que con la técnica en sí.
Desde junio de 2008 hasta la actualidad se han intervenidos 52 pacientes en nuestro centro mediante la implantación de una prótesis aórtica SapienTM por vía transapical, 48% mujeres (edad media de 80,5 años), con EuroSCORE medio de 22,8%. Las características demográficas y perfil de los pacientes se observan en la tabla III. En 32 pacientes se implantó una prótesis de 23mm y en 20 de 26mm. En todos los casos se implantó una bioprótesis de un diámetro mayor al del anillo estimado por ecocardiograma (oversizing). Los resultados perioperatorios se observan en la tabla IV. Tres pacientes requirieron reconversión a cirugía convencional bajo circulación extracorpórea (CEC) por dislocación de la prótesis. Los tres pacientes presentaban en el ecocardiograma intraoperatorio postimplante una insuficiencia aórtica (IAo) grado II.
La mediana del tiempo de intubación orotraqueal posquirúrgico fue de 8h (IQR 9). La mortalidad hospitalaria fue del 15,35% (n=8). Dos de ellos fallecieron por dislocación de la prótesis en las primeras 24h y requirieron reoperación por esternotomía media. Los otros seis por causas no relacionadas con la prótesis. Durante el seguimiento medio de 158 días (desviación estándar [DE] 23,5), cuatro pacientes han muerto, uno de causa no cardíaca y tres de causa cardíaca. Todos los pacientes están en clase funcional I-II, excepto un paciente que está en clase funcional III debido a una insuficiencia respiratoria por EPOC grave.
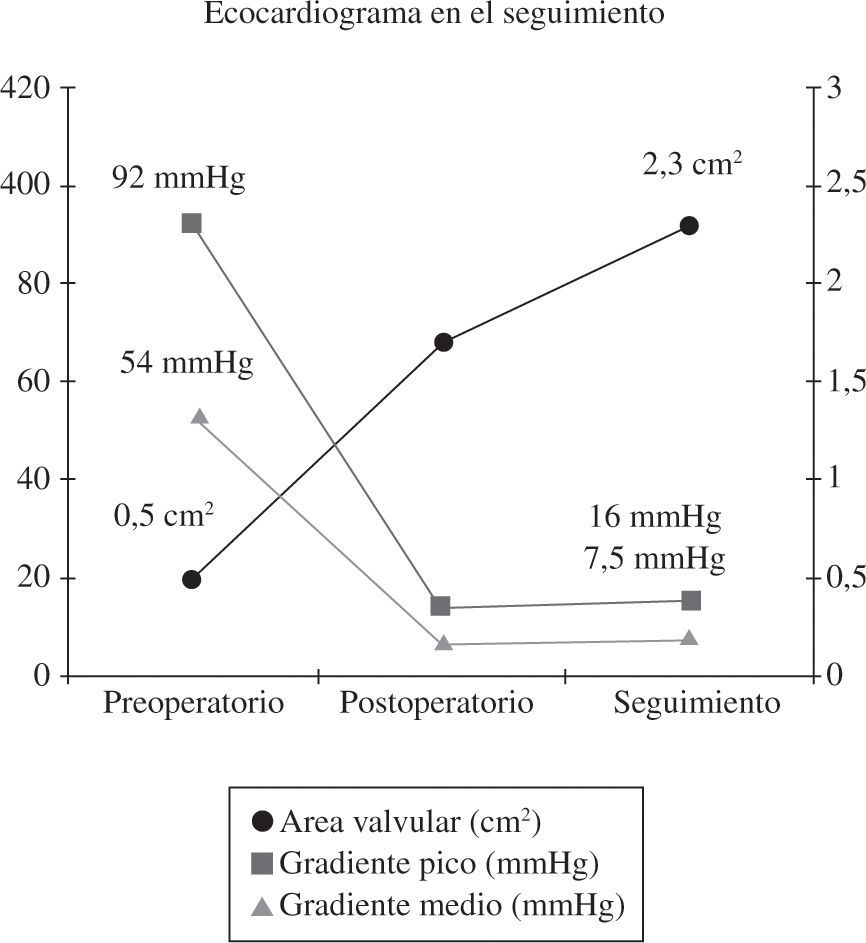
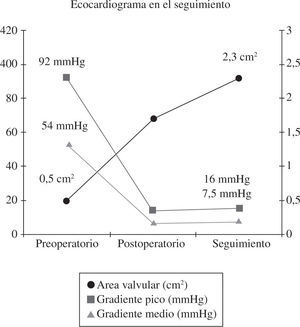
En cuanto a los resultados ecocardiográficos, el 90,4% de los pacientes tienen IAo 0-I al alta hospitalaria. Durante el seguimiento todos los pacientes menos uno tienen IAo grado 0-I. En la figura 1 se observa la evolución de los gradientes y el área desde antes de la cirugía hasta los primeros 6 meses del postoperatorio.
Resultados comparativos entre la técnica transfemoral y transapicalNo existe ningún estudio aleatorizado publicado que compare ambas técnicas. Se ha finalizado la aleatorización del estudio Partner IDE, que es un estudio prospectivo y aleatorizado que se lleva a cabo en EE.UU. y Canadá, y que incluye a pacientes diagnosticados de EAo grave sintomática, divididos en dos cohortes: a) los pacientes considerados no operables son aleatorizados a vía transfemoral con la válvula Edwards SapienTM o a tratamiento médico (objetivo primario: ausencia de muerte al año de seguimiento; diseño de superioridad), y b) los pacientes considerados de alto riesgo quirúrgico son aleatorizados a vía transfemoral o transapical con la válvula Edwards SapienTM o sustitución valvular quirúrgica (objetivo primario: ausencia de muerte durante la duración del estudio; diseño de no inferioridad). El estudio se inició en abril de 2007, la fase de aleatorización finalizó en septiembre de 2009, y los primeros resultados se esperan para finales de 2010. El estudio Partner IDE debería proporcionar mayor evidencia para aconsejar el uso de técnicas transcatéter en los pacientes con EAo grave sintomática considerados inoperables o con muy alto riesgo quirúrgico.
Alternativas a las técnicas transcatéterExisten otras alternativas quirúrgicas al abordaje convencional y el uso de las técnicas transcatéter para los pacientes de alto riesgo. La canulación de la arteria axilar derecha puede ser una opción en los pacientes con EAo grave y aorta de porcelana, cuyo riesgo de complicaciones neurológicas es muy alto70–72. El razonamiento fisiopatológico radica en garantizar un «flujo de lavado» a través del tronco arterial innominado derecho durante los periodos de pinzado y despinzado aórticos, momentos en los cuales se produce la mayor parte de las embolias hacia la circulación arterial cerebral.
Otra alternativa para los pacientes de alto riesgo es la utilización de conductos apicoaórticos con o sin el uso de la CEC y sin la necesidad de realizar pinzado aórtico73,74. Mediante una toracotomía lateral izquierda y con o sin canulación de los vasos femorales es posible la inserción de este conducto desde el ápex del ventrículo izquierdo a la aorta torácica descendente. En el estudio publicado por Gammie, et al.74 sobre 31 pacientes de alto riesgo (puntuación STS media de 9,3) en los que se realizó cirugía de derivación de la válvula aórtica con el implante de un conducto apicoaórtico, se observó una mortalidad de 13%, observándose una baja incidencia de complicaciones neurológicas y renales.
ConclusionesPodemos concluir que el tratamiento de elección de la enfermedad valvular aórtica sigue siendo en la actualidad el recambio valvular convencional. Las técnicas transcatéter han demostrado ser eficaces a corto plazo y tienen unos resultados de mortalidad global esperanzadores. Estas técnicas no están libres de complicaciones. Por otra parte, queda por conocer los resultados de durabilidad de estas prótesis, y es necesario desarrollar estudios aleatorizados que comparen el tratamiento quirúrgico convencional, las dos técnicas transcatéter existentes y el tratamiento médico para determinar cuál es la mejor opción terapéutica en ciertos subgrupos de alto riesgo.