La etiología y otros factores pueden variar los resultados de la reparación mitral. Analizamos la supervivencia y la durabilidad en pacientes de diversa etiología.
Material y métodosFueron intervenidos 406 pacientes de reparación mitral (1997–2011) con edades entre 19–84 años. De ellos, 156 mujeres (38,4%), 57,1% en grado New York Heart Association III-IV. Se consideraron 5 grupos de pacientes: degenerativa (grupo-D), 203; isquémica (grupo-I), 90; funcional no isquémica (grupo-F), 19; reumática (grupo-R), 61 y endocarditis (grupo-E), 33. Se empleó la anuloplastia sobrecorrectora en isquémicas y funcionales. La resección cuadrangular y el implante de neocuerdas fueron predominantes en las degenerativas, mientras que varias técnicas de reseccion-reconstruccion se utilizaron en las reumáticas y endocarditis.
ResultadosHubo 18 éxitus en los 30 primeros días poscirugía (4,4%), mortalidad por grupos: 3,4, 4,4, 0, 6,6 y 10%. Supervivencia actuarial: 86±1% y 70±4% a 5 y 10 años. La mortalidad tardía fue mayor en funcionales e isquémicas (31,6 y 20%) siendo en D, R y E: 12,3, 11,5 y 13,3%. Mayor durabilidad en degenerativas (vs. no degenerativas) estando libres de insuficiencia grado 3–4/4: 86±2 vs. 84±2% (p=0,46) los 5 primeros años y 82±3 vs. 54±1% (p=0,02), posteriormente. El grupo-R se asoció a recidiva grado-3 (odds ratio: 1,98, intervalo de confianza 95%: 1,01–3,89; p=0,05) y grado-4 (odds ratio: 3,31, intervalo de confianza 95%: 1,17–9,32; p=0,02). Catorce pacientes precisaron sustitución protésica: 3, 1, 1, 6 y 3, respectivamente.
ConclusionesLos resultados de la cirugía reparadora fueron satisfactorios. Supervivencia, tasa de recidiva y reoperación fueron excelentes en valvulopatía degenerativa. La reumática presentó menor durabilidad y la isquémica y funcional mostraron menor supervivencia.
Etiology and other factors may influence the outcomes of mitral valve repair. We have analyzed survival and durability in a variety of etiologies.
Material and Methods406 patients underwent mitral valve repair (1997–2011) with ages between 19–84 years. 156 were females (38.4%). 57.1% patients were in NYHA class III-IV. 5 groups were considered: degenerative (group-D), 203; ischemic (group-I), 90; functional (non-ischemic) (group-F), 19; rheumatic (group-R), 61 and endocarditis (group-E), 33 patients. Undersized annuloplasty was used in ischemic and functional groups. Quadrangular resection and neochordal repair were predominant in case of degenerative etiology whereas a variety of resective and reconstructive techniques were used in rheumatic and endocarditis groups.
Results30-day mortality was 4.4%: 3.4%, 4.4%, 0%, 6.6% and 10% in respective groups. 5 and 10-year survival: 86±1% and 70±4%. Long-term mortality was higher in groups F and I (31.6% and 20%) compared with 12.3%, 11.5% and 13.3% in groups D, R and E. Group-D had higher durability and freedom from grade 3–4/4 mitral regurgitation than non-degenerative groups: 86±2 vs 84±2% (p=0.46) at 5 years and 82±3 vs 54±1% (p=0.02) at later follow-up. Group-R was associated with recurrent grade-3 and grade-4 mitral regurgitation (OR: 1.98, 95%-CI: 1.01–3.89; p=0.05 and OR: 3.31, 95%-CI: 1.17–9.32; p=0.02). 14 patients underwent mitral valve replacement: 3, 1, 1, 6 and 3.
ConclusionsThe outcomes of mitral valve repair were successful. Survival, recurrence rate and reoperation were excellent in group-D. Rheumatic regurgitation had shorter durability and functional mitral regurgitation had lower survival.
Actualmente, la reparación mitral es el procedimiento quirúrgico más frecuentemente empleado en Europa y Norteamérica para tratar la valvulopatía mitral1. En nuestro país, esta cirugía ha experimentado un notable crecimiento con el descenso de la patología reumática y la mayor experiencia en procedimientos de reparación valvular alcanzada por los diferentes grupos quirúrgicos2,3. Las tasas de reparación han aumentado con el desarrollo de nuevas técnicas como las basadas en el empleo de neocuerdas o en la ampliación de velos con pericardio autólogo4. La patología degenerativa ofrece las mejores garantías de una reparación exitosa5. Los pacientes con otras causas de insuficiencia mitral también pueden beneficiarse de una cirugía valvular reconstructiva, aunque las posibilidades de una reparación eficaz y duradera son menores y el pronóstico del paciente puede quedar mermado por la patología de base6–8.
El objetivo del estudio es evaluar los resultados precoces y a largo plazo de las diferentes estrategias de reparación mitral en un grupo amplio de pacientes con insuficiencia mitral de diversa etiología. Especialmente, se pretende estudiar la durabilidad de la reparación y la supervivencia alcanzada en pacientes con diversas causas de enfermedad valvular mitral.
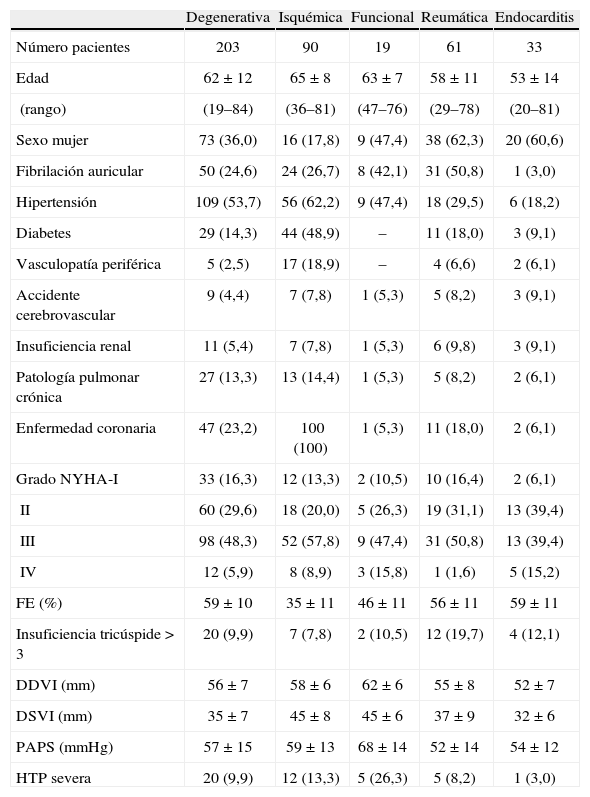
Pacientes y métodosUn total de 425 pacientes fueron sometidos a reparación valvular mitral en nuestro centro entre febrero de 1997 y julio de 2011. Se excluyeron las reoperaciones (6 pacientes), la cirugía urgente salvo endocarditis (8 pacientes) y la malformación congénita de la válvula mitral (5 pacientes). El grupo resultante estaba formado por 406 pacientes, 156 mujeres, con rango de edades entre 19 y 84 años. La mayor parte de los pacientes presentaba clínica de disnea, estando en grado funcional New York Heart Association (NYHA) III-IV el 57,1%. Se consideraron 5 grupos según la causa de la valvulopatía: 203 pacientes (50%) tenían una valvulopatía degenerativa (grupo-D), 90 (22,2%) isquémica (grupo-I), 19 (4,7%) funcional no isquémica (miocardiopatía dilatada idiopática o secundaria a valvulopatía aórtica) (grupo-F), 61 (15%) reumática y 33 (8,1%) endocarditis. Entre las degenerativas, la mayoría presentaban una deficiencia fibroelástica, 143 pacientes (70,4%) y el resto fueron diagnosticados de enfermedad de Barlow (29,6%). El diagnóstico de ambas entidades se realizó con base en la apariencia macroscópica de la válvula. Hubo 151 pacientes que presentaban un prolapso del velo posterior, 28 del velo anterior y 24 de ambos velos.
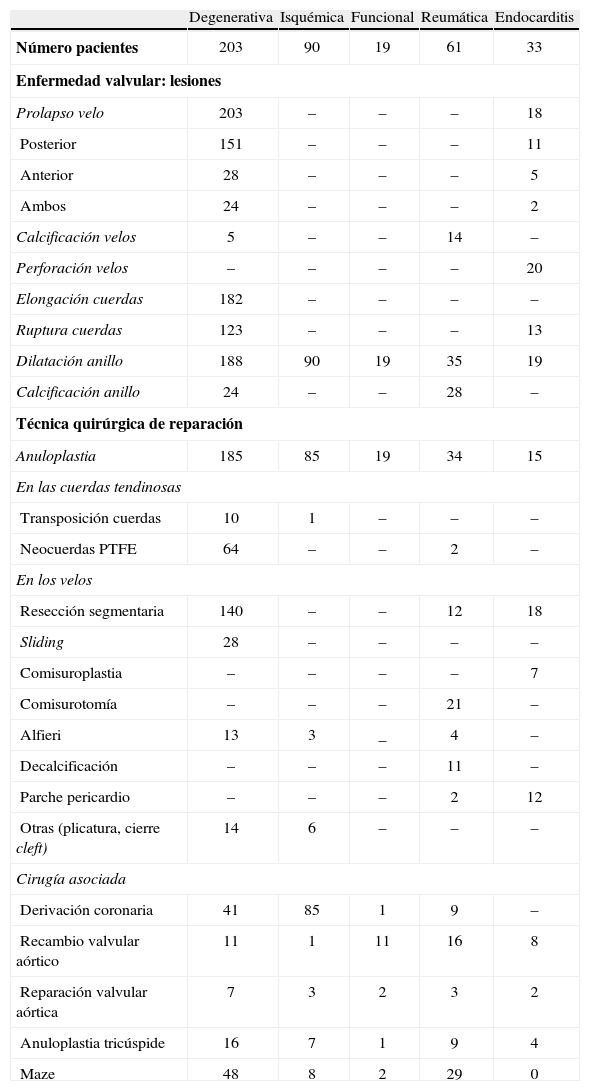
Las principales características de los pacientes y la patología valvular en los distintos grupos etiológicos se presentan en las tablas 1 y 2.
Características preoperatorias.
| Degenerativa | Isquémica | Funcional | Reumática | Endocarditis | |
| Número pacientes | 203 | 90 | 19 | 61 | 33 |
| Edad | 62±12 | 65±8 | 63±7 | 58±11 | 53±14 |
| (rango) | (19–84) | (36–81) | (47–76) | (29–78) | (20–81) |
| Sexo mujer | 73 (36,0) | 16 (17,8) | 9 (47,4) | 38 (62,3) | 20 (60,6) |
| Fibrilación auricular | 50 (24,6) | 24 (26,7) | 8 (42,1) | 31 (50,8) | 1 (3,0) |
| Hipertensión | 109 (53,7) | 56 (62,2) | 9 (47,4) | 18 (29,5) | 6 (18,2) |
| Diabetes | 29 (14,3) | 44 (48,9) | – | 11 (18,0) | 3 (9,1) |
| Vasculopatía periférica | 5 (2,5) | 17 (18,9) | – | 4 (6,6) | 2 (6,1) |
| Accidente cerebrovascular | 9 (4,4) | 7 (7,8) | 1 (5,3) | 5 (8,2) | 3 (9,1) |
| Insuficiencia renal | 11 (5,4) | 7 (7,8) | 1 (5,3) | 6 (9,8) | 3 (9,1) |
| Patología pulmonar crónica | 27 (13,3) | 13 (14,4) | 1 (5,3) | 5 (8,2) | 2 (6,1) |
| Enfermedad coronaria | 47 (23,2) | 100 (100) | 1 (5,3) | 11 (18,0) | 2 (6,1) |
| Grado NYHA-I | 33 (16,3) | 12 (13,3) | 2 (10,5) | 10 (16,4) | 2 (6,1) |
| II | 60 (29,6) | 18 (20,0) | 5 (26,3) | 19 (31,1) | 13 (39,4) |
| III | 98 (48,3) | 52 (57,8) | 9 (47,4) | 31 (50,8) | 13 (39,4) |
| IV | 12 (5,9) | 8 (8,9) | 3 (15,8) | 1 (1,6) | 5 (15,2) |
| FE (%) | 59±10 | 35±11 | 46±11 | 56±11 | 59±11 |
| Insuficiencia tricúspide > 3 | 20 (9,9) | 7 (7,8) | 2 (10,5) | 12 (19,7) | 4 (12,1) |
| DDVI (mm) | 56±7 | 58±6 | 62±6 | 55±8 | 52±7 |
| DSVI (mm) | 35±7 | 45±8 | 45±6 | 37±9 | 32±6 |
| PAPS (mmHg) | 57±15 | 59±13 | 68±14 | 52±14 | 54±12 |
| HTP severa | 20 (9,9) | 12 (13,3) | 5 (26,3) | 5 (8,2) | 1 (3,0) |
Variables presentadas como media ± desviación estándar o como n (%).
DDVI y DSVI: diámetro diastólico y sistólico ventrículo izquierdo; FE: fracción de eyección; HTP: hipertensión pulmonar; NYHA: New York Heart Association; PAPS: presión sistólica pulmonar.
Enfermedad valvular y técnica quirúrgica.
| Degenerativa | Isquémica | Funcional | Reumática | Endocarditis | |
| Número pacientes | 203 | 90 | 19 | 61 | 33 |
| Enfermedad valvular: lesiones | |||||
| Prolapso velo | 203 | – | – | – | 18 |
| Posterior | 151 | – | – | – | 11 |
| Anterior | 28 | – | – | – | 5 |
| Ambos | 24 | – | – | – | 2 |
| Calcificación velos | 5 | – | – | 14 | – |
| Perforación velos | – | – | – | – | 20 |
| Elongación cuerdas | 182 | – | – | – | – |
| Ruptura cuerdas | 123 | – | – | – | 13 |
| Dilatación anillo | 188 | 90 | 19 | 35 | 19 |
| Calcificación anillo | 24 | – | – | 28 | – |
| Técnica quirúrgica de reparación | |||||
| Anuloplastia | 185 | 85 | 19 | 34 | 15 |
| En las cuerdas tendinosas | |||||
| Transposición cuerdas | 10 | 1 | – | – | – |
| Neocuerdas PTFE | 64 | – | – | 2 | – |
| En los velos | |||||
| Resección segmentaria | 140 | – | – | 12 | 18 |
| Sliding | 28 | – | – | – | – |
| Comisuroplastia | – | – | – | – | 7 |
| Comisurotomía | – | – | – | 21 | – |
| Alfieri | 13 | 3 | _ | 4 | – |
| Decalcificación | – | – | – | 11 | – |
| Parche pericardio | – | – | – | 2 | 12 |
| Otras (plicatura, cierre cleft) | 14 | 6 | – | – | – |
| Cirugía asociada | |||||
| Derivación coronaria | 41 | 85 | 1 | 9 | – |
| Recambio valvular aórtico | 11 | 1 | 11 | 16 | 8 |
| Reparación valvular aórtica | 7 | 3 | 2 | 3 | 2 |
| Anuloplastia tricúspide | 16 | 7 | 1 | 9 | 4 |
| Maze | 48 | 8 | 2 | 29 | 0 |
Las variables están presentadas como n. PTFE: politetrafluoroetileno.
El abordaje habitual fue la esternotomía media. La circulación extracorpórea con hipotermia moderada (28–32°C) se estableció mediante canulación bicava y de aorta ascendente. La protección miocárdica se basó en el empleo de cardioplejia hemática fría anterógrada y retrógrada con dosis final de reperfusión caliente (hot-shot). Tras el pinzamiento aórtico, el acceso de la mitral se realizó a través del surco interauricular en 367 pacientes y por vía transeptal en 39 pacientes.
El prolapso de velo posterior se trató en 140 pacientes mediante resección cuadrangular, en 17 pacientes se asoció a la misma el implante de neocuerdas en velo posterior y en 32 pacientes se implantaron solo neocuerdas sin resección alguna. En los pacientes con enfermedad de Barlow y con exceso de tejido del velo posterior (altura velo > 2cm) se asoció sliding plasty (28 pacientes). En el prolapso de velo anterior se empleó inicialmente la transposición de cuerdas (10 pacientes) que fue progresivamente sustituida por el implante de neocuerdas de politetrafluoroetileno (14 pacientes). Solo ocasionalmente se empleó la resección triangular y nunca el acortamiento de cuerdas. La sutura entre ambos velos mediante procedimiento de Alfieri se empleó tan solo en 13 pacientes. En el grupo-D, la reparación con cuerdas de Gore-Tex® se empleó en un total de 64 pacientes, evitando completamente la resección de tejido en 46 pacientes. Fueron empleadas suturas de politetrafluoroetileno CV-4 y la mayor parte de los pacientes fueron intervenidos mediante la técnica de repliegue mitral (o Folding Leaflet) que hemos publicado recientemente9. La técnica busca como principal objetivo facilitar el implante de múltiples neocuerdas en ambos velos y poder reparar lesiones extensas que plantean limitaciones para la técnica clásica. De forma resumida, la inserción de la neocuerda en el músculo papilar correspondiente se hace con un punto de sutura simple sin parches de apoyo ni anudado. En cambio, la inserción en el borde libre del velo debe hacerse pasando la sutura varias veces a lo largo de la superficie de coaptación. Con ello se logra remodelar el velo en forma de “palo de hockey”, lo que facilita la creación de una amplia superficie de coaptación. En caso de exceso de tejido, dicho remodelado permite reducir la superficie auricular del velo a expensas del aumento de la superficie de coaptación, disminuyendo el riesgo de movimiento sistólico anterior. Finalmente, la longitud de la neocuerda se establece tras llevar el borde libre del velo hasta el anillo, lo que ocasiona el repliegue completo del mismo. Con el velo plegado las cuerdas marginales adoptan la posición de cuerdas basales. Ambas cuerdas tienen la misma longitud y por tanto, podemos medir la longitud final de la neocuerda tomando como referencia la de una cuerda basal y el propio anillo mitral. Los nudos de la sutura de politetrafluoroetileno deben deslizarse hasta el nivel del anillo sin rebasarlo para evitar el acortamiento de la neocuerda. Al desplegar el velo, la neocuerda pasará a posición de cuerda marginal con una longitud adecuada.
Se asoció anuloplastia mitral en la mayoría de los pacientes con valvulopatía degenerativa (185 pacientes) y en 6 pacientes fue la única técnica empleada. El tamaño del anillo o banda se ajustó a la distancia intertrigonal y especialmente a la anchura del velo anterior. Se evitó implantar anillos pequeños en patología reumática, en cambio, se realizó anuloplastia sobrecorrectora o undersizing de 1 o 2 tamaños en patología isquémica y funcional. El tamaño medio y rango (en mm) de los anillos empleados fue: 30±2 (26–34) en degenerativas, 28±3 (26–30) en isquémicas, 28±4 (26–30) en funcionales, 28±1 (26–32) en reumáticas y 28±3 (26–32) en endocarditis. En la insuficiencia mitral funcional la anuloplastia fue la única técnica empleada, al igual que en 8 pacientes reumáticos. En la endocarditis aguda se evitó el empleo de anillo protésico. No se implantó ningún anillo en 18 degenerativas, 5 isquémicas, 27 reumáticas y 18 endocarditis. La banda de Cosgrove-Edwards se empleó en 76, 22, 6, 13 y 6 pacientes en los grupos respectivos, el anillo Carpentier-Edwards Physio-I en 51, 30, 5, 17 y 7 pacientes y el Memo-3D (Sorin Group) en 28 degenerativas, 6 isquémicas, 3 funcionales, 4 reumáticas y 2 endocarditis. Otros anillos se implantaron de forma más selectiva: el anillo Carpentier-Edwards Physio-II se implantó en 27 pacientes del grupo D, McCarthy-Edwards IMR ETIlogix en 16 isquémicas, Geo-form (Edwards Lifesciences) en 3 funcionales y 4 isquémicas y Sovering miniband (Sorin Group) en 2 degenerativas, 6 isquémicas y 2 funcionales. De forma muy puntual se empleó el sistema Mitrofix (BioIntegral Surgical Inc, Toronto) en 1 degenerativa y una banda de teflón en 1 isquémica.
Los datos de la técnica quirúrgica de reparación empleada en los diferentes grupos se presentan en la tabla 2.
SeguimientoLas características preoperatorias, las variables quirúrgicas y los resultados intrahospitalarios fueron recogidos de forma prospectiva e introducidos en una base de datos informatizada durante todo el período del estudio. El seguimiento clínico-ecocardiográfico posterior se realizó de forma seriada al mes, a los 6 meses y al año de la intervención en la mayor parte de pacientes. Datos ecocardiográficos posteriores fueron obtenidos consultando el archivo de la unidad de ecocardiografía de nuestro hospital o mediante consulta al hospital de referencia en su caso. Todos los pacientes considerados en este estudio disponían de un ecocardiograma al mes y a los 6 meses de la cirugía. Hubo 378 pacientes con un ecocardiograma al año y 325 en el seguimiento tardío. La insuficiencia mitral se clasificó en escala de 0 a 4 mediante ecocardiografía de acuerdo con las normas publicadas10, siendo 0: ausencia de insuficiencia, 1: trivial o ligera, 2: moderada, 3: moderada a severa, 4: severa. En la insuficiencia tricuspídea también se empleó esta clasificación.
Se completó el seguimiento mediante consulta de historia clínica, contacto telefónico y consulta al Índice Nacional de Defunciones. Se valoró especialmente la mortalidad, la recidiva de insuficiencia mitral, la necesidad de reoperación y el grado funcional al final del seguimiento. La mortalidad se desglosó en aquella acontecida durante los 30 primeros días tras la cirugía o en mortalidad tardía cuando ocurrió posteriormente. Reoperación valvular mitral fue cualquier nuevo procedimiento quirúrgico realizado sobre dicha válvula tras salir del quirófano.
Análisis estadísticoEl análisis de los datos se realizó con el programa estadístico SPSS 12.0 Statistical Package (SPSS Inc, Chicago, IL). Las variables categóricas se expresaron como porcentajes y las continuas como media ± desviación estándar. Estas últimas variables se compararon con el test de la t de Student (o el test de Wilcoxon si distribución no normal), mientras que en la comparación entre categóricas se empleó el test de χ2 o el test exacto de Fisher cuando fue apropiado. Para el estudio de supervivencia, reoperación y seguimiento de recidiva de la insuficiencia mitral se empleó el análisis actuarial de Kaplan-Meier con el test de los rangos logarítmicos para realizar comparaciones. La regresión logística se aplicó en el análisis de factores asociados a mortalidad hospitalaria y la regresión de Cox fue empleada para determinar factores asociados a mortalidad tardía y a recidiva de la insuficiencia mitral.
ResultadosMortalidad tempranaHubo 18 pacientes que fallecieron en los 30 primeros días tras la cirugía (4,4%), siendo la mortalidad desglosada en los grupos D, I, F, R y E: 3,4, 4,4, 0, 6,6 y 9,1%, respectivamente (mortalidad predictiva por EuroSCORE logístico: 4,8±2,8, 8,7±3,2, 6,7±3,7, 4,9±2,7 y 16,8±4,4%). Los principales factores asociados a esta mortalidad en los 30 primeros días (análisis univariable) fueron: la edad (p<0,01), recambio valvular aórtico asociado (p<0,05), grado NYHA III-IV (p<0,05), vasculopatía periférica (p<0,05), insuficiencia tricuspídea de grado 3 o superior (p<0,01) e hipertensión pulmonar severa (p<0,05). La derivación coronaria asociada a la reparación mitral estuvo cerca de la significación estadística (p=0,06). En el análisis multivariable permanecieron como predictores independientes: la edad (p<0,001), la vasculopatía periférica (p<0,05) y la insuficiencia tricuspídea de grado 3 o superior (p<0,05). El recambio valvular aórtico asociado estuvo cerca de la significación estadística (p=0,09). En la tabla 3 se incluyen los principales factores asociados a mortalidad hospitalaria.
Predictores de mortalidad hospitalaria.
| Variables | ||||||
| Univariable | Multivariable | |||||
| OR | IC 95% | P | OR | IC 95% | P | |
| Variables categóricas | ||||||
| Vasculopatía periférica | 4,33 | 1,32–14,18 | 0,02 | 4,20 | 1,06–16,59 | 0,04 |
| Insuficiencia tricúspide ≥3 | 4,47 | 1,59–12,58 | 0,009 | 3,26 | 1,04–10,19 | 0,04 |
| Recambio VAo | 3,16 | 1,07–9,33 | 0,04 | 2,67 | 0,84–8,46 | 0,09 |
| Coronariopatía | 2,31 | 0,89–6,00 | 0,06 | 2,49 | 0,80–7,69 | 0,11 |
| HTP severa | 3,54 | 1,19–10,47 | 0,03 | 2,08 | 0,61–7,15 | 0,24 |
| NYHA III-IV | 3,94 | 1,12–13,83 | 0,01 | 1,19 | 0,45–3,18 | 0,72 |
| Éxitus sí | Éxitus no | P | OR | IC 95% | P | |
| Variables numéricas Edad (años) | 70±8 | 61±12 | 0,004 | 1,43 | 1,11–1,95 | 0,0001 |
IC: intervalo de confianza; HTP: hipertensión pulmonar; NYHA: New York Heart Association; OR: odds ratio; VAo: válvula aórtica.
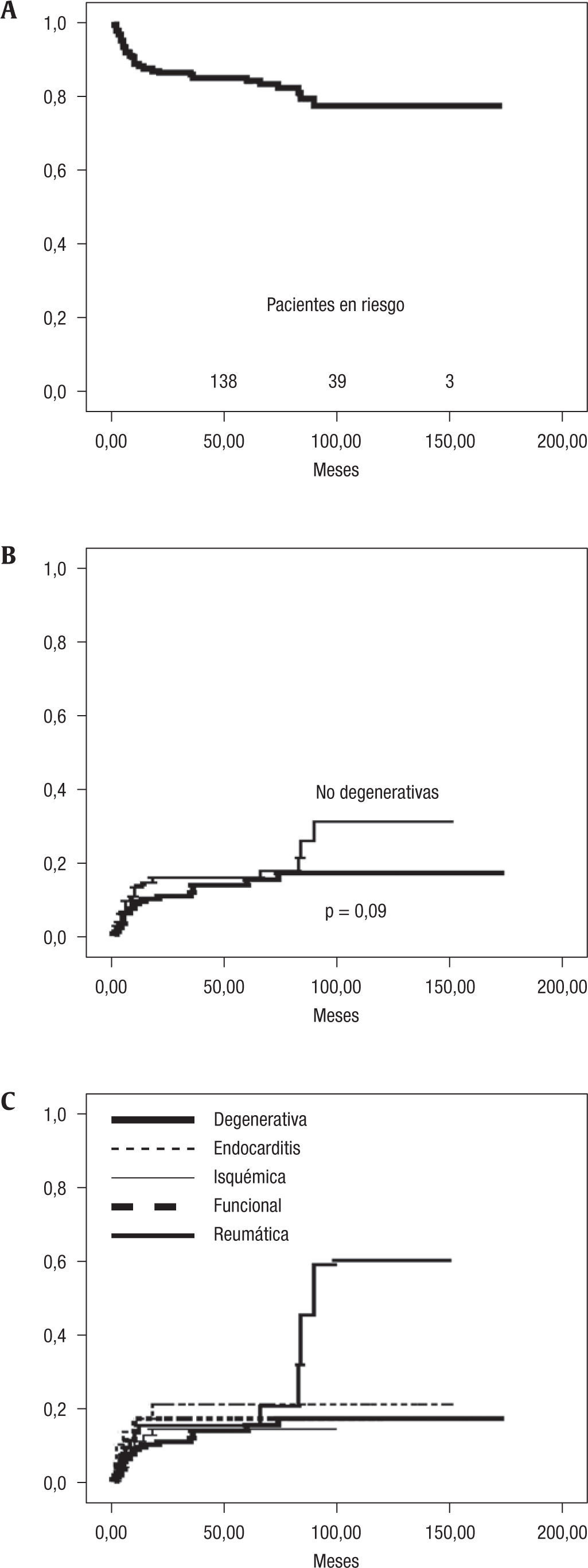
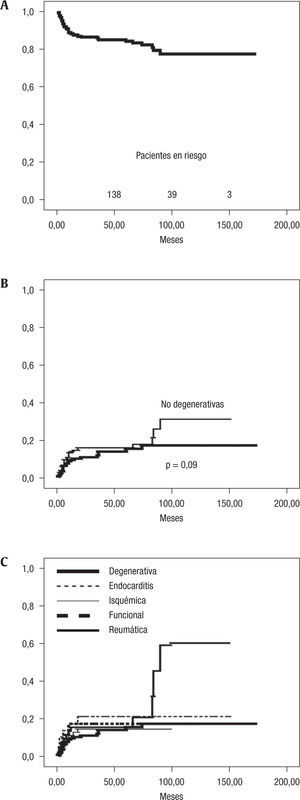
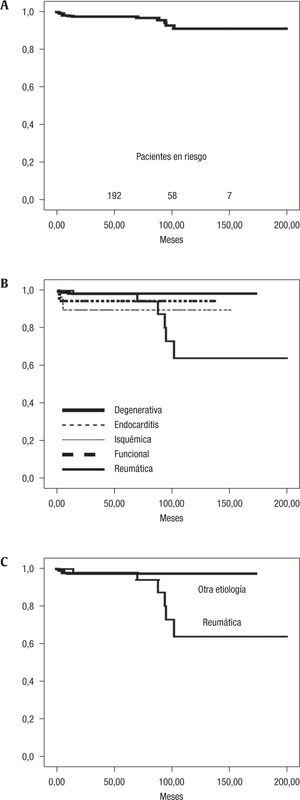
La ausencia de insuficiencia mitral grado 3–4 a los 5 y 10 años fue de 84±2% y 77±3% (fig. 1A). La mayor durabilidad de la reparación valvular se obtuvo en la valvulopatía degenerativa frente a otras causas, especialmente en seguimiento tardío, siendo la ausencia de insuficiencia mitral grado 3–4 en los 5 primeros años de seguimiento de 86±2% versus 84±2% (p=0,46) en degenerativas versus no degenerativas y de 82±3% versus 54±1% (p=0,02), posteriormente. En las figuras 1B y 1C se representa la recidiva de insuficiencia mitral grado 3–4 en la valvulopatía degenerativa frente a la no degenerativa y desglosada según los 5 grupos estudiados. Destaca la mayor tasa de recidiva en el grupo R a partir del seguimiento medio-tardío.
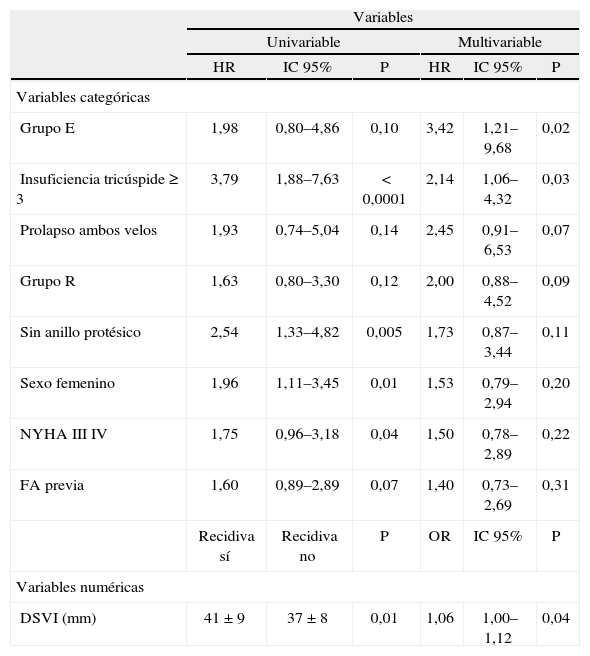
Factores predictores de recidivaDurante el seguimiento, un subgrupo de 57 pacientes presentaron recidiva de insuficiencia mitral grado 3–4 y fueron comparados con los restantes pacientes. Entre ellos existía una mayor frecuencia de mujeres (p<0,05), una mayor frecuencia de grado funcional NYHA III-IV (p<0,05) y especialmente de insuficiencia tricuspídea de grado 3 o mayor (p<0,0001). En este subgrupo de pacientes, el diámetro telesistólico del ventrículo izquierdo también fue mayor (p<0,05) y se observó una tendencia a una mayor prevalencia de fibrilación auricular preoperatoria (tabla 4). Comparado con los pacientes sin recidiva, en un mayor número de estos pacientes no se había empleado anillo protésico (p<0,01). En el análisis multivariante (regresión de Cox) solo alcanzaron significación estadística como predictores de recidiva de insuficiencia mitral grado 3–4 la presencia preoperatoria de insuficiencia tricuspídea grado 3–4 (p<0,05) y un mayor diámetro telesistólico ventricular (p<0,05). El prolapso de ambos velos se acercó a la significación estadística. Respecto a la etiología de base, el grupo R se asoció de forma estadísticamente significativa a recidiva de grado 3 (odds ratio: 1,98, intervalo de confianza 95%: 1,01–3,89; p=0,05) y especialmente de grado 4 (odds ratio: 3,31, intervalo de confianza 95%: 1,17–9,32; p=0,02) en el análisis univariable, estando próximo a la significación en el modelo multivariado (p=0,09). El grupo E sí fue un factor significativo en dicho modelo (tabla 4).
Predictores de recidiva de insuficiencia mitral grado 3–4.
| Variables | ||||||
| Univariable | Multivariable | |||||
| HR | IC 95% | P | HR | IC 95% | P | |
| Variables categóricas | ||||||
| Grupo E | 1,98 | 0,80–4,86 | 0,10 | 3,42 | 1,21–9,68 | 0,02 |
| Insuficiencia tricúspide ≥ 3 | 3,79 | 1,88–7,63 | < 0,0001 | 2,14 | 1,06–4,32 | 0,03 |
| Prolapso ambos velos | 1,93 | 0,74–5,04 | 0,14 | 2,45 | 0,91–6,53 | 0,07 |
| Grupo R | 1,63 | 0,80–3,30 | 0,12 | 2,00 | 0,88–4,52 | 0,09 |
| Sin anillo protésico | 2,54 | 1,33–4,82 | 0,005 | 1,73 | 0,87–3,44 | 0,11 |
| Sexo femenino | 1,96 | 1,11–3,45 | 0,01 | 1,53 | 0,79–2,94 | 0,20 |
| NYHA III IV | 1,75 | 0,96–3,18 | 0,04 | 1,50 | 0,78–2,89 | 0,22 |
| FA previa | 1,60 | 0,89–2,89 | 0,07 | 1,40 | 0,73–2,69 | 0,31 |
| Recidiva sí | Recidiva no | P | OR | IC 95% | P | |
| Variables numéricas | ||||||
| DSVI (mm) | 41±9 | 37±8 | 0,01 | 1,06 | 1,00–1,12 | 0,04 |
DSVI: diámetro sistólico de ventrículo izquierdo; FA: fibrilación auricular; IC: intervalo de confianza; NYHA: New York Heart Association; OR: odds ratio.
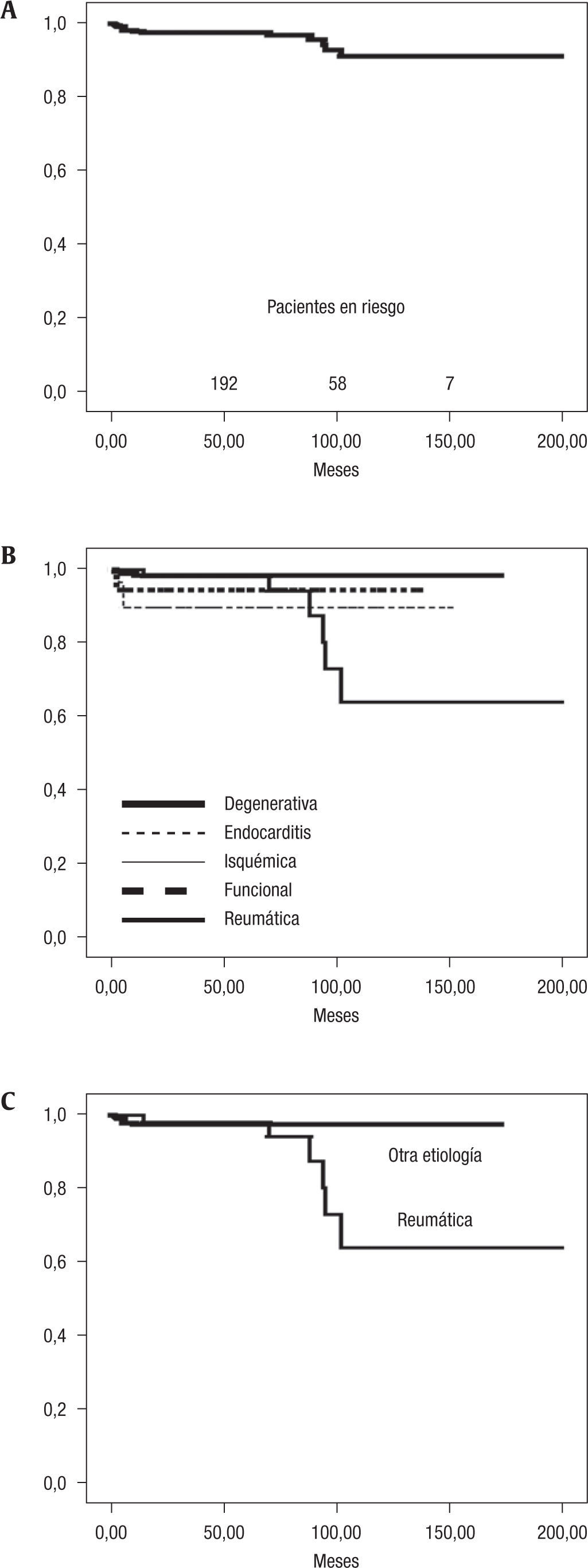
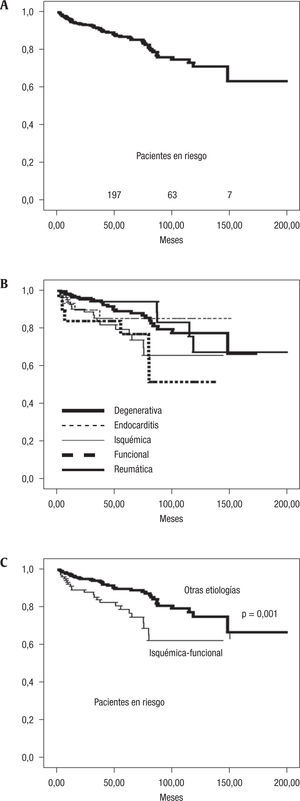
Catorce pacientes fueron reoperados durante el seguimiento y en todos se realizó sustitución valvular protésica. La ausencia de reoperación en el grupo global a 5 y 10 años fue del 97±0,7% y 91±2,9% (fig. 2A). En el grupo de degenerativas se reoperaron 3 pacientes por causas atribuibles a la técnica quirúrgica: SAM (primer mes), desgarro sliding plasty (quinto mes) y dehiscencia anillo (décimo mes). En los 2 grupos con insuficiencia mitral funcional las reoperaciones fueron precoces (durante los primeros 6 meses): recidiva de insuficiencia mitral en una valvulopatía isquémica (quinto mes), endocarditis en una funcional (segundo mes). En los grupos de valvulopatía reumática y endocarditis, las reoperaciones fueron más tardías: 6 pacientes en grupo R y 3 pacientes en grupo E. Especialmente en la reumática, el número de pacientes reoperados fue mayor, concentrándose estas nuevas intervenciones en el seguimiento medio entre 70 y 100 meses. La ausencia de reoperación desglosada por grupos y comparando la valvulopatía reumática con el resto se representa en las figuras 2B y 2C.
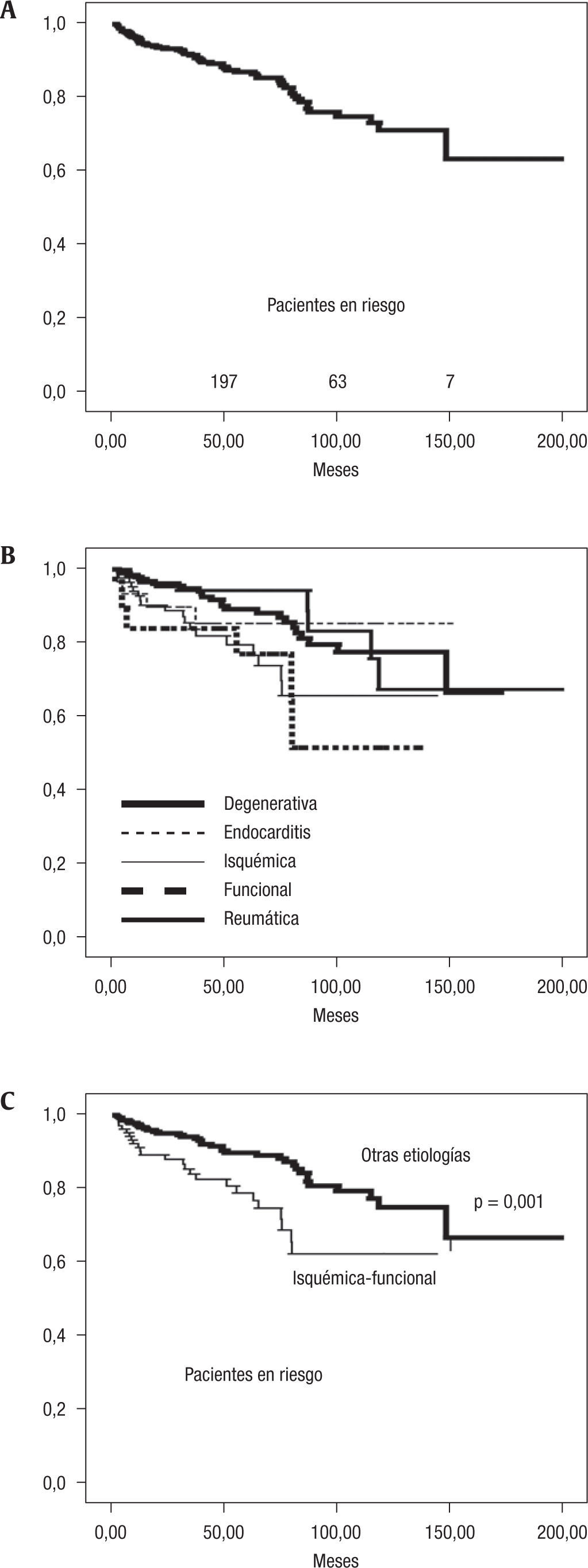
Supervivencia y evolución clínicaEl seguimiento medio de los pacientes del estudio fue de 58±40 meses (rango: 3–174 meses), representando un total de 1.882 años-paciente. La supervivencia actuarial del grupo global a 5 y 10 años fue de 86±1% y 70±4% (fig. 3A). La mortalidad global al final del seguimiento fue mayor en la insuficiencia mitral fun cional isquémica y no isquémica 20,0 y 31,6%. En los grupos D, R y E dicha mortalidad fue: 12,3, 11,5 y 13,3% (en las figuras 3B y 3C se representa la supervivencia actuarial desglosada según los 5 grupos estudiados y según el origen funcional o no de la insuficiencia mitral).
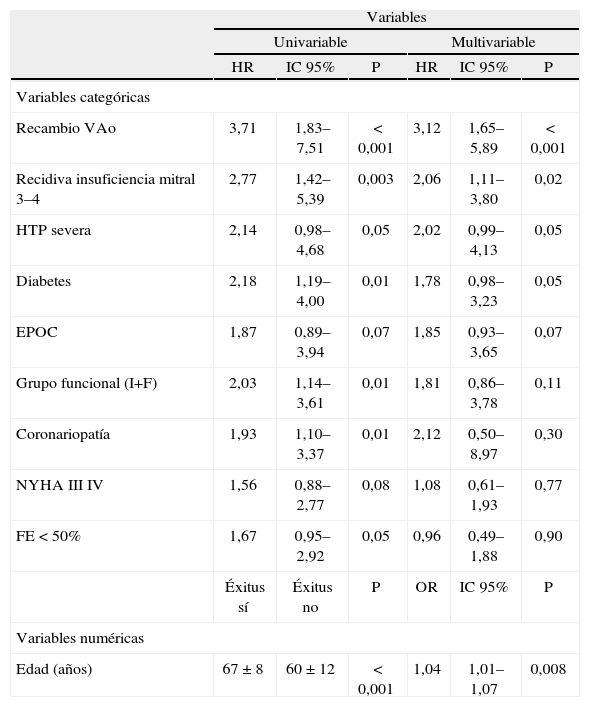
En la tabla 5 se recogen los principales factores predictores de mortalidad tardía. Entre ellos destacaron la edad (p<0,01), el recambio valvular aórtico asociado (p<0,001) y la presencia de recidiva de insuficiencia mitral grado 3–4 durante el seguimiento (p<0,05).
Predictores de mortalidad tardía.
| Variables | ||||||
| Univariable | Multivariable | |||||
| HR | IC 95% | P | HR | IC 95% | P | |
| Variables categóricas | ||||||
| Recambio VAo | 3,71 | 1,83–7,51 | < 0,001 | 3,12 | 1,65–5,89 | < 0,001 |
| Recidiva insuficiencia mitral 3–4 | 2,77 | 1,42–5,39 | 0,003 | 2,06 | 1,11–3,80 | 0,02 |
| HTP severa | 2,14 | 0,98–4,68 | 0,05 | 2,02 | 0,99–4,13 | 0,05 |
| Diabetes | 2,18 | 1,19–4,00 | 0,01 | 1,78 | 0,98–3,23 | 0,05 |
| EPOC | 1,87 | 0,89–3,94 | 0,07 | 1,85 | 0,93–3,65 | 0,07 |
| Grupo funcional (I+F) | 2,03 | 1,14–3,61 | 0,01 | 1,81 | 0,86–3,78 | 0,11 |
| Coronariopatía | 1,93 | 1,10–3,37 | 0,01 | 2,12 | 0,50–8,97 | 0,30 |
| NYHA III IV | 1,56 | 0,88–2,77 | 0,08 | 1,08 | 0,61–1,93 | 0,77 |
| FE < 50% | 1,67 | 0,95–2,92 | 0,05 | 0,96 | 0,49–1,88 | 0,90 |
| Éxitus sí | Éxitus no | P | OR | IC 95% | P | |
| Variables numéricas | ||||||
| Edad (años) | 67±8 | 60±12 | < 0,001 | 1,04 | 1,01–1,07 | 0,008 |
EPOC: enfermedad pulmonar obstructiva crónica; FE: fracción de eyección; HTP: hipertensión pulmonar; IC: intervalo de confianza; NYHA: New York Heart Association; VAo: válvula aórtica: OD: odds ratio.
De los 328 supervivientes, al final del seguimiento, 302 pacientes (92,1%) estaban en grado funcional NYHA I-II. El resto de pacientes estaban en grado funcional NYHA III: 9 (5,2%), 8 (11,7%), 3 (23,1%), 5 (10,0%) y 1 (3,8%) en los grupos respectivos. Treinta pacientes estaban en fibrilación auricular al final del seguimiento: 7 (4,1%), 10 (14,7%), 6 (46,1%), 6 (12,0%) y 1 (3,8%) pacientes en los grupos respectivos. El tratamiento anticoagulante se mantuvo en todos ellos.
DiscusiónEn términos generales, la reparación valvular mitral se considera la operación de elección en la insuficiencia mitral1. Diversos estudios han demostrado que la reparación valvular permite reducir el riesgo de eventos tromboembólicos y la necesidad de anticoagulación crónica comparada con la sustitución valvular protésica11. También se ha logrado una durabilidad excelente a largo plazo, una reducción del riesgo de endocarditis y una mejora en la supervivencia12. Sin embargo, es necesario tener presente que alguno de estos estudios parte de limitaciones metodológicas derivadas de la heterogeneidad de etiologías y lesiones responsables de la insuficiencia mitral. Por tanto, es de gran importancia determinar con exactitud la causa y las lesiones responsables de la insuficiencia valvular y considerar las técnicas concretas de reparación empleadas en cada paciente.
En nuestra práctica clínica actual, la valvulopatía mitral degenerativa representa la causa más frecuente de insuficiencia mitral que precisa de cirugía. Esta etiología permite una reparación valvular eficaz y duradera en un alto porcentaje de pacientes, logrando en aquellos con función ventricular conservada y estadio clínico no avanzado una supervivencia similar a la estimada en la población general (tras ajuste por edad y sexo)12. Este hecho ha favorecido la indicación quirúrgica precoz en pacientes con insuficiencia mitral severa que se encuentran asintomáticos y con preservación de la función ventricular, siempre que la reparación valvular sea altamente probable.13 Frente a esta estrategia de cirugía precoz se encuentra aquella otra que aboga por esperar, bajo estrecha vigilancia clínica y ecocardiográfica, la aparición de los primeros signos de disfunción o dilatación ventricular, hipertensión pulmonar o fibrilación auricular recurrente14.
Sin embargo, existen múltiples factores que pueden influir en los resultados, entre ellos la propia etiología. Por esta razón, no podemos generalizar sin tener en cuenta todo el espectro etiológico de la insuficiencia valvular mitral. En general, las tasas de reparación y durabilidad son inferiores en la valvulopatía mitral reumática, lo que implica una mayor tasa de reoperaciones15. Además, en la insuficiencia mitral funcional (isquémica o no) hay que considerar una historia natural de la cardiopatía de base distinta con unos resultados de supervivencia posquirúrgica inferiores. En estos pacientes, la insuficiencia mitral es secundaria a una enfermedad ventricular o miocardiopatía dilatada y, en sí misma, confiere un mayor riesgo de mortalidad a esta miocardiopatía de base16. Aunque el tratamiento quirúrgico convencional es la anuloplastia sobrecorrectora, sin otras técnicas asociadas de reparación compleja, la recidiva precoz secundaria al remodelado progresivo del ventrículo es una limitación frecuente.
Según un reciente estudio17 que analiza retrospectivamente los resultados de 4 décadas de experiencia en reparación valvular mitral, se demuestra que la etiología es un poderoso factor determinante de la supervivencia y durabilidad de la reparación valvular. La mayor parte de pacientes con valvulopatía reumática que sobrevivió más de 20 años precisó reoperación, mientras que aquellos pacientes diagnosticados de insuficiencia mitral funcional presentaron la mayor tasa de mortalidad precoz y a largo plazo junto con la menor ausencia de reoperación. Por el contrario, la reparación en la valvulopatía mixomatosa degenerativa mostró la mejor durabilidad, con un elevado número de pacientes libres de reoperación a los 30 años de seguimiento.
En nuestra experiencia, los resultados globales de la cirugía reparadora han sido satisfactorios; pero los resultados en supervivencia, tasa de recidiva y reoperación fueron particularmente excelentes en la valvulopatía degenerativa. En las otras etiologías, los resultados fueron inferiores, con una menor durabilidad en el caso de la reumática y una menor supervivencia a largo plazo en la etiología funcional.
Pero aparte de la etiología, existen otros múltiples factores asociados a una menor durabilidad de la reparación y que pueden ser considerados como predictores de recidiva de la insuficiencia mitral. En la valvulopatía degenerativa, el tipo de enfermedad (la enfermedad de Barlow frente a la deficiencia fibroelástica)18, la extensión y tipo de lesiones, el velo afectado (posterior, anterior o ambos)19 o la propia técnica quirúrgica20 pueden ser importantes determinantes de los resultados quirúrgicos. El prolapso aislado de velo posterior en la insuficiencia mitral degenerativa suele ofrecer las máximas garantías de reparación exitosa. En cambio, la afectación del velo anterior o de ambos velos junto con otros tipos de patología como la reumática, isquémica-funcional o la endocarditis ofrecen unos resultados más inciertos. En un reciente estudio sobre cirugía reparadora en la valvulopatía degenerativa21, el principal mecanismo de recurrencia de la insuficiencia mitral fue la degeneración progresiva de la válvula mitral, especialmente con engrosamiento de los velos y prolapso, en particular en aquellos pacientes con prolapso del velo anterior. Un grupo menor de pacientes presentó recurrencia y necesidad de reoperación por causas relacionadas con la técnica quirúrgica.
En nuestro caso, en el grupo D se reoperaron 3 pacientes durante el primer año posquirúrgico por causas atribuibles a la técnica quirúrgica. Posteriormente, a lo largo de nuestro seguimiento, no se realizaron nuevas reoperaciones en este grupo. Entre los predictores significativos de recidiva de regurgitación mitral grado 3–4 hemos encontrado el aumento del diámetro telesistólico del ventrículo izquierdo y la presencia de insuficiencia tricuspídea de grado ≥ 3. Ambos factores pueden reflejar una insuficiencia mitral funcional en el seno de una miocardiopatía o un estadio avanzado de la valvulopatía mitral. Respecto a otros factores, el prolapso de ambos velos se acercó a la significación estadística en el análisis multivariable. Generalmente, la reparación de un prolapso aislado de velo anterior es más difícil que el prolapso del velo posterior, pero el empleo de neocuerdas o la transposición de cuerdas han ofrecido resultados satisfactorios. En cambio, el prolapso de ambos velos precisa de mejoras en la técnica quirúrgica al no disponer de un velo posterior conservado como referencia en la medición de neocuerdas o como donante en la transferencia de cuerdas. El acortamiento de cuerdas y el no empleo de sliding plasty o de anuloplastia con anillo han sido factores técnicos determinantes de recidiva según la literatura publicada, pero en nuestro caso no han sido relevantes. El no empleo de anillo protésico se asoció a mayor recidiva solo en el análisis univariable, y el acortamiento de cuerdas no se realizó en ningún paciente. En nuestra experiencia, el empleo de anuloplastia con anillo (o banda) ha sido una práctica habitual, salvo en la endocarditis y en algunos pacientes reumáticos. La incidencia de enfermedad de Barlow en nuestros pacientes ha sido muy inferior a la incidencia de deficiencia fibroelástica (29,6 vs. 70,4%) y, por tanto, la necesidad de asociar sliding plasty ha sido poco frecuente.
Las reoperaciones en las insuficiencias mitrales funcionales fueron también precoces, debido a recidiva precoz por remodelado ventricular progresivo (un paciente en el grupo I) y por endocarditis (un paciente en el grupo F). Aunque estas insuficiencias funcionales, principalmente las isquémicas, son fáciles de reparar con una simple anuloplastia, la recidiva ha sido un problema frecuente en las series publicadas, alcanzando casi el 30%. Suele ser consecuencia del remodelado progresivo del ventrículo22. Otras técnicas asociadas a la anuloplastia pueden mejorar estos resultados23,24. De cualquier forma, se precisan nuevos estudios que determinen el impacto de la reparación en la recidiva de la insuficiencia mitral funcional, en la función ventricular y en la supervivencia de estos pacientes. En nuestra propia experiencia, la tasa de recidiva obtenida en la insuficiencia mitral isquémica y funcional no superó el 20%, lo que mejora los resultados publicados por algunos grupos quirúrgicos. No disponemos de datos suficientes para explicar convenientemente estos resultados, pues se trata de un subgrupo pequeño de pacientes en los que se ha implantado una diversidad de anillos protésicos. En la mayoría de pacientes con etiología isquémica se implantó una banda o anillo completo con una sobrecorrección de 1 o 2 tamaños. En un subgrupo se implantaron anillos específicos para el remodelado del anillo nativo (McCarthy-Edwards IMR ETIlogix o Geoform en 16 y 4 pacientes, respectivamente) y en otros 6 pacientes se realizó plicatura selectiva de la escara ventricular identificada preoperatoriamente con resonancia magnética nuclear cardíaca. En la gran mayoría de pacientes se completó la cirugía con una revascularización miocárdica completa.
Respecto a las otras etiologías y según nuestra experiencia, las reoperaciones en valvulopatía reumática y endocarditis fueron más tardías y como consecuencia de la progresión del proceso valvular reumático (fibrosis y calcificación progresivas) o por el deterioro estructural progresivo de la válvula endocardítica o del pericardio empleado en su reconstrucción. En el grupo reumático hemos observado la mayor tasa de recidiva y reoperación. Igualmente, según la experiencia aportada por distintos estudios, en la patología reumática se ha observado una mayor tasa de reoperación15. En la endocarditis, la reparación permite disminuir el riesgo de nueva infección valvular, pero en ocasiones el daño estructural avanzado de la válvula hace imposible dicha reparación. En este sentido, algunos autores abogan por una cirugía precoz de la endocarditis aguda como garantía de una óptima reparación mitral25.
La mayor mortalidad hospitalaria afectó especialmente a los grupos de mayor riesgo: isquémica, funcional y endocarditis. De acuerdo con la literatura, estas etiologías de insuficiencia mitral tienen un mayor riesgo de mortalidad temprana y a medio-largo plazo que la valvulopatía de origen degenerativo7,16,25. Pese a ello, los pacientes con insuficiencia mitral isquémica y funcional de nuestro estudio, aunque más sintomáticos al final del seguimiento, presentaron una buena supervivencia posterior durante el período estudiado. Si bien, dicha supervivencia fue significativamente menor que en el global de los otros grupos a lo largo del seguimiento. Es importante reseñar que estos pacientes presentaban, preoperatoriamente, una mayor disfunción ventricular sistólica que otros grupos. Entre los predictores de mortalidad tardía encontramos la edad, el recambio valvular aórtico asociado y la presencia de recidiva de insuficiencia mitral grado 3–4 durante el seguimiento. En cambio, una fracción de eyeccion < 50% preoperatoria no alcanzó significación estadística.
ConclusionesPodemos concluir que la reparación mitral en un grupo variado de pacientes con diferente etiología ha ofrecido unos buenos resultados en cuanto a supervivencia. Los resultados técnicos en términos de ausencia de insuficiencia mitral significativa posquirúrgica y tasa de reoperación fueron satisfactorios en aquellos pacientes con valvulopatía degenerativa. Respecto a otras etiologías, la reumática se asoció a una menor durabilidad aunque, en general, la necesidad de reoperación ha sido poco frecuente. La valvulopatía isquémica y funcional mostraron la menor supervivencia tardía en probable relación con el peor pronóstico de la miocardiopatía de base. Una correcta selección de los pacientes y una elección individualizada de la técnica quirúrgica han podido ser determinantes en la obtención de estos resultados.
Limitaciones del estudioVarias limitaciones del estudio deben ser consideradas al analizar los resultados. Se trata de un estudio retrospectivo, no randomizado y desarrollado en un solo centro hospitalario, por lo que el análisis está sujeto al sesgo de selección propio de este tipo de estudios. El tamaño de la cohorte estudiada es reducido, especialmente si consideramos los diferentes subgrupos. De cualquier forma, el seguimiento clínico y ecocardiográfico ha sido completo durante el primer año y se han realizado ecocardiografías seriadas en un alto número de pacientes más allá del año. Puede añadir interés al estudio el hecho de que la serie de pacientes presentada es representativa de la cirugía reparadora mitral de nuestro entorno.