En pacientes pediátricos puede ser necesario corregir la lesión valvular del tracto de salida del ventrículo derecho, secuela de la reparación primaria de su cardiopatía congénita.
ObjetivoComparar resultados de yugular bovina (YB)-Contegra® versus prótesis porcina (PPP), implantadas en pacientes menores de 18 años.
MétodosTodos los menores de 18 años, reintervenidos entre enero del 2003-junio del 2015 para valvular la vía de salida derecha con una YB/PPP, tras reparación previa de su cardiopatía. Criterios de disfunción protésica: reintervención quirúrgica/percutánea, gradiente > 50mmHg, insuficiencia protésica severa. Análisis estadístico: SPSS 20.0.
ResultadosVeintiuna PPP/20 pacientes, 15 YB/15 pacientes. Varones 60%. Cardiopatía de base más frecuente: Fallot. Grupos no exactamente homogéneos. De 24 variables preoperatorias, en 11 hubo diferencias estadísticamente significativas (p<0,05), destacando: mayor porcentaje de cirugía transanular, indicación por insuficiencia pulmonar, dilatación y disfunción ventricular en grupo PPP.
De 15 variables perioperatorias, hubo diferencias significativas en: edad media en el implante: 8,8±4,4 años YB versus 11,8±4 PPP (p=0,044); diámetro de válvula/conducto (p<0,001), menor en YB y necesidad de pinzado aórtico (p=0,015), mayor en YB.
No hubo mortalidad hospitalaria ni tardía. Seguimiento: 4,8 años YB versus 2,4 PPP (p=0,046). Gradiente transprotésico, insuficiencia pulmonar residual y disfunción protésica, todas mayores en YB, fueron variables postoperatorias con diferencias significativas.
ConclusiónCon la prudencia que imponen las diferencias en el tiempo de seguimiento y el tipo de cirugía previa en ambas cohortes, parece razonable elegir la PPP para recuperar funcionalidad de la vía de salida derecha en menores.
La YB se reservará para cuando sea imprescindible un conducto.
In some patients, in childhood, it may be necessary to recover the valve function of the right ventricular outflow tract, a sequel of the primary repair of their congenital heart disease.
ObjectiveTo compare the outcomes of bovine jugular (YB) -Contegra® versus porcine prosthesis (PPP), implanted in patients under 18 years old.
MethodsThe study included all patients under 18 years old and re-operated on between January 2003 and June 2015 after primary surgery right ventricle outflow tract, and in whom a YB/PPP was implanted. Prosthetic valve dysfunction criteria were, surgical/percutaneous re-intervention, and a gradient>50mmHg or severe prosthetic regurgitation. Statistical analysis was performed using SPSS 20.0.
ResultsThere were 21 PPP implanted in 20 patients, and 15 YB in 15 patients. The study included 60% males. The most common primary congenital heart disease was Fallot. The groups were not exactly homogeneous. Of the 24 preoperative variables, 11 of them showed statistically significant differences (P<.05). These included a higher percentage of transannular surgery, indication of pulmonary regurgitation surgery, ventricular dilation, and dysfunction in the PPP group.
Of the 15 perioperative variables, there were significant differences in, the mean age at implantation: 8.8±4.4 years YB versus 11.8±4 PPP (P=.044); valve diameter (P<.001) lower in YB. Need of aortic cross clamping (P=.015) however, higher in YB.
There was no in-hospital or late mortality. Follow-up: 4.8 years YB versus 2.4 PPP (P=.046). Other postoperative variables with significant differences: transprosthetic gradient, residual prosthetic regurgitation, prosthetic dysfunction, all higher in YB group.
ConclusionsWith prudence imposed by differences in follow-up time and type of previous surgery in both cohorts, it seems reasonable to choose a PPP to recover functionality of the right ventricle outflow tract.
The YB could be used when a conduit is essential.
El momento y el material a emplear para recuperar la funcionalidad del tracto de salida del ventrículo derecho (TSVD) disfuncionante, por secuela de la reparación primaria de una cardiopatía congénita (CC), son motivo de controversia1. Se han implantado homoinjertos criopreservados2, conductos valvulados heterólogos con3 o sin soporte4, bioprótesis no soportadas y soportadas porcinas5 y de pericardio6, neoválvulas de politetrafluoroetileno expandido montadas artesanalmente dentro de conductos del mismo material7, prótesis mecánicas8, con resultados muy dispares en los distintos estudios.
Parece demostrado, al menos en el caso de las bioprótesis soportadas, que la edad en la que se lleve a cabo el implante condiciona significativamente el posterior resultado en seguimiento, de modo que cuanto más joven es el paciente, menor es la durabilidad del biomaterial9-11.
La tolerancia a la disfunción de la vía de salida derecha es muy variable, pero en algunos casos de importante deterioro de la capacidad funcional, arritmias con repercusión clínica, insuficiencia tricúspide funcional severa asociada, gran dilatación del ventrículo derecho (VD) o compromiso de su función contráctil, parece recomendable implantar una válvula en edad infantil, surgiendo la duda de cuál emplear.
En el presente estudio hemos comparado resultados de prótesis porcinas soportadas en posición pulmonar (PPP), modelos Biocor® (St Jude Medical, Inc., St. Paul, Minnesota) y Mosaic® (Medtronic, Inc., Minneapolis, Minnesota), con el conducto valvulado de yugular bovina (YB) Contegra® (Medtronic, Inc., Minneapolis, Minnesota).
MétodosEstudio retrospectivo de todos los pacientes portadores de CC menores de 18 años, reintervenidos en nuestro servicio por secuela derivada de la cirugía reparadora a nivel del TSVD, a los que se implantó una PPP soportada o un conducto Contegra®, entre el 1 de enero del 2003 y el 31 de mayo del 2015.
Se excluyó a los pacientes en los que la sustitución valvular fue realizada mediante dispositivos diferentes, o si el implante no fue en contexto de reparación biventricular.
En la recogida de datos se respetó la confidencialidad.
El implante de la PPP/YB se realizó mediante esternotomía media, circulación extracorpórea y siempre que fue posible sin isquemia miocárdica.
En el caso de la PPP se utiliza una variante técnica de la «peel operation» descrita por la Clínica Mayo para la reintervención de conductos disfuncionantes12, consistente en la exéresis completa del conducto, la sutura del hemianillo inferior de una bioprótesis porcina al «suelo fibroso» que queda en el infundíbulo del VD tras retirar el conducto, y la sutura del hemianillo superior de la prótesis a un parche de pericardio que soporta a la prótesis y «techa» y reconstruye la continuidad entre VD y arteria pulmonar.
Nuestro grupo ha hecho extensiva dicha técnica a los pacientes que previamente habían sido reparados mediante cirugía transanular, no solo a los recambios de conducto. En lugar de emplear pericardio que es inextensible, utilizamos un parche de YB obtenido de un conducto Contegra® por su mayor flexibilidad y capacidad hemostática.
A la hora de implantar un Contegra®, se realizó la exéresis completa del conducto previo en todos los casos, menos en los que existía una coronaria principal cruzando por debajo del mismo, conservándose el suelo del conducto previo en ese supuesto.
Se determinaron 24 variables preoperatorias, 15 perioperatorias y 16 postoperatorias.
Se consideró seguimiento completo si durante el último año se había revisado al paciente o se le había telefoneado si era seguido fuera de nuestro hospital, o si había fallecido durante el seguimiento.
Se estudió la incidencia de endocarditis protésica y sus consecuencias en cuanto a necesidad de reintervención y/o mortalidad.
Se definió disfunción protésica como: necesidad de sustitución de la prótesis mediante nuevo procedimiento quirúrgico/percutáneo, o presencia de un gradiente ecocardiográfico pico superior a 50mmHg, o existencia de insuficiencia protésica pulmonar severa.
Se analizaron la evolución de los volúmenes y la función del VD de aquellos pacientes de los que se disponía de resonancia magnética pre y postoperatoria.
Análisis estadístico con SPSS20.0 para Windows (SPSS inc. Chicago, Illinois, EE. UU.). Las variables cuantitativas se expresan como media±desviación estándar o como mediana y rango intercuartílico. Las variables cualitativas se expresan en valores absolutos y/o porcentaje en relación con el número total de pacientes o de procedimientos.
Para evaluar diferencias por tipo de implante, en variables cuantitativas se usó la prueba de la U de Mann-Whitney, por ser las muestras menores de 30 casos. En variables categóricas se usó la prueba exacta de Fisher.
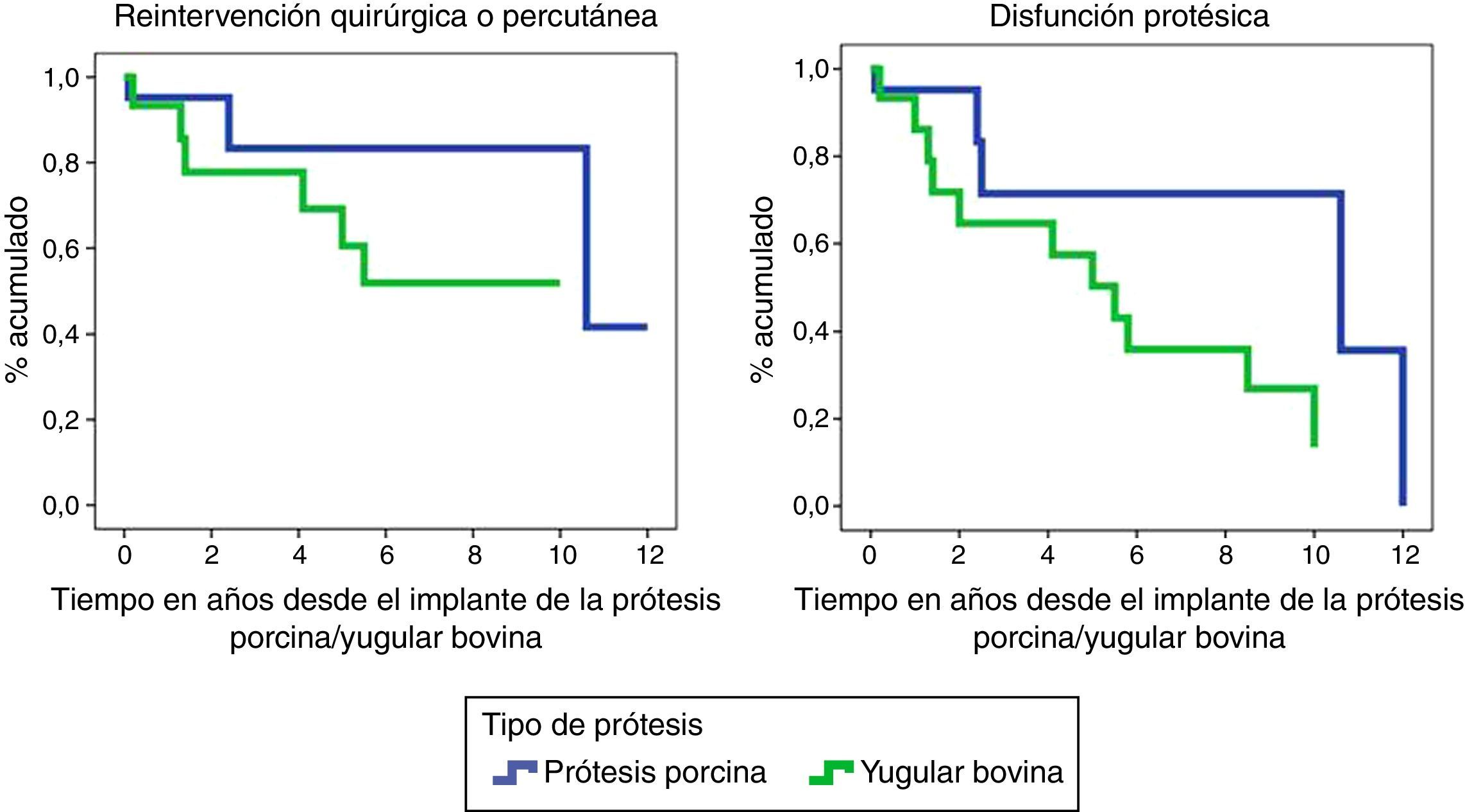
Se construyeron curvas de supervivencia de ocurrencia de evento quirúrgico/percutáneo sobre la PPP/YB y de disfunción protésica. Además, se empleó la prueba de Log-Rank para evaluar si existían diferencias entre ambas cohortes.
ResultadosSe implantaron 21 PPP en 20 pacientes (uno se reintervendría sustituyendo una bioprótesis infectada durante el seguimiento por otra nueva bioprótesis) y 15 YB en otros 15 enfermos.
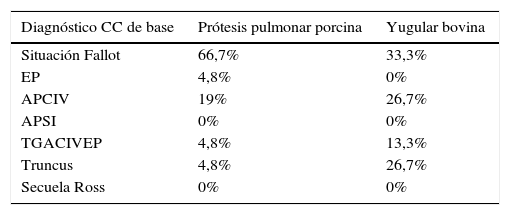
Predominaron los varones (60% YB versus 53,1% PPP). El diagnóstico de CC de base más frecuente fue la situación Fallot, con importante predominio en el grupo PPP. El resto de diagnósticos se recogen en la tabla 1. En cualquier caso, las diferencias por cardiopatía de base no resultaron estadísticamente significativas.
Cardiopatía congénita de base
| Diagnóstico CC de base | Prótesis pulmonar porcina | Yugular bovina |
|---|---|---|
| Situación Fallot | 66,7% | 33,3% |
| EP | 4,8% | 0% |
| APCIV | 19% | 26,7% |
| APSI | 0% | 0% |
| TGACIVEP | 4,8% | 13,3% |
| Truncus | 4,8% | 26,7% |
| Secuela Ross | 0% | 0% |
APCIV: atresia pulmonar con comunicación interventricular; APSI: atresia pulmonar con septo intacto; EP: estenosis pulmonar; TGACIVEP: transposición con comunicación interventricular y estenosis pulmonar.
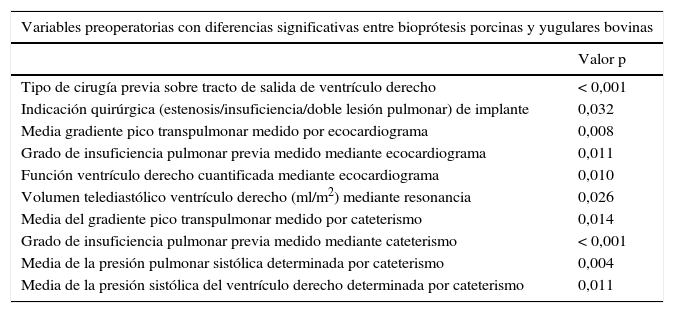
La tabla 2 recoge las variables preoperatorias con diferencias estadísticamente significativas entre ambas cohortes. Destacamos «tipo de cirugía realizado sobre la vía de salida derecha antes del implante de la PPP/YB»: los Contegra® fueron todos implantados como recambio de otro conducto previo. No así las PPP, que se implantaron mayoritariamente sobre TSVD ampliados con parche transanular. En cuanto a la «indicación quirúrgica de implante de PPP/YB» los Contegra® se pusieron sobre vías de salida de VD con más predominio de estenosis o doble lesión pulmonar.
Variables preoperatorias con diferencias estadísticamente significativas entre bioprótesis porcinas y yugulares bovinas
| Variables preoperatorias con diferencias significativas entre bioprótesis porcinas y yugulares bovinas | |
|---|---|
| Valor p | |
| Tipo de cirugía previa sobre tracto de salida de ventrículo derecho | < 0,001 |
| Indicación quirúrgica (estenosis/insuficiencia/doble lesión pulmonar) de implante | 0,032 |
| Media gradiente pico transpulmonar medido por ecocardiograma | 0,008 |
| Grado de insuficiencia pulmonar previa medido mediante ecocardiograma | 0,011 |
| Función ventrículo derecho cuantificada mediante ecocardiograma | 0,010 |
| Volumen telediastólico ventrículo derecho (ml/m2) mediante resonancia | 0,026 |
| Media del gradiente pico transpulmonar medido por cateterismo | 0,014 |
| Grado de insuficiencia pulmonar previa medido mediante cateterismo | < 0,001 |
| Media de la presión pulmonar sistólica determinada por cateterismo | 0,004 |
| Media de la presión sistólica del ventrículo derecho determinada por cateterismo | 0,011 |
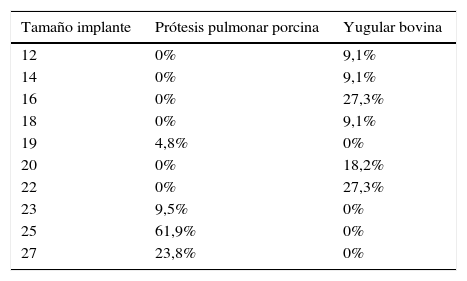
En cuanto a las variables perioperatorias con diferencias estadísticamente significativas, la edad media de implante fue de 8,8±4,4 años para las YB y de 11,8±4 para las PPP (p=0,044); los diámetros de los implantes (tabla 3) son mayores en el caso de las PPP (p<0,001), mientras que la necesidad de pinzado aórtico fue mayor en el caso de las YB (p=0,015). La más frecuentemente implantada en el caso de las PPP fue la número 25. En el caso de las YB, los conductos más empleados fueron los de 16 y 22mm de diámetro.
Los modelos de prótesis implantados fueron 3 Biocor® (St Jude Medical, Inc., St. Paul, Minnesota) y 18 Mosaic® (Medtronic, Inc., Minneapolis, Minnesota). No se analizaron posibles diferencias en cuanto a disfunción protésica entre ambos modelos por ser muy escasa la cantidad en el caso de las Biocor® y además ser las más antiguas de la serie.
El seguimiento es completo, media de 4,8±3,7 años para las YB versus 2,4±3,1 para las PPP. Las diferencias son estadísticamente significativas (p=0,046).
Durante el período de seguimiento no ha fallecido ningún paciente.
La reintervención quirúrgica o percutánea sobre el implante en el TSVD, variable que condiciona disfunción del dispositivo y fin de seguimiento del caso, ocurrió en 6 (40%) de los 15 casos de implante de Contegra®, 4 tratados de forma quirúrgica y 2 mediante implante de prótesis percutánea dentro de la YB.
En cuanto a las PPP, se produjo en 3 (14,2%) de las 21. A pesar de una clara tendencia a reintervenir más las YB, las diferencias entre las PPP y los Contegra® no resultaron estadísticamente significativas.
La disfunción en seguimiento, un criterio más exigente que la reintervención quirúrgica/percutánea, en los Contegra® se ha producido en los 6 casos descritos en el apartado anterior (4 quirúrgicos+2 percutáneos) además de otros 2 cuyo gradiente transprotésico es actualmente superior a 50mmHg y uno más que presenta insuficiencia pulmonar intraprotésica severa. En total 9 (60%) entre las 15 YB, durante su período de seguimiento, han disfuncionado.
Las bioprótesis porcinas soportadas han disfuncionado 5 (23,8%): 2 reintervenidas quirúrgicamente por endocarditis protésica, una de forma percutánea a los 10 años de implantada por doble lesión intraprotésica y 2 más que sin haber sido aún reintervenidas, presentan gradientes pico superiores a 50mmHg.
Las diferencias en cuanto a disfunción protésica entre PPP y YB resultaron estadísticamente significativas (p=0,006). Disfuncionaron más los Contegra®.
Endocarditis protésica: se registraron 3 (20%) casos entre los 15 implantes de YB, mientras que entre las PPP se han producido 2 (9,5%). Las diferencias entre PPP y YB no resultaron estadísticamente significativas en cuanto a endocarditis. En el caso de las YB, se trató de 2 episodios de endocarditis fúngica protésica tardía por Aspergillus y otro de endocarditis bacteriana protésica tardía; todos requirieron reintervención quirúrgica y se resolvieron de la siguiente forma: de las 2 fúngicas por Aspergillus, en una se recambió el Contegra® por un conducto no valvulado, resolviéndose. En la otra se recambió mediante una Biocor® con peel operation, que se recoge también en el grupo de las bioprótesis. Esta válvula porcina también se reinfectaría y necesitaría ser sustituida finalmente por un conducto de Dacron® no valvulado. La endocarditis bacteriana sobre el tercer Contegra® se resolvió recambiándolo quirúrgicamente por otro conducto de Dacron® no valvulado.
En el caso de las PPP ocurrieron 2 episodios: la endocarditis protésica precoz por Aspergillus explicada anteriormente tras el recambio de un Contegra® por una Biocor®, que también se reinfectaría y se sustituiría finalmente por un conducto de Dacron®, y un episodio de endocarditis bacteriana protésica tardía sobre una Mosaic®, que se reemplazó por otra Mosaic®.
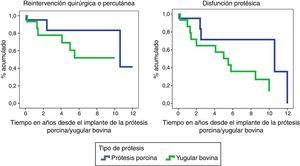
Las funciones de supervivencia de necesidad de reintervención quirúrgica/percutánea y de disfunción protésica (fig. 1) apuntan hacia un mejor funcionamiento de las PPP a lo largo del tiempo, pero sin resultar las diferencias entre ambas cohortes estadísticamente significativas.
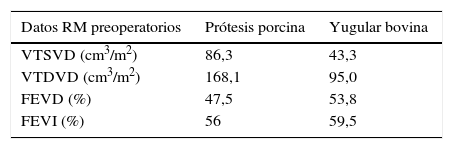
Los datos de resonancia magnética posquirúrgica (tabla 4) indican que tanto las YB como las PPP consiguen el objetivo de recuperar los volúmenes telesistólico y telediastólico del VD postoperatorios, y de mantener su fracción de eyección sin deterioro con respecto al preoperatorio.
Medidas de resonancia magnética pre y postoperatorias
| Datos RM preoperatorios | Prótesis porcina | Yugular bovina |
|---|---|---|
| VTSVD (cm3/m2) | 86,3 | 43,3 |
| VTDVD (cm3/m2) | 168,1 | 95,0 |
| FEVD (%) | 47,5 | 53,8 |
| FEVI (%) | 56 | 59,5 |
| Datos RM postoperatorios | Prótesis porcina | Yugular bovina |
|---|---|---|
| VTSVD (cm3/m2) | 41,8 | 38,5 |
| VTDVD (cm3/m2) | 89,8 | 86 |
| FEVD (%) | 46,4 | 54,2 |
| FEVI (%) | 51,2 | 57,4 |
FEVD: fracción de eyección del ventrículo derecho; FEVI: fracción de eyección del ventrículo izquierdo; RM: resonancia magnética; VTDVD: volumen telediastólico del ventrículo derecho; VTSVD: volumen telesistólico del ventrículo derecho.
Hasta nuestro conocimiento, no existe comparativa en la literatura entre el Contegra® y las bioprótesis porcinas soportadas para solucionar la disfunción del TSVD, secuela de la reparación primaria de una CC.
En cuanto al uso de bioprótesis soportadas para dicha finalidad, existen básicamente 2 alternativas: las porcinas y las de pericardio. Son múltiples los trabajos defendiendo el empleo de unas u otras. Nuestro grupo optó, hace ya 18 años, por las bioprótesis porcinas de tamaño grande, implantándolas inicialmente en adultos, habiendo sido probablemente la mejor alternativa, tal y como concluyen Abbas y Hoschtitzky13 en su revisión de la literatura en busca de la mejor evidencia científica: «en general, y en estudios con seguimientos medios que apenas alcanzan 5 años, las prótesis porcinas parecen funcionar mejor que las de pericardio, pero está por demostrar que estos resultados perduren en seguimientos más prolongados».
En cuanto al empleo de la YB para recuperar la funcionalidad del TSVD, en la mayoría de los estudios la comparativa se realiza con los homoinjertos criopreservados, con resultados dispares14-16 pero con tendencia global a una disminución del empleo de homoinjertos por su menor disponibilidad, su precio más elevado y por su posibilidad de sensibilización inmunológica.
Probablemente, el Contegra® es la mejor opción (o al menos la menos mala) cuando es necesario usar un conducto valvulado entre el VD y la arteria pulmonar, especialmente en niños pequeños. Ha sido también la elección de nuestro grupo quirúrgico en esa situación. La YB prácticamente ha monopolizado el mercado de las alternativas: así, el xenoinjerto Tissuemed™ (raíz aórtica porcina fijada con glutaraldehído) se ha usado y comparado con Contegra® y homoinjertos criopreservados. Boethig et al.17 reportan resultados de 30 Tissuemed™, 52 homoinjertos y 108 Contegra®. En seguimiento a 4 años, se reoperan más los xenoinjertos porcinos, por problemas estenóticos a todos los niveles; en segundo lugar, los homoinjertos y lo que mejor resultado ofrece es la YB. Otros conductos no soportados han sido el LabCor®-Carbomedics, el Biocor®-St Jude (conducto de pericardio bovino con una válvula aórtica porcina) y el Shelhigh®-Union (conducto de pericardio bovino con una válvula pulmonar porcina). Este último cayó rápidamente en desuso, existiendo también sobre el mismo referencias literarias compartidas con el Contegra® que alertan ante posibles efectos adversos inmunológicos18, o disfunción precoz en relación con su uso en pacientes por debajo de un año de vida19. Recientemente, Schoenhoff et al.20 vuelven a recomendar el uso de YB frente al conducto Shelhigh® de segunda generación por disfunción precoz de este último.
Nuestro porcentaje de disfunción en las YB a lo largo del seguimiento medio de 4,8 años es del 60% frente al 23,8% de las PPP en 2,4 años. En cuanto a los Contegra®, es más elevado que el de otras series, con criterios de disfunción similares o incluso más exigentes que los nuestros, si bien con seguimientos medios más cortos21,22.
Una posible limitación de nuestro trabajo es la falta de homogeneidad entre las 2 cohortes que se comparan, como apuntan las diferencias estadísticamente significativas entre determinadas variables pre y perioperatorias. No obstante, un análisis más detallado de las más trascendentes demuestra que es posible la comparación:
- –
En el caso de la edad media de implante de PPP o YB, lo recogido en la literatura indica que la relación entre la disfunción del Contegra® y la edad de implante es cuando este hecho se produce por debajo del año21 o de los 2 años de vida. El paciente más joven recogido en este trabajo entre a los que se ha implantado una YB tenía 3 años de edad. En las PPP, sí existe evidencia científica firme de que cuanto más joven es el paciente en el que se implanta, mayor es la disfunción en seguimiento tardío, sin existir un punto de corte claro, como ya referimos en la introducción de este estudio.
- –
Tampoco el diámetro de las prótesis lo consideramos un impedimento. De nuevo, lo recogido en la literatura apunta a que la disfunción del Contegra® pueda estar en relación con los diámetros inferiores a 14mm21. El porcentaje de Contegra® de nuestra serie que cumplen esa condición es inferior al 20%. Hemos implantado una amplia mayoría de tamaños grandes. En cuanto a las PPP, el tamaño empleado no parece estar relacionado con un mayor o menor porcentaje de disfunción en seguimiento, al menos en menores de 20 años de edad23.
- –
Tampoco la necesidad o no de pinzar la aorta para implantar la prótesis, en cuanto a más necesidad en el grupo de las YB. En ningún trabajo se recoge que esto sea factor de riesgo de disfunción del Contegra®.
- –
Es cierto que el tiempo medio de seguimiento ha sido significativamente más corto en las PPP que en las YB, pero de forma marginal (p=0,046). Es debido a que estas últimas se pusieron mayoritariamente al inicio de la serie y casi ninguna al final, por la falta de confianza creciente en el material al aumentar la experiencia acumulada. Este dato pareciera restar potencia al estudio, al no ser homogéneo el tiempo de seguimiento, pero probablemente con solo un año más de seguimiento medio las diferencias dejarán de ser estadísticamente significativas.
- –
Sí consideramos de gran importancia el tipo de cirugía previa sobre el TSVD y que obliga a analizar con cautela los resultados obtenidos. En determinados trabajos en los que se realiza análisis multivariante de factores de riesgo de disfunción protésica, el hecho de que el implante se realice en un TSVD en el que existía material protésico previo, es factor de riesgo independiente de disfunción9. Este era el caso de la mayoría de nuestras YB, y de la minoría de nuestras PPP.
Otras diferencias no estadísticamente significativas entre ambas cohortes pero con relevancia clínica son:
- –
Reintervención quirúrgica, más frecuente en las YB (26,7% versus 14,3%). Fiore et al.22 reportan un 11% de reintervenciones relacionadas con el Contegra®. Sekarski et al.21 un 9%. Göber et al.24, un 13% con un tiempo medio de seguimiento de 1,5 años. Las series que solo recogen datos de pacientes mayores de 18 años no necesariamente tienen porcentajes más bajos de reintervención: Boethig et al.17 publican un 15%.
- –
Reintervención percutánea, también mayor en grupo YB (20% versus 9,5%). En este caso, es menor de lo reportado en otras series, siendo además nuestro seguimiento medio más largo. Meyns et al.25 refieren un 29% en seguimiento medio ligeramente inferior a 2 años. Rastan et al.26, un 24,4% en tan solo 2,6 años de seguimiento medio.
- –
Endocarditis protésica, también mayor en el grupo YB (20% versus 9,5%). En todos los casos fue necesario el recambio quirúrgico del conducto. En la literatura reciente son frecuentes y alarmantes las referencias a la endocarditis protésica sobre conductos Contegra®: Albanesi et al.27 reportan un 11,3% en seguimiento mediano de 7,6 años. De 12 casos, 10 necesitaron recambiar el conducto infectado. Ugaki et al.28 comunican un 9,4% frente a un 0,7% de otra cohorte control de homoinjertos, durante un seguimiento mediano de 3,4 años. En su estudio, el implante de un conducto en pacientes de menos de 3 años de edad y el conducto Contegra® fueron factores de riesgo para el desarrollo de endocarditis protésica.
Después del análisis de nuestras 2 cohortes, y a pesar de la diferencia marginalmente significativa en su tiempo de seguimiento medio, nos inclinamos hacia el empleo de la PPP para reconstruir el TSVD previamente operado en menores de 18 años, basándonos en que la disfunción protésica es significativamente mayor en las YB durante el seguimiento, si bien este resultado puede estar condicionado por haberse implantado sobre vías de salida con mayor cantidad de material protésico previo.
La tendencia clínica, sin significación estadística, apunta a una mayor necesidad de reintervención quirúrgica y/o percutánea y a un mayor porcentaje de desarrollo de endocarditis protésica en seguimiento en el caso de las YB.
Reservaremos el uso del Contegra® para situaciones en las que exista completa discontinuidad entre VD y arteria pulmonar, sin «suelo» infundibular, y sea obligatorio el uso de un conducto.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.