Las infecciones sobre dispositivos de electroestimulación cardiaca (DEC) son un problema creciente que requiere de una experiencia y habilidad considerables para su adecuado abordaje terapéutico, que en la mayoría de los casos va a ser la tracción percutánea endovascular (TPE). El objetivo de este trabajo ha sido conocer la situación actual sobre la realización de esta técnica en nuestro país.
Material y métodosEncuesta a nivel nacional enviada a centros españoles con capacidad para la cirugía cardiaca, en la que se preguntaba sobre aspectos relevantes de la extracción de estos dispositivos infectados
ResultadosContestaron la encuesta 33 hospitales, reportando una actividad de alto volumen (> 80 extracciones/año) tan solo dos (6%) y medio volumen (40-60) el 18%. El procedimiento era realizado en su mayoría por cirujanos cardiacos (73%) en el quirófano, con un uso muy parejo de vainas de disección mecánicas autorotatorias (54,5%) o láser (45,4%). La mayoría de los equipos habían integrado un infectólogo y utilizaban técnicas de imagen complejas para planificar los casos difíciles. Después de la extracción del dispositivo infectado, la mitad optaban por diferir el reimplante una o dos semanas y el 57,6% habían iniciado un programa de formación específica en este campo.
ConclusiónLa infección sobre DEC en España es un problema complejo que sin embargo parece estar siendo abordado por la mayoría de los centros con cirugía cardiaca. Son deseables sin embargo centros de referencia experimentados para casos complejos.
Infections in cardiac implantable electronic devices are a growing problem that requires considerable experience and skill for proper therapeutic management. In most cases, this technique is performed using Percutaneous Endovascular Traction (PET). The objective of this study was to understand the current status of this technique in Spain.
Materials and methodsA nationwide survey was sent to Spanish centers with cardiac surgery capacity, inquiring about relevant aspects of the exytaction of these infected devices.
ResultsThirty-three hospitals responded to the survey, with only two (6%) reporting high-volume activity (>80 extractions/year) and 18% reporting medium-volume activity (40-60). The procedure was mostly performed by cardiac surgeons (73%) in the (54.5%) or laser (45.4%). Most teams had an infectious disease specialist and used complex imaging techniques to plan for difficult cases. After extraction of the infected device, half chose to defer reimplantation for 1–2 weeks, and 57.6% had begun a specific training program in this field.
ConclusionInfection in cardiac implantable electronic devices in Spain is a complex problem that nevertheless appears to be being addressed by most cardiac surgery centers. However, experienced referral centers are desirable for complex cases operating room, with a very even use of self-rotating mechanical dissection sheaths
Los constantes avances de la electrofisiología y su incidencia en la calidad de vida y supervivencia han generado en las últimas décadas un aumento casi exponencial en la implantación de los dispositivos de electroestimulación cardiaca (DEC) a nivel mundial. Nuestro país no es ajeno a esta realidad, aunque algo por debajo de las tasas registradas en Europa en dispositivos de alta energía1,2. Sin embargo, un aspecto preocupante que ha acompañado a este despegue ha sido el incremento en el número de infecciones sobre estos dispositivos, que en ocasiones ha sido hasta cinco veces mayor que el aumento en su implantación3, con una incidencia muy variable entre las diversas series, pero que en general se cifra entre el 1,5 y el 7% de los diversos implantes4.
Las razones para este aumento son múltiples y, partiendo de un mejor reconocimiento diagnóstico de esta complicación hoy día, son también derivadas del hecho de implantar DEC cada vez más complejos, con más número de cables, muchas veces en centros con poca experiencia quirúrgica, y sobre una población más añosa y frágil, cada vez con mayor esperanza de vida, que hace que sea sometida a periódicas manipulaciones de «actualización» (con frecuentes nuevos implantes de cables) o simplemente recambios periódicos del generador por agotamiento de la batería5,6.
Las infecciones sobre DEC están asociadas a una considerable mortalidad, especialmente en el caso de las infecciones sistémicas en que puede llegar al 10%, y a unos costos sanitarios elevados que varían dependiendo de los sistemas sanitarios, del tipo de infección (local o sistémica) e incluso del abordaje terapéutico, entre 24 y 54.000 € por proceso7.
Su presentación clínica puede ser diversa, con infecciones que son más frecuentemente locales, pero también sistémicas, cuyo manejo no es fácil y requiere la integración de conocimientos en múltiples disciplinas (electrofisiología, cirugía cardiaca, infectología, microbiología, radiología) para llegar a un diagnóstico precoz. Por otro lado, el abordaje terapéutico mas eficiente es siempre la retirada completa del dispositivo, pero esto se va volviendo cada vez mas complejo conforme las adherencias de los cables al sistema venoso van aumentando a lo largo de los años del implante. El método de elección es la tracción percutánea endovascular (TPE) que evita una cirugía cardiaca riesgosa en pacientes muchas veces ancianos y frágiles, y que tiene unas tasas de éxito cercanas al 95% con un porcentaje de complicaciones mayores debidos a la técnica de alrededor del 2%8,9. Sin embargo, esta técnica exige una pericia considerable y un entorno adecuado para lograr el éxito dentro de un marco seguro. Esto ha hecho que en la mayoría de los países europeos se establezcan centros de referencia habilitados para ello, que se benefician del aprendizaje continuado debido a un volumen alto de pacientes10. Sin embargo, la peculiar estructura sanitaria de España, dividida en 17 Comunidades Autónomas (CCAA), cada una con una administración y organización diferente, no ha favorecido precisamente este proceder, y en ese sentido es loable el reciente esfuerzo del Ministerio de Sanidad para la creación de Centros, Servicios y Unidades de Referencia (CSUR), entre las cuales se incluyen los centros habilitados para el procedimiento de extracción de cables11.
El objetivo de este trabajo ha sido conocer la situación actual sobre el manejo de estas infecciones en nuestro país
Material y metodosDesde la Sociedad Española de Cirugía Cardiaca y Endovascular (SECCE) se remitió un cuestionario a 60 servicios, que están adscritos al Registro de Intervenciones, con 83 destinatarios. Por otra parte, el mismo cuestionario se envió también desde la Sociedad Española de Infecciones Cardiovasculares (SEICAV) a cada Investigador Principal de los grupos multidisciplinares de endocarditis formados en 52 hospitales de la geografía española. Solo se contabilizó un cuestionario por cada hospital.
El cuestionario se mostraba en un documento de texto adjunto al correo electrónico y también podía contestarse a través de un cuestionario electrónico del que se facilitaba el enlace.
Las variables analizadas fueron: Hospital, ciudad y comunidad autónoma, número de extracciones percutáneas/año, lugar donde se llevaban a cabo y quien era el operador principal, herramientas utilizadas, utilización o no de técnicas de imagen pre-operatorias, momento de reimplantación, participación de especialistas infectólogos y si existía un programa de formación específico para esta técnica (tabla 1).
Encuesta remitida a los diversos centros
| Encuesta sobre la técnica de Tracción Percutánea Endovascular endovascular de electrodos (TPE) en España |
| Por favor responda teniendo en cuenta que hablamos de la retirada de electrodos de más de 2 años, que generalmente van a precisar el uso de herramientas (estiletes de tracción, vainas de disección, asas ó lazos femorales) |
| 1. ¿En qué hospital trabaja? (Nombre, Ciudad y Comunidad Autónoma) |
| ------------------------------------------------------------------------------------- |
| 2. ¿Su hospital realiza habitualmente técnicas de TPE? |
| - Sí |
| - No (por favor, si ha contestado esta opción, conteste la siguiente pregunta y será el fin de la encuesta) |
| 3. En caso de que su hospital no realice la técnica, ¿encuentra facilidades para derivar al paciente a otro centro? |
| - No, y por ello realizo abordaje local en infecciones locales y cirugía cardiaca abierta en infecciones sistémicas, si las condiciones del paciente lo permiten |
| - Sí, la vía de derivación es accesible y rápida |
| - Suelo derivarlos, pero el proceso es complejo y se demora bastante |
| 4. Por favor, indique el número aproximado de casos en un año: |
| - <20 |
| - 20 – 40 |
| - 40 – 60 |
| - 60 – 80 |
| - > 80 |
| 5. ¿Quién/quienes realizan la TPE? |
| - Los electrofisiólogos |
| - Los electrofisiólogos, con el apoyo de los cirujanos cardiacos |
| - Los cirujanos cardiacos, con el apoyo de los electrofisiólogos |
| 6. ¿Dónde se realizan las técnicas de TPE? |
| - En la sala de electrofisiología |
| - En el quirófano de cirugía cardiaca |
| - En la sala de electrofisiología o en el quirófano, dependiendo de la complejidad |
| - En una sala híbrida |
| 7. ¿Qué tipo de vainas de disección utiliza? |
| - Vainas mecánicas auto-rotatorias |
| - Vainas láser |
| - Ambas |
| 8. ¿Cuál es el motivo principal en hospital para realizar la TPE? |
| - Infecciones en más del 80% |
| - Otros motivos principalmente (retirada de cables abandonados, trombosis de vena cava, malfuncionamiento de cables…) |
| - Aproximadamente el mismo porcentaje en ambos casos |
| 9. ¿En los casos complejos solicita con frecuencia técnicas de imagen complementarias (TAC sincronizado, PET/TC, ¿realidad virtual)? |
| - Sí |
| - No |
| 10. ¿En los pacientes con infección del dispositivo, solicita el apoyo de un especialista en enfermedades infecciosas? |
| - Siempre, porque forma parte del grupo de trabajo |
| - Ocasionalmente, en los casos de infección sistémica |
| - No, no hay infectólogos o internistas en mi centro con experiencia en este sentido |
| 11. Tras la realización de la TPE y en pacientes que necesitan continuar con el dispositivo, ¿Cuándo realiza la reimplantación? |
| - En el mismo acto de la extracción o las 24-48h como mucho |
| - Tras un periodo variable de una o dos semanas, dependiendo del tipo de infección |
| 12. ¿Existe en su hospital un programa de formación en esta técnica para los cirujanos/electrofisiólogos noveles? |
| - Sí |
| - No |
PET/TC: técnica de emisión de positrones con tomografía axial computarizada; TAC: tomografía axial computarizada; TPE: tracción percutanea endovascular.
Encuesta remitida a los diversos centros sobre la TPE en España.
Se consideró extracción de electrodos por vía percutánea endovascular la retirada del torrente circulatorio de los electrodos que llevan más de un año implantados y que precisan de herramientas específicas, tales como los estiletes de liberación o las vainas de disección mecánicas auto-rotatorias o láser.
Consideraciones éticasNo es necesario adjuntar consentimiento informado porque se trata solo de una encuesta de la actividad de los servicios extractores en España.
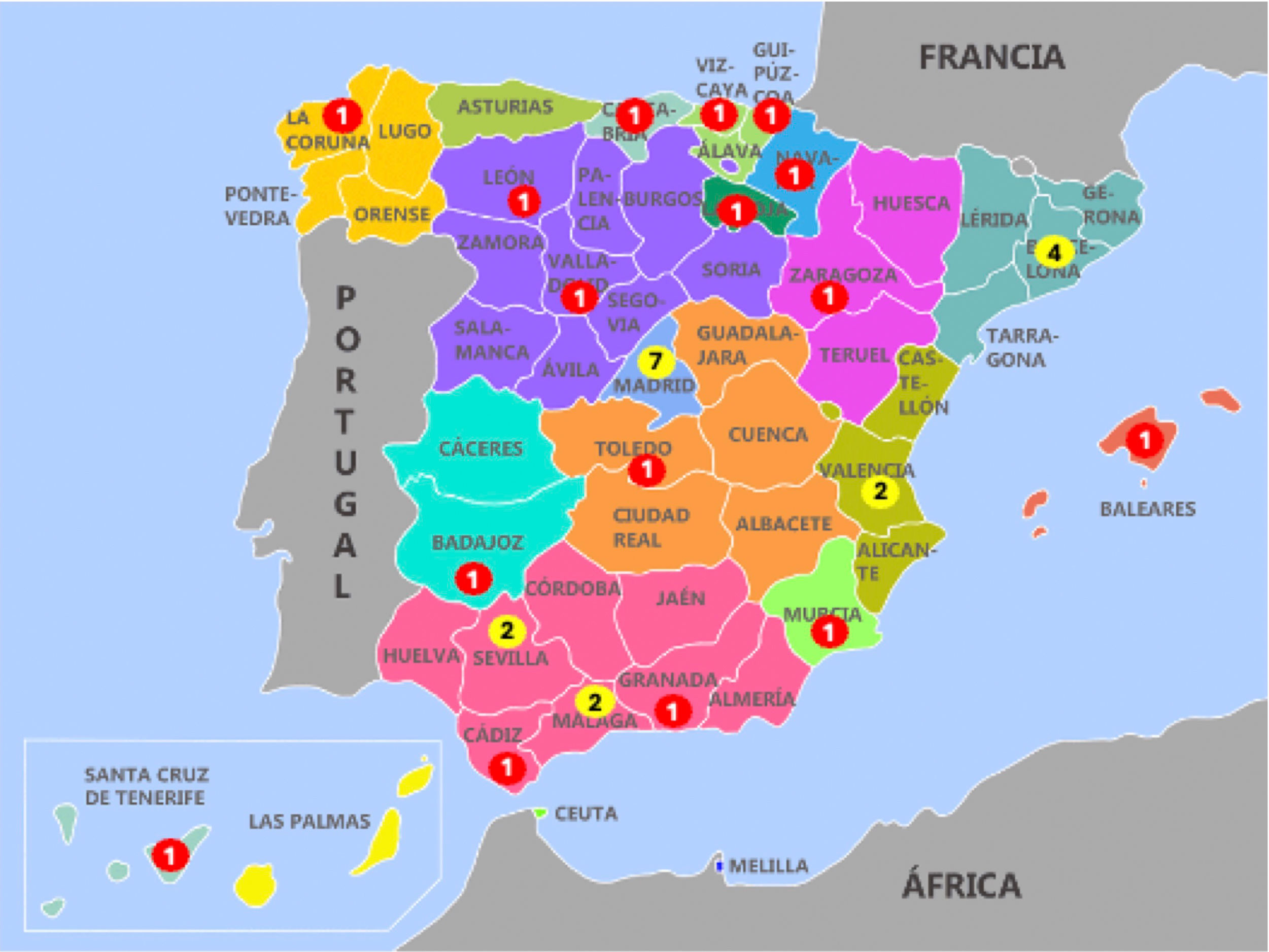
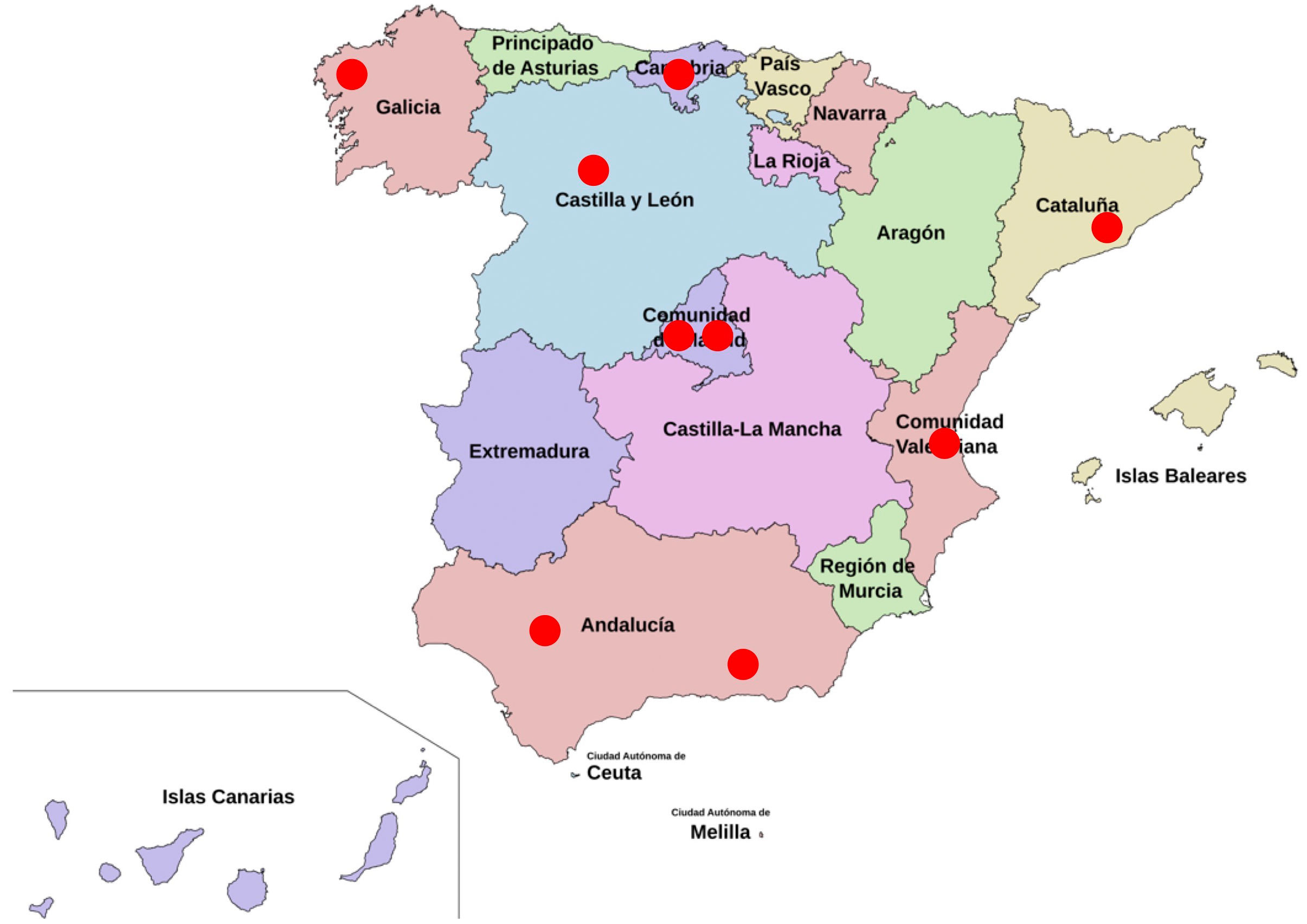
ResultadosSe consiguió la cumplimentación de la encuesta en 33 centros hospitalarios (55%), pertenecientes a 16 de las 17 CCAA del estado español, con una presencia más relevante de los centros procedentes de Madrid (7), Andalucía (6) y Cataluña (4), con la diferencia de que en Madrid y Cataluña todos los centros estaban en la capital, mientras que en Andalucía estaban ubicados en cinco ciudades (fig. 1).
Todos los hospitales que contestaron hacían técnicas de TPE, pero solo nueve (27,3%) estaban acreditados como CSUR, y eran los que comunicaban mayores volúmenes de pacientes anualmente (fig. 2). El número de procedimientos realizados cada año en los distintos hospitales participantes fue inferior a 20 en el 48,5%, entre 20-40 en el 27,3%, entre 40-60 en el 18,2% y superior a 80 en el 6,1% de los centros. De los hospitales extractores, solo derivaron a centros CSUR, dos hospitales (6%): un centro privado en Madrid y uno público en Andalucía. En el primero la derivación les resultaba difícil y al segundo fácil, en cuanto a gestiones administrativas.
En cuanto a la realización de la TPE, en el 72,7% de los casos la hacían los cirujanos cardiacos y en el 27,3% restante los electrofisiólogos. De todas ellas el 57,6% tenían lugar en quirófanos de cirugía cardiaca, el 9,1% en salas de electrofisiología y el 9,1% en salas híbridas, con un 24,2% realizándose en quirófanos de cirugía cardiaca o en salas de electrofisiología, dependiendo de la complejidad del caso.
Las vainas de disección mayoritariamente usadas para la liberación de las adherencias de los electrodos fueron mecánicas auto-rotatorias exclusivamente en el 54,5% de los casos, mientras que el resto utilizó fundamentalmente vainas láser.
La razón más frecuente para la extracción de los electrodos fue el origen infeccioso (72,7%). Sin embargo, un 18,2% de centros reportó como causa de las extracciones un proceso infeccioso solo en el 50% de las ocasiones, con una participación de los infectólogos de manera activa en el manejo diagnóstico y terapéutico en el 90,9%, integrados en el equipo de extracción. Tan solo tres centros (9,1%) refirieron otras causas como la razón principal para la extracción, siendo dos de ellos centros CSUR con un volumen alto (> 80) de pacientes anuales. En la planificación de las extracciones, el 78,8% de los centros realizaba técnicas de imagen complejas en el preoperatorio
Tras la extracción del DEC, el 48,5% de los hospitales contestó realizarlo en el mismo acto quirúrgico ó en las 48h siguientes al mismo, mientras que el 51,5% prefirieron demorarlo entre una y dos semanas.
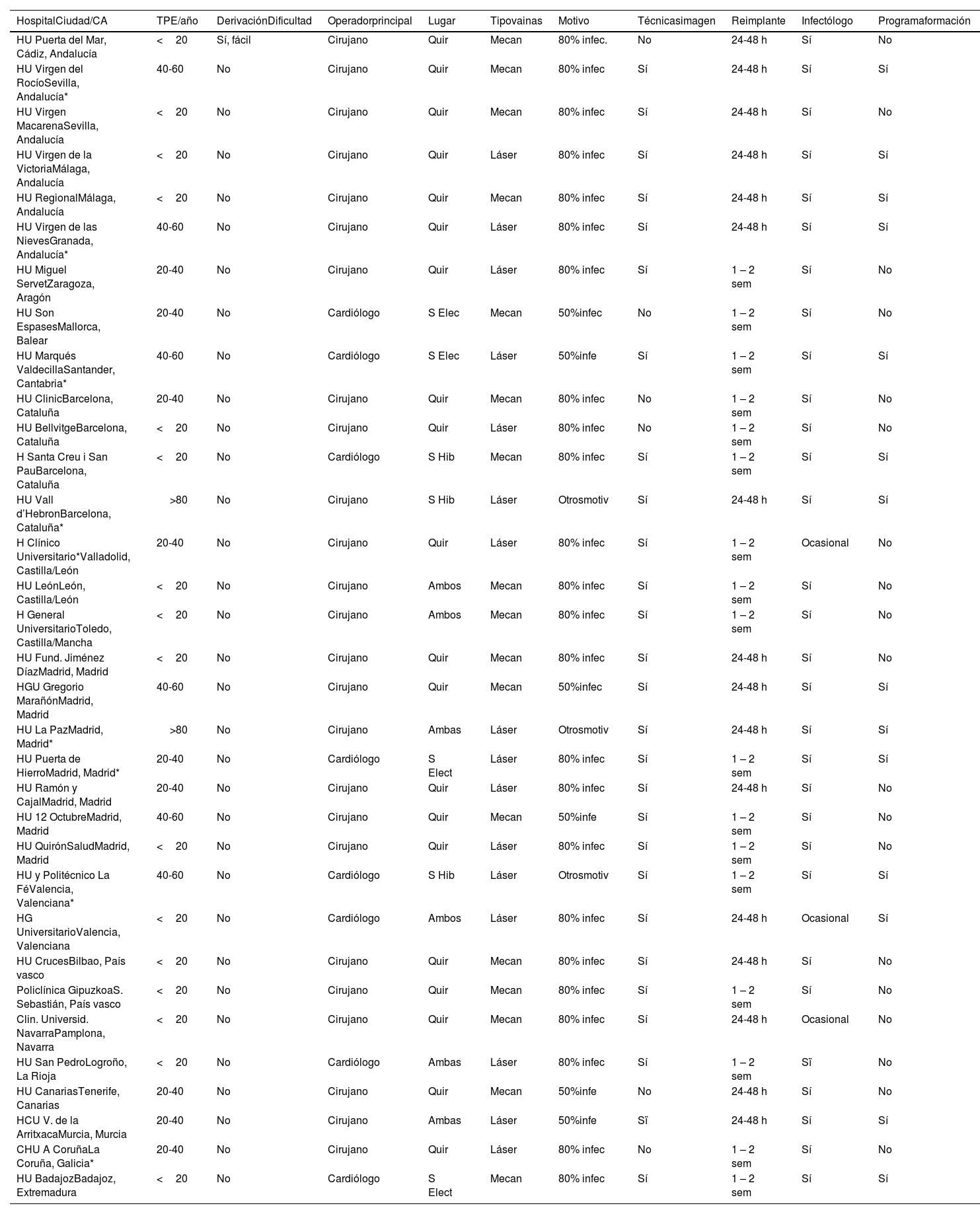
Por último, el 42,5% de los hospitales comunicaron tener un programa de formación específico para esta disciplina. Los datos de los diversos hospitales se muestran detalladamente en la tabla 2.
Resultados de los diversos hospitales
| HospitalCiudad/CA | TPE/año | DerivaciónDificultad | Operadorprincipal | Lugar | Tipovainas | Motivo | Técnicasimagen | Reimplante | Infectólogo | Programaformación |
|---|---|---|---|---|---|---|---|---|---|---|
| HU Puerta del Mar, Cádiz, Andalucía | <20 | Sí, fácil | Cirujano | Quir | Mecan | 80% infec. | No | 24-48 h | Sí | No |
| HU Virgen del RocíoSevilla, Andalucía* | 40-60 | No | Cirujano | Quir | Mecan | 80% infec | Sí | 24-48 h | Sí | Sí |
| HU Virgen MacarenaSevilla, Andalucía | <20 | No | Cirujano | Quir | Mecan | 80% infec | Sí | 24-48 h | Sí | No |
| HU Virgen de la VictoriaMálaga, Andalucía | <20 | No | Cirujano | Quir | Láser | 80% infec | Sí | 24-48 h | Sí | Sí |
| HU RegionalMálaga, Andalucía | <20 | No | Cirujano | Quir | Mecan | 80% infec | Sí | 24-48 h | Sí | Sí |
| HU Virgen de las NievesGranada, Andalucía* | 40-60 | No | Cirujano | Quir | Láser | 80% infec | Sí | 24-48 h | Sí | Sí |
| HU Miguel ServetZaragoza, Aragón | 20-40 | No | Cirujano | Quir | Láser | 80% infec | Sí | 1 – 2 sem | Sí | No |
| HU Son EspasesMallorca, Balear | 20-40 | No | Cardiólogo | S Elec | Mecan | 50%infec | No | 1 – 2 sem | Sí | No |
| HU Marqués ValdecillaSantander, Cantabria* | 40-60 | No | Cardiólogo | S Elec | Láser | 50%infe | Sí | 1 – 2 sem | Sí | Sí |
| HU ClinicBarcelona, Cataluña | 20-40 | No | Cirujano | Quir | Mecan | 80% infec | No | 1 – 2 sem | Sí | No |
| HU BellvitgeBarcelona, Cataluña | <20 | No | Cirujano | Quir | Láser | 80% infec | No | 1 – 2 sem | Sí | No |
| H Santa Creu i San PauBarcelona, Cataluña | <20 | No | Cardiólogo | S Hib | Mecan | 80% infec | Sí | 1 – 2 sem | Sí | Sí |
| HU Vall d’HebronBarcelona, Cataluña* | >80 | No | Cirujano | S Hib | Láser | Otrosmotiv | Sí | 24-48 h | Sí | Sí |
| H Clínico Universitario*Valladolid, Castilla/León | 20-40 | No | Cirujano | Quir | Láser | 80% infec | Sí | 1 – 2 sem | Ocasional | No |
| HU LeónLeón, Castilla/León | <20 | No | Cirujano | Ambos | Mecan | 80% infec | Sí | 1 – 2 sem | Sí | No |
| H General UniversitarioToledo, Castilla/Mancha | <20 | No | Cirujano | Ambos | Mecan | 80% infec | Sí | 1 – 2 sem | Sí | No |
| HU Fund. Jiménez DíazMadrid, Madrid | <20 | No | Cirujano | Quir | Mecan | 80% infec | Sí | 24-48 h | Sí | No |
| HGU Gregorio MarañónMadrid, Madrid | 40-60 | No | Cirujano | Quir | Mecan | 50%infec | Sí | 24-48 h | Sí | Sí |
| HU La PazMadrid, Madrid* | >80 | No | Cirujano | Ambas | Láser | Otrosmotiv | Sí | 24-48 h | Sí | Sí |
| HU Puerta de HierroMadrid, Madrid* | 20-40 | No | Cardiólogo | S Elect | Láser | 80% infec | Sí | 1 – 2 sem | Sí | Sí |
| HU Ramón y CajalMadrid, Madrid | 20-40 | No | Cirujano | Quir | Láser | 80% infec | Sí | 24-48 h | Sí | No |
| HU 12 OctubreMadrid, Madrid | 40-60 | No | Cirujano | Quir | Mecan | 50%infe | Sí | 1 – 2 sem | Sí | No |
| HU QuirónSaludMadrid, Madrid | <20 | No | Cirujano | Quir | Láser | 80% infec | Sí | 1 – 2 sem | Sí | No |
| HU y Politécnico La FéValencia, Valenciana* | 40-60 | No | Cardiólogo | S Hib | Láser | Otrosmotiv | Sí | 1 – 2 sem | Sí | Sí |
| HG UniversitarioValencia, Valenciana | <20 | No | Cardiólogo | Ambos | Láser | 80% infec | Sí | 24-48 h | Ocasional | Sí |
| HU CrucesBilbao, País vasco | <20 | No | Cirujano | Quir | Mecan | 80% infec | Sí | 24-48 h | Sí | No |
| Policlínica GipuzkoaS. Sebastián, País vasco | <20 | No | Cirujano | Quir | Mecan | 80% infec | Sí | 1 – 2 sem | Sí | No |
| Clin. Universid. NavarraPamplona, Navarra | <20 | No | Cirujano | Quir | Mecan | 80% infec | Sí | 24-48 h | Ocasional | No |
| HU San PedroLogroño, La Rioja | <20 | No | Cardiólogo | Ambas | Láser | 80% infec | Sí | 1 – 2 sem | Sï | No |
| HU CanariasTenerife, Canarias | 20-40 | No | Cirujano | Quir | Mecan | 50%infe | No | 24-48 h | Sí | No |
| HCU V. de la ArritxacaMurcia, Murcia | 20-40 | No | Cirujano | Ambas | Láser | 50%infe | Sï | 24-48 h | Sí | Sí |
| CHU A CoruñaLa Coruña, Galicia* | 20-40 | No | Cirujano | Quir | Láser | 80% infec | No | 1 – 2 sem | Sí | No |
| HU BadajozBadajoz, Extremadura | <20 | No | Cardiólogo | S Elect | Mecan | 80% infec | Sí | 1 – 2 sem | Sí | Sí |
Los datos de esta encuesta muestran una amplia distribución de la técnica de TPE en toda la geografía nacional, con presencia de al menos un centro extractor en cada CCAA. La mayor representación de las comunidades de Madrid, Andalucía y Cataluña es comprensible por su mayor población. De la misma manera, el hecho de la mayor dispersión de centros en Andalucía lo explica su mayor extensión geográfica. La existencia de muchos centros con capacidad extractora favorece una mayor accesibilidad del paciente a la técnica dentro de su Comunidad Autónoma e incluso de su provincia, pero hace que no todos los centros puedan tener un volumen alto de pacientes. La TPE es una técnica que precisa de un considerable periodo de aprendizaje12,13 y sus resultados (tanto en porcentaje de éxitos como de complicaciones) se han relacionado con el número de extracciones que realizan10, por lo que es deseable tener centros de alto volumen acreditados, para derivar allí los casos más complejos. De hecho, en esta encuesta, solo tres centros (dos de ellos CSUR) referían un volumen de pacientes por encima de los 80 anuales. Es deseable por tanto que se faciliten los trámites administrativos entre CCAA para la derivación hacia estos centros en casos complejos.
El procedimiento de la TPE en esta encuesta estaba realizado mayoritariamente por cirujanos (72,7%) lo que lo diferencia algo de la situación en otros países de Europa, en los que la esta técnica es realizada mayoritariamente por electrofisiólogos, con el apoyo de cirujanos cardiacos que pueden estar presentes o incluso solo localizados14. Hay que considerar que la TPE ha demostrado ser una técnica eficaz (90-98% de éxito) y segura, con una mortalidad del 3% y un porcentaje de complicaciones mayores de apenas un 2-4%15. Sin embargo, en casos complejos fundamentalmente debidos a la edad de los cables (> 20 años) y al abandono previo de varios dispositivos, la eficacia es menor, teniendo que recurrir a menudo a técnicas mas complejas como el abordaje femoral, lo que aumenta exponencialmente el número de complicaciones hasta el 10%16,17. En estos casos complejos es siempre deseable la planificación meticulosa del acto y en este sentido se han desarrollado pruebas radiológicas avanzadas como la tomografía por emisión de positrones (18F-FDG PET/TC), la tomografía axial computarizada sincronizada y la realidad virtual que permiten analizar previamente el grado de dificultad, incluso con la ayuda de inteligencia artificial (IA)18–20. La utilización de estas técnicas de imagen era reportada por casi el 80% de los centros. Si embargo, es preciso recordar que estas pruebas son bastante precisas para predecir el grado de adherencia de los cables a las paredes venosas, pero no la dureza de estas adherencias, que suele ser siempre mucho mayor en pacientes jóvenes21. Se hace por tanto imprescindible, en nuestra opinión, realizar la TPE en un entorno apropiado como es el quirófano de cirugía cardiaca o una sala hibrida con disponibilidad para un abordaje quirúrgico abierto, al menos para los casos difíciles. En cuanto a las herramientas utilizadas, en esta encuesta una ligera mayoría de centros se inclinaban por el uso de vainas de disección mecánicas auto-rotatorias frente a las vainas con Láser. Existen series amplias con buenos resultados en ambas22,23, aunque la comparación meticulosa de los resultados ha mostrado un menor número de complicaciones con las vainas mecánicas24,25. Esto, unido a su menor coste, quizás explique en parte su mayor uso en nuestro país.
Por otro lado, las razones para la realización de la TPE en esta encuesta siguen siendo mayoritariamente las infecciones (72,7%), lo que parece lógico porque en los casos de infección sistémica es una necesidad perentoria y ello justifica la presencia de un infectólogo integrado en los equipos de extracción (90,9%). Las infecciones sobre DEC son un tema complejo y el abordaje multidisciplinar (cardiólogos, cirujanos, radiólogos, infectólogos y microbiólogos) en un entorno colaborativo se hace siempre imprescindible, como así lo recomiendan las diversas guías de consenso12,13. Sin embargo, conforme avanza la Electrofisiología en los países desarrollados, es cada vez mayor el número de dispositivos implantados, incluso desde edades jóvenes. Esto hace cada vez más frecuentes los abandonos de cables con defectos de funcionamiento que ocurren con el tiempo, y que son sustituidos o complementados por otros con nuevas funcionalidades (upgrades), o simplemente dejadas in situ sin funcionamiento porque la indicación que en su día se hizo de electroestimulación se demostró más adelante innecesaria. De hecho, en EE.UU. y Europa el porcentaje de dispositivos extraídos que no son reimplantados alcanza el 15%26,27, aunque esta cifra parece ser bastante menor en nuestro país28. El abandono de cables sin funcionalidad puede generar efectos perniciosos a largo plazo, entre ellos su infección o el desarrollo de trombosis venosa a nivel de la vena cava superior29. Por otro lado, cuando hay necesidad de extraer un nuevo sistema infectado, la presencia de cables antiguos «olvidados» dificulta extraordinariamente la extracción30. La actuación con estos dispositivos sin funcionalidad ha sido por tanto objeto de debate y la recomendación actual es no tolerar más de tres cables en individuos jóvenes y extraer siempre que sea posible los antiguos8. La plasmación de esta recomendación se ve reflejada en esta encuesta en el hecho de que tres de los centros con más volumen (9%) reportaran como más frecuentes las extracciones de cables no originadas por un proceso infeccioso.
El tiempo de reimplantación del dispositivo en los casos de infección es un hecho controvertido. La mayoría de las guías de práctica clínica aconsejan (recomendación III C) dejar un tiempo entre la extracción y el reimplante8,9. En una encuesta realizada en Europa, la mayoría de los centros reimplantaban los dispositivos en un segundo tiempo con un intervalo que variaba entre 48 horas y dos semanas dependiendo del tipo de infección14. De hecho, las guías al uso recomiendan la explantación del dispositivo con un sistema de estimulación transitorio, empleando en pacientes dependientes de estimulación un sistema transitorio por vía femoral o yugular ipsilateral con generador externalizado o incluso un marcapaso epicárdico. Sin embargo, el uso de sistemas de estimulación transitorios es una frecuente fuente de problemas en pacientes ancianos por la inmovilización que a menudo requiere, y ha sido también señalado como un factor predisponente para la infección de un nuevo dispositivo6. Por ello, en el caso de que los hemocultivos sean negativos a las 72 horas, se recomienda reimplantar entonces prontamente el nuevo sistema definitivo. Sin embargo, esta «recomendación de expertos», ha sido cuestionada recientemente en las infecciones locales, donde varios trabajos han demostrado que el recambio en un solo tiempo no mostraba una mayor incidencia de reinfecciones31. En infecciones sistémicas la renuencia a una reimplantación en el mismo momento de la extracción es aún mayor, pues se asume que una reimplantación en el mismo acto podría contaminar el nuevo sistema desde el antiguo y se aconseja diferir el reimplante unas dos a cuatro semanas, lo que aún aumenta más el riesgo de complicaciones, incluyendo el deterioro de la contractilidad en pacientes que habían experimentado una resincronización exitosa. Sin embargo, esta hipotética posibilidad de mayor reinfección no se ha comprobado en estudios en la vida real28,32. Es preciso que resaltar aquí que, bajo tratamiento antimicrobiano, la adhesión de los microorganismos a materiales abióticos está seriamente comprometida, incluso a concentraciones subóptimas, tal como se ha demostrado en estudios in vitro33 y modelos experimentales34. Por tanto, no hay una razón convincente para pensar en un mayor riesgo de infección del nuevo dispositivo en un paciente con tratamiento antimicrobiano apropiado y hemocultivos negativos en quien va a realizarse un explante completo del material infectado, como se ha demostrado en otros implantes35. De hecho, en nuestra experiencia la reimplantación en un solo tiempo no se asoció a una mayor tasa de reinfecciones y sí en cambio, cuando se realizó en dos tiempos hubo una mayor incidencia de infección en el nuevo dispositivo por microorganismos resistentes al tratamiento administrado28.
Es evidente por tanto que en el manejo de las infecciones en DEC existen muchos aspectos que precisan ser bien definidos y ello se ha visto reflejado en encuestas realizadas en centros a nivel mundial, en los que se demostró una variabilidad importante con respecto a las recomendaciones actuales36. Y aún más, en otra encuesta realizada en 43 países europeos, muchos consultados expresaron su inseguridad con respecto a ciertas actuaciones y la necesidad de una mayor formación en este área37. Son por tanto loables los programas de formación específica en este sentido, reportados por el 42,4% de los centros en esta encuesta.
LimitacionesNuestro trabajo presenta evidentes limitaciones. En primer lugar, el elevado número de encuestas contestadas parece reflejar la realidad de los centros extractores, pero no el proceder de otros centros en los que no está disponible esta técnica. De hecho, solo dos centros reconocieron derivar sus casos complejos, refiriendo las dificultades experimentadas en el proceso. Sin embargo, se ha conseguido una representación bastante fiable de la realidad española, con una representación de casi todas las CCAA. En segundo lugar, en esta encuesta se informa del normal desarrollo en este campo, pero no se dan datos de eficacia y por lo tanto tampoco podemos concluir, por ejemplo, si la actuación de los centros acreditados como CSUR fue más eficiente. Tampoco se preguntó sobre ciertos aspectos complejos como la actuación más frecuente en casos de infecciones locales ó el proceder con los cables abandonados. Es deseable en este sentido la creación de un registro nacional en el que pudiera medirse la actividad de los diversos centros y sus resultados. Esto es especialmente relevante cuando observamos que casi en la mitad de los centros encuestados, el número de extracciones estaba por debajo de 20 al año. Por último, esta encuesta se ha enviado a centros de tercer nivel, con cirugía cardiaca, pero no refleja toda la realidad de la electrofisiología básica. En ciertas CCAA, como la andaluza o la valenciana, por ejemplo, gran parte de los implantes de marcapasos son realizados en hospitales comarcales, dentro del entorno de las unidades de cuidados intensivos38, que generalmente no están luego capacitadas para la realización de TPE en casos de infecciones y realizan, como mucho, un abordaje local en infecciones del generador (lo que no estaba contemplado en nuestra encuesta). Seria por tanto interesante en un futuro conocer cuales son sus actuaciones en casos de infección y si tienen una comunicación fluida para la derivación a centros acreditados para esta técnica.
ConclusionesLas infecciones sobre DEC son un problema creciente y que suponen todo un reto que debemos afrontar de manera coordinada y multidisciplinar. A pesar del elevado número de hospitales extractores recogidos en esta encuesta nacional, son también deseables centros de referencia experimentados y con un alto volumen de pacientes para asegurar una eficacia y seguridad lo más elevadas posibles en los casos complejos. En este sentido, la labor del cirujano cardiaco, bien como operador principal o como apoyo en caso de complicaciones, es esencial y sería fundamental un registro nacional sobre las actuaciones relacionadas con este campo. Por otro lado, algunos aspectos no están respaldados por unas recomendaciones con clara evidencia científica. Son deseables por tanto programas de formación y actualización específica en esta difícil área, tanto en el campo de la adquisición de habilidades técnicas, como en el planteamiento y resolución de problemas complejos.