En la actualidad no existe ninguna comparación de la capacidad predictiva de las diferentes escalas específicas de riesgo quirúrgico en endocarditis infecciosa.
ObjetivoComparar la utilidad de las diferentes escalas específicas publicadas.
Material y métodosEstudio observacional, retrospectivo y unicéntrico. Se incluyeron 180 pacientes, en los que se calcularon 10 escalas. Se calculó la mortalidad estimada por cada escala y se comparó con la mortalidad observada, con su estimación a través del intervalo de confianza del 95%. Se valoró la discriminación, por el área bajo la curva ROC (AUC), y la calibración con el test de Homer-Lemeshow (HLt).
ResultadosLa mortalidad observada fue del 26,82% (IC95%: 20,74-33,57%). Las escalas STS-EI, De Feo y AEPEI infraestimaron la mortalidad; las escalas de Costa y Endoscore la sobreestimaron. La escala de Costa presentó una baja discriminación y AEPEI demostró una calibración subóptima.
En nuestra serie, las escalas que demostraron una estimación precisa fueron: 1)PALSUSE: mortalidad predicha 15-30%, AUC=0,68 (IC95%: 0,58-0,76) y HLt p=0,46; 2)RISK-E score: estima mortalidad 0-30%, AUC=0,76 (IC95%: 0,69-0,82) y HLt p=0,35; 3)SpecificEuroSCORESI yII: mortalidad estimada 30-40%, AUC=0,76 (IC95%: 0,69-0,82) y HLt p=0,42 enI y AUC=0,74 (IC95%: 0,66-0,79) con HLt=0,75 enII; 4) APORTEI: predice mortalidad de 20-40%, AUC=0,75 (IC95%: 0,68-0,82) y HLt p=0,73.
ConclusionesDe las 10 escalas analizadas, PALSUSE, RISK-E, SpecificEuroSCORE y APORTEI demostraron una predicción de mortalidad precisa y una adecuada capacidad predictiva en el postoperatorio inmediato de cirugía cardiaca por endocarditis infecciosa.
A direct comparison among specific endocarditis risk scores has not yet been conducted.
ObjectiveCompare the previously published endocarditis specific scores and analyze their prognostic accuracy.
Material and methodsWe performed an observational single-center and retrospective study. 180 patients were included, and 10 specific risk scores were calculated. Estimated mortality was calculated for each score and it was compared with the observed mortality, with its 95% confidence interval estimation. Discrimination was assessed by area under the ROC curve (AUC) and calibration was assessed by Homer-Lemeshow test (HLt).
ResultsObserved surgical mortality was 26.82% (95%CI: 20.74-33.57). STS-EI, De Feo and AEPEI scores underestimated mortality, whereas Costa score and Endoscore overestimated mortality. Costa score demonstrated a low discrimination (AUC=0.65, 95%CI 0.57-0.72) and AEPEI showed a suboptimal calibration (P=.025).
Resultsshowed an accurate estimated mortality in: 1)PALSUSE showed predicted mortality to be between 15-30%, AUC=0.68 (95%CI: 0.58-0.76) and HLt P=.46; 2)RISK-E score estimated a mortality of 0-30%, AUC=0.76 (95%CI: 0.69-0.82) and HLt P=.35; 3)SpecificEuroSCORESI yII with an estimated mortality of 30-40%, AUC=0,76 (95%CI: 0,69-0,82) y HLt P=.42 for SpecificEuroSCORES I and AUC=0.74 (95%CI: 0,66-0,79) con HLt=0,75 in SpecificEuroSCORES II; 4)APORTEI showed predicted mortality to be between 20 and 40%, with AUC=0.75 (95%CI: 0.68-0.82) and HLt P=.73.
ConclusionAmong the 10 assessed endocarditis specific scores scores, PALSUSE, RISK-E, SpecificEuroSCORE and APORTEI demonstrated an optimal mortality risk estimation and an adequate predictive capacity for postoperative mortality in the postoperative period after cardiac surgery for infective endocarditis.
Las escalas de estimación del riesgo quirúrgico (ER) son herramientas frecuentemente empleadas en los servicios quirúrgicos a la hora de estimar la mortalidad derivada de una determinada intervención quirúrgica. Mediante el análisis de predictores independientes de mortalidad, las ER permiten contrapesar el riesgo que se deriva de la evolución natural de la patología que presenta el paciente frente al generado por la intervención quirúrgica. De esta manera, las ER aportan información sobre el pronóstico esperado para un paciente y ayudan en la toma de decisiones terapéuticas complejas.
En el caso de la cirugía cardiovascular existen dos ER ampliamente empleadas: el EuroSCORE1, la escala más empleada en Europa, y el Society of Thoracic Surgeons, Predicted risk of mortality (STS PROM), que tiene amplia difusión en Estados Unidos2. A pesar de que el EuroSCOREII, creado tras una modificación del EuroSCORE, es la escala utilizada de manera rutinaria en cirugía cardiaca en nuestro medio, ha demostrado una baja capacidad predictiva en el caso de endocarditis infecciosa (EI) activa3-5. La EI constituye una patología con características específicas en la que influyen en la mortalidad algunas variables no calculadas por las ER clásicas. Tanto en el caso del EuroSCORE3,6,7 como en el caso del STS score se demostró la no utilidad en la predicción del riesgo de mortalidad en EI5,8.
Por lo tanto, la incertidumbre en el riesgo quirúrgico que presentan los pacientes con EI ha generado en las últimas décadas la creación de otras escalas que incluyen diferentes variables específicas de esta entidad (como la presencia de abscesos, la sepsis, el microorganismo causal…) que han demostrado ser factores independientes de riesgo. En la actualidad existen numerosas escalas de estimación de riesgo específicas de endocarditis infecciosa (EEREI), y algunas de ellas han demostrado una mejor predicción de riesgo en comparación con las escalas de riesgo clásicas7.
Sin embargo, a pesar del gran número de EEREI disponibles, pocas de ellas han sido validadas de forma externa y ninguna ha demostrado un beneficio claro frente a las demás. Hasta la fecha, se han desarrollado pocos estudios de comparación entre diferentes EEREI9,10, y por lo tanto no existen claras recomendaciones sobre cuál de ellas emplear o la validez de la información que proporcionan.
En el presente trabajo nos proponemos analizar la capacidad predictiva de 10EEREI publicadas previamente para poder establecer recomendaciones respecto de cuáles deberían emplearse en nuestro medio.
Objetivos del estudioComo objetivos primarios del estudio se estableció:
- 1.
Analizar la precisión de la estimación numérica de mortalidad obtenida por cada escala.
- 2.
Analizar la capacidad de predicción de mortalidad de las diferentes EEREI publicadas.
Como objetivos secundarios del estudio:
- 1.
Comparar la capacidad predictiva de las EEREI analizadas.
- 2.
Realizar una validación externa de las EEREI.
Estudio retrospectivo, observacional, unicéntrico, que incluyó a todos los pacientes intervenidos de cirugía cardiaca con diagnóstico de EI aguda.
Población a estudioEl estudio incluyó a todos los pacientes intervenidos desde el año 2002 al 2017 de forma consecutiva con diagnóstico de EI activa según los criterios de Duke modificados11.
Variables a estudioLas variables analizadas fueron recogidas de manera retrospectiva, recopilándose de las tres bases de datos del Hospital: SICCS (Sistema Informático Cirugía Cardíaca Sorin) (Biomenco, Madrid, España), HORUS y CAJAL (Aplicación de informes clínicos V11.1). Se incluyeron todas las variables necesarias para el cálculo de las EEREI.
Definición de las variables- 1.
Mortalidad perioperatoria: mortalidad tanto intraoperatoria como postoperatoria durante el ingreso del paciente.
- 2.
Endocarditis infecciosa activa: cuadro clínico de menos de un mes de evolución.
- 3.
Escalas de riesgo clásicas: nos referimos a escalas clásicas como las no específicas de endocarditis infecciosa, entre las que podemos encontrar el EuroSCORE y el STS score.
- 4.
Shock séptico: se define por la presencia de hipoperfusión e hipoxia tisular en el contexto de un síndrome de respuesta inflamatoria sistémica a un agente infeccioso.
- 5.
Trombocitopenia prequirúrgica: recuento plaquetario <150.000 plaquetas/mm312.
- 6.
Absceso paravalvular: infección y necrosis del tejido adyacente al anillo paravalvular, con formación de una cavidad purulenta con capacidad de invadir estructuras cercanas13.
- 7.
Tasa de embolia: presencia de embolias sistémicas diagnosticadas mediante datos clínicos y pruebas complementarias.
- 8.
Cirugía urgente: intervención quirúrgica que no se puede demorar más de 24-48h.
El análisis estadístico se llevó a cabo empleando Stata/IC 14.2 (Stata Statistical Software: Release 14. College Station, TX: StataCorp LP). Las variables continuas se expresaron como media y desviación estándar (DE). Las variables categóricas se expresaron como frecuencia y proporciones.
Se realizó la estimación de parámetros poblacionales derivados a partir de los resultados de mortalidad observados en nuestra muestra, mediante estimación de intervalos de confianza de proporciones, expresados como IC del 95%.
La valoración de la discriminación de las ER se realizó mediante el cálculo del área bajo la curva ROC (AUC), expresada con su valor y su IC del 95%. La calibración se valoró mediante la prueba de Hosmer-Lemeshow.
Consideraciones éticasEl Comité Ético de Investigación Clínica (CEIC) aprobó la realización del presente estudio (número de CEIC 313/2016, aprobado el 28 de noviembre de 2016). No se exigió consentimiento informado por escrito de los pacientes. La identificación del paciente fue codificada, cumpliendo con los requisitos de la Ley Orgánica de Protección de Datos 15/1999.
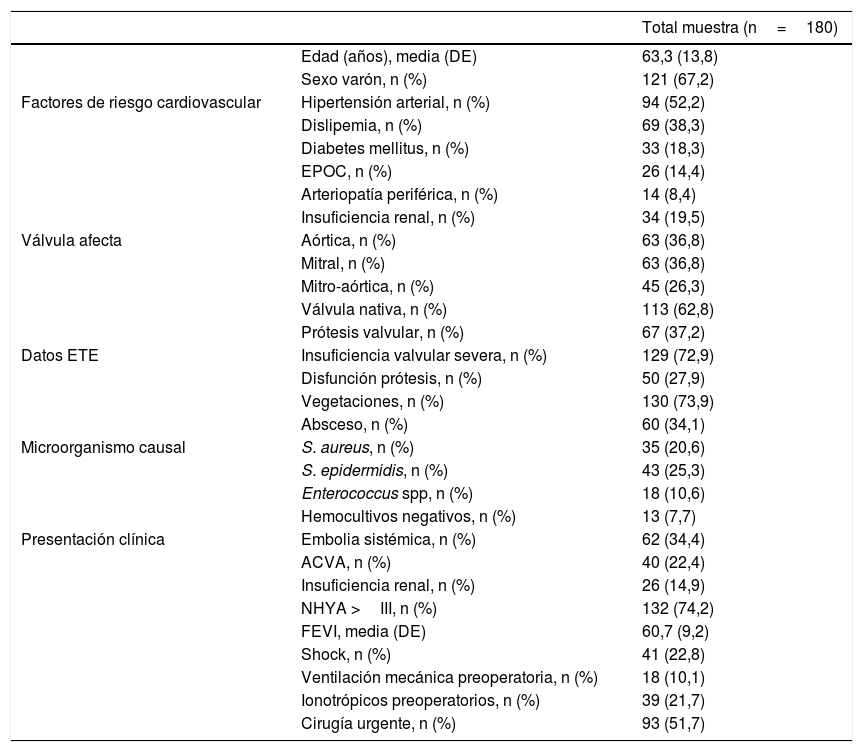
ResultadosDurante el periodo de estudio fueron intervenidos 180 pacientes de EI activa en nuestro centro. La tabla 1 muestra las características basales de los pacientes intervenidos.
Características basales
| Total muestra (n=180) | ||
|---|---|---|
| Edad (años), media (DE) | 63,3 (13,8) | |
| Sexo varón, n (%) | 121 (67,2) | |
| Factores de riesgo cardiovascular | Hipertensión arterial, n (%) | 94 (52,2) |
| Dislipemia, n (%) | 69 (38,3) | |
| Diabetes mellitus, n (%) | 33 (18,3) | |
| EPOC, n (%) | 26 (14,4) | |
| Arteriopatía periférica, n (%) | 14 (8,4) | |
| Insuficiencia renal, n (%) | 34 (19,5) | |
| Válvula afecta | Aórtica, n (%) | 63 (36,8) |
| Mitral, n (%) | 63 (36,8) | |
| Mitro-aórtica, n (%) | 45 (26,3) | |
| Válvula nativa, n (%) | 113 (62,8) | |
| Prótesis valvular, n (%) | 67 (37,2) | |
| Datos ETE | Insuficiencia valvular severa, n (%) | 129 (72,9) |
| Disfunción prótesis, n (%) | 50 (27,9) | |
| Vegetaciones, n (%) | 130 (73,9) | |
| Absceso, n (%) | 60 (34,1) | |
| Microorganismo causal | S. aureus, n (%) | 35 (20,6) |
| S. epidermidis, n (%) | 43 (25,3) | |
| Enterococcus spp, n (%) | 18 (10,6) | |
| Hemocultivos negativos, n (%) | 13 (7,7) | |
| Presentación clínica | Embolia sistémica, n (%) | 62 (34,4) |
| ACVA, n (%) | 40 (22,4) | |
| Insuficiencia renal, n (%) | 26 (14,9) | |
| NHYA >III, n (%) | 132 (74,2) | |
| FEVI, media (DE) | 60,7 (9,2) | |
| Shock, n (%) | 41 (22,8) | |
| Ventilación mecánica preoperatoria, n (%) | 18 (10,1) | |
| Ionotrópicos preoperatorios, n (%) | 39 (21,7) | |
| Cirugía urgente, n (%) | 93 (51,7) |
ACVA: accidente cerebrovascular agudo; DE: desviación estándar; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección de ventrículo izquierdo; n: número de pacientes; NYHA: New York Heart Assotiation scale; %: porcentaje.
De las intervenciones realizadas, en el 32,6% fue sustitución valvular aórtica aislada, en el 30,9% mitral y en el 20,8% de ambas válvulas, siendo en el 15,7% restante otras técnicas quirúrgicas.
La mortalidad en el postoperatorio inmediato observada en nuestra muestra fue del 26,82% (IC95%: 20,74-33,57%).
Características de las EEREISe analizaron un total de 10 EEREI, que incluyeron diferentes variables como factores independientes de mortalidad.
Las EEREI incluidas fueron: STS-IE8, De Feo-Cotrufo14, PALSUSE15, la escala de Costa16, RISK-E score17, AEPEI score18, EndoScore19, SpecificEuroSCOREI yII20 y APORTEI21.
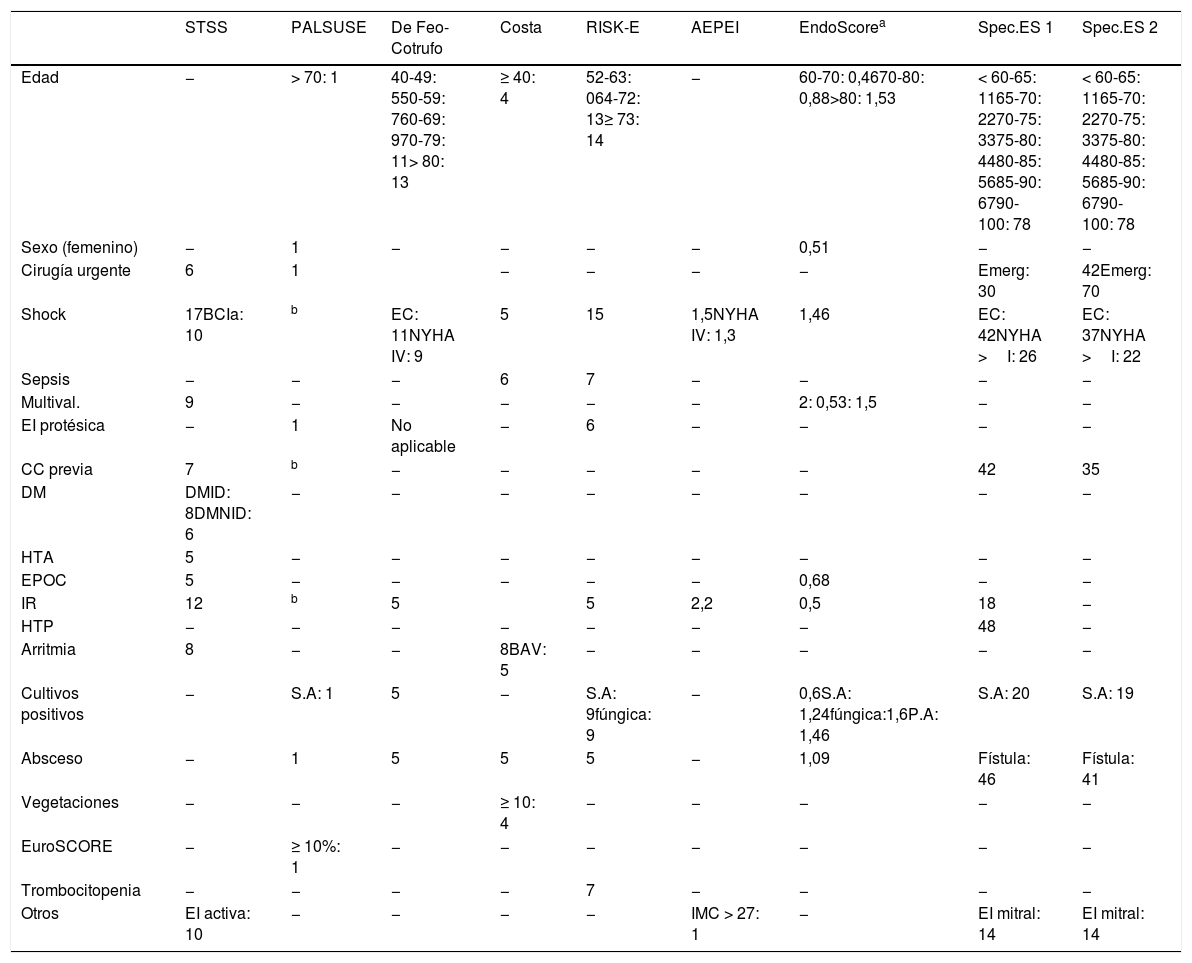
Las variables incluidas en cada una de las 10 EEREI, al igual que la puntuación asignada a cada variable en cada una de las escalas, puede observarse en la tabla 2.
Variables incluidas en las EEREI
| STSS | PALSUSE | De Feo-Cotrufo | Costa | RISK-E | AEPEI | EndoScorea | Spec.ES 1 | Spec.ES 2 | |
|---|---|---|---|---|---|---|---|---|---|
| Edad | − | > 70: 1 | 40-49: 550-59: 760-69: 970-79: 11> 80: 13 | ≥ 40: 4 | 52-63: 064-72: 13≥ 73: 14 | − | 60-70: 0,4670-80: 0,88>80: 1,53 | < 60-65: 1165-70: 2270-75: 3375-80: 4480-85: 5685-90: 6790-100: 78 | < 60-65: 1165-70: 2270-75: 3375-80: 4480-85: 5685-90: 6790-100: 78 |
| Sexo (femenino) | − | 1 | − | − | − | − | 0,51 | − | − |
| Cirugía urgente | 6 | 1 | − | − | − | − | Emerg: 30 | 42Emerg: 70 | |
| Shock | 17BCIa: 10 | b | EC: 11NYHA IV: 9 | 5 | 15 | 1,5NYHA IV: 1,3 | 1,46 | EC: 42NYHA >I: 26 | EC: 37NYHA >I: 22 |
| Sepsis | − | − | − | 6 | 7 | − | − | − | − |
| Multival. | 9 | − | − | − | − | − | 2: 0,53: 1,5 | − | − |
| EI protésica | − | 1 | No aplicable | − | 6 | − | − | − | − |
| CC previa | 7 | b | − | − | − | − | − | 42 | 35 |
| DM | DMID: 8DMNID: 6 | − | − | − | − | − | − | − | − |
| HTA | 5 | − | − | − | − | − | − | − | − |
| EPOC | 5 | − | − | − | − | − | 0,68 | − | − |
| IR | 12 | b | 5 | 5 | 2,2 | 0,5 | 18 | − | |
| HTP | − | − | − | − | − | − | − | 48 | − |
| Arritmia | 8 | − | − | 8BAV: 5 | − | − | − | − | − |
| Cultivos positivos | − | S.A: 1 | 5 | − | S.A: 9fúngica: 9 | − | 0,6S.A: 1,24fúngica:1,6P.A: 1,46 | S.A: 20 | S.A: 19 |
| Absceso | − | 1 | 5 | 5 | 5 | − | 1,09 | Fístula: 46 | Fístula: 41 |
| Vegetaciones | − | − | − | ≥ 10: 4 | − | − | − | − | − |
| EuroSCORE | − | ≥ 10%: 1 | − | − | − | − | − | − | − |
| Trombocitopenia | − | − | − | − | 7 | − | − | − | − |
| Otros | EI activa: 10 | − | − | − | − | IMC > 27: 1 | − | EI mitral: 14 | EI mitral: 14 |
BAV: bloqueo auriculoventricular; BCIa: balón de contrapulsación intraaórtico; DM: diabetes mellitus; DMID: diabetes mellitus insulinodependiente; DMNID: diabetes mellitus no insulinodependiente; EC: estado crítico; EPOC: enfermedad pulmonar obstructiva crónica; HTA: hipertensión arterial; HTP: hipertensión pulmonar, entendida como presión arteria pulmonar ≥55mmHg; IMC: índice de masa corporal; IR: insuficiencia renal considerada como nivel Cr ≥2mg/dl; NYHA: New York Heart Assotiation scale; P.A: Pseudomonas aeruginosa; S.A: Staphylococcus aureus.
La mortalidad estimada por las EEREI resultó fuera del intervalo de confianza del 95% de la mortalidad observada (20,74 a 33,57%) en 5 de las 10 EEREI: STS-EI, De Feo y AEPEI, las escalas de Costa y EndoScore.
La mortalidad estimada por cada una de las EEREI fue:
- 1)
STS-IE score8: estima una mortalidad entre el 5 y el 20%, siendo la media de puntos obtenida 29,94. Conviene destacar que no es posible calcular la mortalidad en afectación mitro-aórtica.
- 2)
Escala de De Feo-Cotrufo14: media de puntos obtenida 19,73, con una mortalidad estimada entre el 7 y el 17%. Además, la escala de De Feo-Cotrufo solamente es aplicable a EI sobre válvula nativa.
- 3)
PALSUSE15: media de puntos 2,5, lo que se corresponde con una mortalidad entre el 15 y el 30%, dado que, según los autores, 2 puntos corresponderían a una mortalidad del 15% y 3 puntos, del 30%
- 4)
Escala de Costa16: predice una mortalidad media del 78,9% para una puntuación media de 20,29 puntos.
- 5)
RISK-E score17: media de puntos obtenida 24,15, lo que se corresponde con una mortalidad de hasta el 30%.
- 6)
AEPEI score18: mortalidad estimada entre el 14,1 y el 18,9% para una media de puntos de 2,42.
- 7)
EndoScore19: media de puntos 0,14 en su modelo de predicción logístico, lo que se corresponde con un 46,5% de mortalidad.
- 8)
SpecificEuroSCOREI yII20: se obtuvo una media de puntos de 149,8 y 124,3, respectivamente, lo que se corresponde en ambos casos con una mortalidad observada entre el 30 y el 40%
- 9)
APORTEI21: Obtuvo una media de puntos de 70, lo que se corresponde con una mortalidad estimada entre el 20 y el 40%.
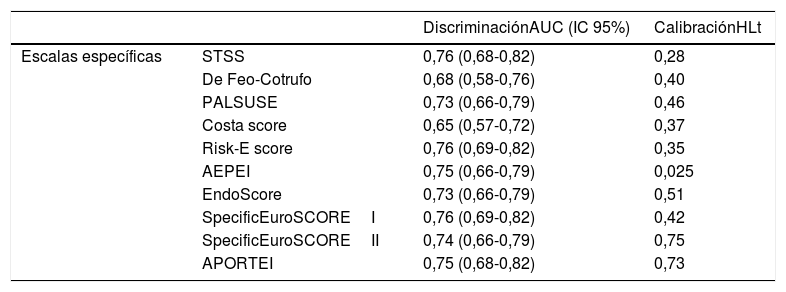
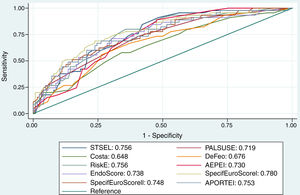
La discriminación y la calibración de las 10 EEREI se muestran en la tabla 3.
Resultados de las validaciones de las EEREI analizadas
| DiscriminaciónAUC (IC 95%) | CalibraciónHLt | ||
|---|---|---|---|
| Escalas específicas | STSS | 0,76 (0,68-0,82) | 0,28 |
| De Feo-Cotrufo | 0,68 (0,58-0,76) | 0,40 | |
| PALSUSE | 0,73 (0,66-0,79) | 0,46 | |
| Costa score | 0,65 (0,57-0,72) | 0,37 | |
| Risk-E score | 0,76 (0,69-0,82) | 0,35 | |
| AEPEI | 0,75 (0,66-0,79) | 0,025 | |
| EndoScore | 0,73 (0,66-0,79) | 0,51 | |
| SpecificEuroSCOREI | 0,76 (0,69-0,82) | 0,42 | |
| SpecificEuroSCOREII | 0,74 (0,66-0,79) | 0,75 | |
| APORTEI | 0,75 (0,68-0,82) | 0,73 |
AUC: área bajo la curva ROC; HLt: test de Homer-Lemeshow; IC95%: intervalo de confianza al 95%.
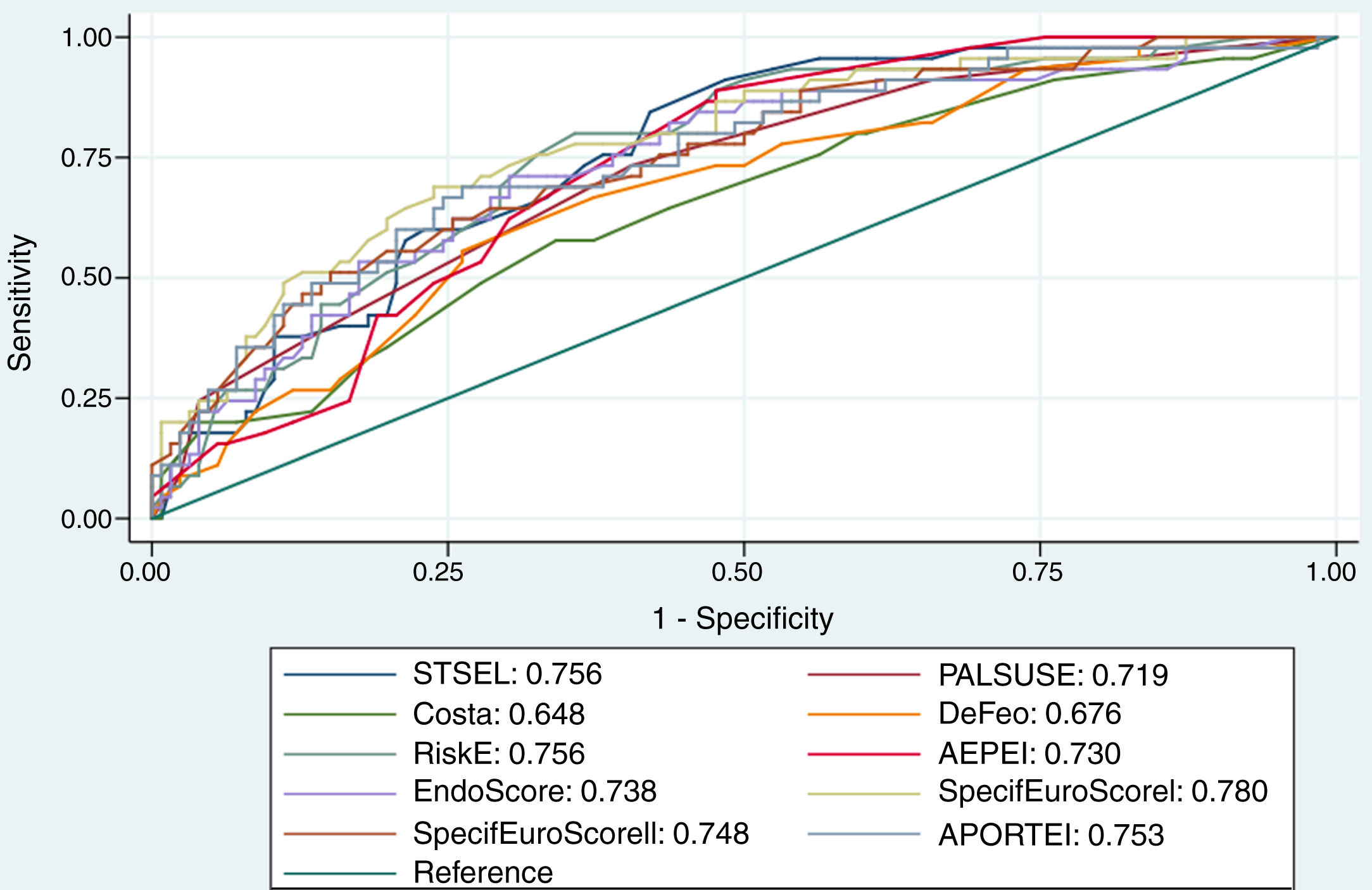
Se puede observar que tanto la discriminación como la calibración fueron óptimas para las EEREI analizadas, salvo en los casos de la escala de Costa, que presentó una baja discriminación (AUC=0,65, IC95%: 0,57-0,72), y AEPEI, donde la calibración fue subóptima (HLt p=0,025).
La discriminación de las 10 EEREI se comparó gráficamente en la figura 1.
DiscusiónLa EI representa una patología grave con una elevada mortalidad, estimada entre el 9 y el 26%22-24. La gran variabilidad en el pronóstico se debe en gran medida a la presencia de factores influyentes en el riesgo quirúrgico, como las comorbilidades de los pacientes, la variabilidad de la respuesta antibiótica, la etiología, la presentación clínica…25. Además de los que podemos considerar factores generales, en EI se conoce de la existencia de lo que llamamos factores de riesgo específicos de EI (abscesos paravalvulares, vegetaciones, dehiscencia protésica, embolia…) o factores independientes de mortalidad, que pueden ser fundamentales a la hora de establecer el riesgo26.
La cirugía cardiaca es el tratamiento de elección en aproximadamente el 20-50% de los casos, pero asocia un alto riesgo por su elevada complejidad. Las indicaciones de llevar a cabo tratamiento quirúrgico se establecen en las Guías de práctica clínica23. Sin embargo, se estima que un alto porcentaje de pacientes con indicación de cirugía según las guías clínicas no son finalmente intervenidos27. Una de las posibles explicaciones es el elevado riesgo asociado a la intervención quirúrgica28 y la gran dificultad técnica que pueden suponer este tipo de cirugías. En cambio, los pacientes con indicación de cirugía que no son finalmente sometidos a procedimiento quirúrgico presentan un pronóstico infausto29. Por el contrario, los estudios realizados en pacientes sometidos a intervención quirúrgica han objetivado una mortalidad a largo plazo aceptable30 una vez superado el postoperatorio inmediato.
En este escenario, valorar el riesgo-beneficio de la cirugía se ha convertido en el objetivo de numerosos estudios, ya que la correcta estimación del riesgo ayuda en la decisión terapéutica en los equipos multidisciplinares y supone una guía en la información facilitada a los pacientes y a sus familiares. La preocupación general de poder objetivar el riesgo quirúrgico se puede observar en la creación de múltiples EEREI en los últimos años. Realizar la validación externa de estas EEREI, además de comprar su capacidad de predicción pronóstica, fueron los objetivos del presente estudio, ya que muchas de las EEREI publicadas solamente disponen de validación interna.
De forma generalizada, las EEREI mejoran la capacidad pronóstica en comparación con los ER clásicos3,5 (EuroSCORE y STS) por la inclusión en su cálculo de factores específicos de EI anteriormente mencionados. Entre las diferentes EEREI desarrolladas hemos analizado:
- 1)
La adaptación de la escala STS, la STS-EI. Al igual que en nuestra muestra, ha demostrado una buena predicción de mortalidad tras validaciones externas5,9, pero presenta el inconveniente de no ser aplicable en el caso de afectación multivalvular, lo que en nuestro caso supone el 26% de la muestra.
- 2)
La escala de De Feo-Cotrufo, exclusiva de EI sobre válvula nativa14 y que en la actualidad es la única que se incluye en las Nuevas Guías de la EACTS23, demostró una infraestimación de la mortalidad en este trabajo.
- 3)
PALSUSE15, con un cálculo sencillo e intuitivo, incorpora la escala clásica EuroSCORE como una de las variables.
- 4)
La escala de Costa16, que en nuestra muestra presentó una baja discriminación (AUC=0,65, IC95%: 0,57-0,72).
- 5)
RISK-E score17: incorpora varios factores no incluidos previamente en el cálculo de riesgo en EI, como la trombocitopenia12,31 y el shock séptico32.
- 6)
AEPEI score18: incluye variables no específicas de EI y aporta el beneficio de un cálculo sencillo, pero en nuestra muestra presentó una mala calibración de la estimación de la mortalidad (HLt p=0,025).
- 7)
EndoScore19: modelo de predicción logístico con un cálculo complicado y que demostró una sobreestimación de la mortalidad en nuestra muestra.
- 8)
SpecificEuroSCOREI yII20: modificaciones de la escala clásica EuroSCORE para hacerla específica de EI.
- 9)
APORTEI21, desarrollada tras una revisión sistemática y metaanálisis26: al contrario de lo que ocurre con otras de las anteriormente mencionadas EEREI, APORTEI fue validada en la cohorte nacional GAMES, tras lo cual se creó una calculadora para facilitar su uso en la práctica clínica habitual.
Además de las EEREI analizadas, debemos destacar otras propuestas recientes que no se adaptaron a la población de nuestro estudio. Entre ellas destacan el ICE score33, creado para estimar la mortalidad a los 6meses en pacientes con tratamiento tanto quirúrgico como antibiótico; el ACEF score34, una combinación de 3 variables como predictor de mortalidad tanto en el postoperatorio inmediato como a largo plazo y también desarrollado incluyendo pacientes no operados, y ANCLA score35, desarrollado a partir de un estudio unicéntrico retrospectivo que combina 5 variables.
Como se ha mencionado previamente, los parámetros incluidos en cada una de las EEREI no son uniformes (tabla 2), lo que hace difícil decantarse por un sistema de predicción del riesgo7. Observamos que el estado preoperatorio crítico, la cirugía de emergencia y el shock cardíaco son predictores casi universales de mal pronóstico después de la cirugía cardíaca, y como consecuencia son variables independientes en todas las EEREI, a pesar de que su peso específico difiere en cada una de ellas. Por ejemplo, en PALSUSE15 la emergencia es una variable independiente secundaria (incluida en el EuroSCORE, que es a su vez un factor de puntuación), mientras que en otras EEREI cobra mayor valor. Por otro lado, en el STS-IE8, en APORTEI21 y en De Feo-Cotrufo14 la condición hemodinámica preoperatoria es el mayor predictor de mortalidad. La presencia de abscesos y destrucción intracardiaca no están presentes en STS-IE ni AEPEI18, pero sí en el resto de EEREI. La presencia de EI protésica es considerada factor de mal pronóstico36,37 pero no es aplicable a la escala de De Feo-Cotrufo, que solo incluye EI nativa. Y la trombocitopenia y el shock séptico cobran especial relevancia en el RISK-E17.
La información sobre el comportamiento de la EI constituye una herramienta fundamental en la toma de decisiones terapéuticas. La validación externa de las EEREI previamente publicadas y su comparación a la hora de predecir la mortalidad pueden proporcionar información relevante y ayudar en la valoración del tratamiento quirúrgico. Tras su estudio en nuestra muestra, observamos diferencias en la precisión de la estimación de mortalidad de las diferentes EEREI. PALSUSE, RISK-E, SpecificEuroSCOREI yII y APORTEI demostraron superioridad frente al resto de EEREI en la predicción de mortalidad.
LimitacionesEs necesario tener en cuenta el limitado tamaño muestral, que solamente incluyó 180 pacientes, y que se trata de un estudio unicéntrico y retrospectivo con sus consiguientes limitaciones a la hora de obtener conclusiones. Al mismo tiempo, se trata de un periodo de tiempo prolongado para el limitado número de intervenciones. La mortalidad global reportada en el estudio es superior a la documentada en la base de datos nacional (cohorte GAMES), que en el periodo 2008-2018 fue del 22,8%.
Las EEREI analizadas presentan importantes diferencias en cuanto a factores incluidos, método de cálculo, estudios de los que derivan, población diana…, por lo que los datos resultantes deben analizarse con precaución. El desarrollo de estudios prospectivos multicéntricos que analicen las diferencias entre las diferentes EEREI podría aportar información relativa al pronóstico y profundizar en el estudio de la EI.
Al mismo tiempo, al tratarse el presente trabajo de un estudio unicéntrico, con un número limitado de pacientes, creemos que nuevos análisis sobre las diferentes escalas creadas podrían ofrecer más datos en cuento a su utilidad en diferentes poblaciones.
ConclusionesDe las 10 EEREI analizadas, PALSUSE, RISK-E, SpecificEuroSCOREI yII y APORTEI demostraron una predicción de mortalidad precisa y una adecuada capacidad predictiva en el postoperatorio inmediato de cirugía cardiaca por endocarditis infecciosa.
PALSUSE demostró una mortalidad predicha media de 15-30%, AUC=0,68 (IC95%: 0,58-0,76) y HLt p=0,46; RISK-E score estimó un mortalidad entre 0 y 30%, AUC=0,76 (IC95%: 0,69-0,82) y HLt p=0,35; SpecificEuroSCOREI yII mostraron una mortalidad estimada del 30-40% y presentaron AUC=0,76 (IC95%: 0,69-0,82) y HLt p= 0,42 en el caso de SpecificEuroSCOREI y AUC=0,74 (IC95%: 0,66-0,79) con HLt=0,75 en el caso de SpecificEuroSCOREII, y APORTEI estimó una mortalidad del 20-40%, AUC=0,75 (IC95%: 0,68-0,82) y HLt p=0,73.
FinanciaciónNo ha habido financiación de ningún tipo.
Conflicto de interesesNo existe conflicto de intereses.
Abstract aceptado como comunicación oral en el próximo XXIVCongreso de la Sociedad Española de Cirugía Cardiovascular y Endovascular (SECCE).