Han transcurrido ya casi 20 años desde la publicación del estudio BARI1. Durante este tiempo, hemos asistido a la comparación de los resultados de la cirugía coronaria (CABG) frente al intervencionismo percutáneo (PCI) a través de múltiples ensayos clínicos, metaanálisis y grandes registros. A pesar del continuo avance tecnológico del PCI (angioplastia simple, stents no recubiertos, stents recubiertos de primera generación, de segunda generación…), y con la argumentación permanente de que los nuevos dispositivos intracoronarios mejoran significativamente los resultados de los anteriores, la realidad continua siendo igual de tozuda: CABG es superior a PCI en la enfermedad coronaria del tronco y/o de los 3 vasos en términos de muerte, infarto y necesidad de nueva revascularización.
Simultáneamente, los cirujanos hemos visto con resignación un incremento en el peso del PCI en las distintas guías de práctica clínica a la hora de establecer el tratamiento más adecuado en la enfermedad coronaria extensa y severa. Esto ha quedado especialmente claro las guías europeas2, donde, en su última versión del 2014, se indica con la misma fuerza de recomendación y similar nivel de evidencia tanto CABG como PCI en determinados subgrupos de la enfermedad del tronco y/o los 3 vasos principales. Una revisión exhaustiva de la bibliografía disponible permite rebatir muchas aseveraciones que se asumen como basadas en evidencia, pero que, tras un análisis riguroso, no pasan de ser meras especulaciones. En este artículo nos vamos a centrar en las recomendaciones realizadas por dichas guías para la enfermedad coronaria estable, aunque en la mayoría de los casos son extrapolables al síndrome coronario agudo sin elevación del ST.
El valor pronóstico de la revascularización en la angina estable en la enfermedad de tronco y/o de 3 vasosLas nuevas guías de 2014 de la ESC/EACTS establecen la indicación pronóstica de revascularización más allá del tratamiento médico óptimo (TMO) con una fuerza de recomendación i y un nivel de evidencia A sin hacer ningún tipo de distinción en la técnica (PCI o cirugía), asumiendo que el impacto es equivalente. Basta con revisar la bibliografía aportada por las mismas3-12 (10 metaanálisis y 67 estudios experimentales u observacionales) para comprobar que el único tratamiento que tiene impacto en la supervivencia y en la incidencia de infarto de miocardio es la cirugía.
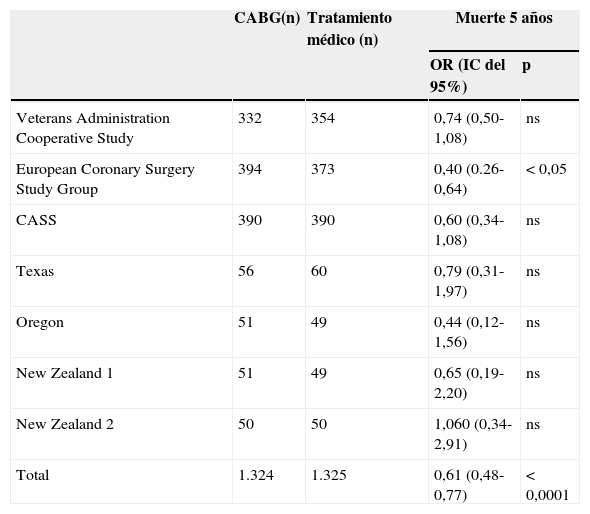
El metaanálisis de Yusuf et al.12 incluyó los 7 ensayos clínicos realizados entre 1972 y 1984 que habían comparado CABG frente a tratamiento médico. Demostró una disminución significativa de la mortalidad a 5, 7 y 10 años, siendo este beneficio mayor en los subgrupos de mayor riesgo (tabla 1). Es importante señalar que en este estudio solo el 50% de los pacientes tenía enfermedad de 3 vasos y únicamente el 10% de los pacientes operados recibió una arteria mamaria. Es cierto que hablamos de ensayos clínicos realizados hace bastantes años, cuando el TMO (inhibidores de la enzima de conversión de la angiotensina, antagonistas de los receptores de la angiotensina II, estatinas y betabloqueantes) no estaba bien establecido y el percutáneo estaba en sus inicios, utilizando técnicas hoy consideradas obsoletas. Pero cuando revisamos la evidencia más reciente, las conclusiones no cambian. En el ensayo clínico BARI-2D13 se aleatorizó a 2.368 pacientes diabéticos a tratamiento médico frente a revascularización. La revascularización fue mediante PCI (con stents convencionales o recubiertos) o CABG atendiendo a los criterios del heart-team local. A los 5 años, el único tratamiento que disminuyó significativamente la incidencia de eventos adversos cardiovasculares mayores fue la cirugía. El estudio FAME 214 aleatorizó a 888 pacientes con al menos un vaso con estenosis funcionalmente significativa (FFR<0,8) a TMO frente a revascularización percutánea con stents recubiertos de segunda generación. Aunque el estudio hubo de ser interrumpido precozmente, la única diferencia detectada a los 12 meses fue una mayor incidencia de necesidad de revascularización urgente en el grupo de TMO. No hubo diferencias en la incidencia de infarto de miocardio ni en la mortalidad. El estudio COURAGE15 aleatorizó a 2.287 pacientes con enfermedad coronaria e isquemia a TMO frente a PCI (la mayor parte con stents convencionales). El 70% de los pacientes tenían enfermedad severa de 2 o 3 vasos, y el 30% lesión en la arteria descendente anterior proximal (DAp). Tras un seguimiento medio de 4,6 años, no hubo diferencias en la incidencia del evento primario (muerte-infarto), ni en la de hospitalizaciones por síndrome coronario agudo. En un metaanálisis5 incluyendo estos estudios, el PCI no disminuyó a los 5 años ni la mortalidad, ni el infarto, ni la necesidad de nueva revascularización, ni la recurrencia de la angina (tabla 2). De hecho, la mayor incidencia de infarto en el grupo de PCI estaba en el límite de la significación (OR 1,24, IC del 95%, 0,99-1,55). Recientemente, Windecker et al.16 han publicado un metaanálisis en red, no incluido en las guías y con todas las matizaciones de esta peculiar metodología (comparaciones múltiples condicionadas), que ahonda en este hecho: el PCI únicamente es capaz de disminuir la necesidad de nueva revascularización, mientras que la cirugía reduce la mortalidad, el infarto y la necesidad de nueva revascularización. Solo al analizar el PCI en función del tipo de dispositivo intracoronario utilizado, y tras múltiples comparaciones indirectas, encontraron una discreta diferencia en la mortalidad a favor de los pacientes tratados con stent de everolimus.
Metaanálisis de cirugía vs. tratamiento médico
| CABG(n) | Tratamiento médico (n) | Muerte 5 años | ||
|---|---|---|---|---|
| OR (IC del 95%) | p | |||
| Veterans Administration Cooperative Study | 332 | 354 | 0,74 (0,50-1,08) | ns |
| European Coronary Surgery Study Group | 394 | 373 | 0,40 (0.26-0,64) | < 0,05 |
| CASS | 390 | 390 | 0,60 (0,34-1,08) | ns |
| Texas | 56 | 60 | 0,79 (0,31-1,97) | ns |
| Oregon | 51 | 49 | 0,44 (0,12-1,56) | ns |
| New Zealand 1 | 51 | 49 | 0,65 (0,19-2,20) | ns |
| New Zealand 2 | 50 | 50 | 1,060 (0,34-2,91) | ns |
| Total | 1.324 | 1.325 | 0,61 (0,48-0,77) | < 0,0001 |
CABG: cirugía coronaria; IC: intervalo de confianza; ns: no significativo; OR: odds ratio.
Tomado de Yusuf et al.12.
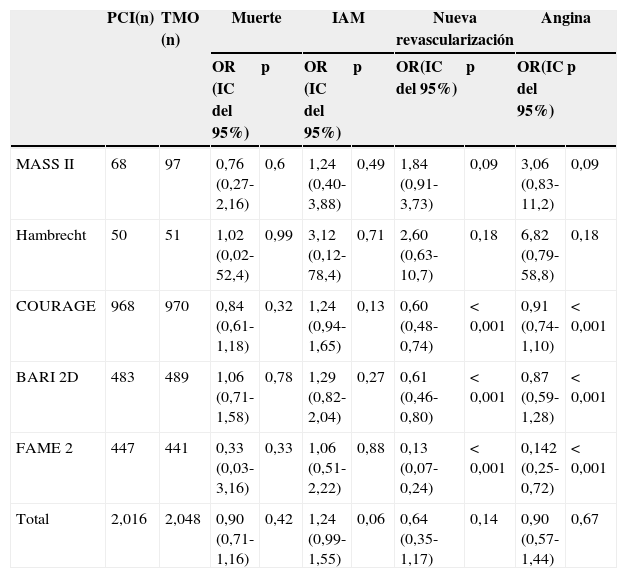
Metaanálisis PCI vs. tratamiento médico
| PCI(n) | TMO (n) | Muerte | IAM | Nueva revascularización | Angina | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| OR (IC del 95%) | p | OR (IC del 95%) | p | OR(IC del 95%) | p | OR(IC del 95%) | p | |||
| MASS II | 68 | 97 | 0,76 (0,27-2,16) | 0,6 | 1,24 (0,40-3,88) | 0,49 | 1,84 (0,91-3,73) | 0,09 | 3,06 (0,83-11,2) | 0,09 |
| Hambrecht | 50 | 51 | 1,02 (0,02-52,4) | 0,99 | 3,12 (0,12-78,4) | 0,71 | 2,60 (0,63-10,7) | 0,18 | 6,82 (0,79-58,8) | 0,18 |
| COURAGE | 968 | 970 | 0,84 (0,61-1,18) | 0,32 | 1,24 (0,94-1,65) | 0,13 | 0,60 (0,48-0,74) | < 0,001 | 0,91 (0,74-1,10) | < 0,001 |
| BARI 2D | 483 | 489 | 1,06 (0,71-1,58) | 0,78 | 1,29 (0,82-2,04) | 0,27 | 0,61 (0,46-0,80) | < 0,001 | 0,87 (0,59-1,28) | < 0,001 |
| FAME 2 | 447 | 441 | 0,33 (0,03-3,16) | 0,33 | 1,06 (0,51-2,22) | 0,88 | 0,13 (0,07-0,24) | < 0,001 | 0,142 (0,25-0,72) | < 0,001 |
| Total | 2,016 | 2,048 | 0,90 (0,71-1,16) | 0,42 | 1,24 (0,99-1,55) | 0,06 | 0,64 (0,35-1,17) | 0,14 | 0,90 (0,57-1,44) | 0,67 |
PCI: intervencionismo percutáneo; IAM: infarto agudo de miocardio; IC: intervalo de confianza; OR: odds ratio; TCI: tronco coronario izquierdo. Tomado de Stergiopoulos et al.5.
Por todo ello, la indicación de revascularización debería ser iA solo para la cirugía (que ha demostrado reducir todos los eventos «duros» respecto de TMO), y iia o iib con nivel de evidencia C (consenso de expertos) para PCI (debido a un beneficio limitado a la reducción del riesgo de reintervención).
Cirugía versus intervencionismo percutáneo según la anatomía coronariaLas indicaciones de revascularización de las guías europeas de 2014 en la enfermedad coronaria estable se estratifican, como en su edición previa de 2010, según la anatomía coronaria (tabla 3).
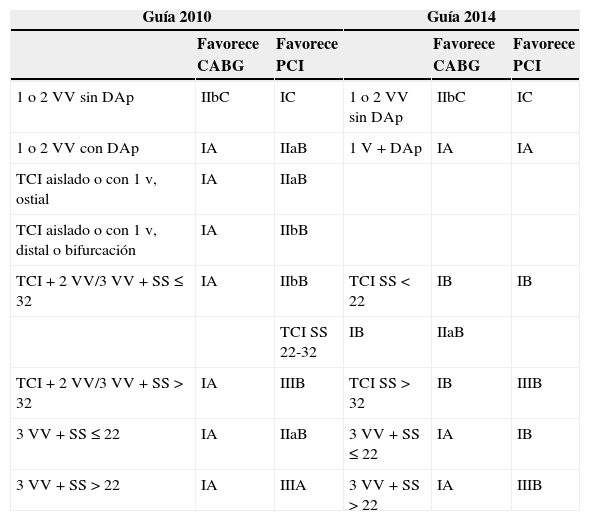
Indicaciones de revascularización
| Guía 2010 | Guía 2014 | ||||
|---|---|---|---|---|---|
| Favorece CABG | Favorece PCI | Favorece CABG | Favorece PCI | ||
| 1 o 2 VV sin DAp | IIbC | IC | 1 o 2 VV sin DAp | IIbC | IC |
| 1 o 2 VV con DAp | IA | IIaB | 1 V + DAp | IA | IA |
| TCI aislado o con 1v, ostial | IA | IIaB | |||
| TCI aislado o con 1v, distal o bifurcación | IA | IIbB | |||
| TCI + 2 VV/3 VV + SS ≤ 32 | IA | IIbB | TCI SS < 22 | IB | IB |
| TCI SS 22-32 | IB | IIaB | |||
| TCI + 2 VV/3 VV + SS > 32 | IA | IIIB | TCI SS > 32 | IB | IIIB |
| 3 VV + SS ≤ 22 | IA | IIaB | 3 VV + SS ≤ 22 | IA | IB |
| 3 VV + SS > 22 | IA | IIIA | 3 VV + SS > 22 | IA | IIIB |
CABG: cirugía; PCI: intervencionismo percutáneo; DAp: descendente anterior proximal; TCI: tronco coronario izquierdo; SS: SYNTAX score; V: vaso; VV: vasos.
Las recomendaciones de 2014 han supuesto un cambio importante respecto de la guía de 201017 en la fuerza de recomendación y el nivel de evidencia asignados al tratamiento percutáneo de la DAp. Así, de una recomendación iiaB ha pasado a iA.
Sin embargo, las referencias que justifican dichas recomendaciones no han cambiado sustantivamente de una guía clínica a la otra. De hecho, los únicos estudios nuevos al respecto son 2 ensayos clínicos de tamaño muestral muy reducido (n<250) que compararon CABG mínimamente invasiva y PCI con stent18,19. Estos 2 estudios no tuvieron potencia para detectar diferencias en el riesgo de infarto o muerte entre PCI y CABG, pero sí un incremento absoluto del riesgo de reintervención del 6,2% a un año y del 23% a 10 años en los pacientes tratados con stent recubierto.
Además de estos 2 nuevos ensayos clínicos, las guías de 2014 fundamentan su recomendación en 4 metaanálisis que ya se incluían en 2010. Dos de esos metaanálisis20,21 (que suponen un nivel de evidencia A) demostraron claros beneficios de CABG sobre PCI en términos de alivio de angina, necesidad de reintervención y riesgo de eventos cardiovasculares mayores. Los otros 2 metaanálisis11,12 no compararon las 2 opciones específicamente en pacientes con enfermedad de la arteria DAp.
En 2010, la indicación de CABG en pacientes con enfermedad de DAp era i en base a su efecto protector frente a PCI en el riesgo de eventos cardio o cerebrovasculares mayores puesto de manifiesto en 2 metaanálisis con miles de pacientes (nivel A).
Dos nuevos pequeños ensayos (nivel B) han demostrado un importante incremento del riesgo de reintervención en PCI, y no han podido detectar diferencias de mortalidad o infarto por tener una potencia muy limitada. Sin embargo, parece que la evidencia de estos 2 pequeños estudios ha convencido al comité de las guías para mejorar la indicación de PCI en el tratamiento de la enfermedad de DAp de iiaB a iA. Objetivamente, como vemos, no se ha producido un incremento sustantivo en la cantidad o calidad de los estudios para mejorar el nivel de evidencia de B a A… y, por esto mismo, tampoco tiene sentido recomendar con idéntica fuerza (i) dos terapias que tienen una eficacia tan dispar en el alivio de la angina o en la reducción de eventos cardiovasculares.
Enfermedad del tronco coronario izquierdoLas nuevas guías han introducido importantes novedades en las indicaciones de la revascularización en la enfermedad del tronco coronario izquierdo (TCI) con respecto a las publicadas en 201017. En 2010, las indicación para CABG en la enfermedad del TCI era iA, independientemente de la anatomía coronaria, mientras que la indicación de PCI variaba en función de la complejidad anatómica entre iiaB y iiiB (tabla 3).
¿Qué ha cambiado desde 2010? Se ha rebajado el nivel de evidencia de la indicación de CABG en la enfermedad TCI (de A a B). Esto viene motivado por una corrección oportuna del peso de bibliografía considerado tradicionalmente: los estudios que han demostrado los beneficios de CABG sobre PCI son ensayos clínicos aislados (nivel B)22-24 y no metaanálisis de los mismos (nivel A). Por el contrario, se ha incrementado la fuerza de recomendación PCI de la enfermedad de TCI con respecto a las guías de 2010. Este incremento es gradual según la complejidad anatómica, de suerte que con el SYNTAX score más favorable (≤ 22), la recomendación es i; en niveles intermedios es iia, y en la anatomía más desfavorable (> 32) está contraindicado (iii).
Este incremento en la fuerza de recomendación de PCI en la enfermedad del tronco con SYNTAX score bajo- intermedio está sustentada en el análisis de: a) los resultados de un subgrupo del ensayo SYNTAX22,23; b) el ensayo PRECOMBAT24; c) otro metaanálisis25 en red de comparaciones indirectas condicionadas con las importantes limitaciones metodológicas que ello supone, y d) un metaanálisis mixto de estudios observacionales, subgrupos de ensayos clínicos y ensayos26. Es decir, las fuentes fundamentales para emitir las recomendaciones actuales son los ensayos SYNTAX22,23 y PRECOMBAT24.
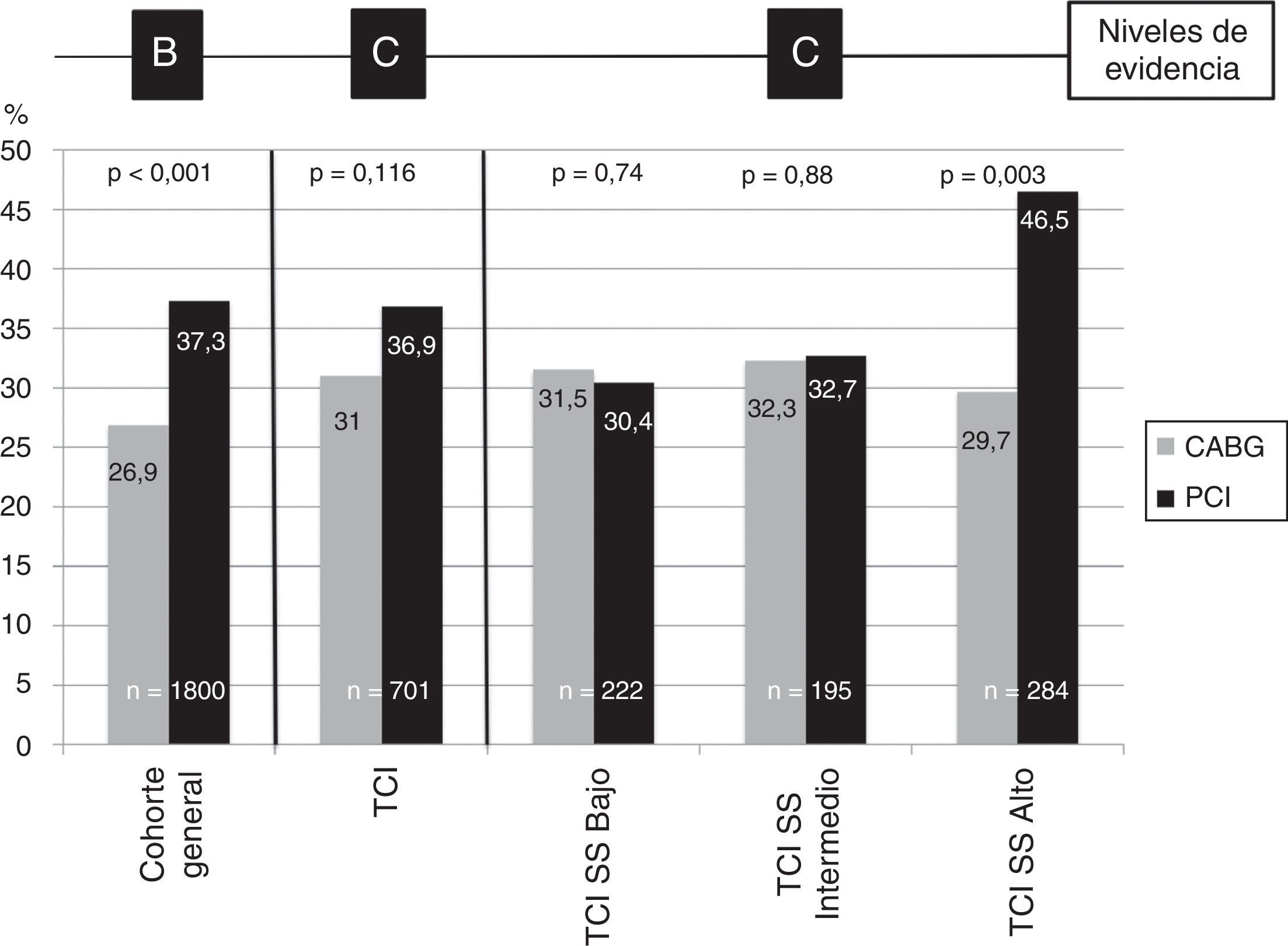
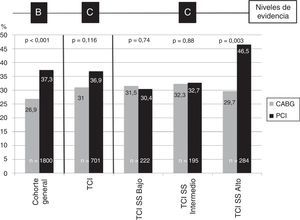
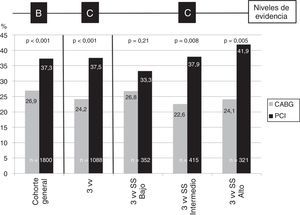
El estudio SYNTAX22 determinó que el riesgo de eventos cardiovasculares de PCI con stents recubiertos fue inferior a CABG en los pacientes con enfermedad de 3 vasos o TCI: nivel de evidencia B, fuerza de recomendación i a favor de CABG. Después de 5 años23, los pacientes sometidos a PCI tuvieron mayor riesgo de infarto (9,7% vs. 3,8%, p<0,001), de reintervención coronaria (25,9% vs. 13,7%, p<0,001), de muerte cardiovascular (9% vs. 5,3%, p=0,003), del evento combinado muerte/ACV/infarto (20,8% vs. 16,7%, p=0,03), y del evento primario (37,3% vs. 26,9%, p<0,001) (fig. 1). Sin embargo, los autores de la guía clínica que nos ocupa obvian esta conclusión (la única a la que se le puede asignar un nivel de evidencia B) y emiten recomendaciones basadas en: 1°) subgrupos del TCI y enfermedad de 3 vasos, y 2) subgrupos de SYNTAX score dentro de esos subgrupos. Así, el análisis del subgrupo de la enfermedad del tronco coronario del ensayo SYNTAX estratificado por los terciles de SYNTAX score no detectó diferencias significativas en la incidencia de MACE en los pacientes con SYNTAX score bajo (CABG 31,5% vs. PCI 30,4%, p=0,74) o medio (CABG 32,3% vs. PCI 32,7%, p=0,88). En el tercil superior, por el contrario, el riesgo fue muy superior en el grupo de PCI (46v5% vs. 29,7%, p=0,003). Este análisis es el que justifica las recomendaciones de la guía de 2014, en las que se incrementa el peso de PCI para tratar pacientes con enfermedad de tronco y SYNTAX score bajo (fuerza i, nivel B), o medio (fuerza iia, nivel B).
Evento primario a 5 años del estudio SYNTAX en la cohorte general y pacientes con enfermedad de tronco coronario.
Frecuencias expresadas en %. n es tamaño muestral de cohorte general o subgrupos. p < 0,05 es significativa.
Arriba: nivel de evidencia que se puede extraer de las comparaciones.
CABG: cirugía coronaria; PCI: intervencionismo percutáneo; TCI: tronco coronario izquierdo; SS: Syntax score.
Tomado de Bittl et al.25.
Desgraciadamente, los resultados de estas comparaciones en subsubgrupos solo pueden interpretarse como hipótesis a demostrar (nivel de evidencia C) y no deben ser puestos al nivel de la evidencia de un ensayo clínico aleatorizado (nivel B) por 4 motivos: a) la hipótesis de no inferioridad de PCI frente a CABG del ensayo SYNTAX no se cumplió; b) la estratificación por subgrupos de SYNTAX score y su análisis no se definieron a priori; c) la potencia estadística de los subgrupos de SYNTAX score de los subgrupos del tronco no fue suficiente para detectar diferencias (el tamaño del subgrupo más grande [tercil > 32] fue de 384 pacientes, con lo que la potencia de su análisis fue inferior a 70%), y d) la reproducibilidad del score SYNTAX es muy pobre27. Por todo esto, la estratificación sobre la base del SYNTAX score de las recomendaciones revascularizadoras en el TCI no mana de un ensayo clínico, sino de hallazgos observacionales, y por ello, su nivel de evidencia es C (acuerdo de expertos).
Por otro lado, el estudio PRECOMBAT24, el otro pilar de estas recomendaciones, no detectó la inferioridad de PCI frente a CABG en pacientes con enfermedad de tronco después de 2 años (12,2% vs. 8,1%, p [no inferioridad] < 0,05). Sin embargo, este estudio tuvo una potencia muy limitada debido a la baja incidencia de eventos en los 2 grupos, una frecuencia excesiva de crossovers de PCI a CABG y un seguimiento muy corto. Por estos motivos, los propios autores del ensayo reconocieron que las conclusiones del estudio no debían servir para tomar decisiones clínicas. Recientemente, se han publicado los resultados a 5 años del ensayo PRECOMBAT, donde se ha detectado, de nuevo sin potencia, un incremento no significativo del riesgo de MACE (17,5% vs. 14,3% p=0,26) y más del doble de reintervenciones (11,4% vs. 5,5%, p=0,012) en el grupo PCI28.
Por último, no existen comparaciones directas en el tratamiento de la enfermedad de tronco entre PCI y TMO, que sí existen en lo que a CABG29 se refiere. Esto limita el conocimiento de la extensión real del beneficio real del tratamiento de PCI en el TCI.
En definitiva, la fuente de evidencia más consistente en las indicaciones de la enfermedad del tronco sigue siendo el estudio SYNTAX. Y en virtud de los resultados de este ensayo clínico (nivel B), CABG sigue siendo preferible a PCI (fuerza i) en la enfermedad de tronco o 3 vasos por una reducción del riesgo de reintervenciones coronarias, infarto miocárdico o muerte cardiovascular. Las distintas fuerzas de recomendación asignadas al PCI en función del SYNTAX score de las guías 2014 no se sustentan en los resultados de ningún ensayo clínico, sino en resultados generadores de hipótesis del estudio SYNTAX (nivel C)… De nuevo, hay que cuestionarse si es correcto asignar fuerzas de recomendación similares (i y iia) para el tratamiento de TCI con SS < 32 a 2 estrategias con eficacia (alivio de angina, reducción del riesgo de infarto y muerte cardiaca) y seguridad (reintervención coronaria) tan dispares.
Enfermedad de 3 vasosLa nueva guía no ha introducido ningún cambio sustancial en las indicaciones de CABG en el tratamiento de la enfermedad de 3 vasos con respecto de la guía de 2010. La nueva evidencia acumulada desde la publicación de la guía de 2010 sigue demostrando un claro beneficio de CABG en términos de supervivencia y libertad de eventos cardiovasculares (fuerza i), mediante ensayos clínicos y metaanálisis firmes (nivel de evidencia A).
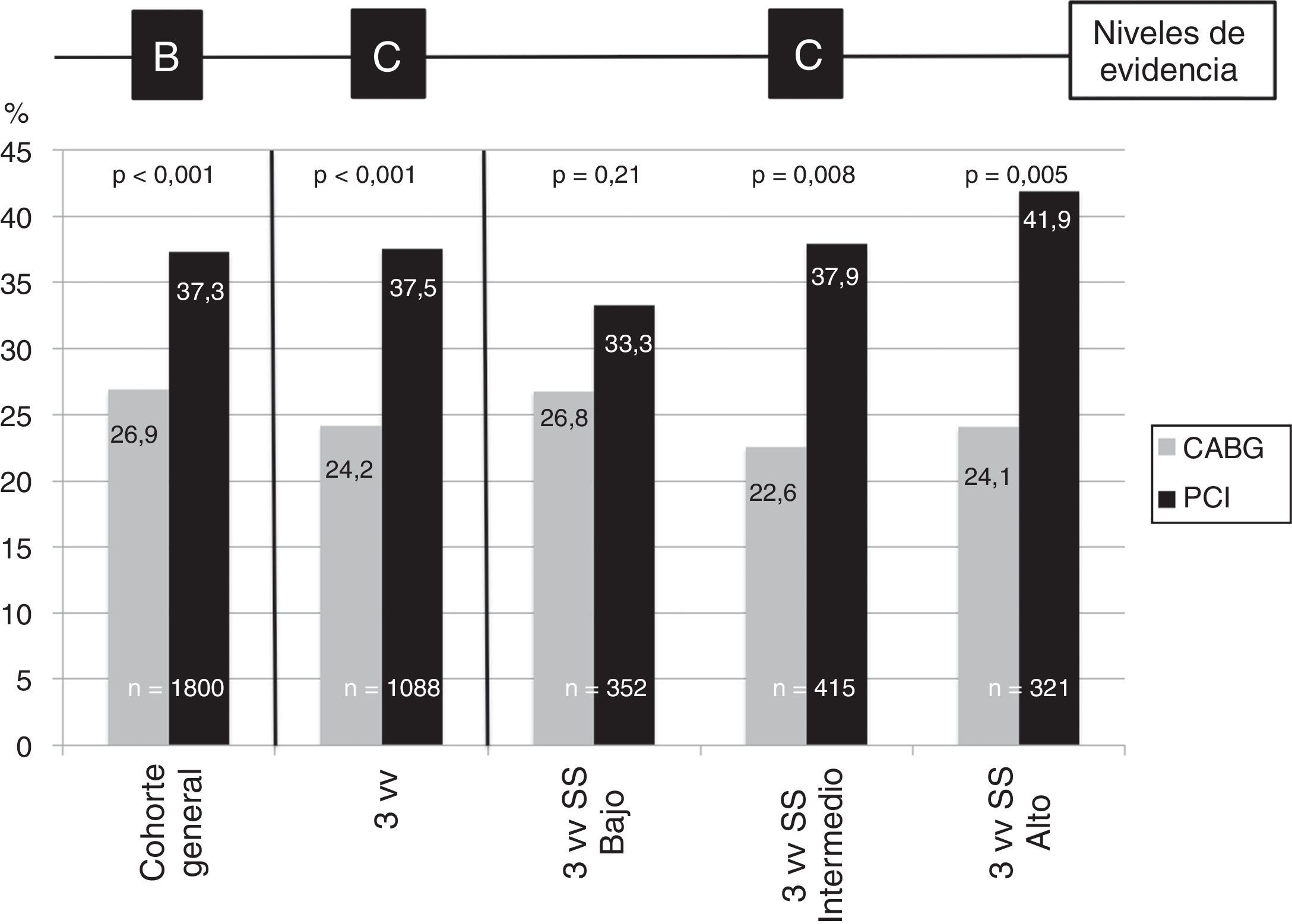
Se mantiene, sin embargo, un aspecto polémico, como es la estratificación de las recomendaciones para PCI en función de la puntuación SYNTAX score (véanse tabla 3 y apartado anterior). Además, se ha incrementado el nivel de recomendación de PCI en la enfermedad de 3 vasos con SYNTAX score bajo de iia a i. El único argumento que puede servir para explicar este cambio es la comunicación de los resultados a 5 años del análisis de los subgrupos de SYNTAX score en el subgrupo de pacientes con enfermedad de 3 vasos30. En el subgrupo de pacientes con 3 vasos, los pacientes sometidos a CABG tuvieron menos riesgo de muerte, muerte cardiovascular, infarto, necesidad de reintervención y del evento combinado. Al estratificar el análisis del subgrupo de los pacientes con enfermedad de 3 vasos por los subgrupos del SYNTAX score, las diferencias entre las PCI y CABG desaparecieron en el estrato con SYNTAX score más bajo. En definitiva, el único argumento a tenor de la evidencia acumulada para incrementar la fuerza de recomendación de PCI en el tratamiento de la enfermedad de 3 vasos con SYNTAX score bajo de iia (guía 2010) a i (guía 2014) es el resultado del análisis de un subgrupo de otro subgrupo, con un tamaño muestral muy reducido, después de una estratificación post hoc y bajo la premisa de que la hipótesis alternativa no se cumplió en el estudio original. Es decir, que las nuevas guías han transformado un hallazgo puramente hipotético, no demostrado por ningún estudio aleatorizado, en una recomendación i con un nivel de evidencia excesivo (B) (fig. 2).
Evento primario a 5 años del estudio SYNTAX en la cohorte general y pacientes con enfermedad de 3 vasos.
Frecuencias expresadas en %. n es tamaño muestral de cohorte general o subgrupos. p < 0,05 es significativa.
Arriba: nivel de evidencia que se puede extraer de las comparaciones.
CABG: cirugía coronaria; PCI: intervencionismo percutáneo; SS: Syntax score; 3vv: 3 vasos.
En febrero del 2014 se publicó el último metaanálisis31 de ensayos aleatorizados que comparaba la mortalidad a largo plazo de CABG y PCI en pacientes con enfermedad de 3 vasos en la era actual. Con 6 ensayos clínicos, más de 6.000 pacientes y 4 años de seguimiento, las conclusiones del estudio fueron rotundas: el PCI aumentaba de forma significativa respecto de la CABG el riesgo de muerte (RR=1,37; p<0,001), infarto (RR=1,72; p<0,001) y reintervención coronaria (RR=3,45; p<0,001), sin existir diferencias significativas en la incidencia de ACV (RR=0,74, p=0,06). A la luz de este metaanálisis y otros previos, el PCI solo debería ser considerado en el caso de que la CABG estuviese contraindicada por cualquier motivo, por lo que no tiene sentido asignar una fuerza de recomendación i a PCI, al mismo nivel que CABG.
Existen 2 argumentos que están ganando peso por parte de la cardiología intervencionista a la hora de justificar los peores resultados del ensayo SYNTAX para PCI: a) los stents recubiertos que se emplearon son peores que los dispositivos recubiertos de everolimus que se utilizan actualmente, y b) la prevalencia de enfermedad multivaso en el SYNTAX pudo estar sobreestimada: las estenosis angiográficas no siempre repercuten funcionalmente en el flujo coronario, de manera que puede que muchas lesiones están siendo sobreestimadas, con lo que la prevalencia real de la enfermedad multivaso sea menor y la indicación del tratamiento percutáneo, más amplia.
El beneficio del stent de everolimus se ha comparado con la cirugía coronaria en un ensayo clínico multicéntrico publicado recientemente: el estudio BEST32. Este estudio demostró que PCI incrementaba el riesgo de infarto, muerte o reintervención coronaria (PCI 15,3% vs. CABG 10,6%, p=0,04) en un estudio con un diseño muy favorable para PCI: se excluyó a pacientes con 2 o más oclusiones completas, con vasos coronarios de menos de 2mm, y más de un 20% de los pacientes tenía enfermedad de 2 vasos. Además, se observó que el riesgo de reintervenciones coronarias debidas a angina en los pacientes tratados con everolimus (11%) fue similar al de los pacientes tratados con stent de placlitaxel (mucho más rudimentario a priori) en el estudio SYNTAX (10,1%). En definitiva, la evidencia más reciente no parece apoyar el aparente beneficio de los stents de everolimus frente a cirugía.
¿Cuál es el papel de los test funcionales de las lesiones coronarias? Podemos asumir que existan lesiones severas angiográficamente que no lo sean funcionalmente y que eso pueda suponer, eventualmente, cambiar un diagnóstico de enfermedad de 3 vasos a enfermedad de 2 o un vaso… ¿pero podemos asumir que, entonces, PCI sea el tratamiento recomendado? La respuesta es no. El cambio en el paradigma diagnóstico de la enfermedad coronaria con el advenimiento del FFR o el IFR exige que el PCI y la CABG vuelvan a ser comparados con esos nuevos métodos diagnósticos, como lo han sido cuando el diagnóstico era anatómico.
El grueso de la evidencia actual más consistente (metaanálisis de ensayos clínicos aleatorizados: nivel A) apoya el tratamiento quirúrgico de la enfermedad de 3 vasos frente a PCI debido a su efecto protector frente al riesgo de infarto, reintervención coronaria o muerte (fuerza de recomendación i). La indicación de PCI con fuerza de recomendación i solo está sustentada por la especulación que mana de análisis de subgrupos de subgrupos muy reducidos, las esperanza depositada en el diseño de nuevos stents y la presión intencionada desde la industria y la cardiología por el cambio en el diagnóstico de la enfermedad coronaria.
Revascularización en diabetesEn el caso de la diabetes, la diferencia entre PCI y cirugía en términos de supervivencia y de incidencia eventos mayores es aún más palmaria si cabe. El estudio FREEDOM33 y un metaanálisis34 reciente han demostrado que, a 5 años, la cirugía disminuye la mortalidad en un tercio frente a la PCI. El estudio FREEDOM aleatorizó a 1.900 pacientes diabéticos con enfermedad multivaso (sin enfermedad de tronco) a CABG frente a PCI con stents recubiertos de paclitaxel o sirolimus. El evento primario (muerte-infarto-ACVA) a los 5 años tuvo significativamente mayor incidencia en el grupo de PCI (26,6% vs. 18,7%, p=0,005). Además, los pacientes sometidos a PCI tuvieron una mayor mortalidad (16,3% vs. 10,9%; p=0,049) y una mayor incidencia de infarto de miocardio (13,9% vs. 6%; p<0,001). Por el contrario, la incidencia de ACVA fue mayor en el grupo de CABG (5,2% vs. 2,4%; p=0,03). Otro aspecto interesante que se debe destacar en este estudio es cómo se modificó la velocidad de la incidencia de los eventos adversos a partir del primer mes. Mientras que en CABG la incidencia de muerte, infarto y ACVA se multiplicó a los 5 años por 6,4, 3,5 y 2,9, respectivamente, en el grupo de PCI lo hizo por 20,4, 7,7 y 8. La publicación de los resultados del estudio FREEDOM tuvo un gran impacto mediático en la prensa americana, que, además, fue seguido de la publicación de muchos otros artículos destacando la sobreutilización en Estados Unidos de PCI.
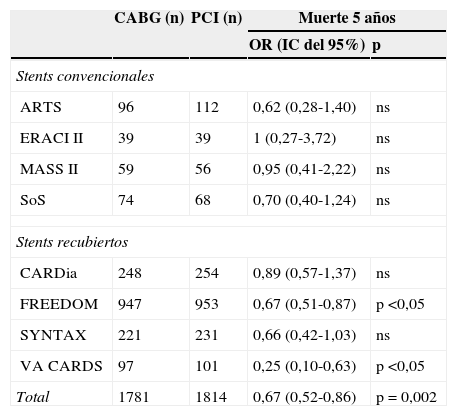
En el año 2014, Verma et al.34 publican un metaanálisis que incluyó a más de 3.500 pacientes de 8 ensayos clínicos, 3 de ellos (CARDia, VA CARDS y FREEDOM) diseñados exclusivamente para pacientes diabéticos. Su conclusión fue: «en la era del tratamiento médico óptimo y de los stents coronarios, la cirugía disminuye en un tercio la mortalidad a los 5 años» (RR = 0,67; IC del 95%, 0,52-0,86, p=0,002) (tabla 4). Por tanto, como señalan las guías, la cirugía en la enfermedad multivaso del paciente diabético tiene una fuerza de recomendación tipo i con nivel de evidencia A.
Metaanálisis CABG vs. PCI en diabetes
| CABG (n) | PCI (n) | Muerte 5 años | ||
|---|---|---|---|---|
| OR (IC del 95%) | p | |||
| Stents convencionales | ||||
| ARTS | 96 | 112 | 0,62 (0,28-1,40) | ns |
| ERACI II | 39 | 39 | 1 (0,27-3,72) | ns |
| MASS II | 59 | 56 | 0,95 (0,41-2,22) | ns |
| SoS | 74 | 68 | 0,70 (0,40-1,24) | ns |
| Stents recubiertos | ||||
| CARDia | 248 | 254 | 0,89 (0,57-1,37) | ns |
| FREEDOM | 947 | 953 | 0,67 (0,51-0,87) | p <0,05 |
| SYNTAX | 221 | 231 | 0,66 (0,42-1,03) | ns |
| VA CARDS | 97 | 101 | 0,25 (0,10-0,63) | p <0,05 |
| Total | 1781 | 1814 | 0,67 (0,52-0,86) | p = 0,002 |
CABG: cirugía coronaria; PCI: intervencionismo percutáneo; IC: intervalo de confianza; ns: no significativo; OR: odds ratio.
Tomado de Verma et al.35.
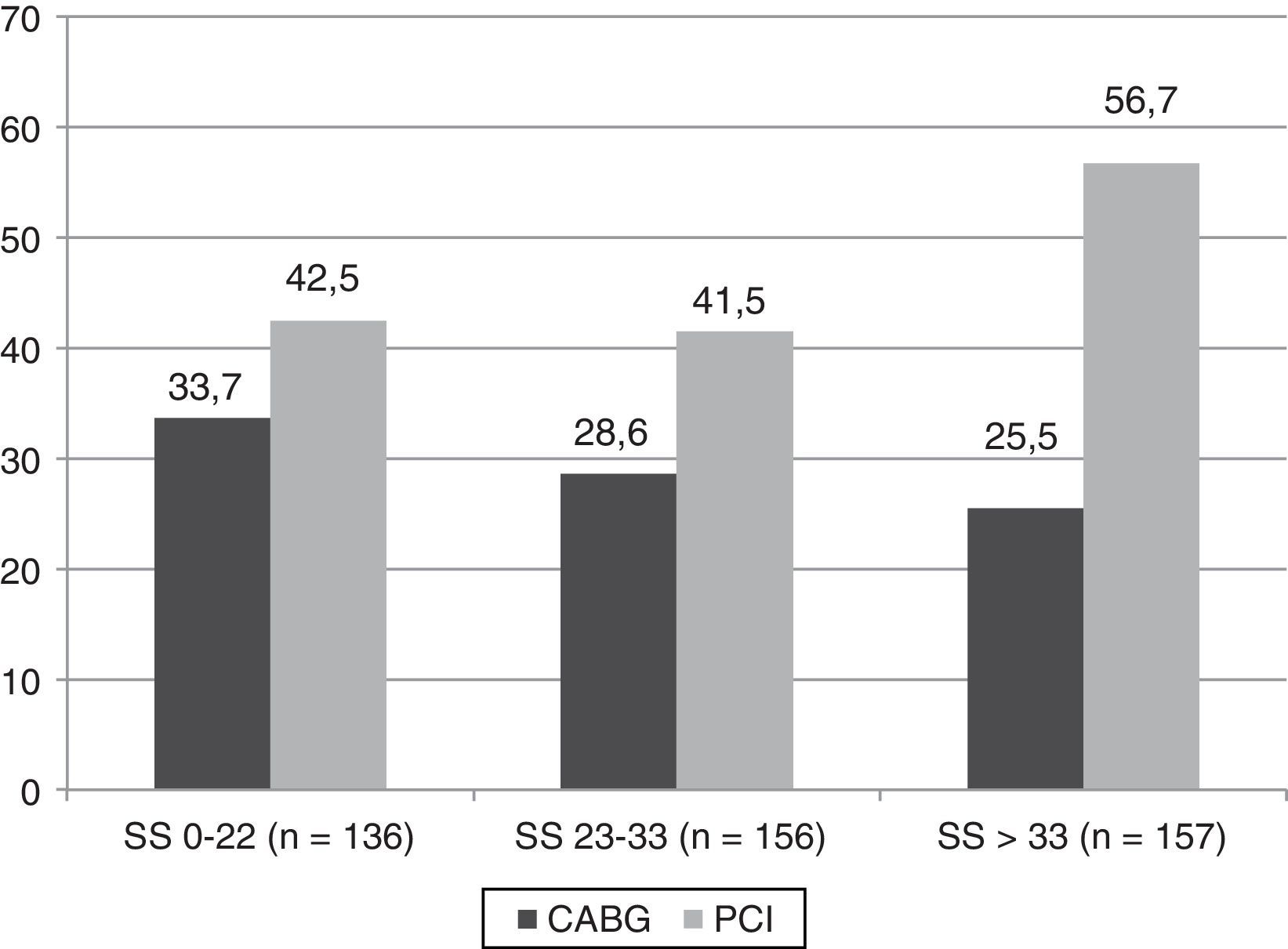
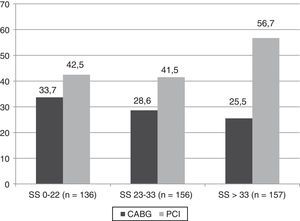
Por todo ello resulta, de nuevo, incompresible que se recomiende en estas guías contemplar el PCI como una alternativa a la cirugía en pacientes diabéticos con enfermedad multivaso y SYNTAX score ≤ 22 (fuerza de recomendación iia y un nivel de evidencia B). Esta recomendación se «justifica» sobre la base de los resultados a 5 años del estudio SYNTAX en el subgrupo de diabéticos35. Los 452 pacientes con diabetes del SYNTAX (de los 1.800 que reclutó) se estratificaron en los 3 terciles de SYNTAX score y solo se observaron diferencias en el subgrupo de SYNTAX score > 32 (fig. 3). Desde el punto de vista metodológico, son conclusiones derivadas del análisis de subgrupos de otros subgrupos y, por lo tanto, como se ha señalado previamente, observacionales (nivel de evidencia C). Pero es que, además, si bien no se encontraron diferencias estadísticamente significativas en los 2 terciles inferiores, estas diferencias sí tuvieron relevancia clínica. La incidencia de eventos fue un 30% mayor en el grupo PCI en el tercil inferior (score<22) (42,5% vs. 33,7%), un 50% en el tercil medio (score 22-32) (41,5% vs. 28,6%) y más de un 100% en el tercil superior (score > 32) (56,7% vs. 25,5%). Si la p no alcanzó significación fue simplemente porque el tamaño muestral fue insuficiente en los 3 terciles (136, 156 y 157 pacientes, respectivamente).
MACE a 5 años en el subgrupo de pacientes diabéticos del estudio SYNTAX. CABG: cirugía coronaria; PCI: intervencionismo percutáneo.
Tomado de Kappetein et al.35.
En resumen, a la luz de la evidencia científica disponible, la cirugía disminuye la incidencia de muerte, infarto y nueva revascularización en la enfermedad de tronco y/o 3 vasos, con o sin diabetes y, por lo tanto, ha de tener una fuerza de recomendación i con nivel de evidencia B para el tronco y A para los 3 vasos. El PCI, por el contrario, debería tener una fuerza de recomendación iib con nivel de evidencia C solo para aquellos pacientes con una anatomía favorable para PCI y riesgo quirúrgico elevado. En el resto de las situaciones, la indicación ha de ser tipo iii con nivel de evidencia A, es decir, una contraindicación formal.
Sin embargo, es obvio que el tratamiento percutáneo de la cardiopatía isquémica ha evolucionado desde su inicio, y lo seguirá haciendo en el futuro. La cirugía coronaria tiene aún argumentos que justifican su superioridad, pero necesita evolucionar para perdurar. El estudio BEST32 ha demostrado un claro beneficio de la cirugía coronaria sobre la última tecnología percutánea (stent recubierto de everolimus), pero a expensas del uso sistemático de más de un injerto arterial (2,1 por paciente), un 72% de revascularizaciones completas y un bajo riesgo de ACV, probablemente debido a un uso mayoritario de cirugía sin circulación extracorpórea (64,3%).
La cirugía cardiaca tiene que asumir que la supervivencia de CABG frente a PCI dependerá de la excelencia de sus resultados, y esta pasa por una selección adecuada de los pacientes, una técnica quirúrgica óptima, asegurar la existencia de unidades de referencia con volúmenes quirúrgicos adecuados, etc… Esta competencia, bien entendida, puede y debe hacernos mejores para seguir ofreciendo al paciente el que siempre ha sido nuestro mejor producto: una revascularización segura, completa y duradera.