El síndrome de la cimitarra es una compleja anomalía congénita del desarrollo pulmonar, infrecuente y de múltiples variables. Se denomina así por su semejanza radiológica con la clásica espada torcida. Su característica definitoria es el drenaje pulmonar anómalo. Se asocia con diversas malformaciones cardiotorácicas y un amplio espectro de manifestaciones clínicas.
Serie de casosSe reporta una serie proveniente de la base de datos del Hospital Infantil de México Federico Gómez, revisión del periodo 2009-2013. Se encontraron nueve pacientes con diagnóstico de síndrome de la cimitarra. Se recabaron del expediente médico las características demográficas, estado clínico y parámetros hemodinámicos reportados.
ConclusionesEn la presente serie llaman la atención ciertas diferencias entre el grupo de estudio y lo reportado en la literatura internacional. Se encontró que la mayoría de los pacientes fueron del sexo femenino, diagnosticados entre el primero y el vigésimo mes de vida. En el momento del estudio estaban asintomáticos; la mitad contaba con antecedentes de enfermedad respiratoria y el total con hipertensión pulmonar. La tercera parte del grupo requirió manejo quirúrgico.
Scimitar syndrome is a rare and complex congenital anomaly of the lung with multiple variables and is named for its resemblance to the classical radiological crooked sword. Its defining feature is the anomalous pulmonary drainage. It is associated with various cardiothoracic malformations and a wide spectrum of clinical manifestations.
Case seriesNine patients diagnosed with scimitar syndrome found in the database of Hospital Infantil de México between 2009 and 2013 were reviewed. Demographic records, clinical status and hemodynamic parameters reported were collected.
ConclusionsThis case series called attention to certain differences between our group of patients and those reported in the international literature. Patients were predominantly female and were diagnosed between 1 and 20 months of life. All were asymptomatic at the time of the study. Half of the patients had a history of respiratory disease and all patients had with pulmonary hypertension. Surgical management was required in on-third of the patient group.
El síndrome de la cimitarra se caracteriza por una conexión anormal entre una o más venas pulmonares y el sistema venoso sistémico. La vena en cimitarra generalmente drena hacia la porción hepática de la cava inferior, pero también puede desembocar en las venas suprahepáticas, la vena porta, la vena ácigos o directamente en la aurícula derecha (provocando un cortocircuito de izquierda a derecha)1.
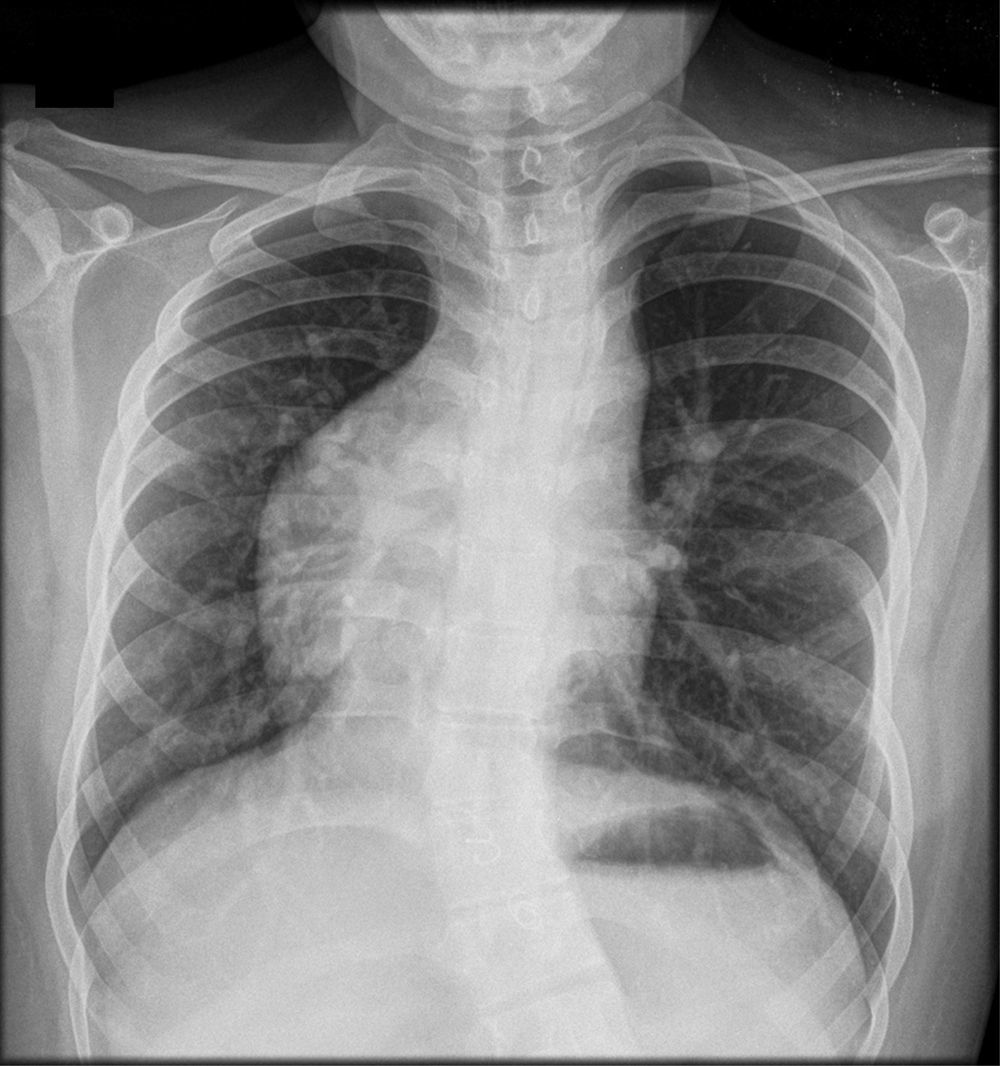
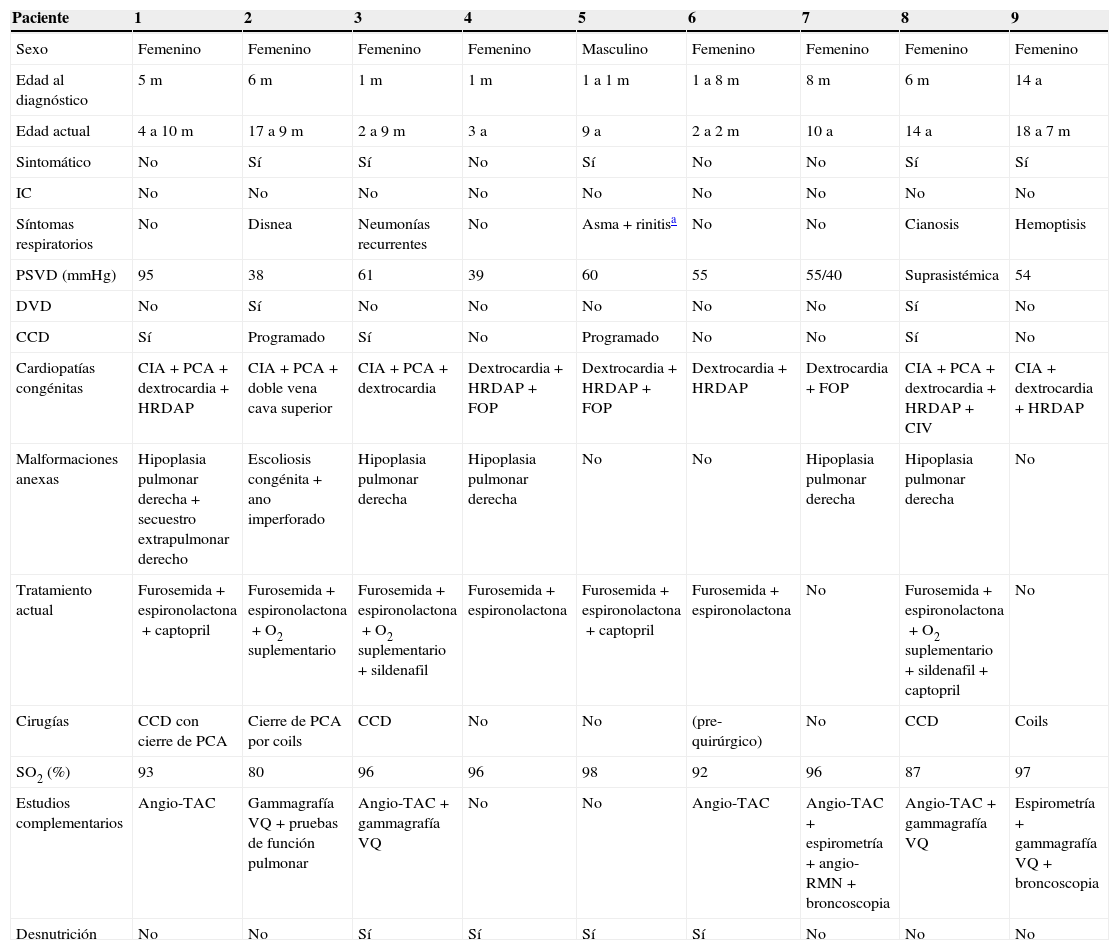
La palabra «cimitarra» proviene de la derivación italiana «scimitarra», del persa shamsir, que se refiere a cualquier sable curvo musulmán u oriental. Se refiere a la opacidad curvilínea que proyecta la vena anómala en la radiografía de tórax, que se extiende hacia abajo desde el hilio pulmonar derecho, bordeando la silueta cardiaca, hasta el ángulo cardiofrénico homolateral, semejando una cimitarra (fig. 1)1.
Radiografía de tórax. Imagen posteroanterior en la que se observa la silueta cardiaca y el ápex hacia la derecha, demostrativa de dextrocardia. También se observa opacidad curvilínea que se extiende del hilio pulmonar derecho, bordeando la silueta cardiaca, hasta el ángulo cardiofrénico homolateral, semejando una cimitarra. Asimismo, se observa escoliosis con convexidad hacia la derecha y asimetría de la caja torácica (imagen correspondiente a paciente femenino de 17 años de edad).
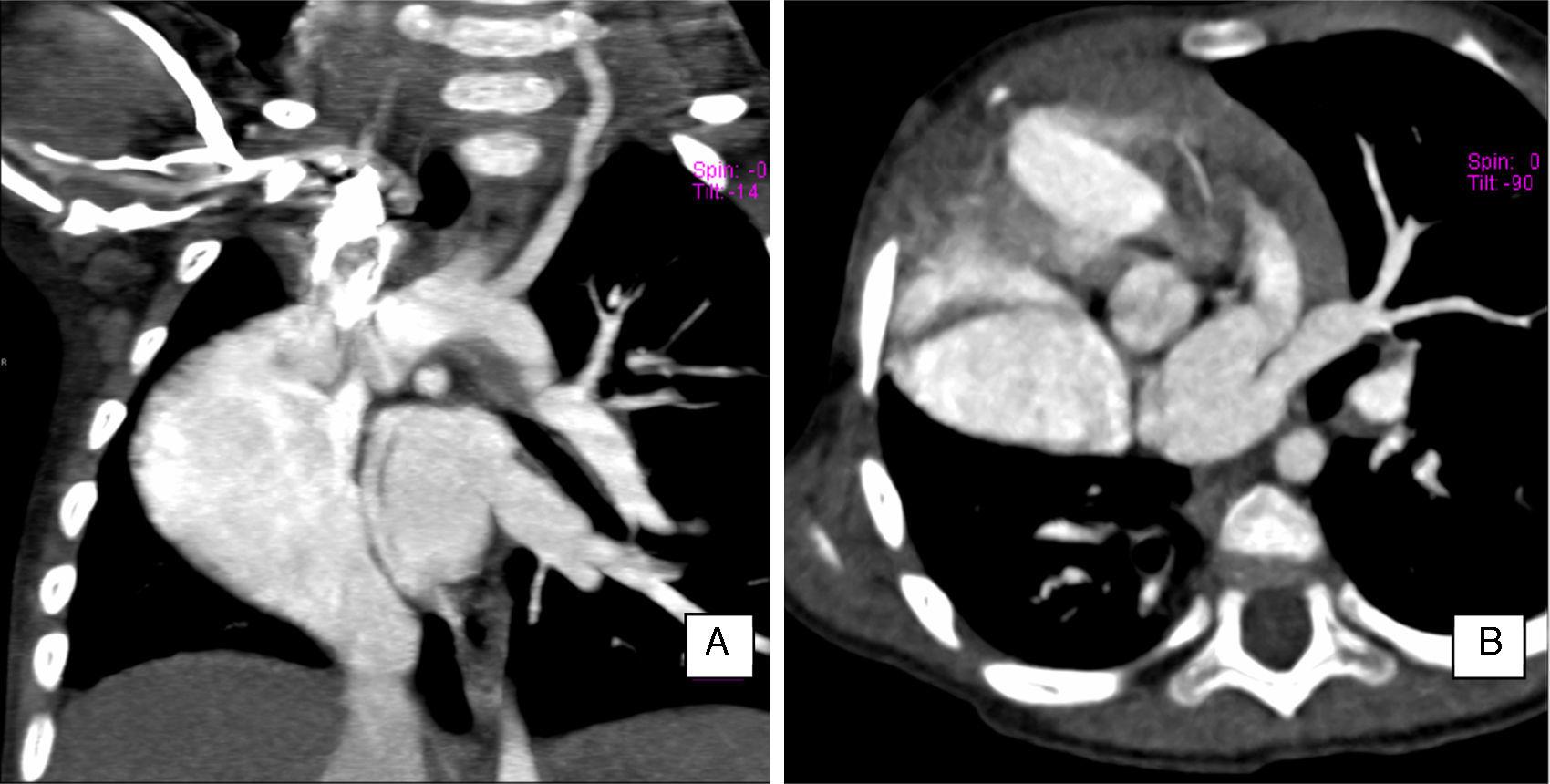
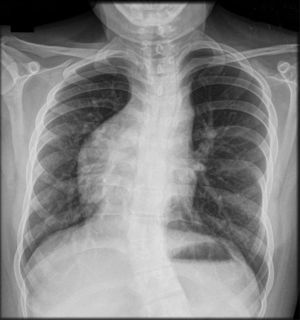
Sin embargo, en algunos casos, el signo de la cimitarra puede estar ausente. Sobre todo en los casos con marcada hipertrofia de la aurícula derecha o en los asociados con dextrocardia e hipoplasia del pulmón derecho que dan lugar al desplazamiento del mediastino a la derecha y a la elevación de la cúpula diafragmática (fig. 2)2,3.
Tomografía de tórax. Ventana para mediastino contrastada: corte coronal (A) y corte axial (B). Se observa dextrocardia e hipoplasia del pulmón derecho, dando lugar a desplazamiento del mediastino a la derecha y ligera elevación de la cúpula diafragmática ipsilateral. Al costado de la silueta cardiaca se aprecia un nicho vascular anormal que corresponde al drenaje venoso anómalo (imagen correspondiente a paciente femenino de 20 meses de edad).
El signo de la cimitarra es uno de los componentes del síndrome del pulmón hipogenético, también conocido como drenaje venoso pulmonar anómalo parcial o síndrome venolobar congénito pulmonar1,4,5.
Constituye el 0.5-2% de las cardiopatías congénitas1 y el 3-5% de los casos de retorno anómalo de venas pulmonares. Se ha descrito una incidencia de 1-3 casos por cada 100,000 recién nacidos vivos6.
Aunque la patogenia no es clara, las múltiples malformaciones pulmonares asociadas parecen evidenciar una alteración del desarrollo de la yema pulmonar en los estadios tempranos de la embriogénesis. Se desconoce el porqué de su localización preferente del lado derecho2. A menudo se asocia con pulmón derecho hipoplásico y arteria pulmonar derecha hipoplásica o ausente2,3. También pueden existir alteraciones traqueobronquiales, ausencia de vena cava inferior y drenaje accesorio2, secuestro pulmonar con irrigación arterial anómala de la aorta o una de sus ramas al pulmón derecho2,7, defectos septales (tanto auriculares como ventriculares), coartación aórtica, dextrocardia, tetralogía de Fallot, conducto arterioso, diafragma accesorio, eventración o hernia diafragmática6. En la literatura se ha reportado la comunicación interauricular en el 60-70% de los casos, y otras cardiopatías congénitas en el 19-31%8.
La edad de diagnóstico es variable. Se puede clasificar como infantil (menores de un año) o en adulto (mayores de un año). En ocasiones, se clasifica un tercer grupo caracterizado por la asociación con anomalías congénitas complejas que modifican los síntomas y la historia natural del síndrome6,9.
La variante infantil presenta peor pronóstico y síntomas más severos, como insuficiencia respiratoria, cianosis, infecciones respiratorias frecuentes y falla de crecimiento. Incluso, se ha reportado bronquitis de repetición asociada con bronquiectasias1,2,6,8.
En el grupo adulto, de pronóstico favorable, el diagnóstico suele ser incidental. Los pacientes se presentan asintomáticos o con síntomas más leves, como soplo cardiaco sistólico, disnea progresiva o infecciones respiratorias de repetición. Se indica el seguimiento clínico de estos pacientes, sin estudios diagnósticos invasivos2,6,8,9.
La asociación con defectos cardiacos se presenta con una frecuencia del 36% en el grupo adulto, y hasta del 75% en la forma infantil. El cuadro clínico depende de la severidad de la disgenesia pulmonar derecha, las infecciones recurrentes, el grado de cortocircuito izquierda-derecha, las cardiopatías congénitas asociadas y la magnitud de la hipertensión pulmonar6. La asociación con estos dos últimos aumenta el riesgo de insuficiencia cardiaca congestiva y muerte8.
En menos del 50% de los casos existen síntomas de hipertensión pulmonar1, aunque esta resulta el factor pronóstico más importante en la evolución del paciente. Puede estar relacionada con resistencias elevadas en el lecho vascular pulmonar (en el que la circulación no se adapta después del nacimiento) y un cortocircuito importante entre arterias anormales originadas en la aorta abdominal que irrigan la parte inferior del pulmón derecho8. Su causa obedece a estenosis de la vena pulmonar anómala (más frecuente), reducción del lecho vascular pulmonar derecho o incremento del flujo sanguíneo pulmonar por la existencia de defectos intracardiacos asociados6.
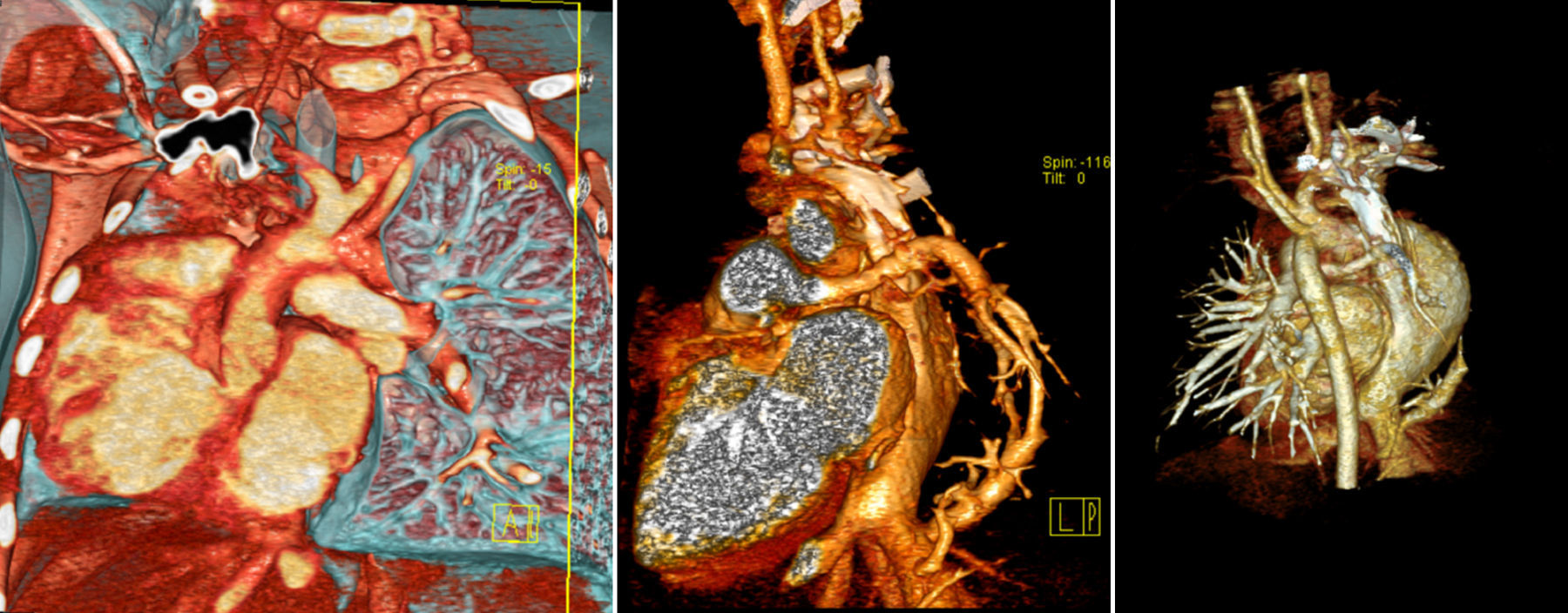
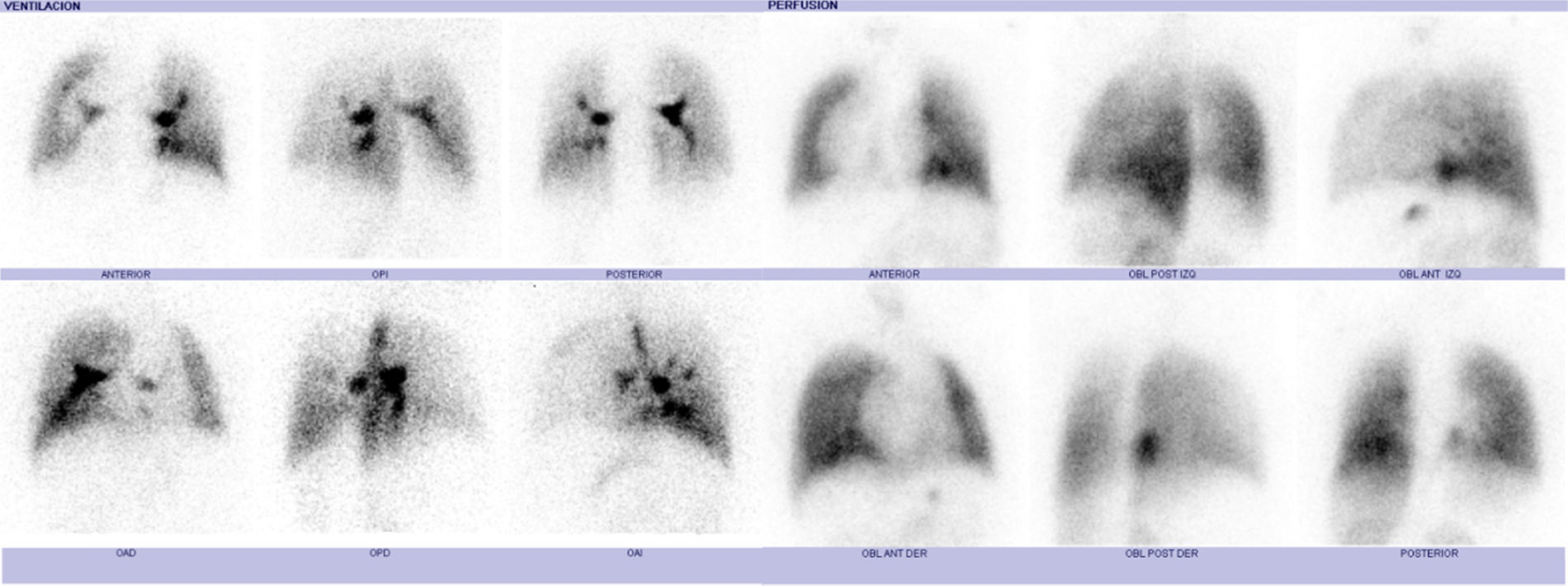
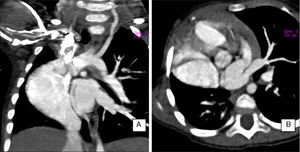
Entre los estudios de imagen complementarios, además de la radiografía de tórax, se encuentran la angiotomografía, que ayuda a detectar anomalías cardiacas, pulmonares y vasculares (fig. 3)2; la gammagrafía de ventilación/perfusión, que informa acerca de las características de perfusión pulmonar (fig. 4); y la resonancia magnética, adecuada para la identificación de arteria aortopulmonar colateral y de anomalías venosas (pulmonares y sistémicas)6.
Angiotomografía de tórax con técnica de reconstrucción. Se observa el drenaje venoso pulmonar anómalo (vena en cimitarra). El estudio corresponde a la misma paciente referida en la figura 2.
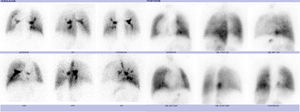
Gammagrafía pulmonar. Se observa ventilación disminuida en pulmón derecho, así como disminución de la perfusión en ambos pulmones con predominio derecho (misma paciente referida en la figura 1).
El diagnóstico puede sospecharse por ecocardiograma fetal. El ecocardiograma bidimensional y el Doppler color podrán valorar la presión pulmonar, el cortocircuito de izquierda a derecha y las cardiopatías asociadas. Sin embargo, el cateterismo cardiaco se considera el estándar de referencia para confirmación diagnóstica (especialmente cuando la cirugía está indicada), además de descartar malformaciones asociadas6. Cuando los síntomas clínicos persisten o empeoran, o si se produce elevación de la presión arterial pulmonar en la determinación indirecta por ecocardiografía bidimensional, se recomienda un estudio angiográfico7,8.
En la mayoría de los pacientes asintomáticos, el síndrome de la cimitarra es manifestación de una lesión aislada; se recomienda manejo conservador ya que el pronóstico es bueno2,6. La corrección de los defectos cardiacos asociados puede proporcionar una evolución benigna comparable con la de las formas aisladas primarias8,10.
La asociación con hipoplasia pulmonar derecha lleva generalmente un flujo sanguíneo bajo, por lo que la corrección quirúrgica del retorno venoso pulmonar anómalo debe considerarse solamente cuando el drenaje en cimitarra cause sobrecarga pulmonar considerable8.
2Serie de casosSe revisó la base de datos del Hospital Infantil de México Federico Gómez de los últimos 5 años. Se encontró el registro de nueve pacientes con diagnóstico de síndrome de la cimitarra que fueron valorados durante el periodo 2009-2013 (tabla 1). En el grupo, ocho pacientes fueron de sexo femenino, con edad entre el primer mes de vida y los 14 años de edad (con una mediana de 6 meses) al momento del diagnóstico, y edad de 3 a 18 años (mediana de 9 años) al momento del estudio.
Pacientes con diagnóstico de síndrome de la cimitarra en el Hospital Infantil de México Federico Gómez, durante el periodo 2009-2013
| Paciente | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
|---|---|---|---|---|---|---|---|---|---|
| Sexo | Femenino | Femenino | Femenino | Femenino | Masculino | Femenino | Femenino | Femenino | Femenino |
| Edad al diagnóstico | 5m | 6m | 1m | 1m | 1a 1m | 1a 8m | 8m | 6m | 14a |
| Edad actual | 4a 10m | 17a 9m | 2a 9m | 3a | 9a | 2a 2m | 10a | 14a | 18a 7m |
| Sintomático | No | Sí | Sí | No | Sí | No | No | Sí | Sí |
| IC | No | No | No | No | No | No | No | No | No |
| Síntomas respiratorios | No | Disnea | Neumonías recurrentes | No | Asma+rinitisa | No | No | Cianosis | Hemoptisis |
| PSVD (mmHg) | 95 | 38 | 61 | 39 | 60 | 55 | 55/40 | Suprasistémica | 54 |
| DVD | No | Sí | No | No | No | No | No | Sí | No |
| CCD | Sí | Programado | Sí | No | Programado | No | No | Sí | No |
| Cardiopatías congénitas | CIA+PCA+dextrocardia+HRDAP | CIA+PCA+doble vena cava superior | CIA+PCA+dextrocardia | Dextrocardia+HRDAP+FOP | Dextrocardia+HRDAP+FOP | Dextrocardia+HRDAP | Dextrocardia+FOP | CIA+PCA+dextrocardia+HRDAP+CIV | CIA+dextrocardia+HRDAP |
| Malformaciones anexas | Hipoplasia pulmonar derecha+secuestro extrapulmonar derecho | Escoliosis congénita+ano imperforado | Hipoplasia pulmonar derecha | Hipoplasia pulmonar derecha | No | No | Hipoplasia pulmonar derecha | Hipoplasia pulmonar derecha | No |
| Tratamiento actual | Furosemida+espironolactona+captopril | Furosemida+espironolactona+O2 suplementario | Furosemida+espironolactona+O2 suplementario+sildenafil | Furosemida+espironolactona | Furosemida+espironolactona+captopril | Furosemida+espironolactona | No | Furosemida+espironolactona+O2 suplementario+sildenafil+captopril | No |
| Cirugías | CCD con cierre de PCA | Cierre de PCA por coils | CCD | No | No | (pre-quirúrgico) | No | CCD | Coils |
| SO2 (%) | 93 | 80 | 96 | 96 | 98 | 92 | 96 | 87 | 97 |
| Estudios complementarios | Angio-TAC | Gammagrafía VQ+pruebas de función pulmonar | Angio-TAC+gammagrafía VQ | No | No | Angio-TAC | Angio-TAC+espirometría+angio-RMN+broncoscopia | Angio-TAC+gammagrafía VQ | Espirometría+gammagrafía VQ+broncoscopia |
| Desnutrición | No | No | Sí | Sí | Sí | Sí | No | No | No |
a: años; Angio-RMN: angiorresonancia; Angio-TAC: angiotomografía de tórax; CCD: cateterismo cardiaco derecho; CIA: comunicación interauricular; CIV: comunicación interventricular; DVD: dilatación de ventrículo derecho; FOP: foramen oval permeable; Gammagrafía VQ: gammagrafía ventilatoria/perfusoria; HRDAP: hipoplasia de rama derecha de arteria pulmonar; IC: insuficiencia cardiaca; m: meses; O2: oxígeno; PCA: persistencia de conducto arterioso; PSVD: presión sistólica de ventrículo derecho; SO2: saturación de oxígeno.
Los nueve pacientes se refirieron asintomáticos en el momento del último reporte en el expediente. Cinco de ellos contaban con antecedentes de enfermedad respiratoria (neumonía recurrente, asma, hemoptisis, disnea), y saturación por oximetría de pulso reportada entre el 80–98% (mediana del 96%) en su última consulta. Cuatro de los pacientes, con diagnóstico de desnutrición.
Todos los pacientes contaron con ecocardiograma. Además, en la última nota médica, todos se reportaron con hipertensión pulmonar (con presión sistólica ventricular derecha de 38-95mmHg). Dos pacientes presentaron dilatación de ventrículo derecho, y tres también contaron con cateterismo cardiaco.
En el grupo se reportó asociación con dextrocardia (en ocho pacientes), hipoplasia de rama derecha de arteria pulmonar (7), hipoplasia pulmonar derecha (5), comunicación interauricular (5), persistencia de conducto arterioso (4), foramen oval permeable (3), secuestro pulmonar (2), comunicación interventricular (1), doble cava superior (1), circulación vicariante de aorta descendente a pulmón derecho (1), escoliosis (1), y ano imperforado (1).
En el momento del estudio, dos pacientes se encontraron con manejo expectante y el resto en tratamiento para hipertensión pulmonar (diurético y/o vasodilatador). De estos, tres se reportaron con oxígeno suplementario en su última visita médica; dos de ellos contaban con cateterismo (de los tres referidos con dicho procedimiento).
Entre los estudios complementarios realizados en el abordaje del grupo se reportaron los siguientes: angiotomografía (5 pacientes), gammagrafía (4), espirometría (3), pletismografía (1), broncoscopia (2) y angiorresonancia (1). No se documentó el diagnóstico por ecocardiograma fetal ni el uso de resonancia magnética.
3DiscusiónEn la presente serie de casos atendidos en el Hospital Infantil de México Federico Gómez se observaron diferencias y similitudes con lo reportado en la literatura internacional.
El grupo estudiado presentó predominio del sexo femenino de 8:1, que difiere de lo reportado en la literatura (1.4:1)6; esto se podría atribuir a lo reducido del grupo.
El promedio en la edad de diagnóstico reportado en la literatura es de 7 meses6; la edad en el momento del diagnóstico en estos pacientes tuvo una mediana de 6 meses y fue tan temprana como el primer mes de vida y tan tardía como un caso diagnosticado a los 14 años de edad. Por lo tanto, en el momento del diagnóstico se compartieron edades tanto del grupo de presentación infantil (66.6%) como de presentación adulta (33.3%).
Mientras que la literatura refiere que cerca de la mitad de los pacientes se mantienen asintomáticos6, la totalidad del grupo se refirió sin síntomas en la última valoración médica. No se presentaron defunciones pese a que dos terceras partes del grupo fueron diagnosticados en la etapa infantil y una tercera parte necesitó tratamiento quirúrgico. Ya que el grupo de estudio pertenece a un hospital de tercer nivel, es imposible aseverar que la razón de no encontrar pacientes sintomáticos fuera porque todos han respondido de manera adecuada al tratamiento ofrecido o porque los pacientes con formas de presentación más graves han fallecido antes de ser referidos a este tipo de nosocomios.
Dentro de los antecedentes de compromiso respiratorio se reportan asma y hemoptisis; la primera no ha sido reportada como parte de la evolución natural de la enfermedad y la segunda se ha asociado a la hipertensión pulmonar más que al síndrome de la cimitarra.
Todos los pacientes de este grupo presentaron hipertensión pulmonar, en comparación con el 60% que se reporta en la literatura6. En igual proporción evidenciaron hipertensión leve, moderada, y severa (tres por cada grupo). No se reportaron pacientes con insuficiencia cardiaca. La diferencia en la cantidad de pacientes con hipertensión pulmonar y la ausencia de insuficiencia cardiaca se pueden relacionar con las cardiopatías congénitas asociadas y el tamaño de la muestra.
En este grupo no se documentó la asociación con alteraciones traqueobronquiales, ausencia de vena cava inferior, coartación de aorta, tetralogía de Fallot, diafragma accesorio, eventración o hernia diafragmática. Se reportó un paciente con ano imperforado, asociación no referida con el síndrome de la cimitarra en la literatura; en dicha paciente, también se documentó doble cava superior y escoliosis (figs. 1–4). El resto de las asociaciones en nuestros pacientes coincide con lo reportado.
Pese a ser una anomalía poco frecuente, es importante recordar que la sospecha diagnóstica se establece a partir de la radiografía simple de tórax (signo de la cimitarra) en pacientes que se presentan desde asintomáticos a gravemente enfermos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.