La insulina degludec es una nueva generación de análogos de insulina ultralenta con un mecanismo de absorción único. El objetivo de este trabajo es revisar las propiedades farmacológicas de la insulina degludec, así como los resultados de eficacia y seguridad obtenidos durante su desarrollo clínico, actualmente en fase iii. Las principales características diferenciales de la insulina degludec frente a los análogos de la insulina de acción prolongada actualmente disponibles radican en sus propiedades farmacológicas. La insulina degludec tiene un perfil de acción ultralento (>24h), estable y sin picos de actividad. Estas propiedades confieren a la insulina degludec un perfil de seguridad con menor riesgo de hipoglucemias nocturnas, sin que ello afecte al control glucémico, que es similar al obtenido con la insulina glargina. En pacientes con diabetes mellitus tipo2, la insulina degludec podría administrarse en intervalos de dosis de flexibles de 8-40h.
Insulin degludec is a new generation of ultra-long acting insulin with a unique mechanism of absorption. The aim of this work is to review the pharmacological characteristics of insulin degludec, as well as the efficacy and safety results obtained during its clinical development, currently in phase iii. The main differential characteristics of insulin degludec compared with long acting insulin analogues currently available are based on its pharmacological properties. Insulin degludec has an ultra-long (>24h), stable and peak-less action profile. These properties provide insulin degludec with a safety profile with a reduced risk of nocturnal hypoglycaemia, without compromising blood glucose control which is similar to insulin glargine. In patients with type2 diabetes mellitus, insulin degludec could be administered at flexible dosing intervals of 8h to 40h.
La prevalencia mundial de diabetes mellitus ha aumentado de forma alarmante durante las últimas 3 décadas (9-10%)1. En países desarrollados este aumento se podría explicar, al menos en parte, por el envejecimiento y el estilo de vida sedentario de la población. En España, la prevalencia de diabetes mellitus es especialmente elevada y afecta actualmente al 14% de la población2.
El descubrimiento de la insulina y su aplicación en la práctica clínica supuso un punto de inflexión en el tratamiento de la diabetes3. Los episodios de hipoglucemia asociados al tratamiento con insulina son su principal limitación, y por ello durante los últimos años se han concentrado todos los esfuerzos en mejorar las propiedades farmacológicas de las insulinas que reduzcan el riesgo de hipoglucemias (evitando los picos de actividad y reduciendo al máximo la variabilidad intraindividuo)4. Además del riesgo bajo de hipoglucemias, otras características que debería tener una insulina ideal son: un efecto hipoglucemiante de al menos 24h con una única administración diaria; bajo riesgo mitogénico; un buen perfil de tolerabilidad, de manera que se reduzca también el riesgo de otros efectos secundarios, como la ganancia de peso; que se pueda utilizar en monoterapia, como parte de una terapia bolo-basal o en combinación con otros antidiabéticos, y que sea igualmente efectiva y segura tanto en la diabetes tipo1 y como en la tipo25,6.
En este contexto, primero se desarrolló la insulina de acción intermedia NPH (Neutral Hagedorn Protamina), cuyo pico de actividad se produce a las 6-8h posteriores a su administración6. Posteriormente se incorporaron a la práctica clínica los análogos de insulina humana, la insulina glargina y la insulina determir, cuya duración máxima de acción es de 24h7,8. Estas insulinas de acción prolongada están asociadas a un menor riesgo de hipoglucemia severa e hipoglucemia nocturna que la insulina NPH, y, en concreto la insulina determir, parece estar también asociada a menor riesgo de ganancia de peso6,9,10.
A pesar de los beneficios añadidos obtenidos con las insulinas de acción prolongada, existen todavía aspectos a mejorar, como es el hecho de que su perfil de acción en el tiempo no es completamente estable, y por tanto todavía existe cierto riesgo de hipoglucemia, y que hay algunos pacientes que precisan 2 inyecciones diarias en lugar de una6,9. Recientemente se ha incorporado a este escenario un nuevo análogo de insulina humana de acción ultralenta, la insulina degludec, cuyo desarrollo clínico está actualmente en fase iii. El objetivo de este trabajo es revisar las propiedades farmacológicas de este nuevo análogo de la insulina basal, así como los resultados de eficacia y seguridad obtenidos en los ensayos clínicos realizados hasta la fecha.
Estructura de la insulina degludecEn el desarrollo de nuevos análogos de insulina basal el principal reto es conseguir un perfil estable sin picos que mimetice en la medida de lo posible la secreción de insulina basal. Los análogos de insulina de acción prolongada disponibles actualmente consiguen este perfil mediante diferentes mecanismos que ralentizan la absorción de la insulina, como la precipitación dependiente del pH (insulina glargina) o la unión local a albúmina (insulina determir). No obstante, el mantenimiento del efecto hipoglucemiante estable durante 24h con una única administración continúa siendo un reto. Para lograrlo de forma holgada, se requeriría un mecanismo de absorción que garantizara un efecto estable durante algo más de 24h11.
La insulina degludec es una nueva generación de análogos de la insulina con un mecanismo de absorción único que le confiere una perfil de acción ultralento y estable11,12. Su estructura se diferencia de la insulina humana en la terminación de la cadena B, en concreto la deleción de treonina en B30 y la adición de un ácido graso de 16C unido a lisina B29 por medio del ácido glutámico. Esta modificación confiere a la insulina degludec propiedades que le permiten formar un depósito soluble de multi-hexámeros tras su administración subcutánea. A partir del depósito subcutáneo, se produce la liberación paulatina de iones de cinc y con ello la disociación gradual de los monómeros de insulina degludec que van pasando a la circulación de forma lenta y sostenida en el tiempo13.
La estructura de la insulina degludec le confiere un perfil farmacológico mejorado con respecto a las insulinas basales existentes, tal y como se describe en el siguiente apartado. Para evaluar las propiedades farmacológicas de la insulina degludec se han llevado a cabo ensayos clínicos en condiciones estables mediante la utilización de la técnica del clamp euglucémico14.
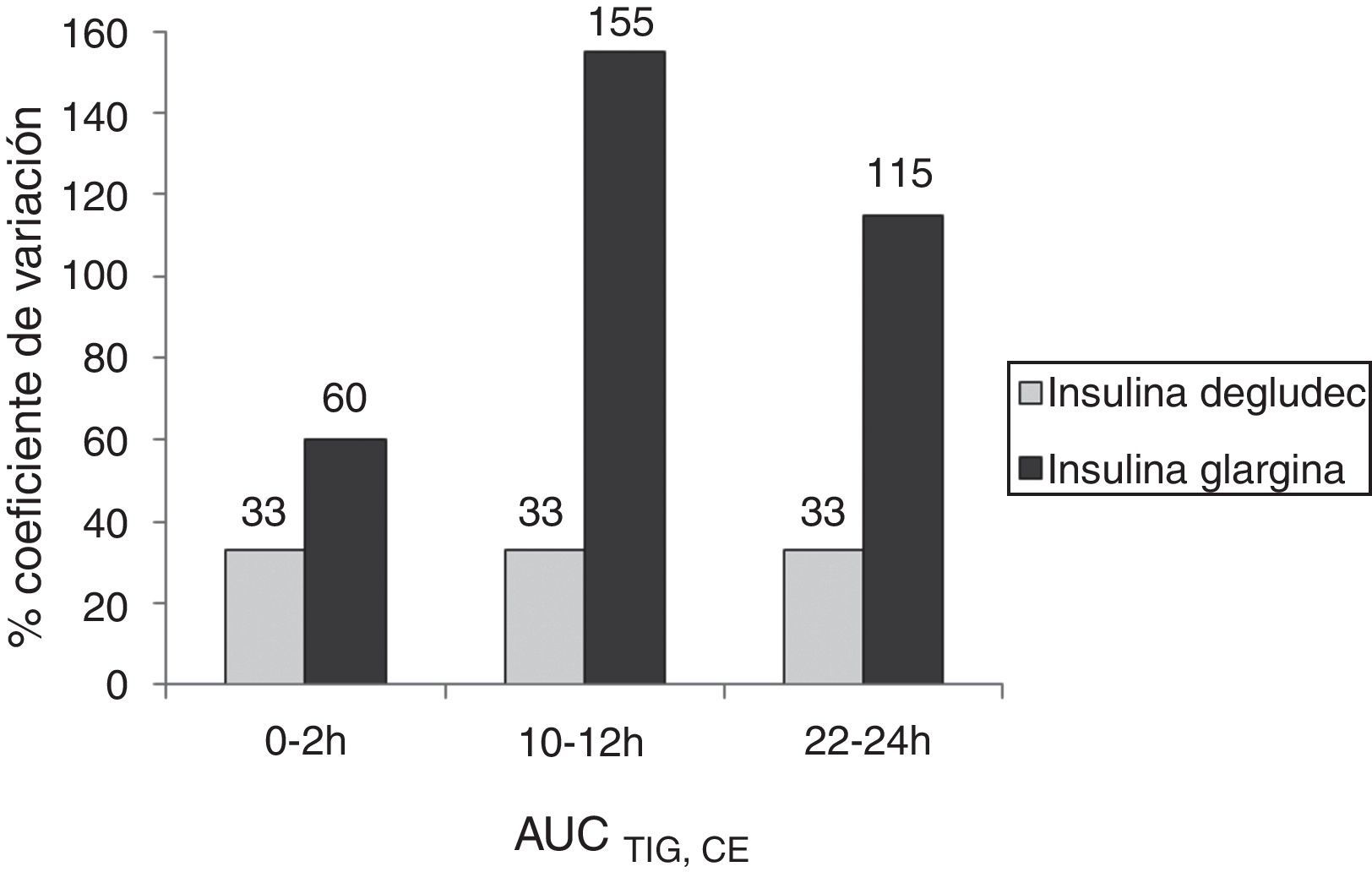
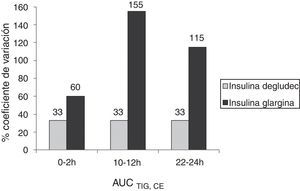
Propiedades farmacodinámicas de la insulina degludecEn un ensayo clínico realizado en pacientes con diabetes mellitus tipo1 en el que se obtuvieron condiciones estables mediante la utilización del clamp euglucémico de 42h, el efecto hipoglucemiante de la insulina degludec (dosis 0,4U/kg, 0,6U/kg, 0,8U/kg, una vez al día durante 8días) se mantuvo durante más de 42h13. En pacientes con diabetes mellitus tipo1 se llevó a cabo otro ensayo clínico doble ciego y cruzado en el cual los pacientes fueron asignados de forma aleatoria a tratamiento con insulina degludec o insulina glargina (dosis de 0,4U/kg, una vez al día) durante 12días y se realizó un clamp euglucémico de 24h los días 6, 9 y 12. Bajo las condiciones estables obtenidas con la técnica del clamp euglucémico, la tasa de infusión de glucosa (TIG) corresponde a la glucosa que utilizan los tejidos, y por tanto nos da una medida de la sensibilidad de los tejidos a la insulina exógena14. El análisis principal de este ensayo clínico demostró que la variabilidad intraindividuo durante un intervalo de 0-24h en condiciones estables (evaluada mediante el área bajo la curva de la TIG, AUCTIR,0-24h,CE) es 4 veces menor con insulina degludec (coeficiente de variación [CV]=20%) que con insulina glargina (CV=82%)15. La variabilidad diaria de la insulina glargina fue significativamente mayor que la de la insulina degludec, se incrementó de forma sustancial a las 6-8h de la administración de la dosis y fue máxima a las 14-16h. El coeficiente de variación de la insulina degludec se mantuvo bajo y constante en el tiempo (CV del 33% para AUCTIR,0-2h, AUCTIR,10-12h, AUCTIR,22-24h), mientras que con insulina glargina fue más elevado y variable en el tiempo (fig. 1)15. El efecto metabólico total (AUCTIR,0-24h,CE) fue mayor con insulina degludec que con insulina glargina, pero no llegó a alcanzar la significación estadística (Ratio IDeg/IGlar de la media geométria de AUCTIR,0-24h,CE=1,34 (intervalo de confianza [IC] del 95%: 0,92-1,95)15.
Las propiedades farmacológicas de la insulina degludec en pacientes con diabetes mellitus tipo2 también se han evaluado en condiciones estables en un ensayo clínico doble ciego y cruzado de 2 periodos16. El objetivo del ensayo era determinar la relación dosis-respuesta de 3 dosis de insulina degludec (0,4U/kg, 0,6U/kg y 0,8U/kg, administradas una vez al día durante 6 días seguidos de un clamp euglucémico de 24h)16. El efecto hipoglucemiante total (AUCTIR,total,CE) aumentó de forma lineal con el incremento de dosis16. El efecto hipoglucemiante de la insulina degludec durante 24h se distribuyó de forma equitativa en las primeras 12h y las siguientes 12h en los 3 niveles de dosis estudiados (AUCTIR,0-12h/AUCTIR,T=0,5)16. De la misma forma, en otro ensayo clínico doble ciego y cruzado en el cual los pacientes con diabetes mellitus tipo1 eran asignados de forma aleatoria a tratamiento con insulina degludec o insulina glargina (0,4U/kg, 0,6U/kg o 0,8U/kg, una vez al día durante 8días), el efecto hipoglucemiante total de la insulina degludec fue parecido durante las primeras y segundas 12h tras la administración de las 3 dosis de insulina degludec (AUCTIG,0-12h/AUCTIG,t∼50:50%), mientras que aproximadamente el 60% de la infusión total de glucosa tuvo lugar durante las primeras 12h con insulina glargina17.
Con respecto al efecto mitogénico, se ha demostrado que la insulina degludec tiene una elevada afinidad por el receptor de insulina y baja afinidad por el receptor IGF-1 (<1% con respecto a la insulina humana), lo que le confiere una actividad mitogénica relativamente baja18.
Propiedades farmacocinéticas de la insulina degludecEl ensayo clínico previamente mencionado17 realizado en pacientes con diabetes mellitus tipo1, en el que se comparaban 3 niveles de dosis de insulina degludec con los mismos niveles de insulina glargina (0,4U/kg, 0,6U/kg o 0,8U/kg, una vez al día durante 8días), cuantificó la distribución de la exposición a la insulina exógena durante el primer intervalo de 12h frente al intervalo completo de 24h (50:50), para lo cual se calculó la razón de la exposición a la insulina (AUC0-12h/AUCt). Los resultados demostraron que la exposición a la insulina degludec fue parecida durante las primeras y segundas 12h para las 3 dosis (AUC0-12h/AUCt∼50:50%), mientras que aproximadamente el 60% de la exposición a la insulina glargina tuvo lugar en las primeras 12h después de la administración17.
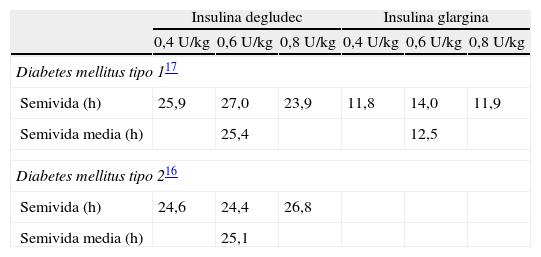
En este ensayo clínico, la semivida de eliminación de los 3 niveles de dosis fue 2 veces superior con insulina degludec que con insulina glargina, con una media de 25,4h para insulina degludec y 12,5h para insulina glargina (tabla 1)17. En pacientes con diabetes mellitus tipo2 se han obtenido resultados similares (25,1h) con los 3 niveles de dosis de insulina degludec (tabla 1)16.
Eficacia y seguridad de la insulina degludec en pacientes con diabetes mellitus tipo1Hasta la fecha disponemos de los resultados de 2 ensayos clínicos para evaluar la eficacia y la seguridad de la insulina degludec como parte de un esquema bolo-basal en pacientes con diabetes mellitus tipo1 (tabla 2). En primer lugar se llevó a cabo un ensayo clínico fase ii, aleatorizado, no enmascarado, de 16 semanas de duración19. El objetivo era comparar, de forma exploratoria, la eficacia, la seguridad y la tolerabilidad de la insulina degludec con la de la insulina glargina, ambas administradas en combinación con insulina aspart en las comidas. Se utilizaron 2 formulaciones de insulina degludec [IDeg A, 600μmol/l; IDeg B, 900μmol/l] (tabla 2) administradas, al igual que la insulina glargina, una vez al día por la noche, preferiblemente a la misma hora todos los días. Los pacientes seleccionados presentaban una Hb1Ac media en vista basal entre 8,3 y 8,5% y una duración media de diabetes mellitus tipo1 de 19-23 años. La mayor parte de los pacientes seleccionados estaban en tratamiento previo con un régimen bolo-basal, con una o 2 inyecciones de insulina basal al día. Los resultados de este ensayo fase ii muestran que la mejoría obtenida en el control glucémico con insulina degludec es similar a la obtenida con insulina glargina, cuando se administran en esquema bolo-basal en combinación con insulina aspart (tabla 2). No obstante, la insulina degludec, en concreto IDeg A (600μmol/l), parece aportar un beneficio añadido al reducirse de forma significativa el riesgo de hipoglucemia nocturna en comparación con la insulina glargina (tabla 2).
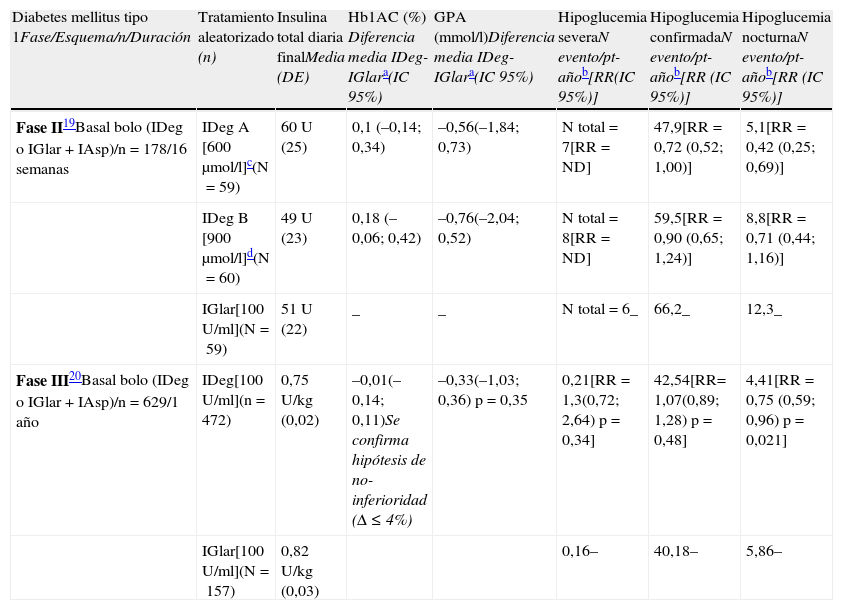
Ensayos clínicos con insulina degludec en la diabetes mellitus tipo 1
| Diabetes mellitus tipo 1Fase/Esquema/n/Duración | Tratamiento aleatorizado (n) | Insulina total diaria finalMedia (DE) | Hb1AC (%) Diferencia media IDeg-IGlara(IC 95%) | GPA (mmol/l)Diferencia media IDeg-IGlara(IC 95%) | Hipoglucemia severaN evento/pt-añob[RR(IC 95%)] | Hipoglucemia confirmadaN evento/pt-añob[RR (IC 95%)] | Hipoglucemia nocturnaN evento/pt-añob[RR (IC 95%)] |
| Fase II19Basal bolo (IDeg o IGlar+IAsp)/n=178/16 semanas | IDeg A [600μmol/l]c(N=59) | 60 U (25) | 0,1 (–0,14; 0,34) | –0,56(–1,84; 0,73) | N total=7[RR=ND] | 47,9[RR=0,72 (0,52; 1,00)] | 5,1[RR=0,42 (0,25; 0,69)] |
| IDeg B [900 μmol/l]d(N=60) | 49 U (23) | 0,18 (–0,06; 0,42) | –0,76(–2,04; 0,52) | N total = 8[RR=ND] | 59,5[RR=0,90 (0,65; 1,24)] | 8,8[RR=0,71 (0,44; 1,16)] | |
| IGlar[100 U/ml](N=59) | 51 U (22) | _ | _ | N total = 6_ | 66,2_ | 12,3_ | |
| Fase III20Basal bolo (IDeg o IGlar+IAsp)/n=629/1 año | IDeg[100 U/ml](n=472) | 0,75 U/kg (0,02) | –0,01(–0,14; 0,11)Se confirma hipótesis de no-inferioridad (Δ ≤ 4%) | –0,33(–1,03; 0,36) p=0,35 | 0,21[RR=1,3(0,72; 2,64) p=0,34] | 42,54[RR= 1,07(0,89; 1,28) p=0,48] | 4,41[RR=0,75 (0,59; 0,96) p=0,021] |
| IGlar[100 U/ml](N=157) | 0,82 U/kg (0,03) | 0,16– | 40,18– | 5,86– |
DE: desviación estándar; GPA: glucosa plasmática en ayunas; IAsp: insulina aspart; IC 95%: intervalo de confianza 95%; IDeg: insulina degludec; IGlar: insulina glargina.
Medida de asociación: riesgo relativo (RR) ajustado = razón de tasas (tasa de incidencia IDeg/tasa incidencia IGlar). Calculado mediante modelo de regresión binomial negativo.
Los resultados exploratorios obtenidos en fase ii son consistentes con los resultados obtenidos en el ensayo clínico fase iii publicados recientemente20. A diferencia del ensayo fase ii, en el cual se permitía cualquier tratamiento previo con insulina y niveles basales de Hb1Ac entre 7 y 11%19, en el ensayo fase iii solo se permitía la inclusión de pacientes que estuvieran previamente en tratamiento con terapia bolo-basal y Hb1Ac ≤10%20. Por otro lado, en el ensayo clínico fase iii la evaluación del tratamiento fue a largo plazo, dado que se trataba de un ensayo de un año de duración20. En este ensayo fase iii se confirmó que la reducción de Hb1Ac obtenida con insulina degludec en combinación con insulina aspart es similar a la obtenida con la misma estrategia bolo-basal basada en insulina glargina (tabla 2). De nuevo, la incidencia de hipoglucemias nocturnas fue significativamente inferior con insulina degludec en comparación con insulina glargina (tabla 2). Con respecto al riesgo de hipoglucemias severas, no se detectaron diferencias significativas entre la insulina degludec y la insulina glargina (tabla 2).
La evidencia disponible hasta ahora demuestra que la insulina degludec, cuando se administra como parte de una terapia bolo-basal en pacientes con diabetes mellitus tipo1, es similar a la insulina glargina en términos de control glucémico y está asociada a un menor riesgo de hipoglucemia nocturna. Cabe esperar que este menor riesgo de hipoglucemia contribuya a mejorar el cumplimiento del tratamiento y, con ello, mejorar el control glucémico en el ámbito de la práctica clínica21. Todo ello redundaría en una mejoría de la calidad de vida de los pacientes, como apuntan los mejores resultados obtenidos con insulina degludec en comparación con insulina glargina en el cuestionario SF-3622.
Eficacia y seguridad de la insulina degludec en pacientes con diabetes mellitus tipo2En pacientes con diabetes mellitus tipo2, se ha comparado la eficacia de la insulina degludec con la de la insulina glargina, utilizando ambas insulinas basales en combinación con metformina23 o con insulina aspart (con o sin antidiabéticos orales)24. Además, se ha evaluado la eficacia de la formulación conjunta de insulina degludec e insulina aspart25, y la posibilidad de flexibilizar la administración de insulina degludec en un intervalo de 8-40h26,27 (tabla 3).
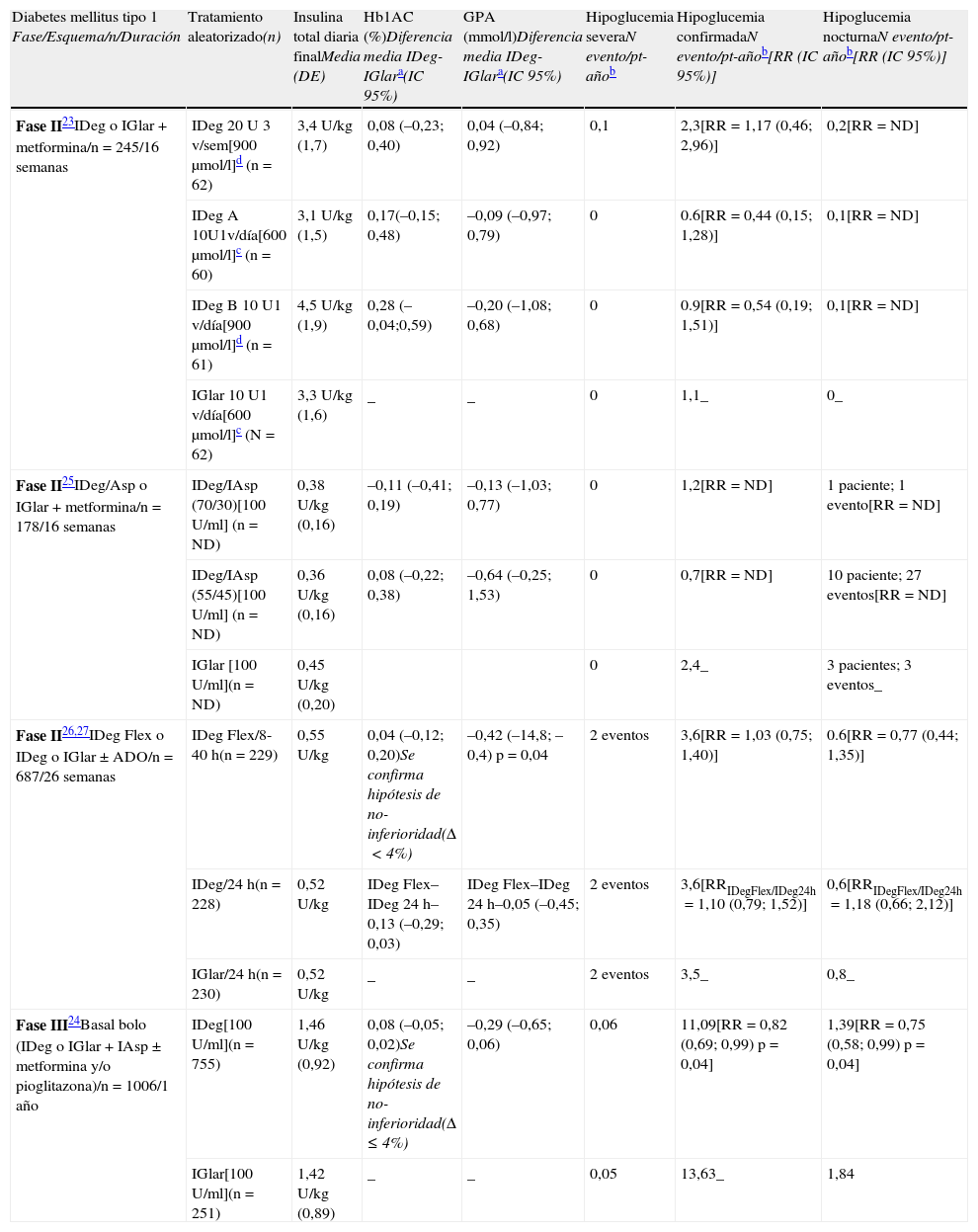
Ensayos clínicos con insulina degludec en la diabetes mellitus tipo 2
| Diabetes mellitus tipo 1 Fase/Esquema/n/Duración | Tratamiento aleatorizado(n) | Insulina total diaria finalMedia (DE) | Hb1AC (%)Diferencia media IDeg-IGlara(IC 95%) | GPA (mmol/l)Diferencia media IDeg-IGlara(IC 95%) | Hipoglucemia severaN evento/pt-añob | Hipoglucemia confirmadaN evento/pt-añob[RR (IC 95%)] | Hipoglucemia nocturnaN evento/pt-añob[RR (IC 95%)] |
| Fase II23IDeg o IGlar+metformina/n=245/16 semanas | IDeg 20 U 3 v/sem[900 μmol/l]d (n=62) | 3,4 U/kg (1,7) | 0,08 (–0,23; 0,40) | 0,04 (–0,84; 0,92) | 0,1 | 2,3[RR=1,17 (0,46; 2,96)] | 0,2[RR=ND] |
| IDeg A 10U1v/día[600 μmol/l]c (n=60) | 3,1 U/kg (1,5) | 0,17(–0,15; 0,48) | –0,09 (–0,97; 0,79) | 0 | 0.6[RR=0,44 (0,15; 1,28)] | 0,1[RR=ND] | |
| IDeg B 10 U1 v/día[900 μmol/l]d (n=61) | 4,5 U/kg (1,9) | 0,28 (–0,04;0,59) | –0,20 (–1,08; 0,68) | 0 | 0.9[RR=0,54 (0,19; 1,51)] | 0,1[RR=ND] | |
| IGlar 10 U1 v/día[600 μmol/l]c (N=62) | 3,3 U/kg (1,6) | _ | _ | 0 | 1,1_ | 0_ | |
| Fase II25IDeg/Asp o IGlar+metformina/n=178/16 semanas | IDeg/IAsp (70/30)[100 U/ml] (n=ND) | 0,38 U/kg (0,16) | –0,11 (–0,41; 0,19) | –0,13 (–1,03; 0,77) | 0 | 1,2[RR=ND] | 1 paciente; 1 evento[RR=ND] |
| IDeg/IAsp (55/45)[100 U/ml] (n=ND) | 0,36 U/kg (0,16) | 0,08 (–0,22; 0,38) | –0,64 (–0,25; 1,53) | 0 | 0,7[RR=ND] | 10 paciente; 27 eventos[RR=ND] | |
| IGlar [100 U/ml](n=ND) | 0,45 U/kg (0,20) | 0 | 2,4_ | 3 pacientes; 3 eventos_ | |||
| Fase II26,27IDeg Flex o IDeg o IGlar±ADO/n=687/26 semanas | IDeg Flex/8-40h(n=229) | 0,55 U/kg | 0,04 (–0,12; 0,20)Se confirma hipótesis de no-inferioridad(Δ<4%) | –0,42 (–14,8; –0,4) p=0,04 | 2 eventos | 3,6[RR=1,03 (0,75; 1,40)] | 0.6[RR=0,77 (0,44; 1,35)] |
| IDeg/24h(n=228) | 0,52 U/kg | IDeg Flex–IDeg 24h–0,13 (–0,29; 0,03) | IDeg Flex–IDeg 24h–0,05 (–0,45; 0,35) | 2 eventos | 3,6[RRIDegFlex/IDeg24h=1,10 (0,79; 1,52)] | 0,6[RRIDegFlex/IDeg24h=1,18 (0,66; 2,12)] | |
| IGlar/24h(n=230) | 0,52 U/kg | _ | _ | 2 eventos | 3,5_ | 0,8_ | |
| Fase III24Basal bolo (IDeg o IGlar+IAsp±metformina y/o pioglitazona)/n=1006/1 año | IDeg[100 U/ml](n=755) | 1,46 U/kg (0,92) | 0,08 (–0,05; 0,02)Se confirma hipótesis de no-inferioridad(Δ ≤ 4%) | –0,29 (–0,65; 0,06) | 0,06 | 11,09[RR=0,82 (0,69; 0,99) p=0,04] | 1,39[RR=0,75 (0,58; 0,99) p=0,04] |
| IGlar[100 U/ml](n=251) | 1,42 U/kg (0,89) | _ | _ | 0,05 | 13,63_ | 1,84 |
DE: desviación estándar; GPA: glucosa plasmática en ayunas; IAsp: insulina aspart; IC 95%: intervalo de confianza 95%; IDeg: insulina degludec; IGlar: insulina glargina.
Medida de asociación: RR (riesgo relativo)=razón de tasas (tasa de incidencia IDeg/tasa incidencia IGlar), a no ser que se especifique otra medida. Calculado mediante modelo de regresión binomial negativo (ajustado).
En el ensayo clínico fase ii en el cual la insulina basal (insulina degludec vs. insulina glargina) se administraba en combinación con metformina durante 16 semanas, el control glucémico obtenido con insulina degludec fue similar al obtenido con insulina glargina, tanto en el grupo de insulina degludec administrada una vez al día como en el grupo de insulina degludec administrada 3 veces al día23 (tabla 3). En la fase iii se confirmó la hipótesis de no-inferioridad del control glucémico obtenido con insulina degludec frente a glargina, cuando ambas insulinas se administraban una vez al día como parte de una terapia bolo-basal en combinación con insulina aspart24. Además, los resultados obtenidos en la fase iii demuestran que la insulina degludec, como parte de un esquema bolo-basal, se asocia a un menor riesgo de hipoglucemias y de hipoglucemias nocturnas que la insulina glargina24 (tabla 3). Por el contrario, la pauta de insulina degludec 3 veces a la semana quedó descartada en la fase iii, porque no se cumplió la hipótesis de no-inferioridad con respecto a la reducción de Hb1Ac frente a la insulina glargina6.
Aunque es evidente que para asegurar el cumplimiento terapéutico la pauta recomendable es una vez al día, las propiedades farmacológicas de la insulina degludec16,17 sugirieron la hipótesis de si seria posible flexibilizar la administración única diaria de insulina degludec de forma que no fuera necesario inyectarla todos los días a la misma hora. Para evaluar esta hipótesis se llevó a cabo un ensayo clínico fase iiia, en el cual, en uno de sus grupos de tratamiento, la inyección diaria de insulina degludec se alternaba de un día para otro entre la mañana y la noche, de forma que los intervalos entre administraciones eran de un mínimo de 8 y un máximo de 40h26,27. En los otros 2 grupos de tratamiento la administración diaria de insulina basal era siempre por la noche (grupo de insulina degludec) o a la misma hora todos los días (grupo de insulina glargina)26,27. Los resultados de este ensayo confirman que con la pauta flexible de insulina degludec (inyectada una vez día, dejando intervalos de 8-40h entre administraciones) se alcanza una reducción de Hb1Ac similar a la obtenida con insulina glargina en la reducción de la Hb1Ac (tabla 3). La reducción de la glucosa plasmática en ayunas fue, incluso, significativamente inferior con la pauta flexible de insulina degludec (tabla 3). La posibilidad de flexibilizar la pauta de administración podría ser de interés en pacientes que, por su trabajo, actividad o estilo de vida, tengan dificultades para inyectarse la insulina todos los días a la misma hora (p.ej., ancianos o personas con importante grado de dependencia). En cualquier caso, es una prueba más de que la actividad de la insulina degludec persiste más allá de 24h, como apuntaban los estudios farmacológicos13, y en este sentido cubre de forma más holgada que el resto de análogos de insulinas basales las necesidades basales de insulina con una única administración diaria.
Tanto la flexibilización de la pauta de administración de insulina degludec como el menor riesgo de hipoglucemias asociado a insulina degludec en pacientes con diabetes mellitus tipo2 demostrados en los ensayos clínicos fase ii y iii son consistentes con las características farmacológicas de la insulina degludec13,16,17 y pueden suponer un beneficio importante en el contexto de la práctica clínica.
ConclusionesLa insulina degludec es una nueva insulina de acción ultralenta que ha demostrado tener una eficacia similar a la insulina glargina pero cuyas propiedades farmacológicas le confieren menor riesgo de hipoglucemias nocturnas, tanto en pacientes con diabetes mellitus tipo1 como en pacientes con diabetes mellitus tipo2. En pacientes con diabetes mellitus tipo2 el riesgo es también menor para las hipoglucemias no severas. El hecho de reducir el número y la severidad de las hipoglucemias es una característica esencial, ya que cada vez existe más evidencia de que las hipoglucemias pueden precipitar episodios cardiovasculares, especialmente en la población diabética de edad avanzada.
El principal reto del tratamiento de la hiperglucemia es alcanzar el umbral de Hb1Ac que reduzca a su vez el riesgo de complicaciones asociadas a la diabetes, sin aumentar con ello el riesgo de hipoglucemias. En este contexto, las guías internacionales de la American Diabetes Association, para las cuales el objetivo de Hb1AC estaba en <7%, han establecido recientemente un objetivo más estricto (<6,5%) para pacientes seleccionados siempre y cuando no suponga un aumento del riesgo de hipoglucemia28. En este escenario, la reducción del riesgo de hipoglucemias asociado a la insulina degludec supone una aportación importante para el arsenal terapéutico de esta enfermedad.
Por otro lado, el menor riesgo de hipoglucemia nocturna convierte a la insulina degludec en una alternativa segura, especialmente para pacientes con diabetes mellitus tipo1 y antecedentes previos de hipoglucemia, para los cuales los análogos de la insulina son el tratamiento de elección28.
Sin embargo, hay que tener en cuenta que los ensayos clínicos en muchas ocasiones no reproducen lo que ocurre en la vida real. Por tanto, serán los estudios post-autorización los que confirmarán o negarán la evidencia que hasta ahora se ha obtenido.
El perfil farmacocinético de la insulina degludec permite que, en pacientes con diabetes mellitus tipo2, el intervalo entre inyecciones pueda llegar a flexibilizarse hasta las 40h sin que se vea afectado el control glucémico, que es similar al obtenido con la insulina glargina. En la práctica clínica, la disponibilidad de insulina degludec abriría nuevas posibilidades de tratamiento para pacientes con dificultad para inyectarse la insulina basal todos los días a la misma hora, lo cual también contribuiría a reducir barreras en la utilización de insulinas y a mejorar el cumplimiento. Sin embargo, de nuevo, serán los estudios post-autorización los que tendrán que validar este aspecto.
En resumen, la evidencia obtenida durante el desarrollo clínico de la insulina degludec demuestra que estamos ante una insulina de acción ultralenta con la que se obtiene un control glucémico similar al obtenido con la insulina glargina pero con unas características farmacológicas novedosas que aportan un beneficio añadido en el perfil de seguridad y en la pauta de administración, que podrían contribuir a mejorar el control glucémico y la calidad de vida de los pacientes en la práctica clínica.
Conflicto de interesesEl Dr. Rafael Simó ha recibido ayudas para la investigación y ha formado parte de consejos asesores de Novo Nordisk, Lilly, Abbott y Novartis. El autor ha contado con el apoyo de Teresa Hernando, de COCIENTE S.L., para la redacción de este manuscrito. Esta ayuda ha sido financiada por Novo Nordisk Pharma S.A., que además ha revisado la fidelidad de la información presentada en este manuscrito.