Determinar la exactitud y el comportamiento de las retinografías realizadas en atención primaria como herramienta de diagnóstico precoz del glaucoma crónico (GAA) en población con factores de riesgo.
DiseñoEstudio observacional, descriptivo y transversal con 2 observadores en paralelo de forma ciega: 2 médicos de atención primaria (MAP) y un oftalmólogo de atención especializada.
EmplazamientoCentro de atención primaria urbano, consultas externas del servicio de oftalmología (hospitalario).
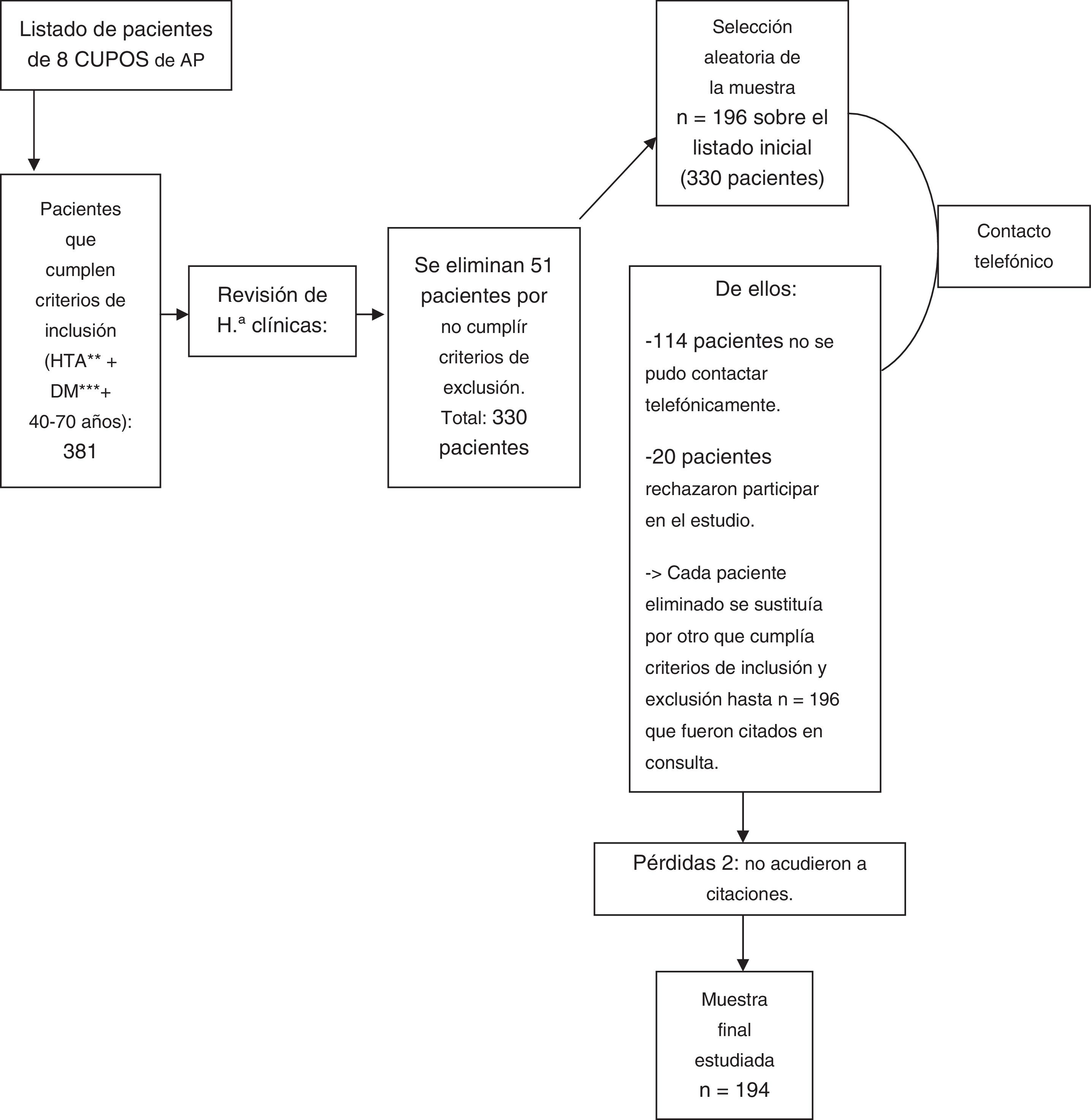
ParticipantesCiento noventa y seis pacientes de ambos sexos, entre 40-70años, diabéticos, hipertensos, no diagnosticados de glaucoma, captados mediante llamada telefónica tras revisión de listados de pacientes. Dos de los pacientes no acudieron a las citaciones para las pruebas oftalmológicas, considerándose como pérdidas.
MedicionesPara la variable cuantitativa diagnóstico de glaucoma por retinografía: exactitud calculada por la sensibilidad y especificidad, comportamiento por los valores predictivos positivo y negativo, cociente de probabilidad positivo y negativo, concordancia interobservador por índices kappa y cociente de correlación intraclase (CCI).
ResultadosSe obtuvo una sensibilidad del 21% (IC95%: 0-43%), especificidad del 93% (IC95%: 89-97%), valor predictivo negativo del 94% (IC95%: 90-97%) y positivo del 20% (IC95%: 0-40%); cociente de probabilidad positivo de 3,07 (IC95%: 0,98-9,62) y negativo de 0,84 (IC95%: 0,64-1,11). El CCI fue de 0,653 (IC95%: 0,495-0,769), y el índice kappa, de 0,140 (ET: 0,106).
ConclusionesLa retinografía no presenta un comportamiento adecuado como herramienta de diagnóstico precoz de GAA desde atención primaria según el modelo planteado en nuestro estudio. Serían necesarios ajustes que subsanasen su baja sensibilidad, como usar otras pruebas combinadas y mejorar el entrenamiento de los MAP.
The aim of this study is to determine usefulness, validity of retinographies performed in Primary Care as a tool for early diagnosis of open-angle chronic glaucoma (OAG).
DesignAn observational, descriptive and cross-sectional study with two blinded parallel observers: 2 general practitioners and 1 ophthalmologist.
LocationUrban Primary Care Health Centre, and the Ophthalmology Department outpatient clinic.
ParticipantsA total of 196 patients of both genders, between 40-70years, with diabetes and hypertension, and undiagnosed with glaucoma, were recruited by phone call after checking patient lists. Two patients that did not arrive for their appointments for the ophthalmology tests were considered as losses.
MeasurementsFor the quantitative diagnostic variable of glaucoma: Accuracy calculated from the sensitivity and specificity, safety from the positive and negative predictive values and the positive and negative probability ratio; interobserver concordance by Kappa index ratio and the intraclass correlation (IC).
ResultsThe retinography for OAG screening has a sensitivity of 21% (95%CI: 0-43%), a specificity of 93% (95%CI: 89-97%), a negative predictive value of 94% (95%CI: 90-97%), and positive of 20% (95%CI: 0-40%); positive probability ratio of 3.07 (95%CI: 0.98-9.62) and negative 0.84 (95%CI: 0.64-1.11). The IC was 0.653 (95%CI: 0.495-0.769) and kappa index of 0.140 (0.106ET).
ConclusionsAccording to this proposed model, retinography is not a useful tool for the early diagnosis of OAG in Primary Care, as it is not safe enough. Before it can be used, it would need adjustments for its low sensitivity, and the use other combined tests. The training of general practitioners would also need to be improved.
Según la Academia Americana de Oftalmología (AAO), el glaucoma de ángulo abierto (GAA) es una neuropatía óptica multifactorial que produce pérdida progresiva de fibras del nervio óptico1. Genera déficits campimétricos, siendo la ceguera su estadio final1-7. Su etiología se relaciona con un defecto de perfusión ocular. En su desarrollo influyen múltiples factores, como los factores de riesgo cardiovascular1,2,5. Se considera la segunda causa de ceguera a nivel mundial. Su infradiagnóstico se estima en el 50%1-5,8,9. En occidente la prevalencia del GAA es del 2,1% a partir de 40años, del 7% a partir de los 80años y del 17,3% en población diabética10,11. En España existen 250.000 casos de GAA y unos 66 millones a nivel mundial3,12,13.
Su diagnóstico se basa en el estudio de la papila mediante la evaluación del campo de visión y el estudio descriptivo papilar. En 1967 Armaly14 desarrolló el concepto que simplifica la descripción papilar: el Cup/Disc Ratio (relación excavación-papila [E/P]). Divide de forma imaginaria el diámetro de la papila en 10 partes, siendo el numerador la medida de la excavación papilar. Un E/P>6 es sugestivo de GAA.
Solo un diagnóstico precoz de GAA permite iniciar un tratamiento que frene y minimice las lesiones15,16. La AAO afirma que un cribado del glaucoma crónico en población con factores de riesgo sería una medida rentable, pudiendo incluirse en los programas de diagnóstico precoz en la población general1. La Organización Mundial de la Salud recomienda la toma de medidas específicas para esta enfermedad en sus programas de prevención de la ceguera17-19.
La Agency for Healthcare Research and Quality (AHRQ) de Estados Unidos presentó en 2012 una revisión de la literatura publicada en la que compara la seguridad y la efectividad de varios métodos de diagnóstico precoz del GAA, entre ellos la obtención de imágenes fotográficas del nervio óptico20. Varios estudios realizados desde diferentes países han comprobado la utilidad del uso de imágenes digitales para el diagnóstico precoz de GAA, presentándola como una prometedora alternativa de diagnóstico desde atención primaria (AP)5,21-25.
Actualmente disponemos de aparataje de alta resolución y personal cualificado para la realización de las retinografías y su lectura en AP26.
La AP es el ámbito útil para la realización de diagnósticos precoces. El desconocimiento del GAA, así como la falta de medios y de un protocolo establecido de cribado, hacen difícil su desarrollo en la práctica11,15.
El objetivo principal de este estudio fue determinar la exactitud y el comportamiento de la retinografía realizada en AP, interpretada por médicos de familia como herramienta en el diagnóstico precoz en población con factores de riesgo para GAA, mediante la valoración de la papila del nervio óptico. Como objetivos secundarios, describir las características de la muestra y valorar la capacidad de los médicos de AP de utilizar las retinografía para emitir diagnósticos de sospecha de GAA.
Material y métodosEstudio observacional, descriptivo y transversal con valoración de forma ciega por 2 observadores en paralelo (médicos de atención primaria [MAP-1 y MAP-2] y oftalmólogo) realizado entre AP y consultas externas hospitalarias durante un periodo de 8meses. El estudio fue aprobado por el Comité Ético del Complejo Hospitalario Universitario de Huelva. Cada participante fue informado y completó el documento de consentimiento informado escrito.
El tamaño muestral (n=196 pacientes) fue calculado por la concordancia esperada entre MAP y oftalmólogo, estimando que la proporción de desacuerdo se encontraba alrededor del 15%, con una precisión del 5% para un intervalo de confianza del 95%.
Debido a que actualmente las retinografías en AP solo se realizan para el cribado de retinopatía diabética y que la población diabética e hipertensa presenta una prevalencia mayor de GAA, la muestra se obtuvo a partir de listados de pacientes incluidos en el Plan Integral de Diabetes de Atención Primaria del Servicio Andaluz de Salud, procedentes de 8 cupos del Centro de Salud de Lepe (Huelva). Tras revisar las historias clínicas, se seleccionaron los que cumplían los criterios de inclusión (ser diabéticos e hipertensos y entre 40-70años) y de exclusión (limitación para realizarse las pruebas diagnósticas [encamamiento, cataratas no intervenidas…] y/o existencia de diagnóstico de glaucoma previo y/o retinopatía diabética en seguimiento por oftalmología): 330 pacientes.
El proceso de selección aleatoria de la muestra (n=196) se realizó tras ordenar numeralmente los 330 pacientes y aplicar una serie de 196 números aleatorios obtenidos previamente. El resto de pacientes no seleccionados por aleatorización se usaron como reservas, respetándose que cumplieran todos los criterios de inclusión y exclusión y su orden de aparición en el listado. En los casos donde tras el contacto telefónico con el paciente seleccionado este era eliminado (por imposibilidad de localización telefónica, enfermedad grave actual o rechazo de participación), era sustituido por otro siguiendo estas pautas.
La citación en consulta fue mediante llamada telefónica. Cada paciente era valorado por oftalmología y posteriormente se le realizaba la retinografía en AP en el mismo día. El oftalmólogo rellenaba una ficha de recogida de datos por cada paciente, y a cada MAP se le enviaban las imágenes retinográficas, rellenando una ficha de datos independiente por cada paciente, prueba y observador. Todas las fichas se entregaban a un cuarto investigador, que realizaba la recogida de datos.
Los MAP, previamente familiarizados con la lectura de retinografías para retinopatía diabética, recibieron un taller para la detección de signos de GAA. Cada uno realizó independientemente la lectura de todas las retinografías en el mismo periodo de tiempo. Sus resultados por cada ojo (derecho e izquierdo) y paciente fueron comparados con los resultados obtenidos por el oftalmólogo mediante las pruebas diagnósticas de referencia: estudio de la presión intraocular (PIO; positiva si >21mmHg), campo visual mediante campimetría (signos de defecto arciforme del campo visual sugestivo de GAA), ángulo de cámara anterior por gonioscopia (abierto o gradoiv) y estado de la papila mediante exploración de fondo de ojo por biomicroscopia con lente de Goldmann (signos sugestivos de GAA). El estudio papilar sobre las retinografías se realizó por descripción papilar según el E/P y la presencia de signos sugestivos de GAA. A cada paciente se le realizaron 4 fotografías retinográficas por cada ojo, en diferentes ángulos. Los signos sugestivos de GAA se recogieron en un documento anexo del que disponían tanto los médicos de familia como el oftalmólogo a la hora de realizar la valoración descriptiva papilar.
La variable a estudio fue el diagnóstico de GAA, siendo cualitativa, nominal y dicotómica (diagnóstico positivo/negativo de GAA). En el caso de los MAP, el diagnóstico se hizo por descripción de características papilares y E/P (considerándose positivo si ≥6) en las retinografías hechas en AP en la Unidad de Gestión Clínica (UGC) Molino de la Vega (Huelva). En el caso de los oftalmólogos, a partir de los resultados de las pruebas diagnósticas de referencia (incluyendo E/P) realizadas en la UGC de Oftalmología del Hospital Infanta Elena, Huelva. El diagnóstico de GAA se consideró por cada paciente, independientemente de si resultó positivo en uno o ambos ojos.
Para el estudio descriptivo de la muestra se analizaron edad, sexo, tiempo de evolución de diabetes, tratamiento actual de diabetes, cifras de presión arterial sistólica y diastólica, y nivel de hemoglobina glucosilada (HbA1c).
Los resultados se comunicaron a cada paciente por correo postal. Los diagnosticados de GAA fueron citados para el posterior seguimiento por oftalmología.
El análisis se realizó por un cuarto investigador tras el vaciado de los datos de las hojas de recogida de datos del oftalmólogo y del MAP en el programa SPPS 15.0 y diseño de una tabla de contingencia para la comparación de pruebas diagnósticas entre observadores (cada MAP con el oftalmólogo de referencia y entre ambos MAP, para ojo derecho y ojo izquierdo, en cada paciente).
Para las variables descriptivas de las características de población se realizó análisis descriptivo de los datos calculando frecuencia, media, mediana, desviación típica, valor máximo y mínimo, y rango.
Se determinaron la exactitud y el comportamiento de la retinografía como prueba de diagnóstico precoz de GAA por la sensibilidad, especificidad, valores predictivos positivo y negativo, y cociente de probabilidad positivo y negativo. La concordancia interobservador para la variable cuantitativa excavación papilar medida por el E/P se determinó por el cociente de correlación intraclase, cuya interpretación se hizo según la escala de interpretación propuesta por Landis y Koch27. La concordancia para la variable cualitativa diagnóstico positivo o negativo de GAA se midió por el índice kappa, interpretándose sus resultados según la escala de interpretación propuesta por López de Ullibarri y Pita Fernández28.
Todos los cálculos se realizaron con intervalos de confianza al 95%.
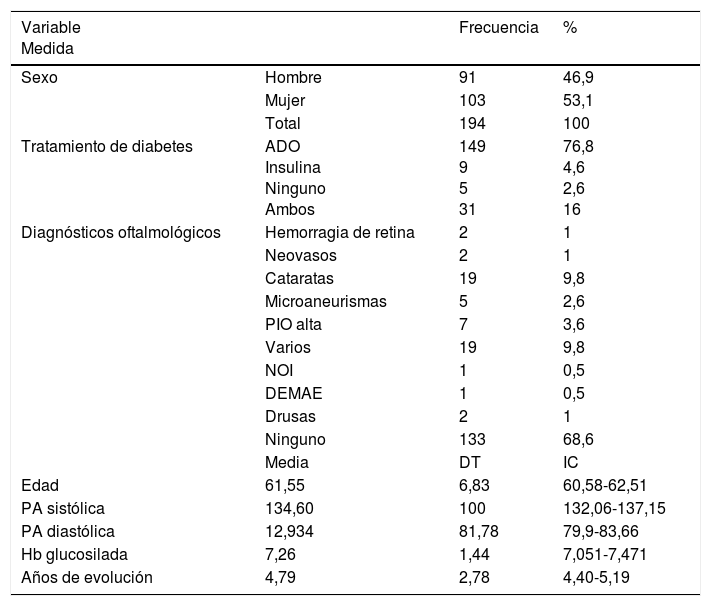
ResultadosSe estudiaron ambos ojos (388) en 194 pacientes: 91 mujeres (46,9%) y 103 varones (53,1%). Se contabilizaron 2 pérdidas por no acudir a la realización de las pruebas. La edad media de los estudiados fue 61,55años (DT: 6,86). En un 68,6% de los pacientes no se encontró ninguna otra patología oftalmológica. En el 9,8% se objetivaron varios hallazgos patológicos concomitantes en la exploración de fondo de ojo. El tratamiento diabético predominante fueron antidiabéticos orales (tabla 1).
Análisis descriptivo de la muestra
| Variable Medida | Frecuencia | % | |
|---|---|---|---|
| Sexo | Hombre | 91 | 46,9 |
| Mujer | 103 | 53,1 | |
| Total | 194 | 100 | |
| Tratamiento de diabetes | ADO Insulina Ninguno Ambos | 149 9 5 31 | 76,8 4,6 2,6 16 |
| Diagnósticos oftalmológicos | Hemorragia de retina | 2 | 1 |
| Neovasos | 2 | 1 | |
| Cataratas | 19 | 9,8 | |
| Microaneurismas | 5 | 2,6 | |
| PIO alta | 7 | 3,6 | |
| Varios | 19 | 9,8 | |
| NOI | 1 | 0,5 | |
| DEMAE | 1 | 0,5 | |
| Drusas | 2 | 1 | |
| Ninguno | 133 | 68,6 | |
| Media | DT | IC | |
| Edad | 61,55 | 6,83 | 60,58-62,51 |
| PA sistólica | 134,60 | 100 | 132,06-137,15 |
| PA diastólica | 12,934 | 81,78 | 79,9-83,66 |
| Hb glucosilada | 7,26 | 1,44 | 7,051-7,471 |
| Años de evolución | 4,79 | 2,78 | 4,40-5,19 |
ADO: antidiabéticos orales; DEMAE: degeneración macular asociada a la edad; DT: desviación típica; Hb: hemoglobina; IC: intervalo de confianza; NOI: neuropatía óptica isquémica; PA: presión arterial; PIO: presión intraocular.
En la valoración por los oftalmólogos se detectaron 11 pacientes con PIO positiva. La campimetría fue positiva en 4 pacientes. Se detectó un E/P positivo en 23 pacientes, y 139 pacientes presentaron un gradoiv de apertura de cámara anterior por gonioscopia. Fueron diagnosticados de GAA 16 pacientes. La frecuencia de GAA en la muestra estudiada según la valoración del oftalmólogo fue del 8,2%.
El MAP-1 valoró como positivas para GAA 35 retinografías. El MAP-2 valoró como positivas 35 retinografías.
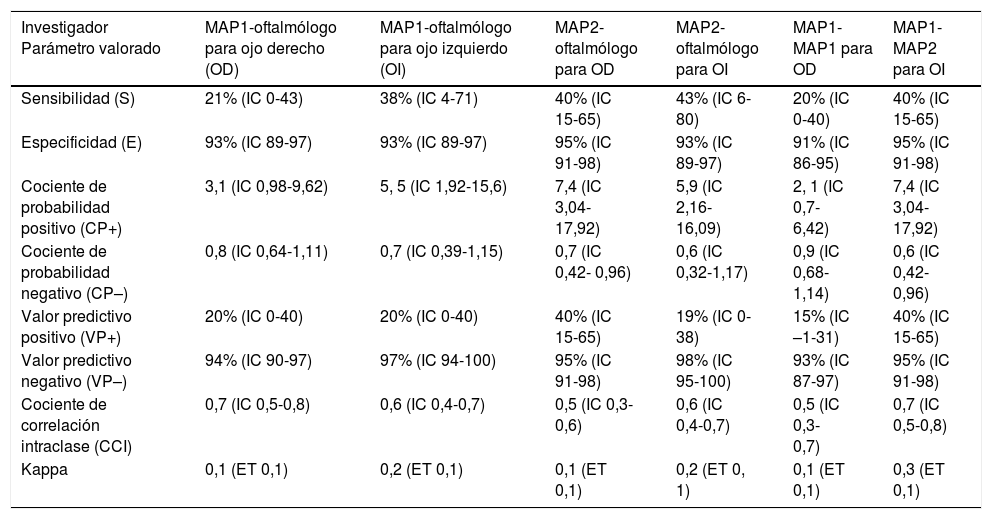
Se obtuvieron resultados similares en todas las comparaciones entre oftalmólogo y cada MAP y entre ambos MAP (tablas 2 y 3). En todos los casos la especificidad y el valor predictivo negativo fueron altos, pero la sensibilidad y el valor predictivo positivo fueron bajos. El cociente de probabilidad positivo fue moderado y el negativo, insignificante. En cuando a la concordancia interobservador, en todos los casos el resultado del CCI fue sustancial, al igual que la concordancia mediante el índice kappa.
Resultados comparativos entre oftalmólogo y MAP y ambos MAP
| Investigador Parámetro valorado | MAP1-oftalmólogo para ojo derecho (OD) | MAP1-oftalmólogo para ojo izquierdo (OI) | MAP2-oftalmólogo para OD | MAP2-oftalmólogo para OI | MAP1-MAP1 para OD | MAP1-MAP2 para OI |
|---|---|---|---|---|---|---|
| Sensibilidad (S) | 21% (IC 0-43) | 38% (IC 4-71) | 40% (IC 15-65) | 43% (IC 6-80) | 20% (IC 0-40) | 40% (IC 15-65) |
| Especificidad (E) | 93% (IC 89-97) | 93% (IC 89-97) | 95% (IC 91-98) | 93% (IC 89-97) | 91% (IC 86-95) | 95% (IC 91-98) |
| Cociente de probabilidad positivo (CP+) | 3,1 (IC 0,98-9,62) | 5, 5 (IC 1,92-15,6) | 7,4 (IC 3,04-17,92) | 5,9 (IC 2,16-16,09) | 2, 1 (IC 0,7- 6,42) | 7,4 (IC 3,04-17,92) |
| Cociente de probabilidad negativo (CP–) | 0,8 (IC 0,64-1,11) | 0,7 (IC 0,39-1,15) | 0,7 (IC 0,42- 0,96) | 0,6 (IC 0,32-1,17) | 0,9 (IC 0,68-1,14) | 0,6 (IC 0,42-0,96) |
| Valor predictivo positivo (VP+) | 20% (IC 0-40) | 20% (IC 0-40) | 40% (IC 15-65) | 19% (IC 0-38) | 15% (IC –1-31) | 40% (IC 15-65) |
| Valor predictivo negativo (VP–) | 94% (IC 90-97) | 97% (IC 94-100) | 95% (IC 91-98) | 98% (IC 95-100) | 93% (IC 87-97) | 95% (IC 91-98) |
| Cociente de correlación intraclase (CCI) | 0,7 (IC 0,5-0,8) | 0,6 (IC 0,4-0,7) | 0,5 (IC 0,3-0,6) | 0,6 (IC 0,4-0,7) | 0,5 (IC 0,3- 0,7) | 0,7 (IC 0,5-0,8) |
| Kappa | 0,1 (ET 0,1) | 0,2 (ET 0,1) | 0,1 (ET 0,1) | 0,2 (ET 0, 1) | 0,1 (ET 0,1) | 0,3 (ET 0,1) |
IC: intervalo de confianza.
Tabla de contingencia diagnóstica por retinografía para ojo derecho (OD) e izquierdo entre MAP1 y MAP 2
| Diagnóstico por retinografía OD médico 2 | ||||
|---|---|---|---|---|
| Positivo | Negativo | Total | ||
| Diagnóstico por retinografia OD médico 1 | Positivo | 3 (20,0%) | 12 (80,0%) | 15 (100,0%) |
| Negativo | 17 (10,1%) | 151 (89,9%) | 168 (100,0%) | |
| Total | 20 (10,9%) | 163 (89,1%) | 183 (100,0%) | |
| Diagnóstico por retinografía OI médico 2 | Total | |||
|---|---|---|---|---|
| Positivo | Negativo | Positivo | ||
| Diagnóstico por retinografía OI médico 1 | Positivo | 6 (40,0%) | 9 (60,0%) | 15 (100,0%) |
| Negativo | 9 (5,4%) | 157 (94,6%) | 166 (100,0%) | |
| Total | 15 (8,3%) | 166 (91,7%) | 181 (100,0%) | |
La muestra estudiada presentó en general un buen control de factores de riesgo cardiovascular y diabetes, predominando la ausencia de signos de daño en órgano diana objetivados por las pruebas utilizadas.
La baja sensibilidad encontrada podría atribuirse a la complejidad de los criterios diagnósticos utilizados para el diagnóstico de glaucoma, así como a la dificultad en la interpretación de la retinografía (valoración papilar en 2 dimensiones en retinografía, dependencia de la colaboración del paciente al realizar las pruebas, subjetividad del observador, luminosidad en la captura de la imagen, opacidad de medios…) y complejidad de la propia patología estudiada dado su carácter evolutivo. Al ser dependientes de la sensibilidad, los cocientes de probabilidad bajos se explican por el mismo hecho.
Observando la concordancia interobservador entre MAP y oftalmólogo, en todos los casos el resultado del CCI fue sustancial. Contrasta con la concordancia para la variable cualitativa diagnóstico de GAA, calculada mediante el índice kappa, donde los resultados indicaron una concordancia pobre-débil para el diagnóstico de GAA mediante retinografía. Se obtuvieron resultados similares en la comparación entre ambos MAP. Este hecho puede explicarse en base a que los criterios diagnósticos utilizados no solo consideraban el E/P, sino un conjunto de parámetros descriptivos papilares que cada observador debía valorar globalmente hasta determinar el diagnóstico de GAA. La posible complejidad en la aplicación e interpretación de estos criterios, con alto índice de subjetividad, apunta como causa de la discordancia en los resultados diagnósticos cualitativos y cuantitativos finales. Podría considerarse este hecho como un sesgo de planificación por protocolos rigurosos y/o complejos. Para comprobar este hecho se diseñó una encuesta tipo escala de Likert de acuerdo-desacuerdo, con 4 posibles respuestas, con el fin de valorar la opinión de los MAP al respecto. Ambos MAP coincidieron en que la aplicación de los criterios diagnósticos globales no fue sencilla, ni en la práctica era fácil poder llegar a un diagnóstico a partir de ellos, pero sí era sencillo y práctico calcular el E/P, donde la concordancia con los resultados obtenidos por oftalmólogos (considerados pruebas de referencia) fue mayor. Consideraron que ajustar los criterios diagnósticos, haciéndolos más sencillos en su aplicación, facilitaría el trabajo de lectura e interpretación del E/P.
A su vez, los valores predictivos positivo bajo y negativo alto se explicarían por la baja prevalencia del GAA10,11.
A partir de estos resultados y dada la baja sensibilidad, concluimos que la aportación de la retinografía en el diagnóstico precoz de GAA sería moderada-insignificante, siendo su comportamiento insuficientemente válido y seguro para el cribado de GAA.
Múltiples estudios nacionales e internacionales han obtenido resultados similares para diferentes pruebas de diagnóstico precoz5,24-26,29, indicando la necesidad de ampliar los estudios para ofrecer resultados más concluyentes.
En su estudio de coste-efectividad de la detección y tratamientos precoces del GAA por oftalmólogos en la Universidad de Maastricht (Holanda) en 2008, Peeters et al.9 concluyeron que la medida con mayor impacto económico en coste-efectividad fue la modificación en la incidencia de diagnósticos de GAA a partir de estrategias de diagnóstico precoz.
Dado que actualmente no se dispone de otros protocolos para el cribado de GAA en AP y que su diagnóstico precoz es la estrategia de mayor impacto en la incidencia del GAA, no descartamos valorar la posibilidad de realizar los ajustes oportunos al estudio planteado con el fin de promoverlo como herramienta para la creación de un protocolo para el diagnóstico precoz de GAA en AP. Se establecería así un primer paso para futuros programas de detección precoz del GAA desde AP en coordinación con atención especializada, permitiendo crear protocolos de manejo del GAA que dotarían de una doble utilización y rentabilidad a la inversión realizada en los retinógrafos disponibles en las UGC de AP actualmente orientados al diagnóstico precoz de retinopatía diabética.
Sería necesario modificar los criterios diagnósticos utilizados, simplificándolos y haciéndolos más prácticos para aumentar la baja concordancia interobservador obtenida. Otras medidas útiles serían ampliar la muestra y número de MAP intervinientes, así como diseñar programas de formación en diagnóstico de GAA para MAP. En este sentido, añadir otras pruebas diagnósticas de GAA concomitantes, como el estudio de la PIO desde AP, o la inclusión de grupos pacientes con mayor prevalencia de GAA, como los antecedentes familiares de GAA, serían medidas que contribuirían a aumentar la sensibilidad del estudio. Del mismo modo, otra medida útil sería modificar las herramientas informáticas disponibles para ajustarlas a una mejor medición papilar sobre las imágenes retinográficas, dado que los programas informáticos utilizados actualmente no están diseñados para la medición de la excavación papilar con precisión.
- •
El glaucoma crónico o de ángulo abierto (GAA) es una patología lentamente progresiva que conduce a ceguera irreversible, infradiagnosticada en el 50% de los casos.
- •
Su diagnóstico es complejo. No existen protocolos de diagnóstico precoz en la actualidad.
- •
Los estudios papilares mediante imágenes digitales realizadas en atención primaria se presentan como una herramienta útil para el diagnóstico precoz de GAA.
- •
El diagnóstico de GAA desde atención primaria es necesario y posible, requiriendo procedimientos complejos y formación específica de los profesionales.
- •
La retinografía sí aportaría información útil como prueba de diagnóstico precoz de glaucoma desde atención primaria, pero esta aportación sería moderada-insignificante.
- •
Serían necesarios ajustes en el estudio presentado para aumentar su sensibilidad y solventar las limitaciones, constituyendo un primer paso para elaborar un programa de diagnóstico precoz de GAA desde atención primaria.
El trabajo ha recibido financiación de la Sociedad Andaluza de Medicina Familiar y Comunitaria mediante el Premio Becas Isabel Fernández para la elaboración de proyectos de investigación y tesis doctorales en su convocatoria de 2014 (tipo: tesis doctoral; referencia: 119/14).
Conflicto de interesesLos autores declaran no presentar ningún conflicto de intereses.
A los compañeros de la UGC Molino de la Vega, a los miembros de la Unidad Docente de Medicina Familiar y Comunitaria de Huelva y al personal de la UGC de Oftalmología del Hospital Infanta Elena. A todos los pacientes que colaboraron en el estudio. A la Sociedad Andaluza de Medicina de Familia por la concesión de su Beca Isabel Fernández. A mi tutor, ya ausente. A mi familia. A Dios.
Parte del contenido de este trabajo ha sido presentado previamente como comunicación póster en el 33.° Congreso la Sociedad Española de Medicina Familiar y Comunitaria (SEMFyC) en 2013, como comunicación oral en el Primer Encuentro Médico de Atención Primaria de Extremadura en 2014, donde recibió el premio a la Mejor Comunicación Previa, y como comunicación oral en el 35.° Congreso de la SEMFyC en 2015.