Las infecciones odontogénicas representan el 10% de las prescripciones antibióticas. A pesar de la reconocida frecuencia e importancia de estas llama la atención la frecuente confusión entre profilaxis y tratamiento. La cavidad bucal forma un complejo ecosistema compuesto por más de 500 especies bacterianas. Es indispensable la anamnesis y exploración de cada infección y conocer los antecedentes que modifiquen nuestra conducta terapéutica y/o profiláctica.
Durante muchos años ha sido aceptado el uso de la profilaxis con antibióticos en pacientes con riesgo de endocarditis infecciosa. Actualmente sus indicaciones se están restringiendo y en muchas ocasiones los riesgos de tomar antibiótico preventivo son superiores a los beneficios.
Carecemos de estudios para conocer el antibiótico y la pauta mejor indicada. Hemos de basarnos en el documento de consenso español. Tampoco sabemos cómo influye el uso de antibióticos en las resistencias, no solo de la cepa patógena sino también en la flora habitual del paciente.
Odontogenic infections account for 10% of all antibiotic prescriptions in Spain. Despite the frequency and importance of these infections, there is often confusion between prophylaxis and treatment. The oral cavity is a complex ecosystem made up of over 500 bacterial species. It is essential to take the medical history, examine each infection, and know about previous illnesses that could change our therapeutic and/or prophylactic attitude.
The use of prophylaxis with antibiotics in patients at risk of infective endocarditis has been accepted for many years. Nowadays this is being restricted, and in many cases the risks of taking preventive antibiotics outweigh its benefits.
There are no serious studies to determine the best antibiotic and its dosage, thus the Spanish consensus guidelines have to be followed. It is not known how the misuse of antibiotics influences bacterial resistance, not only on pathogen strains, but also on the common oral flora.
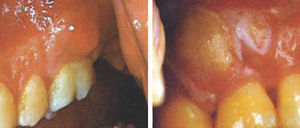
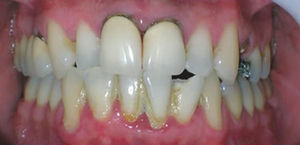
La prevalencia de infección odontogénica es muy elevada en adultos: hasta un 90% presenta caries, un 50% gingivitis y un 30% periodontitis1. Las infecciones odontogénicas incluyen la caries, la pulpitis, el absceso periapical, la gingivitis, la periodontitis, la pericoronitis, la coronaritis, la osteítis y la infección de los espacios aponeuróticos (figs. 1–3). Los antibióticos utilizados como tratamiento o profilaxis para procesos odontológicos cada vez son más frecuentes, suponiendo un 10% del total de las prescripciones2. Acudir a la consulta de odontología no ha de suponer necesariamente la indicación sistemática de un antibiótico, ya que se dispone actualmente de diversas guías para su indicación adecuada. La infecciones odontogénicas son generalmente polimicrobianas. Es importante conocer, en nuestro ámbito, la composición de la flora bacteriana oral y su sensibilidad a los antibióticos más utilizados, para poder adaptar convenientemente el tratamiento, así como para evitar los efectos secundarios y resistencias3. Muchos microorganismos aislados en estas infecciones no parecen tener ningún papel en su patogenia pero su presencia indica que la pueden facilitar suministrando nutrientes o factores de crecimiento, creando un pH favorable, o ejerciendo efectos antagónicos con otros microorganismos4. Una adecuada higiene oral disminuye las infecciones odontogénicas, y especialmente la enfermedad periodontal, que se ha vinculado con el desarrollo de enfermedades cardiovasculares5. A pesar de que la literatura científica apunta que no toda intervención odontológica es tributaria de una profilaxis antibiótica sistemática para la prevención de infección local o a distancia, la gran disparidad de recomendaciones en guías y protocolos demuestra la falta de consenso en este campo6,7. No está claro si los daños potenciales y los costes de la administración de antibióticos superan cualquier efecto beneficioso8. El objetivo de este artículo es el de reflexionar sobre la justificación de dar antibióticos para tratar la infección odontogénica o prevenir sus posibles complicaciones locales o a distancia y razonar las directrices para el uso, si fuese indicado, del antibiótico más adecuado, teniendo en cuenta los datos científicos actualmente disponibles.
Tratamiento de la infección odontogénicaLa cavidad bucal forma un complejo ecosistema compuesto por más de 500 especies bacterianas; Streptococcus, Peptostreptococcus, Veillonella, Lactobacillus, Corynebacterium y Actinomyces representan más del 80% de toda la flora9. Los bacilos gramnegativos son raros en adultos sanos, siendo casi exclusivos de pacientes con enfermedades graves, hospitalizados y ancianos10. Es indispensable la anamnesis, exploración y observación de cada proceso odontogénico, así como identificar los antecedentes previos que puedan modificar nuestra conducta terapéutica y profiláctica.
A pesar de la reconocida frecuencia e importancia de las infecciones odontogénicas llama la atención la frecuente confusión entre profilaxis y tratamiento.
Infección odontogénicaDebe ser abordada desde 3 ámbitos terapéuticos: tratamiento etiológico odontológico que frecuentemente incluirá actuaciones quirúrgicas de mayor o menor envergadura; tratamiento sistémico de soporte, que incluirá manejo del dolor, medidas físicas para el control de la inflamación, hidratación, equilibrio de la glucemia, etc., y tratamiento antibiótico.
Tratamiento antibióticoEn los últimos años ha aumentado el número de microorganismos de la cavidad bucal resistentes a los antibióticos, en parte debido a la mala indicación y al bajo cumplimiento terapéutico de los pacientes por lo que respecta a la dosis y la duración11. Especialmente en la periodontitis, los niveles de resistencia son elevados para muchas de las especies productoras de infección odontogénica12 y, debido a las diferencias nacionales e incluso regionales, es imprescindible conocer cuáles son los gérmenes más frecuentes13 y cuál es su resistencia a cada antibiótico en nuestro ámbito14.
Los tratamientos recomendados para cada tipo de infección se representan en la tabla 12 y la antibioticoterapia en las tablas 2 y 34. El tratamiento antibiótico de las infecciones odontogénicas tiene como finalidad evitar la extensión local de la infección, reducir el inóculo bacteriano en el foco infeccioso y prevenir las complicaciones derivadas de la diseminación hematógena. La duración del tratamiento suele oscilar entre 5 y10 días, y generalmente se prolonga 3 o 4 días después de la desaparición de las manifestaciones clínicas.
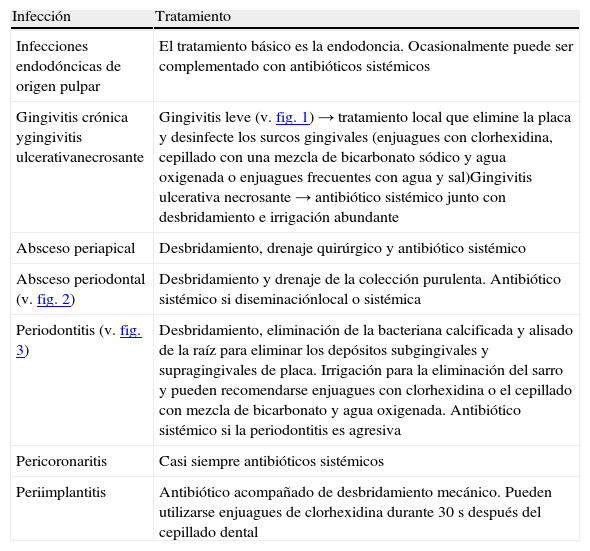
Tratamientos recomendados para las infecciones bacterianas odontogénicas
| Infección | Tratamiento |
| Infecciones endodóncicas de origen pulpar | El tratamiento básico es la endodoncia. Ocasionalmente puede ser complementado con antibióticos sistémicos |
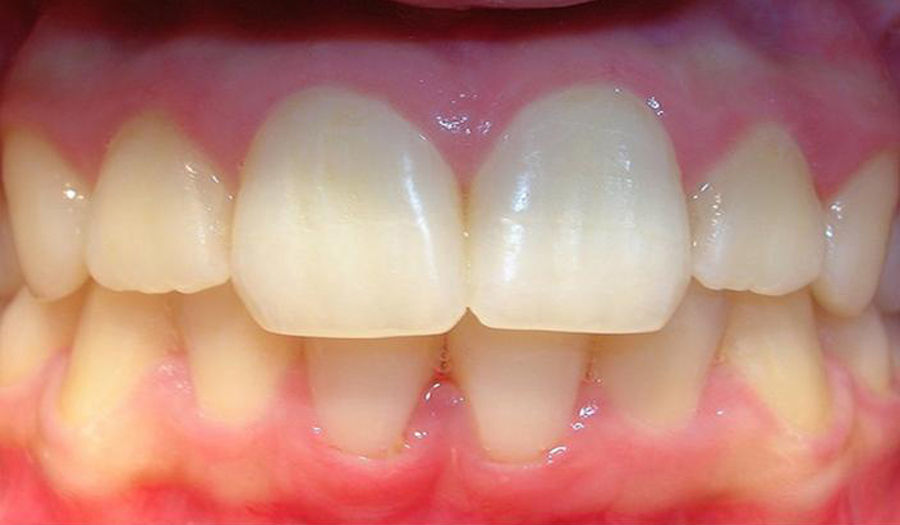
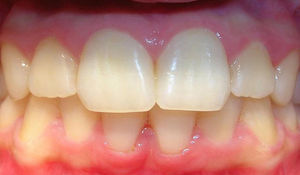
| Gingivitis crónica ygingivitis ulcerativanecrosante | Gingivitis leve (v. fig. 1) → tratamiento local que elimine la placa y desinfecte los surcos gingivales (enjuagues con clorhexidina, cepillado con una mezcla de bicarbonato sódico y agua oxigenada o enjuagues frecuentes con agua y sal)Gingivitis ulcerativa necrosante → antibiótico sistémico junto con desbridamiento e irrigación abundante |
| Absceso periapical | Desbridamiento, drenaje quirúrgico y antibiótico sistémico |
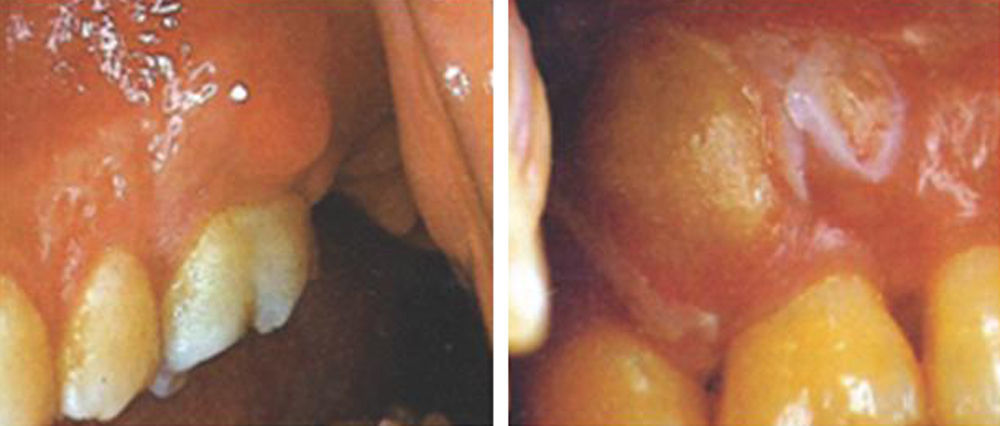
| Absceso periodontal (v. fig. 2) | Desbridamiento y drenaje de la colección purulenta. Antibiótico sistémico si diseminaciónlocal o sistémica |
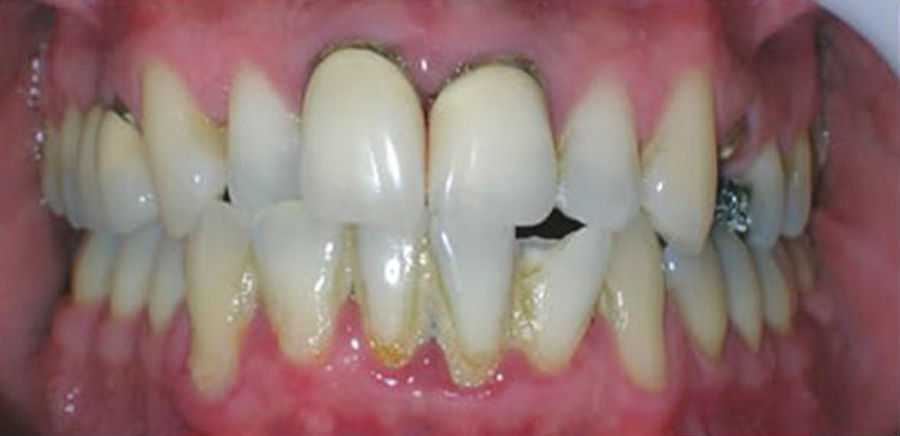
| Periodontitis (v. fig. 3) | Desbridamiento, eliminación de la bacteriana calcificada y alisado de la raíz para eliminar los depósitos subgingivales y supragingivales de placa. Irrigación para la eliminación del sarro y pueden recomendarse enjuagues con clorhexidina o el cepillado con mezcla de bicarbonato y agua oxigenada. Antibiótico sistémico si la periodontitis es agresiva |
| Pericoronaritis | Casi siempre antibióticos sistémicos |
| Periimplantitis | Antibiótico acompañado de desbridamiento mecánico. Pueden utilizarse enjuagues de clorhexidina durante 30 s después del cepillado dental |
Tomada de Rodríguez-Alonso y Rodríguez-Monje2.
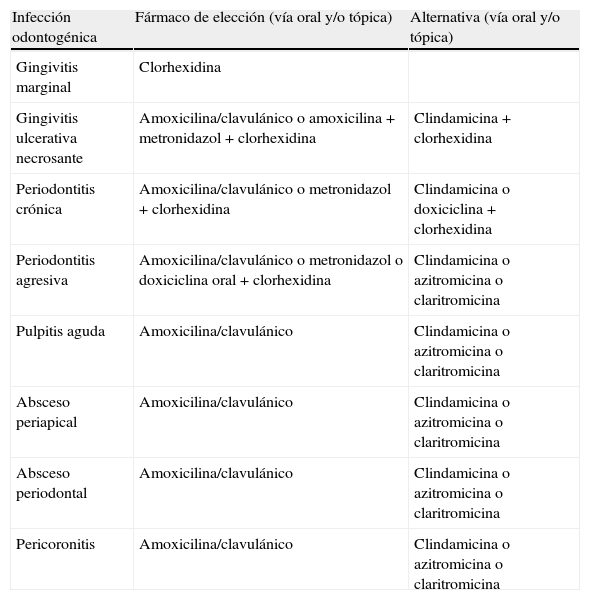
Fármacos de elección para las infecciones bacterianas odontogénicas
| Infección odontogénica | Fármaco de elección (vía oral y/o tópica) | Alternativa (vía oral y/o tópica) |
| Gingivitis marginal | Clorhexidina | |
| Gingivitis ulcerativa necrosante | Amoxicilina/clavulánico o amoxicilina+metronidazol+clorhexidina | Clindamicina+clorhexidina |
| Periodontitis crónica | Amoxicilina/clavulánico o metronidazol+clorhexidina | Clindamicina o doxiciclina+clorhexidina |
| Periodontitis agresiva | Amoxicilina/clavulánico o metronidazol o doxiciclina oral+clorhexidina | Clindamicina o azitromicina o claritromicina |
| Pulpitis aguda | Amoxicilina/clavulánico | Clindamicina o azitromicina o claritromicina |
| Absceso periapical | Amoxicilina/clavulánico | Clindamicina o azitromicina o claritromicina |
| Absceso periodontal | Amoxicilina/clavulánico | Clindamicina o azitromicina o claritromicina |
| Pericoronitis | Amoxicilina/clavulánico | Clindamicina o azitromicina o claritromicina |
Nota: Esta tabla es indicativa de los antibióticos y antisépticos utilizados, lo que no quiere decir que en todas las situaciones sean necesarios.
Tomada de Bascones Martínez et al.4.
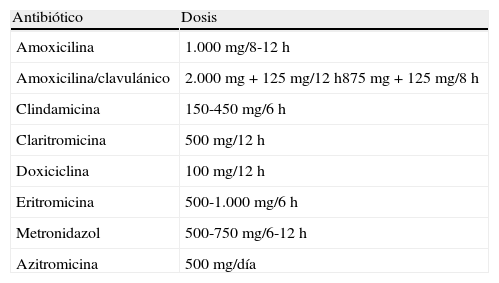
Dosificación recomendada de los fármacos de elección para las infecciones bacterianas odontogénicas
| Antibiótico | Dosis |
| Amoxicilina | 1.000 mg/8-12 h |
| Amoxicilina/clavulánico | 2.000 mg+125 mg/12 h875 mg+125 mg/8 h |
| Clindamicina | 150-450 mg/6 h |
| Claritromicina | 500 mg/12 h |
| Doxiciclina | 100 mg/12 h |
| Eritromicina | 500-1.000 mg/6 h |
| Metronidazol | 500-750 mg/6-12 h |
| Azitromicina | 500 mg/día |
Nota: La duración del tratamiento suele oscilar entre 5 y 10 días. Generalmente se prolonga hasta 3 o 4 días después de desaparecer las manifestaciones clínicas.
Tomada de Bascones Martínez et al.4.
En caso de requerir tratamiento antibiótico, amoxicilina con ácido clavulánico, metronidazol y clindamicina presentan actividad frente a la mayoría de los microorganismos causantes de las infecciones odontogénicas15,16. Las dosis habituales de amoxicilina con ácido clavulánico son de 2.000 mg+125mg/12h o 875mg+125mg/8h para adultos y 40-80mg/kg/día en 3 dosis o 500 mg+125mg/8h para niños4.
Profilaxis antibiótica de la infección odontogénicaLos puntos clave que se deben tener en cuenta antes de recomendar profilaxis para una actuación odontológica son los siguientes:
- •
Una bacteriemia transitoria no ocurre solo tras una extracción dental o cirugía periodontal, sino que también puede ocurrir en el contexto de un simple cepillado bucal o mientras se mastica chicle, y las bacteriemias se relacionan con una mala higiene oral y con la gingivitis, por lo que la prevención debería ir dirigida al control de estos 2 factores17. Un reciente metanálisis publicado por Tomás et al.18 pone de manifiesto que la acumulación de placa dental y la inflamación gingival incrementan la prevalencia de bacteriemia durante el simple cepillado dental. Por lo que una buena higiene oral es básica a la hora reducir el riesgo de endocarditis infecciosa (EI). En la tabla 4 se detalla la incidencia de bacteriemia en relación con procedimientos dentales e higiene oral19.
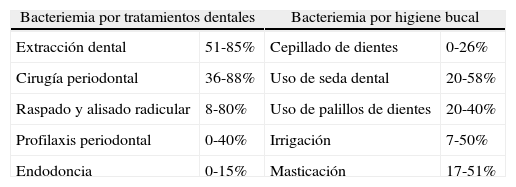
Tabla 4.Incidencia de bacteriemias comparando las actuaciones de tratamiento dental y las maniobras de higiene bucal
Bacteriemia por tratamientos dentales Bacteriemia por higiene bucal Extracción dental 51-85% Cepillado de dientes 0-26% Cirugía periodontal 36-88% Uso de seda dental 20-58% Raspado y alisado radicular 8-80% Uso de palillos de dientes 20-40% Profilaxis periodontal 0-40% Irrigación 7-50% Endodoncia 0-15% Masticación 17-51% Tomada de Gutiérrez et al.19.
- •
Las bocas sépticas con inflamación crónica se asocian también a un aumento de los marcadores de inflamación como la proteína C reactiva y el fibrinógeno, entre otros. Dichos marcadores son predictores de accidentes cardiovasculares, por lo que una mala higiene bucal se asocia a una mayor morbilidad cardiovascular5.
- •
El antibiótico utilizado debe ser de fácil administración recomendándose la vía oral y la dosis única siempre que sea posible.
- •
Según los principios establecidos por Peterson, para indicar la profilaxis con antibiótico debería haber un riesgo de infección superior al 10%20. Dicho límite marcaría el límite del coste-beneficio teniendo en cuenta la probabilidad de infección y los efectos secundarios y la creación de resistencias inherentes a la toma de antibióticos. La cirugía bucal no complicada en general tiene un bajo riesgo de infección, inferior a dicho umbral. Los factores que pueden incrementar dicho riesgo son alargar el tiempo de intervención, si la cirugía es traumática (ostectomía), si ha habido una infección previa, si se coloca un cuerpo extraño o si el paciente presenta algún tipo de trastorno inmunitario21.
- •
No toda cirugía conlleva el mismo grado de riesgo de infección. Debemos distinguir entre 3 tipos de cirugía: limpia, limpia contaminada y sucia. Los procedimientos dentales se consideran «limpia contaminada», aunque si hay que intervenir sobre tejido infectado se considerará contaminada.
- •
La pauta antibiótica debe ser racional. Debemos usar el antibiótico apropiado para prevenir una infección concreta por un germen determinado. En las infecciones odontogénicas el prototipo de antibiótico aconsejable es la amoxicilina22.
- •
La administración de antibiótico debe hacerse de manera que el pico plasmático sea lo suficientemente alto en el momento de la intervención. Si se administra entre 30 y 60 min antes de la intervención y hasta 2 h después de la intervención, el riesgo de bacteriemia disminuye considerablemente21.
- •
La profilaxis en cirugía dental en un paciente sano está recomendada solo en el caso de extracción de una pieza dentaria impactada, cirugía periapical, cirugía del hueso, implantes, injerto óseo e intervención de tumores benignos. En sujetos con riesgo de infección local o sistémica (pacientes oncológicos, inmunodeprimidos, con alteraciones metabólicas, etc.), la cobertura antibiótica debería ser administrada antes de iniciar un procedimiento invasivo7.
Un procedimiento clínico aceptado durante muchos años ha sido el uso de la profilaxis con antibióticos en procedimientos dentales de pacientes con riesgo de EI. En el momento actual las situaciones en las que está indicada la profilaxis se están restringiendo, demostrándose que en muchas ocasiones los riesgos de tomar antibiótico preventivo son superiores a los beneficios23, así como que la evidencia científica para su recomendación es insuficiente incluso en pacientes con enfermedad cardíaca6. La mayoría de guías publicadas en los últimos años ponen en duda su eficacia24–26 e incluso llegan a no recomendarla para ningún procedimiento dental (NICE)25. Además, y a pesar del amplio uso de antibióticos para la profilaxis de EI, esta también ocurre en pacientes no clasificados como de riesgo, y se estima que aunque la profilaxis tuviera una eficacia del 100%, se evitarían muy pocos casos, por lo que se están limitando los grupos de riesgo para recibirla.
Para una correcta profilaxis es necesario tener en cuenta la cardiopatía subyacente y el tipo de procedimiento que se va a realizar.
En las últimas recomendaciones propuestas por la American Heart Association24 y recogidas en las recomendaciones de la Sociedad Española de Cardiología y en el boletín de información terapéutica del ministerio de Sanidad en 200927,28, así como en nuestras últimas guías29, el número de cardiopatías que precisan profilaxis antibiótica queda reducido a:
- •
Valvulopatías cardíacas adquiridas con estenosis o insuficiencia.
- •
Reemplazo valvular.
- •
Cardiopatía congénita estructural (incluidos trastornos estructurales quirúrgicamente corregidos o paliados), excepto un defecto único en el tabique interauricular, una comunicación interventricular completamente reparada o un conducto arterial persistente reparado por completo y dispositivos de cierre que se consideren endotelizados.
- •
Endocarditis infecciosa previa.
- •
Miocardiopatía hipertrófica.
Como se ha comentado anteriormente no solo es necesario seleccionar en qué cardiopatía debemos realizar la profilaxis, sino qué procedimientos pueden producir una bacteriemia transitoria potencialmente causante de EI. Estas recomendaciones también han sido reducidas en estas últimas guías, de tal forma que solo se recomienda en procedimientos dentales en los que se precise manipulación del tejido gingival o de la región periapical o perforación de la mucosa oral24.
Antibióticos recomendados y dosisDesde la atención primaria se debe tener en cuenta que en la cavidad bucal existe una gran diversidad de microorganismos implicados en las diferentes infecciones bucofaciales, hecho que, junto a las diferentes características del huésped, debe ser tenido en cuenta a la hora de decidir el tratamiento y su duración30. Es nuestra función como médicos de atención primaria sospechar la EI, siendo necesaria la derivación hospitalaria para diagnóstico definitivo y elección de tratamiento según antibiograma.
Profilaxis de la endocarditis infecciosaPara la profilaxis de la EI el medicamento de elección es la amoxicilina oral en dosis de 2g en adultos y 50mg/kg en niños22. En caso de alergia a la penicilina se recomienda clindamicina 600 mg en adultos y 20 mg/kg en niños v.o. Ambos tratamientos deben administrarse 30-60 minutos antes del procedimiento con riesgo de EI26.
ConclusionesDado el gran consumo de antibióticos que conllevan los procesos odontológicos y la modificación en la resistencia de la flora bacteriana bucal que producen, sería necesario realizar estudios con la calidad científica suficiente, y no solo consensos entre expertos, para protocolizar qué antibióticos, qué dosificación y posología y en qué procesos deberían estar indicados.
Por otro lado, y puesto que es relativamente frecuente acudir a la consulta del médico de familia por procesos odontológicos, así como para la tramitación de la receta del antibiótico prescrito por el odontólogo, es necesario un mayor conocimiento de las diferentes enfermedades odontológicas por el médico de familia, así como una mayor comunicación entre médico de familia, infectólogos y odontólogos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A Lourdes Ballbé Mallol, odontóloga de atención primaria en Barcelona.