Conocer mejor las variables clínicas, funcionales y analíticas que se asocian al síndrome confusional agudo (SCA) en urgencias y la evolución de las mismas con el fin de obtener una mejora en el abordaje terapéutico del paciente anciano previniendo así la morbimortalidad en este tipo de pacientes.
DiseñoSe trata de un estudio descriptivo prospectivo de SCA en urgencias.
EmplazamientoHospital General Universitario de Ciudad Real.
ParticipantesSe incluyó, en el intervalo de las 24 h siguientes al ingreso en el Servicio de Geriatría, a todos los pacientes procedentes del Servicio de Urgencias con diagnóstico de SCA.
Mediciones principalesSe realizó un análisis de las variables del conjunto de datos (variables sociodemográficas y clínicas), calculando tablas de frecuencias para variables de tipo cualitativo y estadísticos descriptivos para las variables cuantitativas. Posteriormente, se han empleado técnicas de inferencia estadística.
ResultadosEl antecedente médico más frecuente fueron la enfermedad neurológica y la HTA, seguida de las enfermedades reumatológicas. Los motivos de consulta principales fueron el deterioro del estado general, la disnea, la disminución del nivel de consciencia y la fiebre. Se debe destacar la incidencia de la polifarmacia, especialmente de fármacos como los diuréticos, benzodiacepinas o hipnóticos. En relación con la etiología principal, destaca el papel de las infecciones de tipo urinario y respiratorio.
ConclusionesSe destaca el papel fundamental de las enfermedades neurológicas (especialmente la demencia), la HTA, la polifarmacia (uso inadecuado de benzodiacepinas e hipnóticos) y las infecciones urinarias y respiratorias como factores tratables o prevenibles del delirium en el paciente de Atención Primaria en nuestro medio.
To better understand the clinical, functional and analytical variables associated with delirium in emergencies and their evolution in order to obtain an improvement in the therapeutic approach of the elderly patient, thus preventing morbidity and mortality in this type of patient.
DesignThis is a prospective descriptive study of acute confusional syndrome in the emergency department.
SiteGeneral University Hospital of Ciudad Real.
ParticipantsAll patients from the emergency department with a diagnosis of delirium were included in the 24-h interval following admission to the geriatric service.
Main measurementsAn analysis of the variables of the data set (sociodemographic and clinical variables) was performed, calculating frequency tables for qualitative variables and descriptive statistics for quantitative variables. Subsequently, statistical inference techniques have been used.
ResultsThe most frequent medical antecedent were neurological pathology and hypertension, followed by rheumatologic diseases. The main reasons for consultation were deterioration in general condition, dyspnea, decreased level of consciousness, and fever. Highlight the incidence of polypharmacy, especially drugs such as diuretics, benzodiazepines or hypnotics. In relation to the main etiology, the role of urinary and respiratory infections is noteworthy.
ConclusionsHighlight the fundamental role of neurological diseases (especially dementia), hypertension, polypharmacy (inappropriate use of benzodiazepines and hypnotics) and urinary and respiratory infections as treatable and/or preventable factors of delirium in Primary Care patients in our setting.
El síndrome confusional agudo (SCA) es un síndrome, no una enfermedad, de compleja etiología y a menudo multifactorial que está formado por un conjunto de síntomas y signos relacionados con el nivel de consciencia y el deterioro de funciones cognitivas del paciente. Representa una complicación de otra enfermedad subyacente, que en muchas ocasiones pasa desapercibida y que generalmente modifica el pronóstico de nuestros pacientes, por lo que el reconocimiento precoz de un SCA, la correcta identificación de las causas precipitantes y el establecimiento más adecuado de las pautas terapéuticas resultan de crucial importancia1.
La prevalencia del SCA en la población general es del 0,4% en adultos de edad igual o superior a 18 años y del 1,1% en individuos de edad igual o superior a 55 años2. Aproximadamente, del 10 al 20% de los ingresos hospitalarios se deben a la presencia de delirium, mientras que del 10 al 30% de los pacientes desarrollarán este síndrome durante la hospitalización2. Por lo que observamos que la incidencia y la prevalencia de este trastorno varían según la edad, el paciente y el lugar de hospitalización3,4. Pensamos que un incremento de la población anciana podría conllevar un incremento de la incidencia del SCA, el cual es un importante factor de morbimortalidad y empeoramiento del pronóstico y la funcionalidad en esta población5,6.
El objetivo principal de nuestro estudio es estudiar las variables clínicas, funcionales y analíticas que se asocian al SCA en urgencias y la evolución de las mismas a lo largo del tiempo con el fin de obtener una mejora en el abordaje terapéutico del paciente anciano previniendo así la morbimortalidad en este tipo de pacientes.
MétodoTipo de estudioSe trata de un estudio descriptivo prospectivo.
La muestraSe incluyó, en el intervalo de las 24 h siguientes al ingreso en el Servicio de Geriatría del Hospital General Universitario de Ciudad Real (HGUCR), a todos los pacientes procedentes del Servicio de Urgencias con diagnóstico de SCA durante el periodo comprendido entre octubre del 2016 y octubre del 2018 (n=176). La información se recogió a pie de cama de cada uno de los pacientes y se completó con las historias clínicas informatizadas de cada uno de ellos. Se excluyó (n=63) a los pacientes derivados de otros servicios del hospital u otro hospital, pacientes cuyo seguimiento no ha podido completarse debido al traslado a otro hospital o al fallecimiento durante su estancia hospitalaria, y a pacientes en situación terminal. El diagrama de flujo del estudio se muestra en la figura 1.
Variables e instrumentos de medidaTras comprobar los criterios de inclusión y exclusión de cada paciente, se recogió toda la información necesaria sobre las variables objeto de estudio, tanto a su llegada a urgencias como al alta hospitalaria:
- 1.
Variables sociodemográficas: nombre, edad, sexo.
- 2.
Variables clínicas:
- a.
Motivo de consulta.
- b.
Diagnóstico principal y secundarios.
- c.
Antecedentes médicos, comorbilidades y tratamiento habitual:
- –
Enfermedades médicas y quirúrgicas de interés, presencia de déficit visual o auditivo, portador de sonda vesical o nasogástrica e ingresos recientes.
- –
Índice de Comorbilidad de Charlson7,8; es un sistema de evaluación de la esperanza de vida a los 10años. Consta de 19 ítems que miden la edad y diversas comorbilidades.
- –
Tratamiento habitual y modificaciones recientes del mismo. Polifarmacia, que de acuerdo con la Organización Mundial de la Salud (OMS)9,10 se define como el consumo de más de 3fármacos simultáneamente, clasificándose como menor, cuando se consume de 2a 4fármacos y mayor cuando son más de 5en el paciente anciano.
- d.
Exploración física:
- –
Constantes vitales: presión arterial, frecuencia cardiaca, temperatura, glucemia y saturación de oxígeno.
- –
Piel.
- –
Auscultación cardiopulmonar.
- –
Abdomen.
- –
Extremidades.
- e.
Estado mental, funcionalidad y diagnóstico de demencia (se realizó mediante la evaluación con los diversos cuestionarios11 que a continuación presentamos):
- –
Escala de coma de Glasgow12: es un instrumento de evaluación neurológica que sirve para valorar el nivel de consciencia de una persona con daño cerebral. Permite explorar y cuantificar 3 parámetros o criterios de observación clínica: la respuesta ocular, la respuesta verbal y la respuesta motora.
- –
Test Mini-Mental13,14: test de cribado de demencias, útil en el seguimiento evolutivo de las mismas. La versión utilizada puntúa como máximo un total de 30 puntos y los ítems están agrupados en diferentes categorías que representan aspectos relevantes de la función intelectual: orientación, memoria inmediata, atención y cálculo, recuerdo diferido, y lenguaje y construcción.
- –
Índice de Barthel15,16: es un instrumento que mide la capacidad de una persona para realizar 10actividades de la vida diaria, consideradas como básicas, obteniendo una estimación cuantitativa de su grado de independencia.
- –
Cuestionario del estado mental de Pfeiffer17,18: se trata de un breve cuestionario compuesto de 10preguntas que miden el grado de deterioro cognitivo. Las áreas evaluadas son la memoria a corto y largo plazo, la información sobre hechos cotidianos, la capacidad de cálculo y la orientación.
- –
Índice de Katz19,20: es un instrumento para evaluar la independencia de un enfermo en cuanto a la realización de las actividades básicas de la vida diaria. Se trata de 6 ítems dicotómicos (baños, vestirse/desvestirse, uso del baño, movilidad, continencia y alimentación) ordenados jerárquicamente según la secuencia en que los pacientes pierden y recuperan la independencia para realizarlos.
- –
Escala de Blessed21,22: es un instrumento específico para demencia, evalúa la capacidad funcional del paciente para desenvolverse en el día a día. Está compuesta por 22 ítems agrupados en 3 áreas principales: cambios en la ejecución de las actividades de la vida diaria, cambios en los hábitos y cambios en la personalidad, intereses e impulsos.
- –
Índice de Lawton y Brody23,24: recoge información sobre 8 ítems (usar el teléfono, ir de compras, preparar la comida, realizar tareas del hogar, lavar la ropa, utilizar transportes, controlar la medicación y manejar el dinero). Mide la capacidad para la realización de las actividades instrumentales de la vida diaria.
- –
Escala de Hachinsky25,26: diseñada para diferenciar, desde un punto de vista clínico, la demencia degenerativa tipo Alzheimer de la demencia vascular (multiinfarto).
- f.
Exploraciones complementarias:
- –
Analítica: hemograma, bioquímica, coagulación, sistemático de orina, gasometría venosa o arterial.
- –
Electrocardiograma.
- –
Pruebas de imagen: radiografía de tórax, tomografía computarizada (TAC), resonancia magnética nuclear, entre otras.
- g.
Tiempo de hospitalización.
Se realizó un análisis descriptivo de las variables del conjunto de datos; calculando tablas de frecuencias para las variables de tipo cualitativo y estadísticos descriptivos (media, mediana, moda, desviación típica, máximo y mínimo) para las variables cuantitativas. Este análisis nos permite describir el conjunto de datos, sintetizar la información más relevante y ordenar los valores que toman las distintas variables según su porcentaje.
Posteriormente, se han empleado técnicas de inferencia estadística, concretamente se ha realizado la estimación de la media para una población a través de intervalos de confianza (IC) del 95% basados en la t de Student para todas aquellas variables numéricas y estimación de la diferencia de medias de 2poblaciones pareadas a través de intervalos de confianza del 95% utilizando la t de Student para datos pareados, considerando los valores de las variables numéricas a la entrada de urgencia y al alta. Se utilizó el software estadístico IBM SPSS (versión 20).
El estudio fue aprobado por el Comité de Ética e Investigación del HGUCR.
ResultadosDescripción de la poblaciónSe incluyeron un total de 113 pacientes con diagnóstico de SCA; la media muestral de la edad es de 87,9 años, con una desviación estándar (DE)=4,4 y un IC del 95%: 87,2-88,8). De ellos, el 66,4% son mujeres y el 33,6% son hombres, destacando que un 43,4% de los pacientes están institucionalizados frente al 56,6% que no lo están.
Motivos de consulta y comorbilidadPor orden descendente en frecuencia son: deterioro del estado general (31,9%), disnea (17,7%), disminución del nivel de consciencia (14,2%) y fiebre (12,4%). La media muestral del tiempo de hospitalización es de 150,9 h (DE=87) y el IC del 95%:79,5-103,5).
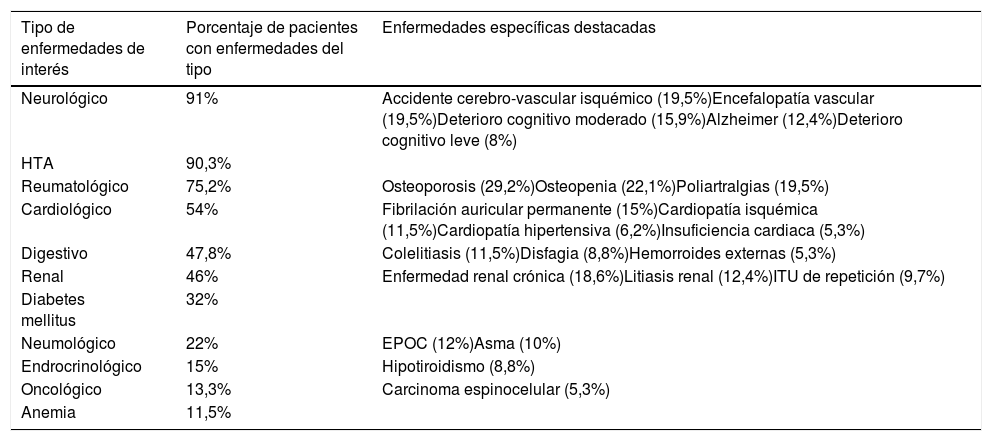
En la tabla 1 se muestran los antecedentes médicos, destacando que un 91% de los pacientes presenta enfermedades de tipo neurológico, señalando por orden descendente: accidente cerebro-vascular isquémico (19,5%), encefalopatía vascular (19,5%), deterioro cognitivo moderado (15,9%), enfermedad de Alzheimer (12,4%) y deterioro cognitivo leve (8%).
Comorbilidad
| Tipo de enfermedades de interés | Porcentaje de pacientes con enfermedades del tipo | Enfermedades específicas destacadas |
|---|---|---|
| Neurológico | 91% | Accidente cerebro-vascular isquémico (19,5%)Encefalopatía vascular (19,5%)Deterioro cognitivo moderado (15,9%)Alzheimer (12,4%)Deterioro cognitivo leve (8%) |
| HTA | 90,3% | |
| Reumatológico | 75,2% | Osteoporosis (29,2%)Osteopenia (22,1%)Poliartralgias (19,5%) |
| Cardiológico | 54% | Fibrilación auricular permanente (15%)Cardiopatía isquémica (11,5%)Cardiopatía hipertensiva (6,2%)Insuficiencia cardiaca (5,3%) |
| Digestivo | 47,8% | Colelitiasis (11,5%)Disfagia (8,8%)Hemorroides externas (5,3%) |
| Renal | 46% | Enfermedad renal crónica (18,6%)Litiasis renal (12,4%)ITU de repetición (9,7%) |
| Diabetes mellitus | 32% | |
| Neumológico | 22% | EPOC (12%)Asma (10%) |
| Endrocrinológico | 15% | Hipotiroidismo (8,8%) |
| Oncológico | 13,3% | Carcinoma espinocelular (5,3%) |
| Anemia | 11,5% |
Dentro de las comorbilidades que presentan nuestros pacientes, se debe destacar que la media muestral en la escala de Charlson es de 1,5 puntos (DE=1,1) y el IC del 95%:=1,2-1,7). Además, el 50% de los pacientes presentan déficit auditivo y visual; un 18,6% ha tenido otros ingresos en los últimos 15 días por diversos motivos y un 18,6% de los pacientes se les ha modificado el tratamiento en los últimos 15 días.
Posible etiología del SCAEl diagnóstico principal fue infección del tracto urinario en el 33,6% de los pacientes, en un 32,6% infección respiratoria de vías bajas y finalmente en el 29,4% probable demencia vascular, mixta o degenerativa.
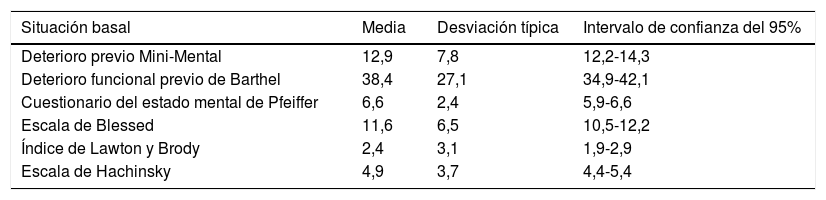
Estado mental y funcional al ingresoEn la tabla 2 se resumen los IC del 95% para la media de los indicadores numéricos que recogen la situación basal de los pacientes.
Situación basal
| Situación basal | Media | Desviación típica | Intervalo de confianza del 95% |
|---|---|---|---|
| Deterioro previo Mini-Mental | 12,9 | 7,8 | 12,2-14,3 |
| Deterioro funcional previo de Barthel | 38,4 | 27,1 | 34,9-42,1 |
| Cuestionario del estado mental de Pfeiffer | 6,6 | 2,4 | 5,9-6,6 |
| Escala de Blessed | 11,6 | 6,5 | 10,5-12,2 |
| Índice de Lawton y Brody | 2,4 | 3,1 | 1,9-2,9 |
| Escala de Hachinsky | 4,9 | 3,7 | 4,4-5,4 |
La frecuencia de polifarmacia (3 o más fármacos) es del 89,4% (101 pacientes), mientras que el uso de más de 5 fármacos presenta una frecuencia del 55,8% (63 pacientes).
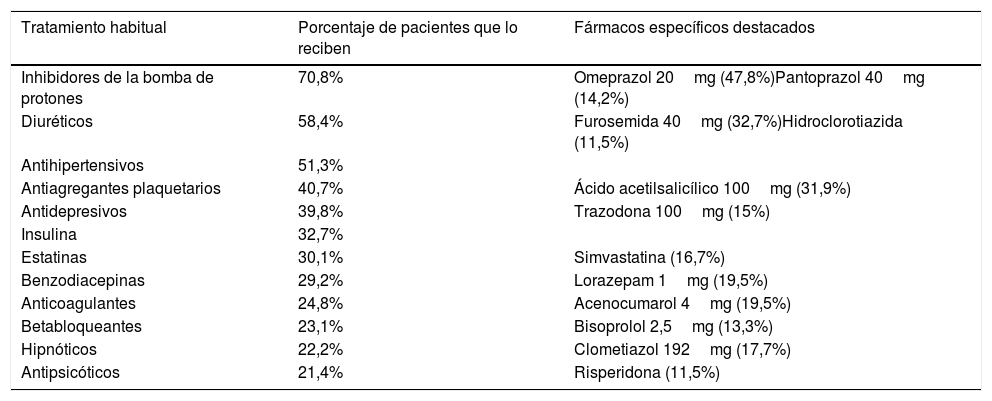
En la tabla 3 se resumen los tratamientos habituales que presentan los pacientes en más de un 20% de los casos, siendo los inhibidores de la bomba de protones (70,8%), los diuréticos (58,4%) y los antihipertensivos (51,3%) los fármacos más frecuentes utilizados por la mayoría de nuestros pacientes.
Tratamiento habitual
| Tratamiento habitual | Porcentaje de pacientes que lo reciben | Fármacos específicos destacados |
|---|---|---|
| Inhibidores de la bomba de protones | 70,8% | Omeprazol 20mg (47,8%)Pantoprazol 40mg (14,2%) |
| Diuréticos | 58,4% | Furosemida 40mg (32,7%)Hidroclorotiazida (11,5%) |
| Antihipertensivos | 51,3% | |
| Antiagregantes plaquetarios | 40,7% | Ácido acetilsalicílico 100mg (31,9%) |
| Antidepresivos | 39,8% | Trazodona 100mg (15%) |
| Insulina | 32,7% | |
| Estatinas | 30,1% | Simvastatina (16,7%) |
| Benzodiacepinas | 29,2% | Lorazepam 1mg (19,5%) |
| Anticoagulantes | 24,8% | Acenocumarol 4mg (19,5%) |
| Betabloqueantes | 23,1% | Bisoprolol 2,5mg (13,3%) |
| Hipnóticos | 22,2% | Clometiazol 192mg (17,7%) |
| Antipsicóticos | 21,4% | Risperidona (11,5%) |
Se encontraron diferencias estadísticamente significativas en las siguientes constantes: frecuencia cardiaca, glucemia, temperatura y saturación de oxígeno, siendo las 3primeras mayores en Urgencias que al alta y la última siendo menor en Urgencias que al alta. Además, destacamos que el 78% de nuestros pacientes presentan sequedad de piel y mucosas; la auscultación es rítmica en la mayoría de los pacientes a la entrada de urgencias (75,2%) y al alta (73,5%) y no observan diferencias significativas. Los ruidos respiratorios patológicos apenas variaron entre el ingreso (60,2%) y el alta (58,5%), siendo los roncus los más frecuentes en ambas situaciones (el 27,4% y el 25,7%, respectivamente). Solo un 8,8% de los pacientes presenta abdomen doloroso a la entrada y un 6,2% al alta, no existiendo diferencias significativas. Un 14,2% de los pacientes presenta edemas en las extremidades y un 12,4% al alta, no existiendo diferencias significativas. La media muestral de Glasgow a la entrada de urgencias es de 13,4 puntos (DE=1,2) e IC del 95%:=13,1-13,6, y al alta la media muestral fue de 14,5 puntos (DE=0,7) e IC del 95%:14,4-14,7. Un 14,2% de los pacientes presentan otras alteraciones neurológicas.
Exploraciones complementariasUn 36,3% de los pacientes presentan un sedimento patológico en el análisis de orina, encontrándose en el urocultivo un 43,6% de positividad en los mismos, destacando con un 14,2% con Escherichia coli como agente causante. Además, en las radiografías de tórax realizadas el 52% de los pacientes presentaban cardiomegalia y el 6,2%, derrame pleural. En el electrocardiograma realizado, se objetivó fibrilación auricular en el 23,9% de los pacientes. Con respecto a las pruebas de imagen, un 7,1% de los pacientes presentan encefalopatía vascular en la TAC.
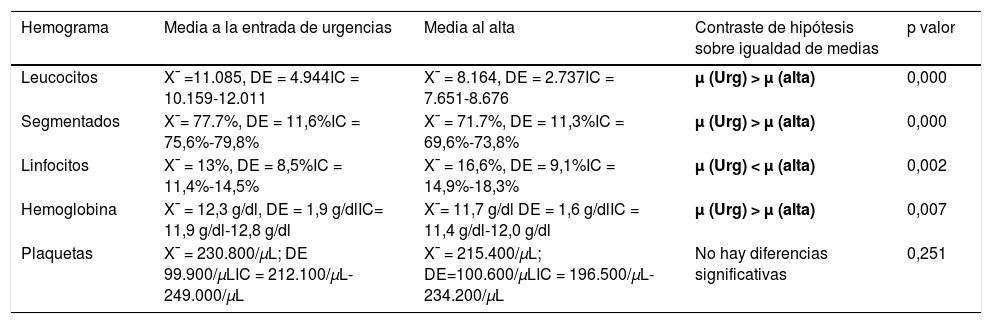
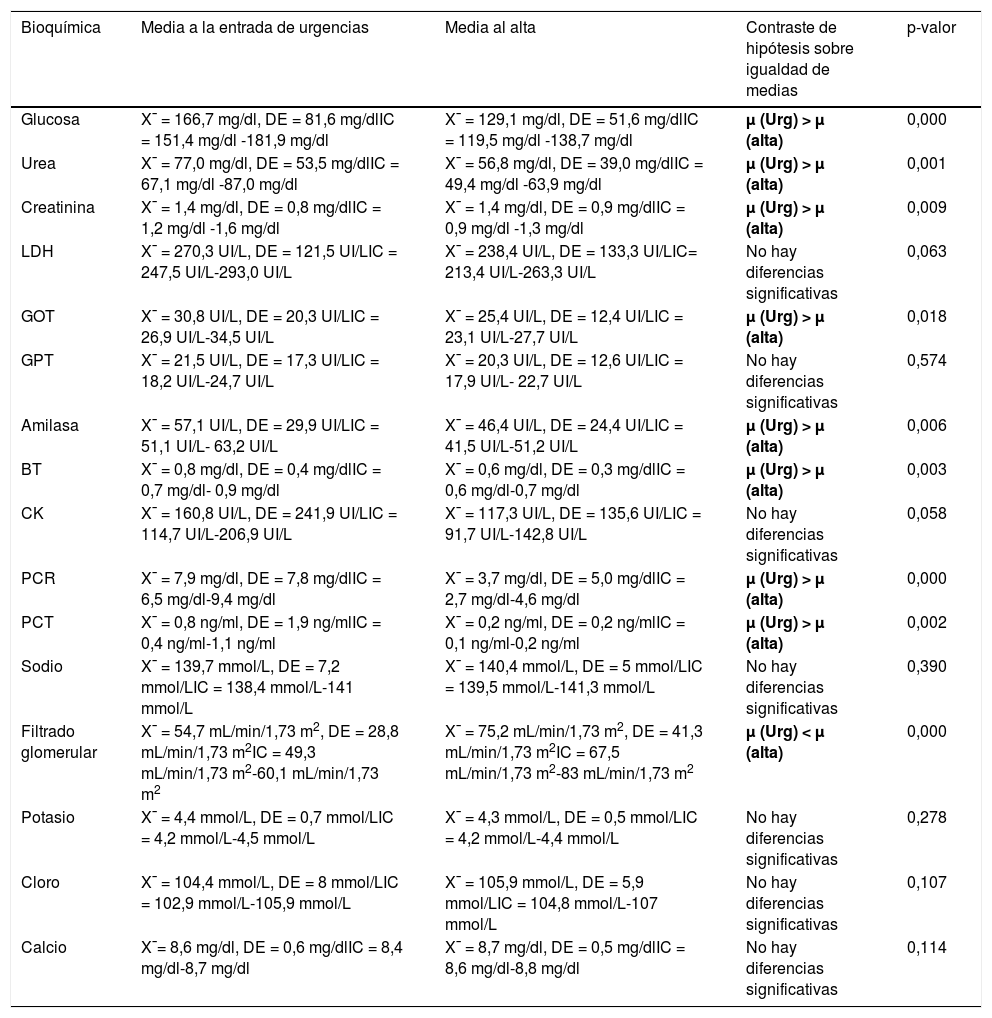
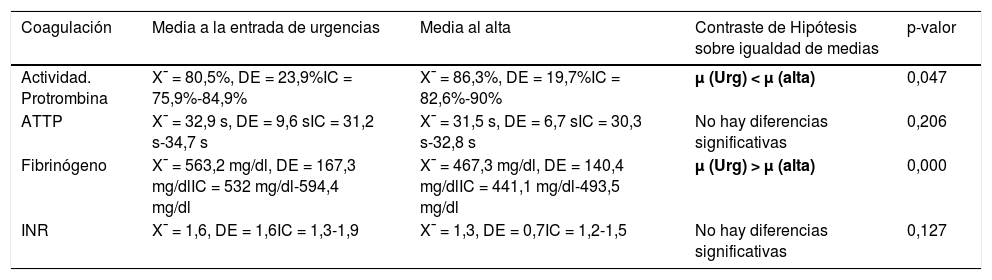
En las tablas 4, 5 y 6 se resumen los resultados de la analítica sanguínea agrupada en hemograma, bioquímica y coagulación.
Resultados hemograma
| Hemograma | Media a la entrada de urgencias | Media al alta | Contraste de hipótesis sobre igualdad de medias | p valor |
|---|---|---|---|---|
| Leucocitos | X¯ =11.085, DE = 4.944IC = 10.159-12.011 | X¯ = 8.164, DE = 2.737IC = 7.651-8.676 | μ (Urg) > μ (alta) | 0,000 |
| Segmentados | X¯= 77.7%, DE = 11,6%IC = 75,6%-79,8% | X¯ = 71.7%, DE = 11,3%IC = 69,6%-73,8% | μ (Urg) > μ (alta) | 0,000 |
| Linfocitos | X¯ = 13%, DE = 8,5%IC = 11,4%-14,5% | X¯ = 16,6%, DE = 9,1%IC = 14,9%-18,3% | μ (Urg) < μ (alta) | 0,002 |
| Hemoglobina | X¯ = 12,3 g/dl, DE = 1,9 g/dlIC= 11,9 g/dl-12,8 g/dl | X¯= 11,7 g/dl DE = 1,6 g/dlIC = 11,4 g/dl-12,0 g/dl | μ (Urg) > μ (alta) | 0,007 |
| Plaquetas | X¯ = 230.800/μL; DE 99.900/μLIC = 212.100/μL-249.000/μL | X¯ = 215.400/μL; DE=100.600/μLIC = 196.500/μL-234.200/μL | No hay diferencias significativas | 0,251 |
Resultados bioquímica
| Bioquímica | Media a la entrada de urgencias | Media al alta | Contraste de hipótesis sobre igualdad de medias | p-valor |
|---|---|---|---|---|
| Glucosa | X¯ = 166,7 mg/dl, DE = 81,6 mg/dlIC = 151,4 mg/dl -181,9 mg/dl | X¯ = 129,1 mg/dl, DE = 51,6 mg/dlIC = 119,5 mg/dl -138,7 mg/dl | μ (Urg) > μ (alta) | 0,000 |
| Urea | X¯ = 77,0 mg/dl, DE = 53,5 mg/dlIC = 67,1 mg/dl -87,0 mg/dl | X¯ = 56,8 mg/dl, DE = 39,0 mg/dlIC = 49,4 mg/dl -63,9 mg/dl | μ (Urg) > μ (alta) | 0,001 |
| Creatinina | X¯ = 1,4 mg/dl, DE = 0,8 mg/dlIC = 1,2 mg/dl -1,6 mg/dl | X¯ = 1,4 mg/dl, DE = 0,9 mg/dlIC = 0,9 mg/dl -1,3 mg/dl | μ (Urg) > μ (alta) | 0,009 |
| LDH | X¯ = 270,3 UI/L, DE = 121,5 UI/LIC = 247,5 UI/L-293,0 UI/L | X¯ = 238,4 UI/L, DE = 133,3 UI/LIC= 213,4 UI/L-263,3 UI/L | No hay diferencias significativas | 0,063 |
| GOT | X¯ = 30,8 UI/L, DE = 20,3 UI/LIC = 26,9 UI/L-34,5 UI/L | X¯ = 25,4 UI/L, DE = 12,4 UI/LIC = 23,1 UI/L-27,7 UI/L | μ (Urg) > μ (alta) | 0,018 |
| GPT | X¯ = 21,5 UI/L, DE = 17,3 UI/LIC = 18,2 UI/L-24,7 UI/L | X¯ = 20,3 UI/L, DE = 12,6 UI/LIC = 17,9 UI/L- 22,7 UI/L | No hay diferencias significativas | 0,574 |
| Amilasa | X¯ = 57,1 UI/L, DE = 29,9 UI/LIC = 51,1 UI/L- 63,2 UI/L | X¯ = 46,4 UI/L, DE = 24,4 UI/LIC = 41,5 UI/L-51,2 UI/L | μ (Urg) > μ (alta) | 0,006 |
| BT | X¯ = 0,8 mg/dl, DE = 0,4 mg/dlIC = 0,7 mg/dl- 0,9 mg/dl | X¯ = 0,6 mg/dl, DE = 0,3 mg/dlIC = 0,6 mg/dl-0,7 mg/dl | μ (Urg) > μ (alta) | 0,003 |
| CK | X¯ = 160,8 UI/L, DE = 241,9 UI/LIC = 114,7 UI/L-206,9 UI/L | X¯ = 117,3 UI/L, DE = 135,6 UI/LIC = 91,7 UI/L-142,8 UI/L | No hay diferencias significativas | 0,058 |
| PCR | X¯ = 7,9 mg/dl, DE = 7,8 mg/dlIC = 6,5 mg/dl-9,4 mg/dl | X¯ = 3,7 mg/dl, DE = 5,0 mg/dlIC = 2,7 mg/dl-4,6 mg/dl | μ (Urg) > μ (alta) | 0,000 |
| PCT | X¯ = 0,8 ng/ml, DE = 1,9 ng/mlIC = 0,4 ng/ml-1,1 ng/ml | X¯ = 0,2 ng/ml, DE = 0,2 ng/mlIC = 0,1 ng/ml-0,2 ng/ml | μ (Urg) > μ (alta) | 0,002 |
| Sodio | X¯ = 139,7 mmol/L, DE = 7,2 mmol/LIC = 138,4 mmol/L-141 mmol/L | X¯ = 140,4 mmol/L, DE = 5 mmol/LIC = 139,5 mmol/L-141,3 mmol/L | No hay diferencias significativas | 0,390 |
| Filtrado glomerular | X¯ = 54,7 mL/min/1,73 m2, DE = 28,8 mL/min/1,73 m2IC = 49,3 mL/min/1,73 m2-60,1 mL/min/1,73 m2 | X¯ = 75,2 mL/min/1,73 m2, DE = 41,3 mL/min/1,73 m2IC = 67,5 mL/min/1,73 m2-83 mL/min/1,73 m2 | μ (Urg) < μ (alta) | 0,000 |
| Potasio | X¯ = 4,4 mmol/L, DE = 0,7 mmol/LIC = 4,2 mmol/L-4,5 mmol/L | X¯ = 4,3 mmol/L, DE = 0,5 mmol/LIC = 4,2 mmol/L-4,4 mmol/L | No hay diferencias significativas | 0,278 |
| Cloro | X¯ = 104,4 mmol/L, DE = 8 mmol/LIC = 102,9 mmol/L-105,9 mmol/L | X¯ = 105,9 mmol/L, DE = 5,9 mmol/LIC = 104,8 mmol/L-107 mmol/L | No hay diferencias significativas | 0,107 |
| Calcio | X¯= 8,6 mg/dl, DE = 0,6 mg/dlIC = 8,4 mg/dl-8,7 mg/dl | X¯ = 8,7 mg/dl, DE = 0,5 mg/dlIC = 8,6 mg/dl-8,8 mg/dl | No hay diferencias significativas | 0,114 |
BT: bilirrubina total; CK: creatincinasa; LDH: lactato deshidrogenasa; GOT: glutámico-oxalacética transaminasa; GPT: glutamicopirúvica transaminasa; PCR: proteína C reactiva; PCT: procalcitonina. La letra griega μ representa la media.
Resultados coagulación
| Coagulación | Media a la entrada de urgencias | Media al alta | Contraste de Hipótesis sobre igualdad de medias | p-valor |
|---|---|---|---|---|
| Actividad. Protrombina | X¯ = 80,5%, DE = 23,9%IC = 75,9%-84,9% | X¯ = 86,3%, DE = 19,7%IC = 82,6%-90% | μ (Urg) < μ (alta) | 0,047 |
| ATTP | X¯ = 32,9 s, DE = 9,6 sIC = 31,2 s-34,7 s | X¯ = 31,5 s, DE = 6,7 sIC = 30,3 s-32,8 s | No hay diferencias significativas | 0,206 |
| Fibrinógeno | X¯ = 563,2 mg/dl, DE = 167,3 mg/dlIC = 532 mg/dl-594,4 mg/dl | X¯ = 467,3 mg/dl, DE = 140,4 mg/dlIC = 441,1 mg/dl-493,5 mg/dl | μ (Urg) > μ (alta) | 0,000 |
| INR | X¯ = 1,6, DE = 1,6IC = 1,3-1,9 | X¯ = 1,3, DE = 0,7IC = 1,2-1,5 | No hay diferencias significativas | 0,127 |
ATTP: tiempo de tromboplastina parcial activada; INR: ratio internacional normalizada. La letra griega μ representa la media.
En nuestro estudio, los antecedentes médicos más frecuentes fueron las enfermedades neurológicas y la HTA, seguidas de las enfermedades reumatológicas. Los motivos de consulta principales fueron el deterioro del estado general, la disnea, la disminución del nivel de consciencia y la fiebre. Resulta de crucial importancia la incidencia de la polifarmacia, especialmente el papel de fármacos como los diuréticos, una potencial causa de trastornos hidroelectrolíticos, o la alta prevalencia de tratamiento con benzodiacepinas o hipnóticos, otra frecuente y conocida causa de delirium. En relación con la etiología principal del síndrome confusional, es destacable el papel de las infecciones, sobre todo las de tipo urinario y respiratorio, junto con el del síndrome demencial.
Como en otros estudios27-29, podemos observar la incidencia de la polifarmacia y su efecto nocivo en pacientes ancianos debido a la influencia de los cambios metabólicos producidos por la edad, al mayor número de comorbilidades y al mayor riesgo de toxicidad e interacciones farmacológicas, destacando sobre todo el uso de fármacos anticolinérgicos, hipnóticos sedantes y antipsicóticos, asociados a una mayor morbimortalidad en pacientes ancianos. En cuanto a los factores precipitantes o desencadenantes encontrados, los más frecuentes son las infecciones de tipo urinario y respiratorio coincidiendo con diversos estudios publicados30-32, señalando además la ausencia en nuestros pacientes de alteraciones hidroelectrolíticas como uno de los factores desencadenantes principales a diferencia de lo mencionado en otros estudios3,30,33, donde sí se constata la presencia de una hiper/hiponatremia. Se deben destacar como implicaciones clínicas de nuestro estudio la mejora en el adecuado conocimiento de los factores de riesgo y precipitantes del SCA, constituyendo éste la base para el desarrollo de medidas preventivas necesarias para el abordaje integral del SCA. Entre estas medidas podemos destacar la prevención de infecciones y evitar el uso continuado de fármacos perjudiciales y precipitantes, entre otras.
Con respecto a las limitaciones la más importante, sería el carácter fundamentalmente descriptivo del estudio y el corto período de seguimiento. Si embargo, creemos que nuestros resultados contribuyen a un mejor conocimiento de los pacientes de nuestro medio, posibilitando así una mejor prevención y abordaje integral del delirium en Atención Primaria y Urgencias.
Finalmente, queremos destacar el papel fundamental de las enfermedades neurológicas (especialmente la demencia), la HTA, la polifarmacia (sobre todo el uso inadecuado de benzodiacepinas e hipnóticos) y las infecciones urinarias y respiratorias como factores tratables o prevenibles del delirium en paciente de Atención Primaria en nuestro medio.
FinanciaciónEl presente trabajo no recibió financiación para su desarrollo. La publicación del mismo fue financiada por la Universidad de Granada.
Conflicto de interesesLos autores declaran no tener ningún conflicto de interés.