Analizar si la adquisición de flujo directo al angiosoma isquémico del pie influye en la cicatrización y en el salvamento de la extremidad ante isquemia crítica tratada mediante terapia endovascular.
Material y métodosAnálisis retrospectivo de 34 extremidades (32 pacientes) consecutivas con isquemia crónica categoría 5 (n = 21; 61,8 %) y 6 (n = 13; 38,2 %) de Rutherford y tratadas exitosamente mediante técnica endovascular, entre 2007 y 2009. Elaboramos dos grupos: el grupo de revascularización directa o RD (la arteria revascularizada nutre directamente el angiosoma isquémico) y el grupo de revascularización indirecta o RI (la arteria revascularizada no nutre directamente el angiosoma isquémico). Se analizó la cicatrización completa, el tiempo de cicatrización y la tasa de salvamento de la extremidad. El análisis estadístico incluyó la prueba de Chi-cuadrado y tablas de supervivencia.
ResultadosSe incluyeron 34 extremidades sometidas a recanalización (n = 27; 79,4 %), angioplastia simple (n = 3; 8,8 %) y angioplastia con stent (n = 4; 11,8 %). El grupo RD incluyó 18 (52,9 %) extremidades y el grupo RI 16 (47,1 %). Al comparar comorbilidades, no se encontraron diferencias significativas. El 76,5% (n = 26) de las heridas cicatrizaron completamente y no resultó diferente el tiempo total de curación (RD 157,8 días frente a RI 124,5 días). Al comparar el éxito de cicatrización completa (RD n = 14 [77,8 %] frente a RI n = 12 [73,7 %]) y la tasa de salvamento de extremidad al año (RD 89 % frente a RI 84 %) tampoco hubo diferencias.
ConclusiónEn nuestra serie, la revascularización directa o indirecta del angiosoma no influye en la tasa de cicatrización y de salvamento de la extremidad.
To determine whether the acquisition of direct flow to ischaemic foot angiosome affects healing and limb salvage in critical limb ischaemia treated by endovascular therapy.
Material and methodsRetrospective analysis of 34 consecutive limbs (32 patients) with chronic ischaemia, Rutherford category 5 (n = 21, 61.8 %) and 6 (n = 13, 38.2 %) and successfully treated with endovascular technique, between 2007 and 2009. We created two groups: the direct revascularisation group or DR (revascularised artery directly feeds the ischaemic angiosome) and the indirect revascularisation group or IR (revascularised artery does not directly feed the ischaemic angiosome). The variables analysed were: complete healing, healing time and limb salvage rates. Statistical analysis included Chi-square test and survival tables.
ResultsWe included 34 limbs who underwent recanalisation (n = 27, 79.4 %), simple angioplasty (n = 3, 8.8 %) and angioplasty with stents (n = 4; 11.8%). The DR group included 18 (52.9 %) limbs and the IR group 16 (47.1 %). We did not find significant differences when comparing comorbidities. There was complete healing in 76.5 % (n = 26) of the wounds and there were no difference in the total healing time (157.8 days in DR against 124.5 days in IR). There were no differences when comparing the success of complete healing (DR n = 14 [77.8 %] against IR n = 12 [73.7 %]) and the limb salvage rate per year (89 % DR against 84 % IR).
ConclusionIn our series, the direct or indirect revascularisation angiosome does not affect the rate of healing and limb salvage.
En la actualidad, gracias a los avances adquiridos en el tratamiento endovascular para la isquemia crítica de miembros inferiores, se dispone de una atractiva alternativa a la cirugía abierta de bypass1,2. Sin embargo, a pesar de una revascularización exitosa, la cicatrización de las lesiones isquémicas de extremidad inferior puede fracasar. Esto puede ser consecuencia del tratamiento inadecuado de la herida durante el postoperatorio. Sin embargo, intuitivamente se puede pensar que las heridas no lleguen a curar debido a una incorrecta conexión vascular entre la arteria revascularizada y la zona isquémica local.
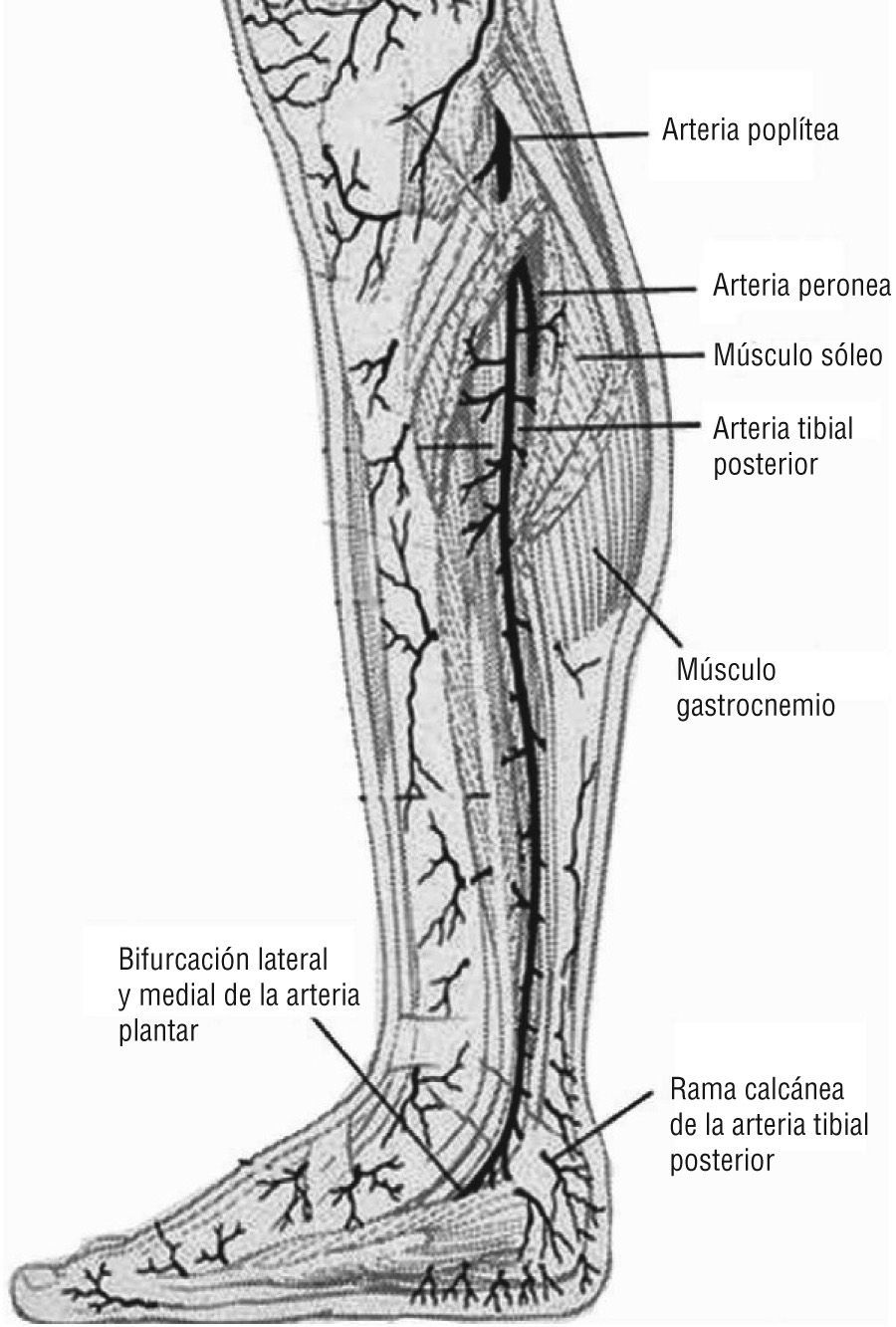
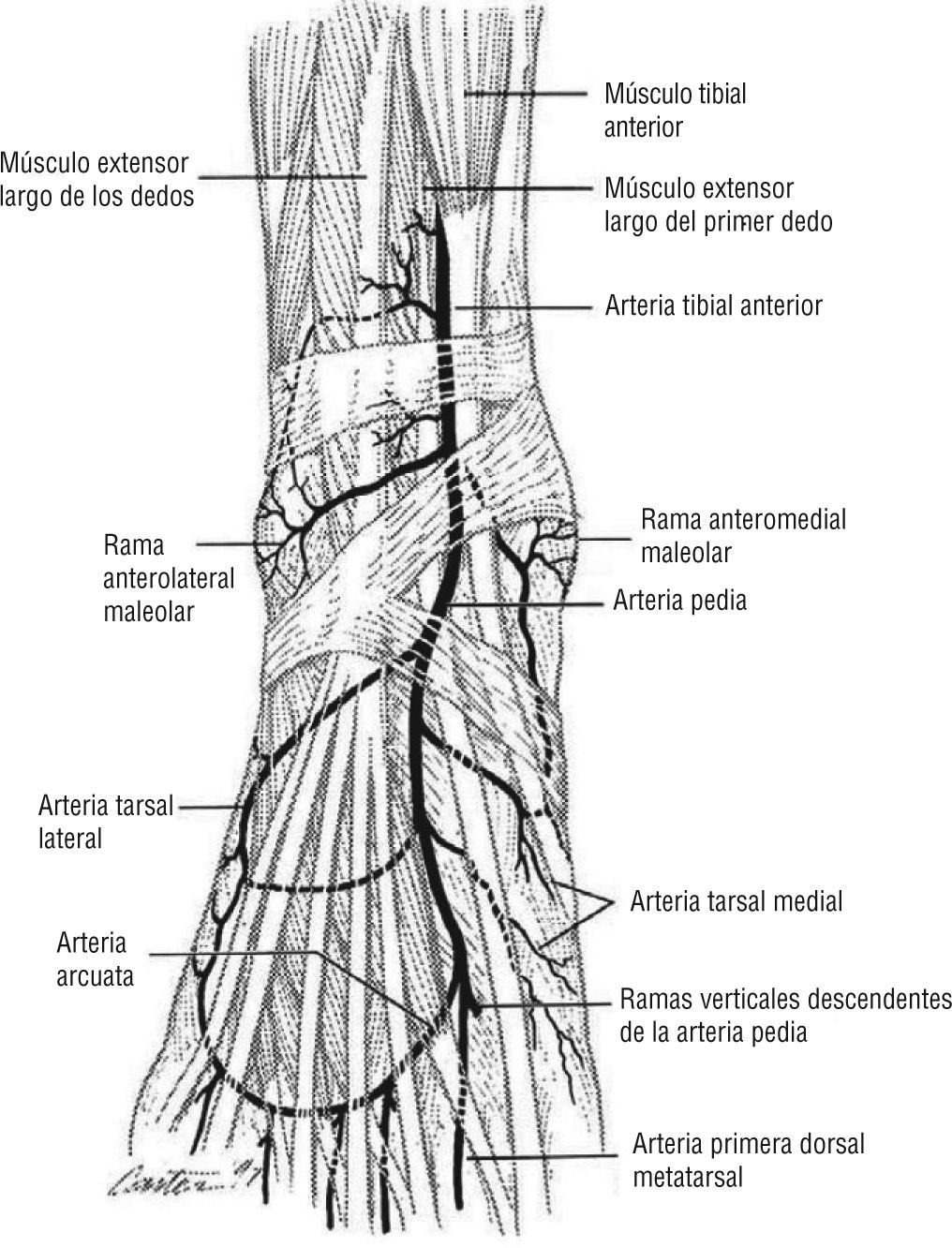
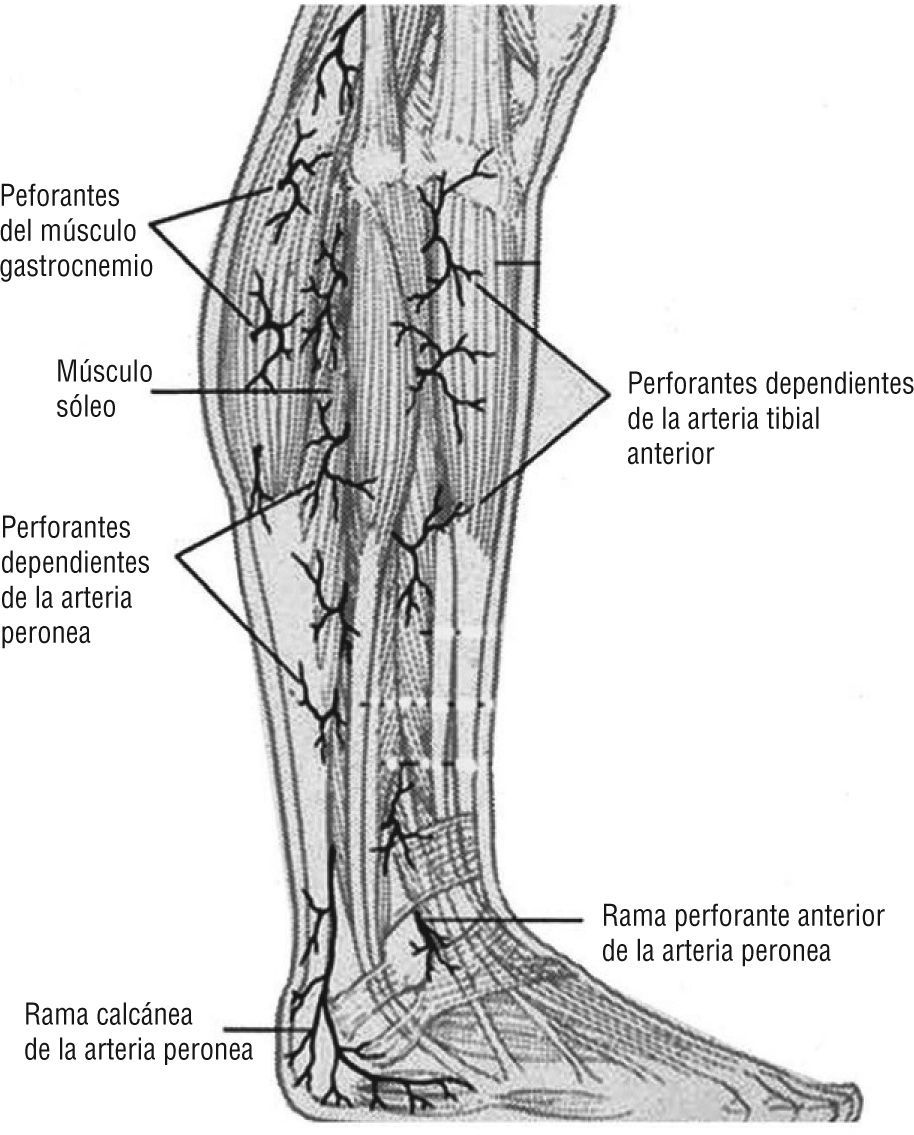
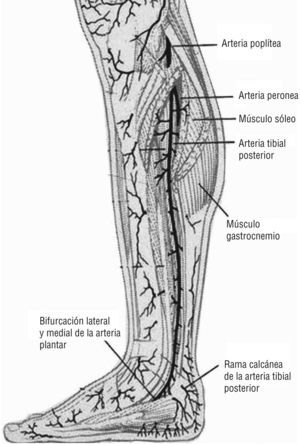
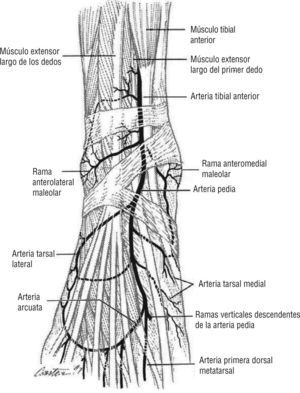
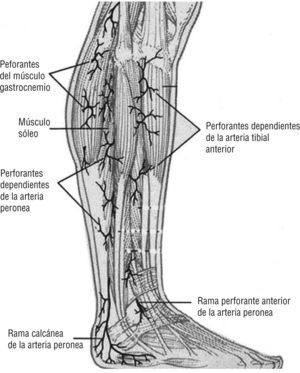
A este nivel entra en juego el concepto de angiosoma, creado por Taylor y Pan en 19873-7, y por el cual el cuerpo queda dividido en territorios vasculares tridimensionales irrigados por arterias específicas y drenados por las venas correspondientes. La zona del pie y el tobillo está formada por cinco angiosomas diferentes4,5 dependientes de la arteria tibial posterior (tres angiosomas), la arteria tibial anterior (un angiosoma) y la arteria peronea (un angiosoma). La arteria tibial posterior (fig. 1) da lugar a la rama calcánea que vasculariza la porción medial del tobillo y plantar del talón; una rama plantar medial que irriga el dorso del pie y una rama plantar lateral que alimenta la porción lateral del antepié y plantar del medio tarso y del antepié. La arteria tibial anterior (fig. 2) continúa por el dorso del pie como arteria pedia. La arteria peronea (fig. 3) nutre la cara lateral del tobillo y plantar del talón a través de su rama calcánea y la cara anterior de la porción superior del tobillo a través de una rama anterior3-7. El talón es una zona privilegiada irrigada por ramas de la arteria peronea y de la tibial posterior. Algunos autores consideran dos angiosomas diferentes a partir de estas dos ramas y dividen el pie en seis angiosomas 1,6,7. En nuestro estudio se tuvo en cuenta la división del pie y el tobillo en cinco angiosomas.
Arteria tibial posterior. Emite perforantes que surgen entre la musculatura flexora y el músculo sóleo. Imagen cedida por Attinger CE et al6.
Arteria tibial anterior. Nutre todo el dorso del pie. Imagen cedida por Attinger CE et al6.
Arteria peronea. Se desplaza sobre la cara medial del peroné y nutre la región posterolateral e inferior de la pierna, el tobillo y el talón. Imagen cedida por Attinger CE et al6.
Aunque el concepto de angiosoma se ha demostrado beneficioso en la cirugía de bypass3,8 para extremidades con úlceras isquémicas, no está claro si resulta también útil cuando se lleva a cabo tratamiento endovascular. Sabemos que el factor a considerar para lograr buenos resultados tras la terapia endovascular es el runoff1,8,9, por ello, nos planteamos la hipótesis de si además debe considerarse la anatomía arterial específica del angiosoma isquémico a la hora de planificar la revascularización.
Pacientes y métodosAnalizamos de forma retrospectiva 32 pacientes consecutivos, con lesiones tróficas isquémicas, que requirieron la revascularización de la extremidad mediante técnica endovascular en el sector infrarrotuliano. En todos los casos incluídos, el tratamiento endovascular resultó exitoso. Se llevó a cabo la exploración de la herida y del estado vascular mediante la palpación de pulsos y el estudio hemodinámico con el índice tobillobrazo (ITB) y la fotopletismografía para valorar el poder de cicatrización. Se consideró la revascularización en los casos con lesiones tróficas compatibles con el diagnóstico de isquemia crítica de la TASC II10. Se realizó estudio arteriográfico en todas las extremidades previo a la revascularización. Las heridas, en los casos que lo precisaran por infección o gangrena húmeda, fueron desbridadas antes de la revascularización.
Se trató de un estudio abierto, en el que un único investigador revisó las arteriografías preoperatorias de cada extremidad y clasificó las heridas según su localización con respecto al angiosoma primario, que incluyó la arteria peronea (calcánea lateral y perforante anterior), la arteria tibial anterior y la arteria tibial posterior (calcánea medial, plantar medial y plantar lateral). De esta manera, se definieron dos grupos de estudio: revascularización directa (RD) y revascularización indirecta (RI). La revascularización directa supuso el tratamiento endovascular directamente de la arteria o arterias que nutrían el angiosoma o angiosomas donde se localizaban las lesiones. La revascularización indirecta implicaba el tratamiento endovascular de arterias que no nutrían directamente el angiosoma o angiosomas isquémicos. Así pues, en algunos casos las lesiones podían ser varias, con localización en distintos territorios del pie y tobillo y, por tanto, con afectación de varios angiosomas. De esta manera, para definir la revascularización directa, se tuvo en cuenta que se hubieran tratado todas las arterias implicadas en la nutrición directa de los angiosomas afectos. Así, pacientes con revascularización directa de un angiosoma, en los que además se revascularizó otro vaso de otro angiosoma pero sin lesión, se consideraron RD. Pacientes con varios angiosomas afectos y en los que se realizó revascularización directa de todos ellos, se consideraron también del grupo RD. Y si había varios angiosomas con lesión pero no todos se revascularizaron a través de su vaso principal, se consideraron del grupo RI.
La técnica endovascular suponía la recanalización seguida siempre de angioplastia en los casos en que había oclusión arterial, o bien angioplastia simple en los casos de estenosis arterial grave, que además, en algún caso, requirió la implantación de stent. Tras la terapia endovascular, las heridas fueron tratadas con los cuidados tópicos adecuados hasta que presentaban tejido de granulación. Las curas eran realizadas por personal de enfermería especializado, a base de higiene diaria con jabón y solución salina estéril, con desbridamiento (normalmente mecánico o químico a base de uroquinasa) en los casos que lo precisaran y con asociación de antibiótico sistémico en los casos de sobreinfección. Cinco (14,7 %) casos fueron tratados además con cámara hiperbárica, dos (12,5 %) del grupo RI y tres (16,7 %) del grupo RD. Además, se realizaron revisiones sistemáticas por parte del médico cada semana tras el procedimiento endovascular, con control de las heridas, exploración de pulsos y realización de ITB y fotopletismografía.
El resultado clínico se consideró exitoso en los casos en los que se logró la curación de las lesiones y la desaparición del dolor, o bien se clasificó como fracaso del tratamiento en aquellos en los que persistió la isquemia crítica. Los casos que fracasaron se consideraron candidatos para la amputación mayor y, en algún caso, se repitió la terapia endovascular.
Se revisaron también los historiales médicos hospitalarios y se recogieron los antecedentes patológicos comórbidos en cada paciente para después comparar su presencia en ambos grupos de estudio. Aparte de los típicos factores de riesgo vascular (tabaquismo, hipertensión arterial, diabetes mellitus y dislipidemia), se recopiló la presencia de episodios previos agudos coronarios (cardiopatía isquémica), incluyendo tanto angor como infarto agudo de miocardio y cerebrovasculares (ECVA), con inclusión tanto del accidente isquémico transitorio, como del infarto o la hemorragia cerebrales. La presencia de tabaquismo incluyó tanto a fumadores activos como a exfumadores. También se tuvo en cuenta la presencia de enfermedad pulmonar obstructiva crónica y de insuficiencia renal crónica. Esta última se consideró presente en aquellos casos con una velocidad de filtración glomerular inferior a 60ml/min/1,73m2.
El análisis estadístico se llevó a cabo con el programa SPSS Statistics 17.0. Se emplearon las pruebas de Chi-cuadrado y exacta de Fisher para la comparación de las comorbilidades, así como de la consecución de curación completa, entre los grupos RI y RD. Se utilizó la prueba de la t de Student para la comparación de las medias del tiempo de curación y de las medias del ITB y la prueba de Mantel-Cox para comparar las tasas de salvamento de extremidad. Se consideró la existencia de significación estadística con un valor p < 0,05. Para el cálculo de las tasas de salvamento de extremidad se calcularon las curvas de Kaplan-Meier.
ResultadosSe revisaron 34 extremidades en 32 pacientes consecutivos. Todos con lesiones tróficas isquémicas tratadas mediante tratamiento endovascular del sector infrarrotuliano. La terapia endovascular resultó exitosa en todos los casos ya que previamente se excluyeron del estudio tres extremidades en las que el tratamiento endovascular fracasó en este mismo período de tiempo. El seguimiento medio de los casos fue de 16,47 (desviación estándar [DE] 49,67; rango 47,2-0,37) meses.
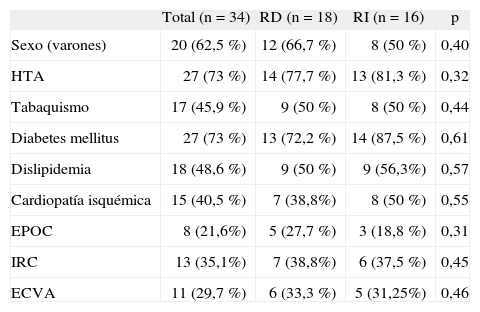
La edad media de los pacientes fue de 73,46 (DE 12,87; rango 89–49) años, 20 (62,5 %) eran varones. Del total, el 73 % (n = 27) eran diabéticos e hipertensos, el 48,6 % (n = 18) referían alteraciones del metabolismo lipídico, el 45,9 % padecían tabaquismo y el 40,5 % sufrían cardiopatía isquémica. No se observaron diferencias estadísticamente significativas al comparar las comorbilidades de ambos grupos de estudio (tabla 1).
Resultados de la comparación de comorbilidades entre los grupos de revascularización directa e indirecta
| Total (n = 34) | RD (n = 18) | RI (n = 16) | p | |
| Sexo (varones) | 20 (62,5 %) | 12 (66,7 %) | 8 (50 %) | 0,40 |
| HTA | 27 (73 %) | 14 (77,7 %) | 13 (81,3 %) | 0,32 |
| Tabaquismo | 17 (45,9 %) | 9 (50 %) | 8 (50 %) | 0,44 |
| Diabetes mellitus | 27 (73 %) | 13 (72,2 %) | 14 (87,5 %) | 0,61 |
| Dislipidemia | 18 (48,6 %) | 9 (50 %) | 9 (56,3%) | 0,57 |
| Cardiopatía isquémica | 15 (40,5 %) | 7 (38,8%) | 8 (50 %) | 0,55 |
| EPOC | 8 (21,6%) | 5 (27,7 %) | 3 (18,8 %) | 0,31 |
| IRC | 13 (35,1%) | 7 (38,8%) | 6 (37,5 %) | 0,45 |
| ECVA | 11 (29,7 %) | 6 (33,3 %) | 5 (31,25%) | 0,46 |
ECVA: enfermedad cerebrovascular aguda; EPOC: enfermedad pulmonar obstructiva crónica; HTA: hipertensión arterial; IRC: insuficiencia renal crónica; RD: revascularización directa; RI: revascularización indirecta.
El 61,8 % (n = 21) pertenecían a la categoría Rutherford 5 de isquemia crítica y el restante 38,2 % (n = 13) a la categoría 6. Revisadas las arteriografías y hojas operatorias, se clasificaron las extremidades en los dos grupos de estudio, de manera que en 18 (52,9 %) se llevó a cabo una revascularización directa (RD) y las restantes 16 extremidades (47,1 %) fueron sometidas a revascularización indirecta (RI) de los angiosomas isquémicos. En el grupo RD, 6 (33,3 %) extremidades presentaban isquemia crítica grado 6 de Rutherford y en el grupo RI, 7 (43,8 %) extremidades pertenecían a esa categoría de isquemia crítica. Tampoco en este aspecto se obtuvieron diferencias estadísticas entre los grupos RD y RI (p = 0,51).
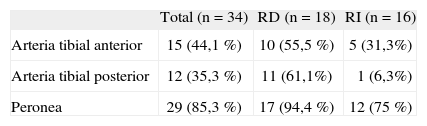
Todos los procedimientos endovasculares se llevaron a cabo sobre arterias infrarrotulianas, siempre que presentaran oclusión o, al menos, estenosis hemodinámicamente significativa (> 50 %) en la arteriografía preoperatoria. Las arterias tratadas se resumen en la tabla 2; la arteria peronea fue la que más se sometió a terapia, en muchos casos por ser el único tronco distal permeable.
Arterias tratadas por técnica endovascular
| Total (n = 34) | RD (n = 18) | RI (n = 16) | |
| Arteria tibial anterior | 15 (44,1 %) | 10 (55,5 %) | 5 (31,3%) |
| Arteria tibial posterior | 12 (35,3 %) | 11 (61,1%) | 1 (6,3%) |
| Peronea | 29 (85,3 %) | 17 (94,4 %) | 12 (75 %) |
RD: revascularización directa; RI: revascularización indirecta.
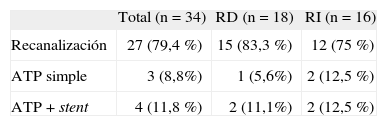
Las técnicas endovasculares llevadas a cabo fueron similares en ambos grupos y se resumen en la tabla 3; el procedimiento más comúnmente efectuado fue la recanalización, en aproximadamente el 80 % de las extremidades, ya que presentaban oclusión del tronco distal afecto.
Técnicas endovasculares realizadas
| Total (n = 34) | RD (n = 18) | RI (n = 16) | |
| Recanalización | 27 (79,4 %) | 15 (83,3 %) | 12 (75 %) |
| ATP simple | 3 (8,8%) | 1 (5,6%) | 2 (12,5 %) |
| ATP + stent | 4 (11,8 %) | 2 (11,1%) | 2 (12,5 %) |
ATP: angioplastia transluminal percutánea; RD: revascularización directa; RI: revascularización indirecta.
En cuanto al factor hemodinámico, el ITB medio del grupo total antes del tratamiento resultó en 0,47 que, tras la revascularización, en el grupo total ascendió a 0,79. En el grupo RD el ITB medio antes del tratamiento era 0,49 (DE 0,19) y tras el procedimiento endovascular 0,88 (DE 0,22). El ITB medio en el grupo RI previo al procedimiento era 0,41 (DE 0,24) y tras el tratamiento 0,65 (de 0,26). Al comparar el ITB medio entre los grupos RD y RI mediante la prueba t de Student, no se obtuvieron diferencias significativas (p = 0,86). Ha de tenerse en cuenta que 4 (11,7 %) casos presentaban calcinosis arterial y, por tanto, el ITB no era valorable, por lo que no se tuvieron en cuenta en el cálculo de las medias. Por ello, también se valoró el estado de cada extremidad mediante fotopletismografía. Antes del procedimiento endovascular en el grupo RD había sólo un (5,6 %) caso con fotopletismografía que resultaba fásica, y tras el tratamiento, en las 18 (100 %) extremidades que conformaban ese grupo era fásica. En el grupo RI hubo una evolución similar, con sólo un (6,3 %) caso con fotopletismografía fásica antes del tratamiento y con los 16 (100 %) casos fásica tras el mismo.
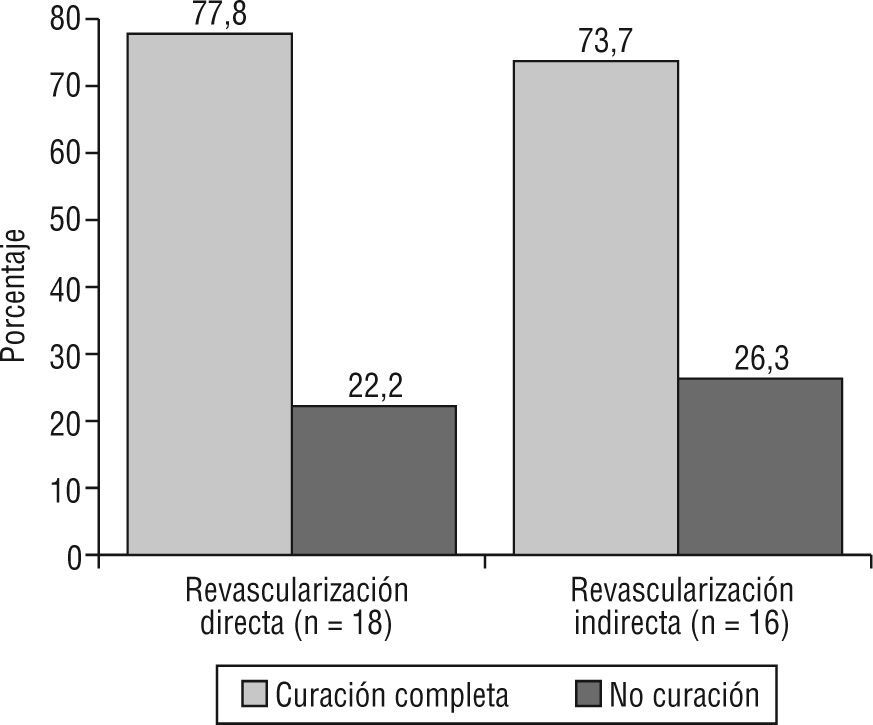
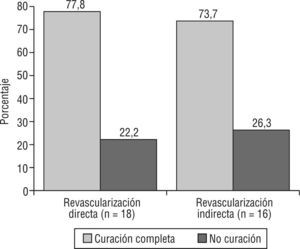
La cicatrización completa se alcanzó en 26 extremidades (76,5 %). En 8 extremidades las heridas no curaron por lo que 6 precisaron la amputación mayor. Al comparar en ambos grupos la tasa de cicatrización (RD 77,8 % frente a RI 73,7 %) mediante la prueba exacta de Fisher, no se obtuvieron diferencias (p = 0,77). La tasa de curación de ambos grupos se representa en la figura 4.
Al comparar la media del tiempo transcurrido hasta la cicatrización completa mediante la prueba de t de Student tampoco se observaron diferencias estadísticamente significativas entre las extremidades sometidas a RD frente a las sometidas a RI (RD 157,8 días frente a RI 124,5 días; p = 0,97).
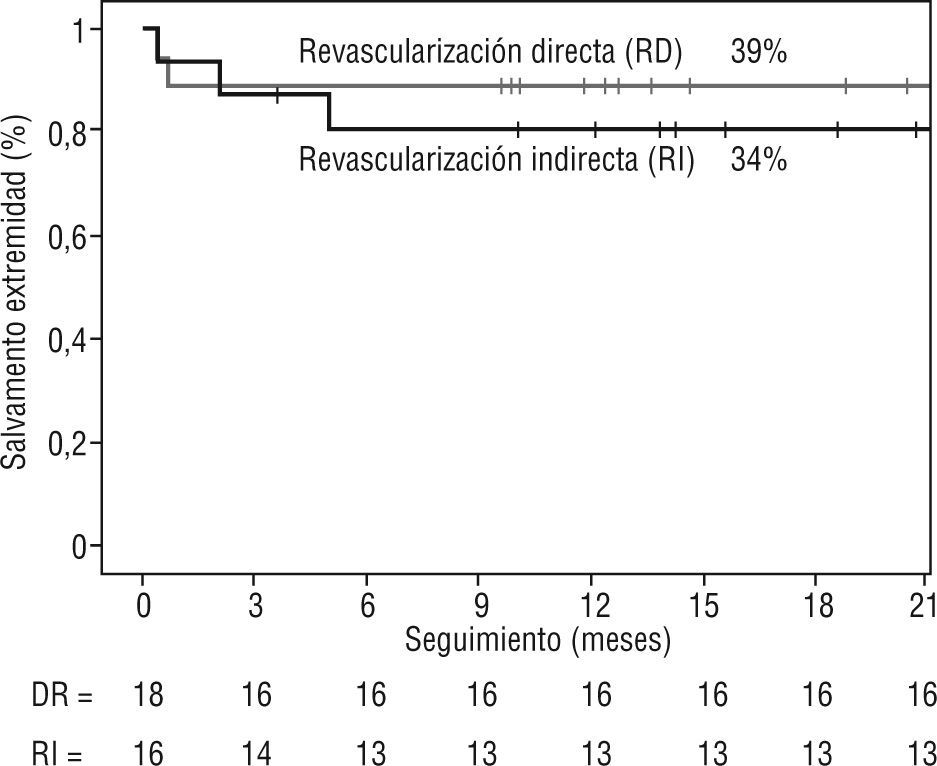
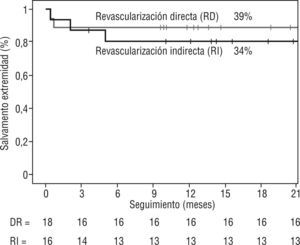
Finalmente se efectuaron 6 amputaciones mayores; en el grupo de RD se amputaron 2 extremidades (11,1 %) y en el grupo RI 4 (25 %). Como se puede observar en la figura 5, al comparar las curvas de supervivencia de Kaplan-Meier para el salvamento de extremidad, tampoco se obtuvieron diferencias significativas (p = 0,35). De los 8 casos que no curaron, en 6 se efectuó una amputación mayor y en 2 se realizó de nuevo terapia endovascular. Dicho procedimiento consistió en nuevas angioplastias simples en el sector poplíteo y distal, en lesiones distintas a las previamente tratadas.
No hubo exitus peroperatorios y en el seguimiento se produjeron dos, uno en el grupo RD (5,5 %) y otro en el RI (6,25 %), ambos del grupo de extremidades que curaron. Las causas no estuvieron relacionadas con la isquemia crítica. El exitus del grupo RD fue tras 6 meses del procedimiento endovascular y se debió a sepsis por infección intraabdominal; el exitus del grupo RI fue a los 22 meses del procedimiento y se debió a insuficiencia cardíaca congestiva.
DiscusiónLa revascularización eficaz sigue siendo el principal componente en el tratamiento de las úlceras isquémicas de la extremidad inferior. De forma intuitiva, proporcionar flujo arterial directo a la zona específica de la úlcera isquémica debería ser preferible a optar por la revascularización inespecífica gracias a la neovascularización espontánea. El concepto de territorios vasculares diferenciados o angiosomas del pie y el tobillo aporta una base anatómica para poder analizar este concepto intuitivo. Esta estrategia selectiva para la revascularización de extremidades isquémicas se basa en el conocimiento de la anatomía de estos bloques de tejido tridimensionales irrigados por arterias específicas que, durante años, ha permitido al cirujano predecir qué colgajo pediculado resultará exitoso o si una determinada amputación sanará7.
Sin embargo, aplicado a la isquemia crítica de extremidades, la revascularización directa del angiosoma afecto no siempre es factible o práctica. De hecho, cuando se plantea la terapia endovascular en estos casos, la realidad es que se suelen tratar todas las lesiones focales posibles en los troncos distales para mejorar el runoff y aumentar el flujo distal al pie. Además, en muchos de estos pacientes, en una avanzada etapa de su enfermedad aterosclerosa, el vaso infragenicular menos enfermo, y muchas veces el único, es la arteria peronea1, como ocurre en nuestra serie.
Nuestro estudio retrospectivo sobre la base del concepto del angiosoma no sugiere que sea más probable que la revascularización directa del angiosoma isquémico sea satisfactoria a la hora de cicatrizar la herida y salvar la extremidad que la revascularización indirecta. Por lo tanto, la consiguiente tasa de amputación no fue menor. Esto no apoya la hipótesis inicial de que es preferible proporcionar flujo arterial directo a la zona anatómica que contiene la herida. En función de estos resultados, parece ser que se puede confiar en el flujo indirecto a través de las conexiones arteria-arteria de los vasos del pie.
Debido a que el pie y el tobillo suponen una estructura terminal en el cuerpo humano, sus arterias principales tienen numerosas conexiones arteria-arteria que permiten rutas alternativas del flujo sanguíneo cuando una de ellas se interrumpe6,7. Estas áreas están limitadas y a la vez unidas a otros angiosomas adyacentes por anastomosis verdaderas (vasos del mismo calibre que las arterias principales, como el arco plantar) y por "choke vessels" (de escaso calibre y que conectan angiosomas a través de un mismo músculo, pero no entre músculos distintos), que forman una red continua en cada tejido4-7. Estos "choke vessels" son conductos importantes de seguridad que permiten proporcionar flujo sanguíneo a un angiosoma contiguo si la arteria principal de este último es dañada7.
Es difícil determinar la calidad funcional de las conexiones arteria-arteria del pie y el tobillo. El estudio angiográfico no siempre muestra estas conexiones, especialmente en situaciones de compromiso del flujo arterial3. El hallazgo de permeabilidad distal se puede demostrar en arteriografías intraoperatorias, aunque ya se puede predecir con una buena exploración con doppler. Los hallazgos angiográficos por sí solos no deberían ser, por tanto, los decisivos en salvamentos de la extremidad o para determinar la posibilidad de revascularización. Datos clave para planificar una revascularización distal, como la permeabilidad de los arcos arteriales del pie, la presencia y calidad de las ramas colaterales y la decisión sobre qué vaso es el más adecuado, también se pueden tomar basándose en estudios con angiorresonancia magnética4.
En nuestro estudio, la RI conduce a la cicatrización de la herida. Por lo tanto, si estas conexiones arteriales existen y son las adecuadas, la RI puede dar buenos resultados. Esto refleja la experiencia clínica de los elevados porcentajes de salvamento de la extremidad gracias a una revascularización satisfactoria, independientemente de la consideración sobre la anatomía del angiosoma 1,2,9. Así, hay estudios que han demostrado que el tratamiento endovascular de la arteria peronea como único tronco distal ofrece resultados similares a la cirugía abierta de bypass, en cuanto a salvamento de la extremidad y tiempo de curación de lesiones tróficas1.
Por otro lado, un aspecto igualmente importante en el tratamiento de las heridas isquémicas es la calidad de los cuidados tópicos. Muchas extremidades con revascularización exitosa deben amputarse debido a infección incontrolable 9. La herida debe tratarse cuidadosamente y la reconstrucción de los tejidos blandos debe posponerse hasta que se hayan resuelto todos los signos de inflamación e infección y existan ya los signos iniciales de cicatrización, o bien debe propiciarse su cierre por segunda intención.
Las carencias de nuestro estudio incluyen su condición de retrospectivo, con un escaso número de pacientes tratados en un solo centro. No se analizaron los resultados en función de la presencia de variables como la diabetes mellitus o la insuficiencia renal crónica, asociados en otros estudios a una mayor tasa de amputación1,2,9. Tampoco se tuvieron en cuenta los microorganismos implicados en los casos de sobreinfección de las lesiones tróficas.
ConclusiónLa revascularización desempeña un papel fundamental en el tratamiento de las heridas isquémicas de la extremidad inferior. Nuestra experiencia sugiere que la tasa de cicatrización y de salvamento de la extremidad es independiente de si se ha realizado revascularización directa o indirecta del angiosoma isquémico.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.