La isquemia tisular es el resultado final de un proceso en el que interviene un gran número de moléculas que median la interacción endotelio-músculo liso vascular, entre las que se encuentra la endotelina-1 (ET-1), que es una molécula sintetizada por el endotelio vascular y que induce vasoconstricción, es proinflamatoria y tiene acción mitógena.
ObjetivoEvaluar el resultado del bosentan, un antagonista dual de receptores de endotelina, en el tratamiento de las úlceras digitales de etiología isquémica.
Pacientes y métodoHan sido tratados con bosentan 18 pacientes con úlceras digitales secundarias a esclerodermia o por otra causa (indicación fuera de guía), con afectación importante de vasos distales e irrevascularizables.
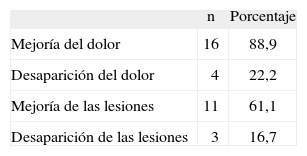
ResultadosLa etiología ha sido arteriosclerosis en 11 pacientes, enfermedad de Buerguer en 5, ateroembolismo en 1 y esclerodermia en 1 paciente. El tiempo mediano de tratamiento ha sido 90 días. Tres (16,7 %) pacientes precisaron de amputación menor, y un caso, de amputación infracondílea (5,5 %). No se produjo elevación de transaminasas en ninguno de los casos. En 16 pacientes (88,9 %) mejoró el dolor y en 11 (61,1 %) se redujo el tamaño de las lesiones.
ConclusionesEn este estudio se presenta por primera vez que el tratamiento con bosentan puede ser útil en pacientes irrevascularizables, mejorando el dolor y el tamaño de las lesiones, con una baja incidencia de amputaciones mayores a corto plazo.
Tissue ischaemia is the end result of a process involving a large number of molecules that mediate the endothelium-vascular smooth muscle interaction, among which is found endothelin-1 (ET-1), a molecule synthesized by the vascular endothelium and induces vasoconstriction, is proinflammatory, and has mitogenic action.
ObjectiveTo evaluate the use of bosentan, a dual endothelin receptor antagonist in the treatment of ischaemic digital ulcers.
Patients and methodA total of 18 patients were treated with bosentan for digital ulcers secondary to scleroderma or other cause (outside indication guidelines), with severe involvement of distal vessels and non-revascularisable.
ResultsThe aetiology was atherosclerosis in 11 patients, Buerguer disease in 5, embolism in 1, and scleroderma in 1 patient. The median length of treatment was 90 days. Three (16.7 %) patients required minor amputation and 1 case (5.5 %) below-knee amputation. There was no increase in transaminases in any case. There was an improvement of pain in 16 patients (88.9 %) and 11 (61.1 %) had decreased the size of the lesions.
ConclusionsThis is the first study to show that treatment with bosentan may be useful in non-revascularisable patients, improving pain and lesion size, with a low incidence of major amputations in the short term.
Las endotelinas (ET-1, ET-2 y ET-3) son potentes agentes presores endógenos, secretadas por diferentes tejidos y células del organismo. De las tres isoformas, la ET-1 es la más importante desde el punto de vista clínico. Se sintetiza predominantemente por el endotelio vascular e induce vasoconstricción, es proinflamatoria y tiene acción potencialmente mitógena. Es decir, desempeña un papel importante en la regulación del tono vascular y en la remodelación vascular. Existen dos diferentes receptores que median acciones antagónicas. Por una parte los receptores ETA son los responsables de inducir vasoconstricción y proliferación celular. Se encuentran fundamentalmente en el músculo liso vascular. Por otra parte los receptores ETB intervienen en la relajación vascular a través de la activación de la síntesis de óxido nítrico (ON) y prostaciclina (PGI) y están implicados en la depuración de la ET-1. Los receptores ETB se encuentran en las células endoteliales. El bosentan es un antagonista competitivo de receptores de ET-1. Presenta un mayor efecto inhibitorio sobre ETA, por lo que disminuye la resistencia vascular tanto pulmonar como sistémica y aumenta el gasto cardiaco sin aumento de la frecuencia. El bosentan está aprobado para la hipertensión pulmonar y en la esclerosis sistémica con alteración digital ulcerosa activa. El posible beneficio del bosentan en úlceras isquémicas de cualquier causa no es del todo conocido, habiéndose comunicado únicamente series pequeñas o casos aislados. El objetivo del presente estudio es evaluar el resultado clínico (mejoría subjetiva del dolor y objetiva del tamaño de las úlceras) del bosentan en pacientes con úlceras digitales de etiología isquémica, no revascularizables.
Material y métodoSe ha realizado de forma prospectiva el seguimiento de una serie consecutiva de pacientes con úlceras digitales en manos o pies, sin opción de tratamiento revascularizador. En todos los pacientes se solicitó autorización para la inclusión en el estudio, mediante la firma de un consentimiento informado y la aprobación por parte de farmacia hospitalaria de la administración del medicamento como uso compasivo.
Desde junio de 2008 hasta diciembre de 2009 se han tratado 18 pacientes con úlceras digitales secundarias a esclerodermia o por otra causa (indicación fuera de guía). El criterio de inclusión ha sido la afectación importante de vasos distales en pacientes irrevascularizables, en los que el tratamiento antibiótico específico y las curas locales no consiguieron una mejoría de las lesiones. La determinación de que el paciente no presentaba opciones de revascularización se ha realizado tomando como base los resultados arteriográficos.
Han sido excluidos los siguientes grupos de pacientes: a) pacientes con hepatopatía conocida moderada o grave, y b) pacientes tratados que reciben en el momento de la visita prostaglandinas por vía intravenosa. La pauta de administración se ha efectuado siguiendo la indicada en la guía clínica del fármaco. El tratamiento ha sido ambulatorio, comenzando con una dosis inicial de 62,5 mg cada 12 horas durante 4 semanas y posteriormente 125 mg cada 12 horas, hasta completar la curación de las lesiones o hasta completar 4 meses de tratamiento. La duración máxima de tratamiento ha sido empírica al no existir literatura al respecto. A todos los pacientes se les ha realizado una determinación de enzimas hepáticas antes de iniciar el tratamiento, a las 4 semanas y a las 8 semanas. Se ha empleado como tratamiento concomitante analgésicos (metamizol magnésico, paracetamol) y antibióticos (según antibiograma), en función de la evolución clínica del paciente. Todos ellos estaban siendo tratados con antiagregantes, que fueron mantenidos tras la inclusión en el estudio. Las curas de las lesiones han sido efectuadas de forma periódica en nuestro servicio. La valoración de la respuesta clínica ha consistido en la realización de un seguimiento iconográfico mediante fotografías seriadas de las lesiones y en la mejoría del dolor expresada por el paciente (mejor, igual, peor), así como por la menor necesidad de analgésicos.
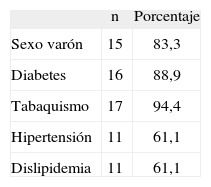
ResultadosHan sido incluidos 18 pacientes con lesiones tróficas en miembros superiores o miembros inferiores. La edad mediana de la serie ha sido 67 años, rango intercuartílico 27 años. La prevalencia de factores de riesgo cardiovascular habituales ha sido elevada, especialmente la diabetes y el tabaquismo (tabla 1). La enfermedad de base en 11 pacientes (61,1 %) ha sido arteriosclerosis, en 5 casos (27,7 %) enfermedad de Buerguer, en 1 (5,5 %) por esclerodermia y en otro (5,5 %) las lesiones aparecieron tras ateroembolismo. En la exploración vascular se observó que 7 pacientes (38,9 %) presentaban obstrucción infrapoplítea, 6 pacientes (33,5 %) obstrucción femoropoplítea y 5 pacientes (27,6 %) tenían los pulsos distales conservados.
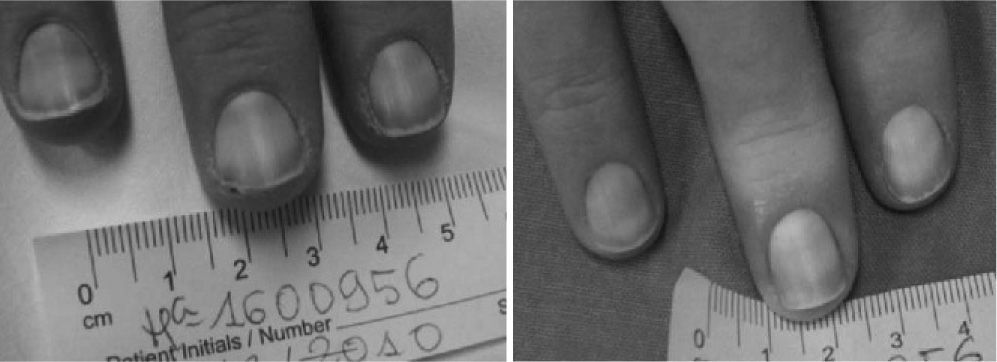
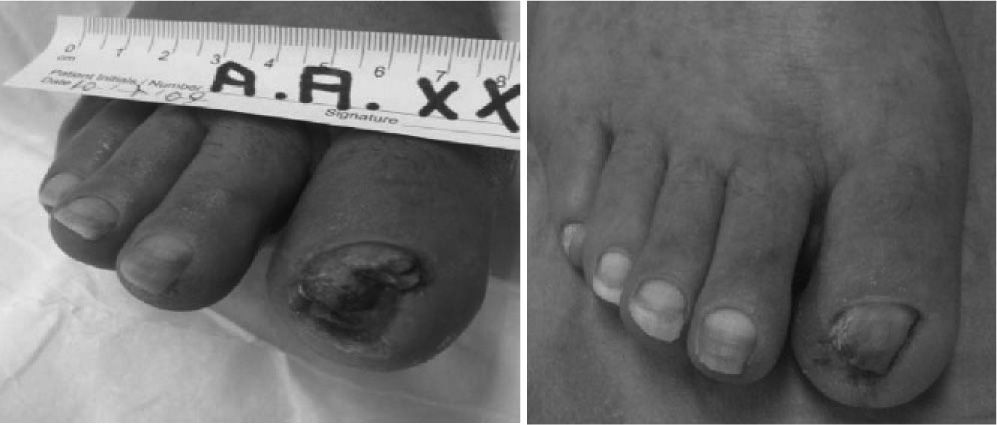
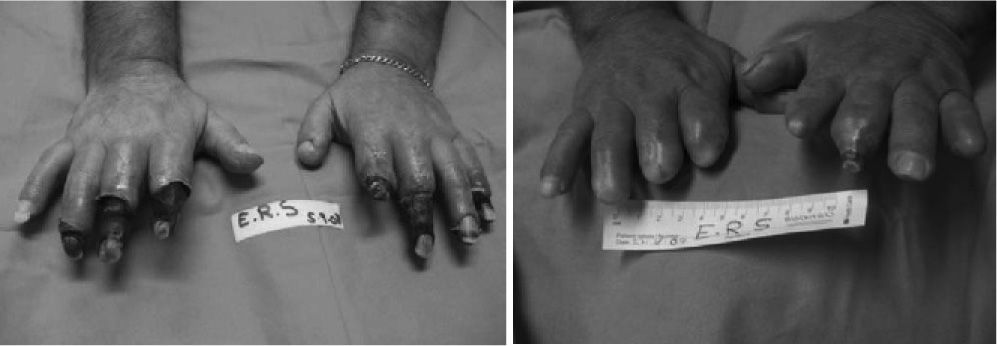
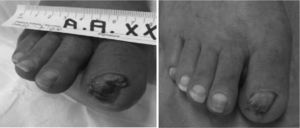
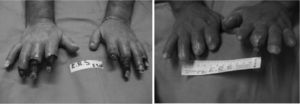
Las lesiones estaban ubicadas en 15 pacientes en dedos de manos o pies (83,3 %). Tres pacientes (16,6 %) presentaron las lesiones en zonas de decúbito (talón o maléolo externo), llegando a tejido muscular-tendinoso (figs. 1-3).
El tratamiento antibiótico se ha realizado mediante antibiograma. Hasta la obtención de dicho antibiograma se ha iniciado tratamiento antibiótico de forma empírica con amoxicilina-clavulánico y clindamicina por vía oral, o ciprofloxacino y clindamicina según criterio del facultativo.
Los fármacos analgésicos pautados en primer escalón han sido metamizol magnésico y paracetamol. Cuando éstos no han sido suficientes se ha pautado tramadol por vía oral o parches de fentanilo, según tolerancia clínica y criterio del facultativo.
El tiempo mediano de tratamiento ha sido 90 días. La desaparición del dolor o la curación completa de las úlceras fue infrecuente. Sin embargo, la mayoría de los pacientes presentaron una respuesta favorable al dolor y al tamaño de las lesiones (tabla 2). En 3 (16,7 %) pacientes se realizó una amputación menor, y en un caso (5,5 %), una amputación infracondílea (5,5 %) por mal control de la infección. No se observó elevación de enzimas hepáticas en ninguno de los sujetos incluidos en el estudio. Tampoco se observaron otros efectos adversos derivados de la administración del fármaco.
DiscusiónLa enfermedad grave de vasos distales condiciona en muchas ocasiones que el paciente presente isquemia avanzada sin opción de revascularización, siendo en muchas ocasiones la amputación mayor la única solución para el control del dolor.
La posibilidad de que un tratamiento farmacológico mejore el pronóstico de estos pacientes resulta ilusionante. Probablemente los fármacos que se han empleado con mayor frecuencia y de los que se dispone de una mayor experiencia han sido las prostaglandinas (PGE1)1. Los efectos antiisquémicos de la PGE1 en pacientes con enfermedad arterial oclusiva periférica son probablemente complejos y no se limitan a una acción vasodilatadora directa. Además de los conocidos efectos sobre el flujo sanguíneo, la viscosidad, la fibrinólisis y la agregación plaquetaria, el fármaco también inhibe la función de los monocitos y neutrófilos, lo que sugiere que PGE1 también tienen efectos antiinflamatorios. Además se ha comprobado que inhiben la expresión de moléculas de adhesión (E-selectina, ICAM-1 y VCAM-1) y median la liberación de citoquinas inflamatorias (factor de necrosis tumoral [FNT] alfa, MCP-1). Muchos de estos efectos comprobados in vitro también se han observado en ensayos clínicos2. Sin embargo, la coexistencia de insuficiencia renal avanzada en estos pacientes limita en muchas ocasiones el empleo de este fármaco. Otro problema añadido para su uso es la necesidad de administración intravenosa intrahospitalaria, lo que además de ser incómodo para pacientes con movilidad reducida incrementa los costes del tratamiento. En las guías TASC II3 se recogen los resultados de 9 ensayos aleatorizados con prostanoides (3 con PGE1, 6 con análogo de PGI2), no mostrando efectos favorables del tratamiento en todos los estudios.
Bosentan es un fármaco activo por vía oral, antagonista de los receptores ETA/ETB de la ET-1. Fue el primer fármaco inhibidor de la endotelina aprobado para la hipertensión arterial pulmonar. En dos estudios aleatorizados, controlados, bosentan demostró que mejoraba la capacidad de ejercicio y la supervivencia en estos pacientes con hipertensión pulmonar avanzada4,5. En los últimos años ha sido creciente el interés en el empleo de bosentan en pacientes con úlceras fundamentalmente secundarias a esclerodermia. Korn et al6 demostraron una menor incidencia de recidiva ulcerosa en pacientes que recibieron bosentan. Publicaciones más recientes han demostrado la utilidad de bosentan en la cicatrización de lesiones en esclerodermia7,8.
No hemos encontrado en la literatura referencias al tratamiento con bosentan en lesiones isquémicas secundarias a patologías diferentes de la esclerodermia. La terapia con bosentan se ha iniciado en pacientes irrevascularizables con la hipótesis del posible efecto beneficioso similar al publicado en algunas series en pacientes con úlceras y esclerodermia. Los resultados obtenidos a corto plazo han permitido un control del dolor y del tamaño de las lesiones en la mayoría de los pacientes, de forma que la amputación mayor ha debido realizarse en un único caso. Por otra parte, el fármaco ha sido bien tolerado, no habiéndose producido abandonos ni habiéndose observado elevación de transaminasas u otros efectos secundarios. Sin embargo, la curación completa de las lesiones sólo se ha producido en el 16,7 %, probablemente por lo extensas que son las lesiones en algunos pacientes y el corto seguimiento que se ha realizado.
Pensamos que en la actualidad el factor más limitante para el empleo generalizado de este fármaco es el coste. Otros fármacos empleados para la isquemia crítica no revascularizable, como las prostaglandinas por vía intravenosa, son menos costosos, si bien el tratamiento intravenoso de estas últimas encarece el precio final del tratamiento (administración hospitalaria, traslados en ambulancia, etc.).
Hay que reconocer las limitaciones del estudio, que son fundamentalmente la heterogeneidad de la muestra al tratarse de pacientes con úlceras de diferente etiología y con tratamientos concomitantes diferentes en muchos casos, y que al tratarse de una serie de casos clínicos no existe grupo control para comparar la eficacia con respecto a los pacientes no tratados con bosentan.
No obstante, se pretende presentar la experiencia inicial de un nuevo tratamiento en pacientes de muy mal pronóstico que habrían precisado de una amputación mayor o que habrían padecido dolor de difícil control. Aunque la curación completa no ha sido frecuente, sí lo ha sido la reducción en el tamaño de las lesiones, lo cual podría indicar un mayor número de cicatrizaciones completas con un mayor seguimiento.
Son necesarios estudios con grupo control y con enfermedades más homogéneas para determinar el efecto beneficioso de bosentan en pacientes con úlceras isquémicas.
ConclusionesEn este estudio se presenta por primera vez que el tratamiento con bosentan puede ser útil en pacientes irrevascularizables, mejorando el dolor y el tamaño de las lesiones, con una baja incidencia de amputaciones mayores a corto plazo y una buena tolerancia al fármaco.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Trabajo presentado en el 56 Congreso Nacional de la Sociedad Española de Angiología y Cirugía Vascular. Madrid, 3-5 de Junio de 2010.