Resumen. Introducción. El tratamiento endovascular en el sector iliaco, que comenzó a aplicarse en pacientes de alto riesgo, hoy día puede ser la primera opción terapéutica. Objetivo. Determinar los resultados de la angioplastia transluminal percutánea en el sector iliaco, con o sin implantación de stent, estratificando el análisis según tipos de lesión TASC-2000 y estimar la influencia de factores pronósticos en la permeabilidad, la salvación de la extremidad y la supervivencia. Pacientes y métodos. Análisis retrospectivo de 101 procedimientos en 91 pacientes, 85/6 hombres/mujeres) con una edad media de 61,54 ± 11,59 años. Factores de riesgo: diabetes, 41,6%; hipertensión, 41,6%; tabaquismo, 56,4%; cardiopatía isquémica, 19,8%; insuficiencia renal, 9,9%. La indicación fue en 35,7% isquemia crítica y claudicación limitante en 61,4%. Lesión tipo TASC A: 44,6%, B: 42,6%, C: 10,9%, D: 1,98%. Técnica: angioplastia, 35,65% y stent, 64,35%. Todas las variables, métodos de evaluación clínica y hemodinámica se definieron según los criterios de la SVS/ISCVS. Resultados. A los 66 meses, las tasas de permeabilidad primaria fueron del 69,84%, secundaria del 80,64%, salvación de la extremidad del 81,5% y supervivencia del 93,6%. Resultados precoces: 4 fracasos técnicos, éxito morfológico del 92,1% y clínico del 85,1%. No se registraron fallecimientos ni amputaciones. A los 66 meses, estratificando según TASC, las permeabilidades primarias morfológicasy clínicas, respectivamente, fueron: A: 75,09%, 63,65%; B: 68,07%, 69,66%y secundarias: A: 89,98%, 73,30%; B: 81,03%, 83,14%. El factor pronóstico significativo de disminución de permeabilidad primaria fue la localización en iliaca externa, y para tasas de salvación de extremidad y supervivencia la insuficiencia renal. Actualmente, el tratamiento endoluminal iliaco, gracias a los avances tecnológicos, los excelentes resultados y la baja morbimortalidad, puede ser la primera alternativa terapéutica para estos pacientes. Conclusiones. El tratamiento endovascular en el sector iliaco es aplicable a este tipo de pacientes, con uso selectivo de stent, obteniendo resultados similares a otras series. [ANGIOLOGÍA 2008; 60:189-98]
Summary. Introduction. Endovascular treatment of the iliac sector, which was first applied to high-risk patients, can now be the preferred therapeutic option today. Aim. To determine the outcomes of percutaneous transluminal angioplasty in the iliac sector, with or without stentplacement, the analysis being stratified according to the TASC-2000 types of lesion. We also sought to estimate the influence of prognostic factors on patency, limb salvage and survival. Patients and methods. We conducted a retrospective analysis of 101 interventions in 91 patients (85/6 males/females), whose mean age was 61.54 ± 11.59 years. Risk factors: diabetes, 41.6%; hypertension, 41.6%; smoking, 56.4%; ischaemic heart disease, 19.8%; renal failure, 9.9%. The indication was critical ischaemia in 35.7% and limiting claudication in 61.4%. TASC A-type lesion: 44.6%, B: 42.6%, C: 10.9%, D: 1.98%. Technique: angioplasty, 35.65% and stent, 64.35%. All the variables, methods of clinical and haemodynamic evaluation, were defned according to SVS/ISCVS criteria. Results. At 66 months, the primary patency rates were 69.84%, secondary rates were 80.64%, limb salvage was 81.5% and survival was 93.6%. Early results: there were 4 technical failures, morphological success was 92.1% and clinical success was 85.1%. No deaths or amputations were recorded. At 66 months, and stratifying according to the TASC, the primary morphological and clinical patencies were, respectively: A: 75.09%, 63.65%; B: 68.07%, 69.66% and the secondary ones were: A: 89.98%, 73.30%; B: 81.03%, 83.14%. The significant prognostic factor for decreased primary patency was location in the external iliac, and for limb salvage and survival rates it was renal failure. At the present time, thanks to the technological advances being made, the excellent outcomes and the low morbidity and mortality rates, endoluminal iliac treatment can be the preferred therapeutic alternative for these patients. Conclusions. Endovascular treatment in the iliac sector is applicable in this type of patients, with selective use of stents; the results obtained are similar to those in other series. [ANGIOLOGÍA 2008; 60: 189-98]
Desde el inicio de la técnica de angioplastia transluminal percutánea (ATP) de Dotter [1], han transcurrido más de cuatro décadas, siendo Tegtmeyer [2], en 1979, quien realizó con éxito la primera recanalización de una arteria iliaca ocluida. En 1987, Johnston [3] recogió 667 procedimientos iliacos, identificando ya cuatro variables pronósticas de éxito a largo plazo.
Aunque comenzó a aplicarse en este sector, como un procedimiento útil en pacientes de alto riesgo y como alternativa a la cirugía abierta, en los últimos años, gracias a los avances tecnológicos, se ha producido un incremento de las indicaciones de terapia endovascular en dichos sectores [4]. La introducción de stents en el tratamiento de las lesiones iliacas ha conducido a un aumento de los porcentajes de éxito técnico primario y de más largas permeabilidades [5].
La publicación del consenso TASC (TransAtlantic Inter-Society Consensus) [6] sobre el tratamiento de la enfermedad vascular periférica en el año 2000 para estratificar morfológicamente las lesiones sustituyó a anteriores clasificaciones que no eran anatómicamente específicas, como las publicadas por Ahn et al [7] en 1993, que las dividía en tres grados de gravedad de enfermedad para procedimientos periféricos endovasculares, la clasificación propuesta por Brewster [8] en tres patrones anatómicos de enfermedad en 1991, y las normas publicadas del Comité de la Sociedad de Radiología Cardiovascular e intervencionista [9] en 1990.
En varios estudios de observación se han identificado diferentes factores independientes de disminución de permeabilidad de los procedimientos endovasculares iliacos: factores demográficos y de riesgo del paciente [5, 10–16]; de localización anatómica [7, 10, 14, 17, 18]; run-off[10, 11, 14, 15, 18, 19]; estadio clínico del paciente [5, 7, 13, 15, 16, 18]; implantación de stent[12, 20–23]; gravedad de la lesión [5, 10, 15, 18, 23, 24]; índice tobillo/brazo mayor de 0,5 [5]; longitud de la lesión [7, 10, 21, 24–26]; tamaño del vaso [12, 13, 27, 28] y tipo TASC [15].
El objetivo de este trabajo es determinar los resultados de la angioplastia, con empleo de stent selectivo, a corto y a largo plazo en el sector iliaco, estratificando el análisis según los tipos de lesión TASC-2000, evaluando la seguridad del procedimiento y estimando la influencia en la permeabilidad, la salvación de extremidad y la supervivencia, de factores pronósticos de riesgo y demográficos del paciente, características de la lesión y del procedimiento utilizado.
Pacientes y métodosSe realizó un análisis retrospectivo de 101 procedimientos consecutivos (abril 1999-abril 2006) en 91 pacientes, 85 de los cuales fueron hombres y sólo 6 mujeres, con una edad media de 61,54 ± 11,59 años.
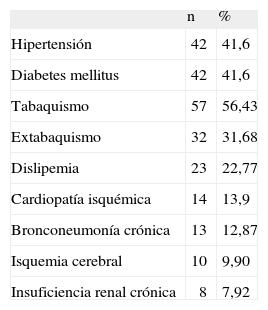
Los factores de riesgo más comúnmente asociados en la totalidad del grupo fueron hipertensión arterial en 42 pacientes (41,6%), diabetes mellitus en 42 (41,6%), tabaquismo en 57 (56,43%), extabaquismo en 32 (31,68%), dislipemia en 23 (22,77%), cardiopatía isquémica en 14 (13,9%), bronconeumonía crónica en 13 (12,87%), isquemia cerebral en 10 (9,90%) e insuficiencia renal crónica (IRC) en 8 casos (7,92%) (Tabla I).
La indicación del procedimiento fue en 35,7% isquemia crítica, siendo el resto por claudicación invalidante (61,4%), objetivando que la edad media de los claudicantes era 10 años menor que la del grupo de los grados III-IV (estos últimos con edad media de 67,7 años).
Respecto al tipo de lesión, fue estenosis en 77 casos (76,2%), oclusión en 18 (17,8%) y ambas en 6 (5,9%).
Diferenciando según la longitud de la lesión, en el 94,05% era menor o igual a 5cm, encontrándose el resto (5,94%) entre 5 y 10cm.
La localización del segmento afectado se encontró casi en la misma proporción en iliaca común, 43 casos (42,57%) y 44 en iliaca externa (43,56%), siendo en ambas en 14 casos (13,86%).
El empleo de stent fue selectivo, implantándose en el 64,35% (65 casos) de las intervenciones, siendo la ATP sola en el resto (36 casos, 35,64%).
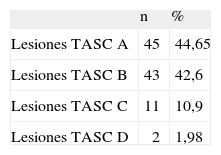
Según la definición del consenso TASC-2000, un 44,65 (45 casos) eran lesiones tipo A, el 42,6% (43 casos) tipo B, 10,9% (11 lesiones) eran tipo C y en sólo 2 (1,98%) eran lesiones TASC D (Tabla II).
Datos demográficos, factores de riesgo, complicaciones, criterios de éxito y variables de resultados fueron definidas, de acuerdo a criterios dispuestos y revisados por el Ad Hoc Comittee on Reporting Standards (Society for Vascular Surgery/Internacional Society for Cardiovascular Surgery, SVS/ ISCVS) [7].
Todas las intervenciones fueron llevadas a cabo en nuestro quirófano, por miembros del Servicio de Angiología y Cirugía Vascular. El arco radiológico empleado en la realización de los procedimientos fue el Siemens Arcadis Avantic ®.
La implantación de stent[21] en el procedimiento fue indicada en oclusiones, cuando persistía una estenosis residual mayor del 30% en dos proyecciones, gradiente de presión mayor de 10mmHg [30, 31], zona de disección en la lesión o contornos irregulares sugerentes de vía subintimal [32].
Basándonos en los criterios de la SVS/ISCVS, se establecieron los métodos de evaluación clínica y hemodinámica para permitir comparar grupos de pacientes.
Dentro de estos métodos, señalamos que se consideró buen run-off una adecuada permeabilidad (estenosis angiográfica menor del 50%) de las arterias femoral común, superficial y profunda para procedimientos de arterias iliacas, y determinamos el tamaño del vaso de acuerdo al tamaño máximo del balón usado para la dilatación y medidas del diámetro de la luz por encima y por debajo de la lesión, que se obtuvo en la arteriografía.
Para procedimientos endovasculares arteriales se consideró éxito técnico morfológico si la estenosis residual es menor del 30%; éxito clínico cuando tras la intervención en pacientes con grado IV se curaron las lesiones y en grados IIB y III si mejoró al menos una categoría clínica de Rutherford; y éxito hemodinámico se consideró un aumento mayor o igual a 0,15 del índice tobillo-brazo como criterio aislado o 0,10 si se asoció a una mejoría en una categoría en la escala clínica.
Los resultados precoces fueron los analizados en los 30 primeros días.
En todos los pacientes se realizó dúplex al alta, para control postoperatorio y como referencia al seguimiento posterior al mes, 3, 6 y 12 meses, y anualmente.
Un deterioro de uno o más niveles categóricos clínicos o hemodinámicos constituyeron fallo. Fallo anatómico se definió como reestenosis mayor o igual al 50% por dúplex y/o arteriografía.
Indicación para repetir la intervención fue estenosis mayor de 70% (ratio de velocidad picosistólica mayor de 3 en dúplex) y gradiente mayor de 15mmHg con papaverina o mayor de 10 en reposo.
Se definió permeabilidad primaria como el tiempo desde la intervención inicial a oclusión o al final del período de observación habiéndose ininterrumpido sin ningún otro procedimiento ni ayuda. Permeabilidad secundaria fue el total del tiempo desde la intervención inicial, después de una trombosis que se ha solventado por otro procedimiento, a la trombosis definitiva o al final del tiempo de observación [33].
Todos los análisis estadísticos se realizaron bajo el principio de intención de tratar, incluyendo los fallos técnicos iniciales. El análisis estadístico usó el SPSS (Statistical Product and Service Solutions) para Windows v. 11.5.
Para valorar las tasas de permeabilidad primaria, secundaria, tasa de salvación de extremidad y supervivencia se utilizaron estimadores de Kaplan-Meier y se usaron pruebas de log-rank para las comparaciones univariantes de las variables, con objeto de determinar si hubo diferencias en las funciones de supervivencia de los dos grupos. Posteriormente, se realizó análisis de regresión multivariante de Cox, empleando las variables encontradas significativas en el análisis univariante, para determinar pronósticos independientes.
Se tomó un nivel de significación de 0,05 para todas las pruebas.
ResultadosLos procedimiento se realizaron con anestesia locorregional en el 70,29% de los casos (71 casos) y general en 29,70% (30 casos), por procedimientos asociados en algunos casos.
La vía de acceso fue ipsilateral en 60 casos (59,4%), contralateral en 7 (6,9%) y bilateral en 34 (33,7%), con un tiempo medio de 89,47 minutos de todo el procedimiento.
En 4 casos (3,96%) no se pudo realizar el procedimiento, por imposibilidad de atravesar la lesión.
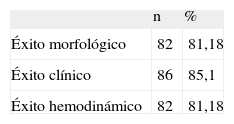
Obtuvimos un éxito morfológico precoz en 92,1% (93 procedimientos), clínico en 85,1% (86 intervenciones) y hemodinámico en 81,18% (82 casos), con una conversión a bypass aortobifemoral por persistencia de grado III y estenosis residual mayor del 30% (Tabla III).
No se produjo ninguna complicación general (cardíaca, renal ni respiratoria), ni locales (disección, rotura arterial, pseudoaneurisma, trombosis, embolismo distal ni hematomas o infecciones que requirieran cirugía). No hubo amputaciones ni fallecimiento.
En el seguimiento a 66 meses se produjeron 13 reestenosis (12,87%) a los 13,59 meses de tiempo medio; en 8 de estos casos se realizó nueva ATP con éxito, salvo en un caso, que precisó de una tercera ATP. Hubo 3 conversiones a bypass por progresión de enfermedad iliaca, femoral y recurrencia del dolor en reposo. Los 2 casos restantes no se repararon por pérdida en el seguimiento.
Sucedieron 4 trombosis (3,96%), en un tiempo medio de 5,8 meses, de las cuales 3 necesitaron conversión a cirugía abierta (en un caso a bypass aortobifemoral y en 2 a bypass femorofemoral).
A pesar del procedimiento endovascular permeable, en 2 casos (1,98%) se realizó, a un tiempo medio de 9,23 meses, un bypass aortobifemoral por progresión de enfermedad y empeoramiento clínico, siendo uno de ellos intento fallido de ATP de las nuevas lesiones.
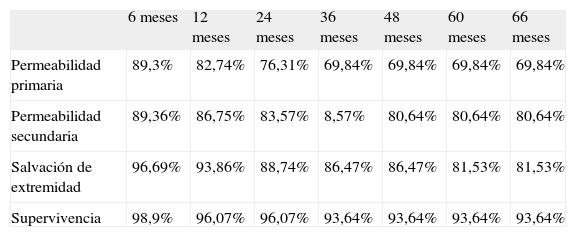
A estos 5 años y medio de seguimiento, englobando todos los tipos de lesiones iliacas, la permeabilidad primaria fue del 69,84%, la secundaria de un 80,64%, salvación de extremidad del 81,53% y supervivencia del 93,64%, con error estándar (ES), en todos ellos, menor del 10% (Tabla IV).
Tasas de permeabilidad primaria y secundaria, salvación de extremidad y supervivencia a los 66 meses, con ES < 10%, del sector iliaco general.
| 6 meses | 12 meses | 24 meses | 36 meses | 48 meses | 60 meses | 66 meses | |
| Permeabilidad primaria | 89,3% | 82,74% | 76,31% | 69,84% | 69,84% | 69,84% | 69,84% |
| Permeabilidad secundaria | 89,36% | 86,75% | 83,57% | 8,57% | 80,64% | 80,64% | 80,64% |
| Salvación de extremidad | 96,69% | 93,86% | 88,74% | 86,47% | 86,47% | 81,53% | 81,53% |
| Supervivencia | 98,9% | 96,07% | 96,07% | 93,64% | 93,64% | 93,64% | 93,64% |
ES: error estándar.
Si estratificamos según clasificación TASC-2000 la permeabilidad primaria morfológica para el tipo A, fue del 75,09 y 68,07%, para el B (ES < 10%). Para el C fue del 60%, aunque no fue significativo (ES de 14,49%) y el D 100% a 12 meses (ES < 10%). Dado el reducido número de casos de los tipos TASC C y D, no se tuvieron en cuenta los resultados obtenidos en estos grupos, a pesar de que algunos eran estadísticamente significativos y todos favorables.
La permeabilidad morfológica secundaria aumentó a un 89,98% en el tipo A y al 81,03% en el B.
La permeabilidad clínica primaria fue del 63,65% para el TASC A y 69,66% para el B y la secundaria elevó la permeabilidad a 73,30 y 83,14% en A y B, respectivamente (todas ellas con ES < 10%).
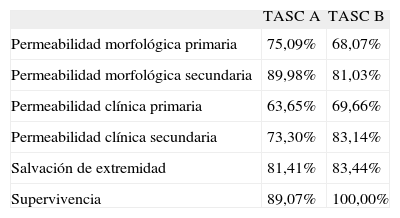
En nuestra serie, la salvación de extremidad obtuvo cifras del 81,41% para el grupo A y 83,44% para el B y la supervivencia en la categoría A del 89,07 y del 100% en el B (Tabla V).
Tasas de permeabilidad, salvación de extremidad y supervivencia en tipos TASC A y B (ES < 10%).
| TASC A | TASC B | |
| Permeabilidad morfológica primaria | 75,09% | 68,07% |
| Permeabilidad morfológica secundaria | 89,98% | 81,03% |
| Permeabilidad clínica primaria | 63,65% | 69,66% |
| Permeabilidad clínica secundaria | 73,30% | 83,14% |
| Salvación de extremidad | 81,41% | 83,44% |
| Supervivencia | 89,07% | 100,00% |
ES: error estándar; TASC: TransAtlantic Inter-Society Consensus.
Se sometieron a un análisis univariante las variables epidemiológicas (sexo, grupos de edad), factores de riesgo (hipertensión arterial, diabetes mellitus, tabaquismo, IRC, cardiopatía isquémica), indicación clínica de intervención, índice tobillo/brazo preoperatorio > 0,5, características de la lesión (tipo, localización y longitud), estratificación TASC, tamaño del vaso, run-off y técnica operatoria (ATP o ATP con stent).
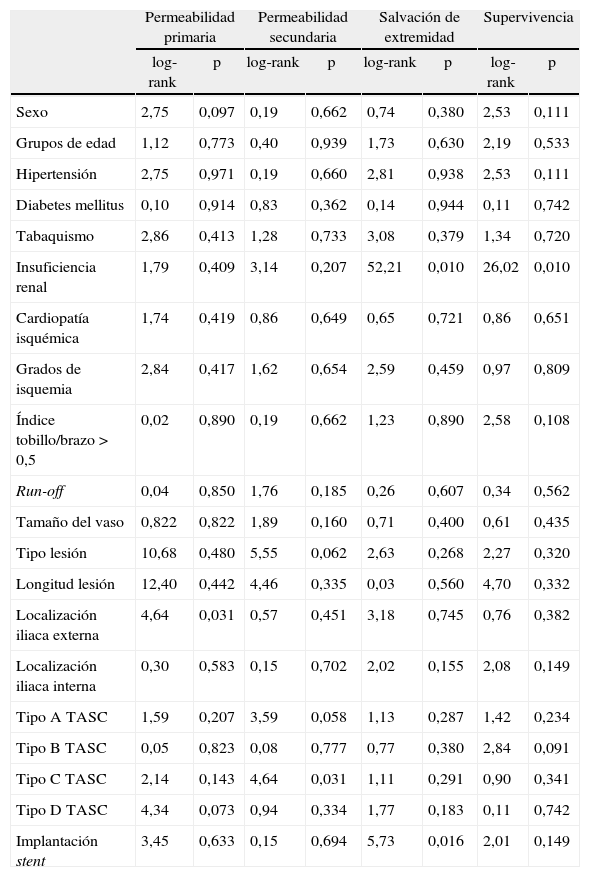
Encontramos significación estadística para disminución de permeabilidad primaria, cuando la lesión se situó en iliaca externa (p = 0,0313; log-rank: 4,64). También fue significativo para reducción de porcentajes de salvación de extremidad en 2 variables: IRC (p = 0,010; log-rank: 52,21) e implantación de stent en el procedimiento (p = 0,016; log-rank: 5,73) (Tabla VI).
Análisis univariante de las variables de riesgo y demográficas del paciente, específicas de la lesión y del procedimiento utilizado.
| Permeabilidad primaria | Permeabilidad secundaria | Salvación de extremidad | Supervivencia | |||||
| log-rank | p | log-rank | p | log-rank | p | log-rank | p | |
| Sexo | 2,75 | 0,097 | 0,19 | 0,662 | 0,74 | 0,380 | 2,53 | 0,111 |
| Grupos de edad | 1,12 | 0,773 | 0,40 | 0,939 | 1,73 | 0,630 | 2,19 | 0,533 |
| Hipertensión | 2,75 | 0,971 | 0,19 | 0,660 | 2,81 | 0,938 | 2,53 | 0,111 |
| Diabetes mellitus | 0,10 | 0,914 | 0,83 | 0,362 | 0,14 | 0,944 | 0,11 | 0,742 |
| Tabaquismo | 2,86 | 0,413 | 1,28 | 0,733 | 3,08 | 0,379 | 1,34 | 0,720 |
| Insuficiencia renal | 1,79 | 0,409 | 3,14 | 0,207 | 52,21 | 0,010 | 26,02 | 0,010 |
| Cardiopatía isquémica | 1,74 | 0,419 | 0,86 | 0,649 | 0,65 | 0,721 | 0,86 | 0,651 |
| Grados de isquemia | 2,84 | 0,417 | 1,62 | 0,654 | 2,59 | 0,459 | 0,97 | 0,809 |
| Índice tobillo/brazo > 0,5 | 0,02 | 0,890 | 0,19 | 0,662 | 1,23 | 0,890 | 2,58 | 0,108 |
| Run-off | 0,04 | 0,850 | 1,76 | 0,185 | 0,26 | 0,607 | 0,34 | 0,562 |
| Tamaño del vaso | 0,822 | 0,822 | 1,89 | 0,160 | 0,71 | 0,400 | 0,61 | 0,435 |
| Tipo lesión | 10,68 | 0,480 | 5,55 | 0,062 | 2,63 | 0,268 | 2,27 | 0,320 |
| Longitud lesión | 12,40 | 0,442 | 4,46 | 0,335 | 0,03 | 0,560 | 4,70 | 0,332 |
| Localización iliaca externa | 4,64 | 0,031 | 0,57 | 0,451 | 3,18 | 0,745 | 0,76 | 0,382 |
| Localización iliaca interna | 0,30 | 0,583 | 0,15 | 0,702 | 2,02 | 0,155 | 2,08 | 0,149 |
| Tipo A TASC | 1,59 | 0,207 | 3,59 | 0,058 | 1,13 | 0,287 | 1,42 | 0,234 |
| Tipo B TASC | 0,05 | 0,823 | 0,08 | 0,777 | 0,77 | 0,380 | 2,84 | 0,091 |
| Tipo C TASC | 2,14 | 0,143 | 4,64 | 0,031 | 1,11 | 0,291 | 0,90 | 0,341 |
| Tipo D TASC | 4,34 | 0,073 | 0,94 | 0,334 | 1,77 | 0,183 | 0,11 | 0,742 |
| Implantación stent | 3,45 | 0,633 | 0,15 | 0,694 | 5,73 | 0,016 | 2,01 | 0,149 |
TASC: TransAtlantic Inter-Society Consensus.
Se realizó regresión multivariante de Cox con las dos variables significativas estadísticamente y obtuvimos la IRC como único factor pronóstico independiente de disminución de la tasa de salvación de extremidad, con un riesgo relativo de 29 con p < 0,001 e intervalo de confianza de 5,73-147.
Para disminución de supervivencia la IRC también fue estadísticamente significativa (p = 0,010; log-rank: 26,02).
DiscusiónLa aparición de técnicas endovasculares en el tratamiento de la enfermedad oclusiva aortoiliaca ha obligado a cambios conceptuales, tanto en el campo de las indicaciones como en el de los tratamientos.
Sólo unos pocos estudios de observación han comparado directamente las técnicas abiertas convencionales con endoluminales [34]. En años recientes, la llegada de nuevas tecnologías con tipos mejorados de stent, evolución de técnicas de diagnóstico de imagen, han aumentado el uso de intervenciones endoluminales, con una reducción paralela de injertos aortobifemorales.
Se establecieron recomendaciones de indicación para procedimientos endovasculares en el sector iliaco, como las de la Society of Cardiovascular and Interventional Radiology (SCVIR) [35], en el año 1990 y la American Heart Association (AHA) [36], en 1997, hasta la llegada de la clasificación TASC 2000 que, aunque no era categórica, recomendaban el tratamiento endovascular en lesiones tipo A, dejando sin definir el tratamiento de las lesiones B y C. La reciente actualización del consenso TASC-2007 [37] expande las indicaciones de tratamiento endoluminal en este sector, por los buenos resultados a largo plazo y la baja proporción de complicaciones en las series publicadas [38].
Ya desde las primeras publicaciones se trataban permeabilidades a largo plazo del 80-90% con baja comorbilidad [2, 5, 18, 22, 38–40]. Sin embargo, al realizar un análisis de las evidencias acumuladas respecto a resultados y utilidad de estas técnicas, en el sector que nos ocupa, surgen limitaciones específicas al tratarse de series heterogéneas de pacientes y, en muchos casos, sin incluir los fracasos técnicos en la valoración de los resultados. Sólo ensayos clínicos aleatorizados comparando ambos tipos de tratamiento, convencional y endovascular, podrían indicar el mejor tratamiento para estas lesiones. No se han realizado ensayos controlados que demuestren superioridad de una de las técnicas salvo el de Wilson et al [34] y Wolf et al [39], que no encontraron diferencias significativas de permeabilidad entre ambas en enfermedad iliaca, femoral ni poplítea. En el sector iliaco, la permeabilidad a 4 años fue del 67% en endovascular frente a 77% en cirugía, sin diferencias estadísticamente significativas.
En nuestra serie obtuvimos unas buenas tasas de éxito técnico inicial, permeabilidad primaria y secundaria, a pesar de no excluir los fallos iniciales de los subsecuentes análisis, es decir, valorándolos en 'intención de tratar'. Nuestros resultados fueron similares a series publicadas, incluyendo también la morbimortalidad y la salvación de extremidad [5, 7, 13, 14, 20, 22, 24, 26, 27, 29, 39, 40]. Existen publicaciones con permeabilidades acumuladas a largo plazo más largas que las nuestras [15, 18, 38], aunque la disparidad entre las series puede explicarse por diferencias en la población y los métodos de análisis. Conviene señalar las limitaciones de nuestro estudio. En primer lugar, se trató de un análisis retrospectivo, llevado a cabo en un área de población joven, por lo que existía alta proporción de pacientes con claudicación invalidante, aunque la mayoría de las series publicadas tienen porcentaje de claudicantes mayor [10, 12, 14, 18–21, 23, 24, 26–30, 34, 38]. Debido a estas características de los pacientes y del tipo de lesiones, en su mayoría TASC A y B, difícilmente se pueden comparar los resultados endovasculares con los de las series quirúrgicas de este sector, dejando sin estudiar las lesiones extensas. Esta es otra limitación de nuestro trabajo, al no poder valorar los resultados del tratamiento endoluminal frente al quirúrgico. Y en tercer lugar, al ser un estudio retrospectivo, no se valoró la calidad de vida de los pacientes sometidos a tratamiento.
A pesar de estas limitaciones y con estos resultados, creemos que el tratamiento endovascular es indicación de elección frente a la cirugía, según morfología y localización de la lesión, siendo también en algunas lesiones oclusivas, como es el caso de oclusiones unilaterales en pacientes jóvenes. La localización en iliaca común ofrece los mejores resultados de esta técnica [5, 7, 10, 14, 17, 18] y en muchos casos se ofrece como primera opción frente a cirugía convencional.
Con la ATP, mantenemos la posibilidad de una redilatación de la zona angioplastiada si existen reestenosis y en la mayoría de los casos no impide la reconstrucción quirúrgica posterior, si fuera necesario [21, 32], dado que este tratamiento no lo consideramos como una alternativa en competencia con la cirugía, y pensamos que el tratamiento endovascular no excluye o complica futuras cirugías y debería intentarse primero en lesiones no difusas del sector iliaco.
Cuando la indicación de intervención son los grados III y IV, las lesiones oclusivas suelen afectar a varios niveles arteriales. Las técnicas endoluminales pueden diferir o simplificar los procedimientos de revascularización más distal mejorando el inflow[21, 32] en casos de bypass femoropoplíteo, femorodistales o acompañando a otros procedimientos endovasculares infrainguinales.
Creemos que los análisis estratificados de variables epidemiológicas como factores de riesgo, indicación de intervención, características de la lesión, estratificación TASC, tamaño del vaso, run-off y técnica operatoria resultan útiles para definir factores de riesgo específicos de disminución de permeabilidad en los distintos subgrupos de pacientes, e insistimos en la necesidad de realizar un seguimiento clínico, hemodinámico y morfológico de las lesiones para aumentar la permeabilidad secundaria, sabiendo que en nuestros enfermos, la evolución final suele venir dada por la enfermedad infrainguinal asociada.
En la revisión de nuestros casos, factores significativos pronósticos de disminución de permeabilidad primaria fueron la localización en iliaca externa y la insuficiencia renal para reducción de tasas de salvación de extremidad y supervivencia. Otros datos, como la extensión de lesión, etc. no fue posible valorarlos por el pequeño tamaño de la muestra. La oclusión frente a estenosis se ha comprobado que no es factor pronóstico de fracaso una vez alcanzado el éxito técnico en traspasar la lesión [4, 5, 21, 22, 32].
Creemos que, dado que el número de ensayos clínicos prospectivos clínicos realizados es escaso, existe una limitación en la validez, debido a los diferentes métodos de seguimiento y criterios de éxito utilizados, por lo que debemos interpretar con cautela los resultados publicados [4], aunque confiamos que en un futuro próximo, la amplia cantidad de información permitirá definir el papel del procedimiento, sacar conclusiones y establecer recomendaciones en nuestra práctica habitual del tratamiento de la enfermedad oclusiva del sector iliaco.
Por tanto, algo que se inició como alternativa al tratamiento quirúrgico abierto, reúne en la actualidad todas las características de ser un verdadero tratamiento de elección, que debemos tener siempre presente para el tratamiento de la enfermedad oclusiva iliaca.
En conclusión, el tratamiento endovascular en el sector iliaco es aplicable a nuestro tipo de pacientes con uso selectivo de stent, obteniendo resultados similares a otras series, por lo que mantenemos el tipo de indicaciones.