La reparación endovascular de los aneurismas de la aorta abdominal (EVAR) con éxito precisa la previa realización de una medición anatómica precisa basada en el estudio angio-TC aórtica. En situaciones de urgencia el tiempo para medición y planificación del caso es limitado y la disponibilidad del estudio en formato DICOM no siempre es posible.
ObjetivoPresentar un protocolo de planificación desarrollado en nuestro centro que permite reducir el tiempo necesario para realizar las medidas en terapia EVAR de aneurismas de aorta abdominal (AAA) rotos en situaciones de urgencia y describir los resultados de nuestro centro antes y después de la aplicación de este protocolo.
MétodoPresentamos un análisis descriptivo de morbimortalidad a 30 días y a un año basado en un registro prospectivo de todos los casos de rotura de AAA admitidos de modo consecutivo (n=32) en el servicio de urgencias de un hospital nacional de referencia durante el periodo enero del 2013 a mayo del 2015 (28 meses). El protocolo SANTIAGO es un acrónimo que describe (en lengua inglesa) 8 pasos que deben ser siempre tenidos en cuenta para una planificación EVAR: S (Size the aneurysms), A (Access), N (Neck), T (bifurcaTion), I (Iliacs), A (Angulations), G (LenGth-LonGitud) y O (OK for material). En nuestro centro, la terapia EVAR en rotura aórtica se realiza bajo anestesia local y de modo percutáneo si la situación clínica del paciente lo permite.
ResultadosTras la aplicación del protocolo SANTIAGO en nuestro centro, desde junio del 2014, se consiguió reducir la mortalidad en el tratamiento urgente de aneurismas aórticos infrarrenales rotos. Fueron desestimados para ningún tipo de intervención por su elevada morbimortalidad 3 pacientes de los 32 (9,3%) admitidos en urgencias. La mortalidad total a 30 días en pacientes tratados disminuyó del 46,6% (7/15) preprotocolo frente al 35,7%(5/14) posprotocolo y en pacientes intervenidos mediante técnica endovascular pasó del 25% (1/4) preprotocolo frente a un 0%(0/6) de mortalidad posprotocolo. El 66,6% (4/6) de los pacientes tratados mediante EVAR tras el implante del protocolo fueron intervenidos de modo percutáneo y bajo anestesia local. La mortalidad al año, registrada en mayo del 2016, fue en el grupo EVAR del 10% (1/10), tasa de reintervención al año del 7,1% (1/9) por endofuga tipo ib, resuelta con éxito. En el grupo de cirugía abierta la morbimortalidad a 12 meses fue del 63,15% (12/19) de los pacientes intervenidos, con registro de un fallecimiento por IAM 7 meses postintervención y sin datos de reintervenciones mayores al año.
ConclusionesBasados en la mejora de resultados observada en nuestro centro, consideramos que la existencia de un protocolo de planificación EVAR permite una planificación esquemática y reproducible que optimiza el tiempo necesario para afrontar una situación de urgencia crítica y propicia el éxito de la reparación. Asimismo, existe la tendencia progresiva en nuestro centro a considerar el tratamiento EVAR como primera opción terapéutica para pacientes con AAA-r. La posibilidad de realizar esta técnica con anestesia local y abordaje percutáneo podría ser considerada como un factor independiente que condiciona la menor morbimortalidad global del procedimiento.
Successful endovascular treatment of ruptured abdominal aortic aneurysms (R-EVAR) requires a detailed planning of the procedure, as planning is the key step. Nevertheless, in cases of emergency the limited time for planning and the non-availability of good quality scan images (DICOM format) are common issues that determine the final result.
ObjectiveThe aim of this paper is to present the results of r-AAA survival before and after a fast protocol was implemented in our centre for measuring and sizing r-EVAR in emergency situations.
MethodMorbidity and mortality at 30 days and 1 year was prospectively recorded in all consecutive cases of r-AAA admitted to the emergency department of our hospital (n=32) from January 2013 to May 2015 (28 months). The “SANTIAGO planning & sizing protocol” was implemented in June 2014. It is a fast method to remember key steps in planning EVAR. With the word SANTIAGO being a mnemonic device in which 8 basic and mandatory steps in planning can be summarised: S: Size, A: Access N: Neck, T: Bifurcation I: Iliacs, A: Angulations, G: Length, O: Ok for material. R-EVAR is performed in this centre under local anaesthesia and using a percutaneous approach, if the patient tolerates it, since June 2014.
ResultsAfter implementation of the SANTIAGO protocol in June 2014, the 30 day mortality was reduced from 46.6% (7/15) to 35.7% (5/14) in all patients treated in our centre for a ruptured AAA. The mortality recorded in the endovascular group was 25% (1/4) pre-protocol and 0% (0/6) after in the period analysed. A percutaneous approach and local anaesthesia was used in 66% (4/6) patients in the EVAR Group after the protocol was implemented. The 1 year mortality was 10% for all patients treated in the R-EVAR group, with a secondary intervention rate of 7.1% (1/9) due to a type Ib endoleak. In the open repair group, the 1 year morbidity/mortality was 63.15% (12/19), with a patient death at 7 months due to a myocardial infarction.
ConclusionsOur first results suggest that a fast protocol for planning and sizing in emergency situations seems to be associated with a lower 30 day mortality. A higher trend for considering the patient candidate for r-EVAR has been observed in our centre. Local anaesthesia and percutaneous approach have a probable influence on the lower morbidity and mortality of the endovascular cases.
En la terapia endovascular para el tratamiento de aneurismas de aorta abdominal (AAA) (EVAR) la medición anatómica precisa basada en un estudio angio-TC reciente y la planificación del dispositivo a implantar son imprescindibles para el éxito del procedimiento1,2. Existen diferentes equipos radiológicos y programas específicos, más o menos automatizados, que permiten el procesamiento del formato de imagen médicas digitales (DICOM) para realizar una planificación adecuada. Hoy en día es indispensable que los especialistas que realizan terapia endovascular aórtica tengan los conocimientos suficientes y necesarios para realizar las medidas y planificación EVAR de modo autónomo2. La rotura de un AAA (AAA-R) es una situación dramática y estresante a la que los especialistas vasculares nos enfrentamos con frecuencia y en la que una vida humana depende de nuestra capacidad de acción, rapidez y habilidades técnicas.
ObjetivoEl objetivo de este artículo es presentar y compartir con otros equipos quirúrgicos un protocolo de planificación desarrollado en nuestro centro y valorado por varios centros internacionales de referencia, que permite esquematizar el procedimiento de medición y planificación en terapia EVAR en AAA en situaciones de urgencia, optimizando los tiempos quirúrgicos y la ejecución del procedimiento, pudiendo influir de forma positiva en los resultados de morbimortalidad.
Protocolo SANTIAGO. Ocho puntos clave en planificación de la reparación endovascular de aortaMediante el empleo del acrónimo SANTIAGO como regla nemotécnica se describen (en lengua inglesa) 8pasos que consideramos deben ser tenidos siempre en cuenta para una planificación de EVAR con éxito en una urgencia (fig. 1).
- –
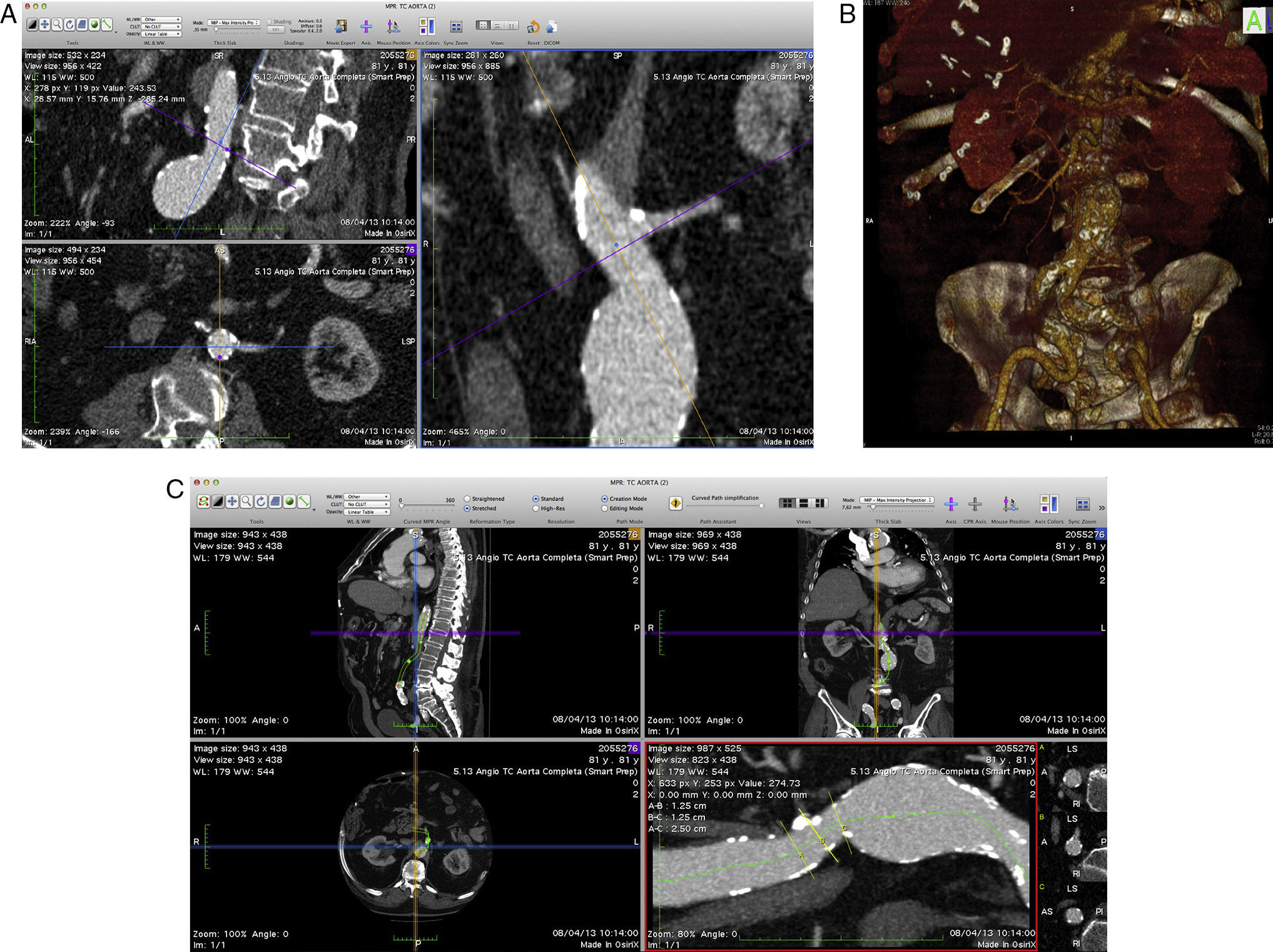
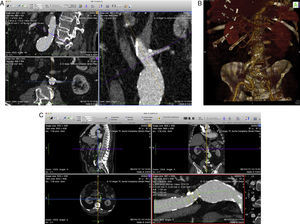
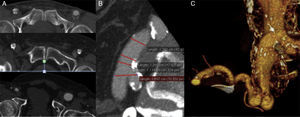
S o Size the aneurysms: debe medirse el máximo diámetro en cuello aórtico e ilíacas comunes/externas. Si disponemos de margen de tiempo y del software adecuado (estaciones de trabajo tipo Osirix, 3mensio, General Electric, Aquiarius-Intuition, etc.), recomendamos realizar una reconstrucción volumétrica tipo volume rendering (VR) para tener una visión global de la anatomía del caso y de las angulaciones (fig. 2). Puede realizarse la medición directa en cortes simples axiales/coronales/sagitales, en función de la angulación del segmento a medir si no se dispone de formato de imagen DICOM o de un visor adecuado.
- –
A o Access: los accesos ilio-femorales pueden valorarse en cortes simples axiales/coronales/sagitales o con más detalle con una reconstrucción multiplanar (MPR). Recomendamos anotar siempre las medidas de los diámetros internos (in-in) y externos (out-out), el grado de calcificación, la presencia de trombo y las diferentes angulaciones. Se deben también evaluar ambos trípodes femorales para considerar si es un caso candidato a tratamiento percutáneo (p-EVAR)/abordaje femoral abierto/endarterectomía femoral (fig. 3). En nuestra opinión, es imprescindible en terapia EVAR urgente la permeabilidad de al menos uno de los ejes ilio-femorales.
- –
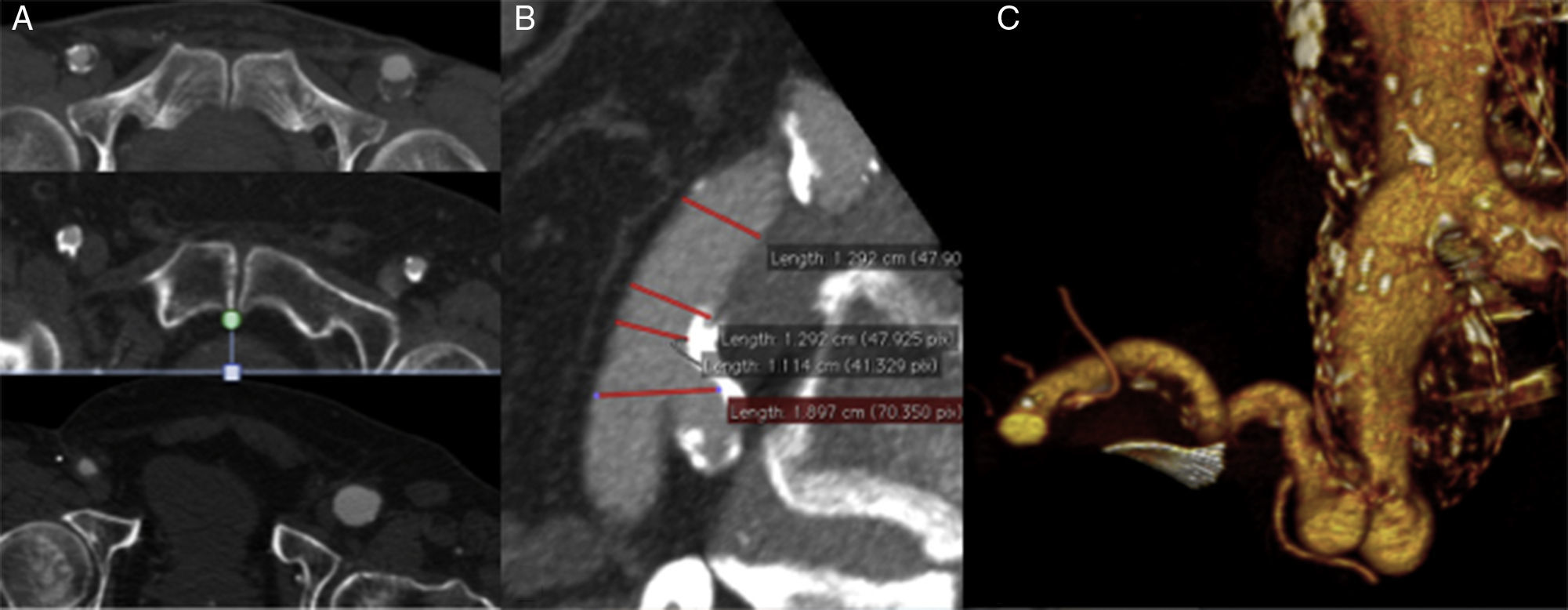
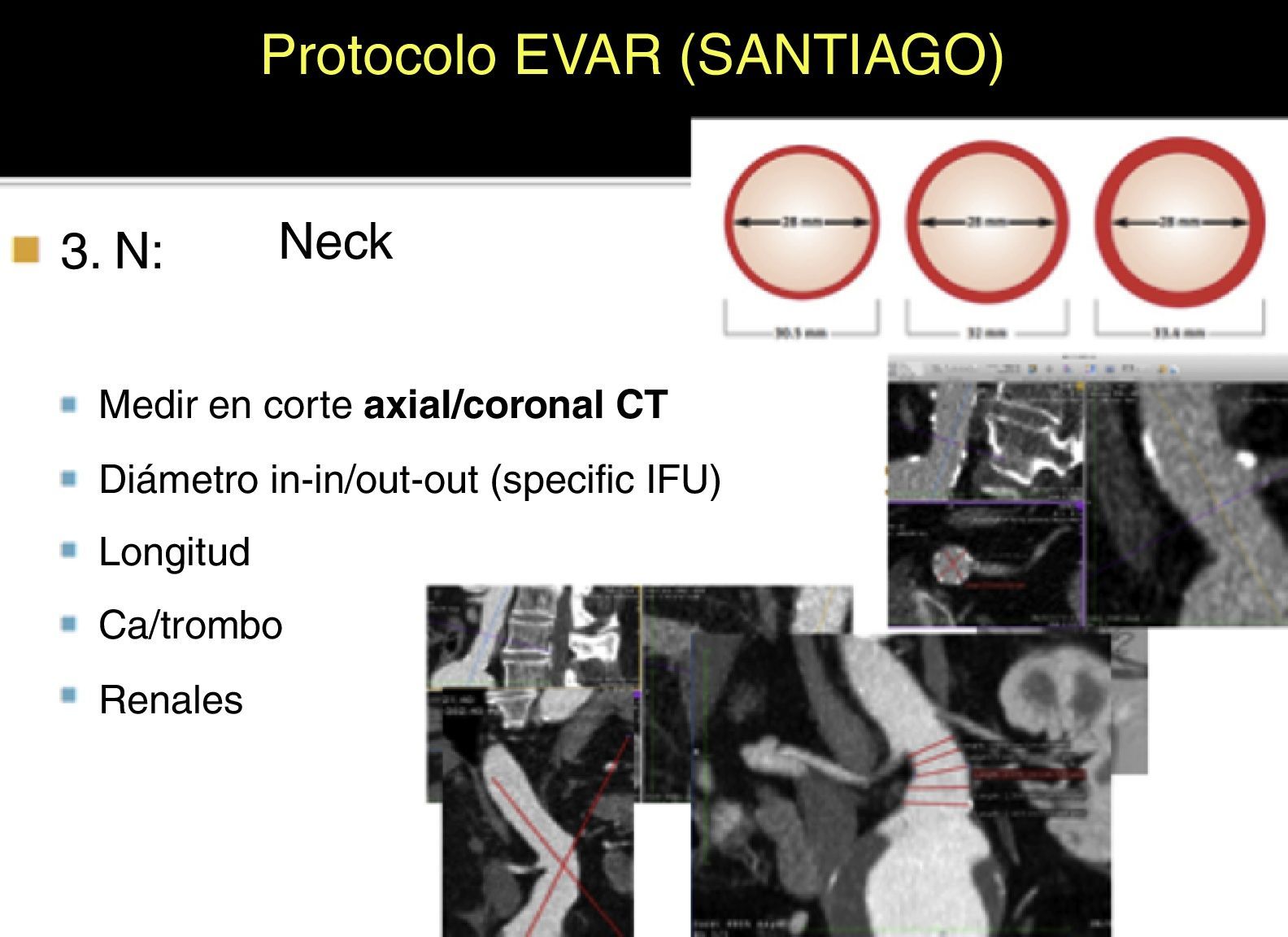
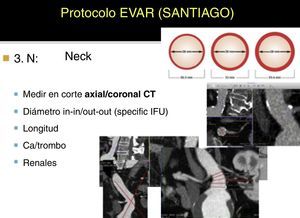
N o Neck: el cuello aórtico infrarrenal es uno de los factores anatómicos clave en planificación por su relación directa con reintervenciones y complicaciones a medio-largo plazo. Recomendamos evaluarlo en MPR o con un center-lumen-line (CPR) específico. Si no se dispone de tiempo, puede valorarse en cortes simples axiales (si la angulación antero-posterior es escasa) o en cortes coronales/sagitales (si angulaciones severas>60°), es decir, lo más ortogonal posible al eje aórtico mayor. Deben registrarse características como el diámetro interno (in-in) y externo (out-out), la longitud desde la arteria renal más baja al inicio del aneurisma, la presencia de trombo y calcio, y la posición horaria de la arteria renal más baja. En cuellos hostiles (longitud de menos de 1cm, angulaciones de más de 60°, presencia de trombo o calcio circunferencial, morfología cónica invertida, etc.), el cirujano responsable debe considerar su experiencia y habilidad en técnicas endovasculares de recurso como (chimeneas, cuffs, etc.) antes de plantear el tratamiento endovascular (fig. 4).
- –
T o bifurcaTion: la bifurcación aórtica, a pesar de no ser un factor anatómico tan estudiado en terapia EVAR como el cuello aórtico o los accesos ilíacos, también debe de ser considerada, ya que puede conducir al fracaso inmediato del procedimiento. Deben medirse su diámetro mínimo y la presencia de trombo/calcio, y puede evaluarse en cortes simples axiales o en una MPR. Se define como bifurcación estrecha cuando el diámetro es<18mm según lo reportado en las guías de práctica clínica de manejo de AAA por la ESVS en 20111. En situaciones de urgencia y con esta situación anatómica, recomendamos el implante de un dispositivo aorto-uni-ilíaco, la realización de un bypass fémoro-femoral cruzado y el implante de un oclusor ilíaco contralateral. Una endoprótesis bifurcada en una bifurcación estrecha puede precisar maniobras accesorias para evitar el colapso de las extensiones ilíacas, como pueden ser: la liberación intencionada en «posición de bailarina», la liberación simultánea de ramas, las técnicas kissing ballon, etc. Maniobras que pueden prolongar el tiempo de intervención en una situación crítica en la que el tiempo va en nuestra contra.
- –
I o Iliacs: la valoración de las arterias ilíacas es imprescindible, ya que constituyen las zonas de sellado distal de la endoprótesis. Puede valorarse su diámetro en cortes axiales/coronales, aunque en presencia de angulaciones extremas puede resultar impreciso. Si se dispone de una estación de trabajo recomendamos hacerlo con un CPR individualmente en cada eje, lo que también nos permitirá evaluar su longitud. Debe medirse siempre el diámetro interno «in-in», ya que es este diámetro, no el externo, el que condiciona el paso de los introductores de gran calibre empleados en terapia EVAR (habitualmente entre12 a 24 french). También se deben valorar como en los otros segmentos de sellado de la endoprótesis: la presencia de calcio y trombo, y las angulaciones severas (figs. 2 y 3). En casos con dilataciones aneurismáticas en arterias ilíacas comunes que condicionen una zona de sellado distal superior a los 24-26mm, recomendamos la liberación de una extensión distal para sellado en un segmento adecuado en arterias ilíacas externas, intentando en la medida de lo posible mantener al menos una hipogástrica permeable. En situaciones de urgencia, no consideramos necesario la medición-planificación de arterias hipogástricas y sus ramas, que sí es imprescindible para el implante de dispositivos para bifurcaciones ilíacas.
- –
A o Angulations: las angulaciones ya deben haber sido consideradas en cada uno de los sectores previos, especialmente las del cuello aórtico y ejes ilíacos. Es muy importante que se analicen en su conjunto, ya que la suma de varias angulaciones complejas es un elemento independiente de complejidad técnica del procedimiento, y porque deben estar registradas de modo claro, comprensible y visible por el resto del equipo en nuestro documento final. Estas medidas estimadas van a condicionar las angulaciones del arco radiológico en C de nuestro quirófano o nuestra sala híbrida. Si disponemos del formato DICOM, la forma más precisa y rápida de estimar angulaciones globales es el realizar un renderizado volumétrico del caso (VR), o realizar una MPR y calcular los ángulos de modo manual. Si solo disponemos de cortes simples, recomendamos visualizarlo en coronal o sagital, pero no en modo axial ya que la interpretación de angulaciones severas en planos axiales es compleja y puede llevar a errores de cálculo dramáticos para el resultado final.
- –
G o LenGth-LonGitud: la longitud es, sin duda, el punto menos importante de este protocolo de urgencia, ya que depende siempre de la disponibilidad de imágenes DICOM y porque la realización de un CPR preciso (CPR con medición de al menos la distancia desde la arteria renal más baja a ambas bifurcaciones aórticas e ilíacas) exige un tiempo real que en una urgencia puede no estar disponible. Consideramos que este paso es recomendable pero no es realmente imprescindible en EVAR de urgencias, ya que siempre puede emplearse un pigtail centimetrado intraoperatorio para determinar la longitud de las extensiones y el grado de solapamiento adecuado de los dispositivos para el sellado distal.
- –
O u OK for material: por último, siempre debe considerarse si disponemos del material adecuado para poder tratar la anatomía del caso evaluado con garantías. El objetivo debe ser siempre el de adaptar nuestro stock de endoprótesis a la anatomía del caso a tratar, pero no lo contrario, nunca adaptar la anatomía del paciente a las medidas de endoprótesis de que dispongamos ya que esta es una conducta de riesgo que, aunque podría llevarnos al éxito inmediato del procedimiento, se asociaría a una elevada incidencia de complicaciones a corto-medio plazo. En nuestra opinión, si no se dispone en una situación de urgencia del material adecuado para la anatomía a tratar debe de plantearse la reparación quirúrgica abierta del caso o la derivación a otro centro que disponga del material necesario si la situación clínica del paciente lo permite.
El material a revisar no debe limitarse a los habituales como: cuerpos de endoprótesis, extensiones ilíacas, guías superstiff, guías de trabajo, introductores, balones de inflado, cuffs, etc., ya que no disponer a tiempo de otros elementos básicos a priori menos importantes, como adaptadores para el inyector de contraste, llaves de 3 pasos, fundas estériles, conectores, sistemas de cierre percutáneo, etc., puede condicionar el resultado final del procedimiento.
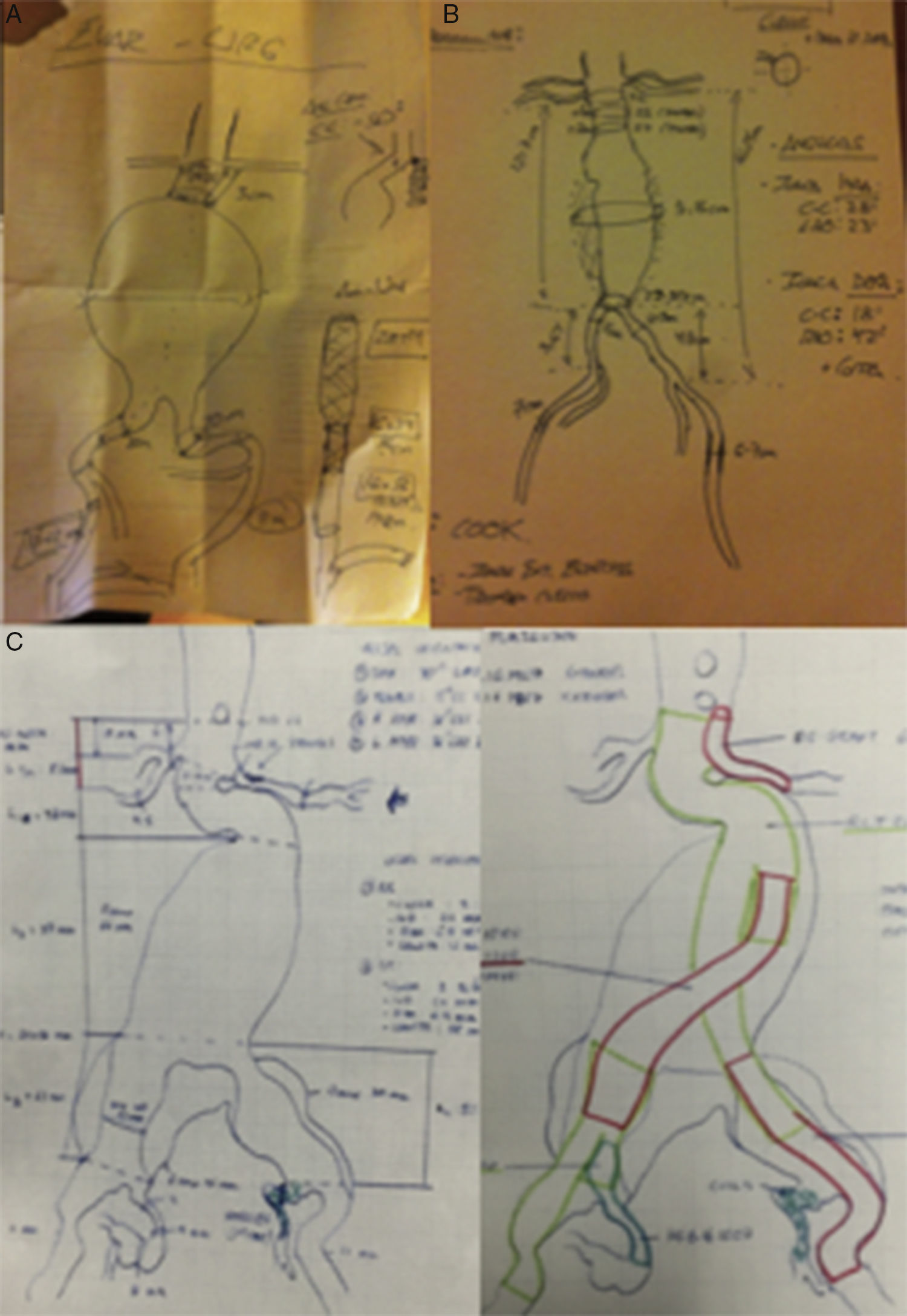
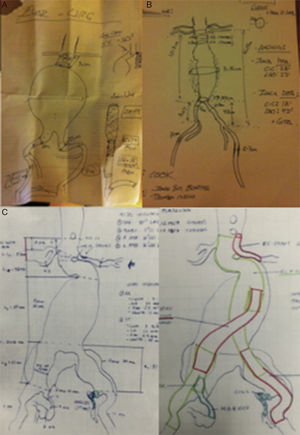
Tras anotar los 8 puntos clave en un dibujo esquemático del caso recomendamos tener este documento en un lugar visible en todo momento para el especialista y el equipo que realiza el procedimiento (en nuestro grupo en el arco en C, bajo una funda estéril trasparente) (fig. 5).
Modelos reales de planificación en terapia EVAR, recomendamos que este documento permanezca siempre visible durante el procedimiento. A) Situación de urgencia sin disponibilidad de DICOM (no center-lumen-line). B) EVAR programado y disponibilidad de DICOM (con center-lumen-line y cálculo de longitudes). C) EVAR complejo con técnica de chimenea en arteria renal izquierda, embolización hipogástrica izquierda y endoprótesis ilíaca ramificada (IBE) derecha. Cortesía Dr. N Mosquera.
De forma preliminar, debemos referir que tras la aplicación del protocolo SANTIAGO en nuestro centro, en junio del 2014, se consiguió reducir de un modo significativo la incidencia de la mortalidad global, en términos absolutos, en el tratamiento urgente de aneurismas aórticos infrarrenales rotos. El registro prospectivo de actividad asistencial iniciado en enero del 2013 en nuestro centro recogió 32 AAA rotos admitidos de modo consecutivo en urgencias, intervenidos o no, durante el periodo de enero del 2013 a mayo del 2015 (28 meses). Los resultados en el periodo estudiado preprotocolo de enero del 2013 a mayo del 2014 (17 meses consecutivos) fueron de 17 AAA-R admitidos en urgencias, de los cuales 2 casos, 11,8% (2/17), fueron considerados no candidatos para tratamiento quirúrgico o EVAR por su elevada comorbilidad asociada. Entre los pacientes intervenidos la mortalidad absoluta en el grupo de reparación quirúrgica abierta fue del 54,5% (6/11) y en el grupo EVAR del 25% (1/4).
Tras la aplicación del protocolo de planificación SANTIAGO en junio del 2014 se registraron consecutivamente hasta mayo del 2015 (11 meses) 15 casos de AAA rotos admitidos en el departamento de urgencias. Un caso fue desestimado para ningún tipo de intervención, 6,7% (1/15), la mortalidad absoluta en el grupo quirúrgico fue del 62,5% (5/8) y en el grupo EVAR no se registró ningún fallecimiento (0/6). La mortalidad absoluta a 30 días en AAA-R en nuestra serie, independientemente de la técnica empleada, se redujo del 46,6% (7/15) al 35,7%(5/14) tras la aplicación del protocolo SANTIAGO.
Analizando las técnicas por separado, se observó que en el grupo que recibió terapia EVAR y se aplicó el protocolo se pasó de una mortalidad previa del 25% (1/4) a una mortalidad del 0% (0/6). En el grupo intervenido por cirugía abierta, y en el que por tanto no fue preciso aplicar el protocolo, se registró un aumento de la mortalidad a 30 días del 54,5% (6/11) frente al 62,5% (5/8).
La supervivencia a un mínimo de 12 meses de los pacientes intervenidos, el 90,6% de la serie (29/32) fue del 100%, sin fallecimiento en el grupo quirúrgico ni en el de EVAR a mayo del 2016. La tasa de reintervención registrada fue del 3,4%, un paciente del grupo EVAR reintervenido por defecto de sellado de una rama distal (endofuga tipo ib).
DiscusiónAunque ningún ensayo clínico aleatorizado publicado hasta la fecha ha conseguido demostrar una disminución estadísticamente significativa de la mortalidad en el tratamiento endovascular respecto a la reparación quirúrgica abierta en los AAA rotos, es innegable que existe una tendencia a nivel mundial en ofrecer la terapia endovascular como la primera opción de tratamiento en aneurismas rotos o con signos de rotura inminente3,4. Esta técnica puede realizarse bajo anestesia local y con acceso percutáneo si las condiciones del paciente lo permiten, lo que disminuye aún más la morbimortalidad asociada al procedimiento3-5. En los últimos años, centros de referencia internacional y gran volumen han reportado series retrospectivas con datos que demuestran que el tratamiento endovascular urgente presenta a 30 días una mortalidad claramente inferior (16-31%) que la reparación quirúrgica abierta (34-44%)3-6. No se conoce de una forma objetiva la mortalidad real del tratamiento de AAA-R en nuestro entorno, debido a que la mayoría de los centros en nuestro país no reportan sus datos y/o existe a su vez una tendencia general a publicar en positivo. Los mejores datos de mortalidad en cirugía abierta de los que disponemos corresponden a centros internacionales con alto volumen, que dudosamente se puedan corresponder con nuestra realidad.
El tratamiento EVAR en situaciones de urgencia tiene aspectos diferenciales con el tratamiento EVAR programado, motivo por el que algunos especialistas vasculares pueden aún considerar a día de hoy que el tratamiento endovascular aórtico urgente en AAA-R no debe considerarse como la primera opción.
Es cierto que existen limitaciones exclusivas e inherentes a la situación de urgencia en EVAR y que ya han sido descritas en la literatura por grupos de referencia7, además de otros aspectos particulares que no se han considerado habitualmente en el tratamiento quirúrgico urgente abierto de un aneurisma aórtico roto:
- 1.
El tiempo disponible y necesario para la medición y planificación endovascular está dramáticamente disminuido.
- 2.
Las imágenes en formato DICOM, necesarias para el procesamiento en estaciones de trabajo, pueden no estar disponibles si el estudio diagnóstico se realizó en otro centro.
- 3.
La disponibilidad de un stock amplio de prótesis endovasculares y material accesorio que permita ofrecer la técnica con garantías es limitada.
- 4.
La capacidad de realizar el tratamiento en un quirófano híbrido o sala capacitada para realizar técnicas intervencionistas es dependiente de la organización de cada centro.
- 5.
La experiencia previa en técnicas EVAR del equipo vascular de guardia y las habilidades endovasculares globales de todos los niveles implicados (anestesia, enfermería, servicios de urgencia, etc.) son condicionantes independientes de resultados.
Reconocemos las limitaciones de este manuscrito y del protocolo de planificación expuesto, que excluye anatomías complejas para EVAR y que está basado en la experiencia personal de un grupo de angiólogos y cirujanos vasculares con experiencia en técnicas endovasculares avanzadas.
En cuanto al análisis de los resultados de nuestra serie prospectiva consecutiva de un número limitado de casos de AAA-R (32 casos), solo hemos descrito la mortalidad de nuestra serie en términos absolutos, a 30 días y a 12 meses, sin haber realizado un modelo estadístico más completo de tablas predictivas de mortalidad, lo que solo nos permite extraer conclusiones con limitado valor estadístico.
Consideramos, por otro lado, que la realización de la técnica EVAR con anestesia local y de modo percutáneo, siempre que la situación específica del paciente lo permita, debe considerarse como primera opción, ya que parece ser un factor independiente que se asocia con mejores de resultados de morbimortalidad en el grupo EVAR, por tanto, la disminución de la mortalidad observada en nuestra serie no puede ser atribuida en exclusiva a la aplicación del protocolo SANTIAGO.
Del mismo modo, el aumento de la mortalidad observado en el grupo quirúrgico puede explicarse por tratarse de casos de roturas aórticas en anatomías más complejas o la sospecha de aneurismas infecciosos, casos no considerados por el cirujano vascular de guardia como adecuados para terapia EVAR, y que además precisaron reparaciones quirúrgicas más complejas con pinzamientos suprarrenales, procedimientos extra-anatómicos o reparaciones venosas complejas asociadas.
ConclusionesBasados en nuestra experiencia y en la mejora de resultados en la mortalidad absoluta de AAA-R observados en nuestra serie, consideramos que la existencia de un protocolo de planificación EVAR permite optimizar la técnica al recordar los pasos clave de un modo esquemático.
En nuestra opinión, los equipos quirúrgicos vasculares con experiencia en terapia endovascular deben de ser capaces de afrontar esta urgencia vital con las garantías suficientes de modo eficaz y autónomo, y consideramos que la planificación es la clave y el paso más importante en el éxito de la terapia EVAR.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesNo existe ningún conflicto de interés por parte de ninguno de los 6 coautores de este trabajo.
AgradecimientosEl primer autor de este trabajo, F. Gallardo Pedrajas, agradece personalmente a sus excompañeros del equipo del Hospital Clínico Universitario de Santiago durante el periodo 2012-2015 por la idea original y el apoyo en el diseño del trabajo. A sus compañeros en el Instituto Vascular y Endovascular Internacional en el Hospital Quirónsalud Marbella por la colaboración y revisión del manuscrito.
Agradecer, igualmente, al Dr. Peter Schneider, Kaiser Permanent de Hawaii, al Dr. Zoran Rancic, Zurich Hospital, y al Pr. Vincent Riambau, Hospital Clinic Barcelona, por sus comentarios y crítica para la mejora de este protocolo y valorar la posibilidad de su aplicación en centros internacionales.