El tratamiento actual de las lesiones de la arteria subclavia (AS) es controvertido. Su transposición a la arteria carótida común (TSC) presenta mayor complejidad técnica a cambio de ofrecer mejores resultados a largo plazo. La angioplastia transluminal percutánea con stent (ATPs) resulta técnicamente más sencilla, pero no siempre es factible. No se han publicado resultados ni comparaciones a largo plazo. Nosotros comparamos ambos métodos realizados por cirujanos vasculares. Los datos se obtuvieron de forma prospectiva mediante un análisis retrospectivo en un centro terciario. La ATPs se realizó a través de un abordaje humeral retrógrado utilizando stents de nitinol autoexpansibles. La cirugía abierta fue siempre mediante TSC. Se aplicaron los estándares de registro de la Society for Vascular Surgery/International Society of Cardiovascular Surgery. Setenta y cuatro pacientes fueron sometidos a tratamiento desde enero de 1995 hasta agosto de 2007 (media de edad: 62,6 años, 40 mujeres; patología de lado izquierdo: 60 [81,1%]; factores de riesgo: hipertensión arterial 45 [60,8%], dislipidemia 47 [63,5%], diabetes 21 [28,4%], tabaquismo 43 [58,1%], oclusión de AS 50 [67,6%]). Cuarenta pacientes (54,1%) fueron sometidos a ATPs primaria (62,5% por oclusiones) y 34 a TSC (73,5% por oclusiones). Ambos grupos fueron comparables en cuanto a los factores de riesgo. En 12 pacientes no se pudieron recanalizar las oclusiones (30%), y en 2 fracasaron los stents al mes de la intervención (ambos por estenosis). Todos excepto uno fueron sometidos posteriormente a una TSC sin más problemas. Todas las TSC fueron satisfactorias. No se pudo identificar ningún factor de riesgo para el fracaso del tratamiento a excepción de la ATPs (p = 0,002, test exacto de Fisher). La media del seguimiento fue de 50,1 meses para la ATPs y de 52,6 meses para la TSC. Ninguna intervención fracasó durante el seguimiento en ninguno de los grupos. Los cirujanos pueden realizar ATPs de forma satisfactoria. La ATPs primaria fracasó en el 48% de las oclusiones (30% de todas las ATPs). No es posible predecir el fracaso. Según nuestra experiencia, recomendamos realizar una ATPs primaria en casos de estenosis de AS y cirugía en caso de oclusiones de AS.
El mejor tratamiento de las patologías estenótica y oclusiva del primer segmento de la arteria subclavia (AS) sigue siendo controvertido. Inicialmente, las lesiones sintomáticas de la AS caracterizadas por insuficiencia vertebrobasilar (IVB) y/o isquemia de la extremidad superior se han tratado mediante la corrección directa. Sin embargo, las intervenciones transtorácicas han demostrado tasas de mortalidad y morbilidad desfavorables1. Por tanto, se han desarrollado estrategias extratorácicas y extraanatómicas para reconstruir las lesiones de la AS proximal (transposición de subclavia a carótida [TSC], bypass carótido-subclavia, bypass de subclavia-subclavia, bypass axilo-axilar) que han gozado de amplia difusión. Según la literatura, la TSC, descrita por Parrott en 1964, es el método más duradero, con índices de permeabilidad a largo plazo del 90-100%2-5. Recientemente, la TSC ha adquirido una importancia renovada en los pacientes con aneurismas de la aorta descendente proximal, para crear una zona de anclaje adecuada para la reparación endovascular6,7. No obstante, debido a razones anatómicas, todas las intervenciones que afectan a la AS son exigentes desde el punto de vista técnico, y las complicaciones locales pueden desempeñar un papel negativo8. Por esta razón, las técnicas endovasculares (angioplastia transluminal percutánea [ATP] con o sin colocación de stent) para el tratamiento de las lesiones estenóticas y oclusivas de la AS, descritas por primera vez en 1980 por Bachman y Kim9, se han ido convirtiendo en una opción terapéutica cada vez más popular. Los ensayos a gran escala comparando el tratamiento quirúrgico y endovascular de las patologías de la AS son limitados. El objetivo de este estudio es un análisis comparativo de la TSC frente a la ATP con stent (ATPs) en pacientes con lesiones sintomáticas de la AS proximal.
Materiales y MétodosLos datos se introdujeron de forma prospectiva en una base de datos vascular computarizada y se analizaron de forma retrospectiva. Desde enero de 1995 hasta marzo de 2007, 74 pacientes recibieron tratamiento de sus patologías sintomáticas de AS mediante TSC o ATPs en un centro universitario terciario. Los dos grupos de pacientes fueron tratados por el mismo grupo de cirujanos. El cirujano a cargo eligió preferentemente un abordaje endovascular. Antes de la intervención, se evaluó la historia clínica y se realizó un examen físico mediante análisis de la onda del pulso y determinación no invasiva de la presión arterial bilateral de las extremidades superiores. Entre las modalidades de técnicas por la imagen realizadas antes de la cirugía o del tratamiento endovascular destacan el eco-Doppler (ED) y la arteriografía o la angiografía por resonancia magnética (ARM) de los vasos del cayado aórtico. Se obtuvieron de forma rutinaria imágenes del cerebro utilizando la tomografía computerizada (TC) o la resonancia magnética (RMN). Adicionalmente, todos los pacientes fueron visitados por un neurólogo independiente antes de la intervención.
Técnica de la ATPsTodas las intervenciones endovasculares se realizaron en la sala endovascular bajo anestesia local mediante la técnica de Seldinger. En todos los pacientes se utilizó el abordaje transhumeral a través de la arteria cubital homolateral, como describieron Queral y Criado10. Tras puncionar la arteria de forma ecoguiada se insertó una guía y un introductor 5-F. Se administró heparinización sistémica (25-100 U/kg) una vez establecido un acceso vascular seguro. Tras pasar la guía y el catéter de angiografía a través de la lesión, se sustituyó el introductor por otro 6-F. Tras realizar la angiografía de los vasos del cayado aórtico, la lesión de la AS se predilató con un catéter con balón, y seguidamente se expandió un stent de nitinol autoexpansible y se dilató para lograr una morfología óptima. Después de realizar el control angiográfico final y determinar el gradiente de presión translesional, se revirtió la heparina para retirar la vaina introductora. La colocación del stent se consideró satisfactoria si se situó en posición correcta y el gradiente de presión a través de la lesión no sobrepasó los 5-10 mmHg o la estenosis residual fue < 30%. El lugar de la punción se comprimió de forma manual durante 15 min.
Técnica de la TSCLa intervención se realizó bajo anestesia general. El paciente se colocó en decúbito supino situando un rollo entre las escápulas para elevar los hombros. El cuello se extendió lo máximo posible con la cabeza girada hacia el lado contralateral. Preferimos un abordaje medial a la AS central a través de un abordaje transverso supraclavicular, 1-2 cm por encima de la clavícula, entre los vientres del músculo esternocleidomastoideo. Los detalles técnicos de la intervención han sido descritos ampliamente por nuestro grupo8.
Pauta antitrombóticaEl tratamiento antitrombótico se inició antes de la intervención e incluyó la administración oral de 100 mg/kg/día de ácido acetilsalicílico más heparina de bajo peso molecular subcutánea ajustada al peso en ambos grupos de pacientes. La heparina de bajo peso molecular se suspendió al recibir el alta médica y el ácido acetilsalicílico se continuó de forma indefinida.
Tratamiento postoperatorio y seguimientoTodos los pacientes fueron sometidos a un examen neurológico tras la intervención para detectar déficits neurológicos centrales. En los casos quirúrgicos se realizó una laringoscopia de forma rutinaria para detectar lesiones recurrentes de los nervios laríngeos. En los pacientes sometidos a ATPs se realizó un examen con ED tras la intervención. Se realizó una fluoroscopia en todos los casos de cirugía abierta para descartar una parálisis del nervio frénico. En casos de TSC del lado izquierdo, los pacientes recibieron una comida rica en grasas el tercer día del postoperatorio para identificar una fuga linfática antes de retirar el drenaje. Tras el alta hospitalaria, todos los pacientes fueron revisados cada 3 meses durante el primer año y posteriormente de forma anual. Las visitas de seguimiento las realizó un cirujano vascular adjunto. El tratamiento rutinario consistió en la obtención de la historia clínica y la realización de un examen físico con análisis de la onda del pulso y la determinación no invasiva de la presión arterial bilateral en las extremidades superiores. Se realizó anualmente un examen con ED y, de forma adicional, al detectar diferencias en la presión arterial > 15 mmHg. Se realizó una ARM y una angiografía por TC (ATC) solamente si existió una sospecha de reestenosis significativa de la AS o la necesidad de realizar una nueva intervención en las ramas supraaórticas, especialmente en las arterias carótidas.
Presentación estadística y estándares de notificaciónSe utilizaron los estándares de notificación de la Society for Vascular Surgery/International Society of Cardiovascular Surgery para preparar este informe11. Los datos se analizaron utilizando la prueba t de Student independiente de dos colas, el test chi cuadrado de Pearson, y el test exacto de Fisher de dos lados. En ambos grupos de estudio se aplicaron el estimador del producto límite de Kaplan-Meier y los análisis de la tabla de vida junto con los errores estándar de la permeabilidad acumulativa. Las curvas de Kaplan-Meier de ambos grupos de pacientes se compararon y comprobaron utilizando el test de logaritmo de rangos, el test Wilcoxon-Gehan, y el test Cox-Mantel. Se consideró que p < 5% fue estadísticamente significativo. Todos los análisis e ilustraciones se realizaron utilizando Statistica 6.1 (StatSoft, Tulsa, OK).
ResultadosDesde enero de 1995 hasta agosto de 2007, 74 pacientes (40 mujeres, media de edad de 61 años, límites de edad 39-85 años) fueron sometidos a ATPs (n = 40) o TSC primaria (n = 34) por lesiones sintomáticas de la AS proximal (oclusión o estenosis hemodinámica significativa [> 70%]). La patología oclusiva de la AS (POAS) fue de origen aterosclerótico en todos los casos.
Demografía de los pacientes e indicación del tratamientoCuarenta pacientes (21 mujeres, media de edad 61 años, límites de edad 44-79 años) fueron sometidos a ATPs primaria. En treinta y cuatro pacientes (19 mujeres, media de edad 60 años, límites de edad 39-85 años) se realizó una TSC primaria por una POAS. No se observaron diferencias estadísticamente significativas entre los pacientes sometidos a ATPs y TSC primaria en cuanto a sexo, edad y factores de riesgo cardiovascular (tabla I). Los síntomas de la POAS también estuvieron distribuidos de forma similar entre los grupos de pacientes (tabla II). Las indicaciones más habituales para la ATPs y la TSC fueron signos de IVB, como vértigo (n = 29, 40%), y vértigo con claudicación del brazo (n = 18, 24%). Otros problemas clínicos, incluida la claudicación del brazo (n = 14, 19%), se observaron con poca frecuencia. No se observaron diferencias estadísticamente significativas en la presentación preoperatoria de ambos grupos.
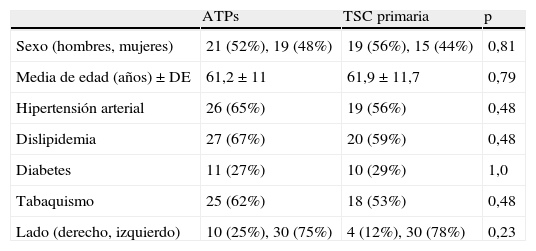
Detalles demográficos de los 74 pacientes sometidos a ATPs o TSC primarias
| ATPs | TSC primaria | p | |
| Sexo (hombres, mujeres) | 21 (52%), 19 (48%) | 19 (56%), 15 (44%) | 0,81 |
| Media de edad (años) ± DE | 61,2 ± 11 | 61,9 ± 11,7 | 0,79 |
| Hipertensión arterial | 26 (65%) | 19 (56%) | 0,48 |
| Dislipidemia | 27 (67%) | 20 (59%) | 0,48 |
| Diabetes | 11 (27%) | 10 (29%) | 1,0 |
| Tabaquismo | 25 (62%) | 18 (53%) | 0,48 |
| Lado (derecho, izquierdo) | 10 (25%), 30 (75%) | 4 (12%), 30 (78%) | 0,23 |
ATPs: angioplastia transluminal percutánea con stent; DE: desviación estándar; TSC: transposición a la arteria carótida común.
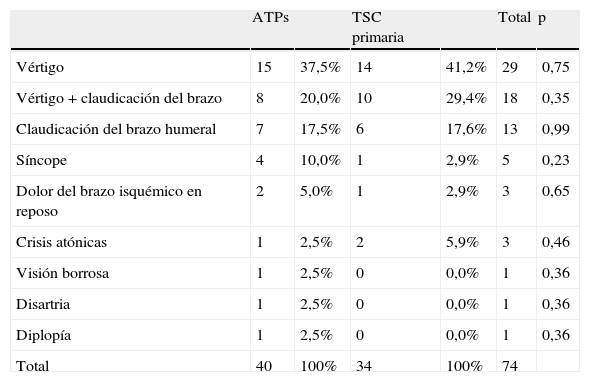
Indicación del tratamiento en los 74 pacientes sometidos a ATPs o TSC
| ATPs | TSC primaria | Total | p | |||
| Vértigo | 15 | 37,5% | 14 | 41,2% | 29 | 0,75 |
| Vértigo + claudicación del brazo | 8 | 20,0% | 10 | 29,4% | 18 | 0,35 |
| Claudicación del brazo humeral | 7 | 17,5% | 6 | 17,6% | 13 | 0,99 |
| Síncope | 4 | 10,0% | 1 | 2,9% | 5 | 0,23 |
| Dolor del brazo isquémico en reposo | 2 | 5,0% | 1 | 2,9% | 3 | 0,65 |
| Crisis atónicas | 1 | 2,5% | 2 | 5,9% | 3 | 0,46 |
| Visión borrosa | 1 | 2,5% | 0 | 0,0% | 1 | 0,36 |
| Disartria | 1 | 2,5% | 0 | 0,0% | 1 | 0,36 |
| Diplopía | 1 | 2,5% | 0 | 0,0% | 1 | 0,36 |
| Total | 40 | 100% | 34 | 100% | 74 |
ATPs: angioplastia transluminal percutánea con stent; TSC: transposición a la arteria carótida común.
Se produjeron más oclusiones que estenosis de la AS (n = 50, 67% frente a n = 24, 33%). Además, otras lesiones del tronco supraaórtico se registraron con poca frecuencia en ambos grupos (tabla III). No se observaron diferencias estadísticamente significativas entre los grupos de tratamiento con respecto a la patología de la AS u otras patologías del tronco supraaórtico. En 3 pacientes se realizó una trombendarterectomía carotídea como mínimo 4 semanas antes de la TSC por estenosis sintomática. No se realizaron intervenciones carotídeas antes de la ATPs.
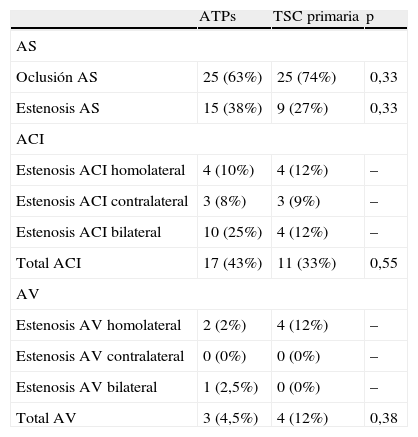
Descripción de las lesiones oclusivas de las arterias supraaórticas en los 74 pacientes sometidos a ATPs o a TSC (estenosis definida como reducción de la luz > 30%)
| ATPs | TSC primaria | p | |
| AS | |||
| Oclusión AS | 25 (63%) | 25 (74%) | 0,33 |
| Estenosis AS | 15 (38%) | 9 (27%) | 0,33 |
| ACI | |||
| Estenosis ACI homolateral | 4 (10%) | 4 (12%) | – |
| Estenosis ACI contralateral | 3 (8%) | 3 (9%) | – |
| Estenosis ACI bilateral | 10 (25%) | 4 (12%) | – |
| Total ACI | 17 (43%) | 11 (33%) | 0,55 |
| AV | |||
| Estenosis AV homolateral | 2 (2%) | 4 (12%) | – |
| Estenosis AV contralateral | 0 (0%) | 0 (0%) | – |
| Estenosis AV bilateral | 1 (2,5%) | 0 (0%) | – |
| Total AV | 3 (4,5%) | 4 (12%) | 0,38 |
ACI: arteria carótida interna; AS: arteria subclavia; ATPs: angioplastia transluminal percutánea con stent; AV: arteria vertebral; TSC: transposición a la arteria carótida común.
No fracasó ninguna TSC. En 12 pacientes (30%) la ATPs primaria fracasó debido a que la guía no pudo atravesar la lesión de la AS. El porcentaje de éxito de la intervención en todos los procesos endovasculares fue del 70% (28 de 40). Todas las intervenciones primarias que fracasaron presentaron oclusión de la AS. El porcentaje de éxito de la intervención en caso de oclusiones de la AS fue del 52% (13 de 25). El porcentaje de éxito primario de la estenosis de la AS fue del 100%. En 2 de los pacientes, se produjo una oclusión temprana del stent los días 7 y 27 tras la intervención, respectivamente. Ambos fracasos se produjeron tras el tratamiento de la estenosis de la AS. Un paciente fue sometido a una TSC secundaria; el otro rechazó más tratamientos. Todos los casos de fracasos primarios (oclusiones) fueron sometidos a una TSC secundaria.
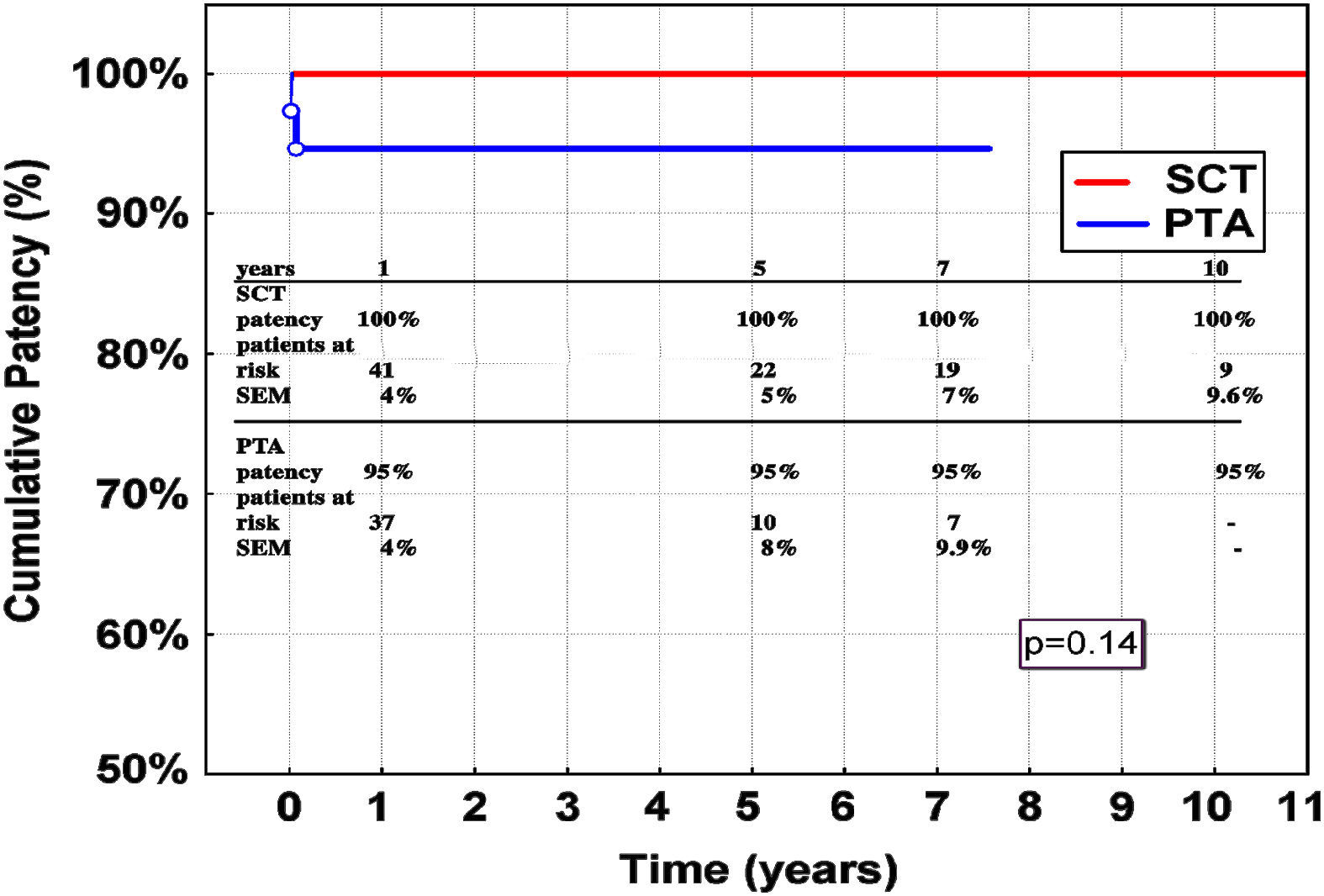
Permeabilidad y seguimientoTodas las intervenciones TSC conservaron la permeabilidad durante el seguimiento. No se detectaron reestenosis en el lugar de la anastomosis ni en la AS distal a la anastomosis. Ningún paciente necesitó una intervención secundaria de la arteria carótida común central en este grupo. No fue necesario realizar reintervenciones en el segmento del stent de la AS o distal a él tras las ATPs satisfactorias durante todo el seguimiento. No se observaron diferencias estadísticamente significativas en los índices de permeabilidad entre los pacientes sometidos a ATPs y los sometidos a TSC (p = 0,14) (fig. 1).
Estimación de Kaplan-Meier de la permeabilidad acumulativa en los 73 pacientes sometidos a TSC o a la ATPs técnicamente satisfactoria durante los 10 años de seguimiento (un paciente rechazó cirugía adicional tras fracasar la ATPs). La diferencia entre ambos grupos no es significativa (p = 0,14). ATP: angioplastia transluminal percutánea; SCT: transposición a la arteria carótida común.
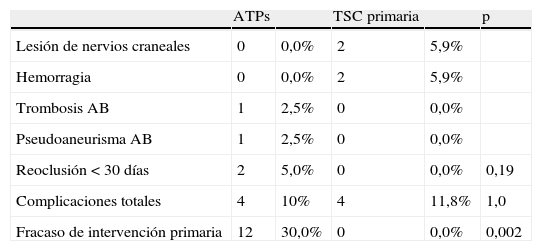
Ningún paciente de ningún grupo presentó complicaciones neurológicas centrales tras la intervención. En dos con TSC primaria fue necesario evacuar un hematoma. En ninguno de los casos se produjo ninguna fuga anastomótica. Además, dos pacientes con TSC primaria desarrollaron una parálisis del nervio craneal transitoria, que se resolvió a las 4 y 6 semanas tras la intervención (una parálisis recurrente del nervio laríngeo, un síndrome de Horner). En un paciente con una TSC secundaria, se observó una fuga linfática postoperatoria, que requirió una revisión quirúrgica. En 2 pacientes sometidos a ATPs se detectaron complicaciones del acceso vascular que requirieron reintervención. Un paciente presentó una isquemia incompleta del brazo debida a una trombosis de la arteria humeral tras la compresión. En otro se desarrolló un pseudoaneurisma de la arteria humeral. Ambos pacientes fueron tratados mediante revisión local y angioplastia con parche venoso. El único factor para el éxito de la intervención primaria fue el uso de una TSC para tratar la patología de la AS (p = 0,002) (tabla IV).
Complicaciones postintervención en los 74 pacientes sometidos a ATPs o TSC primaria
| ATPs | TSC primaria | p | |||
| Lesión de nervios craneales | 0 | 0,0% | 2 | 5,9% | |
| Hemorragia | 0 | 0,0% | 2 | 5,9% | |
| Trombosis AB | 1 | 2,5% | 0 | 0,0% | |
| Pseudoaneurisma AB | 1 | 2,5% | 0 | 0,0% | |
| Reoclusión < 30 días | 2 | 5,0% | 0 | 0,0% | 0,19 |
| Complicaciones totales | 4 | 10% | 4 | 11,8% | 1,0 |
| Fracaso de intervención primaria | 12 | 30,0% | 0 | 0,0% | 0,002 |
AB: arteria humeral; ATPs: angioplastia transluminal percutánea con stent; TSC: transposición a la arteria carótida común.
En nuestro estudio hemos comparado dos métodos utilizados para el tratamiento de la POAS sintomática, una entidad muy poco frecuente comparada con la estenosis de la carótida interna. Sterpetti et al12 informaron que la revascularización de la AS representa solamente el 4,6% de los casos, en comparación con el número de endarterectomías carotídeas. Si bien la TSC se ha realizado desde la década de los sesenta, el tratamiento endovascular de la POAS se describió por primera vez en la década de los ochenta2,9. Existe un debate en curso sobre si la colocación de stent en la AS es superior a la ATP sola10,13. No se han publicado ensayos aleatorizados prospectivos que comparen diferentes modalidades terapéuticas de la POAS y los resultados a largo plazo del tratamiento endovascular. Farina et al14 compararon la ATP sin colocación de stent con las intervenciones de bypass de la carótida a la subclavia en pacientes con POAS proximal. Los autores notificaron unos índices de permeabilidad del 54% en 21 pacientes sometidos a ATP y un índice de permeabilidad al cabo de 3 años significativamente mejor, del 87%, en 15 pacientes sometidos a bypass. En un informe reciente, AbuRahma et al15 compararon la ATPs con los injertos de bypass de carótida a subclavia. Si bien el grupo del bypass no fue homogéneo, los resultados fueron significativamente mejores que los de la ATPs. Por otro lado, es bien sabido que los resultados de los bypass son inferiores a los de la TSC3. Nuestro estudio constituye la primera comparación de la ATPs frente a la TSC en pacientes afectados de POAS proximal sintomática.
En este estudio, las dos poblaciones de pacientes estuvieron bien emparejadas con respecto a los factores de riesgo de patología vascular, así como a la anatomía y a la patología de los troncos supraaórticos. Esto es importante, ya que existe una tendencia al tratamiento endovascular en los pacientes con lesiones estenóticas de la AS. Además, las lesiones del lado derecho suelen tratarse mediante cirugía debido a la elevada incidencia de episodios neurológicos centrales durante la manipulación endovascular en este grupo de pacientes16.
En nuestra población, el índice de permeabilidad a los 5 años de las ATPs realizadas con éxito fue del 95%. Se han descrito índices de permeabilidad del 80-100% con la angioplastia con balón sola para estenosis de AS, mientras que los índices de permeabilidad de la ATP en casos de oclusión de la AS se sitúan en torno al 20-50%17,18. Con la instauración de la ATPs por Queral y Criado10, los índices de permeabilidad en los pacientes con oclusión de la AS aumentaron hasta el 70-100%19. En 1999, Rodriguez-Lopez et al19 notificaron un índice de permeabilidad primaria global del 73% y un índice de permeabilidad secundaria global del 90% en 69 pacientes con POAS sintomática sometidos a colocación de stent primario en AS. Los autores compararon sus resultados con los de la literatura sobre la cirugía para POAS sintomática. No observaron diferencias significativas en los índices de permeabilidad entre la colocación del stent y la cirugía, aunque la TSC no se incluyó en su revisión19. De Vries et al16 informaron en 2005 de un índice de permeabilidad primaria a los 5 años con la ATP con o sin colocación de stent del 89%. Nakamura et al20 publicaron un índice de permeabilidad a los 5 años del 99% en 320 pacientes sometidos a ATPs por una POAS sintomática. Este estudio multicéntrico sigue en curso. Si bien se recomienda la ATP con colocación de stent en casos de oclusión de la AS, disección de la AS, y estenosis residual significativa tras una ATP, algunos autores recomiendan la colocación de stent primario (como nosotros) para lograr mejorías en los índices de permeabilidad y evitar nuevas intervenciones19,21. Por el momento, sigue siendo controvertido si el uso de stent primario o ATP sola arrojan resultados superiores a largo plazo en pacientes con POAS proximal13. Al contrario que en la mayoría de las series, hemos utilizado los stents de nitinol autoexpansibles porque creemos que la flexibilidad en esta región es más importante que la fuerza radial. Se produjo una incidencia del 48% de fracasos de la ATPs primaria en las oclusiones de la AS, lo que no puede atribuirse al uso de un stent, y solamente un porcentaje bajo de fracasos secundarios en las estenosis de ATPs.
Todas las intervenciones TSC seguían permeables tras un seguimiento medio de 52 meses. Los índices de permeabilidad descritos para las reconstrucciones quirúrgicas de la POAS oscilan entre el 80 y el 100%3-5. Cina et al22 describieron en 2002 el resultado de una cohorte de pacientes sometidos a TSC para una POAS y realizaron una revisión sistemática de la literatura sobre TSC y bypass carótida-AS. La permeabilidad y la ausencia de síntomas clínicos fueron más elevadas con la TSC que con el bypass carótida-AS (98 frente a 84%, p < 0,0001). Estos resultados concuerdan con los de otros estudios, que registraron un índice de permeabilidad a largo plazo del 100% con la TSC en pacientes afectados de POAS proximal3-5,8.
Algunos autores recomiendan el tratamiento antiagregante plaquetario dual tras la ATP de una POAS para minimizar las tasas de oclusión del stent23. Nuestros pacientes recibieron una dosis oral de tratamiento antitrombótico (ácido acetilsalicílico, 100 mg/día) en ambas opciones terapéuticas, produciéndose dos oclusiones del stent tras 7 y 27 días, respectivamente. Son necesarios ensayos prospectivos y aleatorizados para evaluar el mejor tratamiento antitrombótico (tratamiento antiagregante plaquetario único frente a dual) tras la revascularización endovascular de la POAS.
En la literatura actual, el porcentaje de éxito técnico primario de la recanalización endovascular de la POAS proximal oscila entre el 70 y el 100%23. En nuestro estudio, en 12 de 40 pacientes sometidos a ATP primaria (30%) no pudo atravesarse con la guía la lesión oclusiva de la AS, a pesar de que preferimos el abordaje transhumeral retrógrado23. Estos pacientes fueron sometidos a una TSC posterior sin complicaciones perioperatorias. Éste es un hallazgo destacable ya que cabría esperar un aumento de la dificultad de la disección tras la manipulación endovascular de la porción central friable de la AS. Un porcentaje de fracaso primario del 30% parece ser alto, pero refleja la experiencia de nuestro grupo con la cirugía abierta en esta región. Si el paso de la guía no puede realizarse de forma segura, es probable que la conversión a la TSC es la mejor opción para el paciente. A ese respecto, puede ser discutible si las oclusiones de la AS deben tratarse principalmente con TSC. Nuestra tasa de complicaciones de las TSC primarias fue del 11,8%. Las complicaciones postoperatorias tras la TSC se observan en el 10-15% de los casos, y son básicamente complicaciones locales reversibles, como hematomas, parálisis nerviosas y lesiones del conducto linfático5,22,24. Cina et al22 notificaron en su revisión sistemática lesiones de nervios craneales en el 11,2% de los pacientes sometidos a TSC y en el 9,2% de los pacientes sometidos a bypass protésico. La incidencia de parálisis nerviosas y lesiones del conducto torácico pueden reducirse de forma significativa utilizando un abordaje medial para la TSC8. El abordaje medial se utilizó preferentemente en los pacientes sometidos a cirugía en este estudio8.
En el grupo ATPs observamos complicaciones en el 10% de los casos. De Vries et al16 observaron una tasa de complicaciones locales del 4,5% y una tasa combinada de ictus y fallecimiento del 3,6% en pacientes sometidos a ATP de la POAS proximal. Los autores argumentaron que las lesiones, especialmente de la AS derecha, comportan el riesgo de embolización distal durante la manipulación endovascular debido a la proximidad de la arteria carótida común. Nosotros no observamos episodios neurológicos mayores en nuestro grupo de ATPs. Todas las complicaciones fueron locales (un pseudoaneurisma y una trombosis de la arteria humeral) con la consiguiente corrección quirúrgica, necesaria en un 5% de nuestros pacientes. Si bien el abordaje femoral para la ATPs se usa con frecuencia, preferimos el humeral, debido a la corta distancia desde el lugar de punción hasta la lesión y la facilidad de maniobrabilidad de las guías. Las complicaciones locales en el lugar de la punción pueden reducirse aún más mediante un abordaje quirúrgico y punción abierta de la arteria humeral.
ConclusionesEn resumen, la ATPs de la POAS sintomática puede realizarse satisfactoriamente por cirujanos vasculares. Los resultados a largo plazo son excelentes cuando la ATP no se ve forzada y se realiza solamente en casos claros. Según nuestra experiencia, recomendamos la ATPs primaria en casos de estenosis de AS y la cirugía en casos de oclusiones de la AS. Puede intentarse realizar una ATPs en caso de oclusión, pero el porcentaje de fracasos esperado es del 50%. Nuestros resultados deben confirmase con un ensayo prospectivo aleatorizado.