Con la complejidad cada vez mayor de los procedimientos endovasculares, ha aumentado la preocupación relativa a la exposición del paciente a la radiación. La corrección de aneurisma aórtico abdominal (AAA) representa el más complejo de los procedimientos efectuados hoy día por cirujanos vasculares. El presente estudio evalúa la dosis de radiación recibida por el paciente durante la reparación endovascular de un AAA. Durante un período de 3 meses, monitorizamos prospectivamente la dosis de radiación en una serie de pacientes sometidos a la reparación endovascular de estas lesiones. Todos los pacientes se sometieron al procedimiento estándar con la implantación de una de las endoprótesis disponibles comercialmente utilizando la unidad GE OEC 9800. Se registró la medición directa de la dosis de máxima radiación a nivel cutáneo (dosis cutánea pico, DCP) mediante una película de dosimetría radiográfica GAFCHROMIC. Con el dosímetro del brazo C se registraron mediciones indirectas de la dosis de radiación (tiempo de fluoroscopia y producto dosis-área [PDA]). Se evaluó un total de 12 pacientes consecutivos, sometidos a la reparación endovascular estándar de AAA. La DCP media fue de 0,75 Gy (límites 0,27-1,25). El tiempo medio de fluoroscopia total fue de 20,6 min (límites 12,6-34,2) con una media del 92% invertido en fluoroscopia estándar y un 8% invertido en cinefluoroscopia. Con respecto al tiempo de fluoroscopia total, el 49% se invirtió en un campo de visión normal y el 51%, en campo de visión aumentado. El PDA medio fue de 15.166 cGy/cm2 (límites 5.207-24.536). La DCP se correlacionó con el PDA (r=0,9, p<0,05) pero no con el tiempo de fluoroscopia total (r=0,18, p>0,05). La DCP también se correlacionó con el índice de masa corporal (IMC; r=0,82, p<0,05). En pacientes obesos la DCP media fue de 1,1 Gy comparado con 0,5Gy en aquellos no obesos. La DCP de todos los pacientes fue muy inferior al umbral aceptado de 2,0 Gy para lesión cutánea. Además, el parámetro se correlacionó con el PDA pero no con el tiempo de fluoroscopia total. La DCP también se correlacionó con el IMC, fue significativamente mayor en pacientes obesos comparado con no obesos. A pesar de la complejidad y duración de la reparación endovascular de los AAA, el procedimiento puede efectuarse sin riesgos de una exposición excesiva a la radiación.
Con la complejidad cada vez mayor de los procedimientos endovasculares, ha aumentado la preocupación relativa a la exposición del paciente a la radiación1-3. La corrección del aneurisma aórtico abdominal (AAA) representa el más complejo de los procedimientos efectuados hoy día por cirujanos vasculares.
La principal preocupación durante dichos procedimientos es la lesión cutánea4 reflejada por la dosis cutánea pico (DCP), es decir, la dosis de radiación máxima en cualquier punto de la piel del paciente5 En general, la dosis cutánea de radiación suele evaluarse utilizando métodos indirectos a través de la determinación del producto dosis-área (PDA). Previamente, los métodos directos han sido laboriosos o de coste elevado, y, como consecuencia, la mayoría de los estudios que describen la exposición de los pacientes a la radiación durante intervenciones endovasculares utilizan una metodología indirecta para efectuar las determinaciones6,7. Los métodos directos son superiores a los indirectos porque son mucho más precisos y exactos en la cuantificación de la DCP8. En el presente estudio tratamos de usar determinaciones tanto directas como indirectas para evaluar la dosis cutánea de radiación recibida por el paciente durante la reparación endovascular estándar de un AAA.
MétodosEl estudio se efectuó como un proceso de mejora de la calidad en el Nebraska Medical Center juntamente con el Nebraska/Western Iowa Veterans Administration Hospital. Durante un período de 3 meses, monitorizamos la exposición a la radiación cutánea en una serie de 12 pacientes consecutivos sometidos a reparación endovascular estándar de un AAA. En todos los pacientes se implantó una endoprótesis bifurcada modular a través de un abordaje abierto en la arteria femoral con una de dos endoprótesis disponibles comercialmente (Zenith AAA Endograft de Cook, Bloomington, IN; Gore Excluder AAA Endograft de W. L. Gore, Flagstaff, AZ) para la corrección de un aneurisma aórtico infrarrenal. Tres cirujanos vasculares certificados, junto con un residente jefe de cirugía general, efectuaron las técnicas quirúrgicas estándar, incluida la exposición abierta bilateral de la arteria femoral común. Los procedimientos se efectuaron en el quirófano con un equipo OEC 9800 con un intensificador de imágenes de 30cm (GE Medical Systems, Waukesha, WI) y una mesa de fibra de carbono con un tablero monitorizado de cuatro vías (Allegro 6800 Mobile Imaging Table; Orthopedic Systems, Union City, CA). Las imágenes se obtuvieron en modo fluoroscópico estándar sin usar fluoroscopia pulsada o dosis bajas. La tasa máxima de fotogramas de cinefluoroscopia fue de 15 por segundo. Todos los datos se obtuvieron prospectivamente.
Medición de la dosis cutáneaLas determinaciones indirectas de la dosis de radiación incluyeron el tiempo de fluoroscopia total y el PDA, que se registró mediante el equipo de fluoscopia durante cada procedimiento utilizando un programa estadístico estándar. La medición directa de la DCP o dosis máxima de radiación administrada a la piel del paciente se registró utilizando una película de dosimetría radiográfica GAFCHROMIC® XR-RV2 (International Specialty Products, Wayne, NJ). Es una película sensible a la radiación con autorrevelado, utilizada para el control de calidad y la medición dosimétrica durante los procedimientos fluoroscópicos. La película, que mide 43 x 35 cm, se coloca inmediatamente debajo del paciente a nivel del abdomen y la pelvis, y, por lo tanto, abarca todo el campo de visión y elimina los efectos de orientación. Antes de la exposición a la radiación, es de color amarillo opaco y revela un color azul, cuya intensidad es proporcional a la exposición a la radiación (fig. 1). Acto seguido, la dosis de radiación se cuantifica con un densitómetro óptico que se ha calibrado utilizando la película expuesta a una dosis de radiación conocida. La película GAFCHROMIC es capaz de medir dosis de radiación de 1 cGy-50 Gy y tiene una variación hoja a hoja<5%. Su coste es de 21 dólares por hoja.
Película GAFCHROMIC después de la reparación endovascular de una AAA. El GAFCHROMIC es una película sensible a la radiación, que se autorrevela, utilizada para medir y mapear la exposición de la piel del paciente a la radiación. La densidad de color de la película aumenta con la dosis de radiación. El área del centro corresponde al despliegue del cuerpo aórtico principal, observándose bilateralmente las regiones de despliegue del brazo ilíaco inferior. La DCP se observó cuando tuvo lugar una superposición entre campos.
Se calcularon los valores medios y las desviaciones estándar (DE) con un programa Excel (Microsoft, Redmond, WA). Se crearon diagramas de dispersión con Excel (Microsoft) y mediante el programa Sigmastat (Jandel, San Rafael, CA) se calcularon los correspondientes coeficientes de correlación de Pearson (valor r). Para comparar las diferencias entre grupos de pacientes obesos y no obesos se utilizaron pruebas t de Student. Se consideró significativo un valor de p≤0,05.
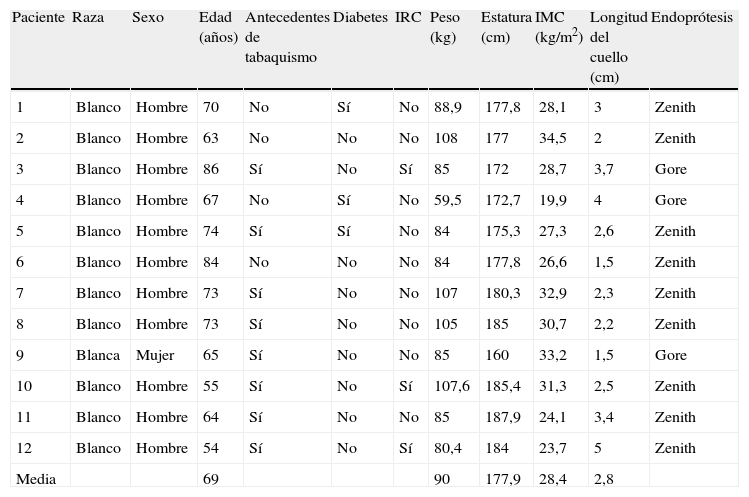
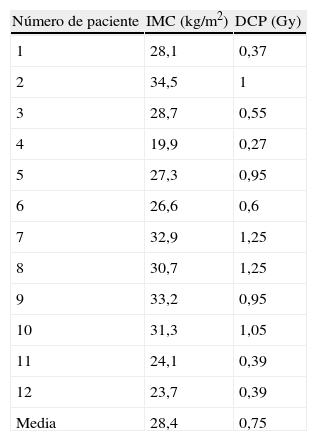
ResultadosDesde el 14 de mayo de 2007 al 22 de agosto de 2007, un total de 12 pacientes se sometieron a reparación endovascular estándar de un AAA. En la tabla I se muestra la información demográfica de la población de pacientes. Su edad media fue de 69 años (DE=9,9, límites 54-86), con un índice de masa corporal medio (IMC) de 28,4 (DE=4,4, límites 19,9-34,5). Sólo un paciente del estudio era de sexo femenino y el resto eran hombres. El tamaño medio del aneurisma era de 5,65cm (DE=1,05, límites 4,4-7,8), y la longitud media del cuello proximal era de 2,8cm (DE=1,06, límites 1,5-5). En todos los aneurismas se identificaron angulaciones de menos de 60 grados. Recibieron una endoprótesis Zenith nueve pacientes y tres, una endoprótesis Gore.
Demografía de los pacientes
| Paciente | Raza | Sexo | Edad (años) | Antecedentes de tabaquismo | Diabetes | IRC | Peso (kg) | Estatura (cm) | IMC (kg/m2) | Longitud del cuello (cm) | Endoprótesis |
| 1 | Blanco | Hombre | 70 | No | Sí | No | 88,9 | 177,8 | 28,1 | 3 | Zenith |
| 2 | Blanco | Hombre | 63 | No | No | No | 108 | 177 | 34,5 | 2 | Zenith |
| 3 | Blanco | Hombre | 86 | Sí | No | Sí | 85 | 172 | 28,7 | 3,7 | Gore |
| 4 | Blanco | Hombre | 67 | No | Sí | No | 59,5 | 172,7 | 19,9 | 4 | Gore |
| 5 | Blanco | Hombre | 74 | Sí | Sí | No | 84 | 175,3 | 27,3 | 2,6 | Zenith |
| 6 | Blanco | Hombre | 84 | No | No | No | 84 | 177,8 | 26,6 | 1,5 | Zenith |
| 7 | Blanco | Hombre | 73 | Sí | No | No | 107 | 180,3 | 32,9 | 2,3 | Zenith |
| 8 | Blanco | Hombre | 73 | Sí | No | No | 105 | 185 | 30,7 | 2,2 | Zenith |
| 9 | Blanca | Mujer | 65 | Sí | No | No | 85 | 160 | 33,2 | 1,5 | Gore |
| 10 | Blanco | Hombre | 55 | Sí | No | Sí | 107,6 | 185,4 | 31,3 | 2,5 | Zenith |
| 11 | Blanco | Hombre | 64 | Sí | No | No | 85 | 187,9 | 24,1 | 3,4 | Zenith |
| 12 | Blanco | Hombre | 54 | Sí | No | Sí | 80,4 | 184 | 23,7 | 5 | Zenith |
| Media | 69 | 90 | 177,9 | 28,4 | 2,8 |
IMC: índice de masa corporal.
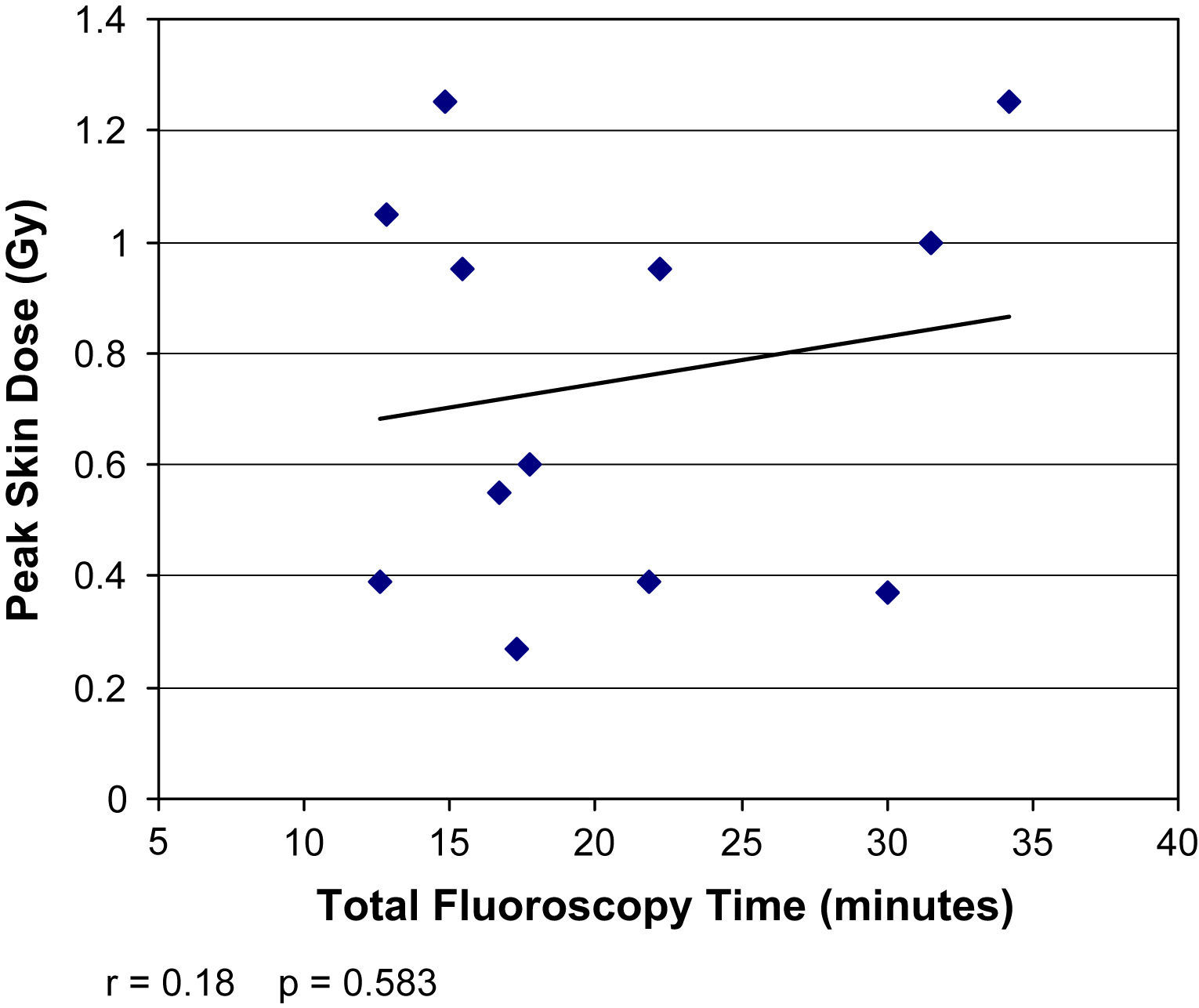
El tiempo medio de fluoroscopia total fue de 20,6 min (DE=7,5, límites 12,6-34,2). Durante el 92% del tiempo total de obtención de imágenes se utilizó fluoroscopia estándar y durante el 8% restante, cinefluoroscopia. Para el 49% del tiempo de fluoroscopia se usó un campo de visión normal y una visión aumentada para el 51%.
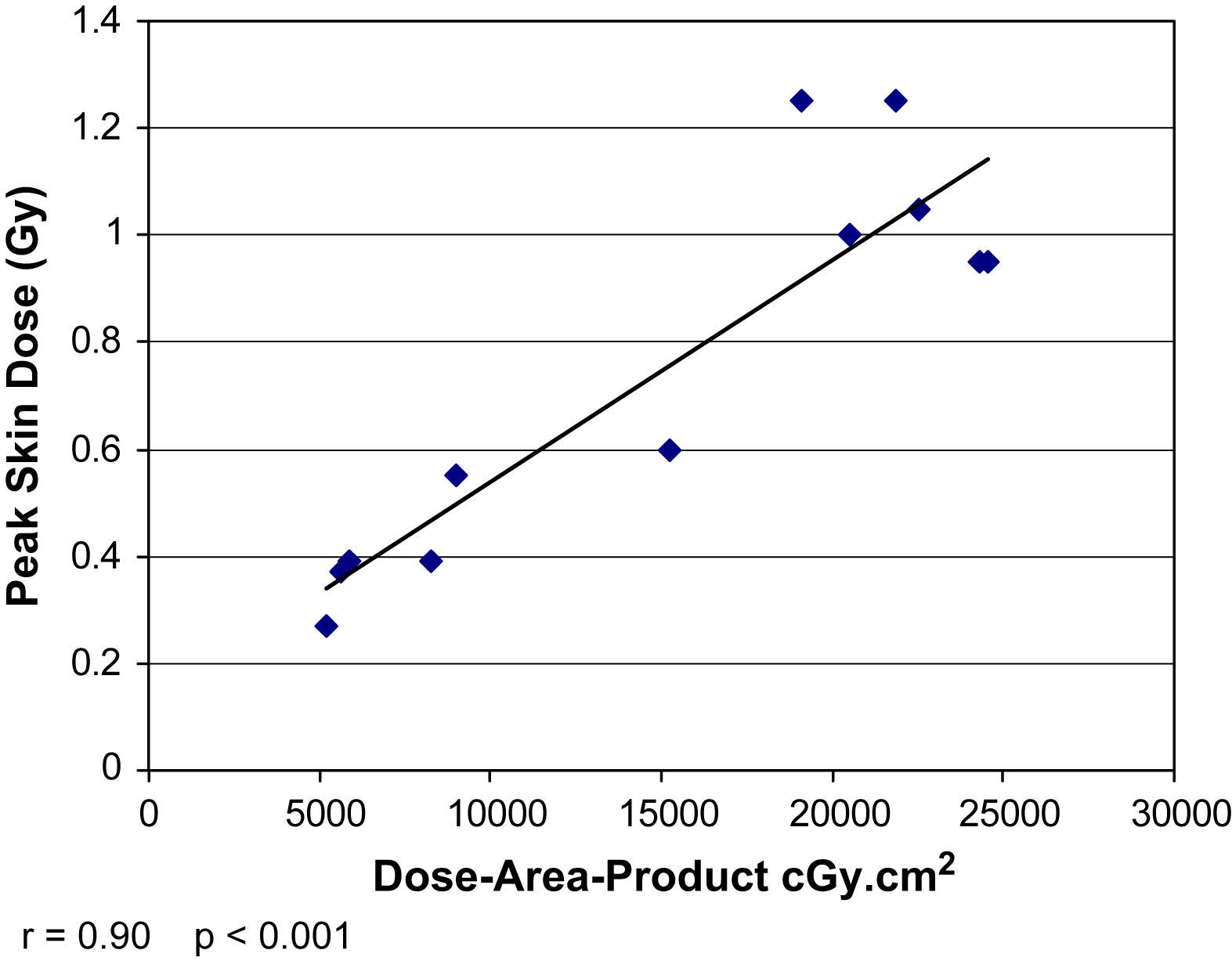
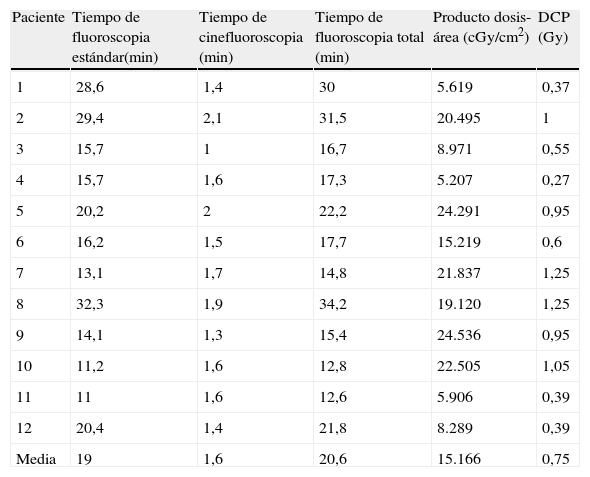
En la tabla II se muestran las mediciones de la dosis de radiación cutánea. La DCP para todos los pacientes fue de 0,75 Gy (DE=0,36, límites 0,27-1,25), y la DCP entre todos los pacientes fue de 1,25Gy. El PDA medio fue de 15.166 cGy/cm2 (DE=7.835, límites 5.207-24.536).
Tiempo de fluoroscopia y dosis de radiación
| Paciente | Tiempo de fluoroscopia estándar(min) | Tiempo de cinefluoroscopia (min) | Tiempo de fluoroscopia total (min) | Producto dosis-área (cGy/cm2) | DCP (Gy) |
| 1 | 28,6 | 1,4 | 30 | 5.619 | 0,37 |
| 2 | 29,4 | 2,1 | 31,5 | 20.495 | 1 |
| 3 | 15,7 | 1 | 16,7 | 8.971 | 0,55 |
| 4 | 15,7 | 1,6 | 17,3 | 5.207 | 0,27 |
| 5 | 20,2 | 2 | 22,2 | 24.291 | 0,95 |
| 6 | 16,2 | 1,5 | 17,7 | 15.219 | 0,6 |
| 7 | 13,1 | 1,7 | 14,8 | 21.837 | 1,25 |
| 8 | 32,3 | 1,9 | 34,2 | 19.120 | 1,25 |
| 9 | 14,1 | 1,3 | 15,4 | 24.536 | 0,95 |
| 10 | 11,2 | 1,6 | 12,8 | 22.505 | 1,05 |
| 11 | 11 | 1,6 | 12,6 | 5.906 | 0,39 |
| 12 | 20,4 | 1,4 | 21,8 | 8.289 | 0,39 |
| Media | 19 | 1,6 | 20,6 | 15.166 | 0,75 |
DCP: dosis cutánea pico.
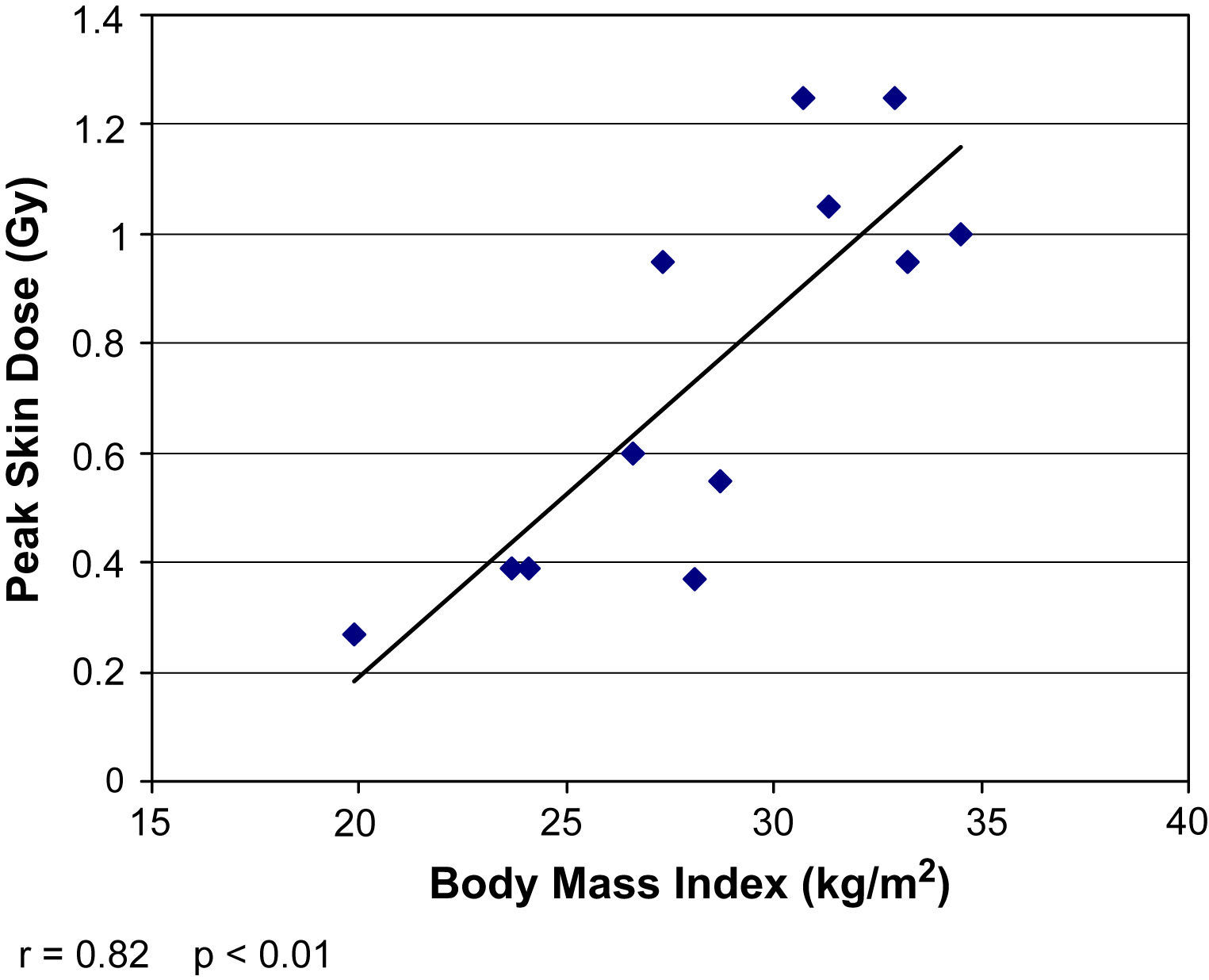
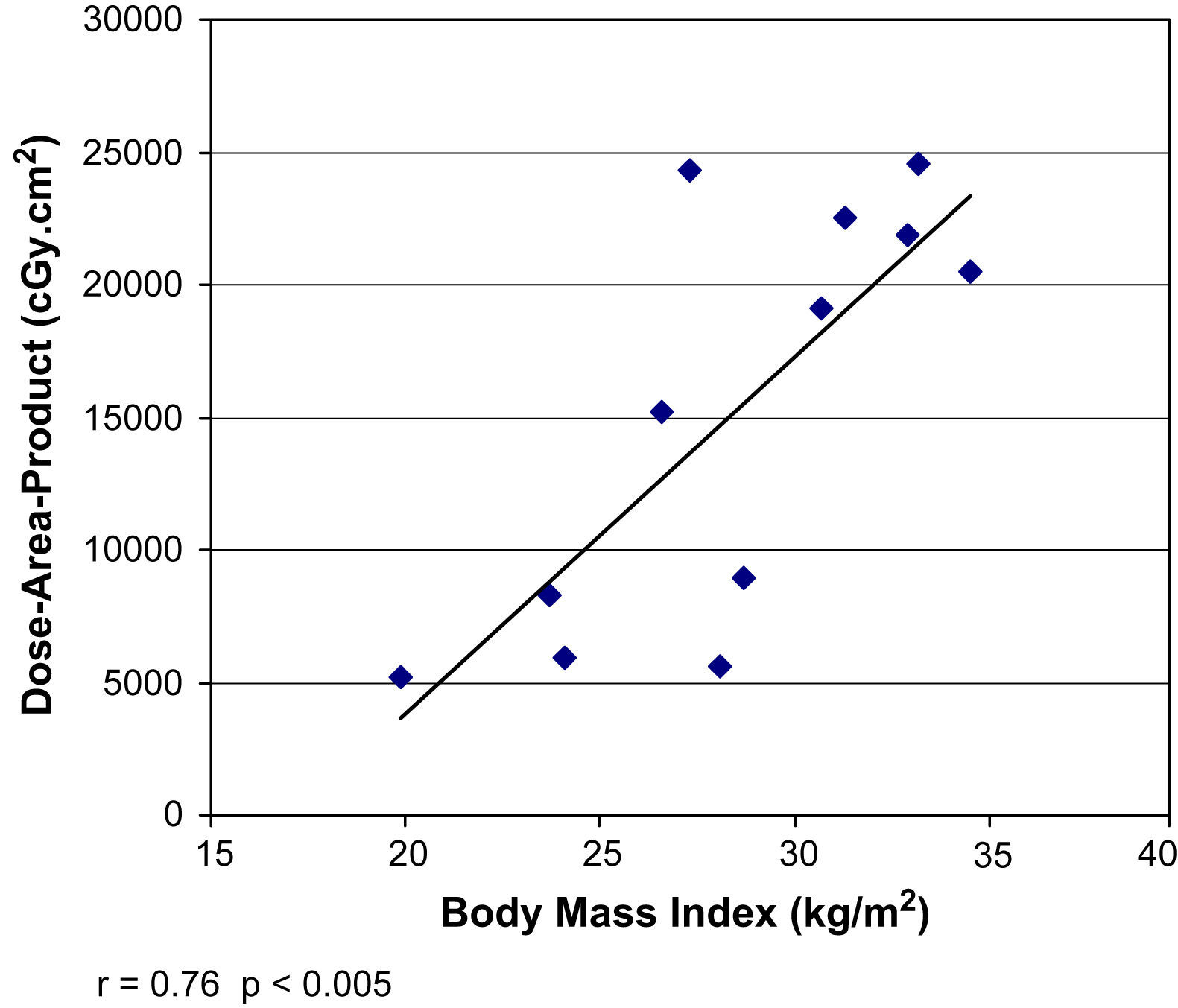
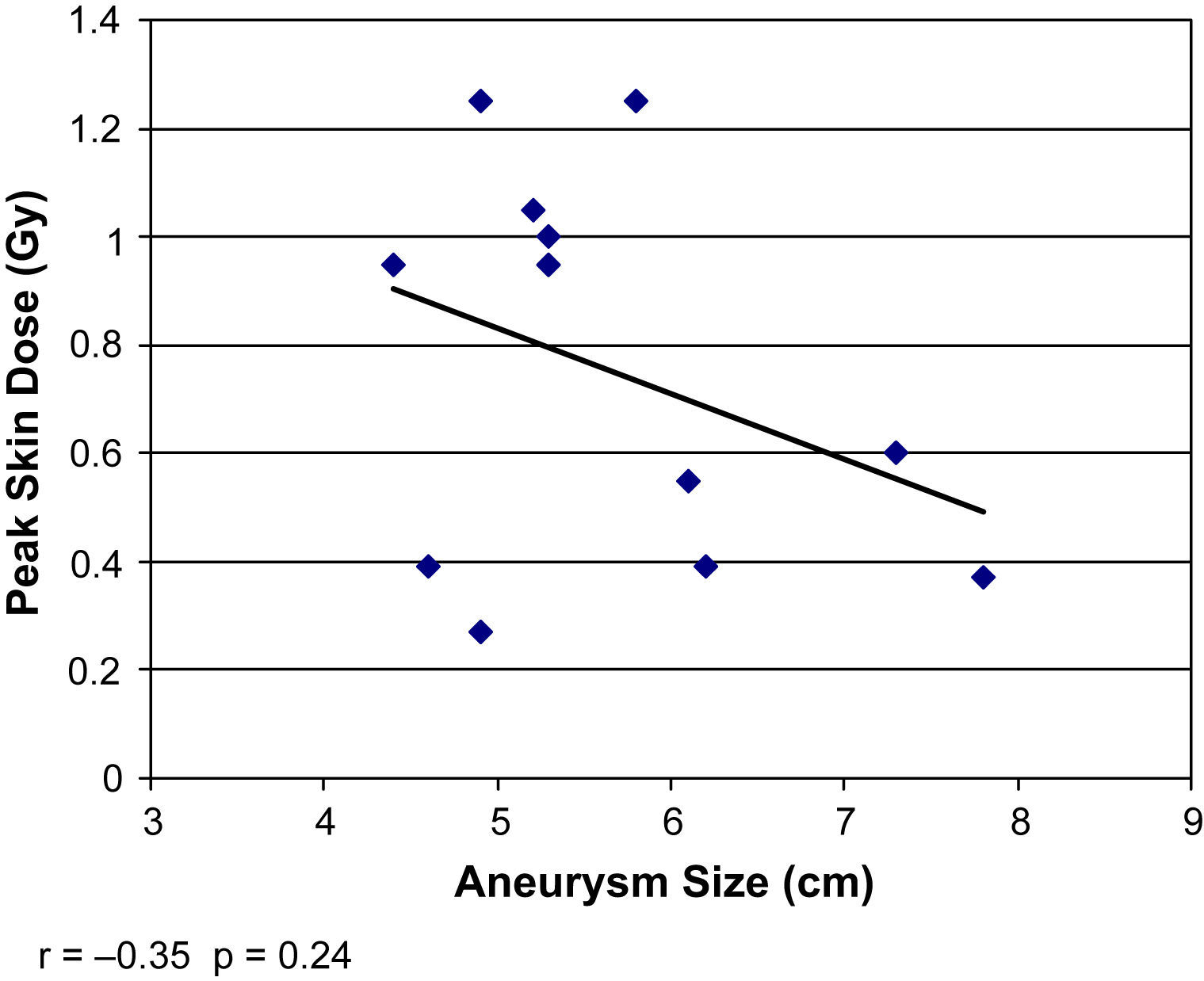
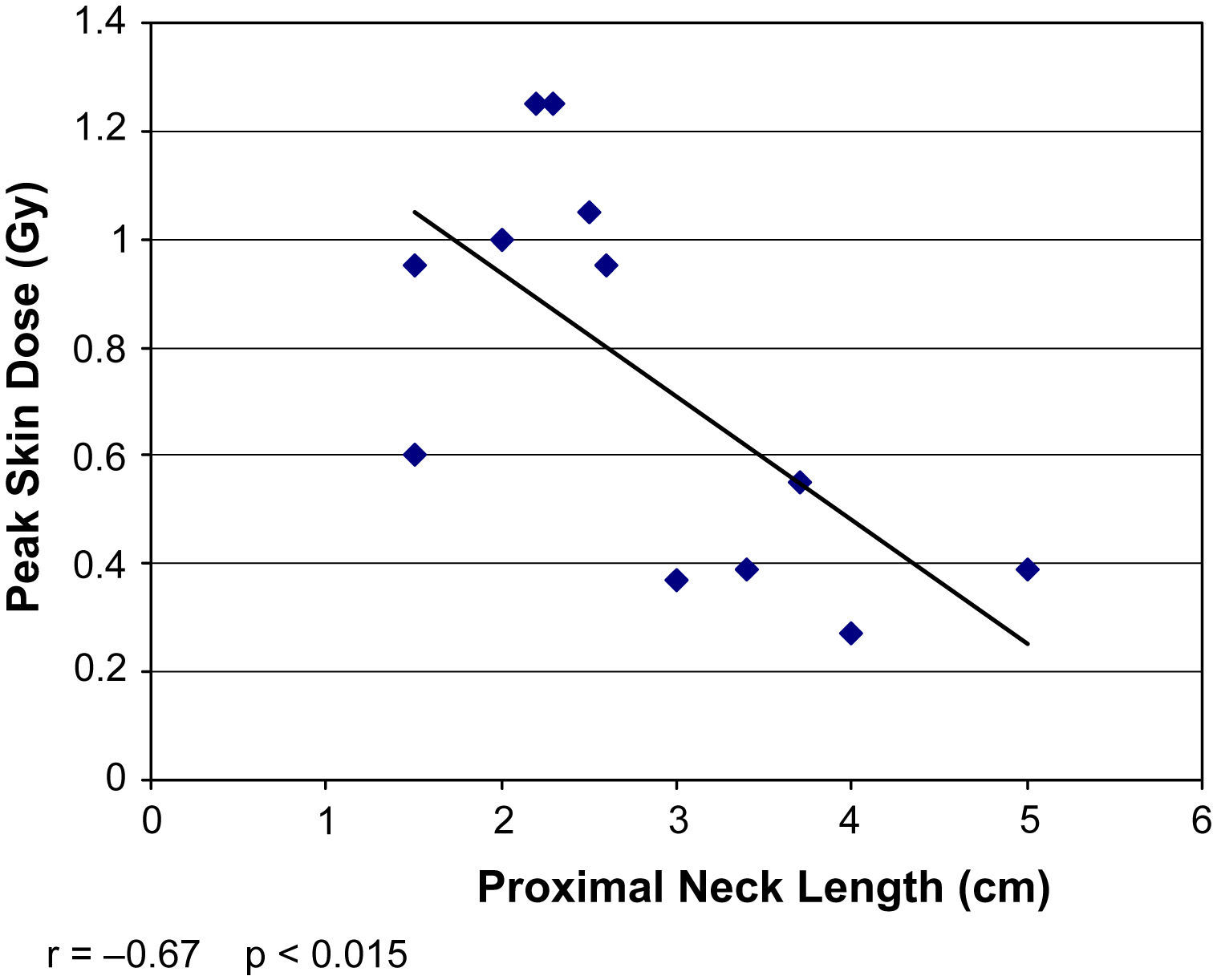
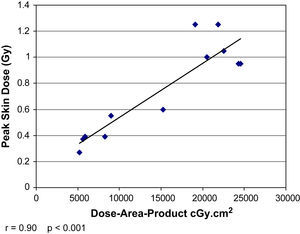
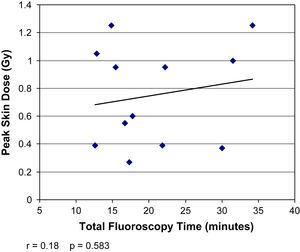
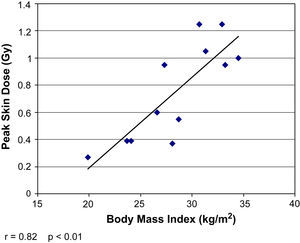
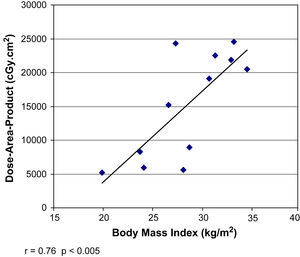
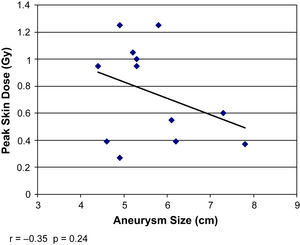
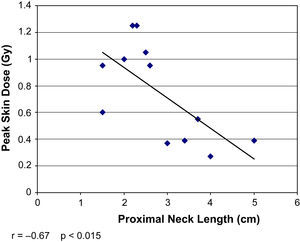
La DCP directa se correlacionó con la medición indirecta del PDA (r=0,9, p<0,001) pero no con el tiempo de fluoroscopia total (r=0,18, p=0,58) (figs. 2 y 3). La DCP también se correlacionó con el IMC (r=0,82, p<0,01) (tabla III, figs. 4 y 5). La DCP media de pacientes obesos (IMC>30) fue significativamente mayor comparado con la de aquellos no obesos (1,1 comparado con 0,5 Gy, p<0,001). La DCP no se correlacionó con el tamaño del aneurisma (r = –0,35, p=0,24) pero se observó una correlación negativa con la longitud del cuello (r = –0,67, p<0,015) (figs. 6 y 7).
Con la complejidad cada vez mayor de los procedimientos endovasculares, ha aumentado la preocupación relativa a la exposición de paciente y médico a la radiación. Los estudios previos han medido la exposición del paciente a la radiación durante procedimientos endovasculares seleccionados, pero no se han documentado mediciones precisas de la exposición a la radiación durante la reparación endovascular de los AAA. El presente estudio se emprendió como parte de un proyecto de mejora de la calidad para garantizar niveles aceptables de exposición del paciente a la radiación durante los procedimientos fluoroscópicos prolongados.
Para estimar la dosis pico de radiación distribuida a la piel pueden usarse diversos métodos. Los métodos dosimétricos indirectos incluyen el tiempo de fluoroscopia y el producto dosis-área4. El tiempo de fluoroscopia no proporciona información sobre la tasa de la dosis y, por lo tanto, se considera insuficiente para determinar con precisión la dosis recibida por el paciente4. El PDA se define como la radiación absorbida en el aire multiplicada por el área transversal del haz de rayos X2. El PDA se mide colocando una cámara de ionización (lo suficientemente ancha para interceptar por completo el haz de rayos X) justo por debajo de los colimadores de los rayos X y es una medida global de la energía de radiación total aplicada al paciente4,9. El PDA no proporciona información sobre la distribución espacial de la dosis de radiación y, por lo tanto, con frecuencia, es una medida insuficiente de la DCP y del riesgo de lesión de la piel8. Además, el PDA pasa por alto el efecto de la retrodispersión a partir del paciente, que puede aumentar la dosis cutánea en un 10-40%4. Las mediciones indirectas pueden usarse para estimar la dosis cutánea que recibe el paciente pero no determinan con precisión la DCP6. En comparación con las determinaciones indirectas, las directas pueden proporcionar mediciones precisas de la dosis cutánea8. Previamente, se ha medido directamente la DCP o dosis de radiación máxima en cualquier punto concreto de la piel del paciente mediante diversas técnicas que, aunque precisas, son laboriosas y de difícil aplicación en la práctica clínica6. Recientemente, en nuestro hospital se utilizó una película disponible comercialmente para la medición directa de la DCP. La película GAFCHROMIC es sensible a la radiación, se autorrevela y se utiliza para el control de la calidad y la medición dosimétrica durante los procedimientos fluoroscópicos. La película mide 43 x 35 cm, cubre todo el campo de visión y elimina los efectos de orientación. Antes de la exposición a la radiación es de color amarillo y se revela en color azul, cuya intensidad es proporcional a la DCP (fig. 1). Acto seguido, la dosis de radiación se cuantifica con un densitómetro óptico que se ha calibrado utilizando una película expuesta a una dosis conocida de radiación. Mediante la utilización de la medición simple y directa de la DCP con esta película, pudimos confirmar rápidamente la falta de riesgos de la reparación endovascular de los AAA con respecto a la DCP.
El presente estudio, que usó mediciones directas y precisas, demuestra que la reparación endovascular de estas lesiones da lugar a niveles de DCP muy por debajo del umbral de 2 Gy para lesión cutánea10,11. En los 12 pacientes estudiados la DCP máxima fue de 1,25 Gy. A pesar de los tiempos más altos de fluoroscopia, estos bajos valores pueden atribuirse a la dispersión del campo de visión en la cavidad abdominal comparado con otros procedimientos intervencionistas documentados, donde se requiere una visión enfocada y aumentada. Aunque el presente estudio demostró una baja DCP en los pacientes, a partir de los estudios previos, está claro que los casos complejos de reparación endovascular pueden dar lugar fácilmente a valores superiores a la dosis umbral de una lesión cutánea. Miller et al6 efectuaron un estudio observacional sobre la dosis de radiación distribuida al paciente durante 21 procedimientos radiológicos intervencionistas habituales. La DCP se calculó indirectamente con un programa de cartografía de la dosis cutánea. Excepto la nefrostomía, angiografía pulmonar e implantación de un filtro en la vena cava inferior, en los 21 procedimientos evaluados se obtuvieron DCP>2 Gy. En el 14% de las angioplastias ilíacas con la implantación de un stent los valores fueron mayores de 2 Gy. Debido a la propensión de los procedimientos endovasculares complejos a dar lugar a dosis cutáneas elevadas de radiación recibida por el paciente, los cirujanos vasculares deben ser concienzudos con el uso de la fluoroscopia, a pesar de los hallazgos obtenidos en el presente estudio.
En esta investigación, la DCP se correlacionó potentemente con el PDA (r=0,90) pero no con el tiempo de fluoroscopia (r=0,18). Esto coincide con los hallazgos del Radiation Dose in Interventional Radiology Procedures Study, en el que también se describió una potente correlación entre la DCP y el PDA (r=0,85), a pesar de una amplia variación entre los casos6. Fletcher et al1 también describieron una correlación significativa entre la DCP y el PDA en diversos procedimientos radiológicos intervencionistas, observándose la correlación más precisa para la implantación de un puerto (r=0,94) y la menor (aunque siguió siendo significativa) para una aortografía con runoff (r=0,6). En función de los resultados del presente estudio y de los estudios previos publicados, aunque no es ideal, probablemente el producto dosis-área es una estimación en tiempo real adecuada de la DCP para el cirujano vascular en ejercicio. Sin embargo, está claro que el tiempo de fluoroscopia total es una variable pronóstica inadecuada de la DCP, ya que los datos del presente estudio no demostraron una correlación entre ambos parámetros. La razón de esto probablemente es que el tiempo de fluoroscopia no tiene en cuenta la variabilidad de la tasa de dosis debida al hábito corporal del paciente o a la técnica. Además, el tiempo de fluoroscopia no proporciona información sobre el tamaño del campo de rayos X, el área corporal irradiada, la posición, el aumento, cinefluoroscopia o distancia de la piel, todos los cuales son importantes determinantes de la dosis de radiación distribuida1,4,6. Por lo tanto, cuando se evalúa la radiación recibida por el paciente, más que en el tiempo de fluoroscopia total, es preciso basar la determinación en otros parámetros.
En el presente estudio, la DCP se correlacionó potentemente con el IMC del paciente. La correlación no es sorprendente si se considera que la obesidad es habitual entre pacientes con lesiones cutáneas inducidas por la radiacion3,12. La fluoroscopia utiliza una radiación de rayos X de baja energía, atenuada rápidamente a medida que atraviesan el tejido3. En pacientes obesos, el haz de rayos X debe penetrar en una mayor extensión de tejido para alcanzar el detector de la imagen2,13. El control de exposición automática presente en los equipos móviles aumenta la tasa de dosis para incrementar la penetración del haz de rayos X. Un fotodiodo detecta la baja emisión de luz por el intensificador de la imagen y produce una señal de respuesta para incrementar la dosis de radiación hasta obtener la penetración suficiente para producir una imagen lo suficientemente luminosa14. En nuestra serie, los pacientes obesos recibieron PDA y DCP 2-3 veces mayores que los pacientes con un IMC dentro de límites normales. En Estados Unidos, con una prevalencia de obesidad>30%, y en otros muchos países de todo el mundo, donde también está aumentando rápidamente, cuando se planifiquen procedimientos endovasculares en pacientes obesos, siempre debe tenerse en cuenta una exposición elevada a la radiación15. Es preciso tratar de reducir la exposición a la radiación con el uso de colimadores, fluoroscopia pulsada y un tiempo de fluoroscopia reducido al mínimo16.
En comparación con la exposición del paciente a la radiación, Lipsitz et al7 y Ho et al17 han examinado la exposición del cirujano durante la reparación endovascular de AAA. En estos estudios se encontró que la dosis de radiación acumulada recibida por el cirujano es muy inferior al límite profesional anual máximo recomendado por la International Commission of Radiation Protection (ICRP). Ho et al17 determinaron las dosis de radiación efectiva, anual corporal, ocular y de las manos para cirujanos vasculares que efectuaban correcciones estándar aórticas, aortografías y angioplastia transluminal percutánea e implantación de stents. La dosis efectiva anual mediana recibida por los cirujanos fue del orden del 1% de la exposición máxima anual de radiación profesional, recomendada por la ICRP. Para las reparaciones aórticas endovasculares se detectó la mayor exposición, pero un cirujano vascular tendría que practicar 2.597 reparaciones aórticas endovasculares para alcanzar el límite de dosis anual17. Aunque estos informes sugieren que la lesión de radiación del cirujano debe ser mínima, siguen estando presentes los efectos estocásticos de la radiación; por lo tanto, los cirujanos deben adherirse a una estrategia de “lo más baja que sea razonablemente alcanzable”. Los estudios mencionados previamente también abordaban la DCP recibida por el paciente durante las intervenciones endovasculares para AAA, aunque de manera relativamente limitada. Ho et al17 midieron la dosis cutánea recibida por el paciente adhiriendo un minidosímetro termoluminiscente (3 mm2 x 1 mm) en un punto predeterminado de la piel del paciente donde predijeron que se localizaría la exposición máxima. La dosis superficial media recibida por el paciente fue de 0,0127 Gy, muy por debajo de la detectada en el presente estudio. Lamentablemente, esta metodología no es precisa para la predicción de la DCP18. Lipsitz et al7 no midieron la DCP pero calcularon la dosis de entrada recibida por el paciente utilizando la energía y las posiciones fluoroscópicas registradas durante el procedimiento (media 0,36 Gy, límites 0,12-0,86). Al igual que en el estudio de Ho et al17, los niveles de DCP fueron bajos, en comparación con los obtenidos en el presente estudio, de nuevo, probablemente como consecuencia de la técnica de determinación.
En último término, el cirujano vascular debe tener en cuenta los efectos deterministas y estocásticos de la radiación para sus pacientes7. Los efectos deterministas son los que se producen cuando se supera una dosis de radiación umbral. La lesión cutánea inducida por la radiación es un ejemplo de efecto determinista, en el que la mayor probabilidad y gravedad de la lesión se correlacionan con una dosis de radiación cada vez mayor10. La lesión cutánea inducida por la radiación varía desde un eritema a la necrosis11. La primera indicación de esta lesión es un eritema transitorio. Éste se presenta al cabo de horas de la exposición a la radiación y se resuelve en alrededor de 48 h10,11. La DCP umbral para el eritema es de 2 Gy10,11. Es preciso tener en cuenta los factores del paciente, como la diabetes o una conectivopatía, ya que pueden dar lugar a una mayor sensibilidad a la radiación10. La incidencia de lesión por radiación es insignificante comparado con el número de procedimientos en los que se usa fluoroscopia. Sin embargo, desde 1990, se han descrito cientos de casos de dermatitis inducida por la fluoroscopia, incluidos numerosos casos de necrosis dérmica19. Auque la incidencia es reducida, cuando se produce una lesión cutánea, puede ser grave. En una revisión de 73 casos de lesión cutánea inducida por la radiación, hubo 38 lesiones graves, como ulceración crónica y necrosis, y 18 casos que requirieron injertos de piel3,10. De estos 73 casos descritos, 59 correspondieron a procedimientos cardíacos, siete fueron implantaciones de un cortocircuito portosistémico intrahepático transyugular (CPSIT), tres correspondieron a intervenciones neurorradiológicas, y cuatro fueron otros procedimientos en el abdomen y el tórax, incluidas dos angioplastias renales3,10. En comparación con la lesión cutánea, el cáncer inducido por la radiación es un efecto estocástico en el que no hay un valor umbral y la gravedad es independiente de la dosis. La probabilidad de incidencia de cáncer aumenta con la dosis, pero éste puede desarrollarse con cualquiera7,10. Cuando se pone en perspectiva el presente estudio, es importante una distinción entre los efectos deterministas y los estocásticos. Los datos del presente estudio demuestran que los pacientes sometidos a la corrección de un AAA reciben una exposición mínima a la radiación durante el procedimiento con respecto a la lesión cutánea determinista. Sin embargo, los pacientes sometidos a esta corrección requieren estudios múltiples de evaluación, tratamiento y seguimiento radiológico y es preciso considerar su mayor riesgo de efectos estocásticos. Se supone la existencia de una relación dosis-respuesta lineal entre la dosis de radiación y el cáncer y, a medida que aumenta la dosis recibida por el paciente con los años de vigilancia, aumenta su riesgo de cáncer20. Tras la reparación endovascular de los AAA, con frecuencia, los pacientes son seguidos con exámenes tomográficos computarizados (TC) a los 3, 6 y 12 meses y, acto seguido, con carácter anual. En función de una estimación conservadora de una dosis efectiva de 10 mSv por TC del abdomen y la pelvis21,22, los pacientes pueden recibir 40 mSv en el primer año sólo a partir de las TC. Recientemente, Brenner y Hall23 utilizaron el aumento de la incidencia de cáncer en los supervivientes de la bomba atómica para estimar el riesgo de cáncer asociado a la TC. En un subgrupo de supervivientes que recibieron una dosis máxima de 150 mSv, con una media de 40 mSv, se identificó un aumento significativo del riesgo de cáncer. Brenner y Hall23 estimaron un aumento del riesgo de cáncer del 0,01-0,02% en los expuestos a la radiación de una sola TC en la década de los 30 años o a una edad mayor. El riesgo de cáncer para el individuo es bajo, pero, dado que cada año se realizan alrededor de 62 millones de TC, el 1,5-2% de todos los diagnosticados podrían atribuirse en último término a esta técnica por la imagen. Se podría argumentar que nuestros pacientes son de edad avanzada y que la probabilidad de desarrollar cáncer que dé lugar a la muerte es baja. Sin embargo, está claro que suscita una preocupación cada vez mayor el uso de TC repetitivas y que es preciso tener en cuenta la cantidad total de exposición a la radiación a la que un paciente con AAA se someterá con el tiempo.
En conclusión, la reparación endovascular de los AAA mediante técnicas fluoroscópicas estándar se traduce en una dosis cutánea pico que está muy por debajo del nivel que induce una lesión de la piel. En función de la experiencia actual, las determinaciones directas de la dosis distribuida a la piel se realizan fácilmente con la película GAFCHROMIC, pero, debido al coste y a la necesidad de determinaciones en tiempo real, utilizando instrumental fluoroscópico, el PDA es una estimación que se obtiene fácilmente y es razonable para determinar la dosis recibida por el paciente. Se requiere precaución para limitar la exposición del paciente y el médico a la radiación, en particular en pacientes obesos. Por último, en pacientes que reciben procedimientos endovasculares es necesaria una consideración sobre la dosis global de radiación ya que requieren un seguimiento a largo plazo con TC repetidas.