El objetivo del presente estudio fue identificar las variables pronósticas preoperatorias e intraoperatorias de mortalidad inmediata, lesión de la médula espinal o isquemia intestinal aguda después de la corrección de aneurismas toracoabdominales tipo IV (ATA IV) como base para optimizar las indicaciones y técnicas quirúrgicas. Desde enero de 1991 hasta junio de 2006, operamos a 171 pacientes portadores de ATA IV. Esta serie incluyó a 149 hombres (87,1%) y 22 mujeres (12,9%), con una edad media de 65,0±10,9 años (límites 23-82). La etiología subyacente fue enfermedad aneurismática degenerativa en 143 pacientes (83,6%). Se sometieron a una intervención quirúrgica con carácter urgente 22 (12,8%) pacientes. Las comorbilidades incluyeron coronariopatía en 72 casos (45,6%), incluidos 39 que se sometieron a un procedimiento de revascularización coronaria, hipertensión arterial en 121 (70,1%), enfermedad pulmonar obstructiva crónica en 81 (47,4%) e insuficiencia renal crónica en 58 (33,9%). Presentaban lesiones concurrentes que afectaban, como mínimo, a una arteria visceral 76 (44,4%) pacientes. Se efectuó arteriografía de médula espinal en 91 pacientes (53,2%). En 25 casos (27,5%) los hallazgos arteriográficos demostraron la necesidad de revascularización de la arteria de Adamkiewicz debido a la localización del ostium a nivel de T12 o por debajo de ésta. La corrección se llevó a cabo con clampaje directo en 160 casos (93,6%). En 11 pacientes (6,4%) se utilizó bypass cardiopulmonar parcial. En el postoperatorio falleció un total de 23 pacientes (13,4%). La causa de la muerte fue una isquemia intestinal aguda en nueve casos, insuficiencia multiorgánica en siete, trastorno de la coagulación en tres, complicaciones cardíacas en dos e ictus en dos. La lesión de la médula espinal afectó a ocho pacientes (4,7%) incluidos dos que fallecieron. De acuerdo con el análisis univariado, las variables pronósticas de muerte inmediata fueron una edad mayor de 70 años, enfermedad aneurismática degenerativa, coronariopatía, insuficiencia renal crónica o lesiones de arterias viscerales, cirujano, duración de la isquemia intestinal, y uso de una técnica quirúrgica “compleja”. A pesar de que la única variable pronóstica significativa de lesión de médula espinal fue la isquemia digestiva, se observó una tendencia casi significativa (p<0,1) para la coronariopatía, bypass coronario previo e insuficiencia renal. Las variables pronósticas significativas de isquemia intestinal aguda fueron la insuficiencia renal y las lesiones de arterias viscerales, aunque la coronariopatía y el bypass coronario previo fueron casi significativos (p=0,06). La frecuente asociación de los ATA IV con enfermedad aterosclerótica en pacientes de edad avanzada que se presentan con coronariopatía e insuficiencia renal crónica explica en parte la razón de que la mortalidad postoperatoria precoz siga siendo alta. La incidencia de lesión de la médula espinal sugiere que la arteriografía preoperatoria de aquélla es obligatoria para su prevención. La frecuencia de isquemia intestinal es más problemática, pero una mayor comprensión del mecanismo subyacente debería permitir el desarrollo de estrategias preventivas.
El aneurisma toracoabdominal de tipo IV (ATA IV) de Crawford1 se considera una lesión cuya corrección entraña un número relativamente menor de riesgos por lo que respecta tanto a la mortalidad postoperatoria como a la lesión de la médula espinal. Una de las razones es que estas lesiones no son aneurismas toracoabdominales en el sentido estricto del término sino que afectan a toda la aorta abdominal, incluida la visceral. Otra razón es que la corrección suele requerir técnicas quirúrgicas relativamente simples sin la necesidad de perfusión distal. Por otra parte, el origen de la arteria de Adamkiewicz casi siempre se localiza proximal al límite superior del aneurisma. El objetivo del presente estudio fue determinar si la reputación de ausencia de riesgos de la corrección de ATA IV está justificada. Con este objetivo, evaluamos las variables pronósticas preoperatorias y postoperatorias de complicaciones por medio de la revisión de las historias clínicas de todos los pacientes tratados para ATA IV entre enero de 1991 y junio de 2006 en la Unidad de Cirugía Vascular del Hôpital Universitaire Pitié-Salpêtrière de París, Francia.
Pacientes y MétodosDesde enero de 1991 hasta junio de 2006, 171 pacientes se sometieron a la corrección quirúrgica de un ATA IV en la Unidad de Cirugía Vascular del Hôpital Universitaire Pitié-Salpêtrière. Hubo 149 hombres (87,1%) y 22 mujeres (12,9%) con una edad media de 65,0±10,9 años (límites 23-82, mediana=66). Eran mayores de 70 años 59 pacientes (34,5%). Las comorbilidades principales incluyeron coronariopatía en 78 pacientes (45,6%), hipertensión arterial en 121 (70,0%), enfermedad pulmonar obstructiva crónica en 81 (47,4%), insuficiencia renal (creatinina>120 μmol/l) en 58 (29,5%) incluidos cuatro que requerían hemodiálisis, y diabetes en 13 (7,6%). La etiología subyacente de la formación aneurismática fue una enfermedad degenerativa en 143 pacientes (83,6%). Otras etiologías observadas en 26 pacientes (16,4%) incluyeron enfermedad de Takayasu en nueve, disección en cinco, infección en cinco, enfermedad de Behçet en cuatro, síndrome de Marfan en dos, traumatismo postoperatorio en dos y policondritis recidivante en uno. La corrección se llevó a cabo con carácter electivo en 149 (87,2%) y con carácter de urgencia (al cabo de 24 h del ingreso) en 22 casos (12,9%).
Excepto para los casos urgentes en los que, para la mayoría, sólo pudo efectuarse tomografía computarizada (TC), en el resto se procedió a una evaluación vascular completa, incluidas visiones aortográficas anterior y lateral de la aorta toracoabdominal, angiogammagrafía de la aorta y ecografía de los troncos supraaórticos. En pacientes que presentaron síntomas clínicos de isquemia miocárdica y/o resultados positivos de una prueba de esfuerzo (gammagrafía miocárdica o, con más frecuencia, ecocardiografía con inyección de dobutamina) se efectuó coronariografía2.
Se habían sometido a procedimientos de revascularización miocárdica 39 pacientes (22,8%), 21 (12,3%) antes de la evaluación preoperatoria, incluido bypass aortocoronario en 14 y dilatación con balón, con o sin implantación de un stent, o inmediatamente después de aquélla en 18, incluido bypass aortocoronario en cinco y dilatación con balón, con o sin implantación de un stent, en 13.
Se habían sometido a endarterectomía carotídea 19 pacientes (11,1%), efectuada antes de la evaluación preoperatoria en nueve (5,3%) o después en 10 (inmmediatamente antes [n=5] o al mismo tiempo que la corrección del aneurisma). En 36 pacientes (21,1%) se efectuó corrección de la aorta proximal: aorta ascendente y/o cayado aórtico en cinco casos (2,9%), torácica descendente o toracoabdominal en siete (4,0%), y aorta abdominal infrarrenal en 24 (14,0%). De estos pacientes, tres ya se habían sometido a corrección de un ATA IV 3,9 y 15 años atrás y habían desarrollado una dilatación aneurismática (> 5cm de diámetro), que afectaba a la angioplastia con parche de la arteria visceral.
La afectación de la arteria visceral se detectó durante la evaluación preoperatoria en 76 pacientes (44,4%). La mayoría de las lesiones de la arteria visceral se clasificaron como oclusivas (estenosis>50%), pero también se observaron unas pocas lesiones aneurismáticas. Los antecedentes de nefrectomía o revascularización renal se contabilizaron como afectación de la arteria renal. Usando esta definición, 37 pacientes (21,6%) presentaban afectación aislada unilateral de la arteria renal, 10 (5,8%) afectación bilateral, 12 (7,0%) presentaban afectación aislada de una arteria intestinal y 17 (10,0%) afectación combinada de una arteria renal e intestinal. Se efectuó arteriografía de la médula espinal sin que acontecieran complicaciones en 91 pacientes (53,2%). De acuerdo con la clasificación de cuatro grupos basada en la localización del origen de la arteria de Adamkiewicz3, los pacientes se clasificaron en un grupo A (ostium de la arteria localizado por encima del nivel superior del clampaje aórtico) en 55 casos (60,4%), grupo C (arteria localizada a nivel del segmento clampado) en 25 (27,5%), y grupo D (el examen no permitió la localización de la arteria de Adamkiewicz) en 11 (12,1%). La arteriografía de la médula espinal no se efectuó en 80 pacientes por diversas razones: a saber, contraindicaciones relativas en 26 casos (15,2%) relacionada con el contexto de urgencia en 19, problemas de accesibilidad relacionada con la oclusión de los vasos iliofemorales en tres pacientes o contraindicaciones absolutas para la inyección de material de contraste como consecuencia de un mieloma en un caso e insuficiencia renal en otro. En la mayoría de los casos (54 pacientes, 31,6%), en especial en la segunda parte de la serie, la arteriografía de la médula espinal se omitió a propósito porque se consideró que el riesgo de que se produjeran complicaciones era bajo.
El procedimiento de corrección se efectuó con el paciente en posición de decúbito lateral derecho a través de una lumbotomía sobre la onceava costilla o, con más frecuencia, a través de una toracolumbotomía sobre la décima costilla en asociación con una frenotomía periférica corta para obtener la exposición. Cuando el aneurisma estuvo confinado a la aorta sin lesiones ilíacas asociadas, se efectuó un abordaje en línea recta a lo largo del borde externo del músculo recto anterior del abdomen que se dejó intacto excepto para el abordaje de la vaina. Este abordaje asociado al abordaje vertical del pilar diafragmático izquierdo fue suficiente para controlar la aorta supracelíaca, todo el lado izquierdo del aneurisma y la arteria ilíaca común izquierda. La derecha se controló intraluminalmente utilizando un catéter de Fogarty de calibre 4 o 5 después de abrirla. Si se requirió una intervención de las arterias ilíacas, el segmento abdominal del abordaje se extendió caudalmente en dirección pararrectal. Esta técnica asociada con la ligadura y sección de la arteria mesentérica inferior permitió el abordaje de la arteria ilíaca derecha por debajo del origen de su bifurcación. Si se requirió la exposición de la arteria ilíaca externa derecha, se abrió el peritoneo para permitir la exposición directa de la misma. En todos los pacientes se efectuó una disección retrorrenal excepto en tres que presentaban una vena renal retroaórtica izquierda y dos que se sometieron a tratamiento para un ATA IV recurrente.
En 160 pacientes (93,6%) los procedimientos de corrección sólo se efectuaron con clampaje directo tras heparinización sistémica con una dosis de 0,5mg/kg, neutralizada mediante la administración de protamina al término del procedimiento. En 11 pacientes (6,4%) se utilizó un bypass cardiopulmonar parcial para tres indicaciones, es decir, presencia de revascularización renal a partir de un vaso ilíaco (seis pacientes), asociación con un aneurisma de la aorta torácica descendente tratado durante el mismo procedimiento (dos pacientes) y ATA IV recurrente (tres pacientes). La apertura del aneurisma se siguió de la extracción del trombo mural, sutura de las arterias lumbares y colocación de catéteres de Foley con balón en el ostium de la arteria celíaca, mesentérica superior y renal derecha. Dichos catéteres se usaron para evitar el reflujo durante la anastomosis aortoprotésica y gas o émbolos trombóticos después del clampaje. Los catéteres se retiraron tan pronto como se implantó la prótesis. La arteria renal izquierda se clampó utilizando un clampaje de tipo bulldog.
En 166 (97,1%) pacientes se utilizó una prótesis de dacrón. En cuatro pacientes (2,3%) que presentaban aneurismas infecciosos diagnosticados en el preoperatorio se utilizó un aloinjerto criopreservado. En un paciente (0,6%) se efectuó sutura directa del falso aneurisma anastomótico. La configuración de la corrección fue aortoaórtica en 110 pacientes (64,9%), aortobiilíaca en 36 (21,1%) y aortoiliofemoral o bifemoral en 24 (14,0%). En 29 pacientes se efectuó anastomosis aórtica proximal terminoterminal. En la mayoría de los casos (142 pacientes, 83,1%), se creó una anastomosis biselada con la inclusión de un número variable de arterias. En 22 pacientes (12,9%) el origen de ambas arterias renales estaba lo suficientemente próximo para permitir su inclusión en una sola anastomosis junto con el ostium de las arterias intestinales. En la mayoría de los casos (112 pacientes, 65,5%), la distancia entre el ostium de la arteria renal izquierda y otras arterias viscerales era demasiado grande. En este caso la anastomosis se efectuó por separado desde la vía de la arteria visceral hasta el lado izquierdo de la prótesis aórtica directamente (76 pacientes, 44,5%), con o sin endarterectomía del ostium de la arteria renal o indirectamente usando un bypass protésico corto (36 pacientes, 21,0%). En 37 pacientes (21,6%) se utilizó una técnica de corrección “compleja”, que incluyó múltiples bypass, en particular en pacientes con aneurismas no degenerativos y lesiones asociadas a arterias renales e intestinales y/o reintervenciones.
La duración media de la isquemia intestinal fue de 30,0±12,8min (límites 6-100, mediana 28). La duración de la isquemia renal derecha fue de 31,8±15,6min (límites 12-118, mediana 29) e izquierda de 46,6±23,9min (límites 4-170, mediana 42,5). En los 25 pacientes en los que la arteriografía de esta estructura demostró que el origen de la arteria de Adamkiewicz se localizaba en el ATA IV, la de la isquemia de la médula espinal fue de 33,1±15,1min (límites 11-75, mediana 29).
La revascularización de la arteria mesentérica inferior sólo se efectuó en cinco pacientes (2,9%). La de la médula espinal se llevó a cabo en 25 pacientes: 21 por la inclusión del origen de la arteria lumbar que daba lugar a la arteria de Adamkiewicz en la anastomosis superior y cuatro mediante un bypass separado.
En 10 pacientes (5,8%) se efectuó esplenectomía de “encuentro”. Además de cuatro nefrectomías (2,3%) que se habían efectuado previamente, durante el mismo procedimiento, se realizaron 14 (8,4%), incluidas 12 por isquemia renal irreversible y dos por cáncer renal. En dos pacientes que presentaban riñones en herradura, se procedió a la reimplantación separada de las gruesas arterias ístmicas asociadas en la prótesis. En otros dos que presentaban una vena cava inferior a la izquierda y tres que presentaban una vena renal izquierda retroaórtica, se requirieron procedimientos quirúrgicos especiales.
ResultadosMortalidadLa mortalidad postoperatoria inmediata (al cabo de 30 días) fue del 11,7% (n=20) y la hospitalaria fue del 13,4% (n=23). Estas muertes acontecieron entre el día 0 (una se debió a insuficiencia cardíaca) y los 90 días (media=15,8±25,4 días, mediana=7). Las dos causas principales de mortalidad fueron la isquemia intestinal (nueve muertes, 39%) e insuficiencia multiorgánica (siete muertes, 30%). Tres pacientes fallecieron de hemorragia debido a un trastorno de la coagulación relacionado con el clampaje prolongado de las arterias intestinales (50, 70 y 75min). Dos fallecieron de complicaciones cardíacas y dos, de ictus masivo. El análisis univariado demostró que, durante la hospitalización, las variables pronósticas preoperatorias estadísticamente significativas de muerte fueron una edad mayor de 70 años (p=0,004), enfermedad aneurismática degenerativa (p=0,024), presencia de coronariopatía (p=0,003), insuficiencia renal crónica (p=0,007) y lesiones de la arteria mesentérica superior o tronco celíaco (p=0,009). La mortalidad postoperatoria no se correlacionó con el sexo; contexto de urgencia; revascularización miocárdica, cerebral, o aórtica previa; y enfermedad pulmonar obstructiva crónica.
Las variables pronósticas preoperatorias estadísticamente significativas de muerte hospitalaria fueron: el cirujano que realizó los procedimientos con una mortalidad postoperatoria del 5,1% para el cirujano A (5/98 intervenciones) comparado con el 24,6% para el cirujano B (17/69 intervenciones) (p=0,002), duración de la isquemia intestinal (p=0,004) y el uso de una técnica compleja (p=0,03). La mortalidad hospitalaria no se correlacionó con la fecha de la intervención (antes comparado con después de 1999).
Lesión de la médula espinalEn total, se produjeron ocho lesiones de la médula espinal (4,7%), incluida paraplejía en seis casos y paraparesia en dos. Los síntomas aparecieron inmediatamente al despertar en cinco pacientes y se demoraron en tres. De estos pacientes, dos fallecieron. De siete pacientes con lesión de la médula espinal, cinco no se habían sometido a una arteriografía preoperatoria.
En el análisis univariado no se identificaron variables pronósticas preoperatorias estadísticamente significativas de lesión de la médula espinal. Es probable que la razón de esto fuera el reducido número de pacientes incluidos. Se observó una tendencia para la coronariopatía (p=0,08), revascularización miocárdica (p=0,06) e insuficiencia renal (p=0,08). No se identificó una correlación significativa (p<0,1) entre la lesión de la médula espinal y el sexo, edad mayor de 70 años, enfermedad aneurismática degenerativa, contexto de urgencia, enfermedad pulmonar obstructiva crónica y lesiones de la arteria intestinal. El único factor con un valor predictivo significativo de lesión de la médula espinal fue la duración de la isquemia intestinal (p=0,03). No se evidenció una correlación con el cirujano, fecha de la intervención antes o después de 1999 y uso de una técnica compleja.
Isquemia intestinal agudaDada su profunda influencia en la mortalidad postoperatoria, la isquemia intestinal aguda fue la variable de referencia específica. Experimentaron el proceso en el postoperatorio 11 pacientes (6,4%), que requirieron un total de 17 reintervenciones. De estos pacientes, fallecieron nueve (82%). Con la excepción de un caso de isquemia colónica que se produjo el día 28, todas las complicaciones se diagnosticaron en las 36 primeras horas después de los procedimientos. Las causas subyacentes pudieron determinarse en siete pacientes. En tres casos la isquemia aislada del colon izquierdo se debió a isquemia pélvica. En cuatro casos la isquemia combinada del intestino delgado y del colon se debió a émbolos de colesterol (n=2) o émbolos ateroscleróticos (n=2), relacionados con el clampaje de la aorta supracelíaca en una zona patológica. En los cuatro pacientes restantes no pudo determinarse el mecanismo subyacente de esta isquemia.
El análisis univariado identificó la insuficiencia renal (p=0,005) y las lesiones de la arteria intestinal (p=0,001) como variables pronósticas preoperatorias significativas de isquemia intestinal. Se observó una tendencia para la coronariopatía (p=0,06) y la revascularización miocárdica previa (p=0,06). No se observó una correlación significativa (p<0,1) entre la isquemia intestinal postoperatoria y el sexo, edad mayor de 70 años, enfermedad aneurismática degenerativa, tratamiento de urgencia o enfermedad pulmonar obstructiva crónica.
Para ningún factor intraoperatorio se observó un valor predictivo de isquemia intestinal postoperatoria, incluida no sólo la duración de ésta sino también el cirujano, fecha del procedimiento, antes comparado con después de 1999, y la utilización de una técnica compleja.
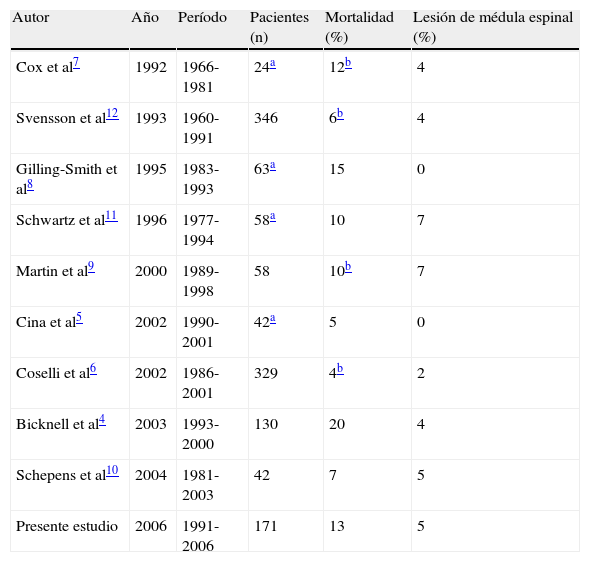
DiscusiónLa corrección de un ATA IV se asocia a riesgos por lo que respecta a la mortalidad hospitalaria y la lesión de la médula espinal4-12 (tabla I). La mortalidad postoperatoria está potentemente influida por las características del paciente. El análisis estadístico del presente estudio reveló que la mortalidad postoperatoria inmediata se correlacionó significativamente con una edad mayor de 70 años, enfermedad aneurismática degenerativa, insuficiencia renal y lesiones de las arterias viscerales. La relación con la insuficiencia renal crónica ya había sido descrita por Bicknell et al4, en cuyo análisis multivariado se demostró que es una variable pronóstica independiente significativa de mortalidad postoperatoria. Las características de los pacientes desempeñan un importante papel en la incidencia de otros acontecimientos postoperatorios, incluidas las complicaciones cardíacas, ictus e insuficiencia multiorgánica. Estos acontecimientos se asocian con cualquier tipo de cirugía con independencia de la indicación.
Principales series que describían la corrección de aneurismas toracoabdominales de tipo IV entre los artículos publicados
| Autor | Año | Período | Pacientes (n) | Mortalidad (%) | Lesión de médula espinal (%) |
| Cox et al7 | 1992 | 1966-1981 | 24a | 12b | 4 |
| Svensson et al12 | 1993 | 1960-1991 | 346 | 6b | 4 |
| Gilling-Smith et al8 | 1995 | 1983-1993 | 63a | 15 | 0 |
| Schwartz et al11 | 1996 | 1977-1994 | 58a | 10 | 7 |
| Martin et al9 | 2000 | 1989-1998 | 58 | 10b | 7 |
| Cina et al5 | 2002 | 1990-2001 | 42a | 5 | 0 |
| Coselli et al6 | 2002 | 1986-2001 | 329 | 4b | 2 |
| Bicknell et al4 | 2003 | 1993-2000 | 130 | 20 | 4 |
| Schepens et al10 | 2004 | 1981-2003 | 42 | 7 | 5 |
| Presente estudio | 2006 | 1991-2006 | 171 | 13 | 5 |
Probablemente como consecuencia del examen de cribado diagnóstico apropiado y del tratamiento preventivo de las lesiones carotídeas y coronarias2, en el presente estudio, las lesiones ateroscleróticas asociadas sólo fueron directamente responsables de cuatro muertes hospitalarias. Sin embargo, la presencia de coronariopatía sin revascularización miocárdica se identificó como una variable pronóstica estadísticamente significativa de mortalidad inmediata. Puesto que en la serie del presente estudio no se evaluó sistemáticamente la función ventricular izquierda, no podemos extraer conclusiones sobre su influencia. Sin embargo, la disfunción ventricular izquierda se ha descrito como una variable pronóstica de mortalidad después de la corrección de un aneurisma toracoabdominal13.
En el presente estudio las variables pronósticas intraoperatorias de mortalidad hospitalaria fueron el cirujano (4,9% para el A comparado con 17,9% para el B), uso de una técnica compleja, y, sobre todo la duración de la isquemia intestinal. Schwartz et al11, Vermeulen et al14 y Bicknell et al4 han descrito su valor predictivo. Una isquemia prolongada también fue responsable de tres trastornos de la coagulación que dieron lugar a la muerte. Los cambios de la coagulación asociados con el clampaje aórtico han sido el objeto de una extensa investigación, experimental y clínica15-20. Es interesante destacar que la duración de la isquemia intestinal no fue una variable pronóstica estadísticamente significativa de isquemia intestinal postoperatoria en la serie del presente estudio. La fisiopatología subyacente es la explicación más probable de este hallazgo en apariencia contradictorio, ya que cuatro de las 11 complicaciones relacionadas con isquemia intestinal observadas en el presente estudio fueron de origen embólico.
En vista de la elevada prevalencia (39% de mortalidad) y gravedad (85% mortales) de isquemia intestinal postoperatoria aguda, nuestro grupo ha prestado una atención especial a dicha complicación. Una de las medidas preventivas más importantes es reducir a un mínimo su duración. Un medio evidente de conseguir este objetivo es utilizar una técnica quirúrgica simple que permita que la revascularización del intestino se obtenga al cabo de 15-20min. Esta estrategia también reduce los problemas de hemostasia relacionados con la isquemia hepática e intestinal. La corrección rápida puede facilitarse creando una anastomosis superior biselada que incluya, como mínimo, las arterias intestinales y renal derecha21,22. Si esta estrategia no es viable, una solución alternativa consiste en revascularizar primero la arteria mesentérica superior (y la arteria renal izquierda) a través de un injerto mediante bypass de la aorta torácica descendente23. También es posible implantar una derivación endoluminal de Javid entre la aorta torácica descendente y la arteria mesentérica superior inmediatamente después de abrir el aneurisma. Aunque en casos especiales también puede ser eficaz una derivación endoluminal auriculofemoral o un bypass cardiopulmonar parcial con una línea arterial en Y, no recomendamos la utilización sistemática de esta técnica. En los estudios publicados, los únicos investigadores que en la actualidad han descrito su utilización sistemática para los ATA IV son Safi et al27. Schepens et al10 describieron su utilización en el 14% de sus casos de ATA IV pero no especificaron sus indicaciones. Sigue por dilucidar la tasa de flujo necesaria para evitar la isquemia intestinal28.
La prevención de émbolos inducidos por el clampaje en la arteria mesentérica superior requiere una evaluación angiográfica preoperatoria cuidadosa. En pacientes que presentan un trombo que recubre la pared de la parte inferior de la aorta torácica descendente, en especial con antecedentes de émbolos de colesterol, puede ser necesaria para evitar un clampaje supracelíaco simple y una anastomosis aórtica superior biselada. En este caso, es necesario efectuar una anastomosis terminoterminal separada, más alta que el límite superior del aneurisma. Puede asistirla un bypass cardiopulmonar parcial con un clampaje secuencial o una perfusión visceral separada para reducir la duración de la isquemia renal e intestinal.
Otro factor que requiere una atención especial es la vascularización pélvica tanto a través de las arterias hipogástricas como de la arteria mesentérica inferior evitando la polarización en las arterias viscerales. Merece la pena mencionar que sólo el 2,9% de los pacientes (n=5) de la serie del presente estudio se sometieron a revascularización de dicha arteria comparado con el 20% en los que se efectuó una modalidad convencional en la aorta abdominal infrarrenal.
Debido al reducido número de lesiones de la médula espinal, los únicos factores preoperatorios para los que el análisis estadístico demostró una correlación casi significativa con esta complicación fueron la coronariopatía, los antecedentes de revascularización miocárdica y la insuficiencia renal. Acher et al29 describieron previamente una relación entre el riesgo de complicaciones postoperatorias de la médula espinal y la disminución del índice cardíaco después del clampaje aórtico. Sin embargo, es difícil extrapolar este hallazgo a los ATA IV ya que, de los 216 pacientes incluidos, sólo 46 eran portadores de estos aneurismas y todos los procedimientos se efectuaron utilizando un clampaje aórtico simple, con independencia del tipo de aneurisma.
En nuestra opinión, la prevención de las complicaciones de la médula espinal depende principalmente de la realización de una arteriografía preoperatoria en la evaluación de todos los pacientes en los que no está contraindicada puesto que este procedimiento no entraña riesgos significativos30. En la serie del presente estudio se destaca su utilidad ya que demostró que el origen de la arteria de Adamkiewicz se localizaba en el aneurisma en más de una cuarta parte de pacientes en los que se efectuó. A pesar de que esta cifra no es significativa en vista del reducido número de complicaciones de la médula espinal, es preciso destacar que cinco de los siete pacientes que experimentaron complicaciones no se habían sometido a la evaluación.
Recientemente, para los ATA IV, se ha propuesto una reparación endovascular y abierta combinada. El principio del tratamiento híbrido consiste en un bypass (habitualmente a partir de la arteria ilíaca) para la revascularización de las arterias renal e intestinal, seguido de la implantación de un stent endoluminal para el tratamiento del aneurisma. Esta estrategia puede evitar la necesidad de clampaje aórtico, lo que puede ser decisivo para pacientes con disfunción cardíaca pero carece de pertinencia en la mayoría de los casos, y acorta el tiempo de clampaje de la arteria visceral. Sin embargo, apenas se observan efectos por lo que respecta a la exposición quirúrgica porque la laparotomía media sigue siendo el abordaje indicado. Una desventaja de las técnicas híbridas es que no permiten la reimplantación de las arterias lumbares que dan lugar a la arteria de Adamkiewicz. Hasta la fecha sólo se han publicado casos clínicos o series a pequeña escala que describen el tratamiento híbrido31-33. Por esta razón, es demasiado pronto para afirmar el papel (si lo tiene) que este abordaje desempeñará en el tratamiento de los ATA IV. Aunque reconocemos la proeza técnica que representa el tratamiento endoscópico34, seguimos siendo prudentes con esta técnica ya que entraña un riesgo elevado de isquemia visceral prolongada en caso de problemas técnicos.24,25,26
Presentado en la 21 Reunión Anual de la Societé de Clinique Vascularis de Langue Française Arcachon, Francia, 17-20 de junio de 2006.