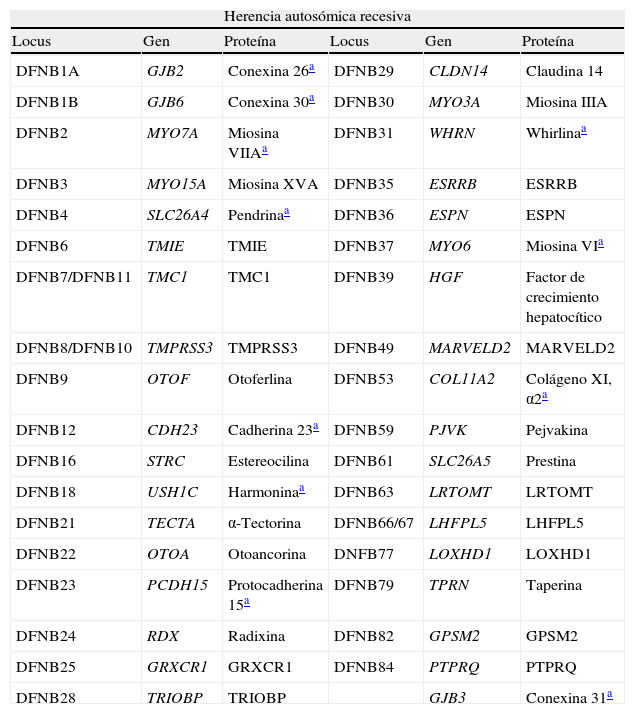
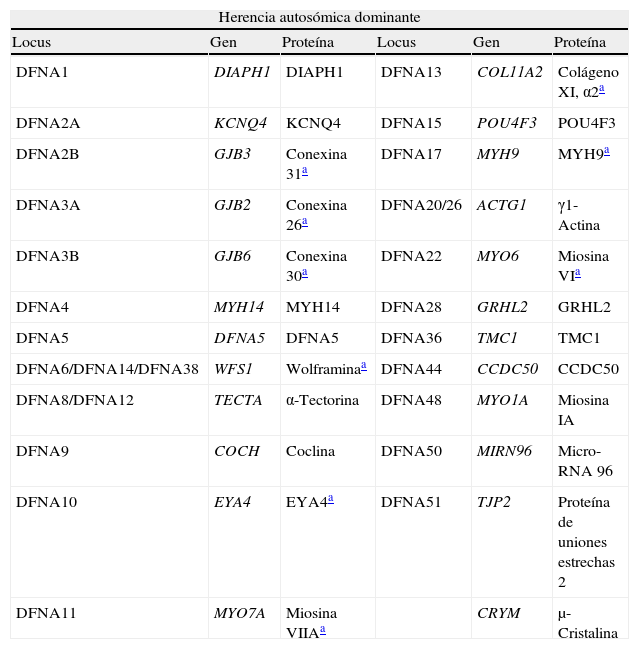
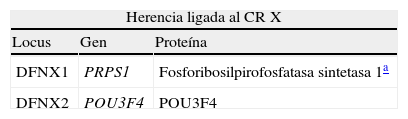
El objetivo de esta revisión es proporcionar una visión actualizada de las hipoacusias hereditarias, prestando especial atención al diagnóstico etiológico de las hipoacusias neurosensoriales, a los genes más frecuentemente mutados en nuestro medio, a las técnicas disponibles para su estudio y a las implicaciones clínicas del diagnóstico genético.
Al menos el 60% de las hipoacusias neurosensoriales infantiles tienen una causa genética. En los adultos desconocemos el porcentaje de hipoacusias hereditarias. Ante una hipoacusia neurosensorial, la prueba con un mayor rendimiento diagnóstico son los análisis genéticos. El proceso de consejo o asesoramiento genético tiene como fin informar al paciente y sus familiares de la probabilidad de presentar una enfermedad condicionada genéticamente, del riesgo de transmitirla, de las medidas de prevención y diagnóstico precoz disponibles, y de la posibilidad de llevar a cabo un estudio genético. La realización de cualquier análisis genético, siempre ha de venir precedida por el adecuado proceso de asesoramiento genético.
The aim of this review is to provide an updated overview of hereditary hearing loss, with special attention to the etiological diagnosis of sensorineural hearing loss, the genes most frequently mutated in our environment, the techniques available for their analysis and the clinical implications of genetic diagnosis.
More than 60% of childhood sensorineural hearing loss is genetic. In adults, the percentage of hereditary hearing loss is unknown. Genetic testing is the highest yielding test for evaluating patients with sensorineural hearing loss. The process of genetic counselling is intended to inform patients and their families of the medical, psychological and familial implications of genetic diseases, as well as the risks, benefits and limitations of genetic testing. The implementation of any genetic analysis must be always preceded by an appropriate genetic counselling process.