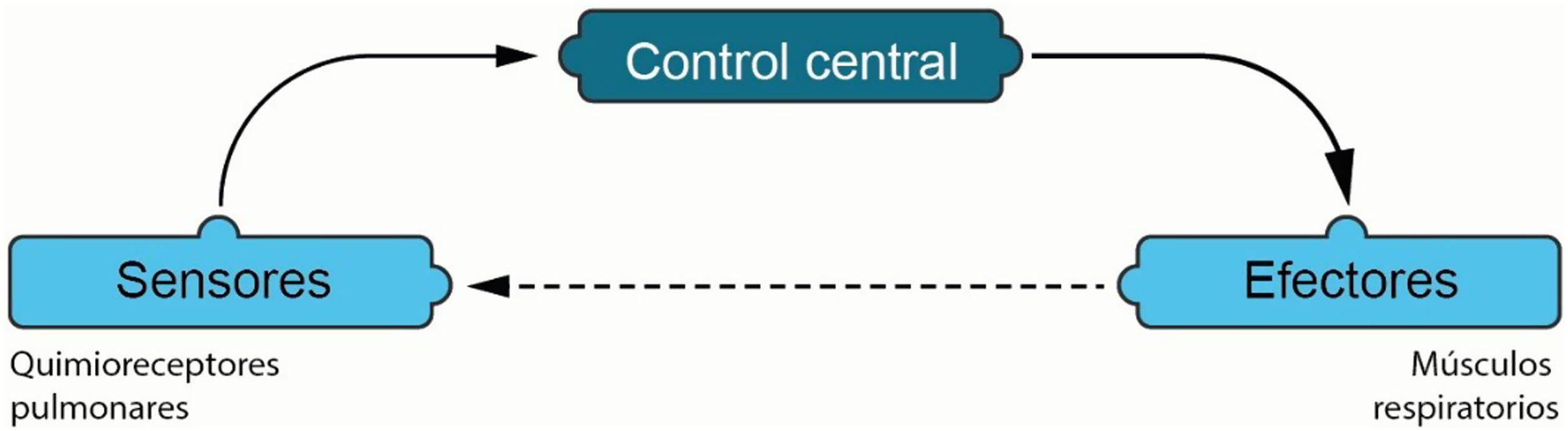
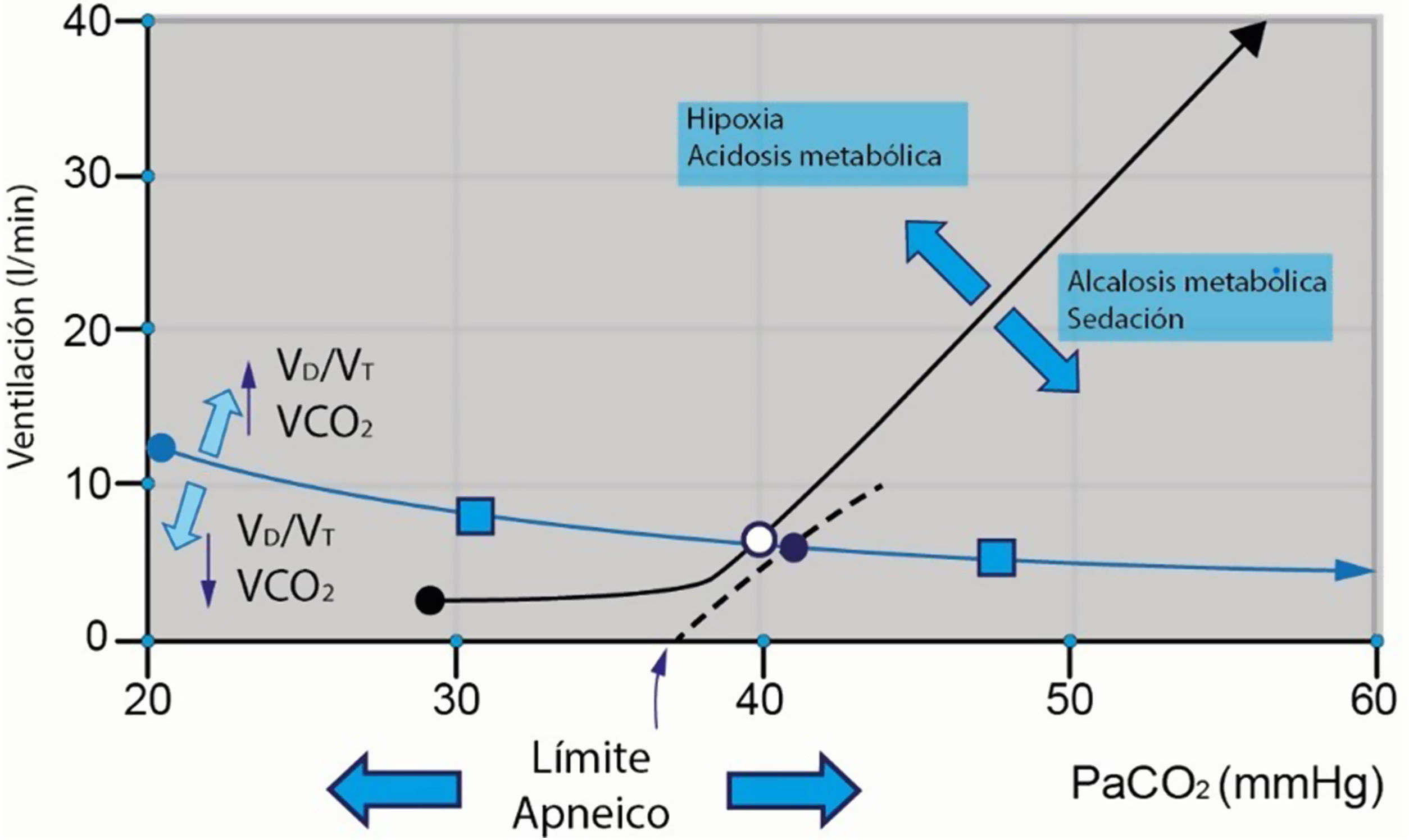
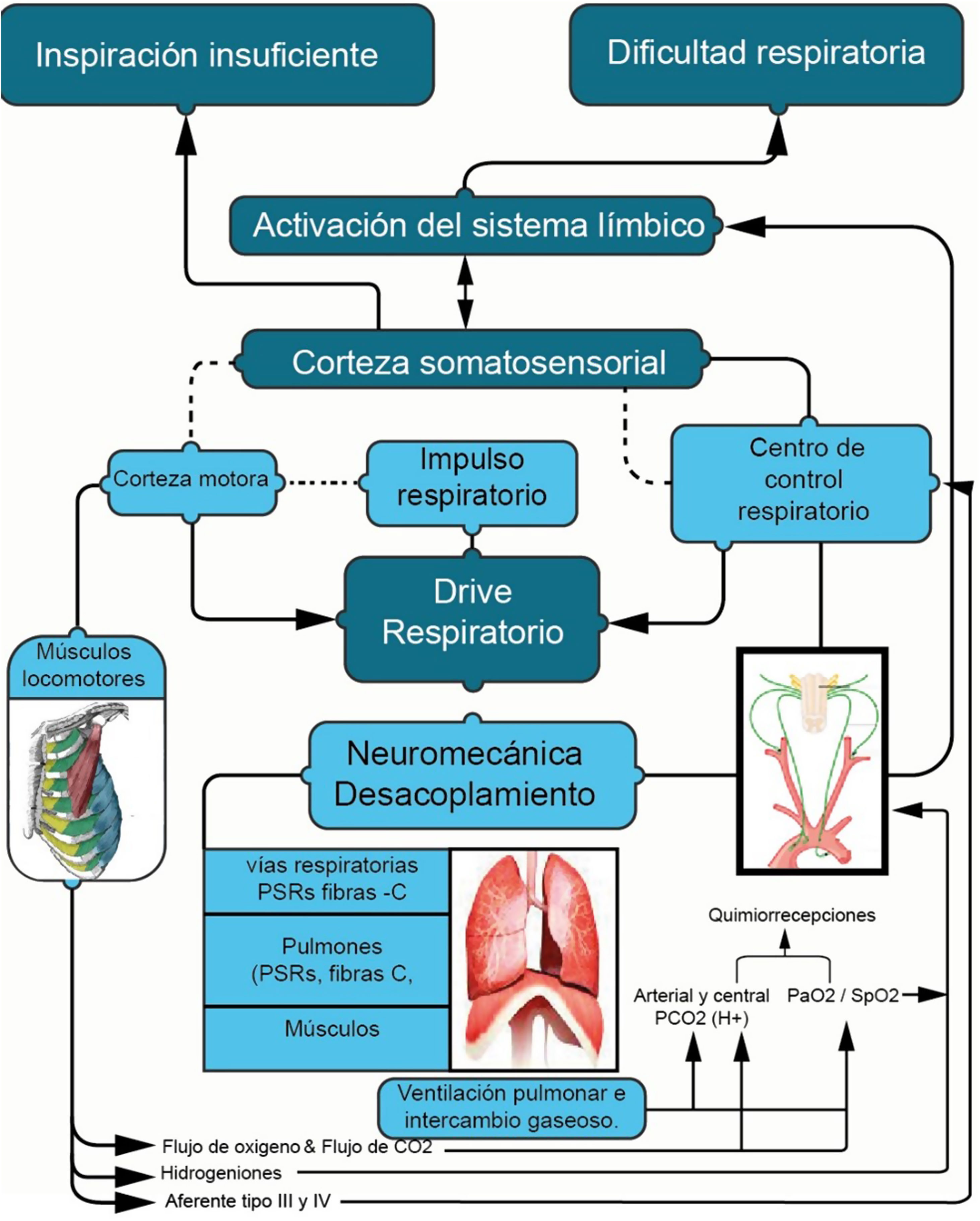
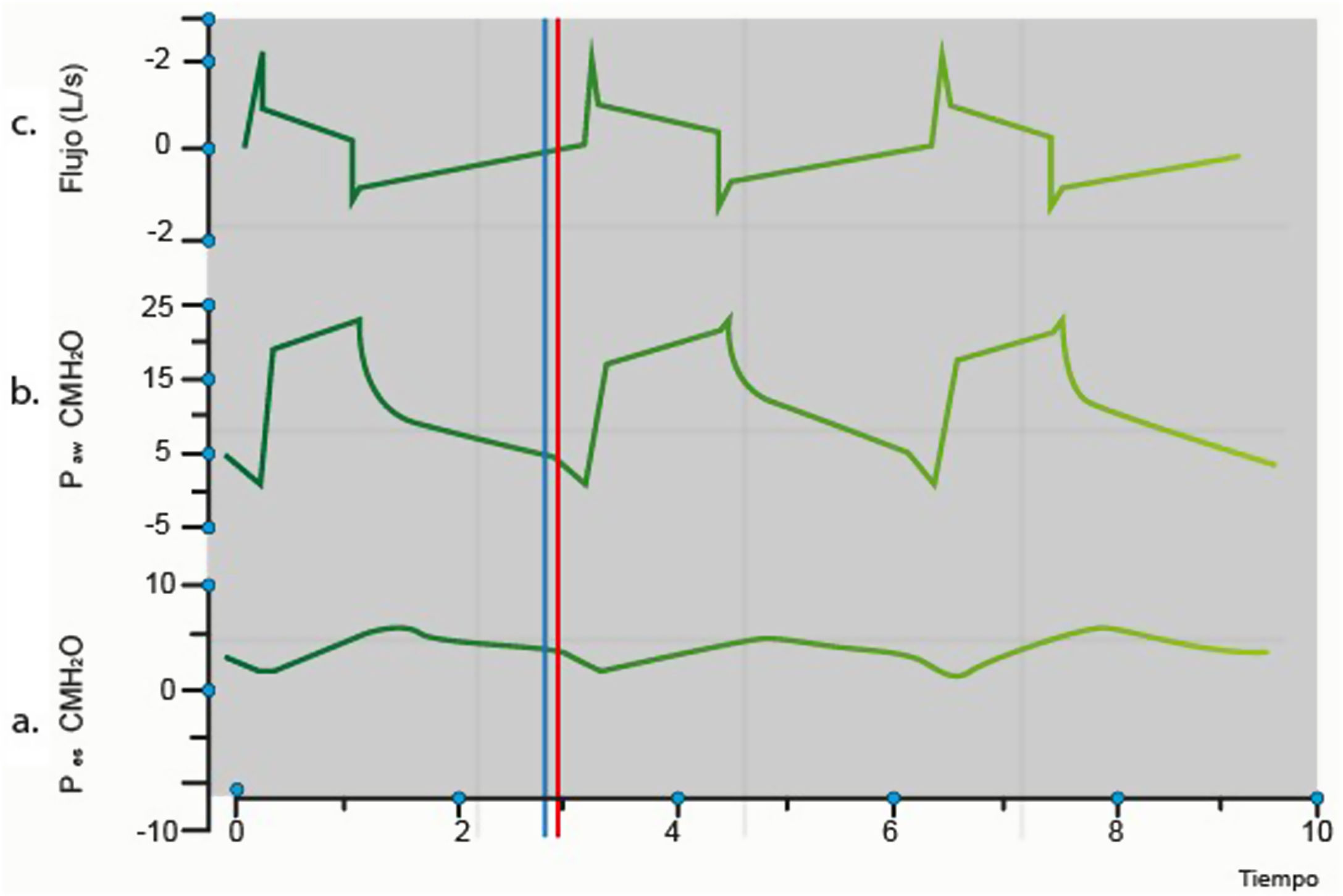
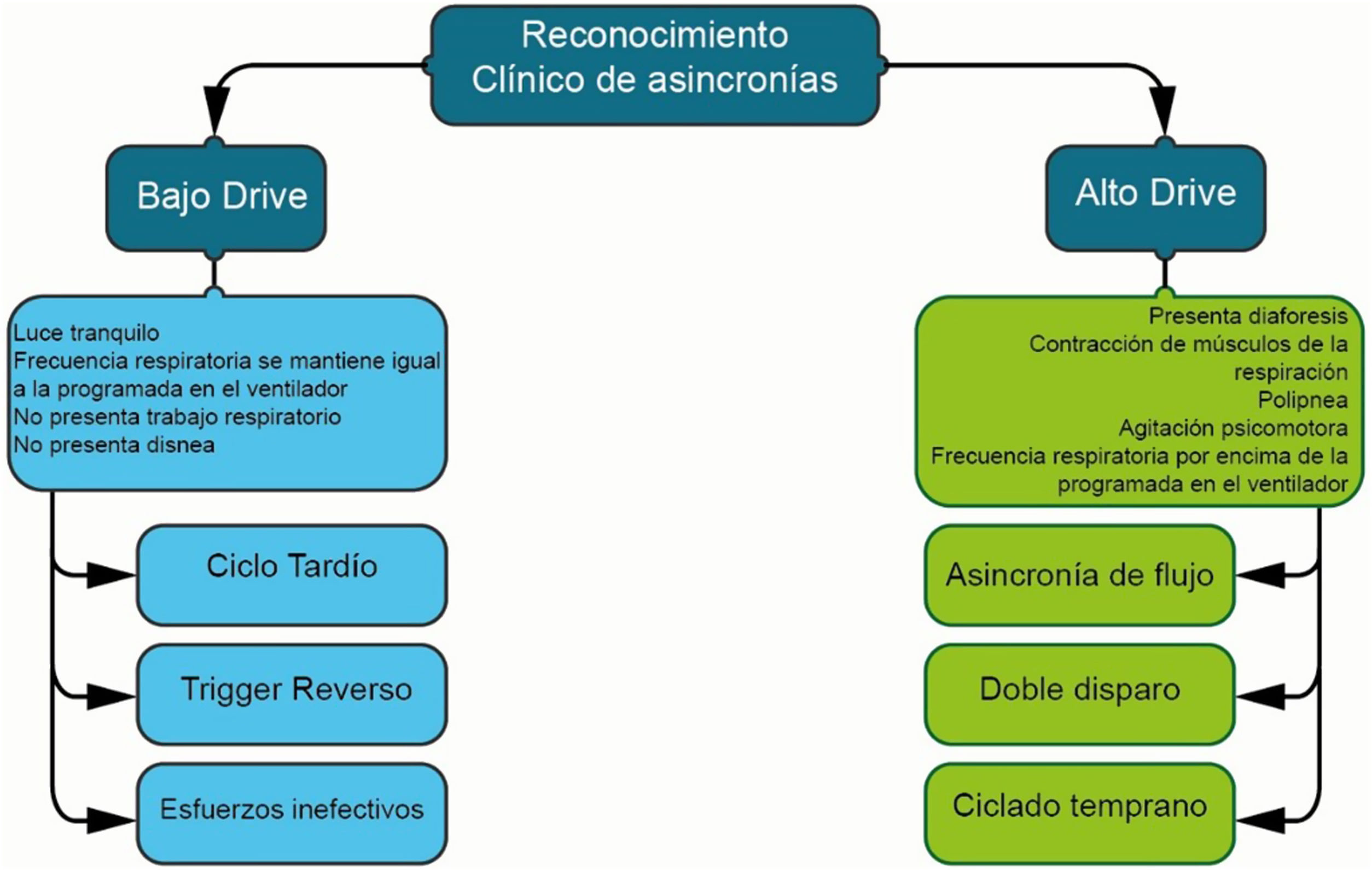
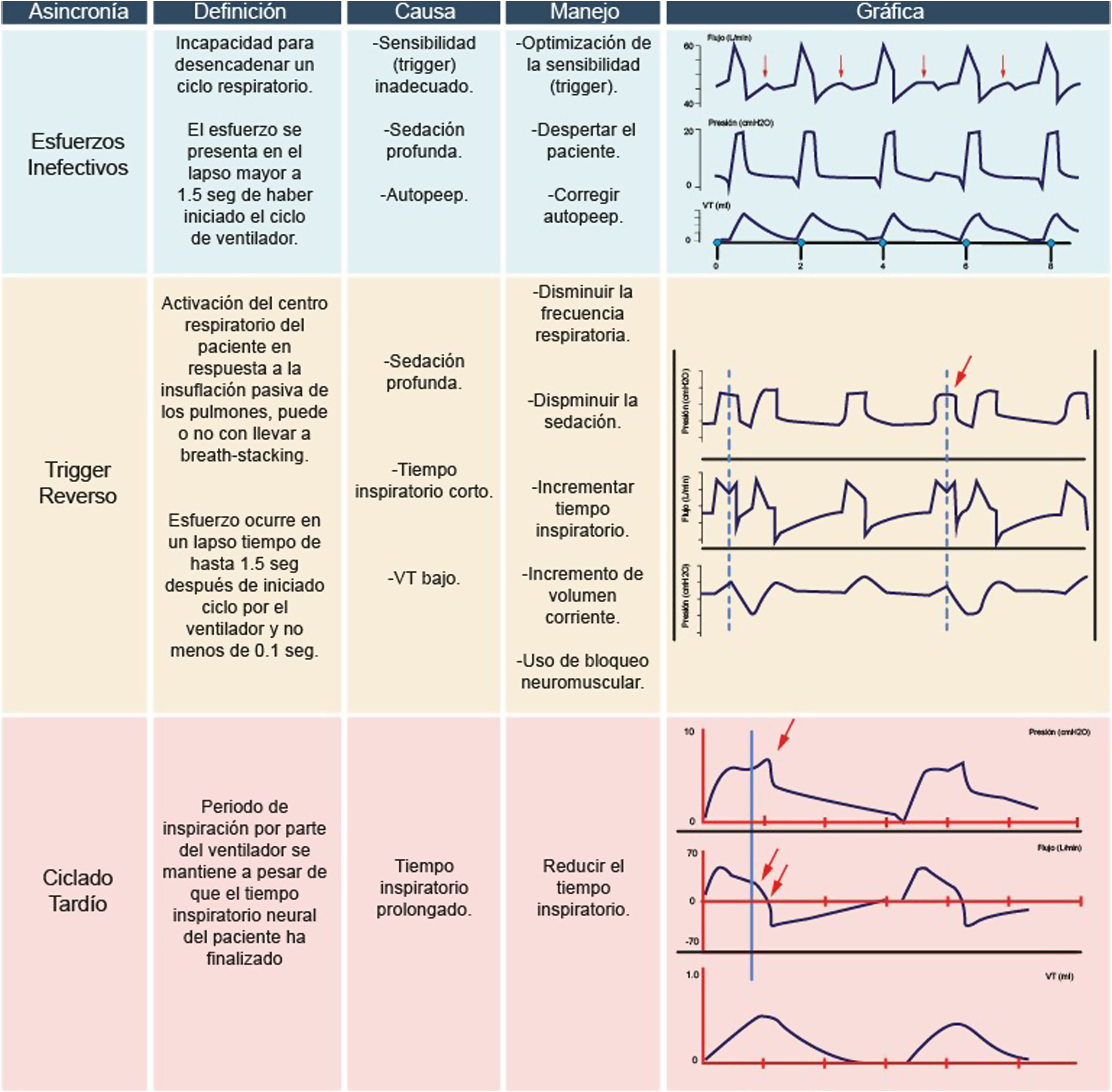
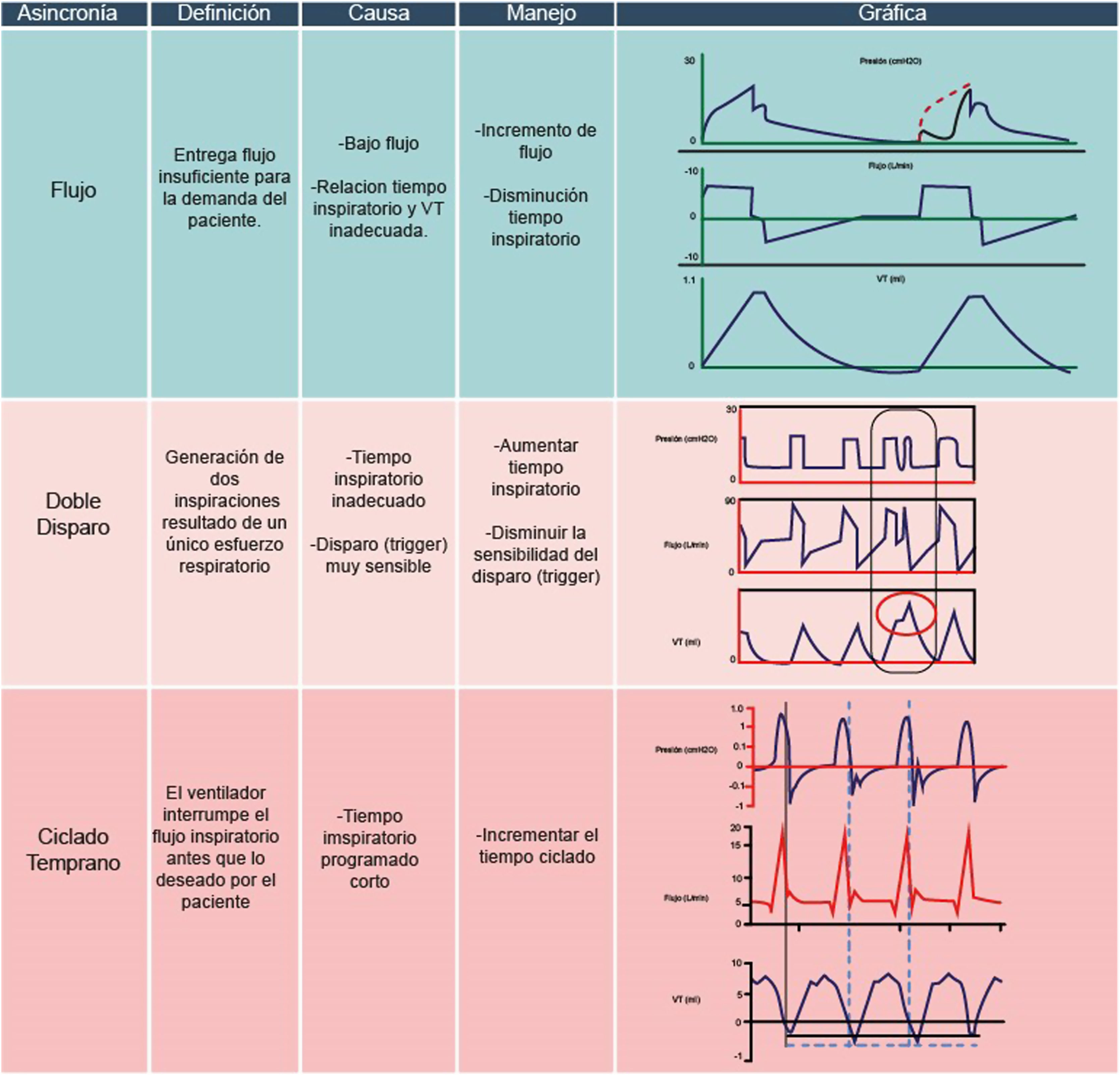
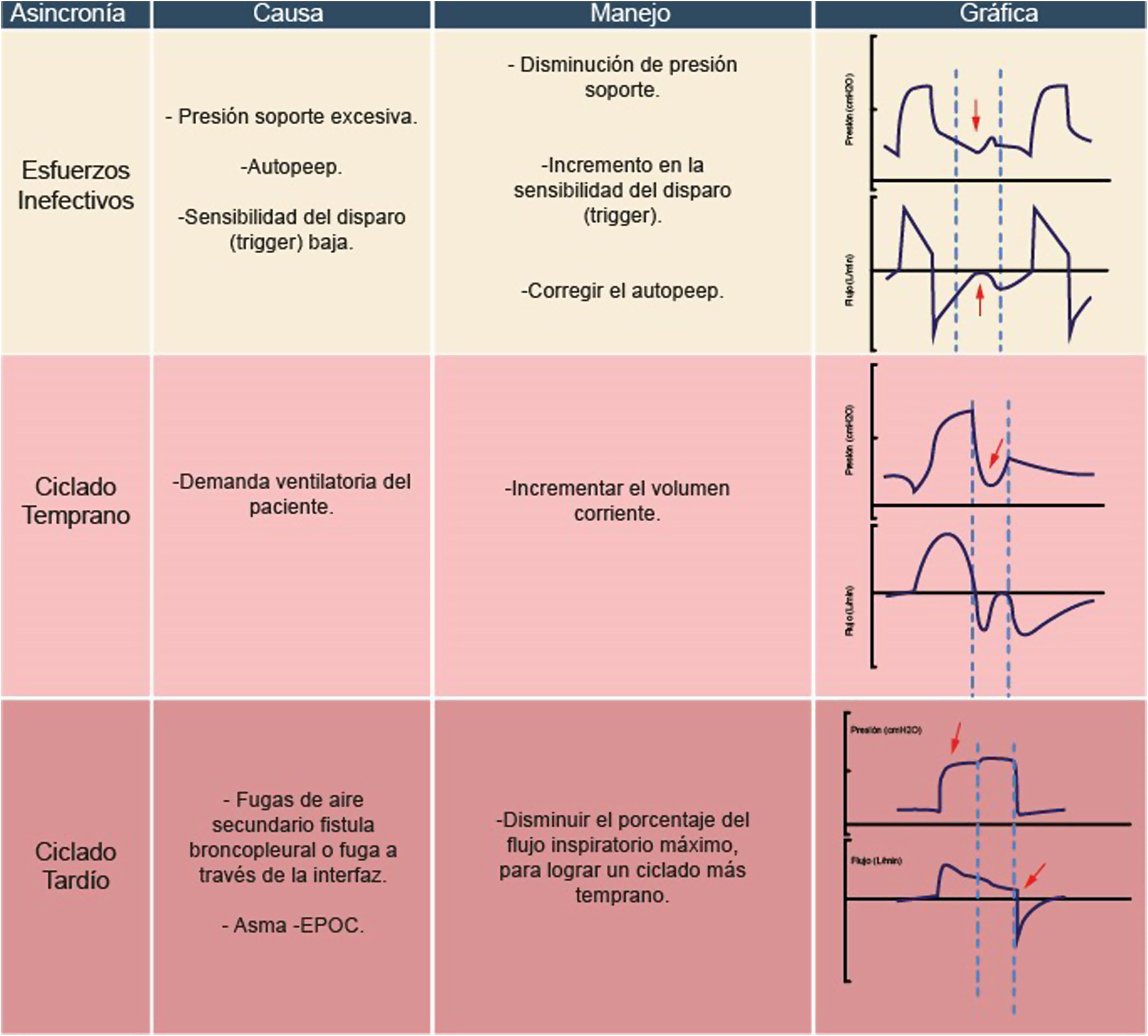
Las asincronías, que se caracterizan por la falta de sincronización entre los momentos en que el paciente realiza inspiraciones neurales y los programados en el ventilador, son comunes en aquellos pacientes que requieren asistencia ventilatoria. A pesar de que la monitorización esofágica se considera la forma más precisa para la detección, el diagnóstico, la intervención, resulta poco práctica en el contexto de la evaluación clínica. La monitorización a través de diversas curvas y bucles, sin embargo, facilita la identificación de asincronías y permite la evaluación de la respuesta a las intervenciones establecidas. Esta revisión se centra en diferenciar los estímulos al centro respiratorio y las respuestas mecánicas, lo cual facilita el diagnóstico y las intervenciones necesarias para su control.
Asynchronies, characterized by the lack of synchronization between the moments when the patient performs neural inspirations and those programmed in the ventilator, are common in patients requiring ventilatory support. Although esophageal monitoring is considered the most accurate method for detection, diagnosis, and intervention, it proves impractical in the clinical evaluation context. Monitoring through various curves and loops, however, facilitates the identification of asynchronies and allows for the assessment of the response to established interventions. This review focuses on differentiating stimuli to the respiratory center and mechanical responses, thereby easing the diagnosis and interventions necessary for their control.
Artículo
Socios de la Asociación de Medicina Crítica y Cuidado Intensivo
Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la AMCI, clique aquí