La ventilación mecánica invasiva (VMI) requiere habitualmente sedación endovenosa (EV), aunque la sedación inhalatoria (SI) con isoflurano tiene propiedades farmacológicas que podrían ofrecer beneficios adicionales en la Unidad de Cuidados Intensivos (UCI).
ObjetivoEstablecer la diferencia en el consumo de opioides entre pacientes adultos bajo VMI con sedación EV vs. SI con isoflurano en el Hospital San José, Bogotá, entre enero y abril de 2023.
MétodosEstudio analítico de cohortes observacional en pacientes adultos sometidos a VMI, comparando EV vs. SI más analgesia EV. Se aplicaron criterios de exclusión (enfermedad pulmonar severa, cirugía cardiaca, infarto, embarazo). Se recogieron datos clínicos y dosis de midazolam, propofol y fentanilo; análisis estadístico usando STATA 17. Pruebas no paramétricas (U de Mann-Whitney, χ2), p<0,05.
ResultadosLa muestra final incluyó 156 pacientes (edad mediana 66,0 años, 57,7% mujeres; 19,3% bajo SI). La mediana de VMI fue de 3,0 días (rango intercuartílico [IRQ] 1,0–6,0). Las dosis de midazolam, propofol y fentanilo (dosis total y diaria) fueron menores en el grupo SI cuando la VMI superó las 48 horas; diferencia significativa para midazolam (p <0,001). En pacientes con VMI> 48h, la dosis diaria de fentanilo también fue menor en SI, aunque no alcanzó significación estadística (p=0,385).
ConclusionesLa SI con isoflurano en pacientes adultos con VMI prolongada (> 48 h) se asocia con reducción en el uso total de opioides, particularmente fentanilo. Esto implica posibles ahorros en costos de atención, menor riesgo de complicaciones y eventos asociados a uso prolongado. Se requiere más investigación con muestras mayores para confirmar estos hallazgos.
Invasive mechanical ventilation (IMV) often requires intravenous (IV) sedation, although inhaled sedation (IS) with isoflurane has pharmacological properties that may provide additional benefits in the ICU.
ObjectiveTo determine the difference in opioid consumption between adult patients under IMV with IV sedation vs. IS with isoflurane at Hospital San José, Bogotá, between January and April 2023.
MethodsAnalytical observational cohort study in adult patients undergoing IMV, comparing IV sedation vs. IS plus IV analgesia. Exclusion criteria included severe pulmonary disease, cardiac surgery, myocardial infarction, and pregnancy. Clinical data and midazolam, propofol, and fentanyl doses were collected; statistical analysis performed using STATA 17. Non-parametric tests (Mann-Whitney U, χ2); p <0.05.
ResultsFinal sample included 156 patients (median age 66.0 years, 57.7% women; 19.3% under IS). Median IMV duration was 3.0 days (IQR 1.0–6.0). Midazolam, propofol, and fentanyl (total and daily doses) were lower in the IS group when IMV exceeded 48hours; significant difference for midazolam (p <0.001). In patients with IMV>48h, daily fentanyl dose was also lower in IS group, though not statistically significant (p=0.385).
ConclusionsInhaled sedation with isoflurane in adult patients undergoing prolonged IMV (>48h) is associated with reduced use of opioids, especially fentanyl. This may result in cost savings, lower risk of complications, and reduced events associated to drug dependence. Further studies with larger samples are needed to confirm these findings.
El uso prolongado de opioides en pacientes hospitalizados, especialmente en Unidades de Cuidados Intensivos (UCI), se ha asociado con complicaciones clínicas relevantes como depresión respiratoria, íleo paralítico, delirium, dependencia, y síndromes de abstinencia, lo cual impacta negativamente en la recuperación y prolonga la estancia hospitalaria1. Frente a este escenario, es prioritario promover estrategias terapéuticas que permitan reducir la exposición acumulada a opioides sin comprometer el control del dolor ni la adecuada sedación de los pacientes críticos. En este contexto, los agentes anestésicos inhalados han emergido como una alternativa farmacológica prometedora que podría contribuir a disminuir el consumo de opioides en la UCI3,4.
Los sedantes endovenosos (EV) como propofol, midazolam y dexmedetomidina, si bien ampliamente utilizados, han mostrado limitaciones importantes. El uso prolongado de propofol se ha asociado con hipertrigliceridemia e inestabilidad hemodinámica, y en casos raros con el síndrome de infusión de propofol5–7. Por su parte, las benzodiacepinas han demostrado aumentar la duración de la ventilación mecánica, el riesgo de delirium y la estancia en UCI, especialmente en regiones como América Latina, donde su uso aún es prevalente2,11–19. Esta evidencia ha motivado a las principales guías internacionales a recomendar, desde 2013, el uso de sedantes distintos a las benzodiacepinas, promoviendo una sedación más ligera y de menor impacto funcional8–10.
La sedación inhalatoria (SI) con agentes como isoflurano ha demostrado ventajas farmacocinéticas clave como inicio y recuperación rápidos, metabolismo pulmonar y menor dependencia de la función hepática o renal. En revisiones sistemáticas y metaanálisis recientes, se ha reportado que esta modalidad acorta el tiempo de extubación y de despertar en pacientes postquirúrgicos, con posibles efectos protectores a nivel miocárdico y reducción de biomarcadores como la troponina20,21. Además, algunos estudios sugieren beneficios en parámetros ventilatorios, inflamación pulmonar, y protección orgánica multisistémica5,6,22–24.
Dado que se estima que hasta el 80% de los pacientes en ventilación mecánica invasiva (VMI) reciben opioides, y que esta cifra asciende al 90% en estancias prolongadas29, la implementación de estrategias que reduzcan esta exposición es crítica. La SI no solo representa una herramienta clínicamente eficaz, sino también una posible intervención costo-efectiva que puede ayudar a mitigar la crisis global de opioides, cuyas consecuencias incluyen farmacodependencia, aumento de la mortalidad y sobrecarga para los sistemas de salud1,25–28. Por ello, el presente estudio tiene como objetivo evaluar si el uso de SI en pacientes con VMI en el Hospital San José de Bogotá se asocia con una menor dosis acumulada de opioides, en comparación con la sedación EV estándar, y explorar su impacto en términos de costo-efectividad.
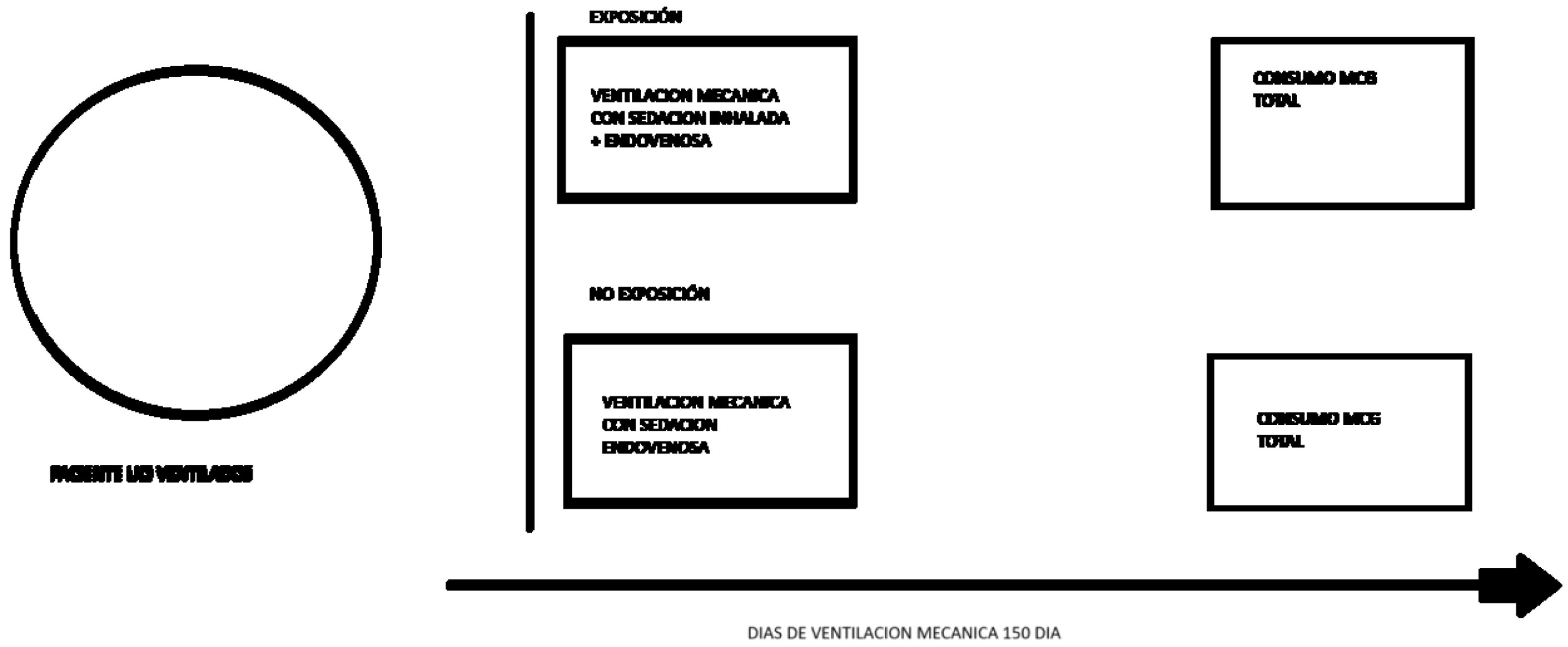
MétodosSe llevó a cabo un estudio observacional, analítico, de cohorte retrospectiva con el objetivo de comparar el uso de sedación EV vs. SI combinada con analgesia EV, en pacientes mayores de 18 años que requirieron VMI y fueron admitidos en la UCI del Hospital San José (Bogotá, Colombia), entre enero y abril de 2023 (fig. 1).
Se excluyeron del análisis los pacientes con diagnóstico de enfermedad pulmonar severa, postoperatorio de cirugía cardiovascular, infarto agudo de miocardio con o sin elevación del segmento ST, así como mujeres embarazadas.
La identificación de los pacientes se realizó mediante el registro institucional de hospitalización en la UCI. Una vez aprobado el protocolo por el comité de ética, se procedió a la revisión sistemática de las historias clínicas electrónicas. La extracción de datos fue realizada de forma independiente por tres investigadores, en distintos momentos, para garantizar la validez interna y la concordancia entre los registros clínicos y la base de datos. La información recolectada fue ingresada en una matriz electrónica diseñada en Microsoft Excel® y posteriormente analizada utilizando el software STATA versión 17 (StataCorp, College Station, TX, USA).
Las variables incluidas en el análisis fueron: sexo, edad, puntaje de gravedad APACHE II, puntaje SOFA al ingreso, diagnóstico clínico inicial, estado séptico al ingreso, y antecedentes médicos relevantes (enfermedad pulmonar crónica, diabetes mellitus, enfermedad renal crónica, hipotiroidismo, hipertensión arterial, alcoholismo, farmacodependencia, inmunosupresión, insuficiencia cardiaca congestiva). Las variables de desenlace primarias incluyeron el tiempo total en VMI y las dosis acumuladas de los opioides y sedantes utilizados: fentanilo, midazolam y propofol.
El análisis univariado de las variables cuantitativas se realizó mediante medidas de tendencia central (mediana) y dispersión (rango intercuartílico [IRQ]), dado que la mayoría de las variables no siguieron una distribución normal, determinada por la prueba de Shapiro-Wilk. Las variables cualitativas se describieron como frecuencias absolutas y proporciones relativas. Para el análisis bivariado, se utilizaron pruebas no paramétricas, específicamente el test de U de Mann-Whitney para comparar las dosis de opioides entre los grupos de sedación (EV vs. SI). En el caso del análisis de frecuencias de uso de opioides por rangos de dosis definidos según literatura previa, se aplicó la prueba de χ2.
Se realizó una exploración multivariada preliminar mediante regresión lineal múltiple y modelos lineales no generalizados, con el objetivo de ajustar por variables confusoras, aunque no se obtuvieron modelos estadísticamente significativos ni clínicamente robustos. Todos los análisis estadísticos se realizaron considerando un nivel de significancia alfa de 0,05 y un intervalo de confianza del 95%.
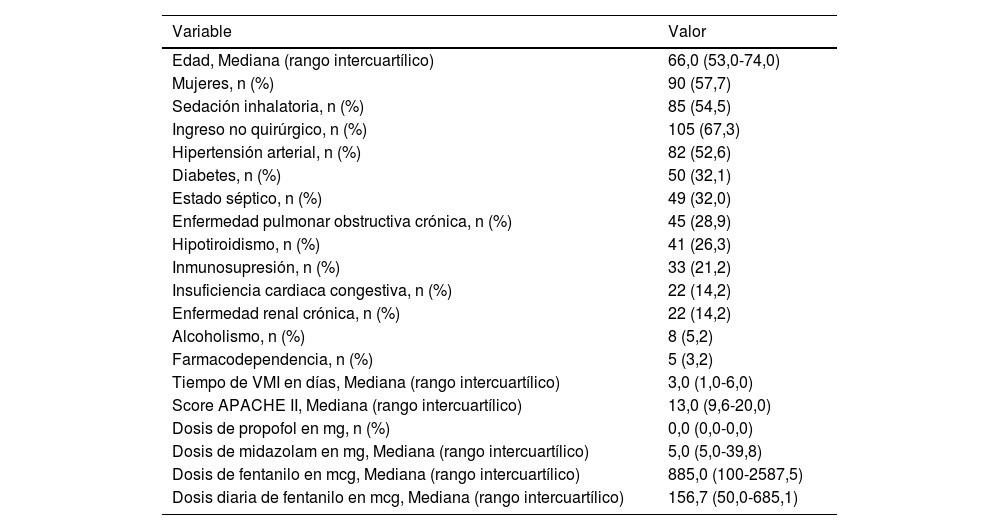
ResultadosTras aplicar los criterios de inclusión y exclusión, se incluyeron 156 pacientes. La mediana de edad fue de 66,0 años (RIC 53,0–74,0), con predominio del sexo femenino (57,7%; n=90). El 19,3% de los casos recibió SI (n=30) (tabla 1).
Sexo, edad, características clínicas y dosis en la muestra
| Variable | Valor |
|---|---|
| Edad, Mediana (rango intercuartílico) | 66,0 (53,0-74,0) |
| Mujeres, n (%) | 90 (57,7) |
| Sedación inhalatoria, n (%) | 85 (54,5) |
| Ingreso no quirúrgico, n (%) | 105 (67,3) |
| Hipertensión arterial, n (%) | 82 (52,6) |
| Diabetes, n (%) | 50 (32,1) |
| Estado séptico, n (%) | 49 (32,0) |
| Enfermedad pulmonar obstructiva crónica, n (%) | 45 (28,9) |
| Hipotiroidismo, n (%) | 41 (26,3) |
| Inmunosupresión, n (%) | 33 (21,2) |
| Insuficiencia cardiaca congestiva, n (%) | 22 (14,2) |
| Enfermedad renal crónica, n (%) | 22 (14,2) |
| Alcoholismo, n (%) | 8 (5,2) |
| Farmacodependencia, n (%) | 5 (3,2) |
| Tiempo de VMI en días, Mediana (rango intercuartílico) | 3,0 (1,0-6,0) |
| Score APACHE II, Mediana (rango intercuartílico) | 13,0 (9,6-20,0) |
| Dosis de propofol en mg, n (%) | 0,0 (0,0-0,0) |
| Dosis de midazolam en mg, Mediana (rango intercuartílico) | 5,0 (5,0-39,8) |
| Dosis de fentanilo en mcg, Mediana (rango intercuartílico) | 885,0 (100-2587,5) |
| Dosis diaria de fentanilo en mcg, Mediana (rango intercuartílico) | 156,7 (50,0-685,1) |
En cuanto a las características clínicas, el 67,3% de los ingresos fueron de causa no quirúrgica (n=105) y el 32,0% se encontraba en estado séptico (n=49). Las comorbilidades más frecuentes fueron hipertensión arterial (52,6%; n=82), diabetes mellitus (32,1%; n=50), enfermedad pulmonar obstructiva crónica (28,9%; n=45), hipotiroidismo (26,3%; n=41), enfermedad renal crónica e insuficiencia cardiaca congestiva (14,2% cada una; n=22), inmunosupresión (21,2%; n=33), alcoholismo (5,2%; n=8) y farmacodependencia (3,2%; n=5).
La mediana de duración de la VMI fue de 3,0 días (RIC 1,0–9,0). El puntaje APACHE II mostró una mediana de 13,0 puntos (RIC 9,6–20,0). En relación con los sedantes, se registró una mediana de dosis de propofol de 0,0mg (RIC 0,0–0,0), ya que fue utilizado solo en 4 casos con dosis entre 21 y 495mg. Para midazolam, la mediana fue de 5,0mg (RIC 5,0–39,8); para fentanilo, 885,0 mcg (RIC 100,0–2.587,5), y la dosis diaria de fentanilo fue de 156,7 mcg (RIC 50,0–685,1). Se encontró una diferencia estadísticamente significativa en la dosis de midazolam entre los grupos SI y EV (p <0,005), evaluada mediante la prueba de U de Mann-Whitney (tabla 2).
Comparación dosis de sedantes en pacientes SI vs. EV en la muestra
| Variable | Valor de p* |
|---|---|
| Dosis de midazolam | 0,100 |
| Dosis de propofol | 0,574 |
| Dosis de fentanilo | <0,001 |
| Dosis de dosis diaria de fentanilo | 0,905 |
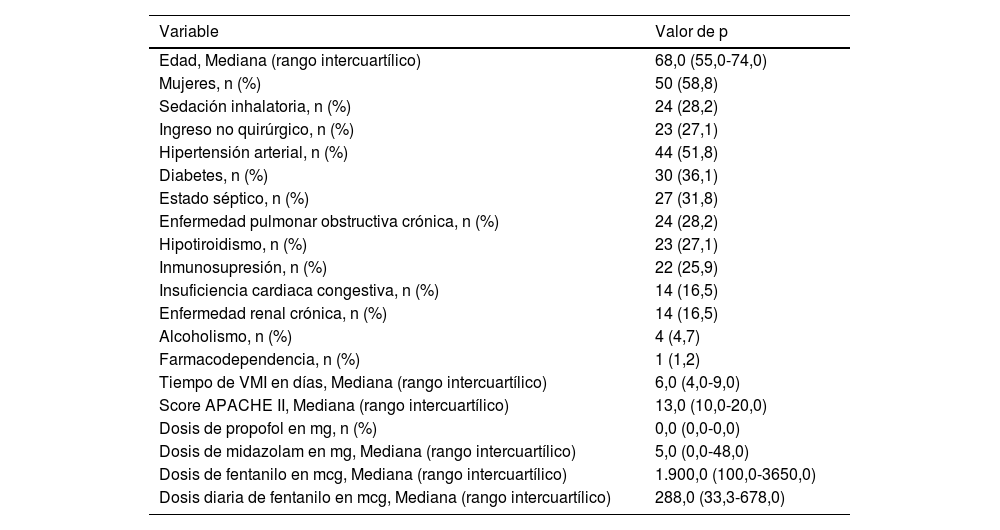
En el subgrupo de pacientes con VMI ≥ 48 horas (n=85), se observó una mediana de edad de 68,0 años (RIC 55,0–74,0), siendo mujeres el 58,8% (n=50). El 28,2% recibió SI (n=24). Las principales comorbilidades se mantuvieron con frecuencias similares: hipertensión (51,8%), diabetes (31,8%), enfermedad pulmonar obstructiva crónica (EPOC) (28,2%), hipotiroidismo (25,9%), inmunosupresión (27,1%), ERC e ICC (16,5%), alcoholismo (4,7%) y farmacodependencia (1,2%) (tabla 3). En este grupo, la mediana de duración de la VMI fue de 6,0 días (RIC 4,0–9,0), y la mediana del APACHE II fue de 13,0 puntos (RIC 10,0–20,0).
Sexo, edad, características clínicas y dosis en pacientes con VMI> 48 horas
| Variable | Valor de p |
|---|---|
| Edad, Mediana (rango intercuartílico) | 68,0 (55,0-74,0) |
| Mujeres, n (%) | 50 (58,8) |
| Sedación inhalatoria, n (%) | 24 (28,2) |
| Ingreso no quirúrgico, n (%) | 23 (27,1) |
| Hipertensión arterial, n (%) | 44 (51,8) |
| Diabetes, n (%) | 30 (36,1) |
| Estado séptico, n (%) | 27 (31,8) |
| Enfermedad pulmonar obstructiva crónica, n (%) | 24 (28,2) |
| Hipotiroidismo, n (%) | 23 (27,1) |
| Inmunosupresión, n (%) | 22 (25,9) |
| Insuficiencia cardiaca congestiva, n (%) | 14 (16,5) |
| Enfermedad renal crónica, n (%) | 14 (16,5) |
| Alcoholismo, n (%) | 4 (4,7) |
| Farmacodependencia, n (%) | 1 (1,2) |
| Tiempo de VMI en días, Mediana (rango intercuartílico) | 6,0 (4,0-9,0) |
| Score APACHE II, Mediana (rango intercuartílico) | 13,0 (10,0-20,0) |
| Dosis de propofol en mg, n (%) | 0,0 (0,0-0,0) |
| Dosis de midazolam en mg, Mediana (rango intercuartílico) | 5,0 (0,0-48,0) |
| Dosis de fentanilo en mcg, Mediana (rango intercuartílico) | 1.900,0 (100,0-3650,0) |
| Dosis diaria de fentanilo en mcg, Mediana (rango intercuartílico) | 288,0 (33,3-678,0) |
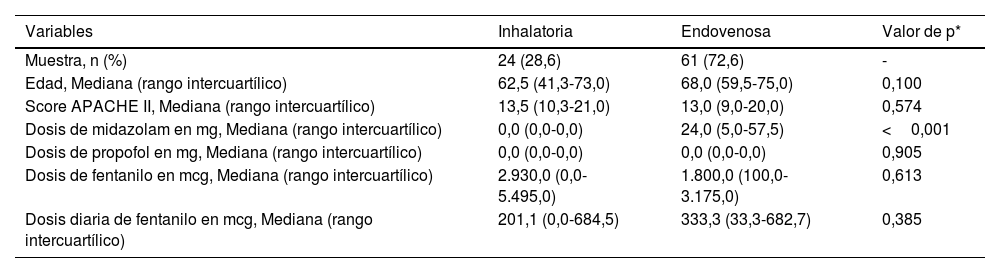
Las dosis de sedantes en este subgrupo mostraron una mediana de 0,0mg para propofol (RIC 0,0–0,0), 5,0mg para midazolam (RIC 0,0–48,0), 1.900 mcg para fentanilo (RIC 100–3.650), y una dosis diaria de fentanilo de 288,0 mcg (RIC 33,3–678,0). En los pacientes con SI, la edad fue de 62,5 años (RIC 41,3–73,0), APACHE II de 13,5 puntos (RIC 10,3–21,0), midazolam y propofol con medianas de 0,0mg (RIC 0,0–0,0), fentanilo de 2.930 mcg (RIC 0,0–5.495), y dosis diaria de fentanilo de 201,1 mcg (RIC 0,0–684,5) (tabla 4).
Comparación edad, APACHE II, SOFA, tiempo de VMI y dosis
| Variables | Inhalatoria | Endovenosa | Valor de p* |
|---|---|---|---|
| Muestra, n (%) | 24 (28,6) | 61 (72,6) | - |
| Edad, Mediana (rango intercuartílico) | 62,5 (41,3-73,0) | 68,0 (59,5-75,0) | 0,100 |
| Score APACHE II, Mediana (rango intercuartílico) | 13,5 (10,3-21,0) | 13,0 (9,0-20,0) | 0,574 |
| Dosis de midazolam en mg, Mediana (rango intercuartílico) | 0,0 (0,0-0,0) | 24,0 (5,0-57,5) | <0,001 |
| Dosis de propofol en mg, Mediana (rango intercuartílico) | 0,0 (0,0-0,0) | 0,0 (0,0-0,0) | 0,905 |
| Dosis de fentanilo en mcg, Mediana (rango intercuartílico) | 2.930,0 (0,0-5.495,0) | 1.800,0 (100,0-3.175,0) | 0,613 |
| Dosis diaria de fentanilo en mcg, Mediana (rango intercuartílico) | 201,1 (0,0-684,5) | 333,3 (33,3-682,7) | 0,385 |
Comparado con el grupo EV, los pacientes con SI requirieron menores dosis de midazolam, propofol y fentanilo, siendo significativa la diferencia para midazolam (p <0,001), determinada mediante la prueba de U de Mann-Whitney. No se reportaron complicaciones relacionadas con los sedantes en el grupo SI. Finalmente, se intentó ajustar un modelo de regresión logística múltiple, el cual no mostró asociaciones significativas entre las variables clínicas y el tipo de sedación, manteniéndose el mismo patrón observado en los análisis bivariados.
DiscusiónEl hallazgo principal de este estudio retrospectivo fue que los pacientes con VMI ≥ 48 horas que recibieron SI requirieron menores dosis adicionales de midazolam, propofol y una menor dosis total de fentanilo, en comparación con aquellos bajo sedación EV. Este resultado refuerza la hipótesis de que la SI podría representar una estrategia efectiva para reducir el consumo de opioides en la UCI, en línea con estudios previos que reportan un menor uso de morfina y remifentanilo en pacientes sedados con agentes inhalados25,26,39.
Las propiedades farmacológicas de la SI —inicio y recuperación rápidos, escaso metabolismo sistémico y eliminación pulmonar— permiten una sedación predecible, con menor riesgo de acumulación y abstinencia, lo cual favorece una reducción en la necesidad de opioides y otros sedantes31–33. Además, su perfil antiinflamatorio, cardioprotector y broncodilatador aporta beneficios adicionales en pacientes críticos, particularmente aquellos con SDRA, broncoespasmo, status epiléptico o sedación prolongada30-32,36.
Kermad et al. encontraron que los pacientes bajo SI requerían dosis significativamente menores de opioides (mediana 720mg equivalentes de morfina) frente al grupo con EV (1.080mg; p <0,001)26. De forma similar, se ha demostrado una menor necesidad de remifentanilo cuando se utiliza sevoflurano vs. propofol25. Si bien nuestra cohorte no incluyó sevoflurano ni comparó indicadores como PaO2/FiO2 o tiempo de extubación, se observó una reducción clínica significativa en la dosis de midazolam, y una tendencia hacia menor uso de fentanilo en el grupo SI, especialmente tras excluir a los pacientes con VMI> 48 horas.
El potencial ahorro en el uso de opioides no solo implica un beneficio clínico, sino también económico. Estudios comparativos han reportado menores costos totales en pacientes sedados con SI vs. midazolam, debido a menor requerimiento de infusión continua y reducción del tiempo de recuperación33-37. Incluso en escenarios como el SDRA por COVID-19, la SI con sevoflurano se ha asociado a mejor oxigenación y menor mortalidad, ampliando su aplicabilidad en cuidados críticos38.
Aunque el presente estudio no logró significación estadística para todas las variables en el modelo ajustado, probablemente por el tamaño limitado del grupo SI, se observó una diferencia clínica relevante en el requerimiento de sedantes y opioides. Este hallazgo respalda la necesidad de considerar la SI como una herramienta potencialmente útil para mitigar la exposición prolongada a opioides en la UCI, reducir riesgos de dependencia y mejorar la eficiencia en la atención.
En conclusión, nuestros resultados sugieren que la SI puede contribuir significativamente a la reducción del uso de opioides en pacientes con VMI prolongada. Dado su perfil farmacológico favorable y el creciente cuerpo de evidencia que respalda sus beneficios, la SI debería ser considerada como una alternativa viable en protocolos de sedación en cuidados intensivos, especialmente en contextos donde se busca optimizar el balance entre eficacia analgésica y minimización del riesgo de dependencia.
Este artículo no ha recibido financiación para su elaboración ni su publicación.
Los autores declaran no tener ningún conflicto de intereses.