Las constantes vitales detectan la presencia de hemorragia al perder grandes cantidades de sangre, lo que comporta una gran morbimortalidad. El Shock Index (SI) es un parámetro que detecta el sangrado con puntos de corte de 0,9. El objetivo de este estudio es valorar si un punto de corte de≥0,8 es más sensible para detectar sangrado oculto, permitiendo iniciar maniobras terapéuticas más precoces.
MétodosEstudio analítico de validación del SI que incluye pacientes politraumatizados graves mayores de 16 años. Se registran constantes vitales y escalas predictivas de sangrado: SI, Assessment of Blood Consumption score y Pulse Rate Over Pressure score. Se analiza la relación del SI con 5 marcadores predictivos de sangrado: necesidad de transfusión masiva, embolización angiográfica, control del sangrado quirúrgico, muerte por shock hipovolémico y «sangrado activo» (presencia de al menos uno de los 4 marcadores anteriores en un paciente).
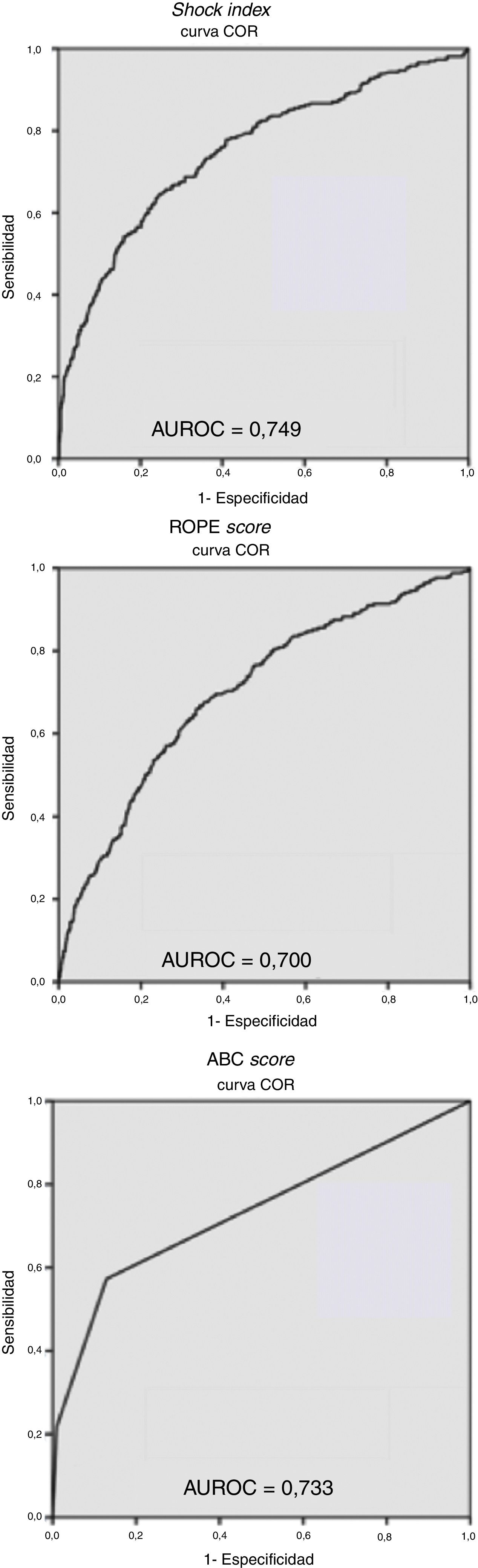
ResultadosRecogida prospectiva de datos de 1.402 pacientes politraumatizados durante 10 años. El Injury Severity Score medio fue de 20,9 (DE 15,8). Hubo una mortalidad del 10%. El SI medio fue de 0,73 (DE 0,29). En total presentaron «sangrado activo» el 18,7% de la serie. El SI medio en los pacientes con «sangrado activo» fue de 0,87, mientras que las constantes vitales estaban dentro de la normalidad. El área bajo la curva ROC del SI para el «sangrado activo» fue de 0,749.
ConclusionesEl SI con un punto de corte≥0,8 es más sensible que aquel con el punto de corte≥0,9 y permite iniciar maniobras de reanimación más precoces en los pacientes con sangrado oculto.
Vital signs indicate the presence of bleeding only after large amounts of blood have been lost, with high morbidity and mortality. The Shock Index (SI) is a hemorrhage indicator with a cut-off point for the risk of bleeding at 0.9. The aim of this study is to assess whether a cut-off of≥0.8 is more sensitive for detecting occult bleeding, providing for early initiation of therapeutic maneuvers.
MethodsSI analytical validation study of severe trauma patients older than 16 years of age. Vital signs were recorded, and scales for predicting bleeding included: SI, Assessment of Blood Consumption score, and Pulse Rate Over Pressure score. The relationship between the SI and 5 markers for bleeding was analyzed: need for massive transfusion, angiographic embolization, surgical bleeding control, death due to hypovolemic shock, and the overall predictor «active bleeding» (defined as the presence of at least one of the 4 markers above).
ResultsData from 1.402 trauma patients were collected prospectively over a period of 10 years. The mean Injury Severity Score was 20.9 (SD 15.8). The mortality rate was 10%. The mean SI was 0.73 (SD 0.29). «Active bleeding» was present in 18.7% of patients. The SI area under the ROC curve for «active bleeding» was 0.749.
ConclusionsAn SI cut-off point≥0.8 is more sensitive than≥0.9 and allows for earlier initiation of resuscitation maneuvers in patients with occult active bleeding.
El politraumatismo constituye una de las principales causas de muerte en la población con edades comprendidas entre uno y 44 años1. El shock hemorrágico es la principal causa evitable de muerte después de un traumatismo, causando alrededor de un tercio de los 6 millones de muertes postraumatismo anuales2. Después de un traumatismo grave, la detección precoz del estado de shock es necesaria para proporcionar un manejo adecuado que ayude a disminuir la morbimortalidad3. Los marcadores clásicos de la estabilidad hemodinámica son las características cutáneas, la frecuencia cardíaca, la tensión arterial y la diuresis4. Desgraciadamente estos parámetros pueden verse alterados debido a dolor, hipotermia, shock neurogénico, shock cardiogénico, medicación analgésica o betabloqueante, haciendo que la interpretación de las constantes vitales se vea alterada5. Otra limitación que podemos encontrar al analizar estos parámetros es su modificación tardía; se registra una elevación de la frecuencia cardíaca por encima de 100-120lpm cuando el paciente ha perdido alrededor de 750-1.500ml de volemia, o bien una disminución de la tensión arterial cuando el paciente ha perdido entre 1.500 y 2.000ml de volemia6. El retraso en la identificación precoz de los pacientes con hemorragia activa a menudo retrasa terapias imprescindibles para el control del sangrado (activación del protocolo de transfusión masiva [PTM], embolización angiográfica, cirugía urgente, etc.) y es causa de mortalidad en la atención inicial7. Por esta razón en los últimos años se han propuesto distintos mecanismos para identificar a los pacientes con probabilidad de sangrado elevado, como por ejemplo el Trauma Associated Severe Hemorrhage Score8, el Assessment of Blood Consumption score (ABC)9, el McLaughlin score10, el Pulse Rate Over Pressure score (ROPE)11,12 y el SI13.
El SI −definido como la división entre la frecuencia cardíaca y la tensión arterial sistólica− se ha propuesto como una herramienta sencilla y precoz para identificar a los pacientes con shock hemorrágico. Se ha considerado un buen indicador de necesidad de transfusión masiva14, para la necesidad de control del foco de sangrado15 e incluso de mortalidad16. Inicialmente se definió el punto de corte≥1 para el shock hipovolémico instaurado, que presenta una mayor especificidad y es más recomendable para su uso a nivel prehospitalario. Con el tiempo se ha ido disminuyendo el umbral para aumentar su capacidad predictiva, centrando la controversia en 2 puntos de corte:≥0,93,13,16 y≥0,815,17, siendo el primero el más utilizado en la literatura actualmente. El principal inconveniente del punto de corte≥0,9 es que, al utilizarlo, corremos el riesgo de perder pacientes que presentan un sangrado oculto; por esa razón se empieza a proponer un punto de corte≥0,8, que es menos restrictivo y permite detectar a los pacientes con sangrado oculto, aunque a cambio realice una selección más amplia de pacientes, con un mayor número de falsos positivos.
El objetivo del estudio es valorar si el punto de corte≥0,8 es más sensible que el≥0,9 para predecir el shock hipovolémico.
MétodosEstudio analítico de validación del SI, unicéntrico, que incluye a los pacientes politraumatizados atendidos en un hospital de tercer nivel, mayores de 16 años, que ingresan en el área de críticos o mueren antes del ingreso en dicha área (a nivel intrahospitalario). Todos los pacientes se han registrado de forma prospectiva en una base de datos diseñada en formato protegido en Access® para evitar la entrada de valores erróneos o fuera de rango. En todo momento se ha seguido la Ley Orgánica de Protección de Datos Personales.
Las variables registradas son: sexo, edad, mecanismo de acción del traumatismo, criterio de gravedad (Injury Severity Score), signos vitales hospitalarios (frecuencia cardíaca, tensión arterial sistólica) y causas de mortalidad. Todos los datos son clínicamente revisados en un momento posterior y de forma cíclica por un comité especializado en la atención de los pacientes politraumatizados.
Se definen las siguientes escalas e índices de predicción de sangrado:
- 1.
SI: división entre la frecuencia cardíaca y la tensión arterial sistólica18. Sus valores normales habituales oscilan entre 0,5 y 0,719.
- 2.
ROPE: división entre la frecuencia cardíaca por la diferencia entre la tensión arterial sistólica y la tensión arterial diastólica. Se ha considerado predictor de transfusión masiva cuando sus valores son≥311,12.
- 3.
ABC: se calcula asignando un valor de 0 o 1 a la presencia de trauma penetrante, eco abdominal dirigida a la valoración del trauma positivo (FAST), tensión arterial sistólica<90mmHg y frecuencia cardíaca>120lpm. Se define como predictor de transfusión masiva para valores≥29,20.
Se definen los siguientes marcadores de sangrado:
- 1.
Activación del PTM.
- 2.
Embolización angiográfica: realizada mediante acceso endovascular.
- 3.
Cirugía para el control del sangrado.
- 4.
Mortalidad por shock hipovolémico.
Para el análisis de regresión se precisa una variable categórica binaria. La variable debe recoger que el paciente esté sangrando o haya sangrado. Para construir esta variable se han utilizado los marcadores de sangrado previamente descritos. Si un paciente presentaba uno o más de los marcadores de sangrado quedaba definido como «sangrado activo» en esta variable que hemos creado de novo. Obviamente un paciente puede tener uno, 2, 3 o 4 marcadores.
Se analiza la relación de SI, ROPE y ABC con los marcadores descritos anteriormente, con distintos grupos etarios (16-64 años y mayores de 65 años) y el tipo de mecanismo lesional (penetrante y cerrado).
Los datos se presentan como media y desviación estándar (DE) en las variables continuas, y como porcentajes en las categóricas.
Análisis estadísticosPara el estudio univariable se utiliza la t de Student en las variables continuas y la Chi cuadrado en las categóricas.
Se obtienen las curvas receiver operating characteristics (ROC) (como representación gráfica de la capacidad discriminativa de una determinada escala a partir de todos sus puntos de corte) y se calculan las áreas bajo la curva ROC (AUROC) para las escalas presentadas con intervalos de confianza del 95%.
Para los puntos de corte≥0,8 y≥0,9 en el SI se calcula la sensibilidad, la especificidad, el valor predictivo positivo y el valor predictivo negativo en relación con la variable «sangrado activo».
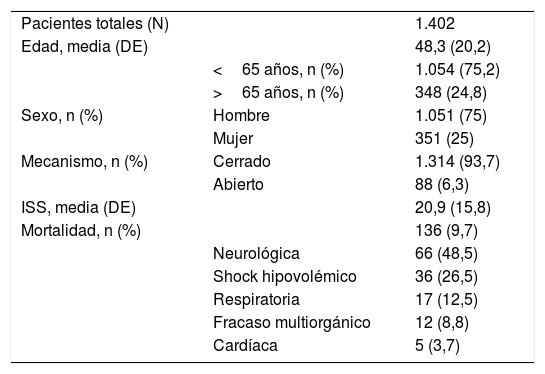
ResultadosDesde marzo de 2006 hasta septiembre de 2016 se registraron 1.402 pacientes politraumatizados atendidos en nuestro centro. La edad media fue de 48,3 años, con un Injury Severity Score medio de 20,9 (DE 15,8). La mortalidad de la serie fue del 10% (136 pacientes), siendo la causa más frecuente la neurológica (48,5%) (tabla 1).
Generalidades
| Pacientes totales (N) | 1.402 | |
| Edad, media (DE) | 48,3 (20,2) | |
| <65 años, n (%) | 1.054 (75,2) | |
| >65 años, n (%) | 348 (24,8) | |
| Sexo, n (%) | Hombre | 1.051 (75) |
| Mujer | 351 (25) | |
| Mecanismo, n (%) | Cerrado | 1.314 (93,7) |
| Abierto | 88 (6,3) | |
| ISS, media (DE) | 20,9 (15,8) | |
| Mortalidad, n (%) | 136 (9,7) | |
| Neurológica | 66 (48,5) | |
| Shock hipovolémico | 36 (26,5) | |
| Respiratoria | 17 (12,5) | |
| Fracaso multiorgánico | 12 (8,8) | |
| Cardíaca | 5 (3,7) |
DE: desviación estándar; ISS: Injury Severity Score.
El SI medio fue de 0,73 (DE 0,29). Había 266 pacientes (19%) con un SI superior a 0,9 y 395 pacientes (28,2%) con un SI superior a 0,8.
El ROPE medio fue de 2 (DE 1,3) y el ABC medio fue de 0,3 (DE 0,6).
Se activó el PTM en 60 pacientes (4,3%). Se realizó una arteriografía con embolización en 109 pacientes (7,8%) y se tuvo que intervenir para controlar el sangrado a 160 pacientes (11,4%). En total presentaron «sangrado activo» 262 pacientes, que representan el 18,7% de la serie. Un 2,6% de los pacientes fueron exitus por shock hipovolémico (tabla 2).
Marcadores de sangrado
| Activación del PTM, n (%) | 60 (4,3) |
| Embolización angiográfica, n (%) | 109 (7,8) |
| Cirugía para el control del sangrado, n (%) | 160 (11,4) |
| Mortalidad por shock hipovolémico, n (%) | 36 (2,6) |
| Variable «sangrado activo» positiva, n (%) | 262 (18,7) |
PTM: protocolo de transfusión masiva.
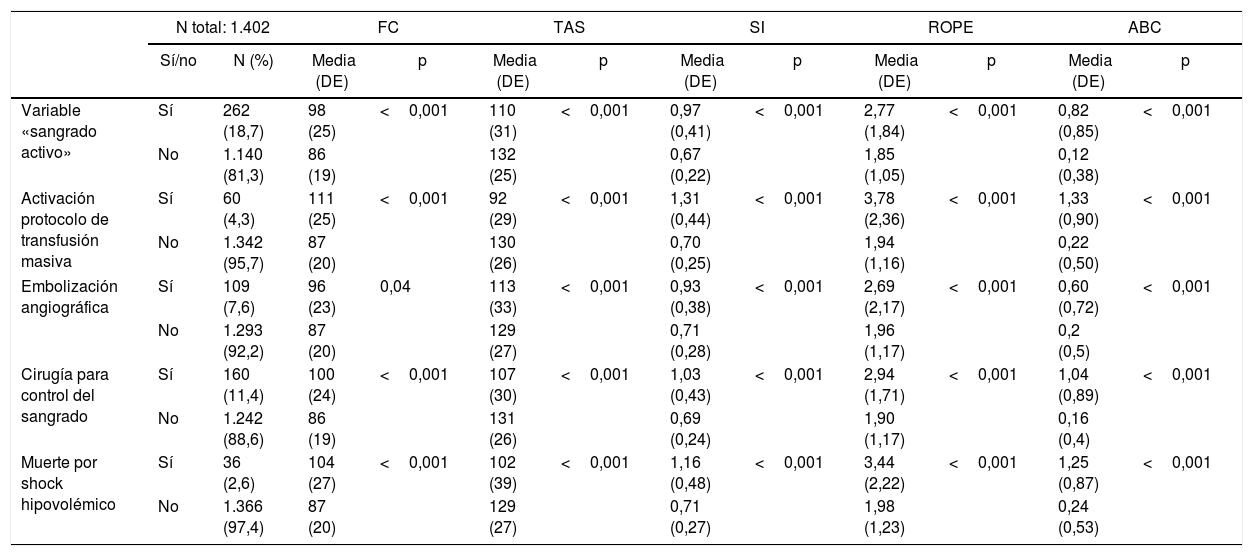
La relación de las constantes vitales (frecuencia cardíaca y tensión arterial sistólica) y las distintas escalas predictivas de sangrado con los marcadores de sangrado se pueden consultar en la tabla 3, junto con las significaciones. El valor medio del SI se encuentra por encima del punto de corte definido en la literatura (≥0,9) en todos los pacientes con sangrado.
Relación de los marcadores de sangrado con las constantes vitales y las escalas analizadas
| N total: 1.402 | FC | TAS | SI | ROPE | ABC | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Sí/no | N (%) | Media (DE) | p | Media (DE) | p | Media (DE) | p | Media (DE) | p | Media (DE) | p | |
| Variable «sangrado activo» | Sí | 262 (18,7) | 98 (25) | <0,001 | 110 (31) | <0,001 | 0,97 (0,41) | <0,001 | 2,77 (1,84) | <0,001 | 0,82 (0,85) | <0,001 |
| No | 1.140 (81,3) | 86 (19) | 132 (25) | 0,67 (0,22) | 1,85 (1,05) | 0,12 (0,38) | ||||||
| Activación protocolo de transfusión masiva | Sí | 60 (4,3) | 111 (25) | <0,001 | 92 (29) | <0,001 | 1,31 (0,44) | <0,001 | 3,78 (2,36) | <0,001 | 1,33 (0,90) | <0,001 |
| No | 1.342 (95,7) | 87 (20) | 130 (26) | 0,70 (0,25) | 1,94 (1,16) | 0,22 (0,50) | ||||||
| Embolización angiográfica | Sí | 109 (7,6) | 96 (23) | 0,04 | 113 (33) | <0,001 | 0,93 (0,38) | <0,001 | 2,69 (2,17) | <0,001 | 0,60 (0,72) | <0,001 |
| No | 1.293 (92,2) | 87 (20) | 129 (27) | 0,71 (0,28) | 1,96 (1,17) | 0,2 (0,5) | ||||||
| Cirugía para control del sangrado | Sí | 160 (11,4) | 100 (24) | <0,001 | 107 (30) | <0,001 | 1,03 (0,43) | <0,001 | 2,94 (1,71) | <0,001 | 1,04 (0,89) | <0,001 |
| No | 1.242 (88,6) | 86 (19) | 131 (26) | 0,69 (0,24) | 1,90 (1,17) | 0,16 (0,4) | ||||||
| Muerte por shock hipovolémico | Sí | 36 (2,6) | 104 (27) | <0,001 | 102 (39) | <0,001 | 1,16 (0,48) | <0,001 | 3,44 (2,22) | <0,001 | 1,25 (0,87) | <0,001 |
| No | 1.366 (97,4) | 87 (20) | 129 (27) | 0,71 (0,27) | 1,98 (1,23) | 0,24 (0,53) | ||||||
ABC: Assessment of Blood Consumption; DE: desviación estándar; FC: frecuencia cardíaca; ROPE: Pulse Rate Over Pressure; SI: Shock Index; TAS: tensión arterial sistólica.
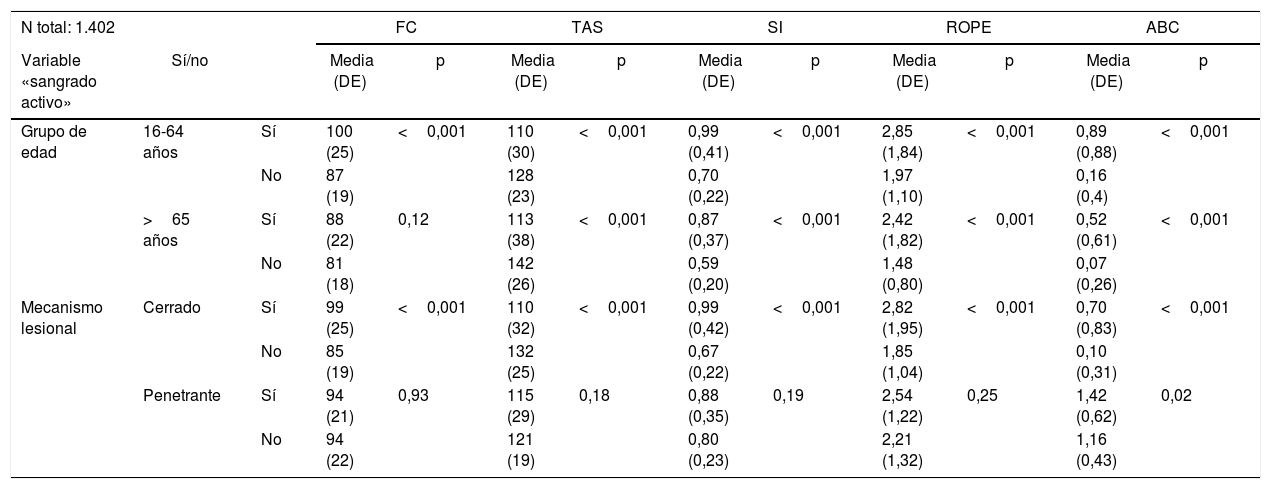
Aplicando la variable «sangrado activo» a los 2 grupos de edad, pacientes jóvenes (16-64 años) y ancianos (>65 años), vemos que las constantes vitales y las escalas evaluadas presentan una relación estadísticamente significativa, exceptuando la frecuencia cardíaca en ancianos, que no es significativa (tabla 4). En pacientes de edad avanzada cabe destacar que las constantes vitales medias se mantienen dentro de los valores de normalidad clínica, mientras que el SI es≥0,8.
Relación de la variable «sangrado activo» con el grupo de edad y el mecanismo lesional
| N total: 1.402 | FC | TAS | SI | ROPE | ABC | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Variable «sangrado activo» | Sí/no | Media (DE) | p | Media (DE) | p | Media (DE) | p | Media (DE) | p | Media (DE) | p | |
| Grupo de edad | 16-64 años | Sí | 100 (25) | <0,001 | 110 (30) | <0,001 | 0,99 (0,41) | <0,001 | 2,85 (1,84) | <0,001 | 0,89 (0,88) | <0,001 |
| No | 87 (19) | 128 (23) | 0,70 (0,22) | 1,97 (1,10) | 0,16 (0,4) | |||||||
| >65 años | Sí | 88 (22) | 0,12 | 113 (38) | <0,001 | 0,87 (0,37) | <0,001 | 2,42 (1,82) | <0,001 | 0,52 (0,61) | <0,001 | |
| No | 81 (18) | 142 (26) | 0,59 (0,20) | 1,48 (0,80) | 0,07 (0,26) | |||||||
| Mecanismo lesional | Cerrado | Sí | 99 (25) | <0,001 | 110 (32) | <0,001 | 0,99 (0,42) | <0,001 | 2,82 (1,95) | <0,001 | 0,70 (0,83) | <0,001 |
| No | 85 (19) | 132 (25) | 0,67 (0,22) | 1,85 (1,04) | 0,10 (0,31) | |||||||
| Penetrante | Sí | 94 (21) | 0,93 | 115 (29) | 0,18 | 0,88 (0,35) | 0,19 | 2,54 (1,22) | 0,25 | 1,42 (0,62) | 0,02 | |
| No | 94 (22) | 121 (19) | 0,80 (0,23) | 2,21 (1,32) | 1,16 (0,43) | |||||||
ABC: Assessment of Blood Consumption; DE: desviación estándar; FC: frecuencia cardíaca; ROPE: Pulse Rate Over Pressure; SI: Shock Index; TAS: tensión arterial sistólica.
La relación de las constantes vitales y las escalas evaluadas con el mecanismo lesional muestra una relación estadísticamente significativa con el traumatismo cerrado, pero con el traumatismo penetrante tan solo es estadísticamente significativo para el ABC score.
Al relacionar los puntos de corte del SI estudiados vemos como se relacionan de forma estadísticamente significativa con todas las variables, mostrando una relación no significativa con el traumatismo penetrante (tabla 5).
Relación de los puntos de corte del Shock Index con las distintas variables analizadas
| N total: 1.402 | SI<0,8 (n=1.007) | SI≥0,8 (n=395) | SI<0,9 (n=1.136) | SI≥0,9 (n=266) | ||||
|---|---|---|---|---|---|---|---|---|
| Sí/no | % | % | p | % | % | p | ||
| Pacientes con «sangrado activo» | Sí | 7,6 | 11,0 | <0,001 | 10,1 | 8,6 | <0,001 | |
| No | 64,2 | 17,2 | 71,0 | 10,3 | ||||
| Activación protocolo de transfusión masiva | Sí | 0,7 | 3,6 | <0,001 | 0,8 | 3,5 | <0,001 | |
| No | 71,1 | 24,6 | 80,2 | 15,5 | ||||
| Embolización angiográfica | Sí | 3,2 | 4,6 | <0,001 | 4,4 | 3,4 | <0,001 | |
| No | 68,6 | 23,6 | 76,6 | 15,6 | ||||
| Cirugía para control del sangrado | Sí | 4,1 | 7,4 | <0,001 | 5,4 | 6,0 | <0,001 | |
| No | 67,7 | 20,8 | 75,6 | 13,0 | ||||
| Muerte por shock hipovolémico | Sí | 0,5 | 2,1 | <0,001 | 1,0 | 1,6 | <0,001 | |
| No | 71,3 | 26,1 | 80,0 | 17,4 | ||||
| Variable «sangrado activo» | Grupo de edad | 16-64 años | 5,8 | 9,3 | <0,001 | 7,7 | 7,4 | <0,001 |
| >65 años | 1,9 | 1,7 | <0,001 | 2,4 | 1,2 | <0,001 | ||
| Mecanismo lesional | Cerrado | 6,1 | 9,4 | <0,001 | 9,0 | 7,4 | <0,001 | |
| Penetrante | 1,6 | 1,6 | 0,39 | 2,0 | 1,2 | 0,33 | ||
SI: Shock Index.
Chi cuadrado de Pearson para valores de Shock Index≥0,8 y≥0,9 para las variables estudiadas.
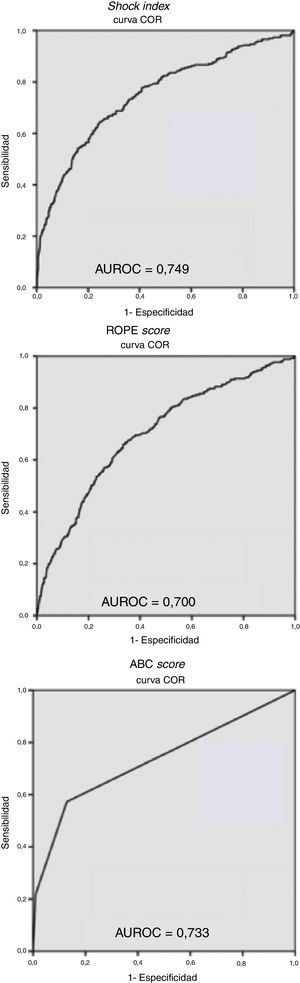
Las curvas ROC (fig. 1) obtenidas para las escalas estudiadas muestran una mayor capacidad predictiva para el SI, con una AUROC de 0,749, mientras que el ABC score y el ROPE score presentan AUROC inferiores, de 0,733 y 0,700, respectivamente.
Curvas ROC y áreas bajo la curva (AUROC) del Shock Index, del ROPE score y del ABC score.
Esta figura incluye la tabla 6, donde se representan los valores de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo de los 2 puntos de corte del Shock Index analizados.
Finalmente, al valorar la capacidad predictiva como prueba de los 2 puntos de corte de SI analizados, podemos ver como el punto de corte≥0,8 presenta una mayor sensibilidad que el punto de corte≥0,9, siendo del 59,2 y del 46,2%, respectivamente.
DiscusiónEl manejo de los pacientes politraumatizados ha mejorado a lo largo de los años gracias a un conocimiento más exhaustivo de los mecanismos que contribuyen a aumentar la morbimortalidad. Desde la primera definición del SI en el año 1967 por Allgöwer y Burri18, numerosos autores han investigado su valor predictivo en referencia a distintos resultados (mortalidad, PTM, días de hospitalización, complicaciones sépticas, etc.)14–16,21.
Con el estudio hemos demostrado que el punto de corte del SI≥0,8 se relaciona con todas las variables analizadas («sangrado activo», activación del PTM, embolización angiográfica, cirugía para el control del sangrado y muerte por shock hipovolémico). La aplicabilidad clínica de estos resultados presenta una gran importancia, ya que los pacientes que presentan valores de SI por encima de 0,8 tienen una probabilidad de sangrado elevada, incluso cuando las constantes vitales se encuentran dentro de la normalidad.
Distintas publicaciones han analizado la aplicabilidad del SI en pacientes de edad avanzada, cuyas constantes vitales pueden parecer normales ante el shock hemorrágico22,23, obteniendo resultados variados, ya que en algunas publicaciones se considera un buen marcador24 y en otras se propone el uso de puntos de corte distintos en función del grupo de edad4,21. Si analizamos los resultados obtenidos al diferenciar 2 grupos de edad (16-64 años y>65 años), vemos como el SI≥0,8 tiene la misma capacidad predictiva que el resto de las variables analizadas. La frecuencia cardíaca máxima disminuye a medida que los pacientes envejecen, por lo que la capacidad de taquicardizarse en respuesta al sangrado es menor. Esta población presenta una incidencia mayor de hipertensión, considerando hipotensiva una tensión arterial sistólica menor de 110mmHg después de un traumatismo en ancianos23. Por esta razón, las constantes vitales no se consideran fiables en la evaluación de los pacientes geriátricos, y sería recomendable el uso del SI en estos casos.
En algunas publicaciones se han analizado por separado los distintos marcadores de reanimación hemodinámica para traumatismos penetrantes y cerrados25,26, sin hallar diferencias significativas. Las variables estudiadas y el punto de corte de 0,8 del SI son buenos predictores de sangrado en pacientes que han tenido un traumatismo cerrado, pero no se han detectado resultados estadísticamente significativos cuando se aplican al traumatismo penetrante. Estas diferencias pueden ser debidas a una menor incidencia de traumatismo penetrante en nuestra serie, que tan solo representa el 6,3% de los pacientes atendidos, frente al 50-70% de las publicaciones que comparan ambos mecanismos25,26. Si además tomamos en consideración que en los traumatismos penetrantes realizamos más exploraciones quirúrgicas, independientemente de la estabilidad hemodinámica, es más probable que la relación no sea estadísticamente significativa. Por esta razón, no podemos considerar el SI como un buen predictor de sangrado en los pacientes con traumatismo penetrante de nuestra serie.
La evaluación de las curvas ROC para las distintas escalas evaluadas muestra como el SI presenta una mayor capacidad predictiva de sangrado que el resto, obteniendo una AUROC de 0,749.
Diferenciando los 2 puntos de corte de SI analizados, el SI≥0,8 presenta una sensibilidad de 59,2, una especificidad de 79 y un valor predictivo negativo de 89,4. Al disminuir el punto de corte aumentamos la sensibilidad para detectar sangrado, manteniendo valores de especificidad aceptables, pudiendo afirmar que el punto de corte de 0,8 permite identificar el sangrado de una forma correcta15.
Como podemos ver en la tabla 6, incluida en la figura 1, el SI con un punto de corte de 0,8 consigue un valor predictivo negativo aún superior al punto de corte de 0,9 y, por tanto, permite afirmar con mayor seguridad que un paciente con un SI menor de 0,8 realmente no está sangrando.
Valores de sensibilidad, especificidad, VPP y VPN para los puntos de corte analizados. Para una prevalencia de 18,7
| SI ≥ 0,8 | SI ≥ 0,9 | |||
|---|---|---|---|---|
| % | IC 95% | % | IC 95% | |
| Sensibilidad | 59,2 | 53,2-65,1 | 46,2 | 40,2-52,2 |
| Especificidad | 79,0 | 76,6-81,3 | 87,3 | 85,4-89,2 |
| VPP | 39,2 | 35,4-43,1 | 45,5 | 41,6-49,4 |
| VPN | 89,4 | 87,2-91,6 | 87,6 | 85,3-90,0 |
VPP: valor predictivo positivo; VPN: valor predictivo negativo.
La limitación del estudio viene condicionada por las pérdidas en la recogida de datos. En nuestro centro no se registra de forma protocolaria el exceso de base de los pacientes, por esta razón no ha sido posible aplicar el Trauma Associated Severe Hemorrhage Score (considerado uno de los mejores en la actualidad) y así poder compararlo con el resto de las escalas utilizadas.
Como conclusión, podemos afirmar que en la atención a pacientes politraumatizados con mecanismo lesional cerrado es mejor fijar un SI≥0,8; así, evitaremos la pérdida de pacientes potencialmente graves con constantes vitales aparentemente normales.
Conflicto de interesesTodos los autores niegan la existencia de conflicto de intereses.