INTRODUCCIÓN
El término síndrome de apneas del sueño fue introducido por Guilleminault et al1 para definir sujetos con apneas obstructivas y excesiva somnolencia durante el día. Una apnea se definió como un cese completo de la señal respiratoria de al menos 10 s de duración y hoy día se acepta como apnea el cese o disminución de la señal respiratoria mayor del 90%. Las definiciones actuales de los principales eventos respiratorios recomendadas por el Consenso Español de Síndrome de Apneas-Hipopneas durante el Sueño (SAHS) se muestran en la tabla 12.
En el momento actual, el SAHS se define como un cuadro de somnolencia excesiva, trastornos cognitivo-conductuales, respiratorios, cardíacos, metabólicos o inflamatorios secundarios a episodios repetidos de obstrucción de la vía aérea superior (VAS) durante el sueño. Estos episodios se miden con el índice de alteraciones respiratorias (IAR), definido como número de apneas, hipopneas y esfuerzos respiratorios asociados a microdespertares. Un IAR $ 5 asociado a síntomas relacionados con la enfermedad y no explicados por otras causas confirma el diagnóstico de SAHS2.
Los mecanismos fisiopatológicos del SAHS son complejos. El estrechamiento o colapso de la vía aérea usualmente ocurre en la orofaringe, zona en la que no existe soporte rígido. La estabilidad en el calibre de la VAS depende de la acción de los músculos dilatadores orofaríngeos y abductores, que normalmente son activados de forma rítmica durante cada inspiración. La VAS es sometida a colapso cuando la fuerza producida por estos músculos, para un área de sección determinada, es sobrepasada por la presión negativa generada por la actividad inspiratoria del diafragma y los músculos intercostales3. Los factores que favorecen el colapso incluyen el estrechamiento de la VAS (factor anatómico), una pérdida excesiva del tono muscular (factor muscular) y el defecto en los reflejos protectores (factor neurológico)4.
El SAHS es una afección frecuente, con una prevalencia entre el 2 y el 4%5, se asocia con importante morbilidad: accidentes de tráfico, hipertensión arterial, deterioro de la calidad de vida, desarrollo de enfermedades cardivasculares y cerebrovasculares y tiene un tratamiento efectivo demostrado, como es la presión positiva continua (CPAP) en la VAS6,7.
En la práctica diaria el número de pacientes diagnosticados de SAHS depende de la disponibilidad de medios técnicos adecuados, el número de laboratorios de sueño y la accesibilidad a éstos8-10. El SAHS está infradiagnosticado; en 1997 Young et al11 estimaban que el 93% de las mujeres y el 82% de los varones con SAHS moderado-severo de EE.UU. permanecían sin diagnosticar; diferentes estudios realizados evidencian que en España en el año 2003 había entre 1.200.000 y 2.150.000 sujetos con un SAHS relevante y subsidiarios de ser tratados, de los cuales tan sólo se ha diagnosticado y tratado entre el 5 y el 9%9.
El papel del médico de atención primaria es fundamental, tanto en el diagnóstico de sospecha como en el seguimiento y control de los pacientes con SAHS, dada sus mayores accesibilidad y conocimiento integral de los pacientes derivados de su actuación médica diaria.
DIAGNÓSTICO PRECOZ
El diagnóstico de sospecha del SAHS se realizará a partir de una historia clínica compatible. No existe ningún síntoma específico de SAHS. Los síntomas del SAHS son el resultado de episodios repetidos de obstrucción parcial o completa de la VAS durante el sueño que condicionan hipoxia intermitente, que puede ocasionar la aparición de problemas cardiovasculares y la distorsión de la arquitectura del sueño. Durante el sueño ser repite muchas veces el mismo ciclo: sueño, apnea-hipopnea, cambios gasométricos, despertar transitorio y fin de la apnea-hipopnea. Los síntomas del SAHS son mayoritariamente subjetivos y se desarrollan progresivamente en el tiempo; no es inusual que los pacientes no reconozcan sus síntomas o sólo cuando mejoran, una vez tratados, reconozcan su situación previa; pueden dividirse en dos grandes grupos: manifestaciones neuropsiquiátricas y cardiorrespiratorias12.
Frecuentemente, los pacientes con SAHS refieren síntomas diurnos, mientras sus parejas refieren sus comportamientos durante la noche, de forma que la investigación clínica no se considerará completa si no se realiza en presencia de la pareja13.
El ronquido nocturno es el más prominente de los síntomas nocturnos y varía de intensidad y de calidad dependiendo del momento de la noche y el estadio de sueño, la posición del cuerpo, la tasa de flujo y las estructuras anatómicas individuales: nariz y faringe. El ronquido es uno de los síntomas cardinales del SAHS y frecuentemente está presente años antes de otros síntomas. Muy frecuentemente los compañeros de cama han observado que el ronquido, es periódicamente interrumpido por pausas respiratorias que finalizan con una respiración ruidosa, y algunos pacientes refieren despertares con sensación de ahogo.
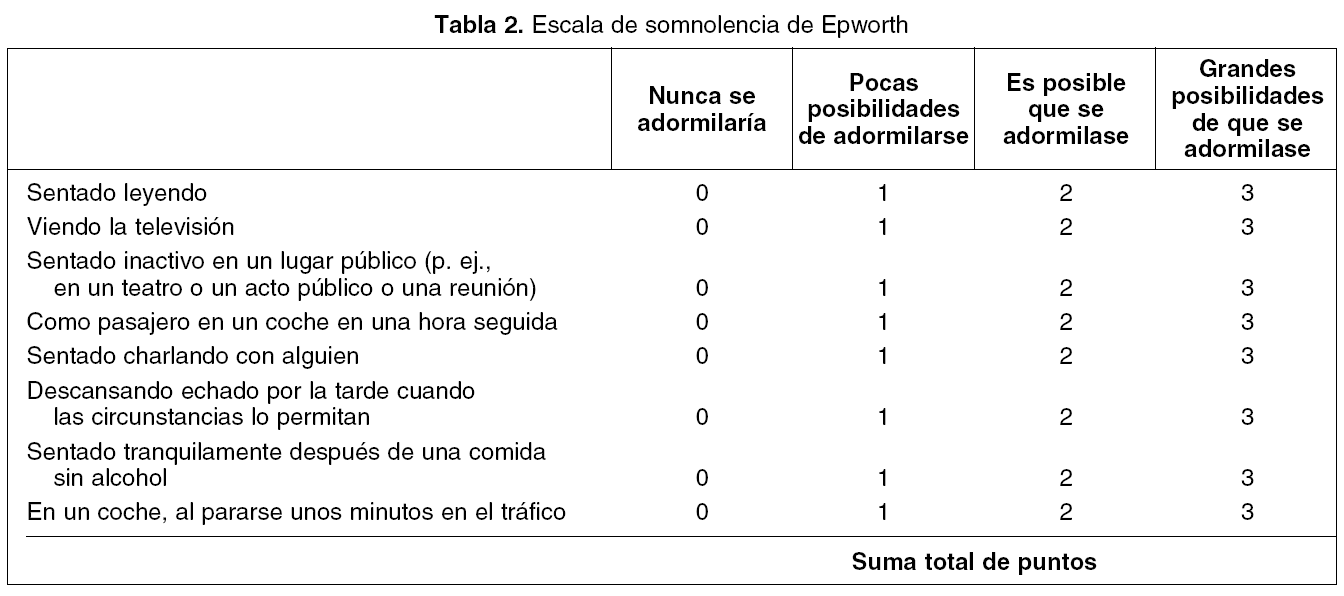
El síntoma diurno más importante es la excesiva somnolencia diurna (ESD), definida como la tendencia a dormirse involuntariamente en situaciones inapropiadas. La ESD se puede medir de forma objetiva y de forma subjetiva. La medida subjetiva más frecuente-mente utilizada es la escala de Epworth (tabla 2), diseñada para ser realizada por el paciente14; consta de 8 preguntas, cada una se puntúa en un rango del 0 al 3, con una escala de graduación de menor a mayor posibilidad de adormilarse: el 0 indica nula posibilidad y el 3, la máxima posibilidad de adormilarse. La puntuación total puede oscilar entre 0 y 24. En la población española el límite superior de normalidad podría estar alrededor de 1215. La medida objetiva de somnolencia diurna más utilizada y reconocida es la prueba de latencia múltiple del sueño, que mide el tiempo que tarda el individuo en quedarse dormido (latencia al sueño) cuando se lo somete a condiciones favorables y potencialmente inductoras de sueño. Otras medidas objetivas son las pruebas de mantenimiento de la vigilia y de Osler, que miden la capacidad de mantener la vigilia en condiciones de baja estimulación2.
Tres síntomas son clave para establecer la sospecha diagnóstica: ronquidos entrecortados, pausas asfícticas y excesiva somnolencia diurna o sueño no reparador. Otros síntomas frecuentes en el SAHS se muestran en la tabla 316.
El morfotipo típico de un paciente con SAHS es varón, de mediana edad, obeso y con cuello corto.
Los factores de riesgo para padecer SAHS más importantes son: el sexo masculino, con una relación varón:mujer de 1-3:1 en edades medias de la vida, aunque tiende a igualarse con la menopausia y en las edades avanzadas; la obesidad; las malformaciones faciales y los factores genéticos. Actúan como factores agravantes del SAHS el consumo de alcohol y de tabaco y dormir en decúbito supino.
Además de la sintomatología característica del SAHS, estaría indicado realizar una búsqueda activa en pacientes con comorbilidad cardiovascular, como hipertensión arterial refractaria al tratamiento o hipertensión de reciente diagnóstico, obesidad, bradiarritmias nocturnas, cardiopatía isquémica y antecedentes cerebrovasculares2.
Ante un paciente con sospecha de SAHS, es preciso realizar:
1. Una historia clínica detallada, con el compañero/a, y especificar:
Hábitos de sueño, tipo y circunstancias de aparición de somnolencia diurna y tiempo de evolución, así como la cuantificación subjetiva de la somnolencia diurna, mediante la escala de Epworth14.
Perfil psicológico.
Antecedentes personales de enfermedad cardiovascular, respiratoria u otorrinolaringológica (ORL), así como antecedentes familiares.
Profesión y horario de trabajo, consumo de alcohol, tabaco y fármacos.
2. Una exploración física general:
Datos antropométricos: edad, sexo, peso, talla, índice de masa corporal (IMC) y presión arterial.
Auscultación cardíaca y pulmonar.
3. Una inspección y exploración ORL:
Distancia hioides-mandíbula: para valorar cuello corto.
Calidad de la mordida: para valorar la posición de ambas arcadas dentarias.
Evaluación de retrognatia-micrognatia.
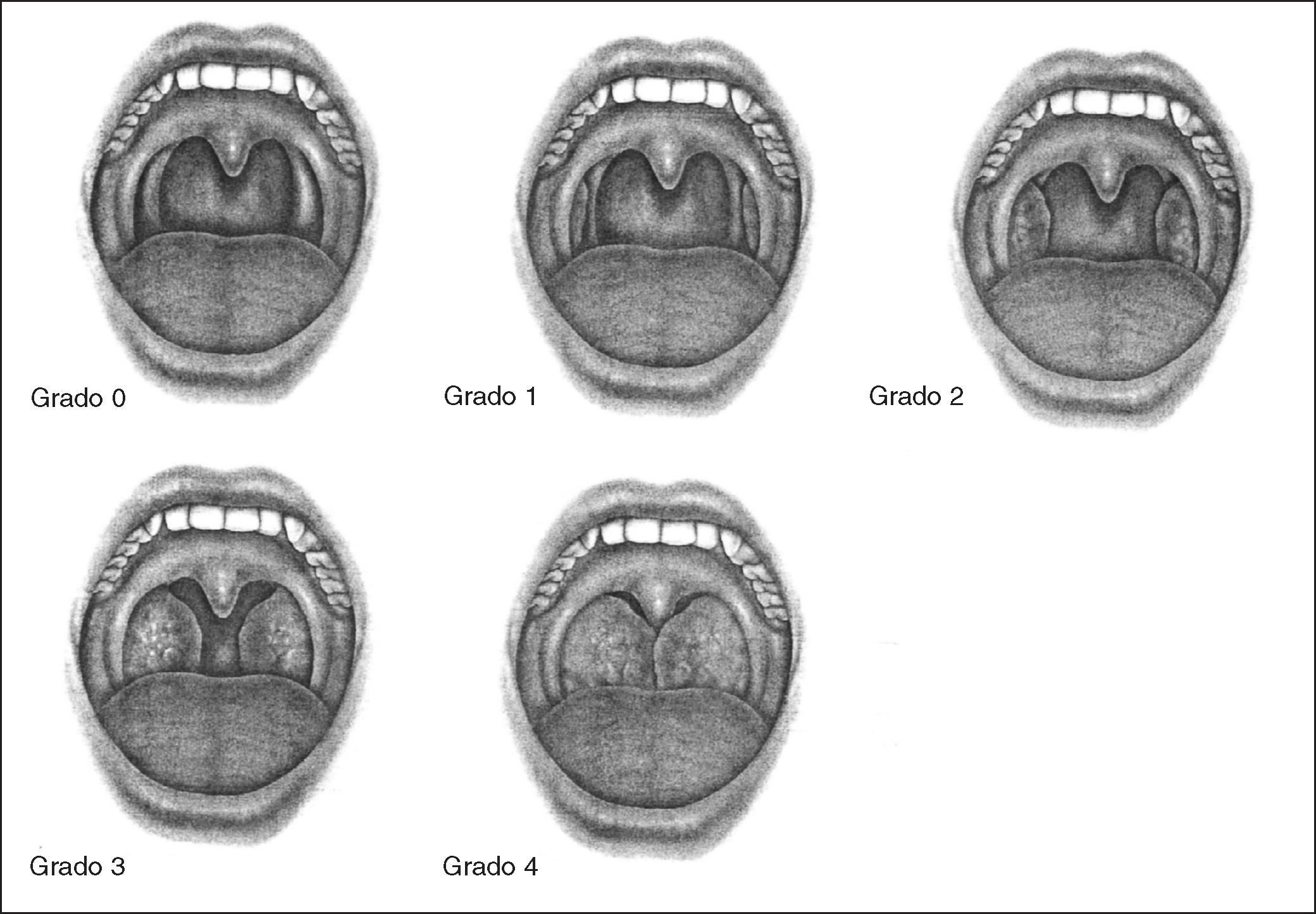
Orofaringoscopia: para valorar el volumen lingual en relación con la cavidad oral, la presencia de hipertrofia amigdalar y el aumento del volumen del paladar blando y su posición en relación con la pared posterior faríngea. La presencia de hipertrofia amigdalar se graduará de 0 a 4 (fig. 1).
Figura 1. Grados de hipertrofia amigdalar. La hipertrofia amigdalar se gradúa de 0 a 4 según el espacio visible interamigdalino: el 100% visible equivaldría a grado 0 de hipertrofia amigdalar hasta el 0% visible, que equivaldría a grado 4 de hipertrofia amigdalar.
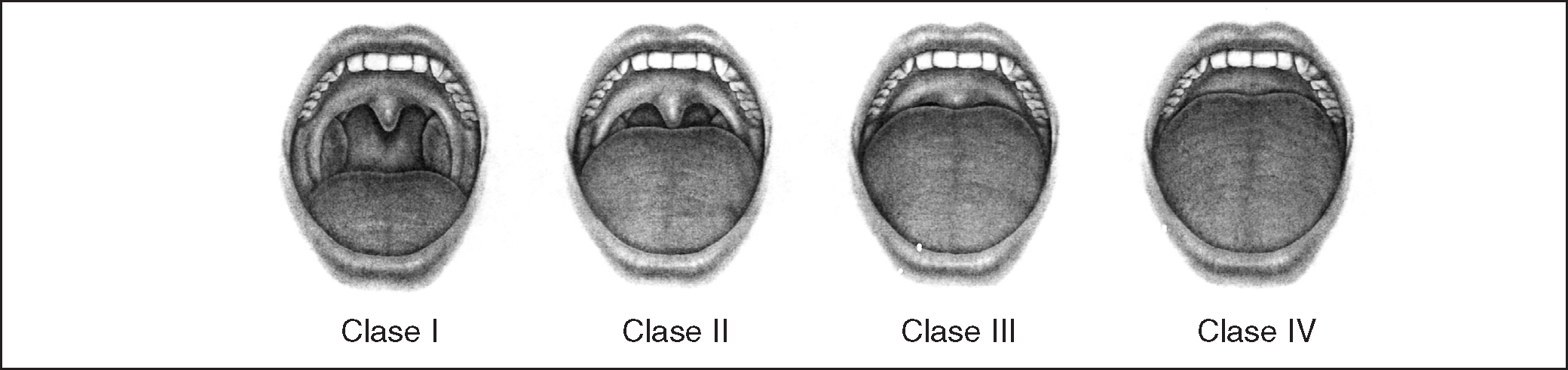
Exploración de los grados de Mallampati17: se realizará con el paciente en posición sentada, buena iluminación de la cavidad oral y máxima apertura oral con el paciente sin fonar. Evalúa en 4 grados según la visualización de la orofaringe; esta técnica es utilizada en anestesia para prever la dificultad de intubación (fig. 2).
Figura 2. Grados de Mallampati: clase I: puede verse paladar blando, fauces, úvula y pilares amigdalinos; clase II: puede verse paladar blando, fauces y úvula parcialmente, que contacta con la base de lengua; clase III: puede verse paladar blando y base de la úvula; clase IV: puede verse únicamente paladar duro y el resto queda fuera de visión.
Exploración nasal: interrogatorio dirigido en relación con los síntomas de dificultad respiratoria nasal: continua, intermitente, diurna o nocturna, otros síntomas como rinorrea, salvas de estornudos, etc. Es recomendable también la realización de una rinoscopia, que permitirá detectar la presencia de desviación de tabique nasal o de pólipos nasales.
4. Una analítica con hematimetría y perfil metabólico.
CRITERIOS DE DERIVACIÓN DE UN PACIENTE CON SOSPECHA DE SÍNDROME DE APNEAS-HIPOPNEAS DURANTE EL SUEÑO DESDE ATENCIÓN PRIMARIA A LA UNIDAD DE SUEÑO
Los pacientes identificados en atención primaria con sospecha de SAHS deben remitirse a la unidad de sueño de los siguientes modos18,19:
1. Derivación preferente/urgente: aquellos pacientes en los que se sospeche la presencia de SAHS y riesgo de consecuencias graves para su salud, como la presencia de excesiva somnolencia diurna incapacitante o hipertensión arterial no controlada, en especial si se asocia a cardiopatía isquémica o patología cerebrovascular, insuficiencia respiratoria, profesiones de riesgo (conductores, trabajos con máquinas peligrosas o en alturas, etc.).
2. Derivación ordinaria: los demás pacientes con sospecha de SAHS.
3. No derivar: pacientes roncadores simples, obesos o hipertensos sin otros síntomas acompañantes.
4. Cuando el paciente está ya diagnosticado y tratado de SAHS, se reenviará al paciente a la unidad de sueño para nueva valoración, en caso de18:
Empeoramiento clínico, con reaparición o modificación de la sintomatología o aparición de nuevos factores de riesgo
Modificaciones importantes en el peso, problemas de intolerancia o efectos secundarios derivados del tratamiento con CPAP.
Incumplimiento continuado del tratamiento con CPAP (menos de 3 h/noche).
SINDROME DE APNEAS-HIPOPNEAS DURANTE EL SUEÑO Y ACCIDENTES DE TRÁFICO, LABORALES Y DOMÉSTICOS
Las alteraciones respiratorias durante el sueño pueden predisponer a los individuos a excesiva somnolencia diurna e interferir con sus actividades diarias, incluida la conducción de vehículos. Los pacientes con SAHS tienen tiempos de reacción retardados y dificultades para mantener la capacidad de concentración; los estudios realizados con simuladores de conducción, al comparar sus resultados en pacientes con SAHS y en sujetos control, demuestran un aumento del tiempo de reacción en pacientes SAHS frente a los controles y un aumento de riesgo de accidentes y mejoría en estudios no controlados después del tratamiento con CPAP20,21. Hoy día está suficientemente probado que el riesgo de accidentes de tráfico está aumentado en pacientes con SAHS no tratados7,20. En España la detección del conductor de riesgo se realizada en los centros de reconocimiento de conductores. Sus facultativos, basándose en el anexo IV del Reglamento General de Conductores22, determinan la aptitud del conductor y emiten un informe para la Jefatura Provincial de Tráfico, que es la autoridad encargada de otorgar los permisos de conducción.
La somnolencia diurna es la causa del aumento de la tasa de accidentes no sólo de tráfico, sino también laborales o domésticos en pacientes con SAHS. Los accidentes laborales se han convertido en un problema social importante y, así, el alcohol, el consumo de fármacos y el trabajo a turnos se han asociado con accidentes de trabajo. El SAHS se asocia a un aumento de riesgo de accidentes de trabajo debido a la excesiva somnolencia diurna asociada al síndrome y a la disminución del grado de atención23. El papel del médico de trabajo es fundamental; la herramienta más importante en la evaluación es la historia clínica, con la utilización de un cuestionario de síntomas y exploración física como se ha expuesto.
SEGUIMIENTO Y CONTROL DE LOS PACIENTES DIAGNOSTICADOS DE SÍNDROME DE APNEAS-HIPONEAS DURANTE EL SUEÑO DESDE ATENCIÓN PRIMARIA
Los médicos de atención primaria deben desempeñar un papel importante en el control y seguimiento de los pacientes diagnosticados de SAHS18 y deberían realizar:
1. Una vigilancia de las medidas higiénico-dietéticas:
Insistir en el horario regular de sueño, en evitar pasar mucho tiempo en la cama y en las siestas largas durante el día.
Interrogar sobre los patrones de ingesta, evitar el alcohol, el tabaco, el consumo de sustancias que contengan cafeína y sustancias estimulantes y comidas copiosas en las horas cercanas a ir a dormir.
Valorar la evolución de la sintomatología: ronquido, apneas, sensación de descanso y, en especial, la somnolencia (escala de Epworth).
Determinar el IMC.
2. Un tratamiento con CPAP12,24: la CPAP ha demostrado ser un tratamiento rápidamente eficaz, eficiente, seguro y bien tolerado. El 70-80% de los individuos lo tolera; se debe utilizar al menos 4 h durante la noche25,26. Mejora la hipersomnia, hace desaparecer el ronquido, mejora la calidad de vida y la capacidad de atención, reduce la demanda sanitaria, reduce la morbimortalidad cardiovascular y el riesgo de accidentes de tráfico en los pacientes con SAHS.
Evaluar el grado de adhesión al tratamiento, mediante la monitorización subjetiva del uso referido por el paciente, así como la lectura del contador horario. Los pacientes tienen tendencia a sobrestimar la utilización de CPAP27; hay estudios que demuestran que la adhesión al tratamiento en los pacientes que han sido supervisados por médicos de atención primaria es buena28,29.
Evaluación de la eficacia del tratamiento: valoración de la sintomatología clínica, especialmente de la somnolencia (escala de Epworth).
Evaluación de la aparición de efectos secundarios y su tratamiento30:
a. Problemas con la mascarilla: actualmente existen en el mercado gran variedad de mascarillas, tamaños, formas y materiales para optimizar el confort de los pacientes.
b. Rampa: durante 20-30 min el aire aportado por la CPAP es a presión baja; se debe aumentar progresivamente hasta la presión prefijada para cada paciente; de esta forma, se permite el inicio del sueño y mejorar la tolerancia a la CPAP
c. Problemas nasales: congestión nasal y rinorrea, al inicio de tratamiento, son efectos que suelen desaparecer en poco tiempo; congestión/obstrucción nasal persistente: puede tratarse con corticoides, ipratropio o antihistamínicos tópicos nasales; epistaxis y sequedad faríngea: producidas por el aire a presión introducido con la CPAP, mejora con humidificador; problemas cutáneos: irritación cutánea y escaras en la zona de presión de mascarilla, se recomienda protección de zona de apoyo y cambio de mascarilla; problemas oculares: conjuntivitis, debido fundamentalmente a la fugas de aire; requiere ajuste de mascarilla.
3. Suplemento de oxígeno: el papel del oxígeno como tratamiento del SAHS continúa siendo controvertido. Si se decide su utilización en pacientes con SAHS que a pesar de la CPAP mantienen saturaciones de oxígeno bajas, es necesario comprobar su eficacia mediante una prueba de sueño que permita comprobar los valores de saturación de oxígeno y si es preciso de CO2.
4. Tratamiento farmacológico:
Se han ensayado más de 100 medicamentos para el tratamiento del SAHS con escasos resultados, por lo que hasta el momento actual no constituyen una alternativa terapéutica eficaz.
Evitar los medicamentos que potencien la mala función de la VAS durante el sueño, como las benzodiacepinas y narcóticos, que disminuyen la respuesta ventilatoria frente a la hipoxia y la hipercapnia.
Aceptado tras revisión externa: 16-03-2006.
Correspondencia: Dra. M.L. Alonso Álvarez. Unidad de Trastornos Respiratorios del Sueño. Sección de Neumología. Hospital General Yagüe. Avda. del Cid, 96. 09005 Burgos. España.
Correo electrónico: mlalonso@hgy.es