Los recién nacidos y lactantes presentan mayor vulnerabilidad frente a la tosferina. La vacunación durante el embarazo con la vacuna dTpa es una estrategia segura y efectiva para proteger a los recién nacidos y lactantes frente a la tosferina mediante la transferencia de anticuerpos pasivos. Además, esta práctica reduce el riesgo de infección y transmisión al proteger a las futuras madres. La Organización Mundial de la Salud (OMS) avala esta estrategia adicional como la más rentable y ha sido implementada en numerosos países.
Newborns and infants are at increased risk for whooping cough. Vaccination during pregnancy with the dTpa vaccine is a safe and effective strategy to protect newborns and infants against whooping cough through transfer of passive antibodies. Furthermore, this practice reduces the risk of infection and transmission by protecting pregnant mothers. The World Health Organization (WHO) endorses this strategy as the most cost-effective additional strategy, and it has been implemented in numerous countries.
La tosferina (TF) es una infección respiratoria altamente contagiosa causada por la bacteria Bordetella pertussis (B. pertussis), siendo su reservorio exclusivamente humano. Se propaga principalmente a través de gotas producidas en los episodios de tos.
La enfermedad se presenta mayoritariamente en población de preescolar y en edad escolar, aunque se presenta en todas las edades, los adolescentes y adultos son el principal reservorio, jugando un papel crucial en la transmisión sostenida1–3.
Los lactantes menores de 6 meses son los más vulnerables, y los que presentan complicaciones vitales, produciéndose más del 90% de las muertes en los primeros 6 meses de vida1,4. Se ha descrito que, en esta población, en más del 96% de los casos la fuente de infección se encontraba en el propio domicilio, siendo principalmente la madre3.
Es una infección endémica a nivel mundial, con un patrón cíclico, causando epidemias cada 3–5 años, a pesar de las altas coberturas vacunales1,2,4. La vacuna protege frente a formas graves y presenta menos protección frente a la infección1,2.
Como resultado de la vacunación sistemática, se observó una reducción importante de la incidencia.
A partir de 2010, Estados Unidos, Reino Unido y Australia describieron una reactivación de la TF, con un incremento de casos y mortalidad en los lactantes menores de un año. Como respuesta al incremento de morbimortalidad en lactantes menores de 6 meses no inmunizados o inmunizados parcialmente, se empezó a recomendar la vacunación frente a la TF en embarazadas con vacuna de baja carga antigénica (dTpa)5,6. En 2015, la OMS publicó el documento de posicionamiento sobre la vacunación contra la TF y después de evaluar diferentes medidas de control adicionales, concluyó que dicha vacunación era la estrategia más rentable para prevenir la enfermedad en los lactantes1.
Actualmente, muchos países han incorporado la vacunación maternal como vacunación rutinaria.
La vacunación de la tosferina en EspañaEl objetivo principal de los programas de vacunación frente a la TF es reducir la carga de enfermedad y el riesgo de formas graves en los lactantes, que son los que tienen mayor morbimortalidad1,7.
La vacunación frente a la TF se inició en España a mediados de los años 60, en forma de campañas, en los menores de un año con la vacuna DTPw de células enteras, que presentaron cierto grado de reactogenicidad. En 1975, se incluyó en el calendario nacional de vacunación infantil, con 3 dosis a los 3, 5 y 7 meses de edad. En 1996, se modificó la edad de vacunación, administrándose a los 2, 4 y 6 meses de edad y se incluyó una cuarta dosis a los 15–18 meses de edad. En 2001 se incluyó una quinta dosis a los 4–6 años. A partir del año 2005 se incorporó la vacuna DTPa tipo acelular, con mejor perfil de seguridad, y que fue sustituyendo las dosis de todas las edades2.
Actualmente, la pauta de vacunación sistemática frente a la TF consiste en una pauta 2 + 1 en el primer año de vida, a los 2, 4 y 11 meses, y un segundo refuerzo a los 6 años8.
Las coberturas de vacunación en España aumentaron progresivamente entre 1982 y 2012, y a partir de 1998 se han mantenido por encima del 95% en 3 dosis2. Los datos publicados por el Ministerio de Sanidad muestran, para 2023, coberturas vacunales del 96,3% para la primovacunación y primer refuerzo, y del 90,5% para la dosis de refuerzo de los 6 años9.
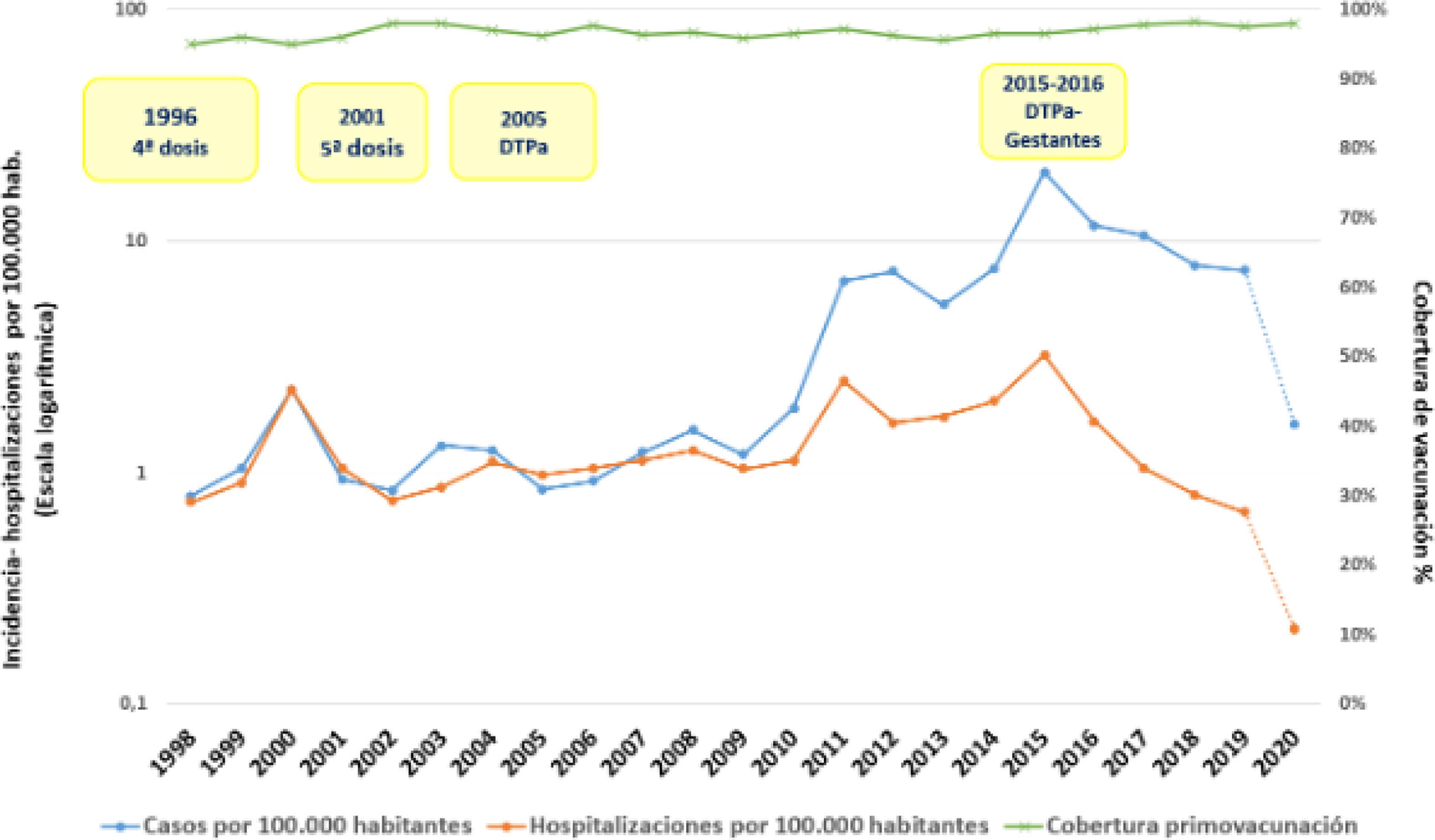
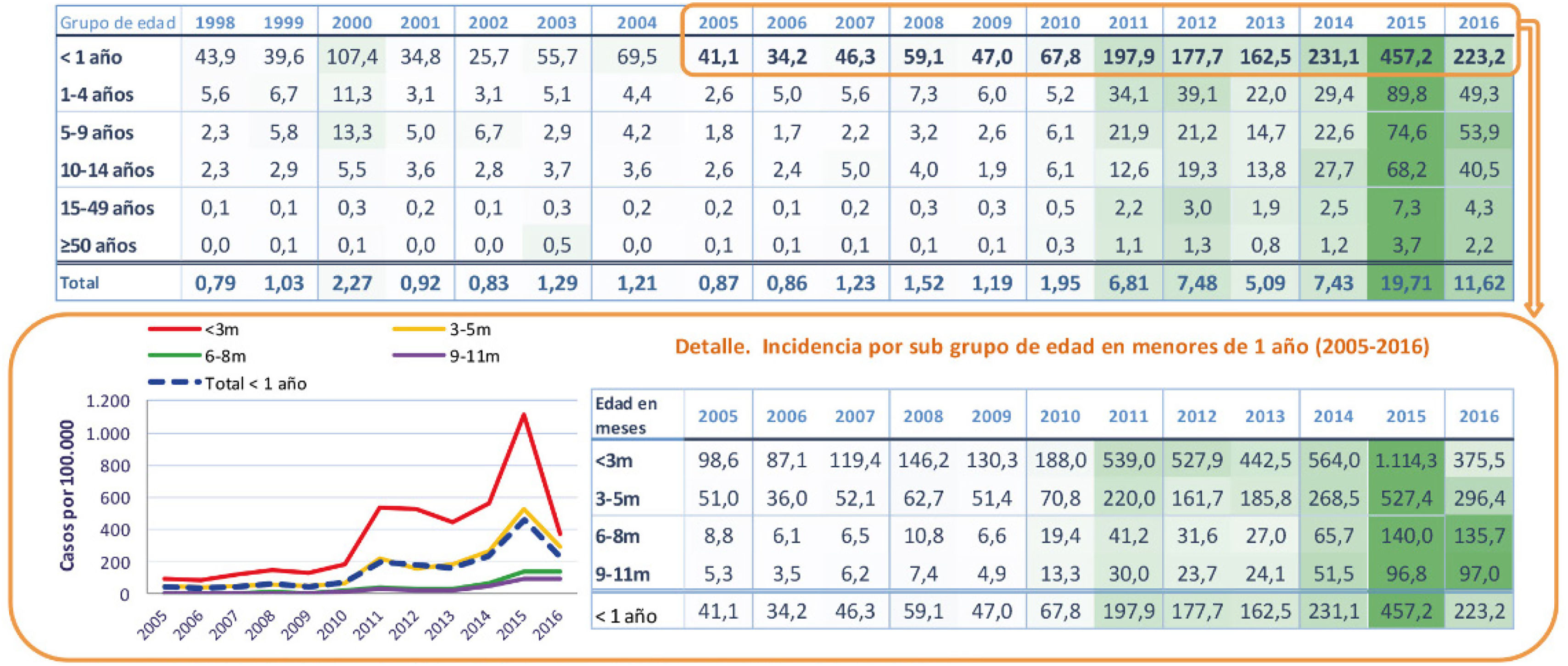
Situación previa a la incorporación de la vacunación frente la tosferina en embarazadasEn España, la TF es una enfermedad de declaración obligatoria desde 1982. A partir de la vacunación sistemática, la incidencia y mortalidad por TF en España ha ido disminuyendo, con una reducción más marcada a partir de 1986, coincidiendo con la introducción de la cuarta dosis de vacuna. A partir de 2010 empezó a incrementarse, con un patrón de situación epidémica sostenida, con incidencias y tasas de hospitalización más elevadas en los menores de 3 meses (figs. 1 y 2)4,10.
Incidencia y hospitalizaciones por TF por 100.000 habitantes y coberturas de primovacunación, España 1998–20204.
Incidencia de TF por 100.000 habitantes por grupo de edad y en menores de un año por subgrupo de edad, España, 1998–20164.
Anterior a la vacunación, se estima que las muertes por TF superaban los 30 casos por año; a partir de los años 70 disminuyó y a partir de los 90 casi no se notificaron muertes. En 2000 se empezó a registrar una media anual de una muerte, pero esta tendencia empezó a aumentar, registrándose 8 muertes en 2011 y 7 en 2015, todas en menores de 3 meses2,4,10. Entre 2010 y 2019 hubo 42 muertes en menores de un año, con una tasa de mortalidad de 5,7 por 1.000 habitantes4.
El incremento de morbimortalidad en menores de un año forzó a plantear nuevas estrategias para el control de la enfermedad grave y de la mortalidad. La protección de los más vulnerables se establece mediante la vacunación del lactante y la inmunización pasiva del mismo, lograda a través de la vacunación materna.
Introducción de la vacunación frente la tosferina en embarazadasEn España, en 2012, la Ponencia de Programas y Registro de Vacunaciones, en el marco de una revisión del programa de vacunación frente a TF en España, valoró posibles estrategias e incluyó la necesidad de valorar estrategias complementarias de vacunación de la embarazada y de los contactos domiciliarios antes del nacimiento si la epidemiología lo aconsejaba2.
En 2014, 3 CCAA introdujeron la vacunación frente a TF en el tercer trimestre de embarazo (Cataluña, Asturias y Navarra). En 2016 todas las CCAA habían incluido la vacunación sistemática, en un primer momento entre las semanas 27, 28 y 36 de embarazo, e idealmente entre las 28 y 32 semanas de gestación, independientemente del estado de vacunación previo y en cada nueva gestación. En 2020 se recomendó a partir de la semana 27, preferentemente en las semanas 27 o 28. En el caso de embarazadas con alto riesgo de parto prematuro y clínicamente estables se recomienda valorar la vacunación a partir de la semana 207,11.
En 2024, la Asociación Española de Pediatría (AEP) y la Sociedad Española de Ginecología y Obstetricia publicaron un documento de consenso sobre la vacunación durante el embarazo, recomendando la vacunación con vacuna dTpa en cada embarazo entre las semanas 27 y 36 de gestación, pero la AEP remarca que es preferible administrar la vacuna entre las semanas 27 y 2812.
La cobertura vacunal de la dTpa en las embarazadas aumentó progresivamente, y en 2023 era de 87,6%9.
Vacunación en el embarazoLa vacunación en el embarazo tiene como objetivo principal proteger pasivamente frente a la TF grave en los lactantes desde el nacimiento hasta alcanzar la edad para la vacunación, siendo esta estrategia más efectiva que la estrategia nido1.
Los recién nacidos presentan un sistema inmunitario poco desarrollado, siendo vulnerables a infecciones. La protección pasiva se fundamenta en la transferencia de anticuerpos (Ac) específicos maternos adquiridos o estimulados después de la vacunación a través de la placenta y la leche materna (LM).
Los Ac maternos transferidos pasivamente, sin haber recibido una dosis de vacuna frente a la TF durante el embarazo, decaen a partir de las 6 semanas de vida y son casi indetectables a los 4 meses de vida13,14. Para mejorar e incrementar la transferencia de Ac de madres a hijos se estableció la estrategia de vacunación en las embarazadas. Esta estrategia, además, reduce la transmisión de la TF al recién nacido, ya que protege a la madre.
Pero esta intervención planteó dudas sobre varios aspectos clave, como son la respuesta inmune maternal, la cinética de las IgG maternas generadas tras la vacunación, la transferencia de Ac específicos vía placenta y a través de la LM, el momento óptimo de vacunación para una mayor efectividad, así como dudas de aceptación por parte de la población y los profesionales sanitarios, y de seguridad en el embarazo y el parto, y en los recién nacidos, añadiendo la perspectiva ética de la vacunación en las mujeres embarazadas para proteger a la población vulnerable sin ser ellas vulnerables1,2,7,13.
Transferencia al feto y al recién nacido, placenta y leche maternaLa transferencia de IgG al feto a través de la placenta empieza hacia la semana 17 de gestación, con un pico a partir de la semana 32, e igualando las concentraciones maternas entre las semanas 32 y 36, para sobrepasarlas en la semana 37. Pero la transferencia de IgG está ligada al tipo de subclases de IgG, debido a que está mediada por receptores Fc neonatales, a las funciones de estos y a su calidad, que puede estar afectada por cambios inmunofisiológicos, siendo las IgG1 e IgG3 las más eficientes13,14.
Durante el embarazo, se dan múltiples adaptaciones fisiológicas para permitir la implantación y desarrollo del feto. Estas adaptaciones podrían interaccionar en la respuesta inmune tras la vacunación, tanto cuantitativa como cualitativamente. Estudios, en los que se compara la inmunogenicidad de la vacunación entre mujeres embarazadas y no embarazadas, muestran un menor título de Ac en las embarazadas, sin ser clínicamente significativo13–15.
Solamente se detectan títulos de anticuerpos anti-PT (≥10 UI/ml) en el 37% de las madres embarazadas antes de la vacunación. Si bien se conoce que las mujeres que han padecido TF presentan títulos más elevados que las vacunadas, la vacunación materna se asocia con niveles de Ac significativamente superiores en los recién nacidos, detectándose en más del 94% de los hijos de madres vacunadas en el segundo o tercer trimestre, sin observarse diferencias según el momento de vacunación13–15.
Los niveles de Ac anti-TP en sangre de cordón se asocian a protección clínica contra la TF13,14.
Algunos estudios muestran que la concentración de Ac en cordón umbilical de mujeres vacunadas al principio del tercer trimestre es significativamente mayor que al final del trimestre, algunos de ellos mostrando mejores resultados tras la vacunación realizada en la semana 26–32 de gestación13–16.
Otros autores destacan como factor clave el intervalo de tiempo de, como mínimo, 8 semanas entre la vacunación y el parto, sobre todo en prematuros15,16.
En lactantes prematuros hay mayor transferencia si las madres se vacunaron en el segundo trimestre, a que si lo hicieron en el tercer trimestre11,13,14. La vacunación en el segundo trimestre da la oportunidad de alargar el periodo de transferencia, así como de proteger en caso de parto prematuro.
Lactancia maternaA través de la LM se detectan los 5 subtipos de Ig (IgA, IgM, IgG, IgE e IgD), siendo la IgA la predominante. Los anticuerpos transferidos son principalmente IgA secretora, IgM secretora e IgG. Dichos anticuerpos específicos frente a TF se han detectado en el calostro y la LM de madres vacunadas durante el embarazo hasta 8–12 semanas posparto. Aunque posiblemente su efecto podría ser mucosal, protegiendo el tracto respiratorio superior, los Ac específicos pueden atravesar la mucosa digestiva y tener un efecto sistémico13,14,16. Estudios recientes han detectado que ni en el calostro ni en la leche recogida a los 14 días se observa correlación entre el momento de la vacunación materna y los títulos de Ac, aunque sí que se ha detectado menor titulación de Ac en la LM de los 14 días respecto al calostro17.
Efecto bluntingLos Ac maternos transferidos pasivamente pueden tener un impacto a corto o largo plazo en la respuesta inmunitaria propia de los lactantes tras su vacunación, tanto en la serie primaria como en los refuerzos. Los datos de los estudios publicados señalan la aparición de esta interferencia, denominada efecto blunting (algunos autores también hablan de efecto modificador o modulador), en las respuestas activas del lactante a antígenos de la vacuna homólogos y heterólogos con una reducción en la respuesta inmunitaria7,12,13,16,17.
Un nivel de Ac homólogos preexistentes 2 veces superior a Ag de la vacuna TF acelular (toxoide de la TF, hemaglutinina filamentosa y pertactina) se asoció con una reducción del 11% de anticuerpos posvacunación contra el toxoide de la TF (GMR 0,89; IC 95%: 0,87–0,90) y la hemaglutinina filamentosa (GMR 0,89; IC 95%: 0,88–0,90) y un 22% menos de Ac contra la pertactina (GMR 0,78; IC 95%: 0,77–0,80). Estos datos plantean la hipótesis de retrasar la vacunación propia del lactante para compensar el efecto inmodulador del incremento entre 2 a 5 veces del nivel de Ac maternales entre 2 y 5 semanas18.
Se desconoce el correlato de protección frente a la TF, aunque tanto los datos de vigilancia epidemiológica de la enfermedad como los estudios de efectividad vacunal (EV) en el primer año de vida muestran una reducción de casos, hospitalizaciones y muertes en las regiones con vacunación implementada4,13,14.
Además de la respuesta cuantitativa está la respuesta cualitativa, medida por la avidez (afinidad funcionalidad), así como la respuesta inmune neonatal celular adaptativa e innata a los antígenos vacunales antes de la vacunación, proponiéndose una posible exposición in utero a los antígenos de la vacuna. Estudios preliminares muestran menor avidez en los Ac TP en los lactantes de madres vacunadas, aunque la capacidad neutralizante de los Ac TP fue alta en los bebés de madres vacunadas, manteniéndose hasta 6 meses después de 2 dosis de vacunación primaria16.
EfectividadLa protección ofrecida por la vacunación maternal está ampliamente demostrada. Los primeros estudios sobre la efectividad de la vacunación frente a la TF mostraron resultados positivos que evidenciaban la bondad de dicha recomendación. En Reino Unido, se estimó tras 11 meses de vacunación una reducción de la incidencia de TF y de la mortalidad en los lactantes menores de 3 meses del 79%. La efectividad vacunal (EV) estimada mediante método de cribado con una cobertura vacunal del 60% fue del 91% (IC 95%: 84–95), manteniéndose a los 3 años, y del 93% (IC 95%: 81–97) mediante estudio de casos y controles15.
En Estados Unidos, se evaluó la EV en los lactantes nacidos a término mediante el seguimiento retrospectivo de la cohorte Kaiser Permanent Northern California, de nacidos entre 2010–2015, estimándose una protección frente a TF en los primeros 2 meses de vida del 91,4% (IC 95%: 19,5–99,1), y del 69% (IC 95%: 43,6–82,9) para el primer año de vida15.
La recomendación en Cataluña de vacunar de TF a las mujeres embarazadas en el tercer trimestre de la gestación a partir del año 2014 tuvo impacto en la incidencia de la enfermedad en los menores de un año, y sobre todo en la de los menores de 2 meses, que disminuyó de forma significativa. En 2011, la tasa de incidencia en menores de un año era de 478,5 por 100.000 habitantes, y tras la vacunación pasó a ser de 235,7 por 100.000 en 2018. El porcentaje de casos en los menores de 2 meses y un año disminuyó entre 2013 y 2018, siendo la diferencia de porcentaje entre 2013 (año previo a la introducción de la vacunación) y 2014–2018 (periodo de vacunación) estadísticamente significativa, 7,6% vs. 1,4% y p < 0,00119.
En España, después de la implementación de la vacunación materna se observó una reducción de la tasa de hospitalización en los menores de un año (331,9 por 100.000 habitantes en 2015 hasta 70,43 por 100.000 en 2019)4.
En Valencia, tras un año de la implementación, se estimó que la EV mediante un estudio de casos y controles en menores de 3 meses era del 90,9% (IC 95%: 56,6–98,1)15.
En Cataluña y Navarra, mediante un estudio de casos y controles, la EV en los lactantes nacidos entre 2016 y mediados de 2018 fue 88% (IC 95%: 58–97). La EV fue ligeramente superior en las madres vacunadas antes de la semana 32 de gestación 88,5% (IC 95%: 54,9–97,1%) que en las vacunadas posteriormente 87,8% (IC 95%: 39,7–97,5%)15.
En Australia, también mediante un estudio de casos y controles, se estimó que en menores de 6 meses la vacunación contra la TF en embarazadas reducía en un 69% (IC 95%: 13–89%) la tasa de infección confirmada. En cuanto a la hospitalización, la reducción fue del 94% (IC 95%: 59–99%)20.
Otro estudio en Australia realizado mediante el seguimiento de una cohorte poblacional, con una cobertura vacunal del 51,7%, mostró una EV de la vacuna dTpa materna entre lactantes menores de 6 meses del 65,1% (IC 95%: 49,5–76,0) contra la infección por B. pertussis y del 60,2% (IC 95%: −18,3 a 86,6) contra TF hospitalizada, sin datos suficientes para analizar el ingreso en UCI y la mortalidad. La EV de la vacunación materna disminuye con la edad del lactante, siendo no significativa a partir de los 8 meses de edad. Se observó que la mediana de edad en la infección por B. pertussis entre los lactantes con vacunación materna fue mayor que la de los lactantes no inmunizados por vía materna (11 meses vs. 7,5 meses, respectivamente, siendo la diferencia estadísticamente significativa, p < 0,001), si bien se detectó una menor EV en los lactantes con 3 dosis en aquellos con vacunación materna (76,5% vs. 92,9%; p = 0,002), la incidencia de TF fue similar en ambos grupos (20,7 casos por 100.000 habitantes vs. 23,1 casos por 100.000)21.
Una revisión sistemática publicada en 2020 estimó que la EV en menores de 3 meses frente a la infección por B. pertussis confirmada por laboratorio, oscilaba entre el 69 y el 91%. Para prevenir la hospitalización, la EV osciló entre 91 y 94%, y para prevenir la mortalidad, alcanzó el 95%. El estudio concluye que la vacunación materna presenta una relación beneficio-riesgo positiva14.
Los datos publicados por la Red Europea de Tosferina en Lactantes (PERTINENT) de vigilancia centinela en hospitales estimaron, mediante un estudio de casos y controles con test negativo, que tomando como grupo de referencia a los bebés y madres no vacunados, y ajustada por lugar, momento de inicio y edad, la EV fue del 74% (IC 95%: 33–90) para los bebés con primovacunación (PV) y vacunación durante el embarazo; del 68% (IC 95%: 27–86) solo para aquellos con PV; y del 36% (IC 95%: −85 a 78) para aquellos con vacunación solo durante el embarazo. Los datos de sensibilidad mostraron que la vacunación materna reduce el riesgo de hospitalización por TF entre un 75 y 88% en lactantes menores de 2 meses. Independientemente del calendario de vacunación recomendado, cuando los lactantes tienen entre 2 y 11 meses y son elegibles para la vacunación, haber recibido al menos una dosis de PV si la madre había recibido la vacuna durante el embarazo reduciría el riesgo de hospitalización por TF confirmada entre un 74 y 95%. En el caso de lactantes cuyas madres no fueron vacunadas, recibir al menos una dosis de PV reduciría el riesgo entre un 68 y 94%22.
Recientemente, se ha publicado un artículo de seguimiento de la cohorte nacional danesa de 2019 a 2023, en el que la EV para lactantes menores de 3 meses fue 72,1% (IC 95%: 41,6–86,7) frente a la TF confirmada. En lactantes contactos hospitalarios de casos de TF, la vacunación materna mostró una protección del 66,0% (IC 95%: 23,4–84,9)23.
Seguridad de la vacunación en el embarazoUna premisa fundamental en la vacunación materna es la seguridad tanto para la mujer embarazada como para el feto y el neonato. La evidencia disponible indica que la vacunación materna contra TF con vacuna dTpa es segura para la embarazada, su feto y el recién nacido. La vacunación frente a TF presenta un buen perfil de tolerabilidad y seguridad, independientemente del número de antígenos contenidos en la formulación7,11–13.
No se ha descrito ningún aumento de riesgo materno grave, como parto prematuro, rotura prematura de membranas, ni efectos adversos en los resultados fetales o neonatales. Aunque algunos estudios sugieren un pequeño riesgo de corioamnionitis asociado con la vacunación frente a TF durante el embarazo, este riesgo está actualmente bajo investigación y se considera bajo y manejable12,13,23.
Por otro lado, la vacunación con la vacuna dTpa se ha asociado a beneficios como son un menor riesgo de bajo peso al nacer, mejor tamaño según la edad gestacional y una reducción en la necesidad de parto por cesárea planificada23.
También se ha demostrado que las vacunas dTpa administradas en embarazos consecutivos son bien toleradas y seguras.
ConclusiónEl principal objetivo de la vacunación contra la TF es reducir el riesgo de enfermedad grave en lactantes y niños pequeños, que son el grupo más vulnerable ante la infección por B. pertussis. Los estudios sobre efectividad vacunal demuestran que la vacunación en embarazadas puede reducir la enfermedad en los lactantes mediante la inducción de anticuerpos maternos protectores, que se transmiten pasivamente a través de la placenta y protegen a los bebés hasta, al menos, los 2 meses de edad, cuando reciben su primera dosis de vacuna antipertúsica. Además, el conjunto de datos muestra que la vacuna es efectiva para prevenir la hospitalización y mortalidad en el grupo de mayor vulnerabilidad.
La vacunación maternal ofrece una oportunidad única para disminuir la morbimortalidad durante el periodo de mayor riesgo, al proporcionar protección pasiva y, al mismo tiempo, proteger a la madre y reducir el riesgo de transmisión al lactante. Proteger a esta población es una prioridad para los programas de vacunación, alineándose con las directrices y objetivos establecidos por la OMS para reducir la mortalidad infantil.
FinanciaciónLa autora declara que no ha recibido ayudas específicas por parte del sector público, sector privado o entidades sin ánimo de lucro.
Conflicto de interesesLa autora declara que no tiene conflicto de intereses que puedan perjudicar este artículo.