Introducción
El uso de titanio (Ti) en Medicina y Odontología ha aumentado durante las tres últimas décadas. Las aleaciones de Ti se han utilizado ampliamente en los implantes dentales, endoprótesis, marcapasos, stents, aparatos de ortodoncia y monturas de gafas. El material de elección para los implantes dentales es titanio puro debido a su biocompatibilidad e idoneidad bien documentadas para el mecanizado. Este material biocompatible1 se ha utilizado durante unos 30 años como sustrato para implantes y ha demostrado una tasa de éxito elevada2.
La superficie del implante de Ti oxidado tiene un buen comportamiento a la corrosión y buenas propiedades de biocompatibilidad y osteointegración2. Por tanto, se ha considerado que el Ti es particularmente adecuado para implantes dentales y protésicos.
Sin embargo, se han descrito casos esporádicos de intolerancia al Ti3-11. Las pruebas cutáneas han detectado excepcionalmente reacciones positivas al Ti3,6,12. La prueba del parche, que puede provocar la sensibilización de los linfocitos T nativos, en general se ha validado solamente para el contacto con el antígeno epidérmico, y es relevante principalmente para detectar efectos dérmicos de hipersensibilidad (dermatItis por contacto)13. Por otro lado, las pruebas in vitro con el test de transformación linfocitaria (TTL) pueden detectar alérgenos sensibilizados tanto dérmicamente como no dérmicamente. Puesto que es una prueba in vitro, el TTL no puede sensibilizar al paciente. Se ha utilizado con éxito para detector hipersensibilidad con efectos tanto locales como sistémicos14-19. Además, varios grupos han documentado la sensibilidad, especificidad, reproducibilidad y fiabilidad de esta estrategia para detectar la sensibilidad al metal, en particular la versión optimizada del TTL denominado ensayo de inmunoestimulación de la memoria linfocitaria (MELISA®)20-26. Así pues, se seleccionó la prueba MELISA para investigar y diagnosticar la hipersensibilidad al Ti en esta paciente.
Una alternativa posible al titanio podrían ser materiales del color de los dientes, como la cerámica27,28. Los materiales cerámicos son altamente biocompatibles y pueden utilizarse como dispositivos dentales29. Un material cerámico que se ha utilizado en el pasado como implante dental es el óxido de aluminio (Al2O3)30-32. Este material tiene una buena osteointegración pero sus propiedades mecánicas son insuficientes para una carga a largo plazo, y el producto se retiró del mercado.
Recientemente se introdujo otro material cerámico con potencial para el uso futuro como implante dental. El óxido de circonio (ZrO2), como sustituto metálico, tiene buenas propiedades físicas, como resistencia flexural elevada (900 a 1.200 MPa), dureza (1.200 Vickers), y módulo de Weibull (10 a 12)33-35. Además, su biocompatibilidad como material para implantes dentales se ha demostrado en varias investigaciones realizadas en animales36-43. Asimismo, los experimentos realizados in vitro mostraron que el material es capaz de sostener cargas simuladas a largo plazo, aunque parece que las propiedades mecánicas del circonio se ven influidas por la preparación mecánica del material40,44,45. Además, la exposición de los implantes de circonio a la boca artificial no ha demostrado efectos estadísticamente significativos en los valores promedio de resistencia a la fractura de los implantes45. Kohal y cols.46 publicaron el caso de un implante de circonio mecanizado y una corona de circonio en un paciente con un excelente resultado estético. La investigación implantaria moderna muestra que es deseable una topografía de superficie rugosa para aumentar el proceso de integración ósea47 pero el mecanizado de los cilindros de circonio resulta en una superficie relativamente lisa. En la misma línea, Sennerby y cols.43 demostraron una mayor resistencia al torque de retirada del implante de las superficies de circonio poroso en conejos, y Gahlert y cols.48 obtuvieron resultados similares. En una revisión sistemática, Wenz y cols.44 concluyeron que la osteointegración de los implantes Y-TZP (policristal tetragonal de circonio estabilizado con itrio) podría ser comparable a la de los implantes de titanio; las modificaciones de las superficies tienen el potencial de mejorar la consolidación ósea inicial y la resistencia al torque de retirada; la degradación a baja temperatura podría afectar el comportamiento de los implantes Y-TZP, aunque este punto sigue investigándose; y son necesarios ensayos clínicos a largo plazo para evaluar el rendimiento clínico de los implantes Y-TZP antes de su uso clínico rutinario.
Con respecto al rendimiento a largo plazo de las restauraciones con implantes Y-TZP, pueden existir diferencias importantes entre los sistemas utilizados. Larsson y cols.49 informaron de que algunos sistemas podrían presentar una cantidad inaceptable de fracturas de las capas de porcelana.
En una publicación reciente50, los autores de este artículo informaron de los resultados preliminares de un año de seguimiento de un estudio clínico en curso con implantes de circonio CeraRoot (Oral Iceberg, Barcelona, España), y el porcentaje de éxitos fue comparable a la de los implantes de titanio. Esta investigación en curso comenzó con dos tipos de superficies rugosas (una recubierta y otra no recubierta), y tras el nuevo desarrollo de la superficie grabada al ácido (ICE) también se incluyó en el estudio. Además, los autores de este trabajo51 han demostrado el potencial estético de este sistema de implantes en un caso con una demanda estética importante. El informe de este caso es parte de la investigación clínica en curso con la superficie ICE (véase la figura 1) y es la primera publicación que informa de una rehabilitación oral de boca completa con implantes y restauraciones de ZrO2.
Figura 1 Microfotografía electrónica de barrido de los implantes CeraRoot con superficie ICE. Izquierda: ×5.000; derecha: ×20.000.
Presentación del caso
Una mujer de 38 años con alergia al titanio y una amelogénesis imperfecta general severa fue referida a nuestro centro para una rehabilitación oral total con implantes de óxido de circonio. La paciente describió que el deterioro de los dientes empezó después de su primer embarazo, a los 28 años y que los descuidó posteriormente ya que no presentaba dolor. Con respecto a la alergia al titanio, la paciente tenía antecedentes de reacción cutánea inflamatoria, enrojecimiento y prurito al contacto con anillos, pendientes, monturas de gafas y cualquier contacto prolongado con el metal. Por este motivo, su dermatólogo le practicó una prueba de proliferación linfocitaria denominada MELISA (Melisa Medical, Suecia) para obtener un diagnóstico. Las pruebas confirmaron su reacción positiva a diferentes metales entre los que estaba el titanio (IS = 40). Aunque no existe una evidencia científica clara de alergias con implantes dentales de titanio, el dermatólogo de la paciente aconsejó no colocar implantes de titanio ni otra restauración metálica debido a sus antecedentes de reacciones cutáneas. La paciente fumaba 5 cigarrillos diarios y, aparte de la alergia cutánea, no existían otros antecedentes médicos relevantes.
Exploración inicial
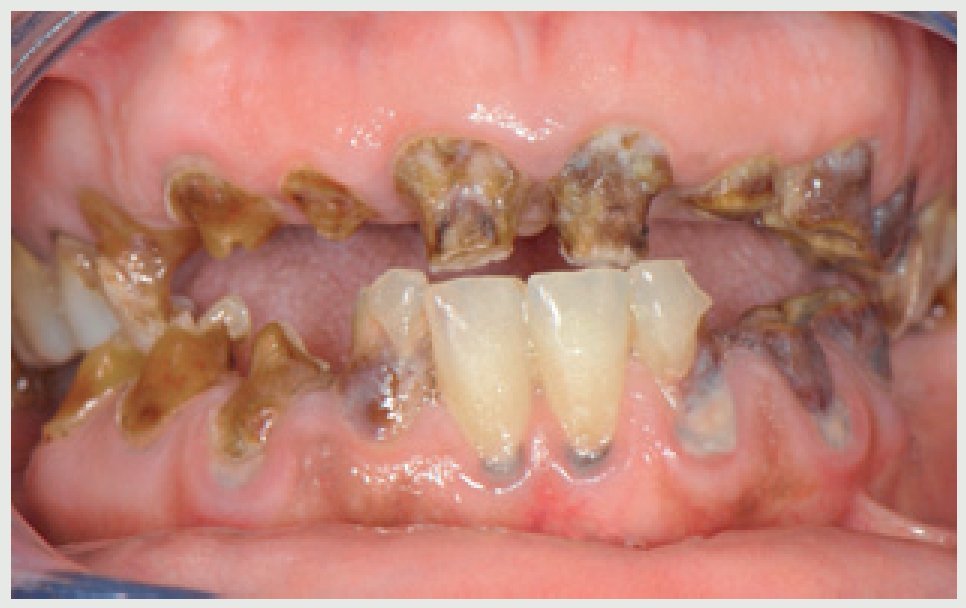
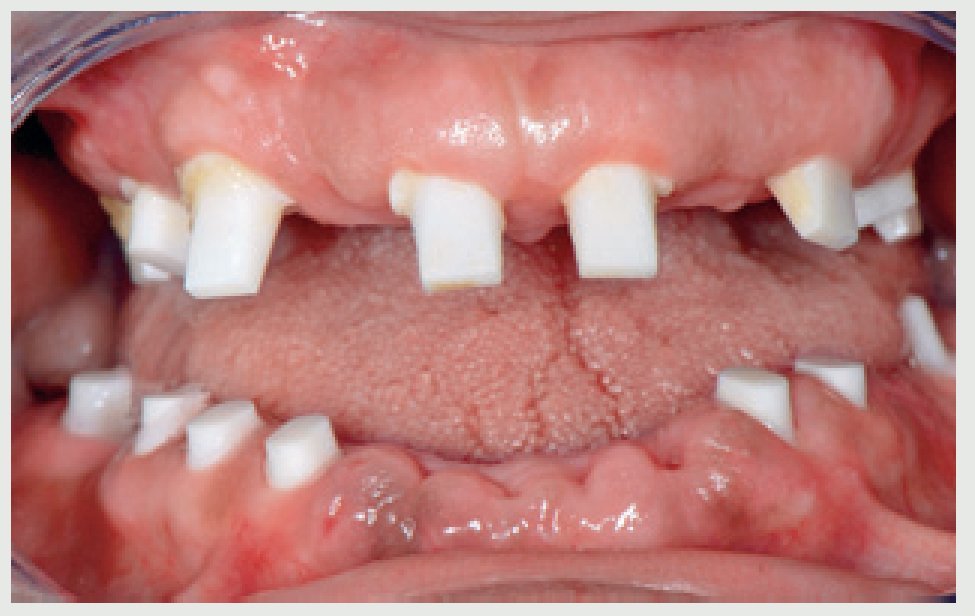
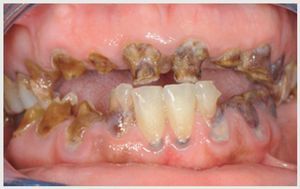
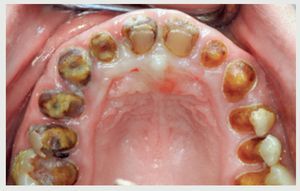
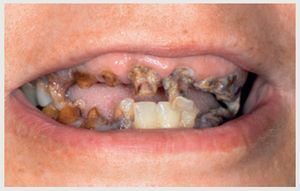
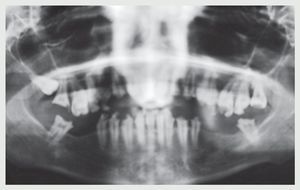
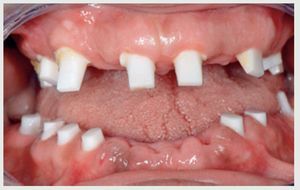
La exploración inicial reveló la amplia destrucción de los dientes (figuras 2 y 3); placa dental y gingivitis generalizada; ausencia de bolsas periodontales en cualquier zona de la boca (profundidad del sondaje ≤3 mm); y ausencia de los dientes 46, 47, 35, 36 y 37. La estructura restante de los incisivos superiores e inferiores sugirió que la dentición tendría un resalte y sobremordida óptimos, y la línea media dental estaría centrada en la cara y los labios. Existía una pérdida de dimensión vertical oclusal debido a la amplia destrucción dental. La paciente tenía una sonrisa gingival (figura 4). La radiografía panorámica (figura 5) confirmó la amplia destrucción dental y la preservación de la cresta alveolar, a excepción de una reabsorción moderada en las zonas con ausencia de dientes. Se detectó una lesión periapical crónica en el canino 13. Llegados a este punto, se consideró que la dentición no era restaurable. Se realizaron impresiones en alginato, y se tomaron los registros de las relaciones céntricas y del arco facial para montar los modelos de estudio en el articulador.
Figura 2 Situación inicial: amplio deterioro dental.
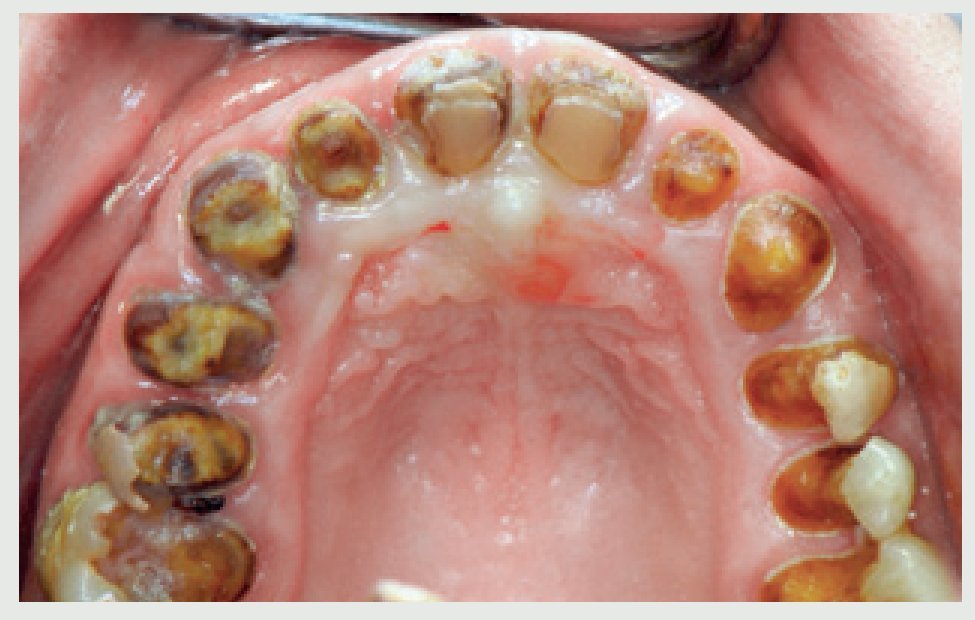
Figura 3 Aspecto oclusal: obsérvese la minima estructura sana remanente de las coronas dentales.
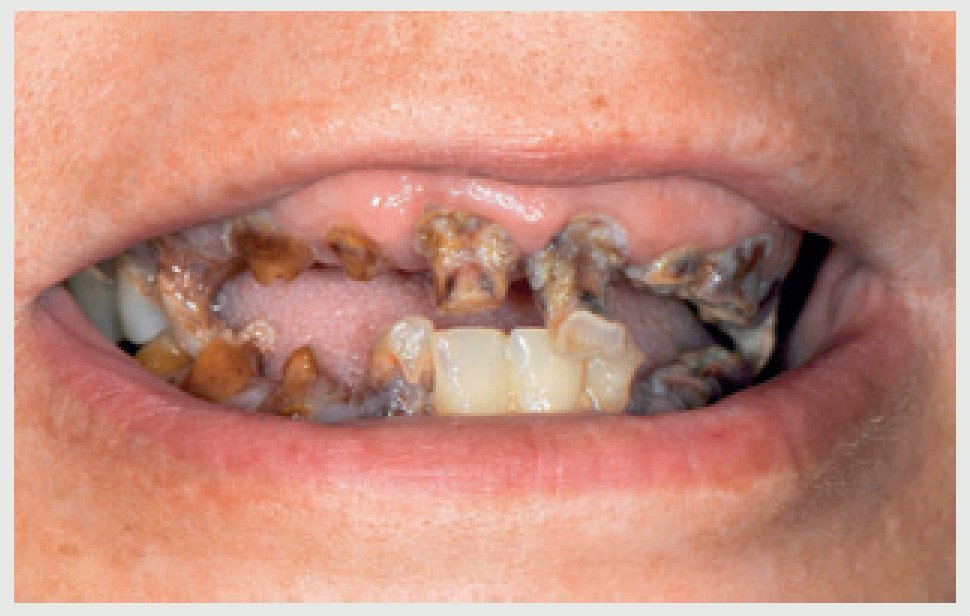
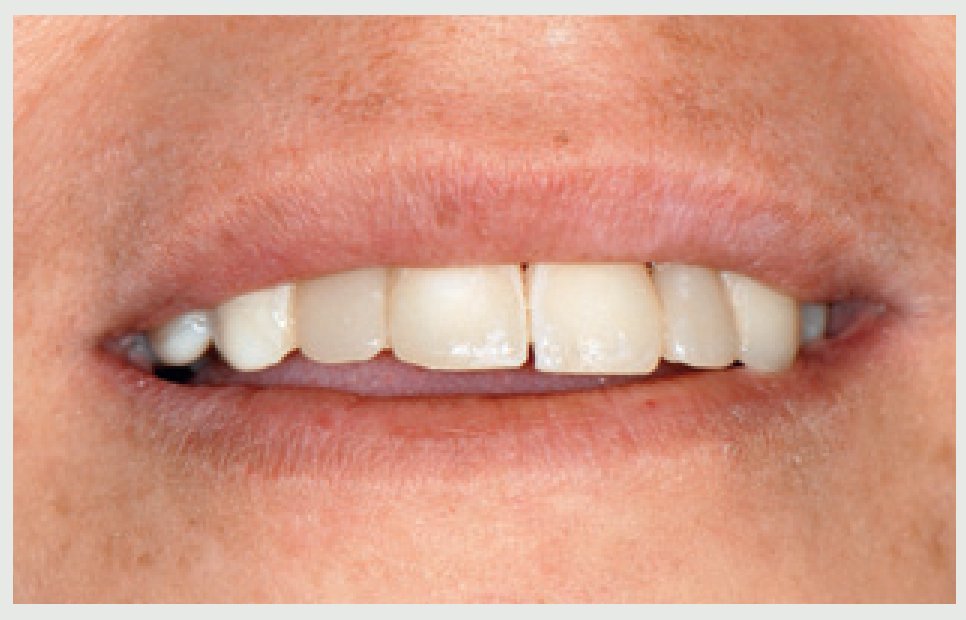
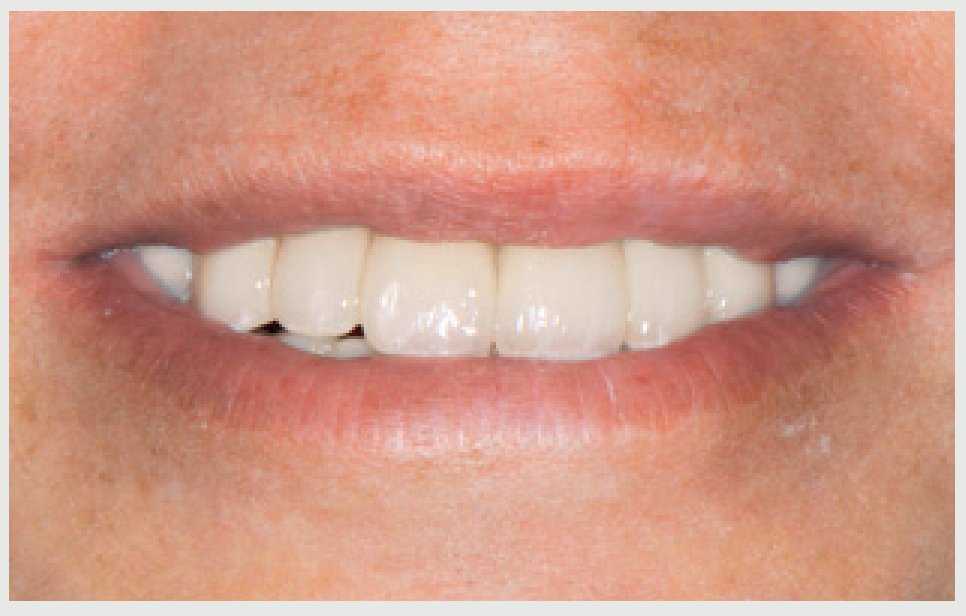
Figura 4 Sonrisa en la situación inicial. Obsérvese la sonrisa gingival.
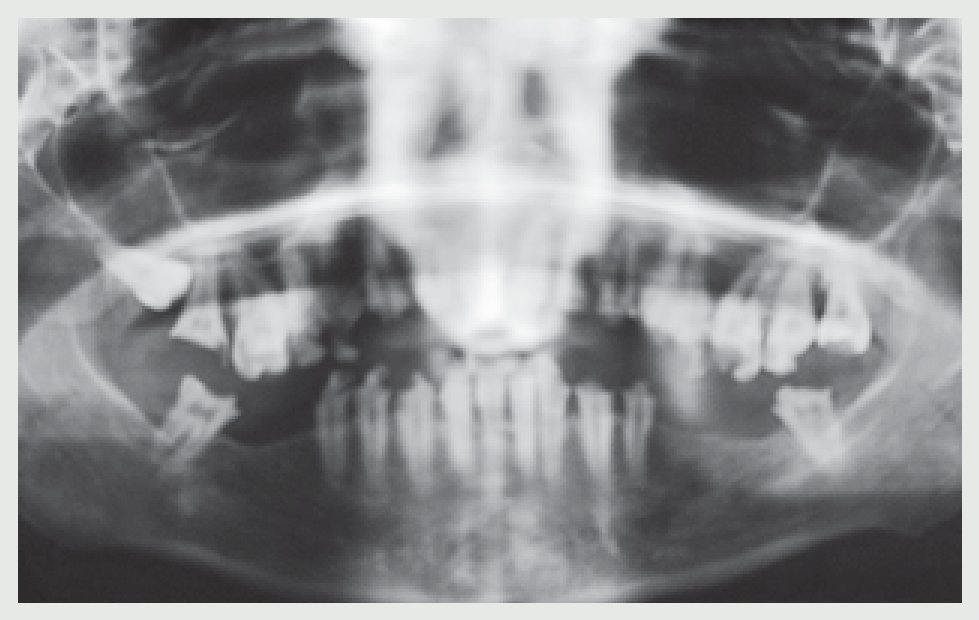
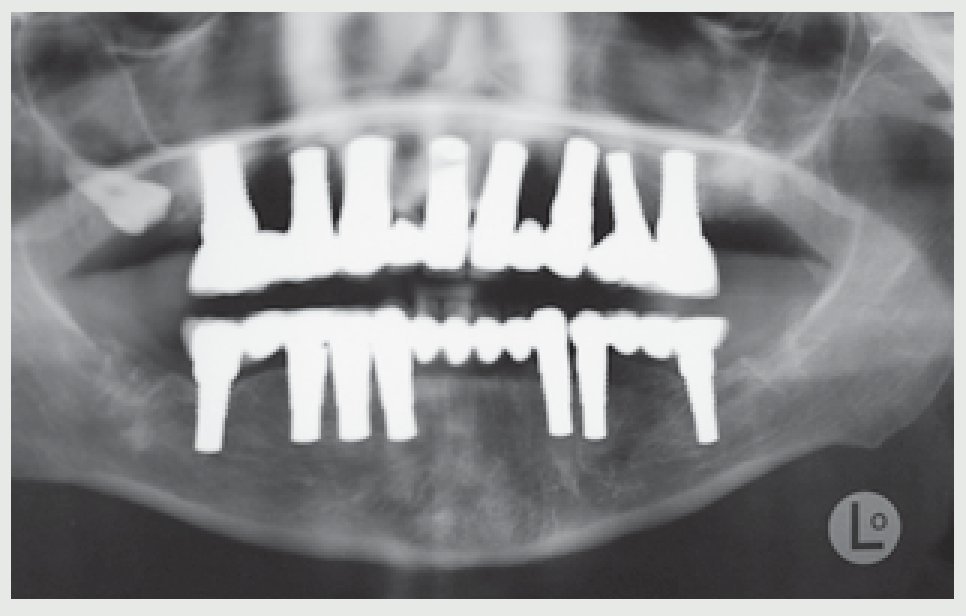
Figura 5 Radiografía panorámica de la situación inicial.
Plan terapéutico
La planificación preoperatoria se realizó con un encerado diagnóstico para tener una idea más exacta del objetivo final del tratamiento. Este modelo posteriormente se duplicó para fabricar férulas quirúrgicas al vacío que actuarían como referencia durante la cirugía.
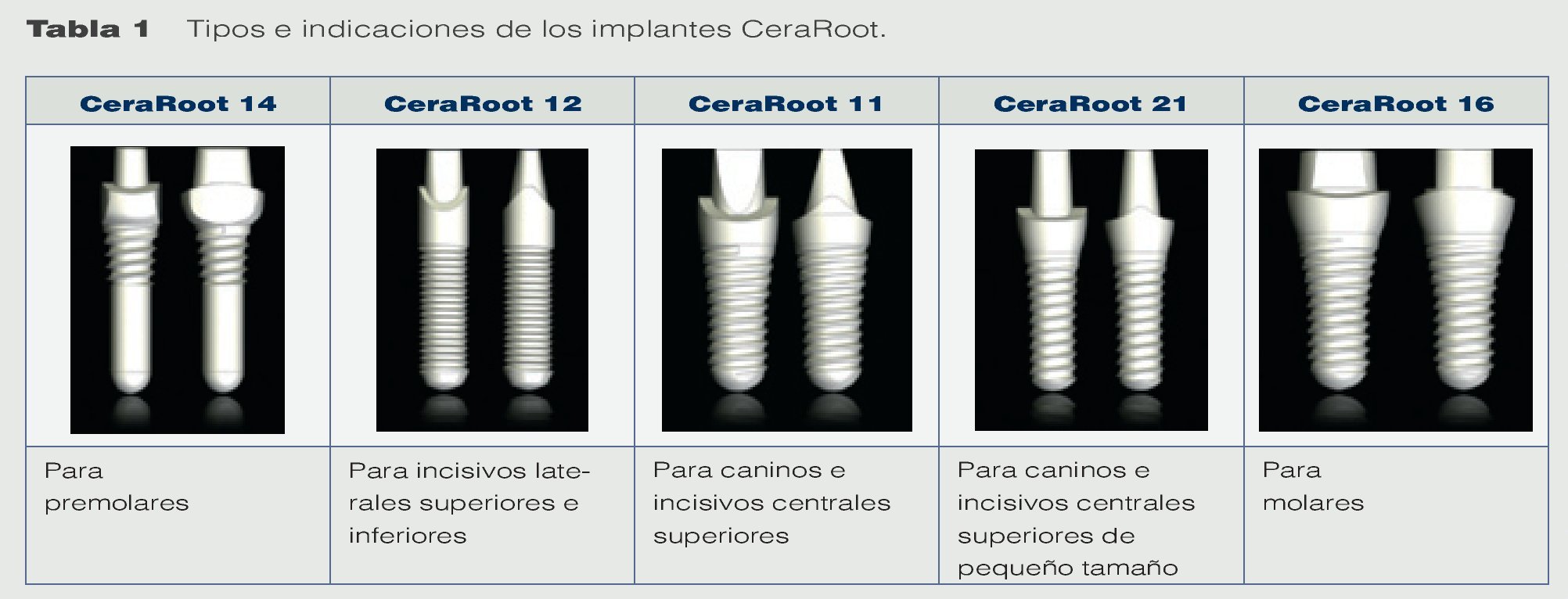
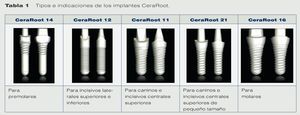
Hubo que extraer todas los dientes y colocar implantes para soportar la rehabilitación oral fija. Se utilizaron implantes y restauraciones de ZrO2 (sistema Cera-Root, véase la tabla 1). Son implantes de una pieza con cinco formas diferentes dependiendo del diente a restaurar. El plan consistió en extraer todos los dientes del maxilar superior y colocar inmediatamente los implantes, y 15 días después proceder con el maxilar inferior. No se planificaron restauraciones provisionales inmediatas en este caso porque no existe evidencia científica ni resultados a largo plazo sobre rehabilitaciones orales de boca completa con implantes de ZrO2 y su función inmediata. Se estimó que la fase de cicatrización podría durar unos 3 meses para la integración óptima del implante y la estabilidad de los tejidos blandos52. Además, los autores no se sintieron seguros colocando restauraciones provisionales durante un período largo con cementación temporal, teniendo que hacer frente a descementaciones y a un posible fracaso de los implantes. En los casos complejos, la seguridad del tratamiento es la principal prioridad. Se valoró el riesgo de sobrecargar prematuramente los pilares de los implantes de ZrO2 y los autores lo consideraron mucho menor que prolongar la utilización de las restauraciones temporales inmediatas.
Se planificaron puentes temporales para una fase posterior (3 meses después de la cirugía), una vez hubieran cicatrizado los tejidos blandos y se hubiese producido la osteointegración del implante.
Cirugía
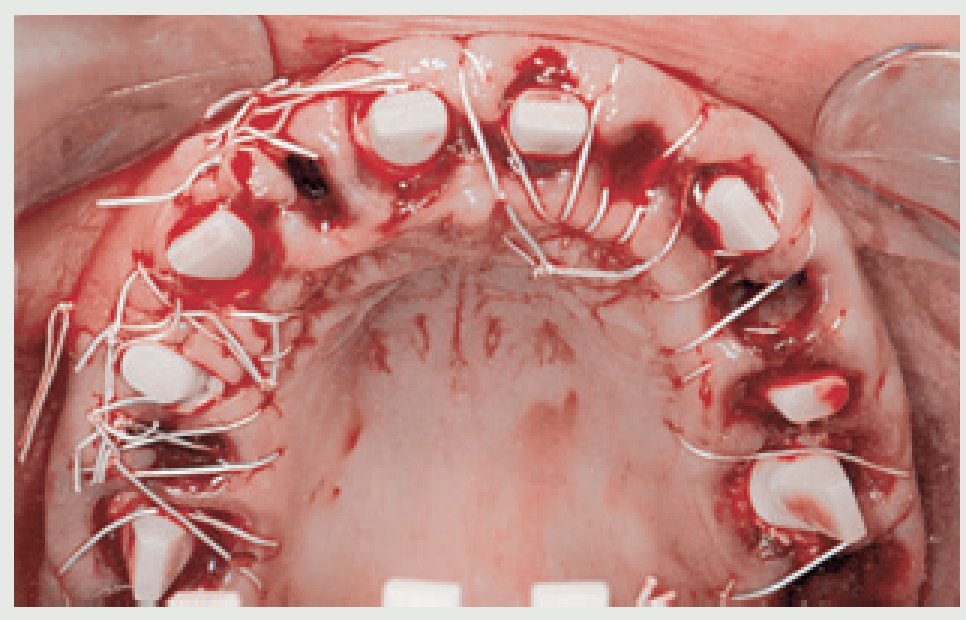
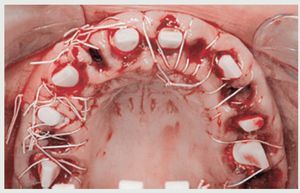
Se planificó una cirugía mínimamente invasiva con la colocación inmediata del implante sin colgajo en las zonas de extracción siempre que fuera posible, exceptuando el área del canino derecho superior en la que existía un quiste apical, y en las zonas edéntulas posteriores del maxilar inferior. Estas zonas se trataron con un abordaje convencional con colgajo. Dado que la oclusión antigua de la paciente era de clase I, y la línea media era correcta, los implantes se colocaron exactamente en la misma posición e inclinación de la dentición natural (figuras 6 y 7). Sin embargo, en el maxilar superior anterior, la preparación con la fresadora se realizó ligeramente en la pared palatal de la fosa alveolar para captar más hueso palatal y evitar la fenestración del implante en la región apical.
Figura 6 Aspecto oclusal tras la cirugía del maxilar superior.
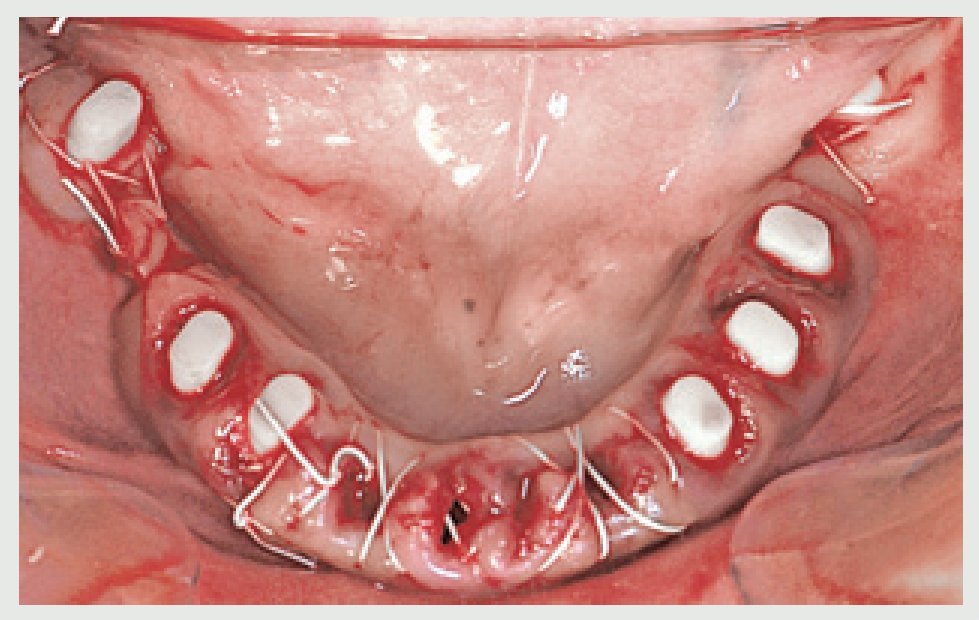
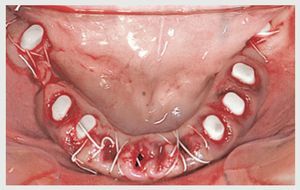
Figura 7 Aspecto oclusal de la cirugía del maxilar inferior.
La cirugía comenzó por el maxilar superior. Se extrajeron los incisivos centrales y laterales y se colocaron dos implantes CeraRoot 11 de 12 mm (diámetro de la espira 4,8 a 6 mm). Las zonas de los implantes se prepararon cuidadosamente y se utilizaron férulas quirúrgicas para verificar la posición correcta de los implantes. En la zona anterior es particularmente importante que estos implantes estén orientados hacia el borde incisal para facilitar la restauración con un resultado estético óptimo. Luego se extrajeron los caninos y se colocó otro implante CeraRoot 11 en la zona del diente23. La lesión periapical y la fístula del canino 13 habían reabsorbido el tercio apical de la placa cortical vestibular. Por este motivo se levantó un colgajo trapezoidal en esta zona. El quiste apical se desbridó cuidadosamente y se irrigó con solución salina. Se colocó un implante CeraRoot 11 y posteriormente se realizó un injerto óseo. El hueso autógeno de las zonas perforadas se colocó inmediatamente en la superficie del implante. Se colocó una segunda capa de Bio-Oss® (Geistlich, Wolhusen, Suiza) sobre el hueso autógeno. Posteriormente se colocó encima una membrana Bio-Gide® (Geistlich) y el colgajo se cerró con suturas Gore-Tex (W L Gore & Associates, Flagstaff, AZ, EE.UU.). Luego se extrajeron los premolares y los molares del maxilar superior. Se colocaron implantes CeraRoot 14 (diámetro de la espira 3,5 a 4,8 mm) en las zonas de los dientes 14, 15 y 24. Dos implantes CeraRoot 11 se colocaron en la zona de los dientes 16 y 26, donde se realizó una elevación de seno con un osteotomo Summer con injerto óseo (Bio-Oss).
Al final de la intervención quirúrgica, los tejidos blandos de alrededor de los implantes y de las fosas de extracción eran muy móviles, y por ese motivo se colocaron suturas en la cresta alveolar para estabilizar los tejidos blandos, especialmente alrededor de los implantes.
Se pidió a la paciente que mantuviese una dieta blanda durante 2 meses para reducir al mínimo la carga sobre los implantes. El riesgo potencial de fracaso del implante tras una carga prematura se comentó claramente con la paciente y ella expresó su compromiso total con el tratamiento y la pauta postoperatoria.
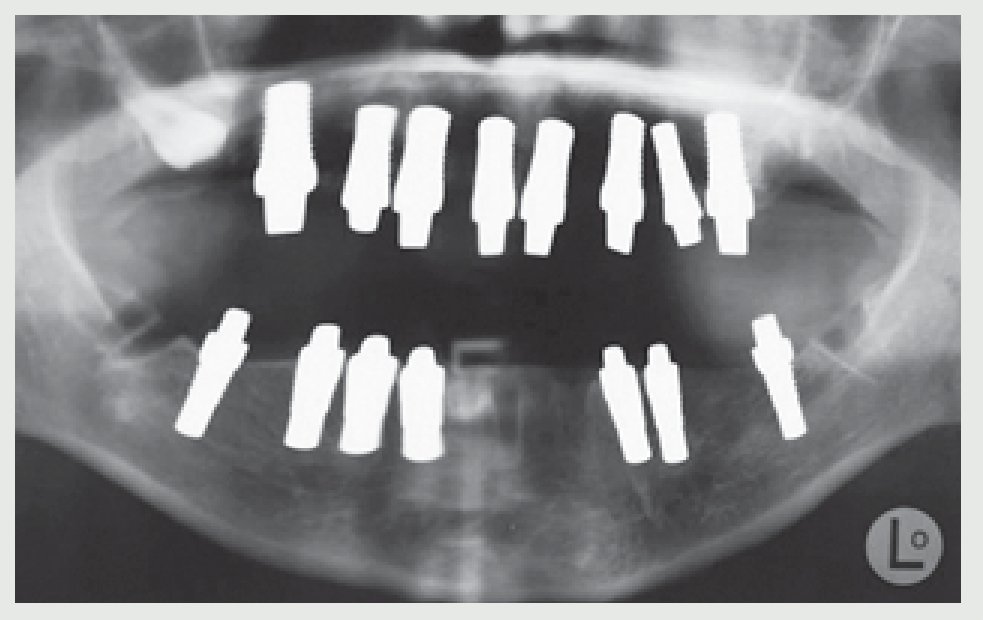
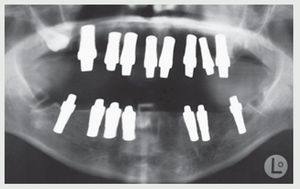
Se aconsejó a la paciente que dejara de fumar durante 15 días antes y después de la cirugía. La radiografía panorámica postoperatoria reveló una buena posición de los implantes (figura 8).
Figura 8 Radiografía panorámica postoperatoria.
La paciente fue citada 15 días después para la cirugía del maxilar inferior. Las extracciones se realizaron sin necesidad de levantar ningún colgajo y se colocaron implantes (CeraRoot 14) de forma inmediata en las fosas de extracción de los dientes 45, 44, 43, 33 y 34 (figura 7). Se colocaron suturas para cerrar las fosas de extracción en la región incisal. Los implantes de las zonas de los dientes 47 y 37 se colocaron tras levantar un colgajo desde la zona del primer al tercer molar. Se colocaron suturas para cerrar la herida. La paciente recibió instrucciones idénticas a las descritas tras la cirugía del maxilar superior.
Período de cicatrización
Durante el período de cicatrización, se solicitó a la paciente que mantuviera una higiene periódica tras las comidas con un cepillo de dientes quirúrgico blando. Quince días después de la cirugía se retiraron los puntos del maxilar inferior. Tres semanas después de la cirugía, el aspecto clínico de los tejidos blandos era muy satisfactorio. Dos meses después de la cirugía, el tejido blando había cicatrizado (figura 9). Se evaluaron los implantes y no se apreció dolor a la percusión ni movilidad.
Figura 9 Aspecto del tejido blando 2 meses después de la cirugía.
Restauración temporal
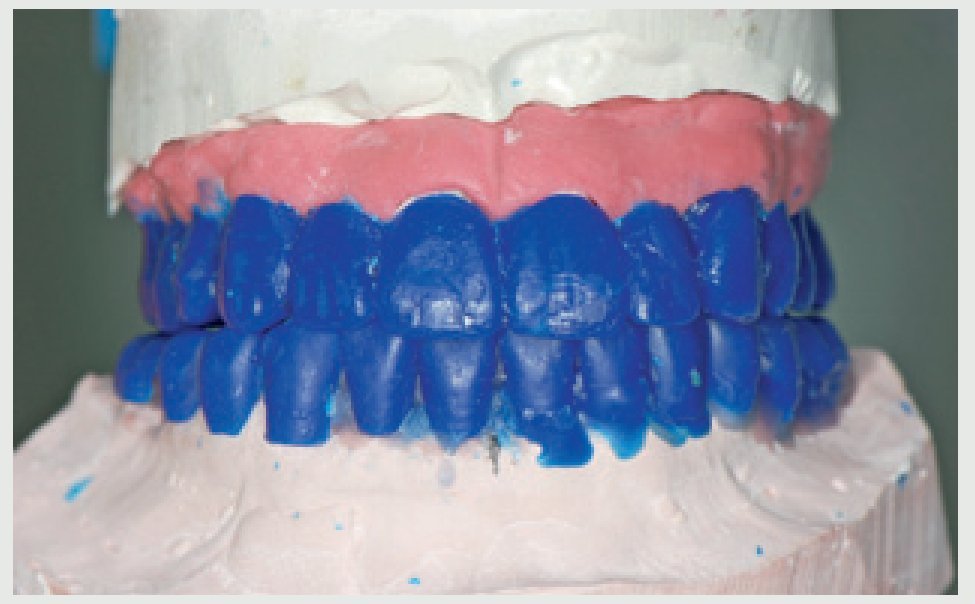
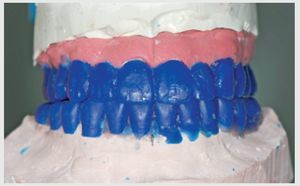
Dos meses después de la cirugía algunos implantes presentaron tejido blando por encima del hombro de los implantes. Este tejido blando se extirpó con ayuda de un bisturí eléctrico y se tomaron impresiones directamente con un poliéter (Impregum TM, 3M ESPE, Neuss, Alemania) y sin ninguna preparación implantaria. Se realizó un encerado de boca completa (figura 10), y con éste una llave de silicona que se rellenó con un material base de resina de curado dual (Protemp TM Garant, 3M ESPE) y se adaptó al maxilar superior e inferior. Luego la restauración temporal se pulió y se cementó en los implantes con cemento GC Temp (GC America Alsip, IL, EE.UU.) (figura 11).Figura 10 Encerado de la rehabilitación provisional.
Figura 11 Provisionales de resina 3 meses después de la cirugía.
La paciente pudo adaptarse a la nueva oclusión y la nueva dimensión vertical mientras se puso especial atención en verificar la estabilidad del patrón de oclusión, así como a la estética y la fonética con transcurso del tiempo. Teniendo esto en cuenta, la oclusión de la paciente se evaluó cada semana durante 1 mes. Se realizaron pequeños ajustes de la oclusión y la estética necesarios para obtener una situación idónea para las restauraciones finales.
Reconstrucción final
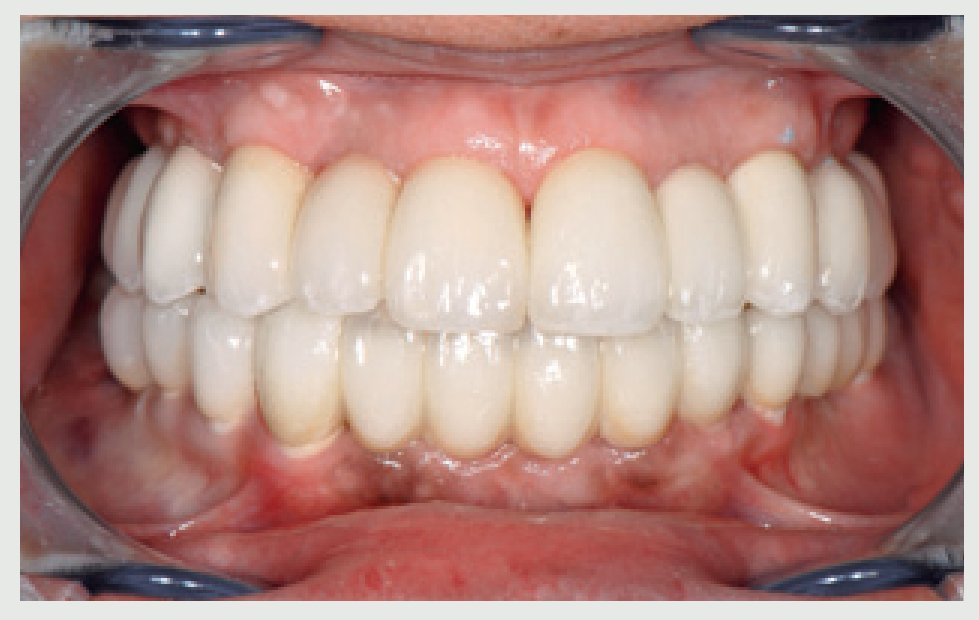
Las impresiones finales se tomaron directamente con un poliéter (Impregum) sin necesidad de preparar ningún pilar implantario ni utilizar hilos de retracción. La restauración temporal actuó como guía para diseñar los puentes finales de circonio (CeraCrown, Oral Iceberg), que se fabricaron finalmente con una técnica de estratificación de la cerámica (IPS e-max, Ivoclar Vivadent, Schaan, Liechtenstein). Los 6 puentes se cementaron con cemento de ionómero de vidrio reforzado con resina (FujiCEM, GC America). El caso se finalizó con una guía incisal anterior y una guía lateral cuspídea (figura 12).Figura 12 Cementación de los puentes de ZrO2.
Seguimiento
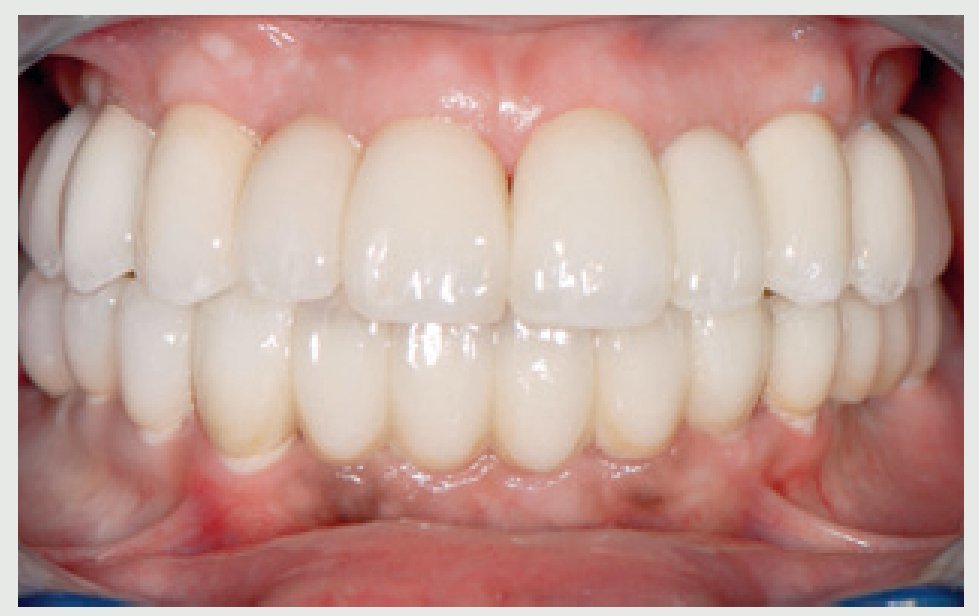
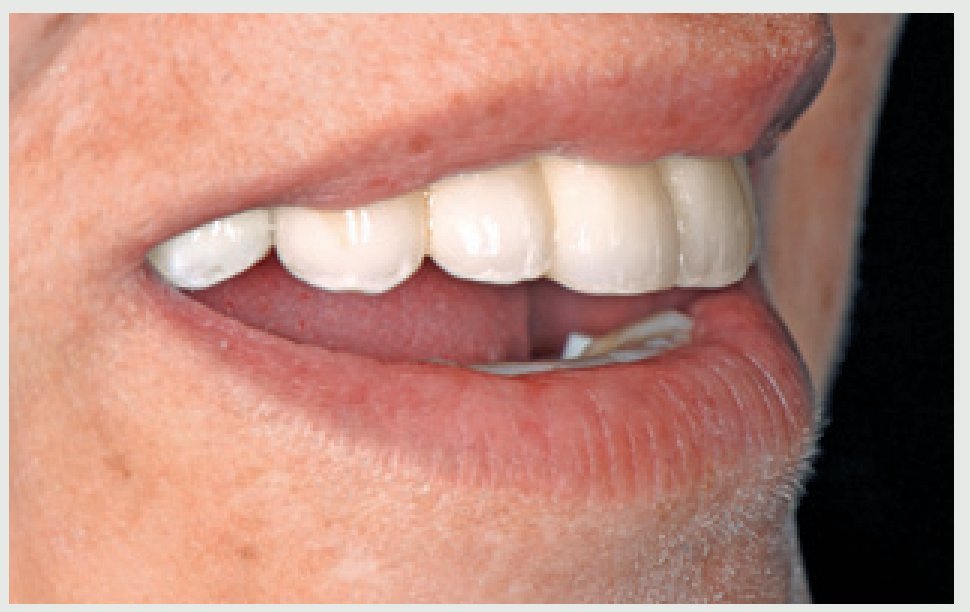
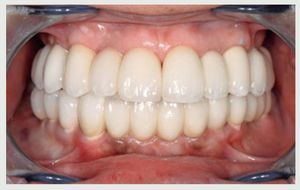
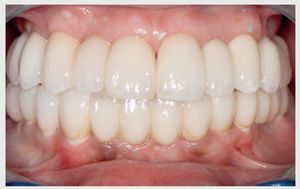
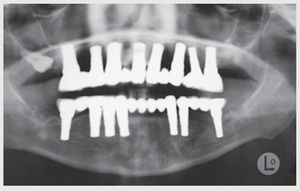
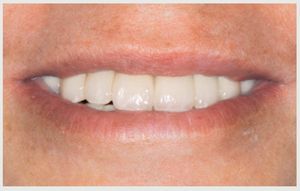
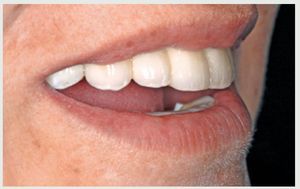
Tres años después de la cementación final los implantes y puentes de ZrO2 eran estables y la paciente expresó su satisfacción (figura 13). La radiografía panorámica (figura 14) muestra la precisión del ajuste marginal de la restauración y la estabilidad del nivel óseo alrededor del implante. La sonrisa gingival (figura 15) y el soporte labial mejoraron (figura 16).
Figura 13 Obsérvese la estabilidad de los tejidos blandos durante el seguimiento a los 3 años.
Figura 14 Radiografía panorámica durante el seguimiento a los 3 años.
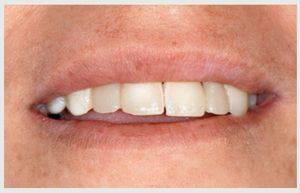
Figura 15 Aspecto de la sonrisa durante el seguimiento a los 3 años.
Figura 16 Vista lateral de la sonrisa.
Discusión
Los implantes dentales de titanio son en la actualidad el gold standard de las rehabilitaciones orales. No obstante, en los pacientes con sospecha de hipersensibilidad a los metales, debe considerarse el diagnóstico de alergias con el TTL. Esta prueba ha demostrado ser la mejor forma de diagnosticar alergias cutáneas y sistémicas al Ti, aunque no se ha demostrado científicamente su relación con los implantes dentales de Ti.
Los implantes de ZrO2 pueden ser una buena alternativa a los implantes de Ti en los casos adecuados. La biocompatibilidad del ZrO2 está generalmente aceptada y parece que la superficie rugosa de los implantes de ZrO2 ha mejorado las puntuaciones del contacto hueso-implante en comparación con la superficie lisa de los implantes de ZrO2.
Sin embargo, el pronóstico a largo plazo de la superficie CeraRoot grabada al ácido (ICE) todavía tiene que demostrarse. Las propiedades mecánicas de los implantes dentales de ZrO2 también se han estudiado en diferentes publicaciones. Se ha demostrado que los implantes de ZrO2 tienen la resistencia suficiente para ser utilizados como implantes dentales. Sin embargo, la preparación con fresas de diamante podría alterar esta resistencia mecánica y comprometer la integridad de los implantes a largo plazo45. Por este motivo, es prudente utilizar los implantes dentales de ZrO2 que no requieren preparación. La degradación de los implantes Y-TZP con las bajas temperaturas, y el astillado de los recubrimientos de cerámica son aspectos que se siguen investigando.
No se colocó ninguna restauración temporal durante la fase de cicatrización de este caso, hasta que los implantes hubieron adquirido una buena osteointegración. En la actualidad no se dispone de evidencia científica, experiencia o resultados a largo plazo que apoyen la función inmediata con los implantes de ZrO2 en rehabilitaciones orales de boca completa. Por este motivo, los autores decidieron no realizar una provisionalización ni función inmediatas. Los autores consideraron este caso muy desafiante y así se lo manifestaron a la paciente. Para evitar una función prematura y la sobrecarga de los implantes, especialmente en las zonas injertadas, la paciente se mantuvo con una dieta blanda durante 2 meses hasta que finalizó la osteointegración completa. Si bien este protocolo, sin ninguna provisionalización inmediata, podría no ser aceptado por la mayoría de los pacientes actuales, puede estar indicado en abordajes terapéuticos especiales en casos como éste. Además, las investigaciones futuras también pueden validar la provisionalización inmediata de los implantes de ZrO2 como un posible protocolo terapéutico. El riesgo potencial del fracaso del implante podría haberse reducido realizando las cirugías por cuadrantes o incluso por sextantes. Sin embargo, el tiempo total de tratamiento hubiese aumentado mucho. Por ultimo, el riesgo de fracaso del implante debido a una sobrecarga prematura se consideró aceptable y razonable dado el compromiso de la paciente con el tratamiento.
Con respecto al pronóstico de los implantes de ZrO2 CeraRoot con superficie ICE, no existen datos clínicos publicados a largo plazo. Este caso clínico forma parte de un estudio clínico en curso50 cuyos resultados preliminares han sido publicados con anterioridad. El seguimiento durante 5 años de más de 800 implantes ha sido recientemente publicado, con una tasa de éxito de cerca del 95 %. Además, no se ha informado de fracturas implantarias, periimplantitis o pérdida de hueso. Desde el punto de vista protésico, no se han producido fracturas de ninguna subestructura de circonio, y el astillado de los recubrimientos de cerámica fue muy raro. Esto se atribuyó al buen diseño de los armazones de circonio, con especial atención al correcto soporte de la porcelana en los aspectos oclusal, lingual e interproximal de las restauraciones.
Conclusiones
A pesar de que este trabajo sólo presenta un caso clínico de un estudio clínico en curso, demuestra que incluso los casos complejos y con una elevada demanda estética pueden tratarse de forma satisfactoria con implantes y restauraciones de ZrO2. Según la información de que disponen los autores, este artículo es el primero que informa de una rehabilitación oral total con implantes de ZrO2 y restauraciones de ZrO2. Aunque la escasa evidencia científica disponible con respecto a los implantes de ZrO2 es muy prometedora, son necesarias investigaciones a largo plazo para demostrar el éxito, la estabilidad y la integridad de los implantes CeraRoot con superficie ICE.
Correspondencia: Dr. Xavi Oliva
Clínica Oliva Dental, Josep Umbert, 126 Granollers, Barcelona, Spain 08402;
tel: +34 938705199; e-mail: info@clinicaoliva.com