Notas preliminares
Se ha comprobado que el trasplante autólogo de condrocitos (TAC) es una opción adecuada para tratar los defectos cartilaginosos profundos. Diversos estudios demuestran una constancia de los resultados clínicos incluso durante más de 10 años, sobre todo en pacientes con operaciones previas en el cartílago7,9. El inconveniente más significativo es la necesidad de una artrotomía para implantar los cultivos celulares. Más del 26% de los efectos secundarios específicos pueden atribuirse a la artrotomía, sobre todo en forma de fibroartrosis7. El abordaje mediante artroscopia permite evitar las adherencias, la limitación de la movilidad, el dolor posquirúrgico y las cicatrices llamativas. La técnica original del TAC de Brittberg et al consiste en inyectar una suspensión celular en el defecto bajo un colgajo de periostio1. Actualmente las nuevas técnicas de cultivo celular y los materiales modernos permiten realizar un implante con materiales portadores absorbibles tridimensionales. La utilización de estos materiales portadores permite distribuir las células por el defecto y simplifica la manipulación quirúrgica. Se puede prescindir de la sutura a través del cartílago intacto para fijarlo. Los materiales portadores se descomponen tras un tiempo definido (3-6 meses) y dejan espacio para la neosíntesis de tejido regenerativo cartilaginoso que ocurre en paralelo.
En la actualidad existen diversos grupos de sustancias absorbibles de utilidad clínica con diversas formas de presentación:
- Colágeno de origen animal (casi siempre colágeno I y III) con una estructura fibrosa o en forma de gel o de membrana.
- Hialuronano y polímeros (PLA, PGLA) fibrosos.
La fijación se realiza en función de las características biomecánicas del implante y del tamaño y localización del defecto. Los geles semirrígidos o las membranas pueden colocarse fácilmente en el defecto, en el que se mantienen mediante fuerzas de adhesión y sin ninguna otra sujeción. Otra alternativa es una adherencia superficial o puntual con adhesivo de fibrina. La máxima estabilidad biomecánica inicial, en caso de sangrado del defecto o localización en un borde sometido a fuerzas de cizalla, se consigue con una fijación transósea2,5.
Hasta ahora se han descrito dos técnicas distintas4,6.
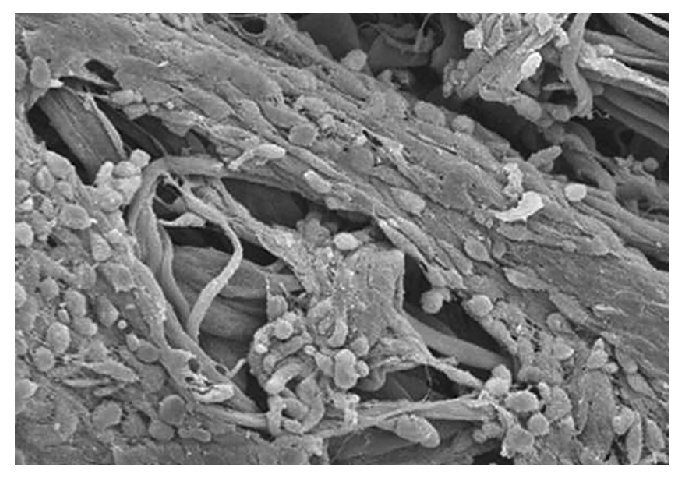
Marcacci et al han desarrollado una técnica con una lámina de fibra de hialuronano para colocar implantes troquelados redondos en el defecto cartilaginoso y sujetarlos con fuerzas de adhesión6. En esta lámina absorbible se han incorporado condrocitos autólogos (fig. 1). El principio equivale a una mosaicoplastia condral. La zona a tratar se desbrida en círculos de tamaño estándar con un instrumental especial. Los autores recomiendan una perforación de la placa subcondral. A partir de un portador celular ya listo para su uso se troquelan los implantes correspondientes al tamaño del defecto y se introducen en la articulación a través de una cánula de implantación. Se fijan aplicando una ligera presión o con ayuda de un adhesivo de fibrina. Para los defectos más grandes se recurre a varios implantes (fig. 2), si bien la técnica es más difícil a medida que aumenta el número.
Figura 1. Imagen de microscopio electrónico de una matriz de hialuronano impregnada de condrocitos (por gentileza de S. Marlovits, Viena, Austria).
Figura 2. Matriz en bruto tridimensional de hialuronano para extraer implantes redondos para la implantación artroscópica de condrocitos autólogos (por gentileza de S. Marlovits, Viena, Austria).
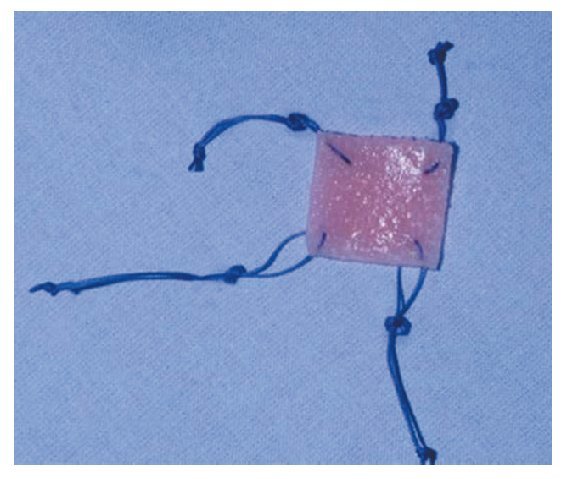
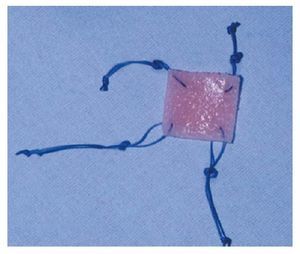
A continuación se describe con detalle una técnica alternativa de Erggelet et al, sobre todo para el tratamiento de defectos más grandes4. Un anclaje biomecánico primario estable permite tratar también lesiones cartilaginosas con límites inestables. Se implanta una matriz polimérica bioabsorbible, de 2 mm de grosor y 2 x 3 cm de tamaño, con 5 x 107 células/cm3 (Bioseed-C®, fig. 3).
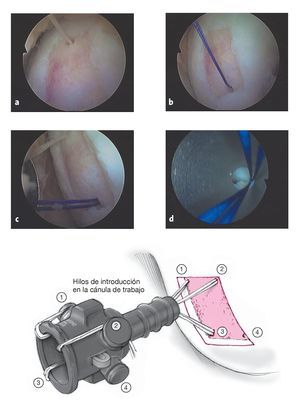
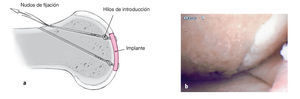
Figura 3. Matriz absorbible portadora de células con hilos de vicrilo ya colocados, antes de introducirla en la articulación a través de la cánula de trabajo.
Principios quirúrgicos y objetivos Implante biomecánico estable de condrocitos autólogos sobre materiales portadores en un defecto condral mediante abordaje artroscópico. Se evitan daños articulares secundarios debidos a una artrotomía.
Ventajas
Abordaje por artroscopia.
Número estándar de células en el defecto y estabilidad biomecánica primaria gracias al uso de una matriz absorbible.
Rehabilitación más rápida y menos efectos secundarios quirúrgicos al evitar una artrotomía.
Inconvenientes
Abordaje en dos tiempos.
Técnica quirúrgica exigente con instrumental especial.
No todos los defectos cartilaginosos pueden tratarse con artroscopia.
Indicaciones
Defectos cartilaginosos de grado 3-4 de Outerbridge, con un tamaño de 1-6 cm2.
Contraindicaciones Absolutas
Artrosis avanzada.
Artritis.
Inestabilidad articular incorregible.
Relativas
Edad del paciente > 55 años.
Obesidad.
Tabaquismo.
Falta de cooperación.
Defectos cartilaginosos coincidentes ("kissing lesions").
Información para el paciente
Explicación antes de la operación de los costes que asumirá el seguro médico.
Ingreso hospitalario de 1-5 días.
Hasta 6 semanas con muletas, según tamaño y localización del defecto.
Hasta 3 meses de rehabilitación posquirúrgica.
Baja laboral de entre 2 semanas aproximadamente (trabajo sentado) y 3 meses (trabajo con gran esfuerzo físico y requisitos especiales, por ejemplo de coordinación y estabilidad). Los procesos de maduración del injerto pueden durar hasta un año o más.
Persistencia de las molestias (alrededor del 20%) o empeoramiento (< 5%).
Riesgo de desprendimiento del implante.
Riesgo de reacciones alérgicas a los compuestos de PLA/polidioxanona (Vycril®, PDS®).
Riesgos quirúrgicos generales.
Preparación para la intervención
Artroscopia para obtener una biopsia de cartílago 3 semanas antes de la intervención.
Confirmación de la fecha de implantación a cargo del laboratorio citológico.
Instrumental
Kit de implantación (Biotissue Technologies, Engesser Strasse 4, 79108 Friburgo).
Juego de curetas de diversos tamaños.
Cánula de trabajo con portahilos (fig. 4).
Figura 4. Cánula de trabajo para introducir en la articulación una matriz absorbible portadora de células. Los cuatro norays para los hilos puestos en la periferia sujetan los hilos tensores y evitan que el implante se gire (Karl Storz, Tuttlingen, Alemania).
Aguja con escala.
Manipulador con posibilidad de bloqueo.
Cuatro agujas de Kirschner de 1,7 mm con ojales (p. ej., Arthrex, Karlsfeld).
Cuatro hilos de Vicryl 2-0, 70 cm con aguja atraumática (Ethicon).
Anestesia y posición del paciente
Posición para artroscopia (flexión hasta 120º, según la localización del defecto).
Anestesia general, anestesia de conducción.
Isquemia del muslo opcional.
Técnica quirúrgica
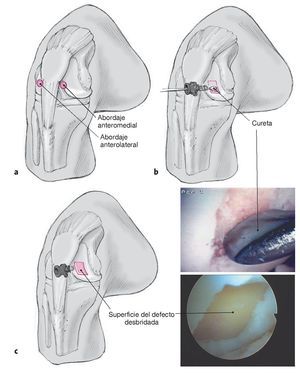
Figuras 5 a 11
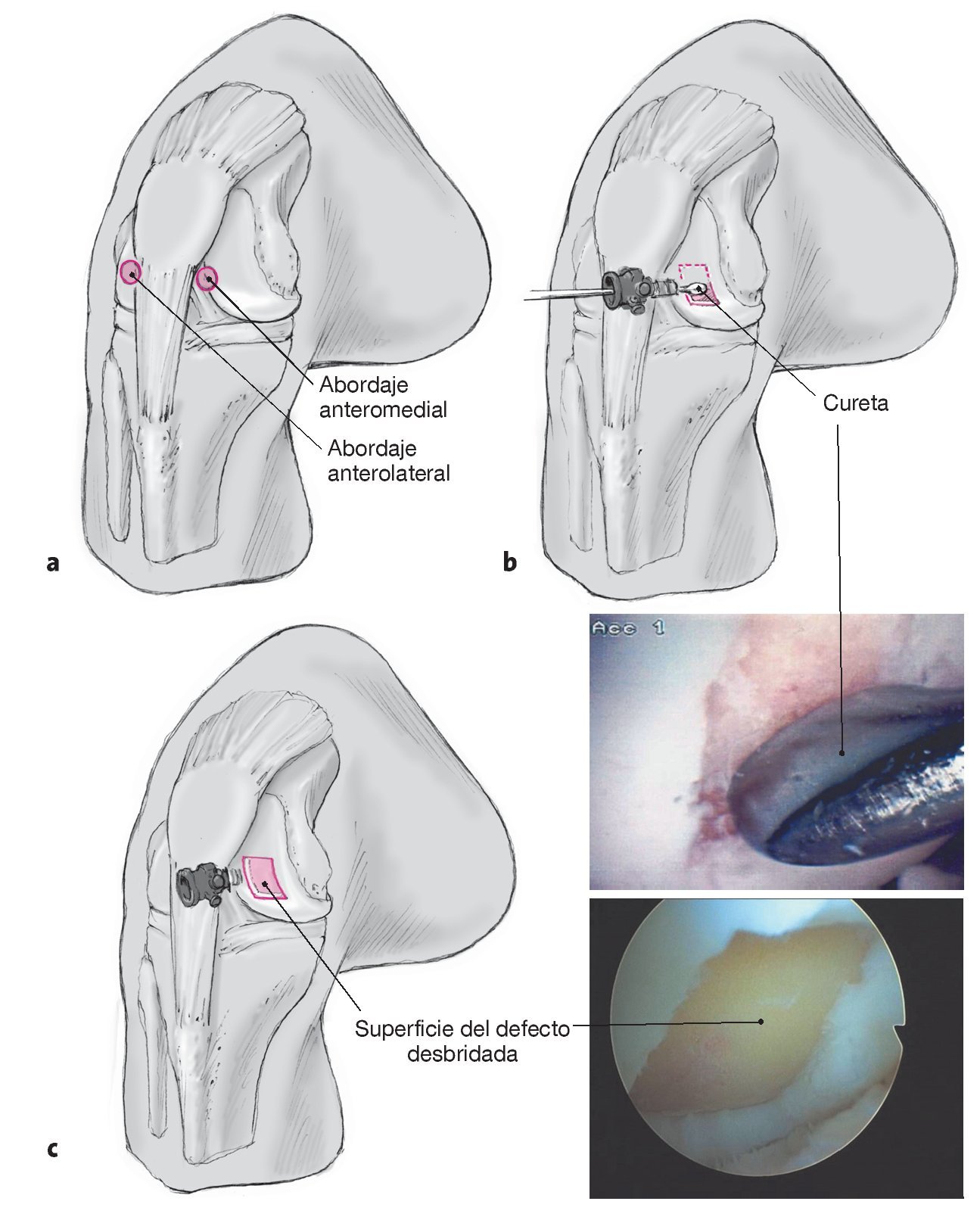
Figuras 5a a 5c. Abordaje anteromedial y anterolateral (a). El defecto articular del cóndilo femoral se desbrida con curetas de distintos tamaños (b) hasta conseguir un defecto cuadrado con bordes sólidos (c). Para esto es imprescindible disponer de un juego de curetas de diversos tamaños. El desbridamiento con la fresa hace que los bordes del defecto queden aplanados. Darle forma cuadrada al defecto, tal y como se ha indicado, facilita la implantación.
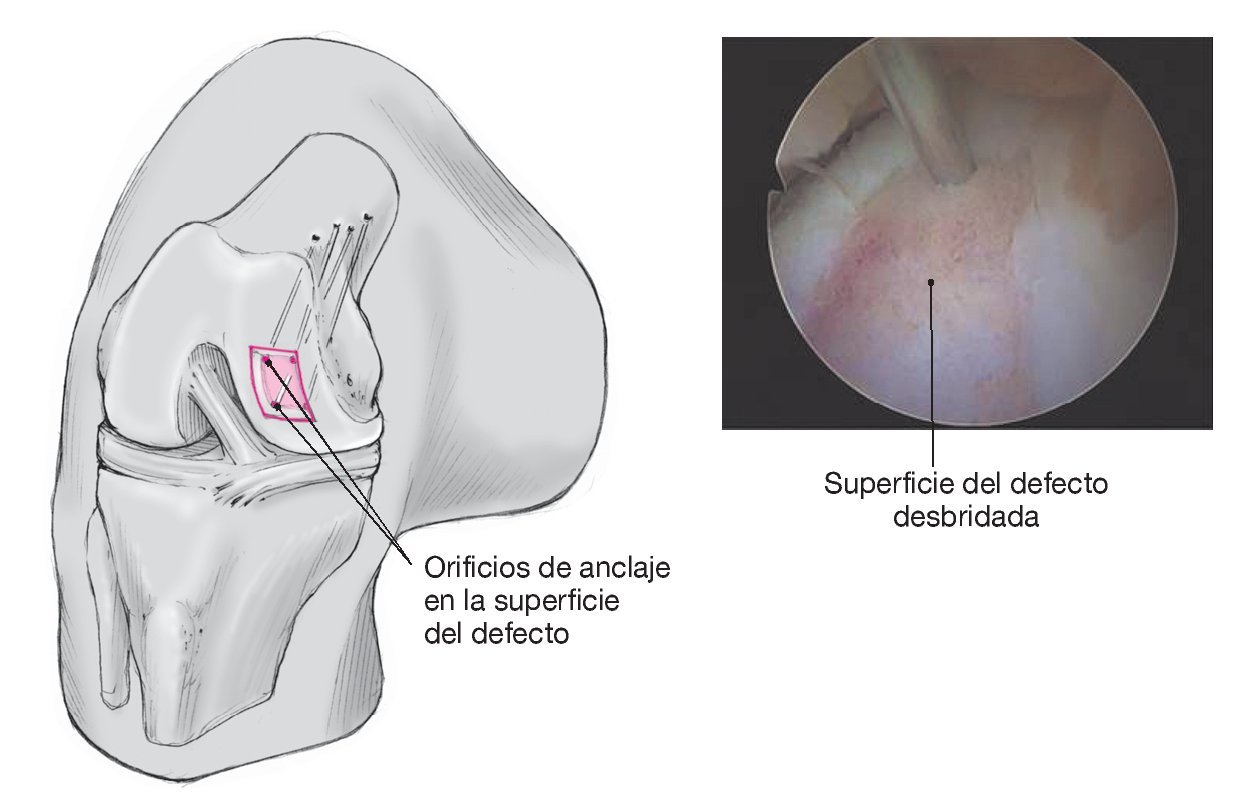
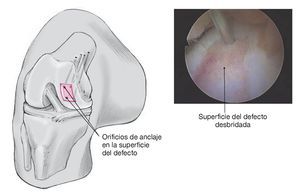
Figura 6. Realización de orificios de anclaje con agujas de Kirschner de 1,7 mm con ojales; como mínimo dos, casi siempre cuatro. Los orificios se hacen muy próximos a las esquinas del defecto para crear dos o más puntos de fijación, en dirección anterógrada, a través del hueso y saliendo a través de la piel. Se deben evitar las perforaciones dorsales de los tendones del bíceps por el riesgo de lesionar vasos y nervios. Por el mismo motivo son preferibles las agujas de Kirscher con talla de diamante en vez de taladros finos3.
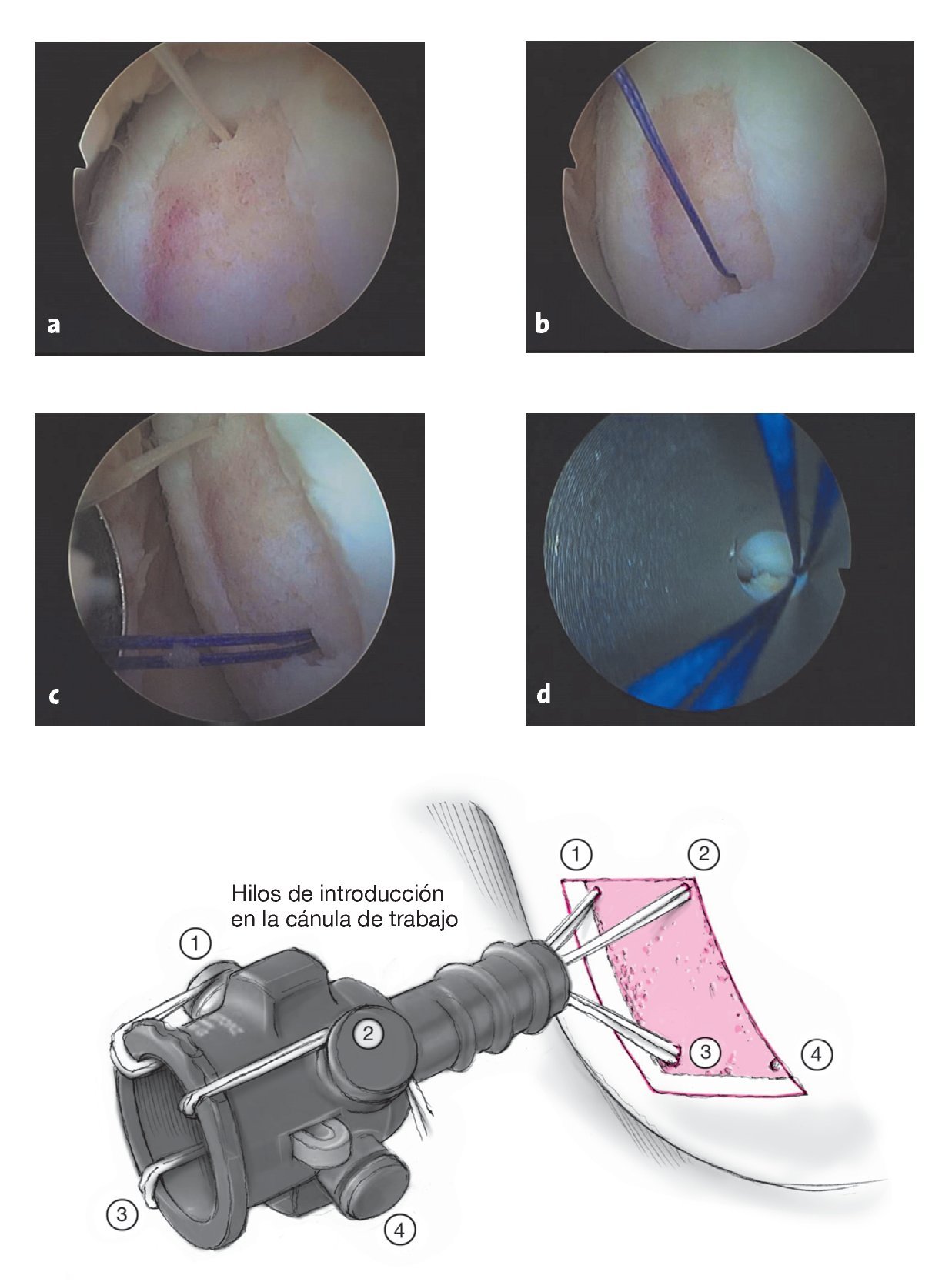
Figuras 7a a 7d. Introducción de los hilos de vicrilo 2-0, de 70 cm, con lazada y sin aguja a través de los orificios taladrados y salida percutánea. Colocación de un hilo de introducción por el borde superior (a) y el inferior (b) del defecto. Los lazos deben sujetarse en los norays de la cánula de trabajo según su posición en el borde del defecto para evitar que los hilos se retuerzan. Después ya no debe girarse la cánula. Usar hilos de distintos colores facilita su manipulación. Control artroscópico del recorrido paralelo de los hilos (c). Control del recorrido paralelo de los hilos en la cánula de trabajo con el artroscopio (d).
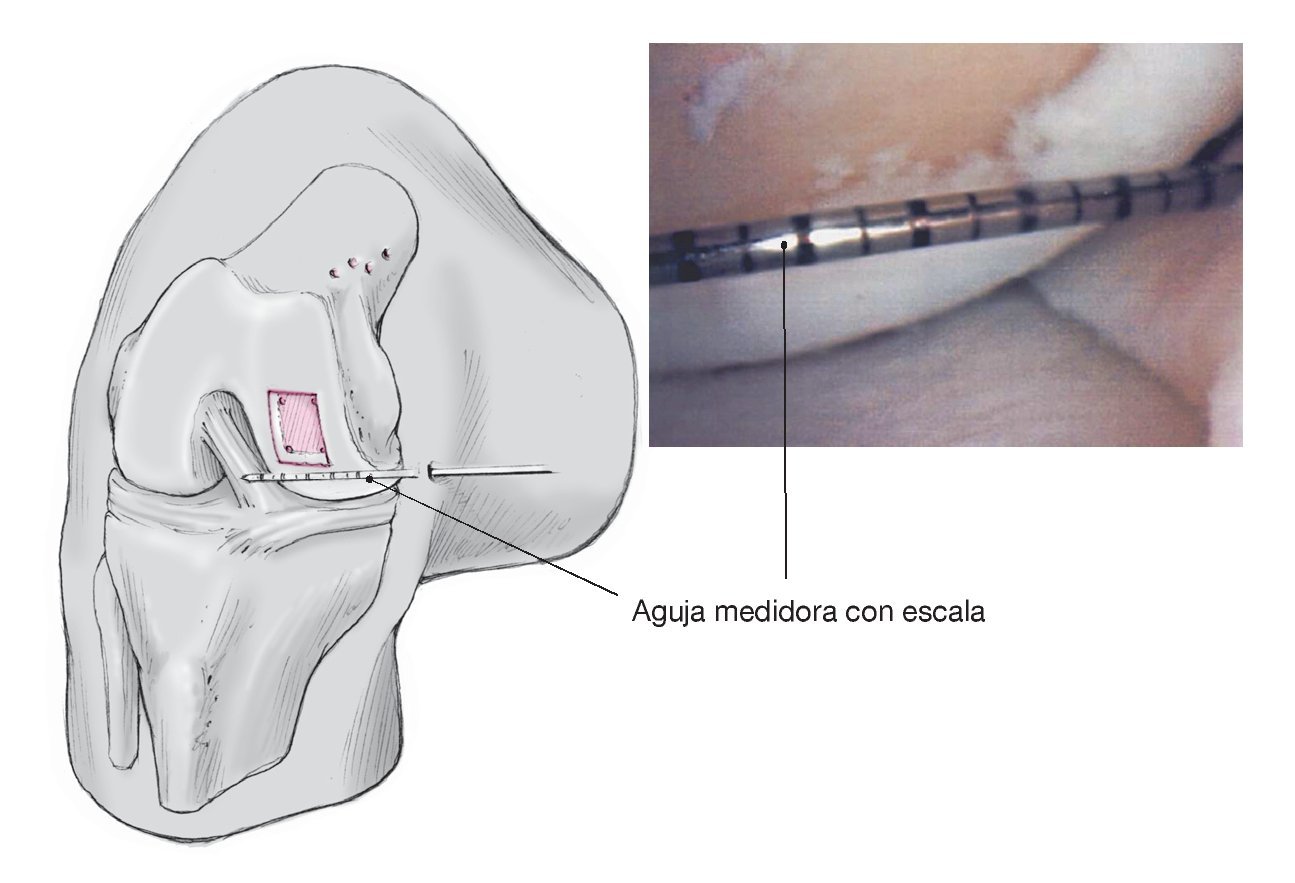
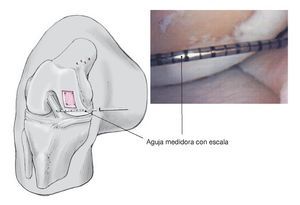
Figura 8. Medición del tamaño (distancia entre los orificios taladrados) del defecto del cartílago con una aguja con escala que se introduce en la articulación a través de la piel desde distintos ángulos. Recorte del implante con una tijera recta, si es necesario tras marcarlo con un rotulador dermográfico.
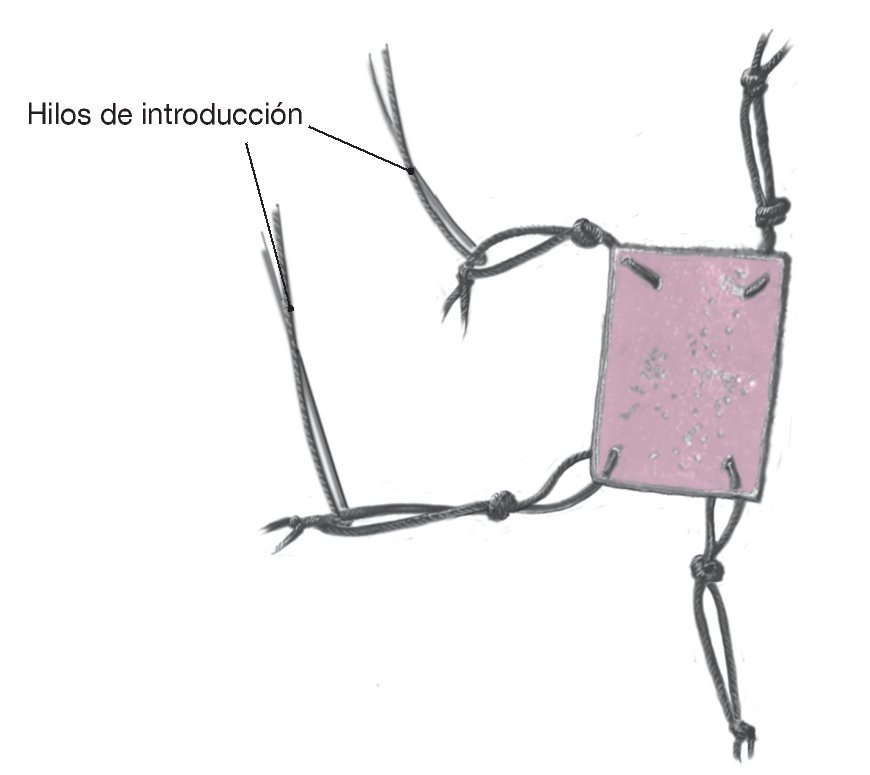
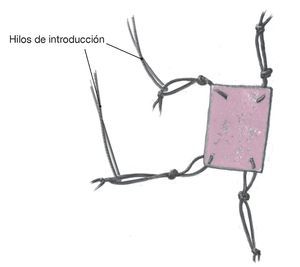
Figura 9. Montaje del implante con hilos de vicrilo 2-0 con una técnica especial de anudado en las esquinas según la posición de los orificios taladrados. Los nudos cuádruples son escasamente mayores que el diámetro del canal perforado (1,7 mm). Esto permite una fijación estable por presión. Se ha demostrado la utilidad de realizar un total de 12 nudos (4 a derechas, 4 a izquierdas y 4 a derechas) a una distancia aproximada de 1 cm del implante. Se hace un segundo lazo con dos nudos normales a otro centímetro de distancia del implante, que sirve para guiar el hilo de introducción vicrilo 2-0, que se pasará a continuación por dicho lazo.
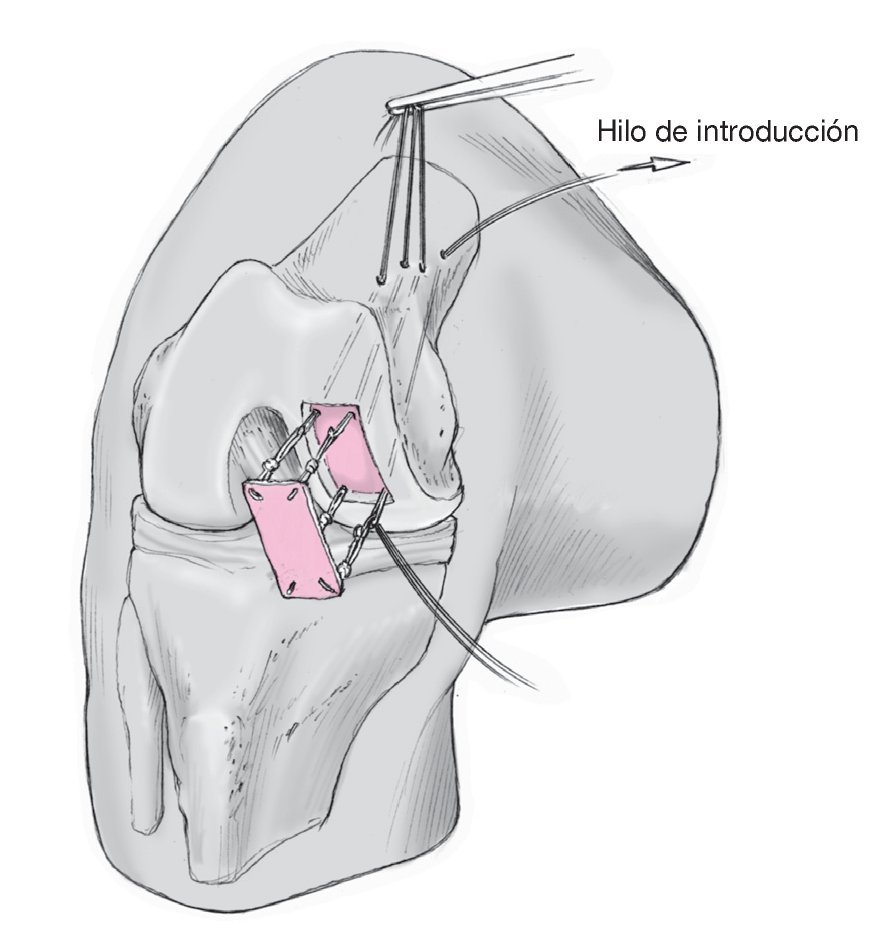
Figura 10. Colocación de los hilos de introducción en los lazos preparados al efecto, controlando la posición del implante en relación con el defecto. Para introducirlo en la articulación a través de la cánula de trabajo, el implante puede enrollarse o plegarse. Si durante la preparación se han pasado los hilos correctamente, el implante se desplegará dentro de la articulación según la posición del defecto. Puede utilizarse el manipulador atraumático como ayuda para guiar el implante. Nuevo control del recorrido paralelo de los hilos en la cánula de trabajo. Si los hilos no están paralelos el implante no podrá fijarse plano sobre la superficie.
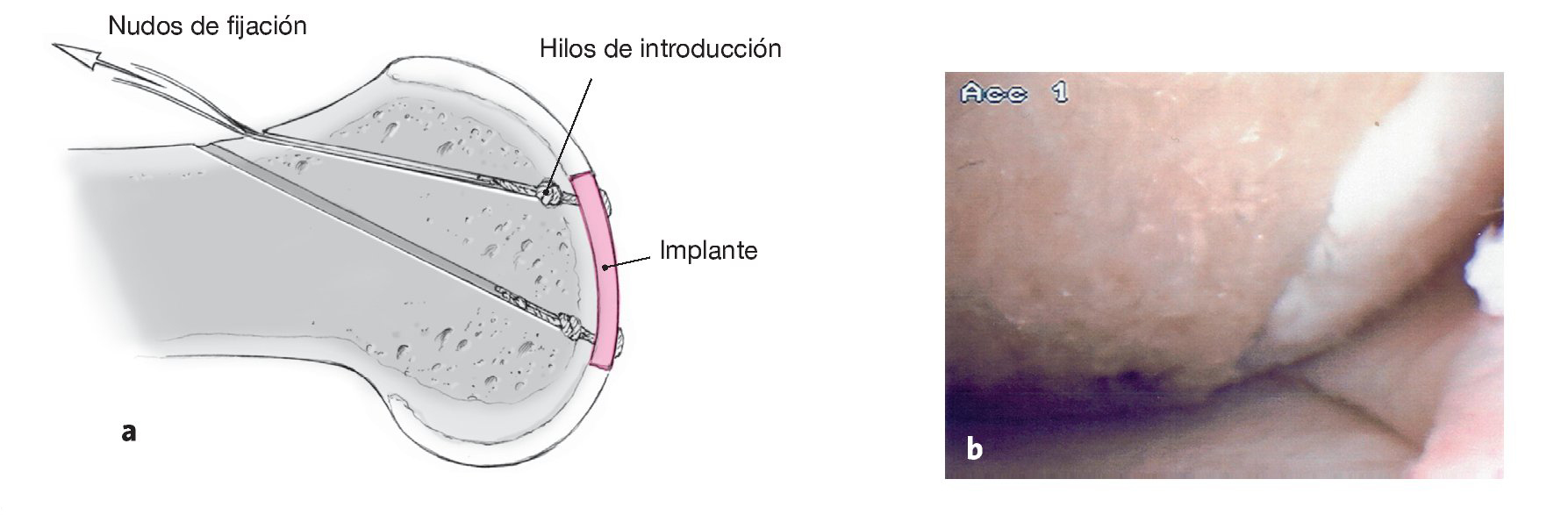
Figuras 11a y 11b. Introducción de los nudos de fijación en el hueso mediante los hilos de introducción y fijación a presión en el hueso (a). Observaciones: la fuerza de desgarro de estos nudos supera la resistencia del implante. La medición de las fuerzas de cizalla necesarias para desprender el implante arrojó valores de 2.500 p (± 350 p). En comparación, un implante fijado con adhesivo de fibrina se deslamina a 100 p5. No debe utilizarse la fresa para manipulaciones correctoras del implante, dado que el implante podría ser arrancado por la fresa. Control final de la posición del implante (b) y varios movimientos de la articulación. Retirada de los hilos de introducción tirando de un extremo. Vendaje elastocompresivo.
Particularidades
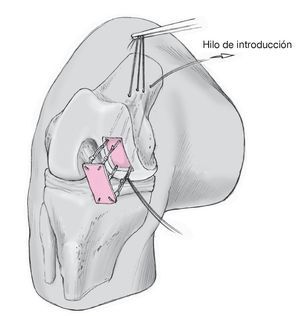
Los defectos de la tibia y retrorrotulianos se abordan de forma similar (fig. 12). Los orificios de los taladros se hacen con una guía especial, los hilos de introducción se sujetan por vía retrógrada y se hacen salir por el plano tibioventral o suprarrotuliano respectivamente (fig. 13). El implante se hace como se ha descrito y si es necesario se refuerza anudando los hilos de introducción por parejas sobre un puente óseo (fig. 14).
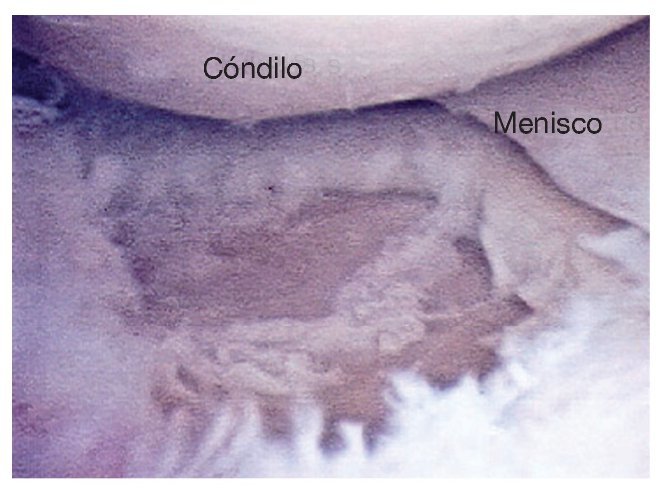
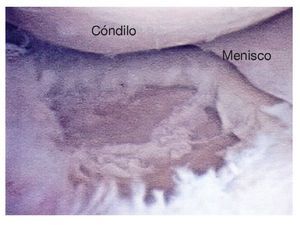
Figura 12. Defecto condral en la meseta tibial tras desbridamiento.
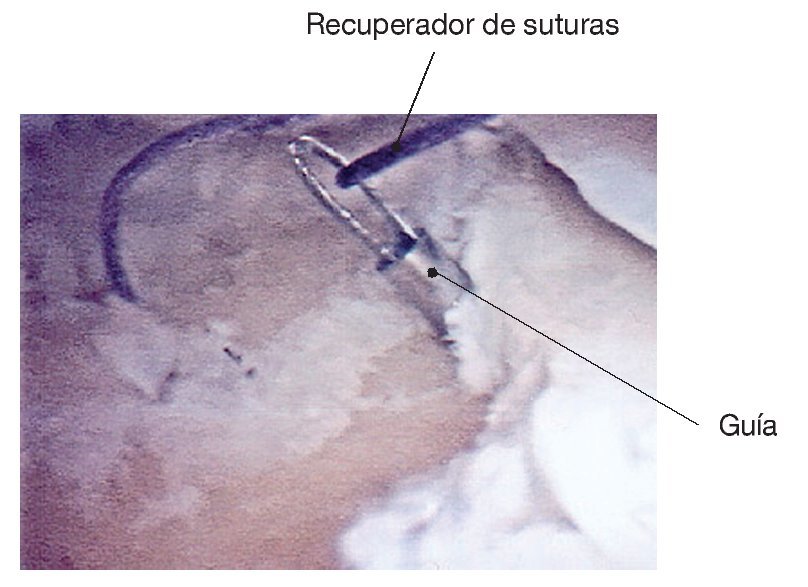
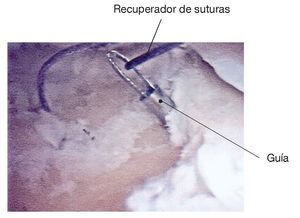
Figura 13. Introducción retrógrada de los hilos de introducción con un recuperador de suturas en el borde medial de un defecto condral de la tibia.
Figura 14. Imagen artroscópica de una matriz de polímero con condrocitos tras implantación artroscópica dentro de un gran defecto cartilaginoso de la cabeza de la tibia.
Tratamiento postoperatorio
Movimientos activos/pasivos, en su caso con limitación de la movilidad, dependiendo de la localización del defecto.
Esfuerzo progresivo en función del dolor y ayudándose con muletas.
Descarga de la articulación durante más tiempo, hasta 12 semanas, en caso de defectos con borde cartilaginoso ausente o inestable.
Analgésicos a demanda.
Tromboprofilaxis hasta carga total.
Errores, riesgos, complicaciones
El implante se gira al introducirlo en la articulación; no puede fijarse: con el manipulador atraumático es posible volver a sacar el implante de la articulación a través de la cánula de trabajo. Antes de volver a intentar una nueva fijación, debe controlarse la posición de los hilos.
El nudo de fijación no se sujeta en el hueso (por ejemplo, a causa de una técnica de anudado errónea); el implante es inestable: existen tres posibilidades alternativas a una laboriosa repetición del proceso que pondría en peligro la estabilidad de los otros nudos:
1. Fijación de la parte móvil del implante con una varilla absorbible para fijación de fragmentos osteocondrales (Smartnail®, Linvatec).
2. Fijación con adhesivo de fibrina.
3. Anudado subcutáneo del hilo de introducción.
El implante se desprende al mover la articulación; fijación inestable: fijación del implante mediante puntos de retención adicionales (véase arriba).
Resultados
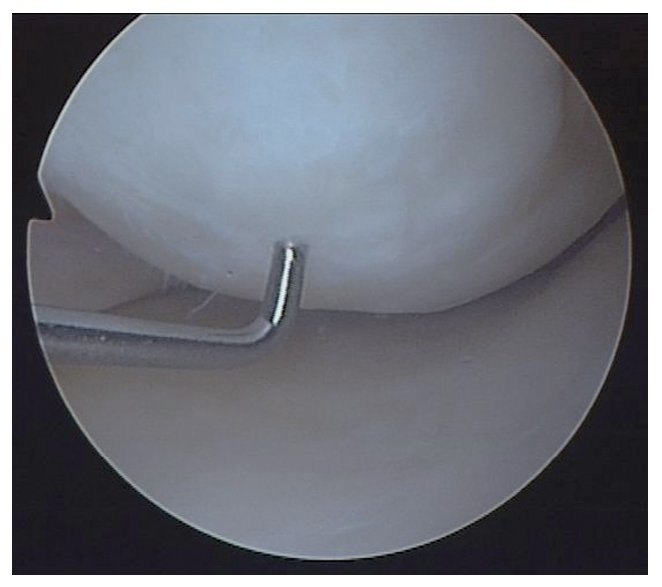
En un primer estudio se trataron 45 pacientes con una edad media de 39 años. Habían pasado por una media de 3,3 operaciones previas de cartílago. Los primeros 20 pacientes, tras dos años de seguimiento y un tamaño medio de los defectos de 4,52 cm2, mejoraron su estado clínico según la escala modificada de Cincinnati7, desde 3,5 hasta 6,2 puntos en una escala de 1 (muy malo) a 108 (excelente). En 17 pacientes se hizo un trasplante por artroscopia (fig. 15). En los resultados a dos años no se observó ninguna diferencia de eficacia del método entre las técnicas abierta y artroscópica. La inflamación, el nivel de dolor y la movilidad tras la intervención con artroscopia tendían a ser mejores aunque no de forma significativa. Los controles de resonancia magnética demostraron siempre una curación completa del defecto con un grosor y una señal normales del cartílago. Sólo en algunos casos se describió una cierta "aspereza" de la superficie cartilaginosa. En algunos casos se sometió a algunos pacientes a artroscopias de control. En ellos se observó una delimitación lisa y un relleno completo del defecto. Tras la técnica de artroscopia no se formaron adherencias.
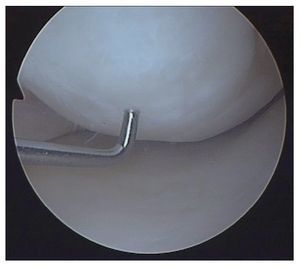
Figura 15. Imagen artroscópica del cóndilo femoral 24 meses después de un trasplante autólogo de condrocitos por vía artroscópica.
Correspondencia
PD Dr. Christoph Erggelet
Departamento de Ortopedia y Traumatología,
Hospital Universitario de Friburgo
Hugstetter Strasse 55
79106 Friburgo (Alemania)
Tel.: (+49/761) 270-2608; fax: -2675
Correo electrónico: christoph.erggelet@uniklinik-freiburg.de
Arthrose Clinic Zürich
Toblerstrasse 51
8044 Zúrich (Suiza)
Tel.: (+41/43) 268-2835; fax: -2830
Correo electrónico: erggelet@arthroseclinic.ch