Introducción
En el contexto de los mecanismos del dolor neuropático —definido por la Asociación Internacional para el Estudio del Dolor, como aquel iniciado o provocado por lesión o disfunción del sistema nervioso— se describe un gran número de procesos fisiopatológicos, tanto centrales como periféricos, que involucran la presencia de daño en estructuras nerviosas, que son la base fundamental para su interpretación1, y estos procesos, implicados en el dolor neuropático, aún no son conocidos del todo. Debido a la complejidad que lo integra y, en ocasiones, a la falta de respuesta a los tratamientos existentes, por la impredecible efectividad, la complicada dosificación, los efectos adversos y la respuesta analgésica tardía de los medicamentos establecidos2, su manejo debe plantearse bajo un enfoque multidisciplinario3. Aunque estos datos no pueden ser extrapolados a la población general, la prevalencia de los síndromes de dolor neuropático en población adulta en el Hospital General de México en el año 2002 ha sido reportada en un 47,5%4.
La oxicodona, derivado alcaloide de la tebaína, es un fármaco analgésico semisintético, agonista puro de los receptores opiáceos mu y kappa sin techo terapéutico, que actúa en el sistema nervioso central y músculo liso, cuya principal acción es la analgesia5,6. Por su adecuada liposolubilidad, menor metabolismo hepático de primer paso, mayor biodisponibilidad, menor incidencia de émesis y efectos adversos, así como su rápido mecanismo de acción por vía parenteral5, pueden explicar el efecto analgésico superior5-7, útil y efectivo en el tratamiento de dolor oncológico8 y no oncológico9, así como primera opción en el tratamiento de dolor intenso no controlado con morfina o con intolerancia a ésta, y en el manejo de dolor postoperatorio, con incidencia baja de efectos adversos, como náusea10, vómito3, sedación11 y mejoría en la calidad del sueño, debido parcialmente a su acción ansiolítica y efecto relajante5.
Tramadol es un analgésico sintético de acción central, que tiene mecanismo de acción opiáceo puro no selectivo y monoaminérgico, y es una elección terapéutica para los pacientes con dolor neuropático, dolor moderado a severo, dolor agudo y crónico, dolor oncológico y no oncológico, así como en analgesia perioperatoria12-14. En modelo de dolor neuropático, tramadol se ha utilizado en pacientes que carecen de una adecuada respuesta a los fármacos de primera línea, y en ocasiones como manejo inicial2, con efectos favorables sobre la intensidad de dolor, índice de Karnofsky y disminución de la dosis de antiepilépticos y analgésicos; también sobre la mejora en la calidad de vida, sueño y estado nutricional, efectivo y seguro a largo plazo en el manejo de éste en neuropatía diabética, neuropatía de diferentes etiologías, neuralgia posherpética y dolor de miembro fantasma12,13,15.
La lidocaína intravenosa (i.v.) es un agente analgésico antiinflamatorio, antipirético, antihiperalgésico, así como su bajo precio, facilidad de administración y relativa seguridad, muestra una atractiva intervención con gran número de aplicaciones. Estas propiedades han sido mediadas por una gran variedad de mecanismos, incluyendo el bloqueo de los canales de sodio, además de los receptores acoplados para proteína G y los receptores para N-metil-D-aspartato16. Su uso sistémico en el manejo inicial de los síndromes periféricos de dolor neuropático ya se ha descrito17,18, motivo por el cual su utilización está indicada por sus efectos antialodínicos y antihiperalgésicos18.
Reconociendo las propiedades farmacológicas de estos medicamentos como adyuvantes en el tratamiento de dolor neuropático, así como la búsqueda de alternativas adecuadas con menores efectos adversos, mayor tiempo y potencia analgésica, además de la falta de estudios realizados sobre oxicodona más lidocaína i.v. como punto principal, resulta importante evaluar de forma comparativa los efectos de oxicodona en perfusión continua con lidocaína frente a tramadol más lidocaína, en los pacientes con dolor neuropático crónico agudizado.
Material y métodos
Con la aprobación del comité local de investigación y de ética (DIC/08/203/03/070), y previo consentimiento informado aceptado y firmado por los pacientes, se realizó un ensayo clínico controlado de tipo experimental, prospectivo, comparativo, longitudinal y aleatorizado, en la Clínica del Dolor y Cuidados Paliativos del Hospital General de México. Se estudiaron un total de 27 pacientes, de cualquier sexo, de 22 a 84 años de edad, con diagnóstico de dolor espontáneo de tipo neuropático crónico agudizado, moderado a severo evaluado, de cualquier etiología, de al menos 1 mes de evolución, con escala visual analógica (EVA) ≥ 4 y escala de LANSS > 12 puntos.
Se excluyeron los pacientes con enfermedades cardiopulmonares, hepáticas, renales, neurológicas y/o psiquiátricas; alergia conocida a los medicamentos en estudio; embarazo o lactancia; bradicardia y anormalidades electrocardiográficas; trastornos abdominales agudos o crónicos; antecedentes de náusea y vómito intratable; ayuno incompleto; hipovolemia; síndrome complejo regional; uso crónico de opiáceos, bloqueadores de canales de sodio, antidepresivos tricíclicos, e historia de abuso de drogas o alcohol.
Los pacientes fueron asignados de manera aleatoria a través de tabla de números aleatorios de la siguiente manera: grupo de estudio oxicodona (10 mg) más lidocaína (3 mg/kg) en perfusión continua durante 2 h en unidosis, y grupo con tramadol (100 mg) más lidocaína (3 mg/kg) en perfusión continua también por 2 h como unidosis. En ninguno de los grupos de tratamiento se utilizó dosis adicionales así como analgésicos no esteroideos y ningún otro fármaco (antidepresivos, esteroides, estabilizadores de membrana, etc.).
El tamaño de la muestra se estableció a través del programa EPISTAT 2 para Windows XP por medio de la diferencia de proporciones de estudios previos.
El personal que participó en cada uno de los casos estaba enterado del objetivo y diseño del estudio, pero desconocía a qué grupo pertenecía cada uno de los pacientes, y otro investigador fue el que administró los medicamentos en estudio. El investigador a cargo de la valoración de los pacientes durante la perfusión de los fármacos en estudio, desconocía el tipo de medicamento administrado.
En la sala de tratamiento con perfusiones i.v. se realizó monitoreo no invasivo a través de monitor automático programable a los pacientes del estudio, que incluyo: electrocardiograma de 3 derivaciones II, V y AVF; presión arterial (PA) no invasiva, y oximetría de pulso, así como administración de oxígeno por puntas nasales a 3 l/min.
Se consideró el efecto analgésico del tramadol en la bibliografía como grupo control.
Se anotaron las variables de estudio: edad, peso, talla, índice de masa corporal (IMC), sexo, tipo y número de características del dolor espontáneo, categoría diagnóstica previa perfusión de los medicamentos en estudio, así como las variables de frecuencia cardíaca y PA sistólica (PAS) y diastólica (PAD) durante la administración de los fármacos.
En el área de consulta, previo ingreso a la sala de perfusiones, los pacientes fueron instruidos acerca del uso de la EVA (puntuación de 0, ausencia de dolor, a 10, el peor dolor imaginado) en dolor espontáneo, alodinia táctil, alodinia térmica (frío), prueba de hiperalgesia con estesiómetro de Wartenberg para la evaluación del dolor durante el estudio, escala categórica para náusea y vómito así como satisfacción a tratamiento a los 60 min posteriores al término o a la suspensión de los mismos.
El registro de las variables relacionadas a la EVA para dolor espontáneo, alodinia táctil, prueba de hiperalgesia a carretilla de Wartenberg se realizó por el investigador a cargo de la evaluación de los pacientes en el siguiente orden: momento (M) 1 o basal, 25 a 35 min previa administración de perfusión; M2, 15 min posteriores a la administración inicial de los fármacos en estudio; M3, a los 30 min; M4, a los 45 min; M5, a los 60 min; M6, a los 90 min; M7, a los 120 min, y M8, a los 60 min al término de la perfusión.
La alodinia térmica (frío) por medio de acetona se evaluó a los 25 a 35 min (M1) previos a la administración de medicamentos, a los 60 min (M5) y a los 120 min (M7) posteriores a la administración de la perfusión.
Se evaluó el estado de conciencia de los pacientes a través de la escala de Ramsay (1, sedación superficial, a 6, sedación profunda) durante la administración de los fármacos en los 8 momentos descritos, así como la presencia de náusea y vómito (1, ausente o sin presencia de síntomas o accesos, a 5, muy intensa o necesidad incontrolable de expulsión de contenido gástrico) y satisfacción al tratamiento (1, sin cambios en la intensidad del dolor, a 4, reducción superior del 50% de dolor espontáneo respecto a la basal con el medicamento activo) a los 60 min del término de la perfusión.
Para el análisis estadístico se utilizó el programa SPSS versión 11 para Windows XP. Los resultados se muestran para las variables cualitativas como frecuencia y porcentajes así como χ2, y para las variables cuantitativas como mediana y amplitud de variación de U de Mann-Whitney. Análisis inferencial con Friedman, con nivel de significanción de 0,05.
Resultados
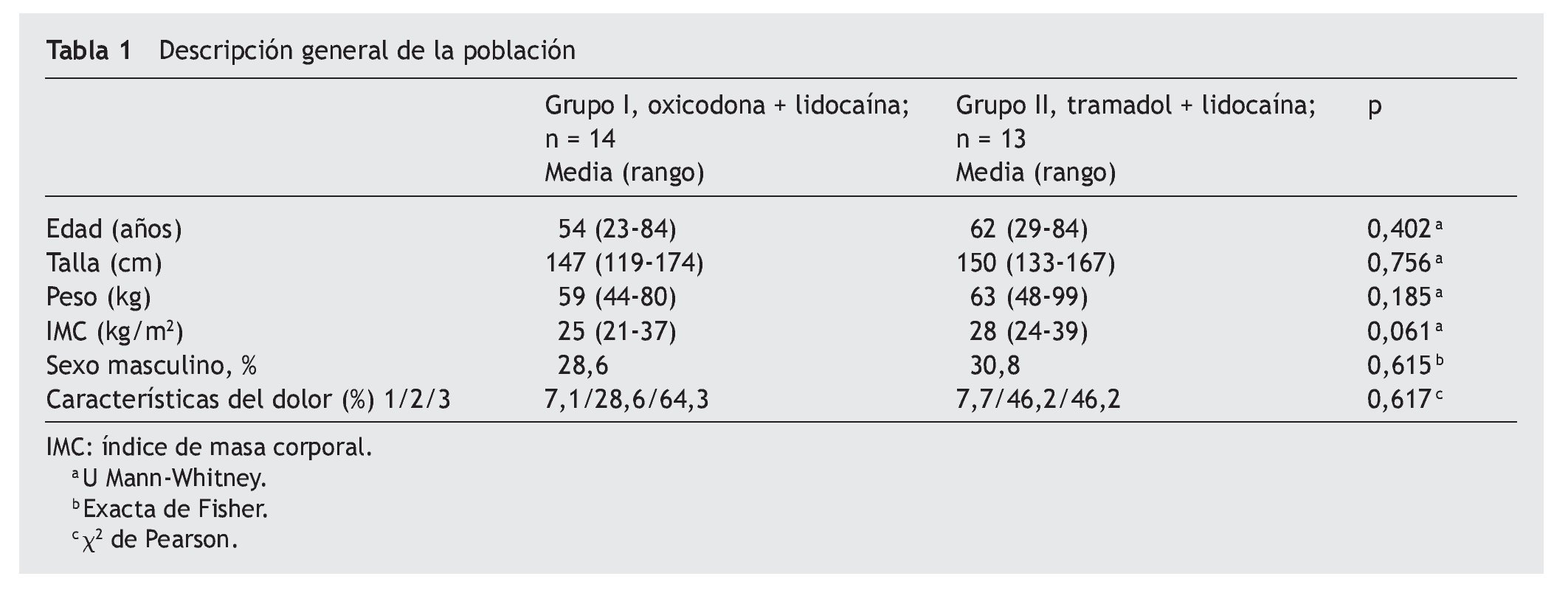
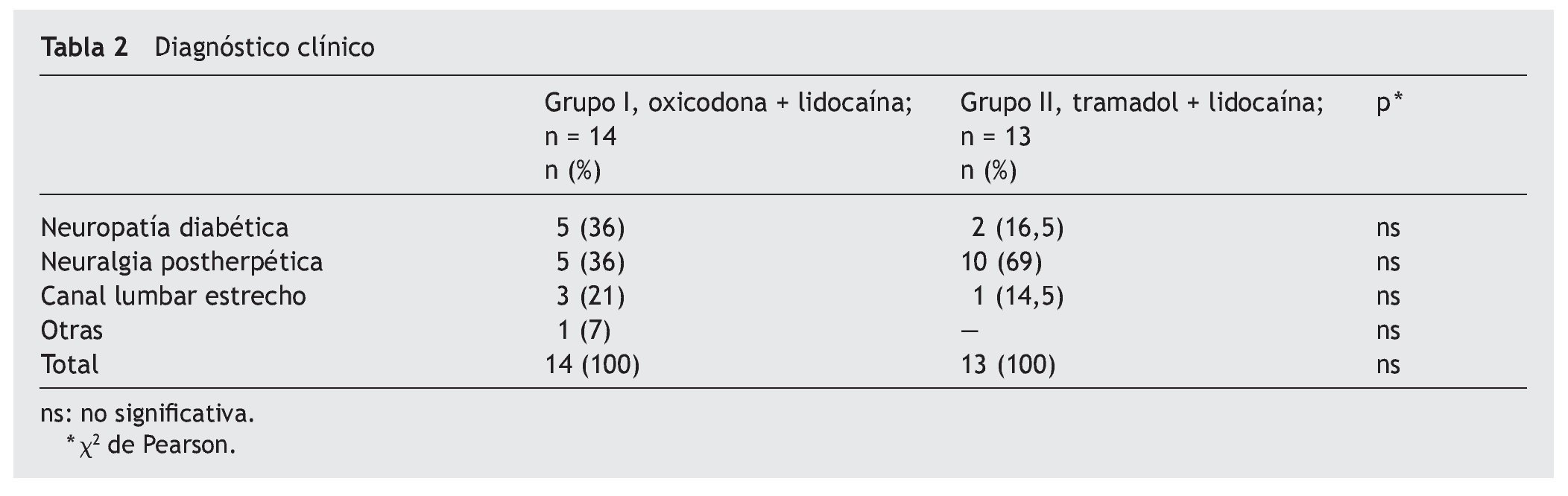
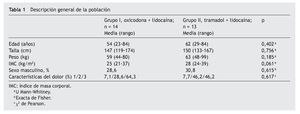
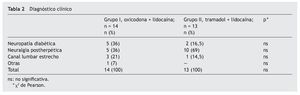
Se estudió un total de 27 pacientes, ninguno se eliminó del estudio, quedando en el grupo I 14 pacientes, de los cuales el 28,6% eran varones, y en el grupo 2 fueron el 30,8%. No se encontró diferencia en ambos grupos en cuanto a edad, peso, talla, así como en las características de dolor y categoría diagnóstica (tablas 1 y 2).
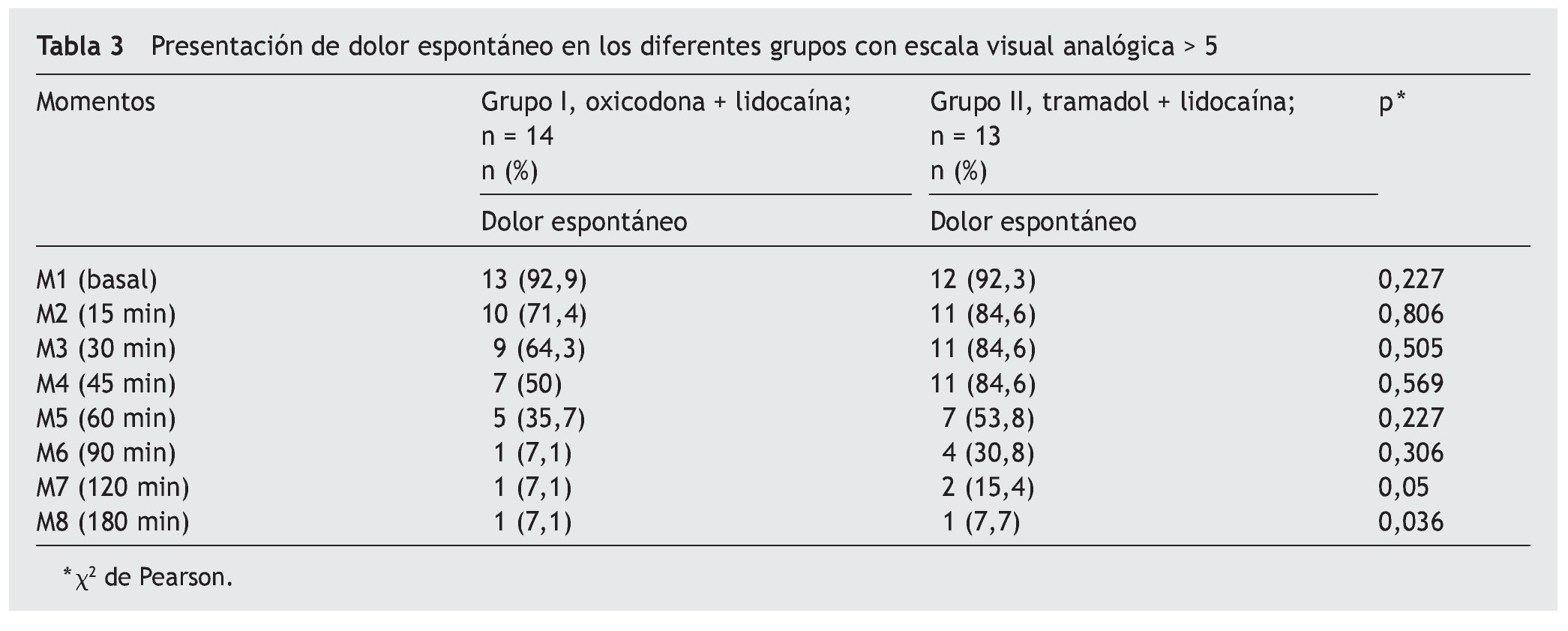
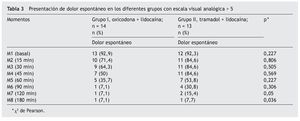
En cuanto a la presentación de dolor espontáneo evaluado a través de la EVA, no hubo diferencia significativa desde M1 hasta M6 en ambos grupos, pero en M7 (120 min) y M8 (180 min) se observó una diferencia de p < 0,05 (tabla 3).
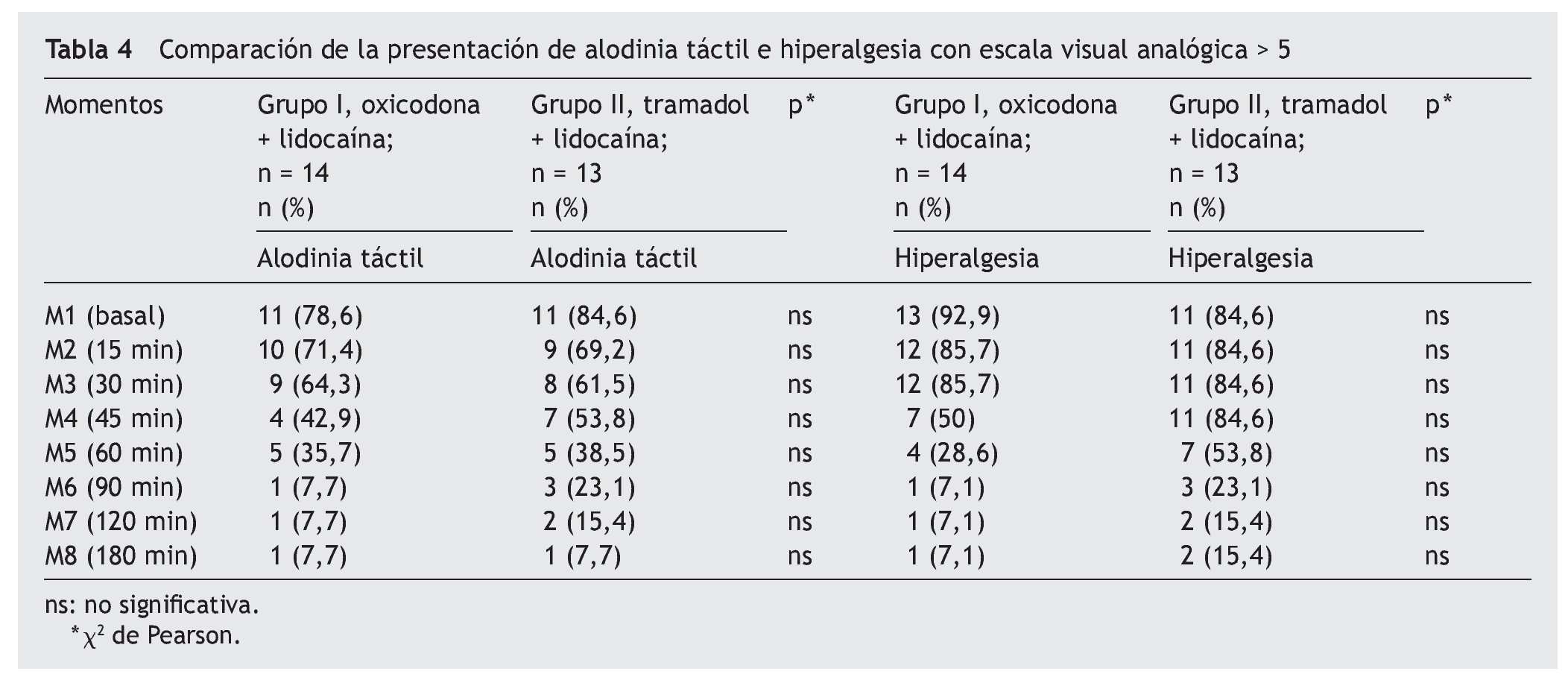
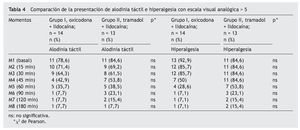
En cuanto a la evaluación de alodinia táctil por medio de pincel en los diferentes momentos, no hubo diferencia estadísticamente significativa, así como en el estado de hiperalgesia con estesiómetro de Wartemberg (tabla 4).
Se evaluó la presencia de alodinia al frio por medio de acetona, y no se encontró diferencia significativa en ambos grupos en los diferentes momentos.
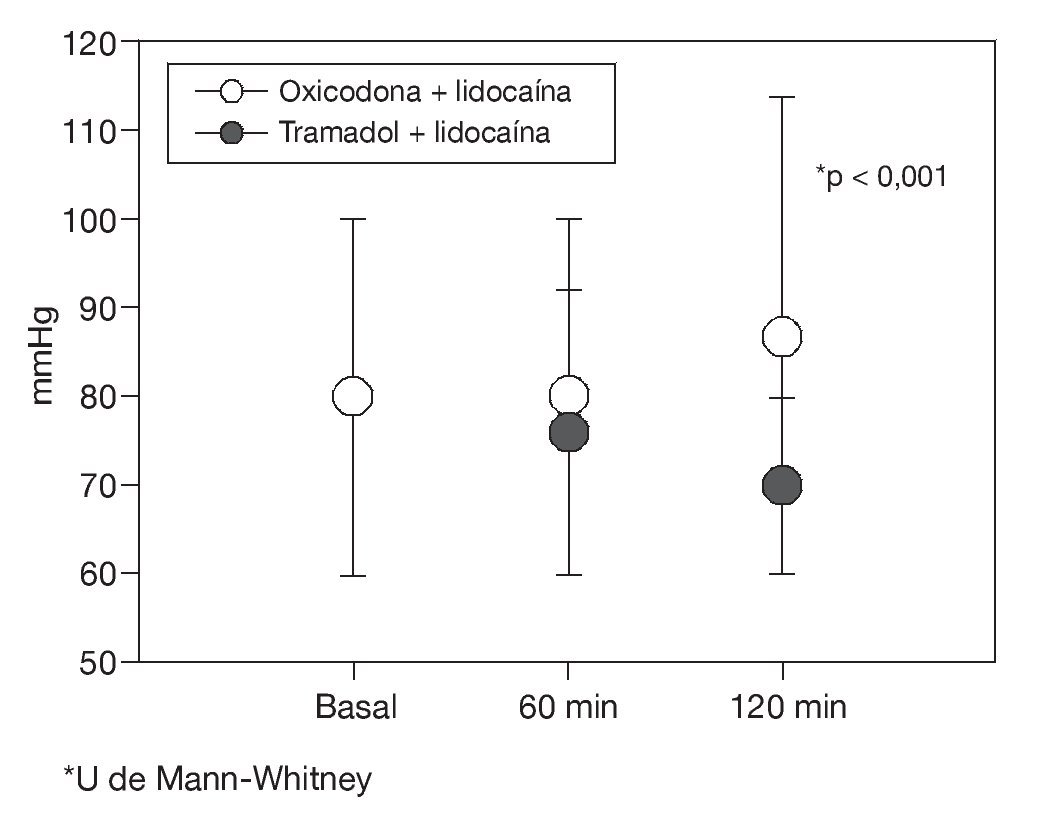
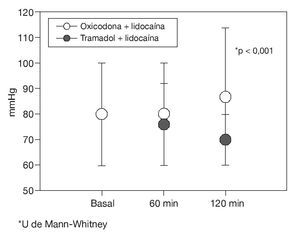
Al evaluar los signos vitales en ambos grupos en los diferentes momentos, no se encontró diferencia significativa en cuanto a la frecuencia cardíaca y PAS (p > 0,05), no así en la comparación de la PAD, donde se mantuvo dentro de rangos normales en el grupo de oxicodona más lidocaína en comparación con el grupo de tramadol más lidocaína a los 120 min (fig. 1).
Figura 1 Comparación de la presión arterial diastólica en ambos grupos de tratamiento.
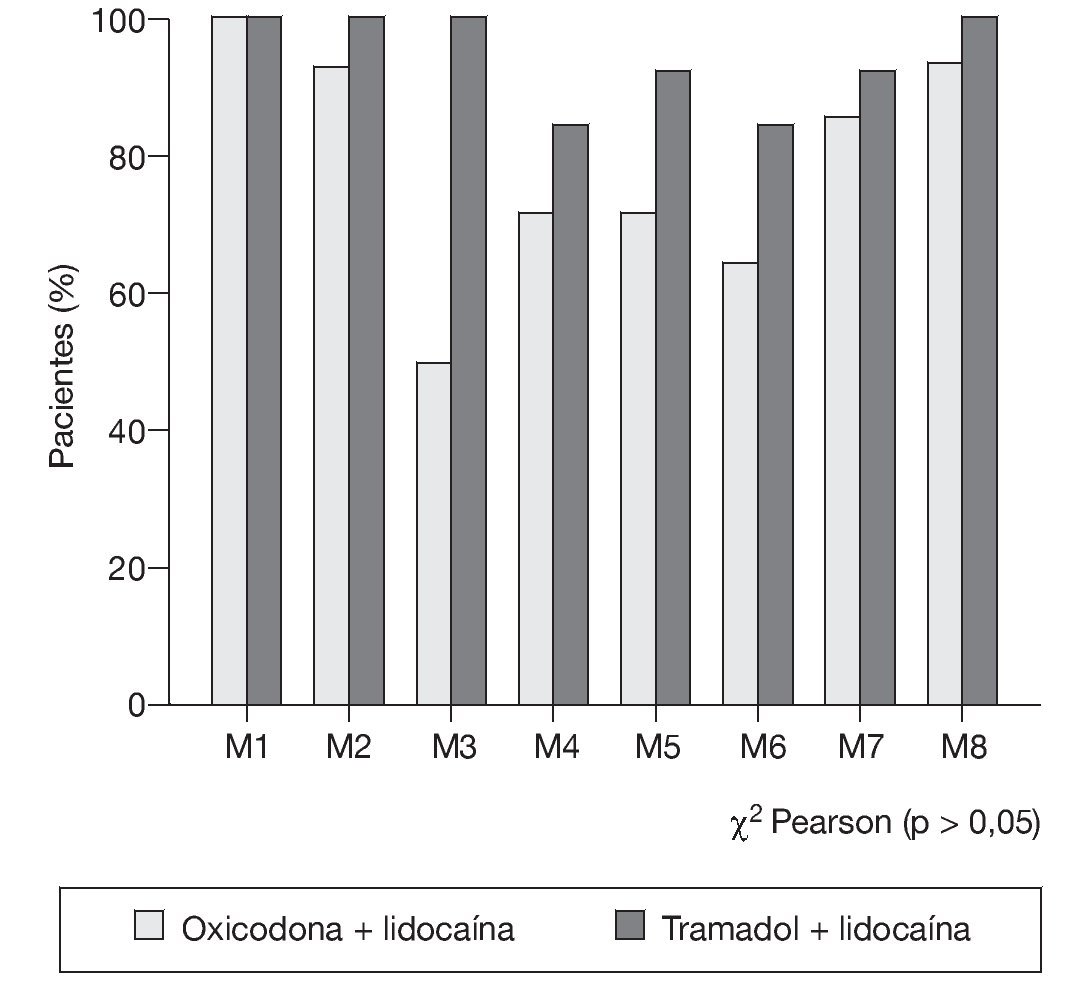
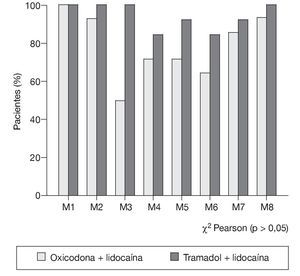
En la evaluación de sedación a través de la escala de Ramsay, en los pacientes que presentaron puntuación < 2 no se encontró diferencia estadísticamente significativa (fig. 2).
Figura 2 Pacientes que presentaron puntuación ≤ 2 en la escala de sedación de Ramsay.
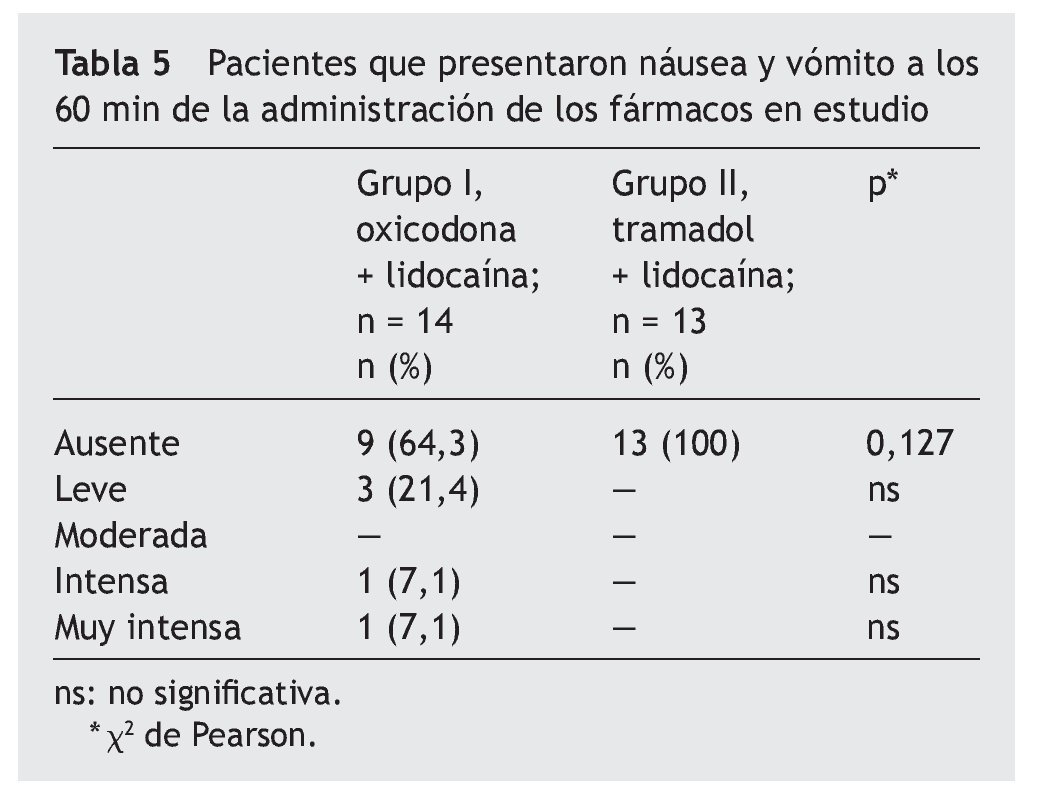
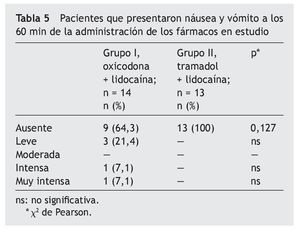
En cuanto a la presentación de náusea y vómito, evaluada a los 60 min posteriores a la administración de los medicamentos en estudio, en el grupo oxicodona más lidocaína la manifestaron 5 pacientes (36%) (tabla 5).
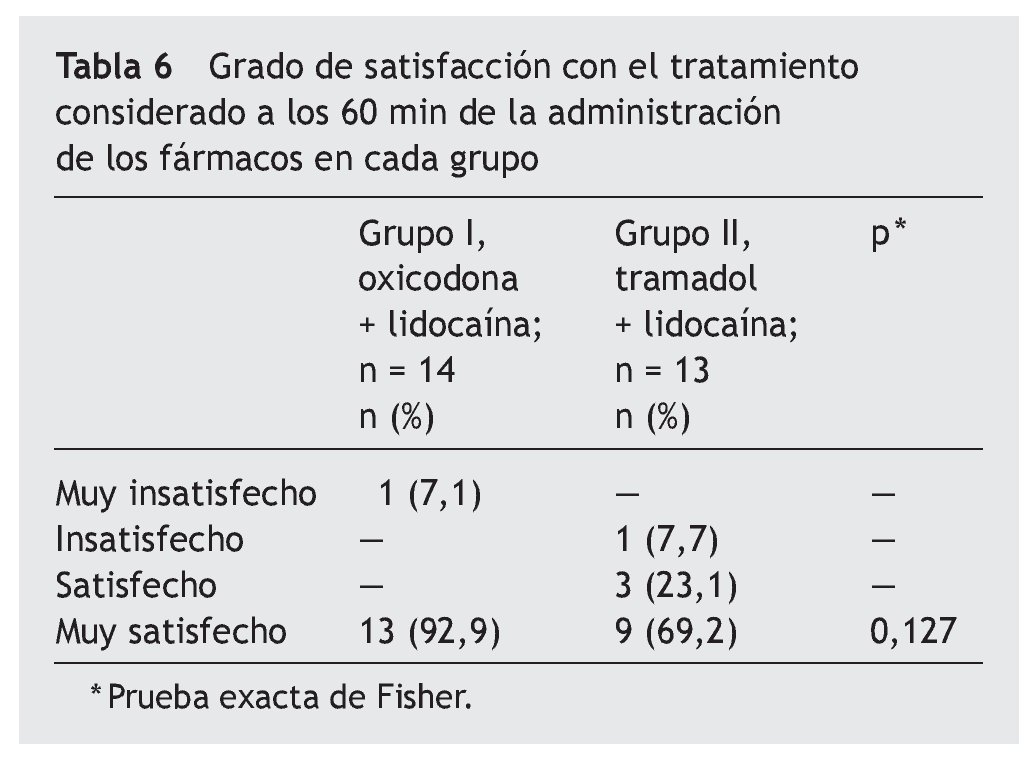
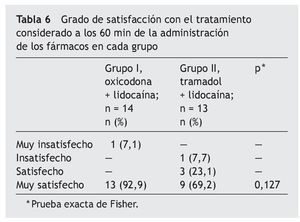
También se evaluó el grado de satisfacción con el tratamiento, donde el 92,9% de pacientes del grupo oxicodona más lidocaína quedó muy satisfecho, en comparación con el grupo tramadol más lidocaína, donde el 69% de los pacientes quedó dentro de este rango (tabla 6).
Discusión
La oxicodona es un derivado de alcaloide de la tebaína, agonista puro de los receptores opiáceos mu y kappa, con acción ansiolítica y efecto principalmente analgésico, incidencia baja de efectos secundarios, útil y efectivo en síndromes de dolor neuropático.
En estudios en modelos de dolor neuropático tratados con oxicodona, se ha observado mayor participación del sexo femenino8,19. En los datos preliminares de nuestro estudio se observa, de acuerdo con los resultados obtenidos, que el sexo femenino predomina en ambos grupos.
En las variables como edad, peso, talla e IMC, al no haber diferencias en ambos grupos, y por lo tanto ser homogéneos, nos indica que los criterios de inclusión y aleatorizacion se llevaron a cabo cuidadosamente.
En la evaluación del dolor, el uso crónico de oxicodona ha mostrado mejoría en el alivio de sus diferentes características, principalmente en la disminución de las puntuaciones de dolor continuo y espontáneo, así como la alodinia y la incapacidad20 y mejoría en la calidad de vida3. El uso i.v. de oxicodona provee un período de analgesia de aproximadamente de 1,3 a 2,6 h, con inicio de acción a los 25 min20 y mejora de sintomatología del 91% a los 60 min de su administración5. Del mismo modo, el uso de lidocaína administrada de forma sistémica, puede reducir diferentes tipos de dolor en diferentes síndromes de componente neuropático21 al disminuir los impulsos ectópicos espontáneos en neuronas del asta posterior17 e hiperexcitabilidad neuronal22, con efectos antialodínicos y antihiperalgésicos16 a dosis de 1 a 5 mg/kg17,22.
En nuestro estudio, el 90% de los pacientes en ambos grupos presentaba dolor espontáneo en M1 (criterios de inclusión), hasta los 120 min donde se marca una diferencia estadísticamente significativa a favor del grupo de oxicodona más lidocaína, en que se observó, en un 92,9%, una disminución de la EVA en comparación con el grupo 2 (84,6%), siendo estadísticamente significativa (p < 0,05). Esto indica que en el grupo tratado con oxicodona más lidocaína en el dolor neuropático crónico agudizado, se obtiene mejor respuesta en comparación con el grupo tramadol más lidocaína. Esto se puede comprobar cuando se evaluó el grado de satisfacción al tratamiento, donde más del 90% de los pacientes del grupo de oxicodona refirió estar muy satisfecho. No se encontró diferencia en el momento de evaluar alodinia táctil, alodinia térmica e hiperalgesia, probablemente debido a la falta de una muestra mayor; sin embargo, clínicamente, se puede observar que en ambos grupos esta respuesta va siendo menor en los diferentes momentos evaluados.
Los efectos adversos cardiovasculares y centrales relacionados con el uso de tramadol son mínimos23. Es importante no sólo la evaluación de dolor con la EVA sino el reflejo en los signos vitales. En este estudio se tomó en cuenta la frecuencia cardíaca así como la PAS y la PAD, donde el impacto sólo se observó en M7 y M8 de la PAD, manteniéndose en rangos normales en el grupo oxicodona más lidocaína, no así en el grupo tramadol más lidocaína. Sería aventurado predecir, con estos resultados, que tramadol es menos cardioestable; sin embargo, al correlacionar con la escala de sedación de Ramsay, observamos que en el grupo de tramadol más lidocaína los pacientes se mantuvieron con puntuaciones de Ramsay de 2 (despiertos debido a la presencia de dolor), por los efectos centrales mínimos que se presentan con su uso24 o, posiblemente, por la acción ansiolítica de la oxicodona5,6, situación que no podemos afirmar hasta completar el tamaño de muestra.
Se ha reportado náusea y vómito como los efectos secundarios más frecuentes con el uso de oxicodona3,5,6. Es evidente que el grupo de oxicodona más lidocaína presentó mayor incidencia de náusea y vómito, sin embargo ningún paciente requirió más de 1 dosis de antiemético al final del estudio y no lo refirieron como incomodo.
Éste es un estudio preliminar del uso de oxicodona más lidocaína en comparación con tramadol más lidocaína. Aunque no hubieron diferencias estadísticamente significativas, el uso de oxicodona y lidocaína demostró utilidad en el tratamiento de dolor neuropático crónico agudizado. Es necesario continuar con este estudio y completar el tamaño de muestra, y evaluar de manera objetiva la calidad de la analgesia en pacientes con dolor neuropático crónico agudizado.
Conclusiones
— El uso de oxicodona más lidocaína frente a tramadol más lidocaína es efectivo para disminuir el dolor neuropático crónico agudizado.
— No hubo diferencias en la presentación de alodinia táctil, alodinia térmica ni hiperalgesia en los diferentes grupos.
— No hay diferencias en cuanto al estado de sedación en ambos grupos.
— Se observó mayor grado de satisfacción al tratamiento con el uso de oxicodona más lidocaína que con tramadol más lidocaína.
— Se observó mayor presentación de náusea y vómito en el grupo de oxicodona más lidocaína.
— Se requiere mayor número de muestra.
Agradecimientos
Agradecemos a la Dra. América del Rocío Gonzalo Ugarte de Medicina Física y Rehabilitación del Hospital General de México OD, por la traducción del texto.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
* Autor para correspondencia.
Correo electrónico: drakassianrak@hotmail.com (A.A. Kassian Rank).
Recibido el 28 de enero de 2009;
aceptado el 19 de abril de 2009