La clozapina es un fármaco de probada efectividad, sin embargo, su uso se asoció a la aparición de agranulocitosis y así, fue restringido para esquizofrenia resistente y con un estricto control hematológico. El objetivo de nuestro trabajo es evaluar el riesgo de discrasias sanguíneas en una población de pacientes en tratamiento con clozapina seguidos durante 5 años.
Material y métodosSe trata de una cohorte de pacientes en tratamiento con clozapina en los que se evaluó el riesgo de aparición de alteraciones en la serie blanca, a través de analíticas semanales durante las primeras 18 semanas y mensuales a partir de entonces.
ResultadosSe trata de una muestra de 271 pacientes, con una media de edad de 32,3 años y un 63,5% de hombres. La dosis media administrada fue de 227,6mg/día (25 a 600mg). Durante las primeras 18 semanas de seguimiento, se observó una incidencia de neutropenia de 3,0% y de leucopenia de 1,3%. Durante los dos años siguientes, se encontró un nuevo caso de leucopenia y uno de neutropenia (n=120). No se observaron nuevos casos en los pacientes que completaron 5 años de seguimiento (n=69). A lo largo de todo el seguimiento, no hubo ningún caso de agranulocitosis.
ConclusiónSe observó una incidencia de neutropenia del 3%, concentrado en los primeros meses de seguimiento. Ningún paciente presentó agranulocitosis. La evidencia actual disponible sobre efectividad y seguridad de la clozapina y los resultados del presente estudio, hacen adecuado plantearse revisar los protocolos de seguimiento y utilización de este fármaco.
Clozapine is an efective antipsychotic. However, its use has been associated with agranulocitosis. For this reason, it has been restricted for the treatment of resistant schizophrenia under a strict hematologic control. The objective of this work was to assess the risk of hematologic dyscrasias in a sample of clozapine-treated patients in a 5-year period.
Materials and methodThis is a follow-up study in a cohort of clozapine-treated patients in which the risk of haematological dyscrasias was assessed. Complete blood cell count was made for each patient in a weekly basis for the first 18 weeks and thereafter monthly.
Results271 patients in treatment with clozapine were followed up. The mean age was 32.3 years, with 36.5% women. The mean dose was 227,6mg, ranging from 25 to 600mg/day. During the first 18 weeks of follow-up, we observed a 3% incidence of neutropenia and 1.3% of leucopenia. During the next two years, only one new case of neutropenia and leucopenia was observed (n=120). No new cases were observed during the rest of follow up (n=69). No cases of agranulocytosis were observed.
ConclusionsA 3% incidence of neutropenia concentrated in the first months of follow up and no cases of agranulocitosis were observed in our sample. Actual evidence on clozapine effectiveness and safety and the results of this study suggests that a critical revision of follow-up protocols is suitable.
La clozapina, un antipsicótico de segunda generación, es el tratamiento de elección para pacientes con esquizofrenia refractaria, ya que ha probado su efectividad sobre los otros antipsicóticos existentes, tanto típicos como atípicos1–7. Descubierta en el año 1958, fue el primer antipsicótico atípico, eficaz para el tratamiento de los síntomas positivos y negativos de la esquizofrenia8,9, lo que sumado a su perfil favorable en cuanto a efectos adversos extrapiramidales, generó grandes expectativas en el mundo científico y clínico de la época. Sin embargo, su desarrollo y comercialización fueron interrumpidos en 1975, debido a informes sobre pacientes en tratamiento con el fármaco que desarrollaron agranulocitosis en Finlandia8,10,11.
No obstante, en los años posteriores, se realizaron estudios que incluyeron la monitorización hematológica, los cuales mostraron resultados clínicos favorables7,12. Su uso fue aprobado por la Food and Drug Administration (FDA) en 1990 para pacientes con esquizofrenia resistente como única indicación, y sujeta a monitorización hematológica estricta. Desde entonces, la clozapina fue progresivamente reintroducida en distintos países. En España fue reintroducida en 1993, también bajo estrictas condiciones exigidas por el Ministerio de Sanidad, que aseguraban su uso controlado, restringiendo las indicaciones y obligando a un estricto control de recuento diferencial leucocitario antes de iniciar el tratamiento, con una periodicidad semanal durante las primeras 18 semanas y posteriormente mensual (figs. 1 y 2).
La incidencia de agranulocitosis y neutropenia muestra marcadas variaciones, dependiendo del tamaño de la muestra y del lugar donde ha sido realizado el estudio13. En las cohortes de seguimiento con mayor tamaño muestral se ha observado una incidencia de agranulocitosis y neutropenia cercana al 1 y 3% respectivamente14–16. El 95% de los casos de agranulocitosis han aparecido durante los primeros seis meses de tratamiento, siendo el riesgo aún mayor en los tres primeros16. El mecanismo exacto por el que la clozapina induce agranulocitosis no está del todo claro. Hay evidencia de que se trataría de una reacción mediada inmunológicamente17 y que intervendrían factores como son el origen étnico de las poblaciones estudiadas y la edad14–16,18–21. Teniendo en cuenta la importancia de este fármaco para el tratamiento de pacientes resistentes y la falta de datos sobre el riesgo de agranulocitosis en nuestra población, presentamos el seguimiento prospectivo durante cinco años de una cohorte de pacientes en tratamiento en la Clínica de Clozapina para valorar el riesgo de desarrollo de discrasias sanguíneas (tablas 1 y 2).
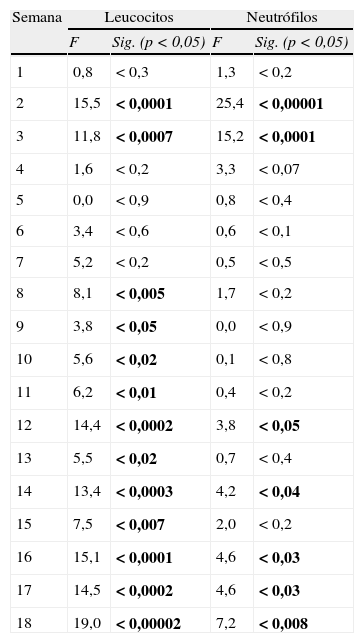
Análisis de la varianza para medidas repetidas. Se realizaron contrastes a priori intrasujetos comparándose cada medida con la inicial. Valores F y p (en negrita p<0,05), según Traza de Pillai, para recuento de leucocitos y neutrófilos durante los primeras 18 semanas de seguimiento
| Semana | Leucocitos | Neutrófilos | ||
| F | Sig. (p<0,05) | F | Sig. (p<0,05) | |
| 1 | 0,8 | <0,3 | 1,3 | <0,2 |
| 2 | 15,5 | <0,0001 | 25,4 | <0,00001 |
| 3 | 11,8 | <0,0007 | 15,2 | <0,0001 |
| 4 | 1,6 | <0,2 | 3,3 | <0,07 |
| 5 | 0,0 | <0,9 | 0,8 | <0,4 |
| 6 | 3,4 | <0,6 | 0,6 | <0,1 |
| 7 | 5,2 | <0,2 | 0,5 | <0,5 |
| 8 | 8,1 | <0,005 | 1,7 | <0,2 |
| 9 | 3,8 | <0,05 | 0,0 | <0,9 |
| 10 | 5,6 | <0,02 | 0,1 | <0,8 |
| 11 | 6,2 | <0,01 | 0,4 | <0,2 |
| 12 | 14,4 | <0,0002 | 3,8 | <0,05 |
| 13 | 5,5 | <0,02 | 0,7 | <0,4 |
| 14 | 13,4 | <0,0003 | 4,2 | <0,04 |
| 15 | 7,5 | <0,007 | 2,0 | <0,2 |
| 16 | 15,1 | <0,0001 | 4,6 | <0,03 |
| 17 | 14,5 | <0,0002 | 4,6 | <0,03 |
| 18 | 19,0 | <0,00002 | 7,2 | <0,008 |
Se trata de un estudio en una cohorte de pacientes tratados en la Clínica de Clozapina del Hospital de Día del Instituto de Neurociencias del Hospital Clínico de Barcelona. Los pacientes cumplían criterios definidos por el CIE-10 para el diagnóstico de esquizofrenia, trastorno esquizoafectivo o trastorno bipolar con síntomas psicóticos. Comenzaron tratamiento con clozapina debido a resistencia al tratamiento antipsicótico previo, definido como la persistencia de síntomas psicóticos a pesar del tratamiento consecutivo con dos antipsicóticos a dosis terapéuticas y durante un mínimo de seis semanas cada uno, o bien por intoleracia al tratamiento con otros antipsicóticos debido a reacciones adversas neurológicas graves o intratables (síntomas extrapiramidales o discinesia tardía).
A estos pacientes se les realizaron, según la normativa vigente, un recuento leucocitario y absoluto de neutrófilos semanalmente durante las primeras 18 semanas de tratamiento y posteriormente en forma mensual.
Se determinaron las concentraciones plasmáticas de clozapina y norclozapina mediante cromatografía líquida de alta resolución, a un subgrupo de 112 pacientes. Se incluyeron en este subgrupo todos aquellos pacientes que ingresaron al estudio desde que la técnica estuvo disponible en nuestro laboratorio.
En relación con las evaluaciones hematológicas, se consideraron como criterios de inclusión aquellos casos que tenían un seguimiento mínimo de 4 meses en nuestro centro y no inferior a 24 meses para pacientes que fuesen derivados desde otro centro, o bien, iniciaron el tratamiento con clozapina antes de la entrada en vigor de la normativa ministerial que regula el seguimiento de estos pacientes22.
Para el propósito de este estudio se han utilizado las definiciones de leucopenia, neutropenia y agranulocitosis admitidas internacionalmente. De este modo, leucopenia se define por un recuento de leucocitos <3×10^9/L y la neutropenia como un recuento de neutrófilos entre 0,5 y 1,5×10^9/L. La agranulocitosis ha sido definida como un recuento de granulocitos <0,5×10^9/L. Igualmente se ha hecho para las definiciones de neutrofilia y leucocitosis, definidos como un recuento de neutrófilos >7,5×10^9/L y como un recuento de leucocitos >11,5×10^9/L respectivamente. El criterio temporal en nuestro estudio ha sido definido como tres recuentos anómalos consecutivos durante el seguimiento semanal y dos durante el mensual.
Para el análisis de las diferencias en los valores de neutrófilos y leucocitos en las determinaciones realizadas desde la medida inicial a las medidas siguientes, se utilizó el análisis de la varianza para medidas repetidas. Para determinar los puntos donde se localizaron las diferencias significativas se calcularon los contrastes a priori intrasujetos, comparándose cada determinación con la inicial.
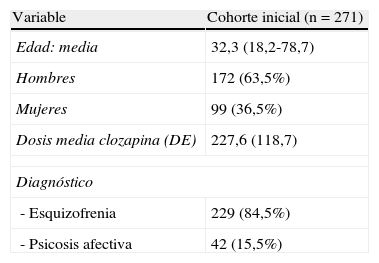
ResultadosSe trata de una muestra de 271 pacientes, de los cuales el 63,5% son hombres. La media de edad es de 32,3 años (DE 10,5), con un intervalo que va desde 18,2 hasta 78,7 años. Las dosis de clozapina administradas durante el seguimiento fueron desde 25 hasta 600mg al día. La dosis media administrada fue de 227,6mg al día (DE 118,7), la mediana fue de 200mg al día.
Se realizó una monitorización de las concentraciones plasmáticas de clozapina y norclozapina a un subgrupo de 112 pacientes de la cohorte compuesto de 38 mujeres con dosis media 207,6mg al día y 74 hombres con dosis media de 256mg al día. Las concentraciones plasmáticas de clozapina y norclozapina fueron de 239,1ng/ml y 138,2ng/ml respectivamente, para las mujeres y de 274,7ng/ml y 166,3ng/ml respectivamente, para los hombres.
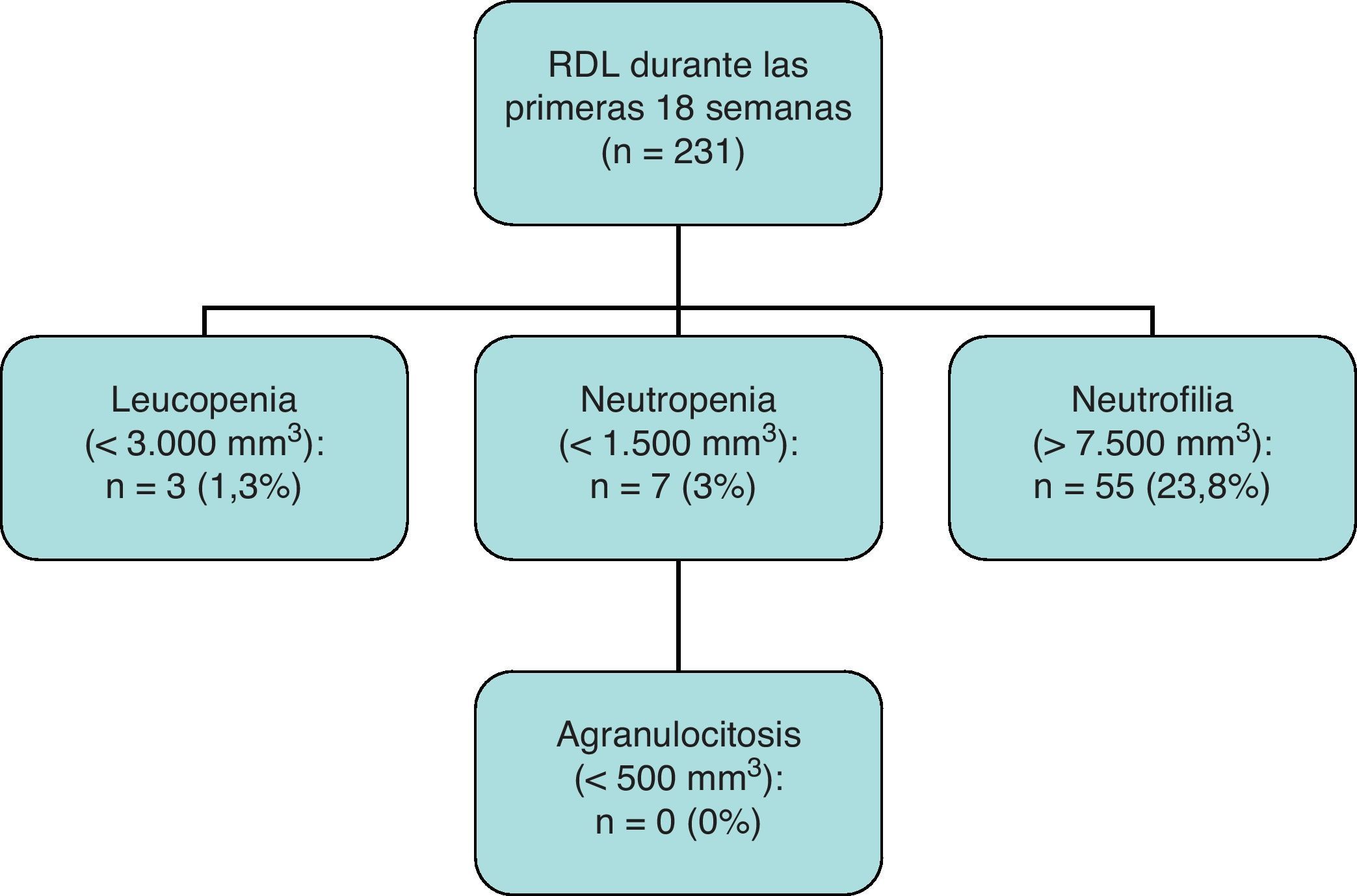
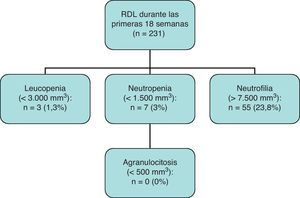
Del total de 231 casos que completaron las primeras 18 semanas de seguimiento, se observaron 3 casos de leucopenia (1,3%), 7 casos de neutropenia (3,0%) y ninguno de agranulocitosis.
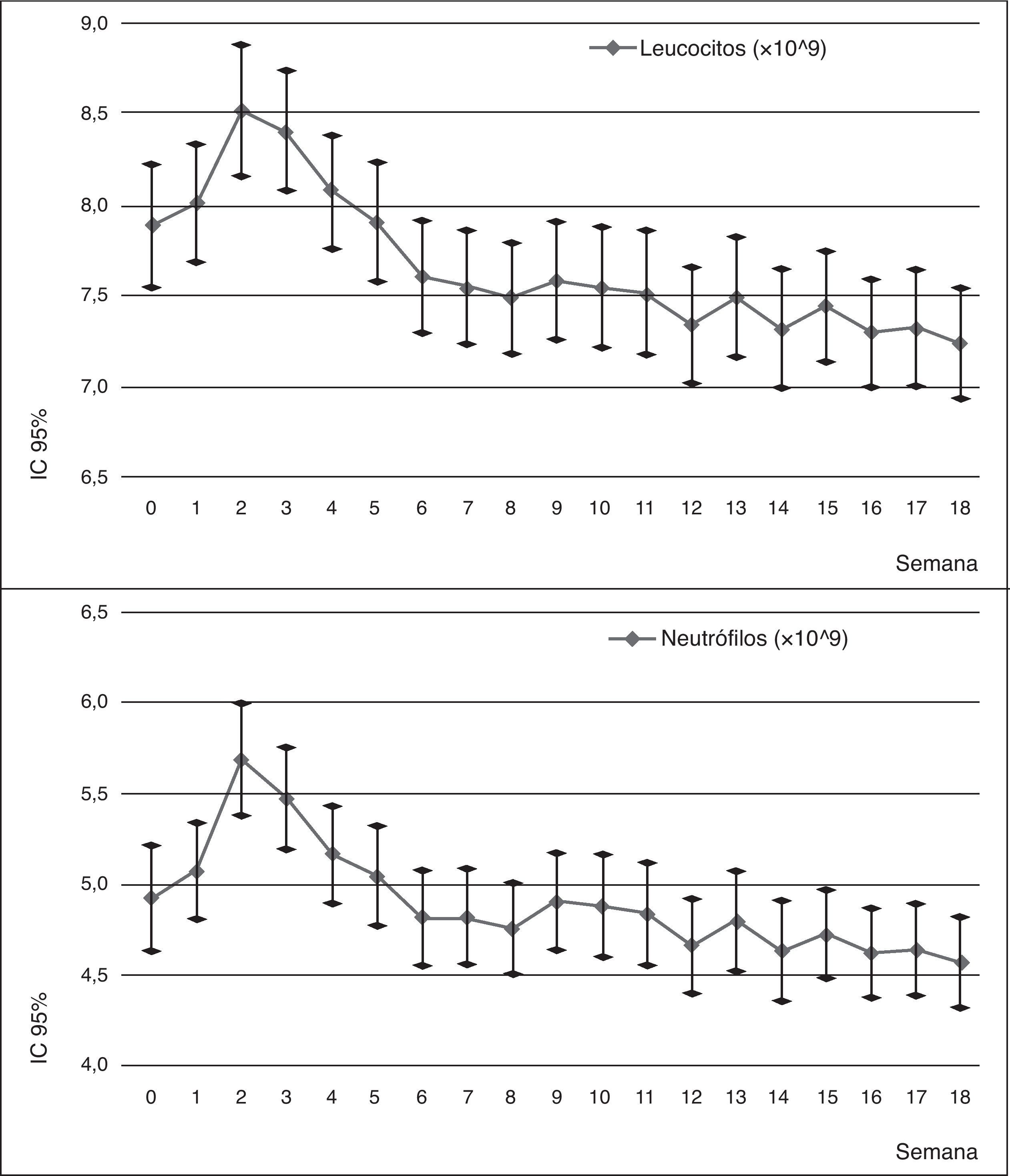
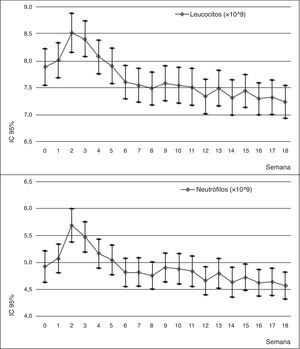
Llama la atención el incremento brusco de la cifra de neutrófilos y leucocitos durante las primeras semanas. Este incremento alcanza su punto máximo entre la segunda y tercera semana, siendo una diferencia significativa entre estas determinaciones y la determinación de base. A partir de este punto, comienza una disminución progresiva del recuento hasta hacerse significativa la diferencia durante las últimas 4 semanas para los neutrófilos y las últimas 10 semanas para los leucocitos.
Durante los dos años siguientes de seguimiento, esta diferencia se mantiene significativa (p<0,005 según la Traza de Pillai), aunque los recuentos tienden a estabilizarse. Se observan un caso nuevo de leucopenia y neutropenia del total de la muestra (n=120).
Contamos con el seguimiento mensual completo de recuentos hematológicos durante 5 años para 69 pacientes. Durante estos años, no se han observado nuevos casos de leucopenia o neutropenia y se ha observado como la curva del recuento tiende a la estabilización de los parámetros.
De los casos señalados, se decide suspender el tratamiento en uno de ellos por la tendencia a mantener las cifras de neutrófilos bajas y en otro por la aparición de crisis epilépticas simples.
DiscusiónEn esta cohorte de pacientes tratados con clozapina, se ha observado una prevalencia de neutropenia del 3%, concentrado en los primeros meses de seguimiento, lo que concuerda con datos publicados por otros autores23. Ningún paciente ha presentado agranulocitosis.
La mayor parte de los pacientes de la muestra tenían un diagnóstico de psicosis resistente o habían presentado efectos adversos significativos asociados al uso de otros tratamientos antipsicóticos.
Las estimaciones de la prevalencia de esquizofrenia resistente varían según su definición, pero se estima que entre un quinto y un tercio de los pacientes con esquizofrenia tiene una respuesta sub-óptima al tratamiento antipsicótico. Llama la atención que, a pesar de la evidencia científica actual sobre los beneficios de la clozapina sobre otros antipsicóticos en el tratamiento de la esquizofrenia, este fármaco siga siendo infrautilizado24. En EE. UU., el porcentaje de prescripción de clozapina en relación con otros antipsicóticos no llegó al 3,5% durante el período 2008-200925. En una muestra Italiana, el porcentaje observado fue de 1,5%26.
La prescripción de clozapina se ve limitada por sus efectos adversos como la sialorrea, el mareo, el estreñimiento y algunos que potencialmente podrían aumentar la morbimortalidad de los pacientes, como son el síndrome metabólico, la agranulocitosis, la miocarditis, la cardiomiopatía y la disminución del umbral convulsivante. Por otro lado, en un estudio publicado recientemente por Tiihonen et al.27, en el que se realizó seguimiento durante 10 años a una cohorte Finlandesa de 66.881 pacientes con diagnóstico de esquizofrenia, los autores concluyeron que los pacientes en tratamiento con clozapina tuvieron el riesgo más bajo de muerte prematura, comparados con los pacientes que tomaban otros antipsicóticos y con los pacientes que no tomaban antipsicóticos de forma regular. Este efecto protector, podría estar mediado en parte por la disminución del riesgo de suicidio28. Los autores sugieren que las restricciones en el uso de clozapina «podrían haber causado miles de muertes prematuras».
El hecho de que la mayoría de pacientes en tratamiento con clozapina son resistentes o han tenido previamente efectos adversos importantes a otros antipsicóticos, hacen que la decisión de suspender el tratamiento con clozapina sea difícil. Muchos de los médicos consideran reiniciar la clozapina en pacientes con antecedentes de neutropenia a pesar del riesgo que ello implica29,30.
La clozapina puede relacionarse con la neutropenia de manera directa como hemos revisado anteriormente y de manera indirecta. Ejemplos de esto último, son la neutropenia étnica benigna, efectos secundarios de otros fármacos administrados concomitantemente o mediante la interacción con clozapina y la comorbilidad médica29. Se han descrito métodos para el manejo de la neutropenia en estos pacientes, que incluyen la co-administración de litio, la administración de factores de estimulación de granulopoyesis y el manejo racional de fármacos concomitantes. Si bien estos tratamientos dan un margen de seguridad, han sido utilizados en un número limitado de casos y su nivel de evidencia aún es débil29,31,32.
Los protocolos asociados al uso de clozapina, tienen un alto coste para el paciente y el servicio sanitario. La evidencia actual disponible en relación con la efectividad y seguridad de este fármaco y los resultados del presente estudio, hacen adecuado plantearse la revisión y discusión de los protocolos de utilización y seguimiento de la clozapina. Tomando en consideración que el mayor riesgo se concentra en los primeros 6 meses de tratamiento y que a partir del primer año el riesgo de aparición de agranulocitosis se equipara al de otros fármacos que no precisan de monitorización, estaríamos a favor de mantener un control semanal durante las primeras 18 semanas, mensual hasta el primer año y pasar a control bimensual a continuación. Este cambio supondría un menor coste para el paciente y para el servicio sanitario y podría mejorar la adherencia a los controles y al tratamiento.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.Derecho a la privacidad y consentimiento informado. Los autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónEl Dr. Bernardo ha recibido fondos para investigación y/o ha participado como consultor y/o ponente en actividades organizadas por las siguientes empresas: Adamet, Almirall, Bristol-Myers Squibb, Eli Lilly, Janssen-Cilag, Mylan, Pfizer, Roche y Rovi.
El Dr Pons ha participado como consultor y/o ponente para las siguientes empresas: Janssen-Cilag, Johnson & Johnson.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Con el soporte de la Generalitat de Catalunya, Comisionado para Universidades y Desarrollo del Departamento de Innovación, Universidades y Empresa (DIUE) 2009SGR1295 y del Instituto de Salud Carlos III, Centro de Investigación Biomédica en Red de Salud Mental, CIBERSAM (para JU, AP, AB, MB) y con el soporte de l’Ajut a la Reçerca Josep Font del Hospital Clínic de Barcelona (para JU).