En este artículo se presenta la rehabilitación implanto-soportada de un paciente previamente tratado mediante resección de carcinoma epidermoide de piso de boca y radioterapia (dosis total de 56 Gy). El tratamiento consistió en la administración de terapia de oxígeno hiperbárico mediante el siguiente protocolo: previa a la colocación de los implantes de 20 sesiones diarias con 100% de oxígeno a 2.4 ATM de presión, durante 90 minutos y 10 sesiones diarias con 100% de oxígeno, a 2.4 ATM de presión durante 90 minutos posterior a la colocación de los implantes. La rehabilitación protésica fue realizada seis meses posteriores a la colocación de los implantes mediante una prótesis removible implanto-soportada con sistema de anillos para la retención de la misma. Actualmente, el paciente se encuentra a dos años de seguimiento de la rehabilitación, libre de actividad tumoral en la zona tratada y con un adecuado resultado funcional y estético.
The present article presents a case of implant-supported rehabilitation of a patient who had previously undergone a procedure of floor of the mouth squamous cell carcinoma resection followed by radiotherapy (56 Gy total). Treatment consisted on hyperbaric oxygen therapy by means of the following protocol: previous to implant placement: 20 daily sessions, 100% oxygen at 2.4 ATM pressure during 90 minutes as well as 10 daily sessions of 100% oxygen at 2.4 ATM pressure, during 90 minutes after implant placement. Prosthetic rehabilitation was conducted six months after implant placement. It consisted of an implant-supported removable prosthesis with a ring system to achieve retention. Presently the patient is at a two year follow-up period after rehabilitation, and is free of tumor activity in the treated zone. The patient has so far achieved appropriate esthetic and functional results.
Los pacientes que han recibido terapéutica quirúrgica y de radiación para el tratamiento de cáncer de cabeza y cuello son considerados grandes retos desde el punto de vista reconstructivo por la restauración estética y la función de los tejidos involucrados.1 Las secuelas y complicaciones producto de la combinación de estos tratamientos dan como resultado arcadas difíciles o imposibles de rehabilitar con dentaduras convencionales, debido a la deficiente estabilidad en un ambiente bucal comprometido.
El uso de implantes oseointegrados puede mejorar la calidad de rehabilitación al permitir al paciente una adecuada función y estética.2
La radioterapia produce cambios en los tejidos haciéndolos hipocelulares, hipovasculares e hipóxicos, que condicionan una cicatrización lenta e inadecuada, con alto potencial de desarrollar osteorradionecrosis, siendo la mandíbula el sitio más afectado en la región de la cabeza y el cuello.3 Se ha demostrado ampliamente que la integración de implantes en tejidos irradiados previamente estará comprometida debido a la hipovascularidad de los mismos y a la alteración de la capacidad de regeneración ósea.4
La radioterapia se ha considerado una contraindicación para la cirugía implantológica.7 Sin embargo, se ha demostrado que el uso de terapia con oxígeno hiperbárico es la única vía para aumentar la vasculari-dad y la tensión de oxígeno en tejidos irradiados.4
Este artículo describe la secuencia de tratamiento y consideraciones que deben tomarse en cuenta en la rehabilitación de un paciente con prótesis implanto-soportada, previamente sometido a resección tumoral y radioterapia.
Reporte clínicoPaciente masculino de 56 años de edad referido al Servicio de Cirugía Oral y Maxilofacial de la Facultad de Odontología de la Universidad Nacional Autónoma de México (UNAM) por parte del Servicio de Prótesis Maxilofacial del Instituto Nacional de Cancerología de México (INCAN).
El paciente fue valorado inicialmente por el Servicio de Cabeza y Cuello del INCAN, por presentar una lesión exofítica en la región anterior y del lado izquierdo del piso de la boca, de cinco meses de evolución, de consistencia dura, dolorosa a la palpación y con una dimensión aproximada de 20mm. Además, se detectaron dos adenomegalias yugulodigástricas del lado izquierdo de 2 y 1.5cm de diámetro respectivamente, no dolorosas a la palpación y de consistencia dura. Usando el sistema de clasificación actual para estadios tumorales, el paciente entraba en el estadio III (T2N1M0).5
Fue sometido a tratamiento quirúrgico por parte del Servicio de Cabeza y Cuello del INCAN, quienes le realizaron resección de mucosa de piso de boca, mandibulectomía marginal y disección supraomohioi-dea del cuello bilateral. El estudio histopatológico de la lesión confirma el diagnóstico de carcinoma epidermoide moderadamente diferenciado que infiltraba al tejido muscular y a la glándula sublingual.
Dos meses posteriores al tratamiento quirúrgico, recibió teleterapia en el piso de boca y en áreas ganglionares yugulodigástricas por parte del Servicio de Radioterapia del INCAN. El tratamiento fue dividido en tres campos: anterior, lateral derecho y lateral izquierdo, para una dosis total de 56 Gy.
Posterior a esto, fue valorado por el Servicio de Prótesis Maxilofacial del INCAN, quienes proponen la rehabilitación del paciente mediante implantes endoóseos de titanio y prótesis total removible implantosoportada.
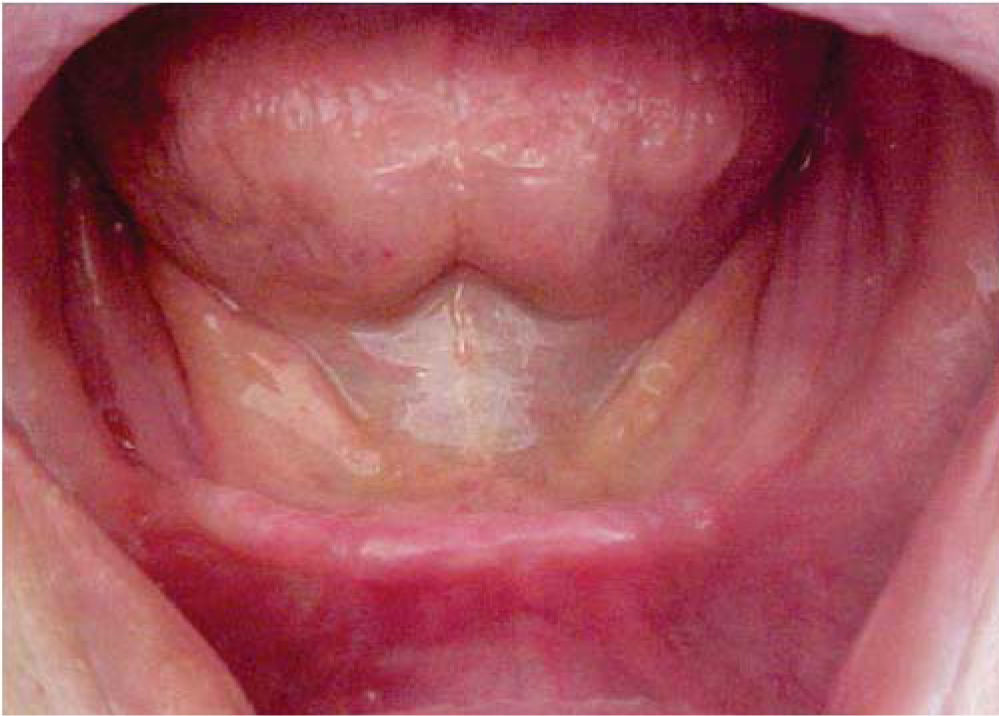
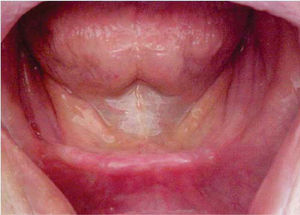
Al momento de la valoración por parte de nuestro servicio, el paciente presentaba un seguimiento de cinco años libre de actividad tumoral con limitaciones en la función masticatoria y en la fonación. A la exploración física intraoral del paciente se observa rehabilitación con prótesis fija convencional en maxilar y edéntulo en la región mandibular, mucosas con datos de xerostomía y reborde alveolar clase IV de Cawood y Howell (Figura 1).6
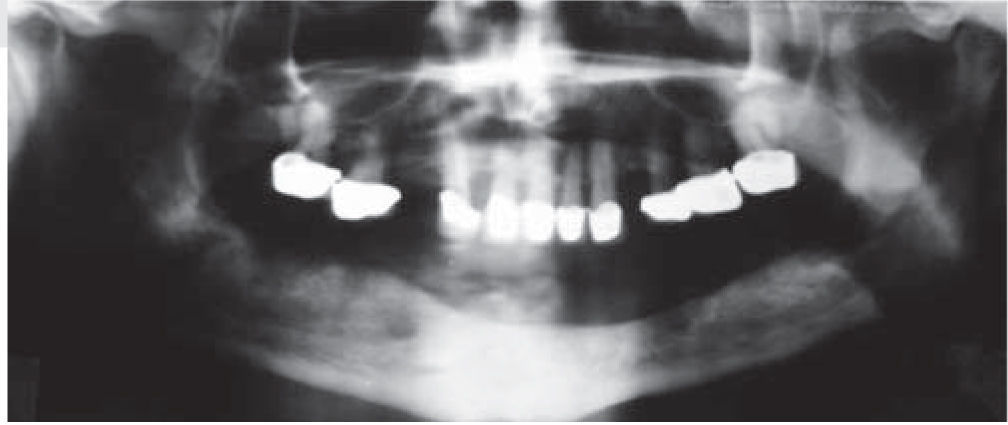
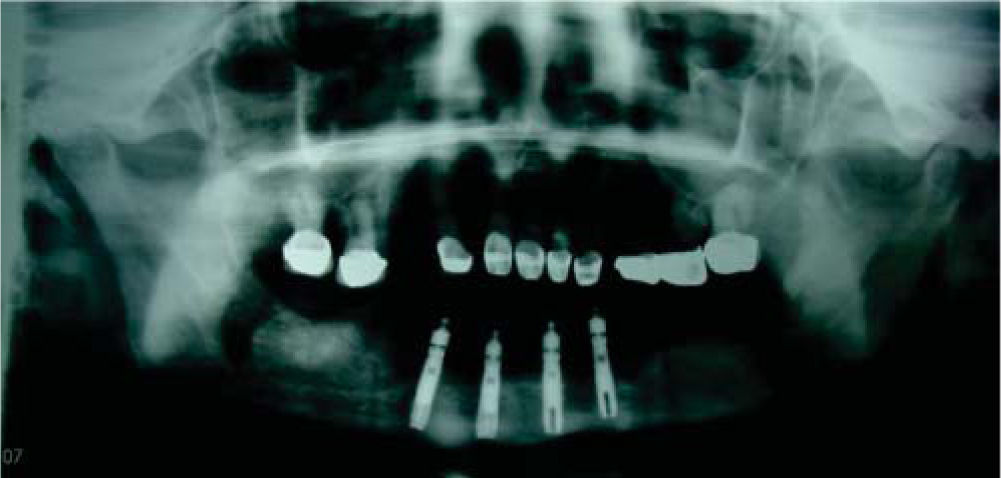
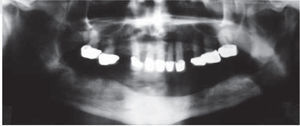
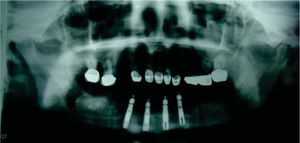
Se decide iniciar protocolo de oxígeno hiperbárico que consistió en 20 sesiones diarias a 2.4 ATM de presión, 100% de oxígeno, durante 90 minutos (cámara hiperbárica monoplaza Sechrist Industries, Inc, 2820 Gretta LN, Anaheim, CA), previas a la colocación de implantes (Figura 1). Radiográficamente en ortopantomografia se observa imagen correspondiente a reborde alveolar residual de características normales (Figura 2).
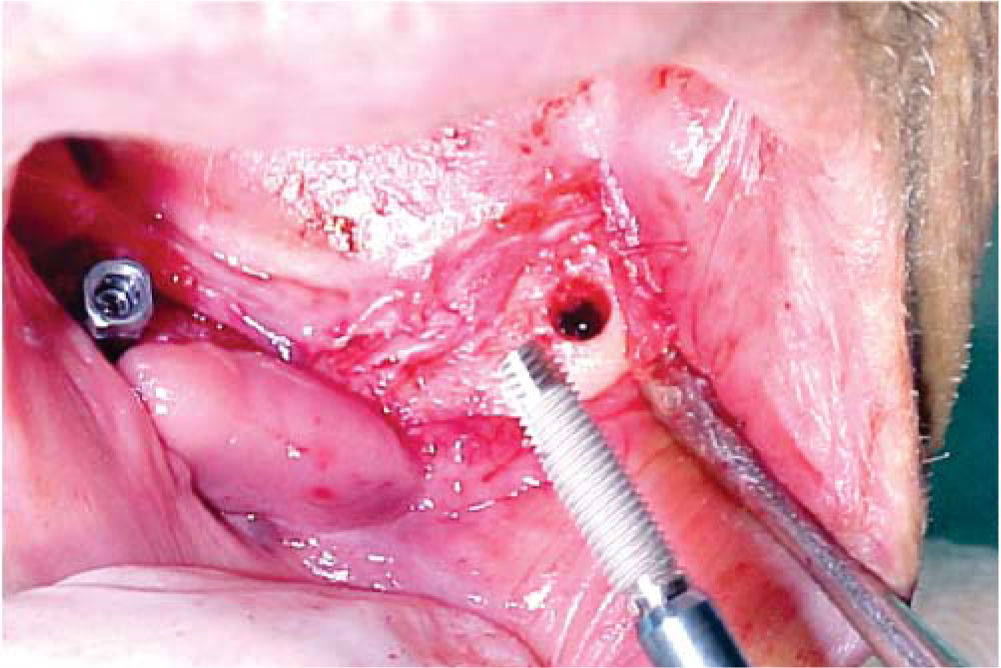
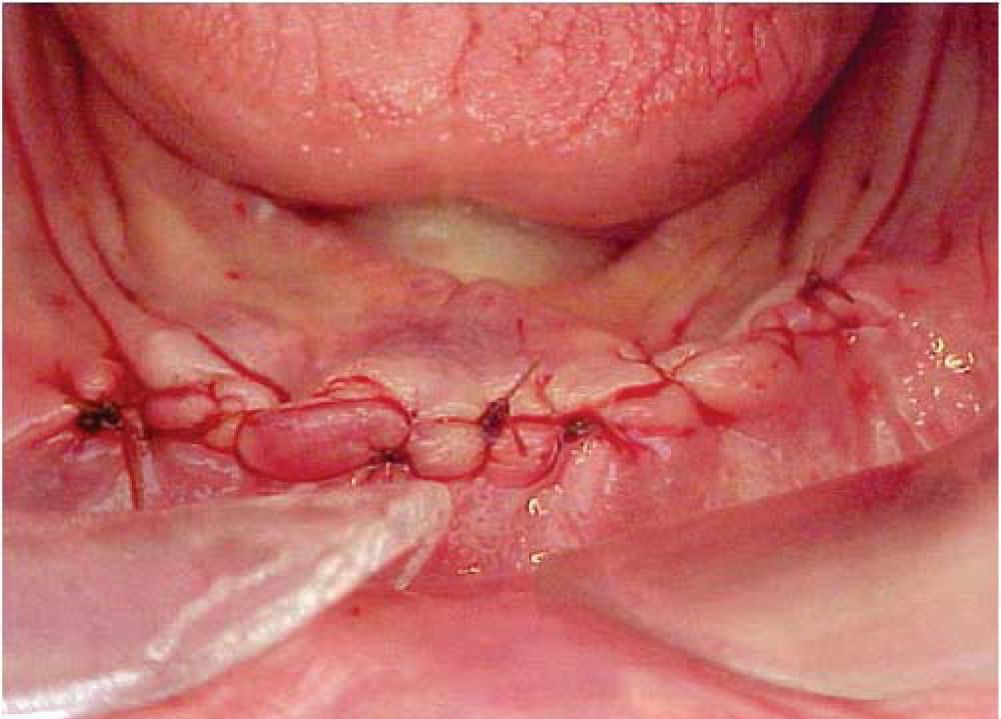
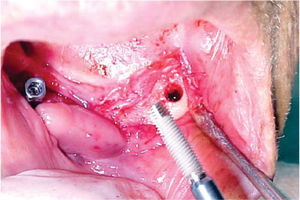
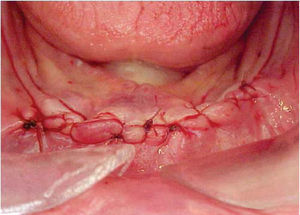
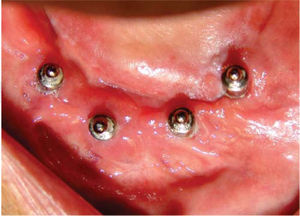
Bajo anestesia local con lidocaína al 2% con epinefrina 1:100,000 se realiza incisión de aproximadamente 4cm de longitud encima del reborde alveolar anteroinferior (en zona de incisivos inferiores). Se levanta colgajo mucoperióstico exponiendo el hue so alveolar residual de la zona anteroinferior de la mandíbula. Se realiza el primer lecho quirúrgico y se coloca un pin de paralelismo previa realización del segundo lecho quirúrgico y así sucesivamente hasta realizar cuatro lechos receptores. Se colocan cuatro implantes de rosca de titanio de 4.0mm de diámetro x 16mm de longitud (Sulzer Dental Inc, Taper Lock Screw, TLB16) (Figura 3). Se sutura de primera intención con puntos continuos (Figura 4) y se dan indicaciones postoperatorias. Se medica amoxicilina 500mg vía oral cada 8 horas durante 7 días e ibuprofeno 400mg vía oral cada 8 horas durante 4 días. Al día siguiente, se continúa con 10 sesiones diarias de oxígeno hiperbárico con 100% de oxígeno a 2.4 ATM de presión durante 90minutos, para un total de 30 sesiones (20 sesiones previas a la cirugía y 10 posteriores a la misma). El paciente cursó el postoperatorio sin complicaciones.
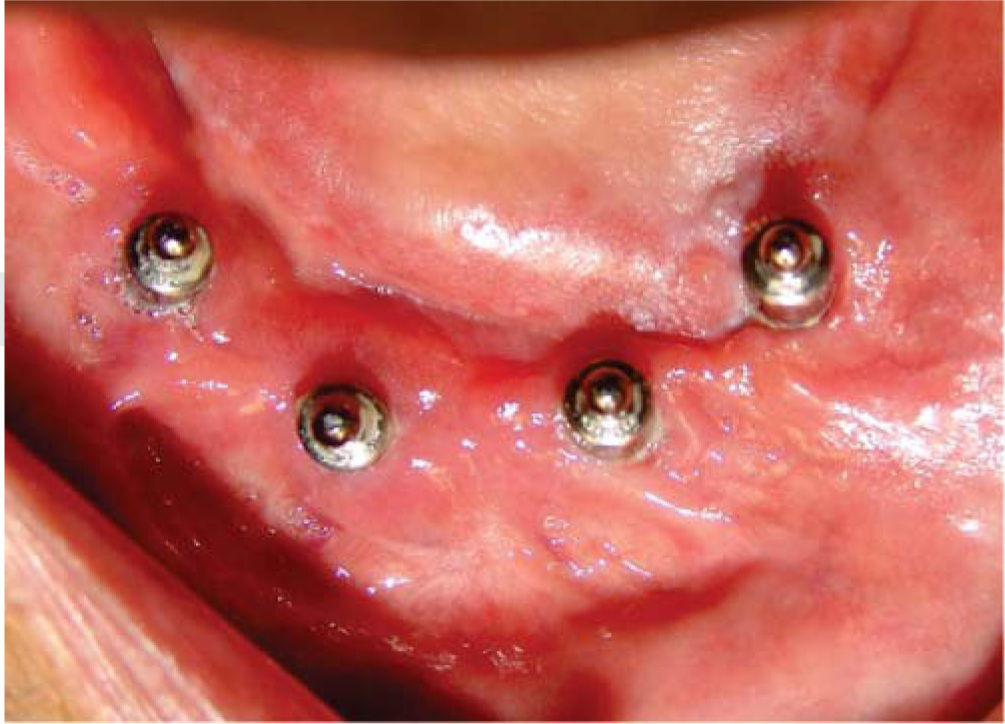
Seis meses más tarde, se indica ortopantomografía, en la cual se observan datos de integración de los implantes. Se procede a descubrir los implantes, colocando los tornillos de cicatrización y observando integración clínicamente de los mismos.
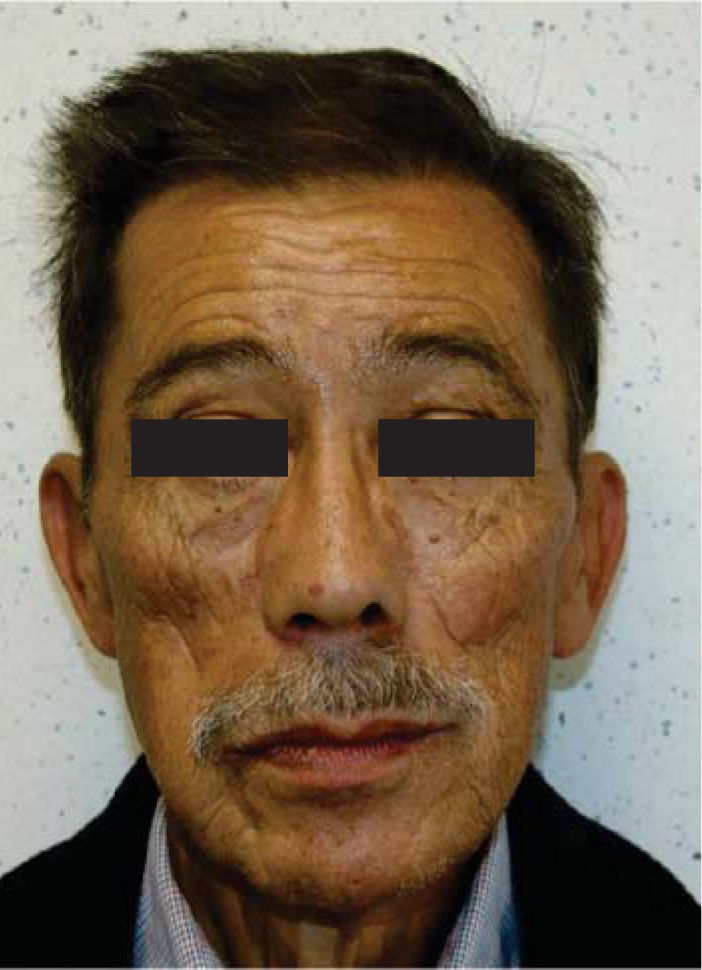
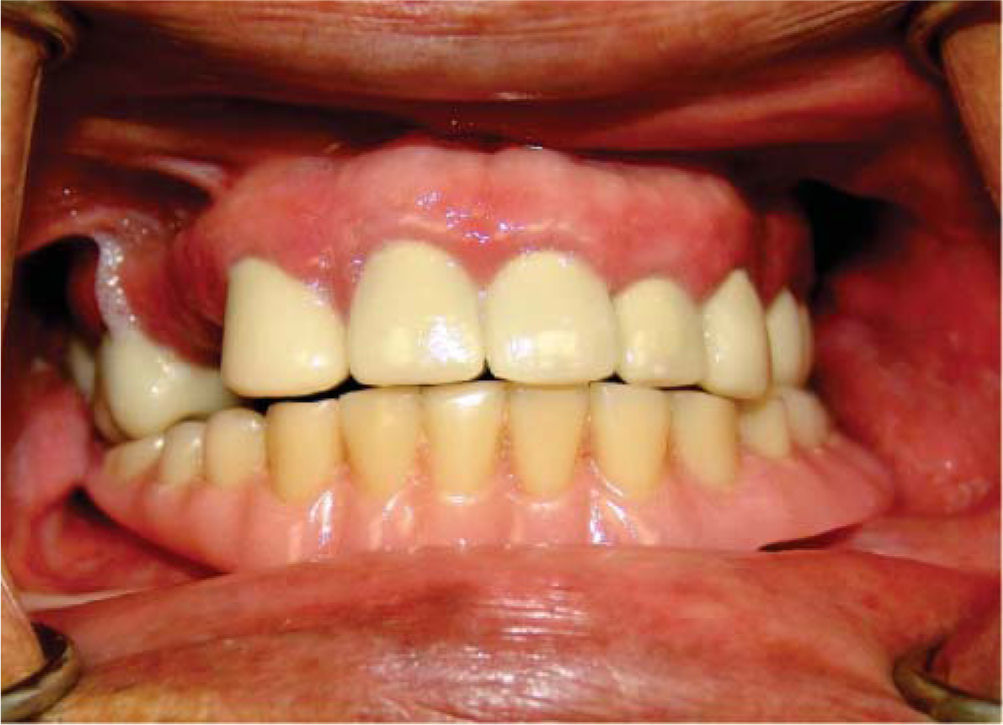
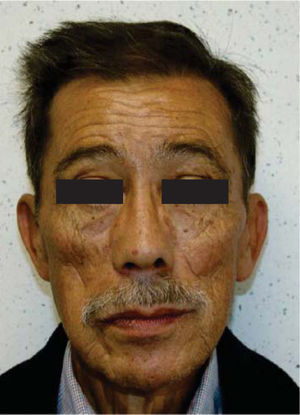
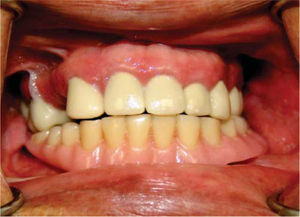
Dos semanas más tarde, el Servicio de Prótesis Maxilofacial del INCAN realiza el proceso de rehabilitación. A dos años de seguimiento de la rehabilitación, el paciente se encuentra satisfecho con el resultado, sin signos de inflamación adyacente a los implantes y con adecuada estética y función (Figuras 5, 6, 7y8).
DiscusiónActualmente, el tratamiento más usado para tratar tumores malignos de la región craniomaxilofacial es la combinación de cirugía y radioterapia.7 Los pacientes edéntulos, como resultado de resección de tumores malignos presentan de manera frecuente alteraciones estéticas en la función masticatoria y del lenguaje.9
Los efectos colaterales de la radioterapia pueden dividirse en efectos tempranos y efectos tardíos. En los efectos tempranos se produce una alteración en las estructuras intrínsecas de los tejidos blandos: glándulas salivales, piel, mucosa oral y nasal (dermatitis, mucositis, xerostomía, mucosa atrófica, friable y funcionalmente inadecuada). Y en los efectos tardíos, el tejido óseo es el involucrado y se produce una desmineralización del mismo, fibrosis reparativa, aumento en la susceptibilidad de infecciones y, finalmente, necrosis avascular (osteorradionecrosis).8
La radioterapia causa cambios significativos en el tejido óseo que reducen el potencial para la oseointegración de los implantes, aumentando la tasa de no integración de los mismos.8
Se ha demostrado histológicamente, mediante estudios experimentales, que el uso de oxígeno hiperbárico como tratamiento adyuvante reduce la tasa de rechazo de implantes colocados en huesos previamente irradiados.9 Sin duda alguna, el problema reconstructivo de mayor reto se presenta en pacientes con defectos tisulares, producto de cirugías oncológicas radicales y que recibieron más de 50 Gy de radioterapia.10 Estudios realizados previamente en este tipo de pacientes, demuestran una alta tasa de complicaciones y una baja tasa de éxito en la reconstrucción posterior a cirugía y radioterapia.11
El efecto de la terapia de oxígeno hiperbárico sobre tejidos irradiados ha sido estudiado previamente. La elevación de la tensión de oxígeno en huesos hipóxicos y tejidos blandos da como resultado la proliferación fibroblástica, el crecimiento de capilares, la síntesis de colágeno y la angiogénesis capilar, eventos necesarios para una adecuada integración de los implantes.11
Además de los beneficios de anclaje obtenidos con el uso de implantes oseointegrados, este tipo de rehabilitación produce un adecuado resultado estético al permitir dar volumen a una zona deficiente, producto de las resecciones realizadas, y una mayor comodidad y seguridad al paciente, por ser rehabilitaciones con adecuado anclaje; además mantiene la accesibilidad de la zona al tratarse de rehabilitaciones que pueden ser retiradas fácilmente por el paciente, permitiendo una adecuada higiene y una zona accesible para la inspección constante y control de cualquier recurrencia tumoral.7