Los síntomas del tracto urinario inferior (STUI) son muy frecuentes en los varones, sobre todo en los mayores de 65 años. La hiperplasia benigna de próstata (HBP) es la enfermedad del varón que más se asocia a los STUI, y es una causa frecuente de alteración en la calidad de vida. Los alfabloqueantes en monoterapia representan el tratamiento de primera elección en pacientes con STUI moderados-severos secundarios a HBP.
Silodosina actualmente es el alfabloqueante más uroselectivo sobre los receptores α1A, uroselectividad que ha sido confirmada en diversos estudios tanto in vitro como in vivo. En este trabajo se analizan los principales beneficios de la silodosina, tanto en los ensayos clínicos fase iii (enfoque estándar) como en la «vida real» (analizando el estudio «Silodosin in Real-life Evaluation [SiRE]», estudio de fase iv), para validar los datos de los ensayos de registro, y confirmar el perfil de riesgo-beneficio positivo de silodosina en un entorno que pueda reflejar más estrechamente la práctica clínica.
Lower urinary tract symptoms (LUTS) are very frequent in men, especially in those above 65 years of age. Benign prostatic hyperplasia (BPH) is the pathology most associated with LUTS in men and is a frequent cause of altered quality of life. Monotherapy with alpha blockers is the treatment of choice in patients with moderate-to-severe LUTS secondary to BPH.
Silodosin is currently the most uroselective alpha blocker acting on the α1A receptors. Its uroselectivity has been confirmed in different in vitro, as well as in vivo, studies. The present study analyzed the main benefits of silodosin in phase iii clinical trials (standard approach) and in «real life» (analyzing the «Silodosin in Real-life Evaluation (SiRE)» phase iv trial) to validate the registrational trials and confirm the positive risk-benefit profile of silodosin in an environment that can more closely reflect clinical practice.
Los síntomas del tracto urinario inferior (STUI) son muy frecuentes en los varones, sobre todo en los mayores de 65 años, en los que la prevalencia es superior al 40%. Según los resultados de un estudio realizado en Europa1, algunos de los síntomas más frecuentes notificados por los pacientes con STUI son los síntomas de llenado, los síntomas de vaciado y, especialmente, la nicturia, que se informa en el 77% de los casos. Es importante tener en cuenta que, en la práctica clínica, los pacientes rara vez presentan solo un síntoma, sino que, muy a menudo, los tienen combinados, como nicturia y vaciamiento incompleto, o nicturia y frecuencia, o incluso una combinación de los 3síntomas. Por consiguiente, el objetivo es tratar varios STUI al mismo tiempo en el mismo paciente.
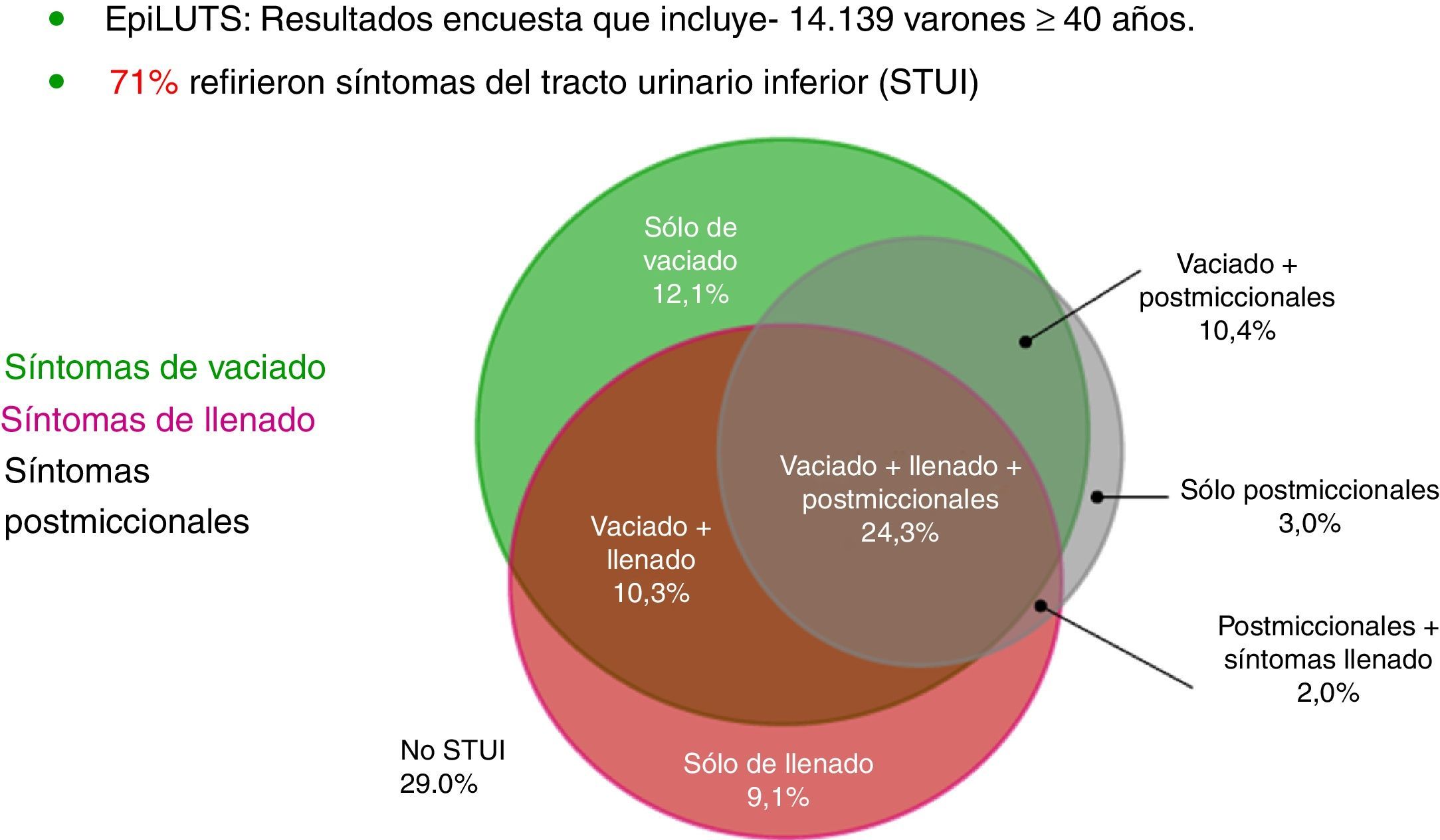
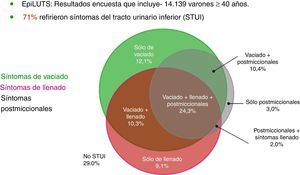
El estudio EpiLUTS, que evaluó a más de 14.000 pacientes en Europa y EE. UU., muestra que los STUI pueden ser muy variables (fig. 1)2.
Variedad y grado de molestia de los STUI (adaptado de Sexton et al.2).
Entre los diferentes STUI, la nicturia es sin duda el más importante y molesto, ya que tiene un impacto considerable en la calidad de vida de los pacientes. Se ha notificado que los pacientes que experimentan más de 3 episodios de nicturia por noche sufren una disminución importante en su calidad de vida, sobre todo cuando tienen entre 40 y 59 años de edad3.
Otro aspecto importante es que los hombres con STUI, especialmente si tienen más de 65 años, presentan generalmente una serie de comorbilidades como hipertensión, dolor de espalda, cambios en la visión, enfermedad de las arterias coronarias, diabetes, incontinencia y riesgo de caídas debido a hipotensión arterial. Todos estos trastornos han de ser tratados de manera adecuada, y se deben tomar en consideración debido a posibles interacciones con diferentes terapias médicas4.
Los pacientes con STUI experimentan con frecuencia cambios en la función sexual. Los resultados de un estudio realizado por Rosen et al. mostraron que, frecuentemente, los pacientes mayores de 60 años tienen pocas erecciones o ninguna, mientras que casi el 20% de los pacientes con edades entre los 60 y 70 años experimentan disfunción eréctil. Se comunican datos similares en términos de disfunción eyaculatoria, caracterizada por una disminución o por la no eyaculación. Esta condición es particularmente frecuente entre los pacientes mayores de 70 años5.
La hiperplasia benigna de próstata (HBP) es la enfermedad del varón que más se asocia a los STUI, y es una causa frecuente de alteración en la calidad de vida6.
Papel de los alfabloqueantes en el tratamiento de los síntomas del tracto urinario inferior/hiperplasia benigna de próstataLa práctica totalidad de las guías consultadas concluyen desde hace años que, con un nivel de evidencia ia y con un grado de recomendación A, los alfabloqueantes en monoterapia representan el tratamiento de primera elección en pacientes con STUI moderados-severos secundarios a HBP7–10.
El sistema nervioso simpático desempeña un papel fundamental en la regulación del aparato urinario inferior. Mientras que el sistema parasimpático inerva el músculo detrusor, el simpático ejerce un papel fundamental en el trígono, cuello vesical y uretra proximal. Existen 2 tipos de receptores α-adrenérgicos, los α1, postsinápticos, y los α2, que pueden ser pre- o postsinápticos. Cuando se estimulan los receptores α1 se produce una contracción de la musculatura lisa y, al mismo tiempo, una contracción miocárdica, un aumento de la glucogenólisis, por acción central, y una mayor psicomotricidad. La estimulación de los receptores α2 postsinápticos consigue una contracción de la musculatura lisa junto con un aumento de la agregación plaquetaria, una inhibición de la lipolisis y una mayor liberación de insulina11. Sabiendo que, en buena medida, la presión uretral en la HBP está mediada por la activación de los receptores α1-adrenérgicos, la diana farmacológica es el bloqueo de estos receptores.
Los alfabloqueantes constituyen un grupo farmacológico que, en su origen, debido a su efecto vasodilatador, se utilizaron para tratar la hipertensión arterial. Posteriormente se observó que presentaban un efecto beneficioso sobre los STUI al actuar sobre los receptores α1-adrenérgicos. Los receptores α1 se encuentran a nivel de vejiga, cuello vesical y próstata. Se conocen diferentes subtipos de receptores α1 (A, B, D). En la vejiga, el subtipo α1 más frecuente es el α1D, en el cuello vesical existen el α1D y el α1A, mientras que en la próstata predomina el subtipo α1A en un 98%, y el subtipo α1B se encuentra en mayor proporción a nivel vascular12.
Inicialmente se utilizaron en el tratamiento de la HBP alfabloqueantes no selectivos, que actuaban sobre los receptores α1 y α2 (fentolamina, fenoxibenzamina), pero se dejaron de usar en la HBP porque producían muchos efectos secundarios (hipotensión ortostática, taquicardias, síncopes, congestión nasal y arritmias). Posteriormente aparecieron alfabloqueantes selectivos de los receptores α1 (doxazosina, terazosina, alfuzosina), y actualmente se dispone de fármacos más uroselectivos, como son tamsulosina y silodosina7,11.
Un objetivo en los últimos años ha sido el encontrar fármacos con un nivel de uroselectividad mayor, es decir, que sin disminuir su eficacia consigan un menor porcentaje de efectos secundarios. En este sentido, ha surgido el concepto de «uroselectividad», el cual hace referencia a la mayor afinidad que tienen la tamsulosina y la silodosina sobre el subtipo de receptor α1A para conseguir los efectos beneficiosos (mejoría de los STUI) con un mejor perfil de seguridad. Los otros alfabloqueantes (doxazosina, terazosina, alfuzosina) presentan más efectos secundarios (sobre todo hipotensión ortostática, cefalea, mareo y síncope), mediados fundamentalmente por el bloqueo de los receptores α1B y α1D, con una eficacia clínica similar7,11.
Globalmente, los alfabloqueantes producen una mejoría rápida de los síntomas (4-6 puntos en el IPSS [índice internacional de los síntomas prostáticos]), mejoría en la calidad de vida (1-1,5 puntos) y en el flujo máximo (2-3ml/s). Su acción beneficiosa máxima aparece a partir de la 2.ª-4.ª semana de iniciar el tratamiento. No tienen ningún efecto sobre el volumen de la próstata, no modifican la progresión natural de la enfermedad ni alteran los valores del antígeno prostático específico (PSA)7,13.
La tamsulosina fue el primer alfabloqueante que apareció con mayor grado de uroselectividad, aunque esa mejora no redundó en una mayor mejoría clínica: la ventaja se basaba en poder utilizar la dosis de 0,4mg sin necesidad de escalar dosis11,14.
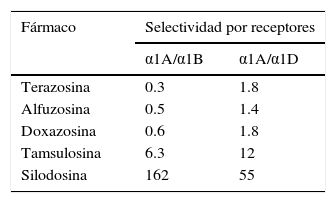
A principios de la década de los noventa del siglo xx se descubrió la silodosina, que es el alfabloqueante más uroselectivo sobre los receptores α1A. Esta selectividad para receptores α1A vs. α1B es 38 veces superior a la de la tamsulosina, por lo que apenas tiene efectos sobre la presión arterial15, con un alto perfil de seguridad en pacientes afectos de insuficiencia cardiaca o tratados con diversos fármacos antihipertensivos (IECAS, ARA-II, betabloqueantes, antagonistas del calcio y diuréticos). En la tabla 1 se resume la selectividad de los alfabloqueantes por el receptor α1A16.
Selectividad de los alfabloqueantes por el subtipo α1A
| Fármaco | Selectividad por receptores | |
|---|---|---|
| α1A/α1B | α1A/α1D | |
| Terazosina | 0.3 | 1.8 |
| Alfuzosina | 0.5 | 1.4 |
| Doxazosina | 0.6 | 1.8 |
| Tamsulosina | 6.3 | 12 |
| Silodosina | 162 | 55 |
Fuente: Adaptado de Roehrborn16.
Se realizaron un total de 3 ensayos para el dossier de registro de silodosina en el tratamiento de pacientes con HBP17,18. Estos ensayos aleatorizados y controlados con placebo se llevaron a cabo tanto en EE. UU17. como en Europa18 con un total de 1.878 pacientes, de los cuales 847 recibieron silodosina. La dosis recomendada es de 8mg diarios.
El objetivo principal de los ensayos realizados en EE. UU. fue evaluar la eficacia y seguridad de la silodosina en el tratamiento de la HBP, mientras que el ensayo en Europa demostró la superioridad de la silodosina en comparación con placebo y la no inferioridad respecto a la tamsulosina. En ambos casos, el objetivo primario fue un cambio en el IPSS desde la basal hasta la última observación. Los resultados de los ensayos en EE. UU. indican que silodosina produjo una mejoría rápida de los síntomas urinarios que se mantuvo durante 12 semanas, y que fue bien tolerada, con una baja incidencia de efectos secundarios (hipotensión ortostática incluida). El estudio en Europa también mostró que la silodosina es un tratamiento eficaz y bien tolerado para el alivio de los síntomas tanto de vaciado como de llenado en los pacientes con STUI. Este ensayo también demostró que, en general, silodosina no es inferior a tamsulosina y que únicamente la silodosina tiene un efecto significativo sobre la nicturia vs. placebo18.
Las características de los pacientes en los ensayos de registro fueron en general consistentes con todos los demás estudios con alfabloqueantes publicados en la literatura científica. Cabe mencionar que casi 1/3 de los pacientes incluidos presentaron hipertensión, disfunción eréctil o trastornos de la eyaculación19.
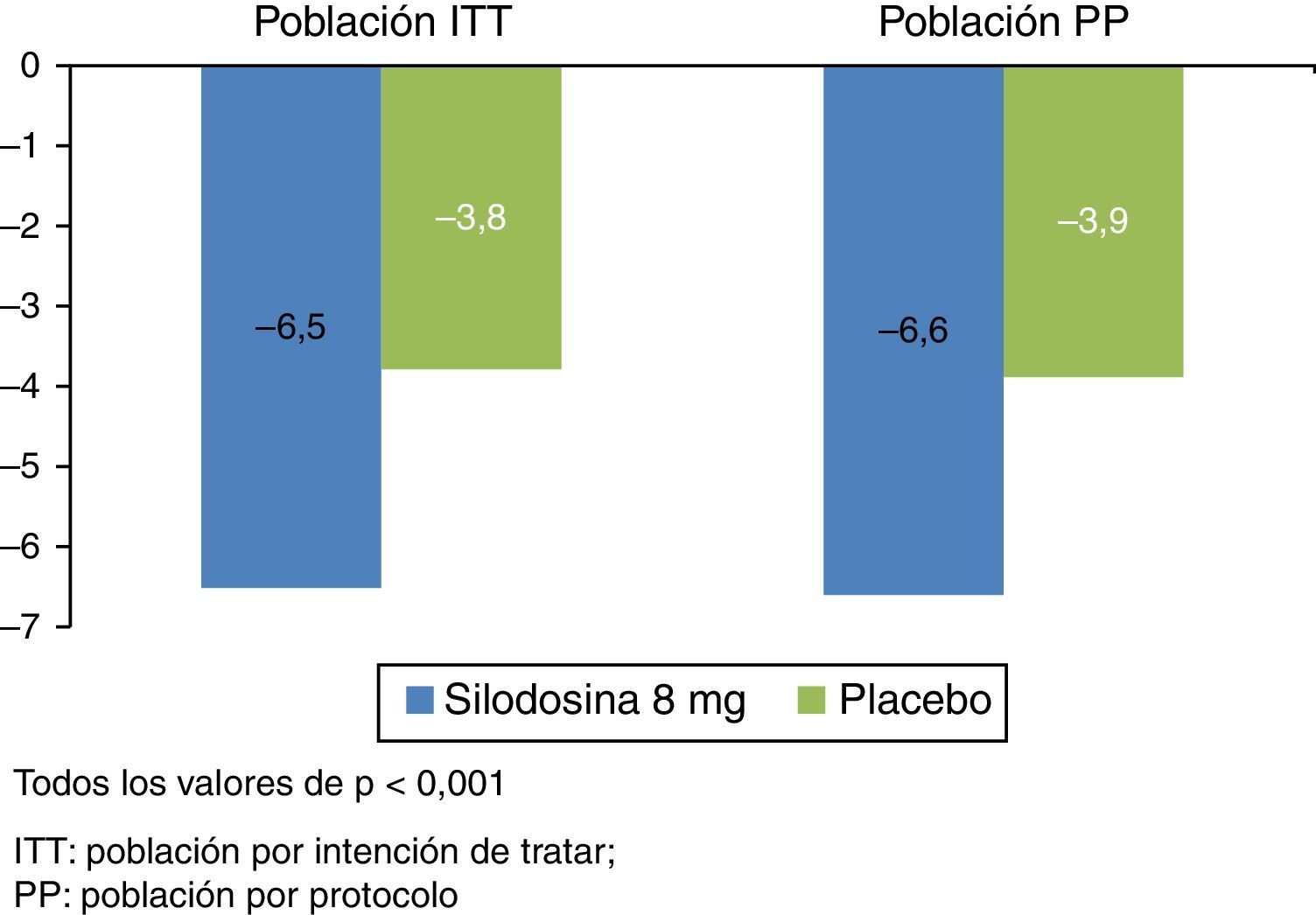
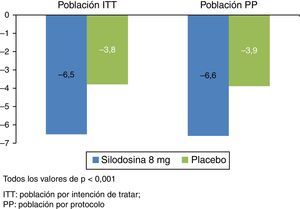
El análisis combinado de los datos de estos 3 ensayos muestra que el tratamiento con silodosina se asoció con una reducción estadística y clínicamente significativa en el IPSS, tanto en el grupo por intención de tratar (ITT) como en grupo de población por protocolo (PP), en comparación con placebo (fig. 2)19. Se observó la misma respuesta cuando los pacientes fueron estratificados de acuerdo con la gravedad de los síntomas al inicio del estudio (IPSS ≤ o>20). El beneficio conseguido asociado al tratamiento con silodosina fue clínica y estadísticamente significativo en los subgrupos de pacientes, con una disminución del 25% en la puntuación total del IPSS, independientemente de la gravedad de la enfermedad.
Reducción del IPSS en pacientes tratados con silodosina 8mg frente a placebo en la población ITT y en la población PP (adaptado de Novara et al.19).
El tratamiento con silodosina también se asoció con una reducción estadísticamente significativa en los STUI más frecuentes, como los de llenado y vaciado, con una mejora significativa en la puntuación de la calidad de vida. La velocidad de flujo también mejoró cerca de 1ml/s tanto en el análisis del grupo ITT como en el PP19.
Silodosina fue eficaz independientemente de la edad del paciente, según el análisis estratificado de los pacientes de acuerdo con la edad. Del mismo modo, el beneficio relacionado con el tratamiento fue muy similar en los pacientes con diferentes niveles de antígeno prostático específico (PSA) (≤ o>1,5ng/ml), lo cual muestra que el beneficio terapéutico de silodosina es independiente del volumen de la próstata20. De hecho, aunque se cree que el tratamiento con alfabloqueantes es más eficaz en pacientes con próstatas pequeñas, hay datos que muestran que cuanto más grande es la glándula, mayor será la mejoría conseguida con silodosina21.
Una de las características únicas de silodosina es su perfil de seguridad, el cual parece ser superior a todos los otros alfabloqueantes disponibles. A excepción de la eyaculación retrógrada, mejor definida como anaeyaculación, que se reportó en el 22% de los casos, solo se observó una ligera diferencia entre silodosina y placebo en todos los efectos secundarios comunes a los alfabloqueantes, tales como mareos, hipotensión ortostática, congestión nasal y rinitis19.
La estratificación de los pacientes según la edad mostró que los hombres menores de 65 años experimentaron anaeyaculación en casi el 30% de los casos, mientras que todos los demás efectos secundarios estaban prácticamente ausentes. Por otro lado, los hombres mayores de 65 años de edad experimentaron anaeyaculación con menos frecuencia y, curiosamente, rara vez presentaban otros acontecimientos adversos, incluyendo hipotensión ortostática, una de las principales preocupaciones en este grupo de pacientes20.
Dada la importancia de la eyaculación retrógrada, se realizó un análisis post hoc para evaluar la respuesta a silodosina según el trastorno de la eyaculación. Los resultados indican que los hombres con disfunción eyaculatoria obtienen un mayor beneficio clínico con silodosina en términos de mejoría clínica en el flujo urinario y en síntomas (representado ya sea por una mejora del 30% o por una mejora de 3 unidades en el IPSS)22.
Además, la anaeyaculación no influye en la tasa de abandono, que no mostró prácticamente ninguna diferencia (0,5%) entre silodosina y placebo. De hecho, la anaeyaculación parece ser más preocupante en los pacientes más jóvenes (≤65 años), en los que la tasa de abandono fue del 3,2%, mientras que los pacientes de edad avanzada que reciben tratamiento con silodosina mostraron tasas de abandono más bajas frente a placebo20.
Otro aspecto importante es el efecto que cada síntoma individual tiene sobre la calidad de vida del paciente. Así, diversos estudios han puesto de manifiesto que la nicturia es el STUI más frecuente por el que lo pacientes acuden a su médico de Atención Primaria1, mientras que la combinación de STUI más común que tiene un impacto notable en la calidad de vida de los pacientes parece ser la tríada: nicturia, aumento de la frecuencia miccional y sensación de vaciado incompleto1,23.
En este sentido, un subanálisis del estudio europeo sobre el efecto de silodosina sobre la nicturia informó de una reducción significativa de este síntoma, con silodosina respecto a placebo (67 vs. 55%; p<0,05) en el subgrupo de la población ITT con al menos 2 episodios de nicturia al inicio. Curiosamente, la mejoría frente a placebo fue estadísticamente significativa solo en el grupo de silodosina, pero no en el grupo de tamsulosina (el porcentaje de pacientes con una reducción de al menos un episodio fue del 63%, y fue muy similar al grupo placebo)18.
Considerando como síntomas de especial importancia clínica por su impacto en la calidad de vida de los pacientes la sensación de vaciado incompleto, la frecuencia miccional y la nicturia, en otro subanálisis del estudio europeo se evaluó el número de pacientes que presentaban una mejoría simultánea en estos 3síntomas. Un número significativamente mayor de pacientes tratados con silodosina presentó una mejoría simultánea de los 3síntomas comparados con placebo. En particular, el porcentaje de pacientes con una mejora simultánea de los 3síntomas fue mayor con silodosina que con tamsulosina, tanto en el análisis de toda la población del estudio (35 vs. 27,7%; p=0,03) como en el subgrupo de pacientes con al menos 2episodios de nicturia al inicio del estudio (40,7 vs. 32,4%; p=0,03). En conclusión, los datos de eficacia de este subanálisis indican que silodosina es significativamente más eficaz que tamsulosina y placebo en la mejoría simultánea de la nicturia, vaciado incompleto y frecuencia miccional18,24.
La comparación entre silodosina y tamsulosina ha sido evaluada en otro estudio a corto plazo aleatorizado, doble ciego, cruzado, en el que los pacientes fueron tratados con 4mg de silodosina 2 veces al día durante 4 semanas y después con 0,2mg de tamsulosina durante 4 semanas, o a la inversa. El primer grupo de pacientes, que recibió silodosina antes de tamsulosina, mostró una mejoría significativa en la puntuación total del IPSS después de la terapia con silodosina, mientras que posteriormente no se observaron cambios al pasar a tamsulosina. Por otra parte, los pacientes del segundo grupo también comunicaron un beneficio clínico después del tratamiento con tamsulosina, aunque más pequeño en comparación con aquellos tratados con silodosina, con una mejoría significativa posterior, después de cambiar a silodosina. Además, silodosina parece ofrecer una ventaja frente a tamsulosina en el tratamiento de la nicturia; de hecho, este síntoma mejoró más notablemente en el primer grupo de pacientes en comparación con el segundo25.
En estudios más a largo plazo se ha constatado que el efecto clínico de la silodosina perdura sin modificaciones significativas26,27.
Diversos estudios han puesto de manifiesto la frecuente asociación entre los STUI y la disfunción eréctil, siendo la presencia y severidad de STUI factores de riesgo independiente para el desarrollo de esta disfunción5,28. Por este motivo, no es raro que los pacientes con HBP y disfunción eréctil puedan estar recibiendo inhibidores de la 5-PDE (IPDE-5), que son vasodilatadores leves. Dado que algunos alfabloqueantes pueden inducir hipotensión ortostática incluso en pacientes normotensos, existe la posibilidad de que la combinación de los alfabloqueantes con los IPDE-5 pueda aumentar el riesgo de hipotensión ortostática (y, como consecuencia, en la ficha técnica y en el prospecto de los medicamentos IPDE-5 se incluyen consejos de prudencia sobre el uso concomitante de estos fármacos con alfabloqueantes). Un ensayo clínico de fase i controlado con placebo realizado en voluntarios sanos señala que la administración conjunta de silodosina con una dosis máxima terapéutica única de sildenafilo o tadalafilo en comparación con la administración conjunta de placebo solo no tiene ningún efecto clínico sobre la presión arterial ortostática ni sobre la aparición de síntomas ortostáticos. Dado que el estudio no planteó problemas de seguridad, se concluyó que no es necesario realizar ningún ajuste de dosis cuando la silodosina se administra conjuntamente con IPDE-529.
Los alfabloqueantes pueden tener diversos efectos sobre el intervalo QT (expresión electrocardiográfica de despolarización y repolarización ventricular) y pueden causar arritmias ventriculares. En este sentido, se realizó un ensayo aleatorizado, doble ciego, de grupos paralelos para evaluar el impacto de la silodosina sobre la prolongación del intervalo QT. Este estudio demostró que el tratamiento con silodosina no demora la repolarización cardiaca, mientras que el control activo (moxifloxacino, un antibiótico con ligero aumento del intervalo QT conocido) produjo los cambios esperados del intervalo QT. Estos resultados demuestran que silodosina no tiene efecto sobre la prolongación del intervalo QT30.
Evaluación de silodosina: uso en la «vida real» y perfil del pacienteEl estudio «Silodosin in Real-life Evaluation (SiRE)» es un estudio de fase iv, europeo, realizado en la «vida real», para validar los datos de los ensayos de registro y confirmar el perfil de riesgo-beneficio positivo de silodosina en un entorno que pueda reflejar más estrechamente la práctica clínica31.
Este ensayo se caracteriza por unos criterios de inclusión y exclusión muy amplios, con el fin de maximizar la similitud con una población «en la vida real». Los criterios de inclusión englobaban: edad mayor de 60 años, STUI de leves a moderados que requerían tratamiento médico, un diagnóstico clínico de agrandamiento benigno de la próstata/obstrucción prostática benigna/HBP y una puntuación IPSS total ≥ 12. Los criterios de exclusión fueron minimizados en lo posible: sin límite de edad, aceptación de la mayoría de las enfermedades cardiovasculares, de las enfermedades endocrinas y restricciones excepcionales en términos de medicación concomitante31.
El parámetro de eficacia primario utilizado en este estudio fue un descenso ≥ 25% en la puntuación total del IPSS respecto al valor inicial, un criterio de valoración ya utilizado en estudios anteriores y en los ensayos de registro. Los criterios de valoración secundarios incluyeron: una disminución>3 puntos en la puntuación total del IPSS, un cambio desde la basal en la puntuación total del IPSS y las subpuntuaciones de llenado y vaciado, un cambio desde la basal en la calidad de vida, un cambio desde la basal en la nicturia grave y el porcentaje de sujetos que mostraron una mejoría en los síntomas percibidos como más molestos al inicio del estudio (cuestionario ICS-varones)31.
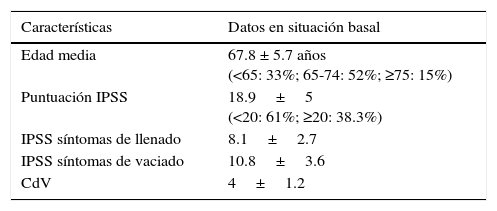
Las características basales de los pacientes mostraron que la población de este ensayo fue muy similar a la que se observa con mayor frecuencia en la práctica clínica en términos de edad, puntuación IPSS, subpuntuación IPSS de llenado y vaciado y calidad de vida (tabla 2).
Características basales de los pacientes incluidos en el estudio SiRE
| Características | Datos en situación basal |
|---|---|
| Edad media | 67.8 ± 5.7 años (<65: 33%; 65-74: 52%; ≥75: 15%) |
| Puntuación IPSS | 18.9±5 (<20: 61%; ≥20: 38.3%) |
| IPSS síntomas de llenado | 8.1±2.7 |
| IPSS síntomas de vaciado | 10.8±3.6 |
| CdV | 4±1.2 |
CdV: calidad de vida; IPSS: índice internacional de los síntomas prostáticos; SiRE: silodosin in real-life evaluation.
Adaptada de Montorsi et al.31.
Cabe señalar que, según los resultados de la pregunta 8 del IPSS, los pacientes se sentían muy molestos por sus síntomas, y que el 67% de ellos consideraban su situación como insatisfactoria, infeliz o terrible. La nicturia fue muy frecuente entre los pacientes: casi el 85% de los hombres experimentaba al menos 2 episodios de nicturia por noche y el 54%, al menos 3 episodios por noche. De acuerdo a los resultados del IPSS, la mayoría de los pacientes consideraban la nicturia como el síntoma más molesto, seguido por la frecuencia y la disminución del flujo31.
Una característica peculiar de los pacientes reclutados en el SiRE era que estos también presentaban enfermedades concomitantes como hipertensión (54,5%), dislipidemia (19,5%) y diabetes (17,4%), debido a que los criterios de exclusión fueron muy extensos. La disfunción sexual también estaba presente en estos pacientes, ya fuera como disfunción eréctil (15,5%) o disfunción eyaculatoria (3,8%). Dada la presencia de diversas comorbilidades, los pacientes recibieron varios medicamentos de forma concomitante (tabla 3).
Fármacos concomitantes que recibían los pacientes al inicio de estudio SiRE
| Silodosina 8mg N= 1.036 n (%) | ||
|---|---|---|
| Activadores del sistema renina -angiotensina | 434 (41.9) | |
| Hipolipemiantes | 240 (23.2) | |
| Betabloqueantes | 226 (21.8) | |
| Antitrombóticos | 208 (20.1) | |
| Antidiabéticos | 163 (15.7) | |
| Diuréticos | 139 (13.4) | |
| Bloqueantes canales del calcio | 140 (13.5) |
Adaptada de Montorsi et al.31.
Sorprendentemente, la mayoría de los pacientes no tenían experiencia con otros tratamientos similares, y solo el 20% había recibido previamente tratamiento para los STUI31.
Datos de eficaciaDespués de 6 meses de tratamiento, el 77% de los pacientes mostró una reducción en el total de la puntuación IPSS de al menos el 25%. Se observó una respuesta precoz al tratamiento después de 4 semanas desde el comienzo del tratamiento, y alcanzó una meseta (alrededor de 70%) en la semana 12 hasta el final del tratamiento (tabla 4)31.
Porcentajes de pacientes que respondieron a silodosina en cada visita
| Porcentaje de pacientes respondedores según IPSS | FAS population N = 994 |
|---|---|
| Visita 3 (semana 4) | |
| N | 963 |
| R | 621 |
| % | 64.5 |
| WCL | 61.4–67.4 |
| Visita 4 (semana 12) | |
| N | 909 |
| R | 698 |
| % | 76.8 |
| WCL | 73.9–79.4 |
| Visita 5 (semana 24) | |
| N | 921 |
| R | 715 |
| % | 77.6 |
| WCL | 74.8–80.2 |
| Endpoint (final del estudio) | |
| N | 994 |
| R | 766 |
| % | 77.1 |
| WCL | 74.3–79.6 |
FAS: full analysys set; IPSS: índice internacional de los síntomas prostáticos; N = número; R: respondedores; WCL: Wilson confidence limits (95%).
Adaptada de Montorsi et al.31.
El 80% de los pacientes obtuvo una disminución en 3 dominios del IPSS, con una reducción en la puntuación total del IPSS de 8,3±6,1 (de 18,9±4,9 a 10,6±6,0). Los pacientes informaron de mejoras también en las subpuntuaciones de llenado (−3,2±3,0) y vaciado (−5,1±4,1) y en términos de calidad de vida31.
En casi el 50% de los casos el tratamiento con silodosina también se asoció con una mejora sustancial respecto a los síntomas más molestos. Es de destacar que, a pesar de que el 20% de los pacientes sufrían poliuria nocturna, el tratamiento con silodosina disminuyó la nicturia en un 30% de los casos31.
Los análisis de los subgrupos demostraron que la respuesta a silodosina fue independiente de la edad (≤65 años, 65-74 años, ≥75 años) o de la gravedad de la enfermedad (IPSS<o ≥ 20). Además, no hubo diferencia significativa en el porcentaje de respondedores de acuerdo con la presencia de enfermedades concomitantes o tratamiento concomitante con inhibidores de la PDE-5 o medicamentos antihipertensivos, lo que indica que la eficacia de silodosina es independiente de la medicación concomitante y de las comorbilidades. El análisis de los subgrupos realizado al inicio del estudio mostró que los pacientes naive (no tratados previamente) tuvieron una tasa de respuesta más alta (79%) en comparación con los pacientes que habían recibido tratamiento previo. Este hallazgo señala que la silodosina podría ser recomendada como tratamiento de primera línea31.
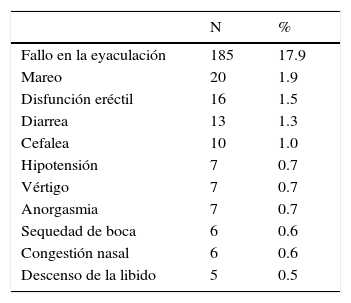
Datos sobre seguridadEl perfil de seguridad de silodosina observado en este ensayo «en la vida real» es totalmente comparable con el observado en los estudios de registro. La mayoría de los efectos secundarios como mareos, hipotensión y vértigo fueron extremadamente raros (tabla 5); el acontecimiento adverso más relevante, reportado por un 17,9% de los pacientes, fue el de trastorno de la eyaculación. Este efecto secundario fue notificado especialmente por los pacientes menores de 65 años (25,1%), mientras que se observó con menos frecuencia en pacientes mayores de 75 años. Sin embargo, es importante señalar que los trastornos de la eyaculación no fueron percibidos por los pacientes como un problema grave, y esto fue confirmado por la baja tasa de abandono en el ensayo (2,4%)31.
Acontecimientos adversos en los pacientes que recibieron tratamiento con silodosina en el estudio SiRE
| N | % | |
|---|---|---|
| Fallo en la eyaculación | 185 | 17.9 |
| Mareo | 20 | 1.9 |
| Disfunción eréctil | 16 | 1.5 |
| Diarrea | 13 | 1.3 |
| Cefalea | 10 | 1.0 |
| Hipotensión | 7 | 0.7 |
| Vértigo | 7 | 0.7 |
| Anorgasmia | 7 | 0.7 |
| Sequedad de boca | 6 | 0.6 |
| Congestión nasal | 6 | 0.6 |
| Descenso de la libido | 5 | 0.5 |
Fuente: Adaptado de Montorsi et al.31
Una de las principales preocupaciones en los pacientes tratados con alfabloqueantes es la seguridad cardiovascular; sin embargo, en este ensayo, la silodosina confirmó la ausencia de cambios significativos en la presión arterial sistólica y diastólica o en la frecuencia cardiaca31.
En general, los resultados del ensayo SiRE confirman los previamente demostrados en ensayos de registro. Silodosina de 8mg es altamente eficaz en la mejoría de los STUI en todos los grupos de edad, con independencia de las enfermedades/medicamentos concomitantes; además, silodosina disminuye marcadamente los STUI/HBP más molestos, como la nicturia, la frecuencia o el vaciado incompleto. Silodosina presenta también una buena tolerabilidad: es la anaeyaculación el acontecimiento adverso más frecuente, especialmente comunicado por los pacientes más jóvenes, pero no está asociada con un aumento en la tasa de abandono31.
Conclusiones- -
Los alfabloqueantes representan el tratamiento de elección en pacientes con STUI moderados-severos secundarios a HBP.
- -
El concepto de «uroselectividad» hace referencia a la mayor o menor afinidad que tienen los alfabloqueantes sobre el subtipo de receptor α1A (que es el que predomina a nivel del tracto urinario inferior) para conseguir los efectos beneficiosos (mejoría de los STUI) con un mejor perfil de seguridad.
- -
Silodosina actualmente es el alfabloqueante más uroselectivo sobre los receptores α1A; uroselectividad que ha sido confirmada en diversos estudios tanto in vitro como in vivo.
- -
Silodosina comparada con tamsulosina presenta una mejora significativa cuando se analizan conjuntamente 3de los síntomas más molestos de la HBP: nicturia, frecuencia miccional y vaciado incompleto.
- -
Tanto los estudios de registro de silodosina como el estudio realizado en «la vida real» han confirmado la eficacia y la seguridad de este fármaco en el tratamiento de los pacientes con STUI. En particular, silodosina se muestra eficaz en todos los grupos de pacientes, independientemente de su edad y del volumen de la próstata y se puede administrar con seguridad en aquellos que presenten varias comorbilidades y medicamentos concomitantes. El acontecimiento adverso observado con más frecuencia es la anaeyaculación, comunicada con mayor frecuencia por los pacientes más jóvenes, pero no se asociaba con un aumento de la tasa de abandono.
No se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesEl Dr. Alcántara es miembro del Grupo de Trabajo de Urología (Nefrología y Vías Urinarias) de la Sociedad Española de Médicos de Atención Primaria (SEMERGEN).