Introducción: Es bien conocido que el espesor del colgajo corneal en cirugía de LASIK es determinante en el riesgo de ectasia corneal, el propósito del presente estudio es evaluar el espesor del colgajo corneal planeado vs el posoperatorio (medido) con cuatro diferentes sistemas de corte.
Material y métodos: Ciento veinte ojos de 60 pacientes se sometieron a cirugía de LASIK. Grupo a: 30 ojos, utilizando el microqueratomo Hansatome para crear un colgajo corneal de 160 µm. Grupo b: 30 ojos, utilizando el microqueratomo BD K-3000 para crear un colgajo corneal de 130 µm. Grupo c: 30 ojos utilizando el láser de femtosegundos para crear un colgajo corneal de 100 µm. Grupo d: 30 ojos utilizando el microqueratomo Amadeus II para crear un colgajo corneal de 140 µm. Se realizó un escaneo del espesor central con el microscopio confocal, a las dos semanas después de la cirugía.
Resultados: Las mediciones de los espesores de los colgajos corneales fueron las que a continuación se presentan. Grupo a: 148.5 ±20.3 µm (para un espesor planeado de 160 µm), grupo b: 110.5 ±12.9 µm (para un espesor planeado de 130 µm), grupo c: 113 ± 13.7 µm (para un espesor planeado de 100 µm) y grupo d: 135 ±12.9 µm (para un espesor planeado de 140 µm).
Conclusiones: Existen variaciones pequeñas en el espesor del colgajo corneal de todos los sistemas de corte estudiados, que deben de ser tomados en cuenta para la ablación en cirugía de LASIK.
Background: Is well known that the corneal flap thickness in LASIK surgery is a risk factor to determine a corneal ectasia, the purpose of this study is to determine corneal flap thickness planed vs measured after LASIK with four different systems to create the flap.
Material and methods: One hundred and twenty eyes of 60 patients underwent LASK. Group A: 30 eyes by using the Hansatome microkeratome to create a 160 µm corneal flap; Group B: 30 eyes by using a BD K-3000 microkeratome to create a 130 µm corneal flap; Group C: 30 eyes by using the Femtosecond surgical laser to create a100 µm corneal flap; and Group D: 30 eyes by using the Amadeus II to create a 140 µm corneal flap. A central scan of the total corneal thickness was taken with the confocal microscope at 2 weeks and 1 month after surgery.
Results: Corneal flap thickness measurements were Group A: 148.5 ±20.3 µm (for a planed 160 µm flap thickness), group b: 110.5 ±12.9 µm (for a planed 130 µm flap thickness), group c: 113 ±13.7 µm (for a planed 100 µm flap thickness) and group d: 135 ±12.9 µm (for a planed 140 µm flap thickness).
Conclusions: There are smalls corneal flap thickness variations that must considered in for stromal ablation in LASIK surgery.
Introducción
La cirugía de LASIK (Laser in situ keratomileusis) es uno de los procedimientos aceptados y más utilizados para corregir errores refractivos, tales como miopía, astigmatismo o hipermetropía. En esta técnica se utiliza un sistema de corte para realizar un colgajo o flap corneal (keratomileusis), y un excimer láser para la fotoablación del estroma corneal, por debajo del colgajo corneal.1,2 El espesor del colgajo corneal es un factor para el cálculo del monto de la ablación a operar, y por ende, una condición importante para evitar complicaciones como el caso de la ectasia post-LASIK.3,4
Material y métodos
Se realizó cirugía de LASIK en 120 ojos de 60 pacientes, se dividieron en cuatro grupos dependiendo del sistema de corte que se utilizó para la realización del corte del colgajo corneal. Grupo a: 30 ojos, se utilizó el microqueratomo Hansatome (Chiron Vision Corp®, Claremont, California, USA), para crear un corte de 160 µm de espesor; grupo b: 30 ojos, se utilizó el microqueratomo BD K-300 (B-D Ophthalmic Systems®, Milford, USA), para crear un corte de 130 µm de espesor; grupo c: 30 ojos, se utilizó el láser de femtosegundos a 60 kHz (Intralase Corp®, Irvine, California, USA), para crear un corte de 100 µm de espesor; grupo d: 30 ojos, se utilizó el microqueratomo Amadeus II (Surgical instruments systems®, Switzerland), para crear un corte de 140 µm de espesor.
La ablación estromal se realizó en todos los pacientes con el sistema de excimer láser VISX STAR S4 (VISX®, Santa Ana, California). El promedio de refracción preoperatorio fue -4.45 ±1.58 Dioptrías (D) de equivalente esférico. El tratamiento posoperatorio fue mediante el uso tópico de la combinación de tobramicina y dexametasona (TOBRADEX®, Alcon Laboratorios, Forth Worth, TX, USA), a razón de una gota tres veces al día por dos semanas.
Se realizó examen de microscopía confocal in vivo a las córneas operadas de todos los pacientes a las dos semanas del posoperatorio, mediante el uso del microcopio confocal de hendidura (Confisca 4®, Fortune Technologies, Vigonza, Italy), obteniendo una secuencia de imágenes digitalizadas (JPEG), que consta de dos rastreos consecutivos de la profundidad total del espesor corneal, siendo un rastreo equivalente a la obtención de imágenes de endotelio a epitelio y nuevamente a endotelio, es decir, de lo posterior a lo anterior y de nuevo a lo posterior, para permitir el desplazamiento en el eje "Z" del espesor corneal central. Las imágenes son capturadas automáticamente en el disco duro (CPU) de una computadora para su posterior análisis, mediante el uso del programa Navis v. 3.5.0. (NIDEK®, Multi-Instrument Diagnostic System, Japan). El espesor del los colgajos corneales se midió evaluando la distancia en µm, entre el epitelio superficial y la interfase del colgajo corneal.
Análisis estadístico
Se utilizaron medias y desviaciones estándar. Se realizó un análisis de Bland y Altman, para obtener las diferencias de los espesores de los colgajos cornéales obtenidos, menos los deseados contra el promedio de ambos, en cuatro diferentes sistemas de creación del colgajo corneal.
Resultados
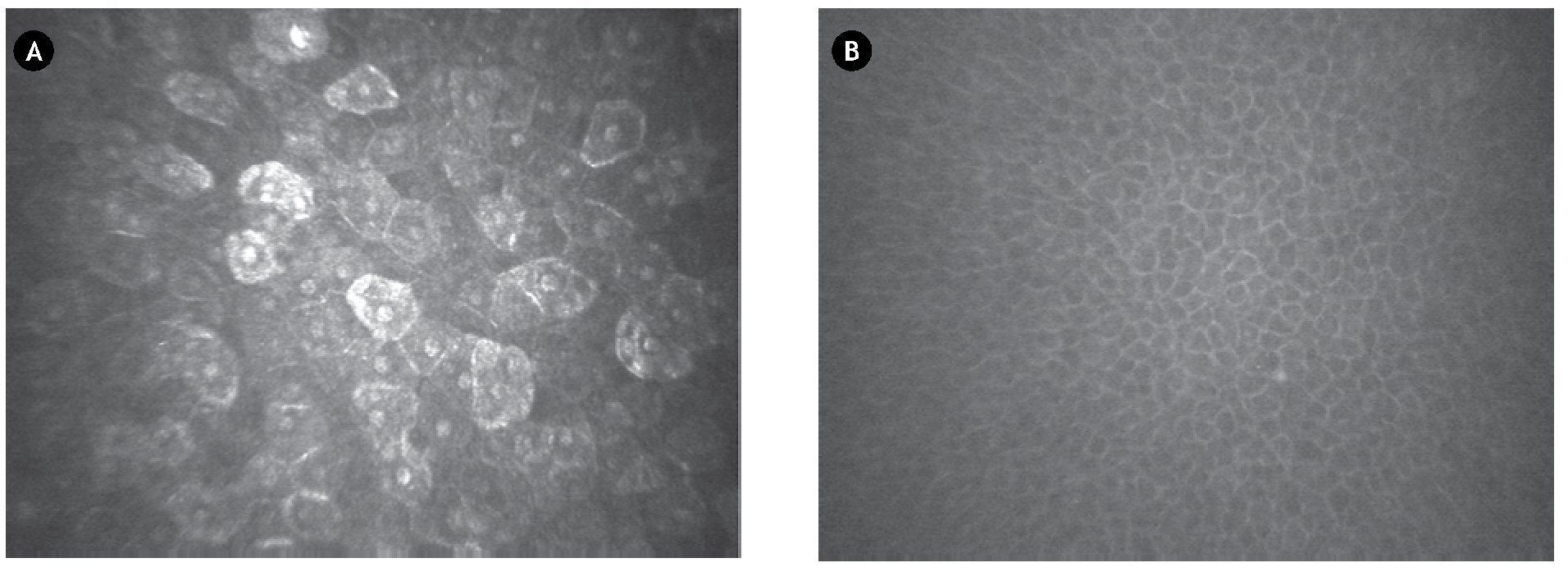
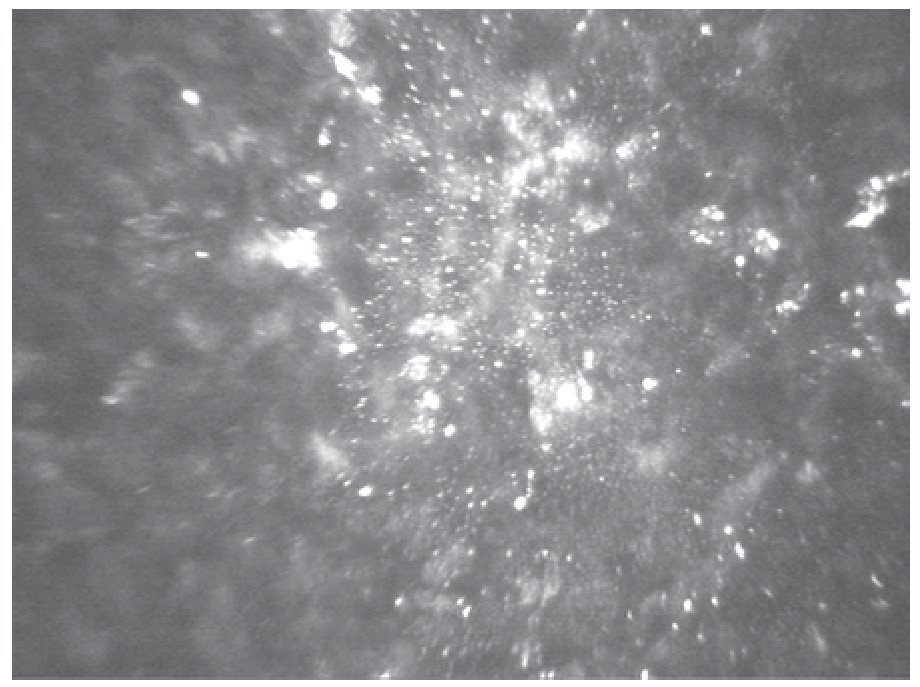
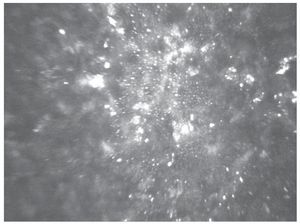
A nivel del epitelio superficial así como las células basales epiteliales, los hallazgos fueron de características morfológicas normales en todas las córneas evaluadas (Figuras 1A y 1B), el plexo nervioso subepitelial fue ausente en todos los ojos examinados (Figura 2). La porción estromal del colgajo corneal presentó queratocitos de características morfológicas normales en todos los casos. La interfase del colgajo corneal fue posible localizar en todos los casos, mediante la observación de pequeñas partículas hiperreflécticas en todas las córneas evaluadas (Figura 3).
Figura 1. A) Fotografía de microscopía confocal del epitelio superficial de la córnea de características normales (340 x 255 µm). B) Fotografía de microscopía confocal de células basales epiteliales de la córnea de características normales (340 x 255 µm).
Figura 2. Fotografía de microscopía confocal a nivel subepitelial, en la que se aprecia la ausencia del plexo nervioso subepitelial (340 x 255 µm).
Figura 3. Fotografía de microscopía confocal de la interfase del colgajo corneal, en la que se aprecian queratocitos activados y partículas hiperreflécticas (340 X 255 µm).
Las mediciones de los espesores de los colgajos corneales fueron las siguientes, grupo a: 148.5 ±20.3 µm (para un espesor planeado de 160 µm), grupo b: 110.5 ±12.9 µm (para un espesor planeado de 130 µm), grupo c: 113 ±13.7 µm (para un espesor planeado de 100 µm) y grupo d: 135 ±12.9 µm (para un espesor planeado de 140 µm).
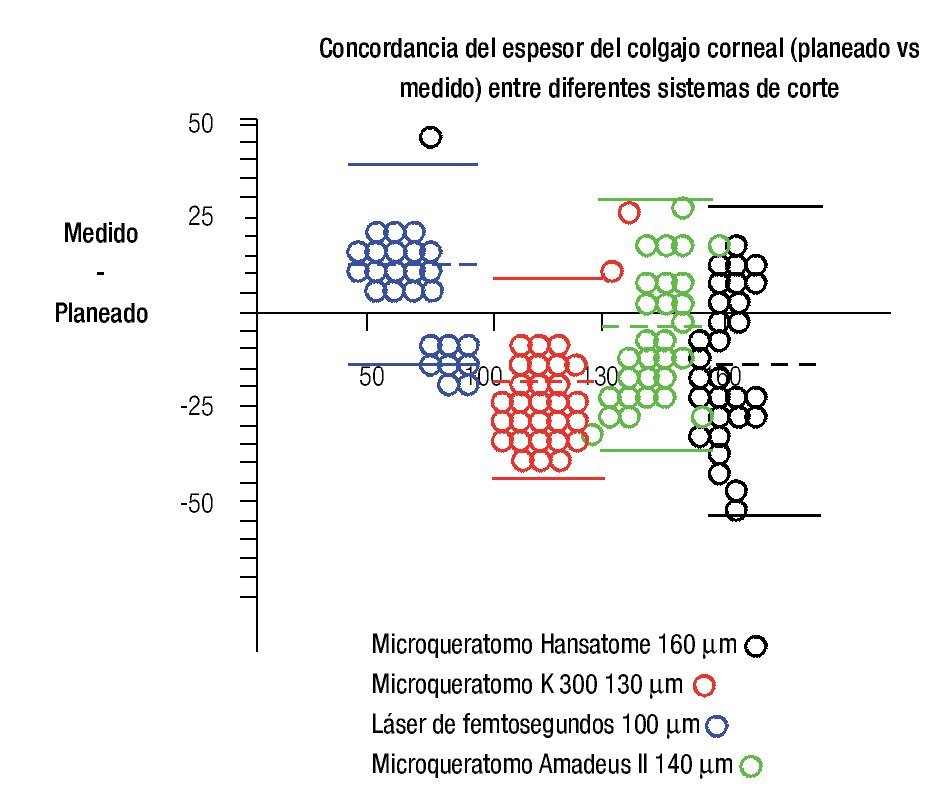
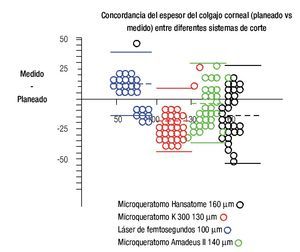
El análisis de Bland y Altman mostró las siguientes diferencias promedio, entre el espesor obtenido menos el planeado, grupo a: -13.66 ±20.35 µm, grupo b: -18.32 ±12.89 µm, grupo c: 10.92 ±13.75 y grupo d: -4.79 ±16.49. Se observó una mejor precisión promedio del microquera- tomo Amadeus II (grupo d). El método de corte que mostró una menor variación fue el microqueratomo K-3000 (grupo b), donde el 95% de los casos se encontraron entre 84.7 y 136 µm (Figura 4).
Figura 4. Análisis de Bland y Altman en la que se observa la diferencia del obtenido menos el deseado contra el promedio de ambos, en cuatro diferentes sistemas de creación del colgajo corneal. Se evidencia una mejor precisión promedio del microqueratomo Amadeus II. El método de corte que mostró una menor variación fue el microqueratomo K-3000, donde el 95% de los casos se encontraron entre 84.7 y 136 µm.
Discusión
Estudios previos de microscopía confocal han descrito epitelio corneal normal, así como la ausencia de plexo nervioso subepitelial en estadios tempranos del posoperatorio de LASIK y la recuperación de éste en el centro de la córnea, hasta los seis meses después de la cirugía.5,6 En el presente estudio, se observó la misma ausencia del plexo nervioso subepitelial a las dos semanas del posoperatorio. El hallazgo y detección por microscopía confocal de partículas hiperreflecticas, a nivel de la interfase del colgajo corneal en córneas posoperadas de LASIK, se ha descrito ampliamente en la literatura médica.6,7 Existen varias teorías que explican la presencia de dichas partículas a nivel de la interfase corneal, como partículas remanentes en la navaja del microqueratomo,8 o restos de las esponjas de merocel que fueron expuestas a la ablación por el excimer láser.9 Este tema ha sido resuelto últimamente por Dawson, quien realizó un estudio de microscopía confocal en el cual hizo una correlación histopatológica de estas partículas en la interfase corneal después de LASIK, en el que sugiere que se tratan de restos de colágena fragmentada y colapsada por el corte, al realizar el colgajo corneal.10 Esta teoría es la más aceptada y fue soportada en un reporte posterior, que compara la interfase corneal de colgajos de 160 µm de espesor realizados en un ojo con microqueratomo y en el contralateral con láser de femtosegundos. En ese estudio se demuestra la presencia estas partículas después de LASIK con ambos equipos, asimismo, el número de estas partículas en la interfase no mostró diferencia estadísticamente significativa en el comparativo del posoperatorio de los dos equipos (microqueratomo y láser de femtosegundos).11
La importancia de la reproducibilidad así como la predictibilidad en el espesor del flap corneal en cirugía de LASIK, está directamente relacionada al riesgo de ectasia corneal inducida,12 aunado al dejar una cama estromal residual de más de 250 µm después de la ablación, mediante el sistema de excimer láser.13
Estudios previos reportan mediciones del espesor del colgajo corneal con diferentes sistemas de corte,14 presentando variaciones semejantes a las encontradas en el presente estudio que van de entre 4.6 µm15 hasta 20 µm,16 comparados con los espesores planeados, incluyen estudios realizados mediante paquimetría ultrasónica,17,18 tomografía óptica coherente (OCT),19 así como microscopía confocal.20,21
En el presente estudio, el único no multicéntrico que involucró cuatro diferentes sistemas de corte, se pudo demostrar que la predictibilidad del espesor del colgajo corneal en los sistemas estudiados no varía más de 20 µm de diferencia, comparados con el espesor planeado, siendo el más predecible el microqueratomo Amadeus II (grupo d), con una variación en promedio de menos de 5 µm (-4.79 µm). El menos predecible fue el microqueratomo BD K-3000, presentando una variación con respecto al espesor planeado de 18.32 µm, aunque paradójicamente le proporciona más seguridad, puesto que esta variación es más delgada en espesor con respecto al planeado (-18.32 µm, planeado de 130 µm vs obtenido de 110.5 ± 12.9 µm). Este fue el microqueratomo que presentó la mayor reproducibilidad en la medición obtenida (posoperatoria).
Conclusiones
1. Los cuatro sistemas de corte presentan variación discreta, con respecto al espesor del colgajo corneal planeado.
2. Las variaciones en la predictibilidad del espesor del colgajo corneal deben de ser tomadas en cuenta para dar margen a la ablación estromal, y así disminuir el riesgo de ectasia corneal inducida.
Correspondencia:
Acad. Dr. Manuel Ramírez Fernández,
Servicio de Córnea y Cirugía Refractiva, Asociación para Evitar la Ceguera en México, Hospital "Dr. Luis Sánchez Bulnes",
Vicente García Torres 46, Colonia San Lucas, Delegación Coyoacán,
C.P. 04030. México D.F., México.
Teléfono: 5666 3383. Celular: (04455) 5400 0579.
Correos electrónicos: mramirezf@medicasur.org.mx, mramirez-f@prodigy.net.mx