Presentamos 2 casos de edema de papila en el contexto de un GPCAA: el primero, una congestión de disco óptico con resolución completa y buena agudeza visual tras la normalización de la PIO, y el segundo una NOIAA con evolución a atrofia de papila y agudeza visual de no percepción luminosa.
DiscusiónLa coexistencia de edema de papila y PIO elevada puede deberse, bien a la congestión del nervio óptico secundaria a un GPCAA, bien a una NOIA concomitante, por lo que es de gran relevancia hacer un correcto diagnóstico diferencial en relación con su evolución clínica y morfológica.
We present 2 cases of optic disc edema in the context of an APCG, the first one is an optic disc swelling with complete resolution and good visual acuity after the regularization of the IOP, and the second one is an AAION leading to optic atrophy and visual acuity of no light perception.
DiscussionThe coexistence of optic disc edema and high IOP might be caused by an optic disc swelling secondary to APCG or by an AION associated, so is very important to make a correct differencial diagnosis depending on its clinical and morphological follow-up.
La congestión de papila tras glaucoma primario por cierre angular agudo (GPCAA) es una de las alteraciones asociadas a dicho cuadro, junto con la atrofia óptica, neuropatía óptica isquémica anterior no arterítica (NOIANA), hemorragia vítrea y retinopatía por descompresión ocular1. Presentamos 2 casos de edema de disco óptico en un GPCAA y el diagnóstico diferencial con NOIANA y neuropatía óptica isquémica anterior arterítica (NOIAA).
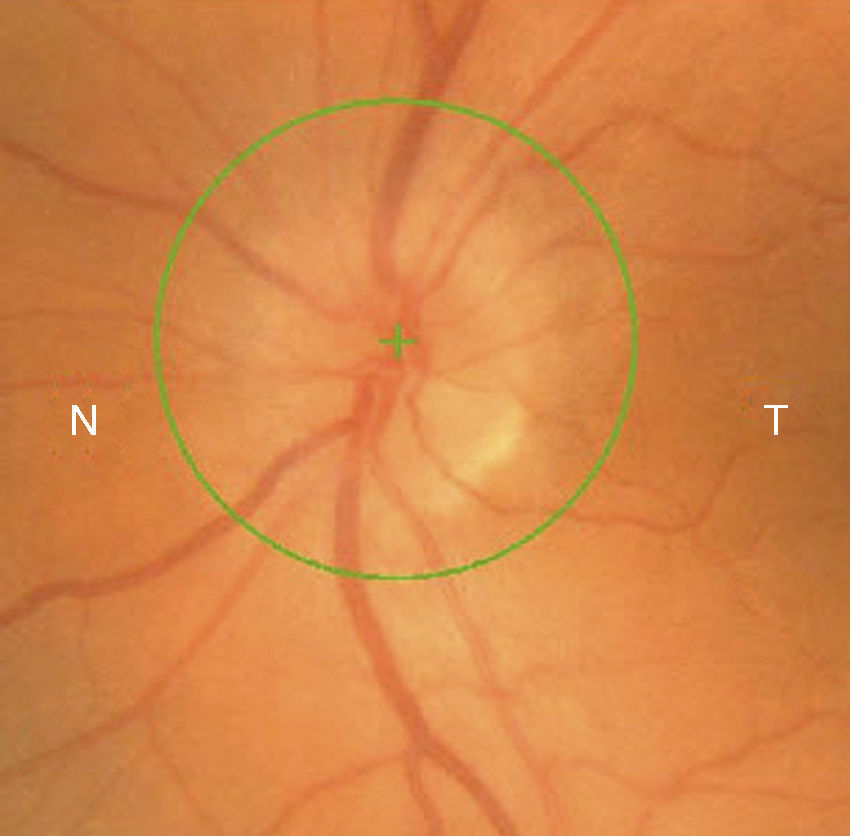
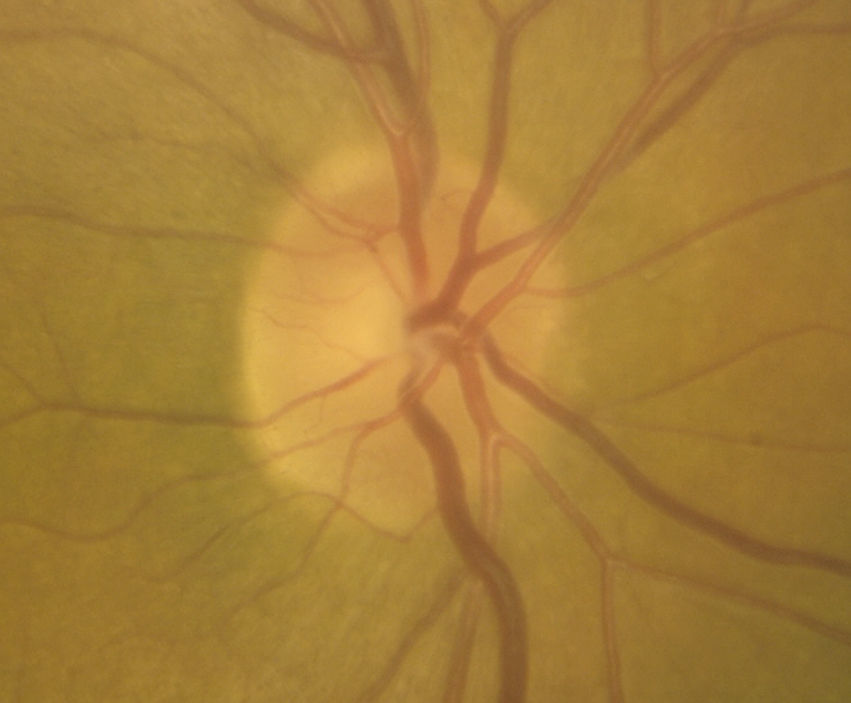
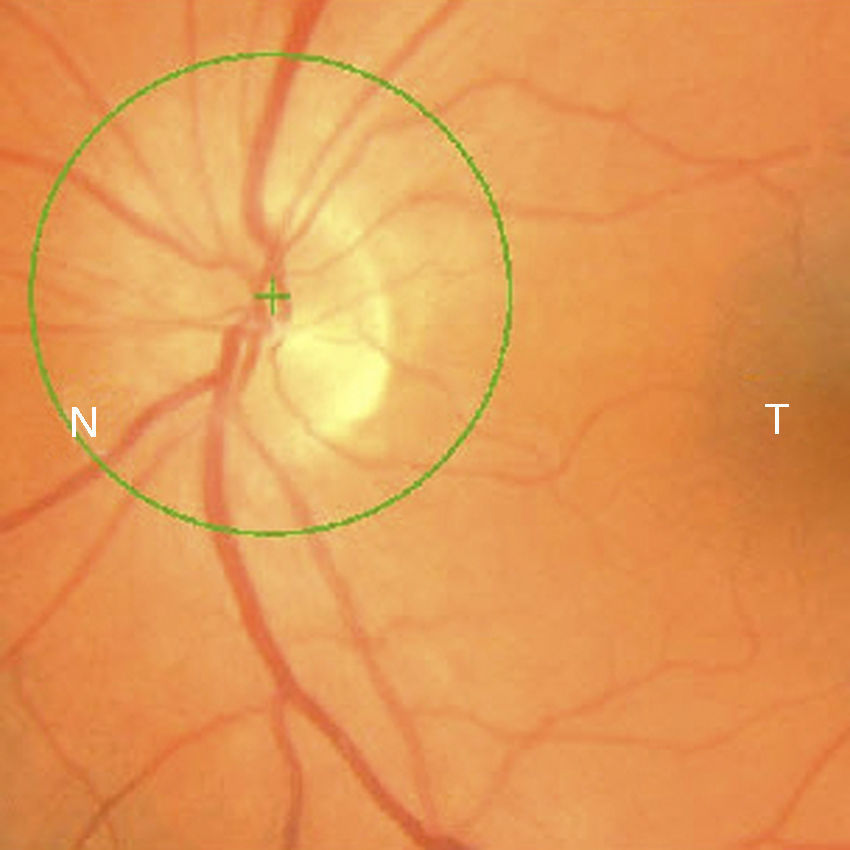
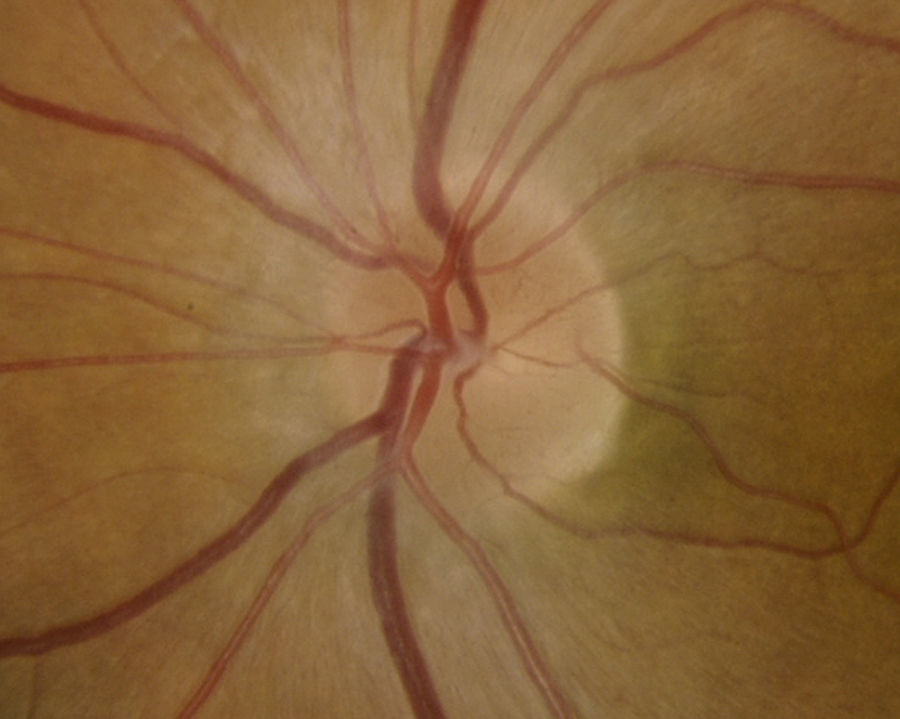
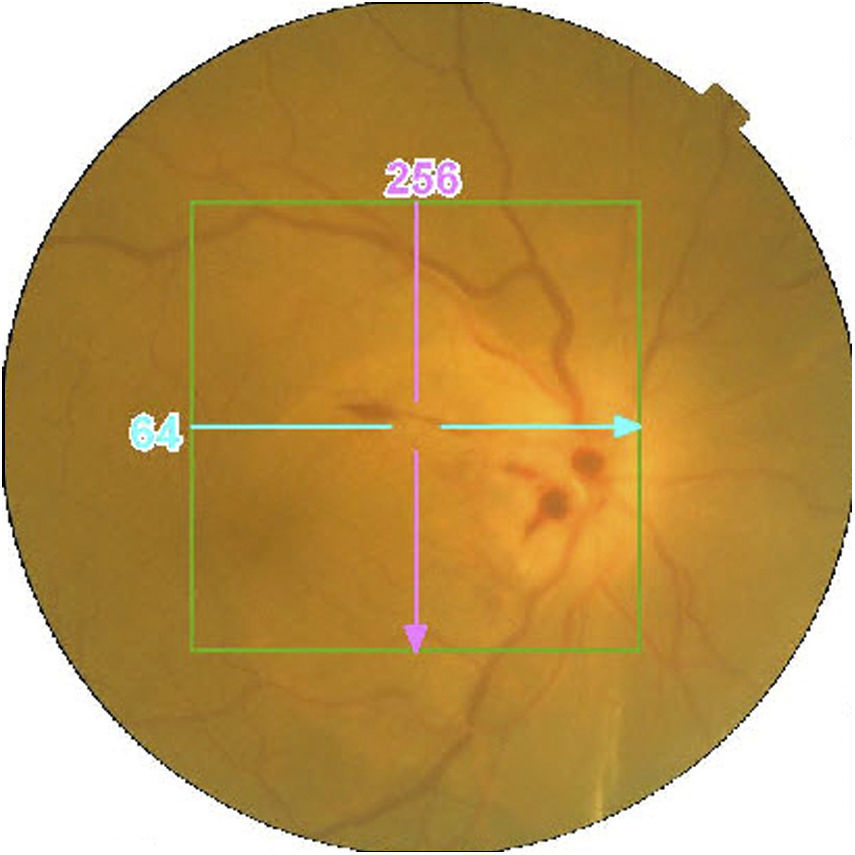
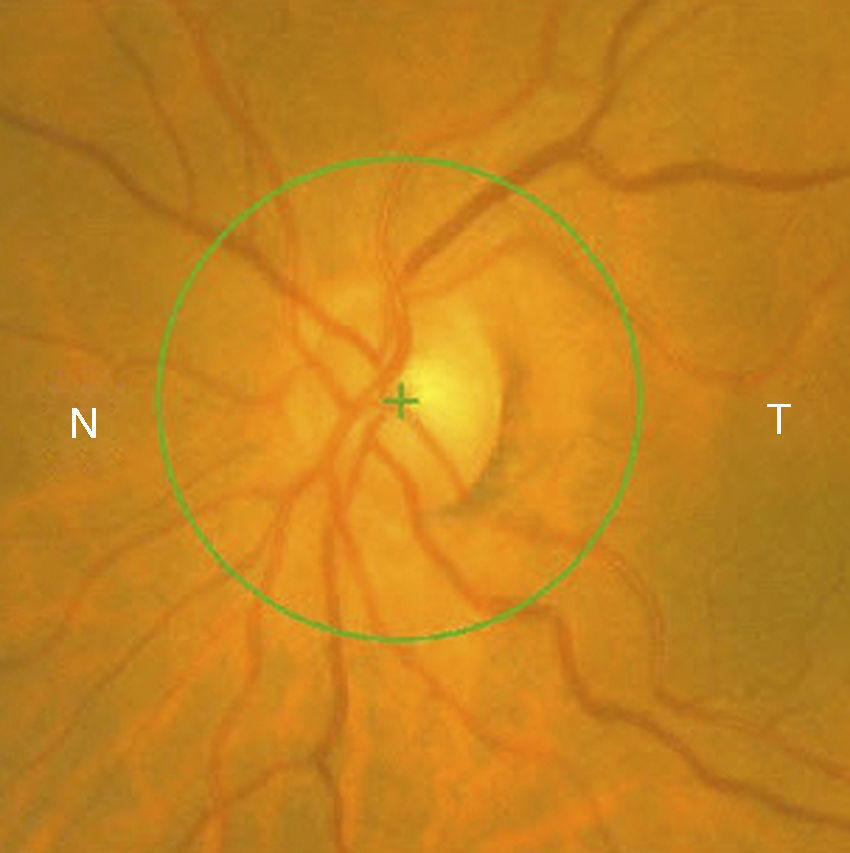
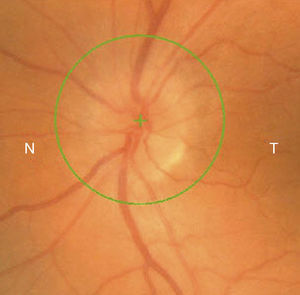
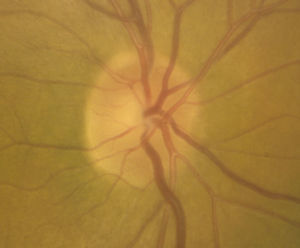
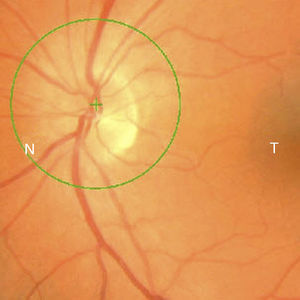
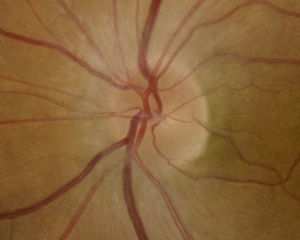
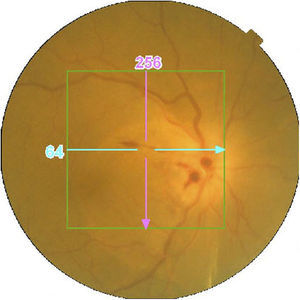
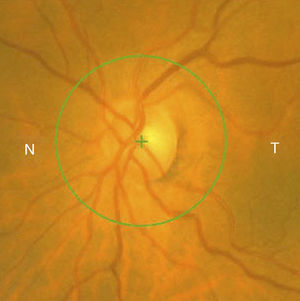
Casos clínicosCaso 1Mujer de 56 años refiere pérdida de visión dolorosa del ojo izquierdo (OI) de 24h de evolución. Hipermétrope de +5. La agudeza visual (AV) del ojo derecho (OD) es de 20/20 y la del OI de movimiento de manos (mm). La biomicroscopia del OI muestra edema epitelial, cámara anterior grado i (clasificación de van Herick), midriasis arreactiva, presión intraocular (PIO) de 64mmHg y edema de papila (fig. 1). La papila del OD tiene una relación excavación/papila (E/P) de 0.1 (fig. 2). Es tratada con colirios de tobramicina-dexametasona, carteolol hidrocloruro 2%, apraclonidina hidrocloruro 1% y brinzolamida, y con 2 perfusiones intravenosas de 250cc de manitol 20%, obteniéndose una PIO de 45mmHg. Se realizan iridotomías a las 10 y a las 2h, reduciendo la PIO a 15mmHg. A la semana disminuye el edema de papila con AV en el OI de 20/30 (fig. 3). Al mes se realiza facoemulsificación del cristalino e implante de lente intraocular. Se observa resolución del edema de papila con coloración normal del disco óptico y AV en el OI final de 20/25 (fig. 4).
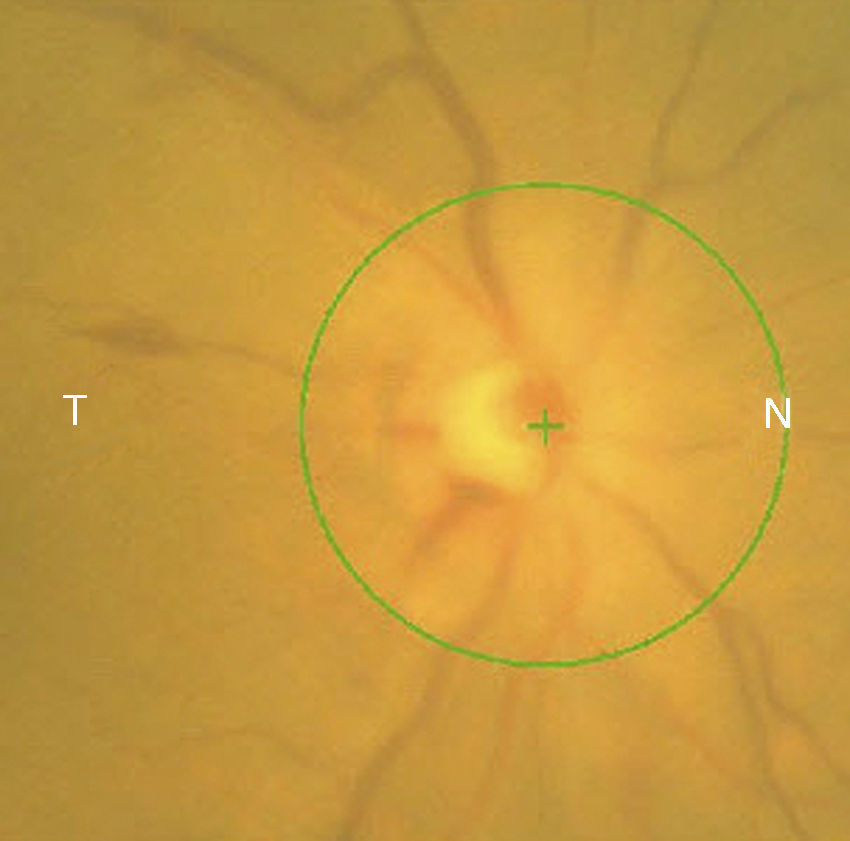
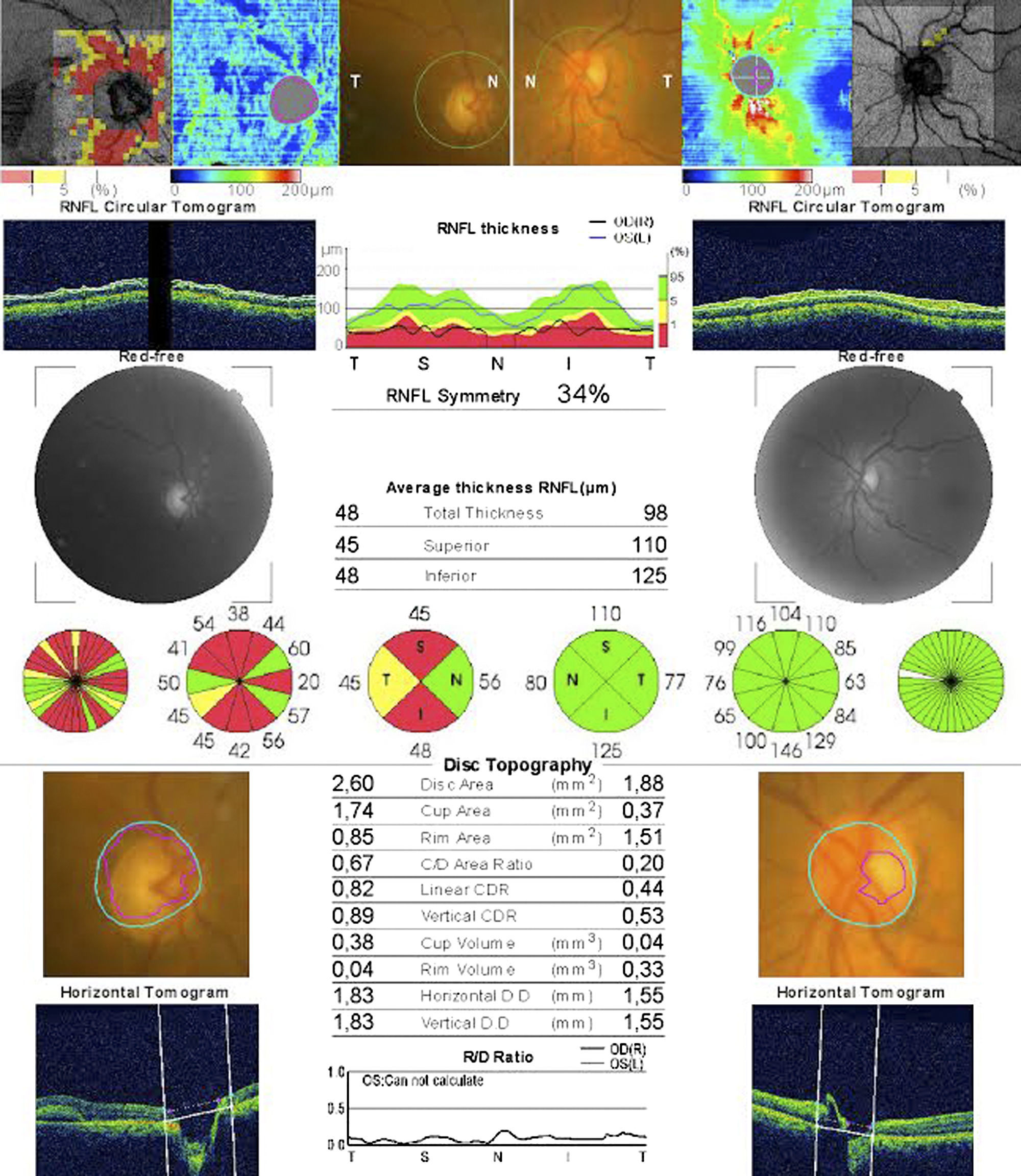
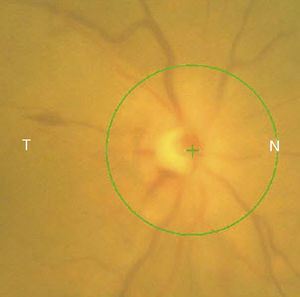
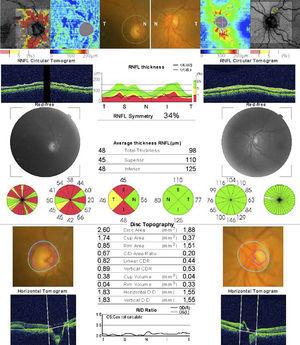
Caso 2Mujer de 78 años ingresada por colitis ulcerosa en tratamiento con metilprednisolona intravenosa 16mg/8h durante 4 días refiere pérdida de visión del OD de 3 días de evolución asociada a cefalea hemicraneal derecha. Antecedentes de insuficiencia renal e hipermetropía de +2.25 y +1.25. La AV en el OD es de percepción luminosa. La AV en el OI es de 20/25. La biomicroscopia del OD muestra córnea transparente, cámara anterior grado i, midriasis arreactiva, PIO de 40mmHg y edema de papila con hemorragias en llama (fig. 5). La velocidad de sedimentación globular es de 85mm/h y la proteína C reactiva de 110mg/L. El disco del OI tiene una E/P de 0.3 (fig. 6). Se trata con colirios de brinzolamida y carteolol hidrocloruro 2%. El manitol está contraindicado por la insuficiencia renal. Al día siguiente hay menos hemorragias pero persiste el edema (fig. 7). La PIO es de 40mmHg. Las iridotomías se realizan una semana después por su mal estado general. A los 10 días la AV en el OD es de no percepción luminosa. Al mes se aprecia atrofia de papila, disminución de la capa de fibras nerviosas retinianas (CFNR) y E/P 0.′8, sin palidez del anillo neurorretiniano (ANR) (fig. 8).
El edema de disco óptico congestivo tras un GPCAA puede tener lugar en la primera semana tras el proceso de aumento de PIO y previo a la excavación definitiva del nervio2, siendo el mecanismo del daño óptico de tipo isquémico.
Sin embargo, tras un único episodio de GPCAA no suele haber alteración del disco a no ser que la PIO esté elevada al menos una semana3. Sí hay palidez del disco óptico en aquellos casos en los que el intervalo es largo hasta la resolución de la PIO, y además se correlaciona con aumento de la relación E/P, disminución del área media del ANR, pérdida de CFNR y alteración del campo visual3.
La NOIANA precipitada por GPCAA ha sido descrita en la literatura en escasas ocasiones2,4,5. Puede ser debida a la obliteración de los vasos coroideos peripapilares en la región prelaminar del disco debido al aumento de PIO en un disco óptico de riesgo2,4,5.
El riesgo de NOIANA no se debe tanto al área del disco (es decir, discos ópticos pequeños) sino a un área de la excavación y una relación E/P pequeñas6.
A los 6 meses tras un episodio de NOIANA no suele haber aumento de la relación E/P3 y sí se suele observar palidez del ANR5,7.
La pérdida de la CFNR suele ser mayor en ojos con glaucoma que en ojos con neuropatía óptica isquémica anterior (NOIA)8. Los pacientes con NOIANA tienen menor cantidad de CFNR porque su disco óptico suele ser más pequeño8. El grado de profundidad de la excavación también es mayor en el glaucoma que en la NOIA, debido a una mayor afectación de la zona posterior de la lámina cribosa (zona laminar) en los primeros.
En el caso 1 se aprecia una congestión de disco óptico en el contexto de una PIO elevada en una papila de riesgo (E/P 0.1). El restablecimiento de la PIO a valores normales tiene lugar en un período inferior a una semana por lo que no se produce un daño definitivo del nervio óptico (pérdida de CFNR, aumento de la E/P y palidez del nervio óptico). La ausencia de excavación tras el proceso así como la presencia de un disco de riesgo podría hacer pensar en una NOIANA3 pero el color rosado del ANR y la ausencia de atrofia óptica orientan hacia una congestión de disco precipitado por un GCAA4,5,7.
En el caso 2 observamos un edema de papila del OD en el contexto de una PIO elevada. En el glaucoma, la pérdida de CFNR suele ser difusa, apareciendo también en los cuadrantes en los que no hay daño funcional, mientras que la pérdida de la CFNR en la NOIANA suele limitarse al cuadrante más afectado8. Los cambios estructurales que se aprecian al mes en la papila de la paciente son un aumento de la relación E/P y una pérdida de la CFNR media total con predominio de los polos superior y posterior, sin palidez franca del ANR y en ausencia de una papila de riesgo (E/P 0.3), lo que nos hace desestimar una NOIANA donde no suele haber aumento de la relación E/P y sí palidez del disco2,5,7.
Se realiza el diagnóstico diferencial entre una neuropatía óptica glaucomatosa o una NOIAA, en la que el adelgazamiento del ANR, la excavación y la relación E/P suelen ser mayores que en la NOIANA8.
Las características de la papila junto a una PIO de 40mmHg mantenida durante una semana orientan hacia un edema en el contexto de un GPCAA con evolución a atrofia óptica. Pero dada la mala evolución funcional y que la paciente cumple 3 de los 5 criterios de la American College of Rheumatology para la arteritis de células gigantes, esto es, edad mayor de 50 años, cefalea localizada de inicio reciente y aumento de velocidad de sedimentación globular por encima de 50mm/h9, se establece el diagnóstico definitivo de NOIAA.
ConclusionesEl edema de papila es un signo poco frecuente de daño óptico en el contexto de un GPCAA. Cuando la PIO se restituye a valores normales en un intervalo inferior a una semana, la congestión desaparece y el ANR alcanza una coloración normal.
El daño morfológico del nervio óptico tiene lugar cuando la PIO se mantiene elevada durante más de una semana. Se produce un aumento de la excavación y de la relación E/P y una pérdida difusa de la CFNR.
Es importante realizar el diagnóstico diferencial de edema de papila en el contexto de una PIO elevada con la NOIAA y la NOIANA.
La NOIANA desencadenada por un GPCAA es poco frecuente. Para su diagnóstico se debe tener en cuenta la presencia o no de una papila de riesgo. El edema de papila suele ser de tipo congestivo. No suele haber aumento de la relación E/P y sí palidez del ANR. La pérdida de la CFNR es de predominio inferior y tiene una correspondencia funcional con el campo visual más marcada que en el glaucoma.
En la NOIAA el edema de papila suele ser pálido y cursa con un aumento de la excavación, aumento de la relación E/P y palidez del ANR. Para su diagnóstico se deben tener en cuenta los criterios clínicos y bioquímicos de dicha entidad. Las enfermedades que cursan con velocidad de sedimentación globular y proteína C reactiva elevadas, como la enfermedad inflamatoria intestinal, pueden hacer retrasar el diagnóstico de NOIAA, con resultados devastadores para el paciente.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.