El tratamiento médico de pacientes con colitis ulcerosa se basa en aminosalicilatos, corticoides, inmunomoduladores y en los últimos años en terapia biológica predominantemente con anti-TNF. La falla de este tratamiento, efectos adversos de los fármacos o complicaciones de la enfermedad, incluyendo el desarrollo de neoplasias, pueden llevar al paciente a requerir un tratamiento quirúrgico. Este procedimiento, habitualmente en etapas, consiste en la extirpación de colon y recto. En caso de urgencia, se procede inicialmente a la colectomía subtotal con ileostomía, para luego resecar el recto en forma electiva. Para evitar una ileostomía definitiva, el procedimiento de elección es la reconstitución del tránsito intestinal con reservorio ileal. En centros especializados, esta operación de alta complejidad se puede realizar con tasas de complicaciones razonables y con una baja mortalidad. La calidad de vida de los pacientes operados es en general adecuada, y la gran mayoría volvería a someterse al procedimiento si tuviera que elegir nuevamente.
Medical treatment of ulcerative colitis is based on aminosalicylates, corticosteroids, immunomodulators and lately biological therapy mainly with anti-TNF antibodies. Failure of these treatments, adverse effects of the medication, or disease-related complications including neoplasia may take the patient to require a surgical treatment which consists in a complete removal of colon and rectum, most frequently in a staged fashion. In urgent cases, subtotal colectomy with end ileostomy is performed, followed by an elective proctectomy later on. In order to avoid a permanent ileostomy, restorative surgery with an ileoanal pouch anastomosis (IPAA) is the procedure of choice. In specialized centers, this complex operation can be performed safely with an adequate complication rate and low mortality. Overall quality of life of patients with IPAA is adequate, and the vast majority of patients would undergo surgery again if they had to choose a second time.
La colitis ulcerosa (CU) forma parte de un grupo de enfermedades denominado enfermedad inflamatoria intestinal (EII), cuya etiología exacta aún se desconoce. Se caracteriza por una respuesta inmune inadecuada, en cuyo desarrollo influyen factores genéticos, ambientales y microbiológicos (microbiota). La CU específicamente se destaca por un compromiso intestinal que se limita a colon y recto, independiente del hecho que se puede acompañar de manifestaciones extraintestinales, como por ejemplo colangitis esclerosante primaria, artritis, afectaciones dermatológicas y oculares, entre otras. El tratamiento de la CU se basa en diferentes fármacos, desde 5-aminosalicilatos (5-ASA), corticoides, inmunomoduladores hasta tratamiento biológico con anti-TNF1, incluso en los últimos años se han usado anti-integrinas e inhibidores de JAK.
Dado que el compromiso intestinal de la CU se limita a colon y recto, el tratamiento quirúrgico puede ser curativo en la medida que se remueven ambos segmentos. Este tipo de tratamiento se considera de alta complejidad y conlleva complicaciones tempranas y tardías, además de interferir en la calidad de vida de los pacientes. Es por ello que hay que elegir cuidadosamente los pacientes, las condiciones de su enfermedad, el momento de una eventual intervención, y el tipo de procedimiento a realizar. Para garantizar un manejo óptimo para el paciente, es indispensable trabajar en el marco de un equipo multidisciplinario dedicado al tratamiento de EII, que dispone por un lado de suficiente conocimiento y experiencia, y por el otro de recursos humanos e institucionales adecuados para poder ofrecer al paciente el mejor tratamiento en cada etapa de su enfermedad. El propósito de este artículo es revisar en detalle las indicaciones quirúrgicas en pacientes con CU, los aspectos técnicos de los diferentes procedimientos disponibles, y sus resultados inmediatos y a largo plazo, tanto con respecto a eventuales complicaciones como a la calidad de vida de los pacientes.
Aspectos históricosHasta el comienzo de la década de los ‘70 del siglo pasado, el tratamiento quirúrgico disponible consistía en remover todo el colon y recto de los pacientes con CU refractarios al tratamiento médico. Con esta cirugía se logró disminuir la mortalidad de estos pacientes. Sin embargo, hubo un gran impacto en su calidad de vida dada la necesidad de una ileostomía permanente, cuyo manejo en esos años era aun más difícil que hoy en día2. Sobre ese trasfondo, un grupo de cirujanos liderado por el Dr. Alan Parks del Hospital St. Mark's en Londres desarrollaron una técnica de reconstitución de tránsito intestinal luego de una proctocolectomía, en base a un reservorio ileal que se conecta al canal anal, reportada por primera vez en 1978 en la revista British Medical Journal3. En la actualidad, este procedimiento representa el tratamiento quirúrgico de elección en pacientes con CU.
Indicaciones quirúrgicasFrente a un tratamiento farmacológico de CU cada vez más amplio y variado, algunas de las indicaciones quirúrgicos han sido modificadas. Lo que sigue vigente, son las indicaciones de colectomía de emergencia en pacientes que se encuentran inestables debido a complicaciones graves de la enfermedad como hemorragia digestiva baja masiva, perforación colónica con peritonitis, o megacolon tóxico. En estos casos, el tratamiento médico se debe limitar a terapia de soporte para estabilizar al paciente mientras se procede rápidamente a una colectomía total4.
La indicación quirúrgica de urgencia incluye a pacientes con crisis grave de colitis ulcerosa que no responden a tratamiento con corticoides intravenosos y a terapias de rescate como anti-TNF (infliximab) o calcineurínicos (ciclosporina/tacrolimus). En estos pacientes la evaluación multidisciplinaria es esencial. Esta debe ser diaria, permitiendo detectar oportunamente la falta de respuesta al tratamiento médico dentro de los primeros 3-5 días 5. Mientras más tiempo pasa antes de operar a un paciente con falta de respuesta, empeoran las condiciones clínicas del paciente, aumentan las complicaciones quirúrgicas y se prolonga la hospitalización.
Las indicaciones semi-electivas se dan en pacientes que responden parcialmente al tratamiento, pero no logran inducir remisión clínica, y en aquellos que inicialmente respondieron, pero cuya enfermedad se reactiva bajo tratamiento (corticodependencia sin opción de inmunomoduladores o biológicos, inmunorefractariedad sin opción a biológicos, falla primaria o secundaria a biológicos y/o moléculas pequeñas) 5.
Finalmente, las indicaciones electivas para la proctocolectomia restaurativa en CU, incluyen pacientes en quienes se diagnostican displasia irresecable endoscopicamente, o estadíos más avanzados como un adenocarcinoma de colon o recto. Por otro lado, aquellos pacientes que no pueden mantener su tratamiento por reacciones adversas o falta de recursos, pueden ser candidatos a tratamiento quirúrgico, al igual que pacientes que desean operarse1.
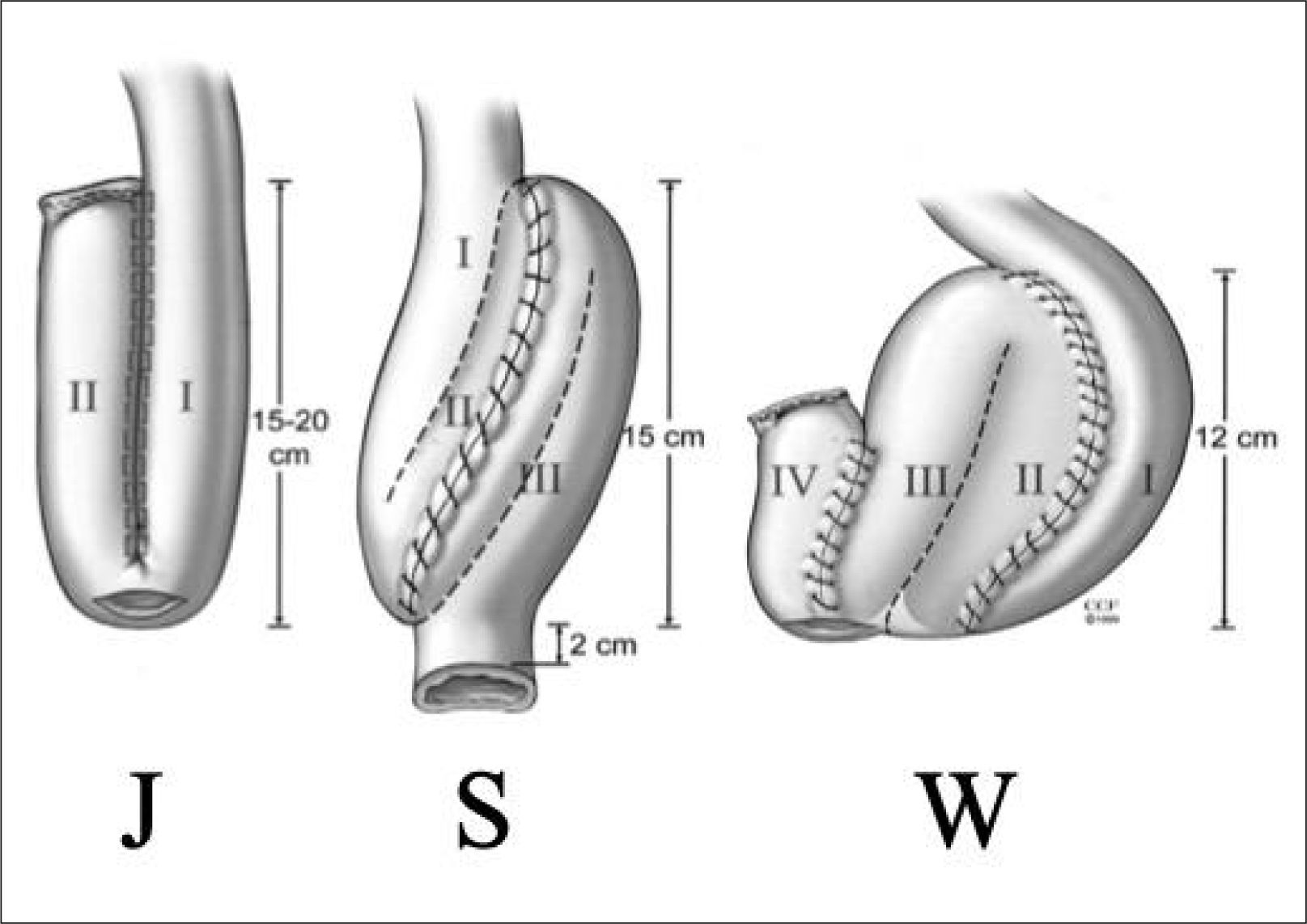
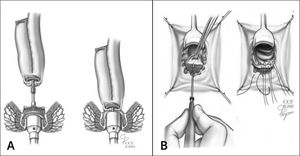
Proctocolectomía restaurativaLa operación de elección para el tratamiento de la CU entonces es la proctocolectomía restaurativa, lo que significa que luego de la extirpación completa de colon y recto se procura la reconstitución del tránsito por vía anal. Esto requiere la confección de un reservorio que logra reemplazar al menos parcialmente la función del colon y el recto, principalmente extraer agua y electrolitos del contenido intestinal para aumentar su consistencia, y almacenar la deposición hasta su defecación. Si bien el intestino delgado en general no es capaz de cumplir estas funciones en la misma medida que colon y recto, mediante la creación de un reservorio a partir del íleon terminal se consigue que el contenido intestinal aumente su consistencia y se almacene en ese reservorio antes de ser expulsado. Existen varias formas de confeccionar tal reservorio ileal. El reservorio original del Dr. Parks fue configurado en forma de W. En la actualidad, el que más se usa es el reservorio en J, cuya ventaja es que se puede confeccionar mediante corcheteras quirúrgicas (stapler lineal), lo que facilita el proceso y acorta los tiempos quirúrgicos (Figura 1). En ocasiones especiales se pude usar un reservorio en S.
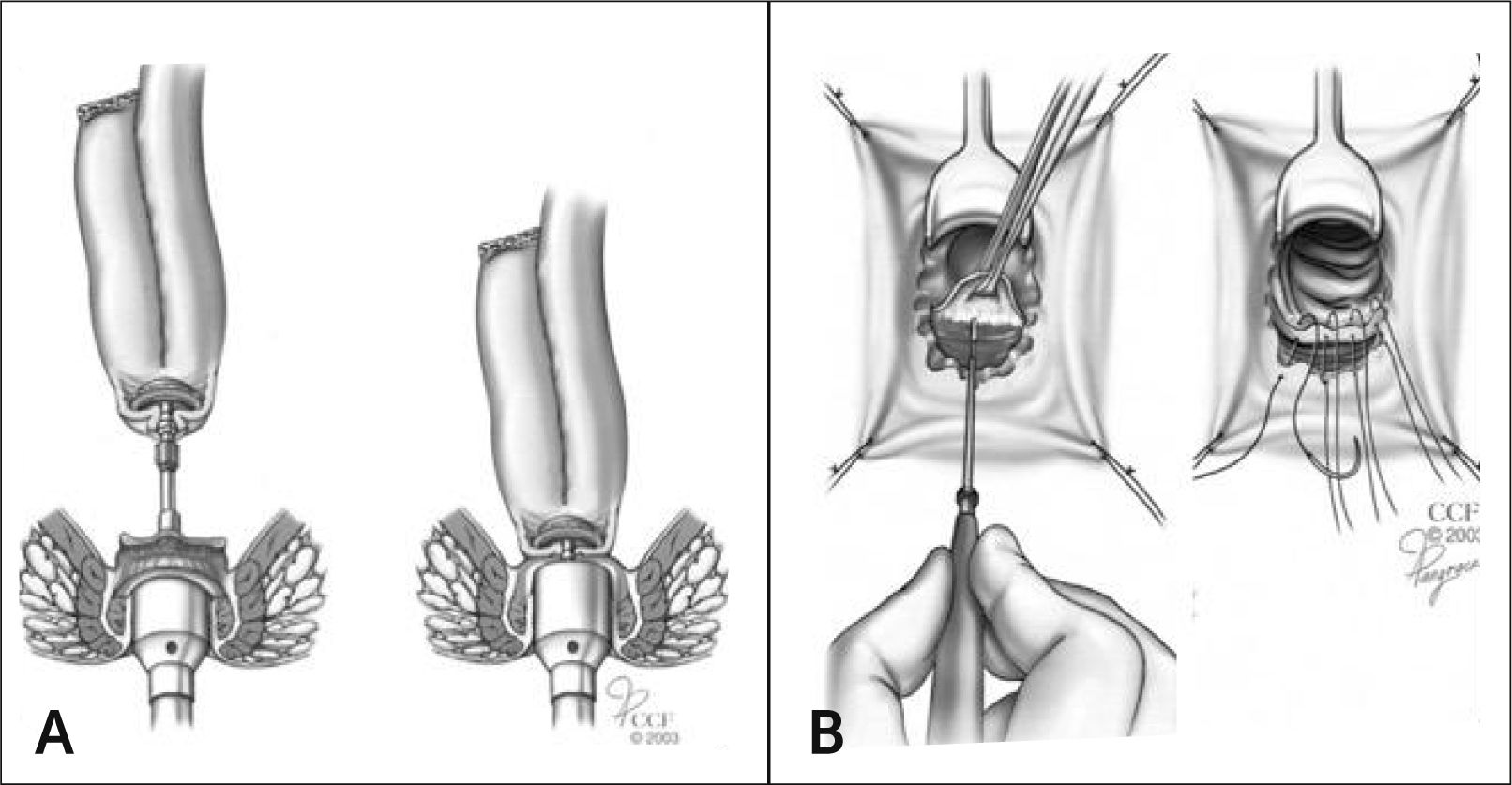
Luego de confeccionado el reservorio este se tiene que conectar al canal anal. Eso puede realizarse en forma mecánica mediante técnica de doble corchetera (cierre del muñón rectal a nivel de los elevadores del ano con corchetera perpendicular y luego anastomosis íleo anal mediante corchetera circular), o en forma manual con puntos separados entre el reservorio y la línea pectínea del canal anal, previa mucosectomía de la zona de transición y el muñón rectal (Figura 2). La anastomosis mecánica tiene la ventaja de ser técnicamente más fácil y reproducible y de ofrecer resultados funcionales 2–4 veces superiores en cuanto a la continencia, sobre todo bajo el aspecto de ensuciamiento nocturno y uso de protectores6. Su desventaja consiste en que queda la zona de transición con mucosa rectal de aprox. 2cm proximales a la línea pectínea sin resecar, lo que significa que se puede reactivar la enfermedad en este segmento (cuffitis), lo que es generalmente de fácil manejo con 5-ASA tópicos (supositorios). Si bien la anastomosis manual incluye la extirpación de toda la mucosa del recto distal y del canal anal proximal, lo que protege contra la reactivación de la CU y contra futuras neoplasias, es técnicamente mas demandante, y puede predisponer al paciente a problemas de continencia como ensuciamiento, falta de discriminación entre gases y deposiciones, entre otras7.
Dado que la confección del reservorio ileal con anastomosis ileo anal es un procedimiento de alta complejidad, se debe procurar que el paciente esté en las mejores condiciones fisiológicas posibles al momento de la cirugía, para favorecer una cicatrización rápida y completa sin complicaciones, por ejemplo, la dehiscencia anastomótica. Esto significa, que la confección del reservorio no se debe realizar en pacientes que se operan de urgencia, o en pacientes con anemia, desnutrición, actividad inflamatoria sistémica y tratamiento con corticoides sistémicos. Aún en pacientes que cumplen estas condiciones, la tasa de filtraciones anastomóticas rodea el 6%, por lo que la mayoría de los cirujanos prefiere dejar al paciente desfuncionalizado mediante una ileostomía en asa de protección por 2-3 meses8.
Cirugía en dos y tres tiemposLa mayoría de los pacientes requiere un tratamiento quirúrgico de la CU en una situación de crisis moderada o grave de la enfermedad, que no responde al tratamiento farmacológico con corticoides o tratamiento biológico con anti-TNF u otros. En general se operan de emergencia, urgencia o en forma semi-electiva. En ese contexto, muchos pacientes sufren de anemia, desnutrición e inflamación sistémica al momento de intervenir. Dado el riesgo elevado de complicaciones del mismo reservorio en esas condiciones, se divide el proceso quirúrgico en 3 etapas:
- •
En la primera operación, el equipo quirúrgico se limita a extirpar el colon, dejando el recto en su lugar (idealmente con el cierre del muñón rectal a nivel subcutáneo en posición suprapúbica) y abocando el íleon terminal a la piel en fosa iliaca derecha en forma de una ileostomía. De esta forma, el paciente obtiene la oportunidad de recuperar su estado de salud en general, corregir su situación nutricional, recuperar una eventual anemia y eliminar inflamación sistémica y corticoides sistémicos.
- •
Una vez completamente recuperado, se procede a la segunda etapa, que consiste en extirpar el recto enfermo, confeccionar el reservorio ileal y anastomosarlo al canal anal. Se recomienda, dejar al paciente desfuncionalizado mediante una ileostomía en asa.
- •
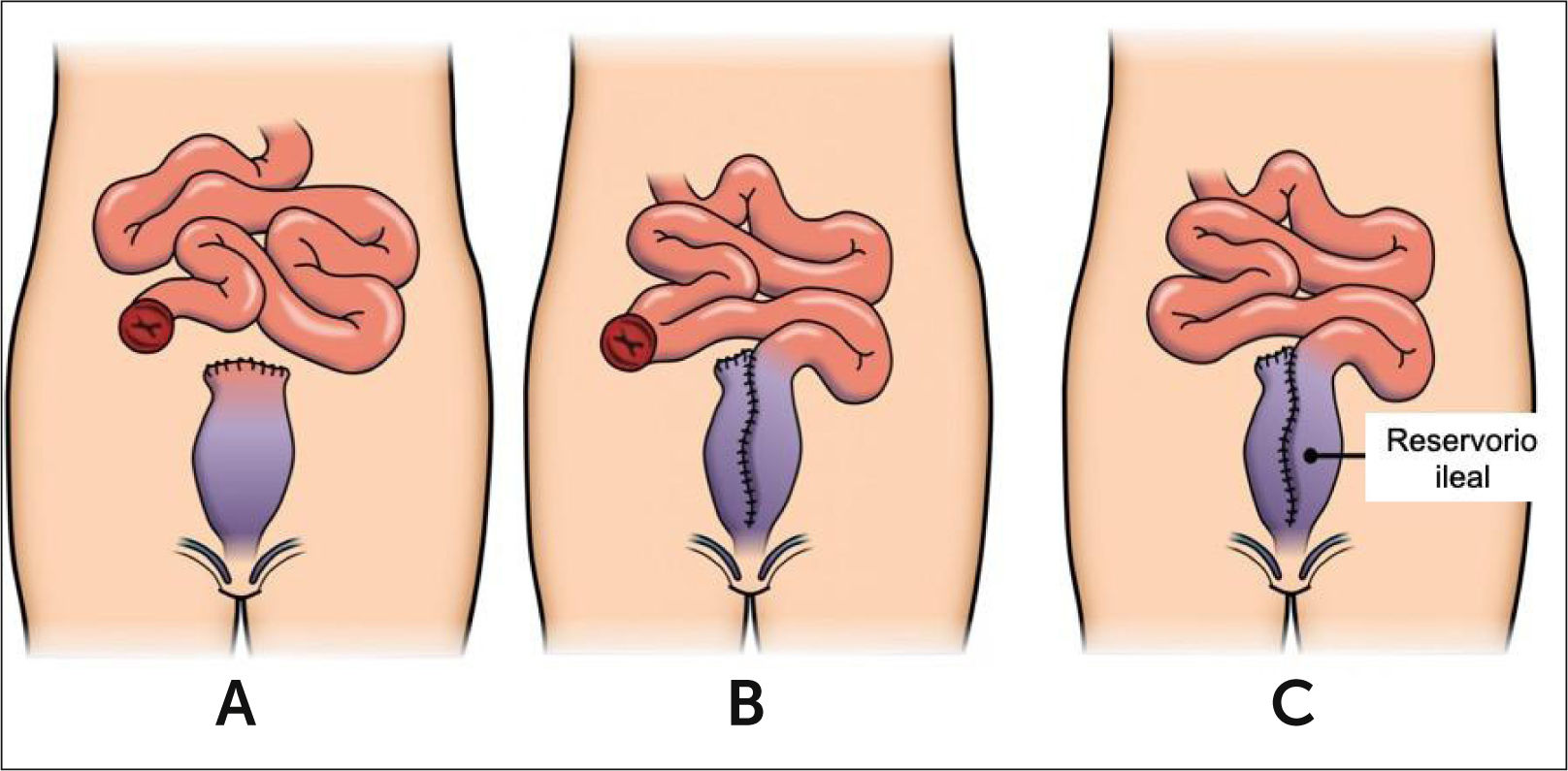
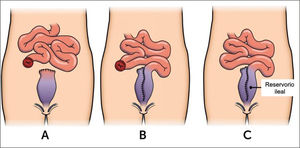
Luego de 2-3 meses, se realizan las pruebas de rigor para descartar una dehiscencia de sutura del reservorio mediante reservoriografía con medio de contraste hidrosoluble y/o reservorioscopía. De no detectar ninguna filtración, se procede a la tercera etapa, el cierre de la ileostomía, con lo que el reservorio entra en función (Figura 3).
En algunos pacientes con indicación semi-electiva y en pacientes electivos, se puede optar por combinar las primeras dos etapas en un solo acto quirúrgico, es decir, realizar la procto- colectomía y la confección del reservorio ileal inmediatamente, protegido por una ileostomía en asa. La última etapa es idéntica en ambos enfoques. La decisión de la cirugía en 2 o 3 tiempos se debe evaluar en forma individual dependiendo de la situación fisiológica de cada paciente, del tipo de tratamiento que está recibiendo al momento de la intervención, y otros factores como el deseo del paciente.
Complicaciones quirúrgicasConsiderando la complejidad del procedimiento, es esperable que ocurran complicaciones quirúrgicas tanto perioperatorias, como también tardías. Aproximadamente un tercio de los pacientes operados sufrirán algún tipo de complicación8, la mayoría de ellas transitorias y fácilmente tratables.
Una de las complicaciones perioperatorias más severas es la dehiscencia anastomótica con relación al reservorio (aprox. 4.8%), que lleva en general a una sepsis pélvica (6.3%), que puede ser de difícil manejo. El tratamiento incluye antibióticos, punción bajo TAC en caso de colecciones, e incluso reoperaciones con aseo y drenajes en caso de no ser posible la punción percutánea. En casos seleccionados de una dehiscencia a nivel de la anastomosis íleo anal, existe la posibilidad de un drenaje transanal a través de la misma dehiscencia. Otras complicaciones incluyen la infección del sitio quirúrgico (7.2%), la estenosis anastomótica (5.3%), la obstrucción intestinal por adherencias (4.9%), la hemorragia digestiva (3.6%) y la fistulización del reservorio hacia el periné o la vagina (1.3%), entre otras8.
Complicaciones del mismo reservorio a mediano y largo plazo incluyen las fístulas (2.7%), la reservoritis aguda (35%) y crónica (17%), la estenosis fibrótica (11.2%), la obstrucción intestinal por adherencias (13.2%) y otras complicaciones menos frecuentes como la rotación e incluso el prolapso del reservorio. A largo plazo, la tasa de pérdida del reservorio o necesidad de un neoreservorio en pacientes con CU es de alrededor del 5%8.
Cabe destacar, que las secuelas de algunas de estas complicaciones, especialmente la dehiscencia anastomótica con sepsis pélvica, determinan un deterioro de la función del reservorio y por ende una calidad de vida inferior10. Por lo mismo es esencial, realizar la confección del reservorio en condiciones fisiológicas óptimas del paciente y dejar al paciente desfuncionalizado, en el intento de minimizar los riesgos de filtración.
Resultados funcionalesEn general, pacientes con reservorio ileal refieren una función digestiva adecuada, compatible con una vida relativamente normal. Tanto es así que la gran mayoría los pacientes operados se encuentran satisfechos con los resultados a largo plazo (94–96%)8,11,12.
La frecuencia defecatoria promedio es de 7 deposiciones en 24 horas (4-5 en el día más 1-2 en la noche), con una continencia normal en el 80% de los pacientes. Un tercio de los pacientes experimentan episodios de urgencia defecatoria o ensuciamiento nocturno, lo que lleva a que un 25% de los pacientes usa protectores. Aun así, el 96% de los pacientes volvería a someterse a la misma cirugía, en vez de quedarse con una ileostomía definitiva13.
En cuanto a la calidad de vida, los pacientes refieren buenos resultados en aspectos generales, especificas de salud y nivel de energía. Aproximadamente un cuarto de los pacientes señala sentir restricciones alimentarias y entre un 11% y 13% indica tener restricciones sociales, laborales y sexuales8.
Otras opciones quirúrgicas en CULa proctocolectomía restaurativa incluye en su esencia dos partes: la parte curativa que es remover colon y recto, y la parte restaurativa que genera el reservorio ileal que busca mejorar la calidad de vida de los pacientes operados. En condiciones especiales puede que un paciente reciba solamente la parte curativa, quedando con una ileostomía terminal definitiva. Esta situación se da sobre todo en pacientes que tienen una contraindicación para el reservorio ileal: pacientes con daño previo del aparato esfinteriano por cirugías proctológicas o radioterapia, partos traumáticos, fístulas anorrectales complejas, incontinencia fecal previa y cáncer de recto inferior que requiere resección parcial de esfínter, entre otras14. Aún sin contraindicaciones formales, hay pacientes que desean quedarse con su ileostomía, sobre todo pacientes con buena función y adaptación a ella. En estos casos, se recomienda realizar una proctectomía completa incluyendo mucosa del canal anal y esfínter interno, para evitar futuras complicaciones inflamatorias y/o neoplásicas de la mucosa remanente15.
En casos seleccionados, otro tipo de cirugía a considerar es la colectomía total con ileorrectoanastomosis. Hay que destacar que no es el procedimiento de elección en la actualidad, pero en casos aislados puede ser una alternativa válida de tratamiento. Hay que tener en consideración, que se exige como condición sine qua non que el recto esté completamente recuperado, sin actividad endoscópica de la enfermedad, ni secuelas de cicatrización que generan rigidez o falta de distensibilidad y sin evidencia de displasia16. Además, hay que considerar que en estos pacientes queda una superficie no despreciable de mucosa potencialmente enferma, que tiene un alto riesgo de recaída y de malignización, requiriendo muchas veces tratamiento y una vigilancia endoscópica estrecha.
En vista del riesgo elevado de infertilidad en mujeres portadoras de un reservorio ileal por adherencias pélvicas, la ileorectoanastomosis podría considerarse ocasionalmente como terapia puente en mujeres fértiles con un recto recuperado y paridad no cumplida, que luego de culminar su planificación familiar o en caso de reactivación, se puede convertir en un reservorio ileal16.
Planificación quirúrgicaEn pacientes que se operan en una situación de emergencia o urgencia, en general no es posible elegir la institución donde se realizará la operación, ni definir el momento adecuado de la cirugía, porque ambos factores obedecen a un cuadro clínico de difícil control, lo que obliga muchas veces a un equipo sin experiencia en el manejo de la EII a intervenir al paciente en una condición clínica subóptima. En esas condiciones, realizar la colectomía subtotal, confeccionar una ileostomía terminal y el cierre del muñón rectal en posición suprapúbica en el subcutáneo son tareas que un equipo de cirugía digestiva con cierta experiencia puede enfrentar sin mayor problema. Sin embargo, la resección del recto remanente, confección del reservorio y la anastomosis íleo anal requieren de un equipo quirúrgico con formación específica, suficiente experiencia, y un número adecuado de procedimientos anuales, logrando así resultados funcionales favorables17.
La elección del momento óptimo para la cirugía semi-electiva y electiva depende de varios factores, entre ellos parámetros fisiológicos (ausencia de anemia, situación nutricional con recuperación ad integrum, ausencia de inflamación sistémica e idealmente con ausencia de corticoides sistémicos). Para lograr los mejores resultados quirúrgicos, se requiere un trabajo coordinado multidisciplinario, incluyendo aparte del gastroenterólogo y coloproctólogo la participación del nutriólogo para la optimización de la situación nutricional, de la enfermera especializada en ostomías para la educación del paciente y la correcta marcación preoperatoria del sitio de la ileostomía, apoyo psicológico por psicólogo y/o psiquiatra según sea el caso, y de otros especialistas en algunos casos. Por otro lado, es muy importante considerar el deseo del paciente en el proceso de toma de decisiones. Del total de pacientes operados quienes recibieron terapia médica prolongada y solo lograron una respuesta parcial hubiesen preferido operarse antes, y ninguno de ellos hubiese postergado su operación en post de una terapia intensificada para lograr remisión. Los argumentos más utilizados fueron que tras la cirugía lograron alivio del dolor, normalización del tránsito intestinal y una disminución del sangrado rectal18,19.
Tratamiento quirúrgico bajo terapia biológicaEn la era de la terapia biológica, aproximadamente un 10% de los pacientes con CU requieren una proctocolectomía restaurativa dentro de 5 años de su diagnóstico20. Dado que la terapia biológica es cada vez más usada, la mayoría de estos pacientes se operan luego de haberla recibido. Aunque los fármacos más utilizados previos a la indicación de cirugía son los anti-TNF, es posible que algunos pacientes hayan sido tratados además con otros biológicos como anti-integrinas (vedolizumab) y moléculas pequeñas (tofacitinib). Los efectos de estos fármacos, especialmente los anti-TNF, en los resultados quirúrgicos, son variables, tanto en complicaciones a corto y largo. Aunque en Enfermedad de Crohn se ha demostrado que las tasas de complicaciones postoperatorias, sobre todo infecciosas, son más altas en pacientes bajo tratamiento con anti-TNF, en CU esta tendencia no es tan clara. En pacientes expuestos a anti-TNF, se han observado tasas mayores de sepsis pélvica, cuando se realiza el procedimiento en dos tiempos. Esta tendencia desaparece al realizar el reservorio ileal en 3 tiempos, por lo que los autores recomiendan utilizar esta estrategia21,22. Esto se correlaciona con que la sepsis pélvica es uno de los factores de riesgo más importantes para un deterioro de la función del reservorio ileal, influyendo en la calidad de vida de los pacientes10. A pesar del hecho que también existen publicaciones que no observan diferencias en las complicaciones en pacientes expuestos, un reciente meta análisis sigue considerando la terapia con anti-TNF como factor importante para inclinarse hacia una estrategia quirúrgica en 3 etapas23.
Displasia y cáncer colorrectal (CCR) en CUDebido a la inflamación crónica de larga data, el riesgo de CCR en pacientes con CU es elevado comparado con la población general. El riesgo depende en primer lugar de la duración de la CU, siendo 2% a los 10 años de enfermedad, 8% a los 20 años y 18% a los 30 años24. De acuerdo con estos conocimientos, se recomienda iniciar una vigilancia endoscópica a los 8-10 años de enfermedad. Otro factor de riesgo independiente es la presencia de colangitis esclerosante primaria (CEP) en pacientes con CU. Aquellos pacientes tienen un riesgo 4 veces elevado comparado con pacientes con CU sin CEP25. Hay otros factores de riesgo de CCR en CU, como la edad de diagnóstico, extensión de la enfermedad e historia familiar de CCR (Tabla 1)26. Según su perfil de riesgo, se recomienda a los pacientes una vigilancia endoscópica en forma anual o cada 3 años.
Factores de riesgo para cáncer colorrectal en colitis ulcerosa
| Factores de alto riesgo: Vigilancia anual |
| Colitis extensa (pancolitis, en EC compromiso colonico> 50%) |
| Inflamación moderada a severa en endoscopía o histología mantenida sobre el tiempo |
| Colangitis esclerosante primaria |
| Edad de inicio de enfermedad <15 años |
| Historia familiar de CCR en un familiar de primer grado menor de 50 años |
| Presencia de estenosis o displasia diagnopsticada en los 5 años previos |
| Factores de alto riesgo en reservorio ileal |
| Displasia |
| Antecedentes de CCR |
| Factores de riesgo intermedio: Vigilancia cada 3 años |
| Inflamación leve a moderada en endoscopía o histología mantenida sobre el tiempo |
| Historia familiar de CCR en un familiar de primer grado mayor de 50 años |
| Presencia de múltiples pólipos inflamatorios |
| Factores de bajo riesgo: Vigilancia cada 5 años |
| Pancolitis sin inflamación |
| Colitis izquierda en CU o compromiso colonico <50% en EC |
La vigilancia endoscópica en pacientes con CU es más difícil en comparación con la población general, debido al daño inflamatorio crónico y sus secuelas como pólipos inflamatorios y fibrosis entre otros, que pueden dificultar el correcto reconocimiento de lesiones sospechosas de displasia y/o adenocarcinoma. Como en toda colonoscopia, los procedimientos en estos pacientes requieren una excelente preparación, y la intubación cecal obligatoria. Para identificar con mayor sensibilidad lesiones sospechosas, se recomienda usar equipos de alta resolución con luz blanca, y complementar el procedimiento con la aplicación de tinción directa en spray con azul de metileno o indigocarmina. La tinción electrónica con FICE, NBI u otros aún no es recomendado en forma generalizada por su rendimiento inferior comparado con la tinción directa27. Sin embargo, en un reciente consenso se determina que en manos entrenadas puede representar una alternativa válida con buenos resultados28.
En el caso de observar una lesión sospechosa, hay que evaluar el aspecto y los bordes. Si no se logra observar bordes definidos, la lesión se clasifica endoscópicamente irresecable. En estos casos hay que tomar biopsias y dejar el lugar marcado con un tatuaje endoscópico. En caso de confirmarse la presencia de displasia y/o adenocarcinoma, el paciente requiere una resección quirúrgica. Lo mismo aplica cuando la lesión tiene bordes definidos, pero características que hacen sospechar una invasión de la submucosa (centro deprimido, “no lift sign”, Kudo V, etc). En lesiones con características más favorables, se procede a resección endoscópica en bloc, y además se toman biopsias de la mucosa endoscópicamente conservada alrededor de la lesión, en un frasco separado9. En el caso de detectarse una lesión con displasia de alto grado, compromiso del margen profundo independiente del tipo de displasia, adenocarcinoma o displasia en la mucosa sana adyacente, se recomienda la colectomía para controlar el riesgo oncológico. En lesiones con displasia de bajo grado y resección endoscópica completa, el manejo es controvertido, pero hay opiniones de que en estos pacientes se puede realizar una vigilancia endoscópica estrecha sin aumentar el riesgo oncológico. El uso de biopsias aleatorias de todo el colon ya no se recomienda desde el consenso SCENIC en 2015 por sus dificultades técnicas en conjunto con un bajo rendimiento en la detección de neoplasias27,29.
ConclusionesEl tratamiento quirúrgico tiene una indicación clara dentro de la estrategia terapéutica de la CU. Los procedimientos que se pueden realizar son de alta complejidad, pero en manos de un equipo especializado se logran resultados funcionales satisfactorios y una potencial curación del componente inflamatorio intestinal de la enfermedad. Estos resultados permiten situar a la cirugía como una alternativa terapéutica válida en CU y no solo como una terapia de rescate frente a la ausencia de respuesta a la terapia farmacológica.
Declaración conflicto de interesesEl autor no presenta ningún conflicto de intereses.