Las personas con una pérdida auditiva, con caída abrupta en las frecuencias agudas, a menudo pueden oír el habla, pero no la entienden, y los tratamientos convencionales, incluyendo audífonos de transposición de frecuencia, suelen ser ineficaces cuando la pérdida auditiva es severa a profunda. La estimulación electro-acústica (Electro Acustic Stimulation-EAS) es una opción de tratamiento relativamente nueva para esta población, en el que la información de la frecuencia media alta está proporcionada por un implante coclear (IC) que se inserta en la espira basal de la cóclea, complementado por la amplificación acústica de las frecuencias graves. Nuevos diseños de electrodos de IC atraumáticas y las técnicas quirúrgicas respectivas han demostrado facilitar la conservación de la audiencia en las frecuencias graves en una manera suficiente para permitir el uso de EAS en la mayoría de los candidatos indicados. Los estudios clínicos han demostrado consistentemente la combinación.
Los audífonos convencionales representan el estándar de cuidado para la mayoría de los individuos con pérdida auditiva sensorineural y son particularmente efectivos cuando los umbrales auditivos están dentro del rango moderado a severo. Sin embargo, para pérdidas auditivas muy severas, la restauración de reconocimiento de voz por audífonos ha sido limitada aún cuando se puede lograr una mejora de acuerdo a los algoritmos de prescripción ajustados según la receta médica. Esto es particularmente cierto para amplificación de frecuencia mediana-alta, lo cual incluso puede ser perjudicial para la comprensión de habla son menores que 60 - 70dB HL1,2. Esto, es probablemente relacionado al hecho que más umbrales más severos estén asociados con daño a las células ciliadas internas además de la pérdida de la función de sintonía fina de las células ciliadas externas y en casos extremos, puede haber una pérdida total de células ciliadas internas en áreas de la cóclea, denominado “áreas muertas”3.
En muchos casos de pérdida auditiva sensorineural, los umbrales auditivos son mejores para bajas frecuencias que para altas frecuencias. En ciertos individuos, esta diferencia de umbral puede ser muy amplio, a veces con audición normal o prácticamente normal en las frecuencias bajas y pérdida auditiva severa a profunda en las frecuencias altas. En dichos casos, es posible que la amplificación de frecuencia alta no entregue un beneficio significativo. Estos individuos frecuentemente pueden oír habla pero no lo entienden debido a que la información importante en las frecuencias media y alta no es audible.
Las opciones de tratamiento para estas personas son limitadas. Generalmente es difícil proporcionar la gran variación en la ganancia requerida en las distintas frecuencias usando un audífono convencional y algunos individuos ni siquiera requieren amplificación en las frecuencias bajas. Se puede esperar que los audífonos de transposición de frecuencias, los cuales comprimen un rango de frecuencia de entrada amplia a las frecuencias bajas (audibles), otorguen un beneficio significativo para esta población, pero hasta la fecha, los resultados clínicos con los audífonos disponibles actualmente han sido decepcionantes4,5.
Durante los últimos 30 años, el implante coclear se ha convertido en el tratamiento de rutina para pérdida auditiva severa a profunda y se ha demostrado de manera consistente que el rendimiento auditivo ha mejorado en individuos que no tenían audición antes de la operación o en aquellas personas que no se benefician de manera significativa usando audífonos convencionales. Sin embargo, a pesar de que altos niveles de rendimiento son frecuentemente reportados en situaciones auditivas favorables, las personas con implantes cocleares comúnmente tienen bastante dificultad en diferenciar a las personas cuando hay mucho ruido de fondo. Se cree que esta dificultad se debe en gran parte a una representación relativamente pobre de la “estructura fina” de la frecuencia baja de la señal acústica (i.e. el rango de frecuencia fundamental para voz) por estimulación eléctrica6,7.
Los criterios para seleccionar a los candidatos para un implante coclear, comúnmente involucran niveles específicos de comprensión de habla antes de la operación (usando audífonos cuando corresponde) y umbrales audiométricos sin asistencia8. Los individuos con pérdida auditiva de frecuencia alta muy empinada generalmente están dentro de estos criterios, pero pueden ser reacios a proceder con una implantación por temor a perder su audición natural restante. En los primeros años de implante coclear, se asumió que cualquier audición restante se perdería después de la cirugía, pero la experiencia ha demostrado que la pérdida auditiva no es inevitable especialmente cuando se utilizan técnicas de “cirugía suave”.
Los individuos con pérdida auditiva muy inclinada han representado últimamente una población particularmente interesante en el área de implante coclear. Dado que un electrodo para implante coclear generalmente es insertado vía la región basal (alta frecuencia) de la cóclea, se planteó que una combinación de estimulación acústica y eléctrica podría proporcionar una opción de tratamiento factible para esta población. En principio, un electrodo para implante coclear insertado en la región basal de la cóclea podría entregar información de alta frecuencia por estimulación eléctrica y posiblemente conservar la función coclear residual apical (frecuencia baja), lo cual podría ser proporcionado con amplificación acústica si fuese necesario. Dicha combinación podría ser más efectiva que la estimulación eléctrica o acústica de manera aislada. En este artículo, buscamos entregar una perspectiva general de la experiencia clínica existente en relación a “estimulación electro acústica” (EEA) junto con las opciones de hardware disponibles de Cochlear Ltd y con un informe actualizado de los resultados clínicos más recientes.
PRINCIPIOS E IMPLEMENTACIÓN DE EEALa mayoría del trabajo inicial en EEA incluyó estudios de la fisiología de la estimulación acústica y eléctrica combinado en animales9, como un intento para aclarar si las dos modalidades podrían entregar estimulación sinérgica de las células ganglionares espirales. Esto se consideró importante debido a que los patrones de activación producido por la estimulación acústica y eléctrica son considerablemente distintas. Sin embargo, progreso con la aplicación clínica de EEA ha sido afectada más directamente por estudios clínicos paralelos. Dado que los resultados de un implante coclear generalmente han mejorado a través de los años, los individuos con mayores niveles de audición residual han recibido un implante. Cuando existe algún nivel de audición útil, los individuos frecuentemente son implantados en el oído más débil para tratar de evitar peores resultados post- implante. Muchos estudios han informado que dichos receptores de un implante coclear pueden beneficiarse de la combinación de estimulación eléctrica en el oído implantado e input acústico en el oído opuesto, i.e. “estimulación bimodal”10,11. Esto demuestra que el sistema auditivo central puede combinar efectivamente las respuestas neuronales a la estimulación acústica y eléctrica.
Muchas de las pruebas iniciales con estimulación acústica y eléctrica combinada en el mismo oído utilizaron guías de electrodos relativamente cortas con la esperanza de que estos facilitarían una mejor conservación de la audición acústica de baja frecuencia más que las guías convencionales largas. Cochlear Ltd fabricó dos dispositivos comerciales basados en el estimulador coclear implantables CI24RE Freedom. El dispositivo Hybrid S8 utilizo guías de electrodos de 10mm con 6 contactos de electrodos activos. Un ensayo multicéntrico realizado en Estados Unidos reportó audición de baja frecuencia conservada útil en 80% de los sujetos luego de un año, y una mejora significativa en la comprensión del habla en 82,5% de los sujetos al agregar input acústico12. Sin embargo, una minoría de los sujetos parece haber perdido su audición posterior a la cirugía o más adelante13, y en esta situación, una guía de electrodos muy corta entrega menor beneficio auditivo que una guía convencional14. Por este motivo, una guía alternativa, el “Hybrid L24” fue posteriormente fabricado por Cochlear. El Hybrid L24 tiene 22 contactos repartidos en 17mm, y se extiende a aproximadamente 270o de la ventana redonda, i.e. a la región 2000Hz de la cóclea15. Altos niveles de conservación auditiva también han sido informados para este dispositivo, y se demostró que el rendimiento solo de una implante coclear era comparable a aquella lograda por los receptores convencionales16. Estos resultados son analizados en mayor detalle a continuación.
El hardware para EEA más reciente de Cochlear Ltd incluye un electrodo atraumática, la guía “Slim Straight” (SS), lo cual ha sido acoplada a los paquetes de implantes CI24RE y CI500 Profile para formar los dispositivos Nucleus CI422 y CI522 respectivamente (Figura 1). La guía SS es una guía de electrodos derecha, flexible y delgada que puede ser insertada por medio de una cocleostomía o a través de la ventana redonda y toma posición por la pared lateral de la cóclea. El portaelectrodo soporta contactos de electrodos de media banda, lo cual le entrega a la guía un lado liso que disminuye significativamente la fuerza requerida para la inserción y puede reducir el trauma cuando es desplazado por la pared lateral de la scala tympani (ST). Los 22 contactos de electrodos ahora están distribuidos en 20mm y la guía tiene dos marcadores que están diseñados para indicar una profundidad de inserción de 20 o 25mm. Se recomienda una profundidad de inserción cuando la conservación auditiva es de importancia, tal como con usuarios potenciales de EEA.
La serie de procesadores de sonido CP900 (CP910 y CP920) pueden, de manera opcional, ser equipados con un “componente acústico”, lo cual reemplaza el auricular estándar e incorpora un transductor (receptor) acústico que entrega su output directamente al canal auditivo. Esto permite el uso de un solo dispositivo integrado en vez de necesitar dispositivos de estimulación acústica y eléctrica por separado (Figura 2A). Otra ventaja de un solo dispositivo integrado es que los ajustes de output acústico y eléctrico pueden ser fácilmente realizados con un solo sistema de ajuste (software de sonido personalizado), así permitiendo un ajuste óptimo del sistema EEA (Figura 2B).
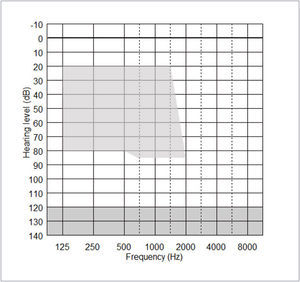
El componente acústico del procesador CP900 puede ser colocado o retirado en cualquier momento, pero su uso efectivo depende del grado de audición acústica post-operatoria residual, lo cual no se puede predecir de forma fiable antes del implante. Las indicaciones para el uso del componente acústico son entregadas por el rango de ajuste mostrado en la Figura 3 a continuación. Los umbrales postoperatorios que caen dentro de los rangos sombreados indican frecuencias que pueden ser amplificados por el CP910/920 en modalidad EEA.
Varios estudios clínicos han abordado las indicaciones para estimulación híbrida en términos de niveles de audición pre-implante. Inicialmente, solamente los sujetos con umbrales de baja frecuencia menor de aproximadamente 65dB HL eran implantados17, pero los resultados iniciales alentadores generaron que dichos límites se flexibilizaran. Estudios recientes han sugerido que la amplificación acústica puede ser efectivamente otorgada para umbrales de audición de baja frecuencia que están alrededor de 70dB HL a 250Hz. Cuando los umbrales son peores que esto, los sujetos tienden a preferir estimulación sola (eléctrica) del implante coclear18. En frecuencias más altas, los umbrales deberían estar bajo 80dB HL aproximadamente (i.e. de acuerdo a las indicaciones para un implante coclear convencional), dado que los audífonos acústicos no otorgan beneficios de audición útiles para pérdidas de audición de frecuencia alta. Sin embargo, aunque estas pautas de umbral audiométrica generales, son relativamente claras, existe una heterogeneidad considerable en los tipos de receptores. Algunos individuos tienen muy buena audición de baja frecuencia y por lo tanto, no requieren la amplificación de bajas frecuencias19. Muchos tienen un nivel de audición considerable en el oído no implantado y se pueden beneficiar de audición de baja frecuencia binaural además de la información de frecuencia media-alta entregado por el implante coclear.
Las influencias del diseño del dispositivo y técnica quirúrgica en la conservación de la audiciónLa conservación de audición de baja frecuencia es un prerrequisito para el uso exitoso de EEA y este tema fundamental sigue recibiendo mucha atención a través de estudios clínicos e investigación. Los resultados de estos estudios han demostrado que la conservación auditiva depende de varios factores específicos, particularmente:
- (i)
Diseño de electrodos para implante coclear
- (ii)
Técnica quirúrgica
- (iii)
Factores en los pacientes como, por ejemplo, el grado de audición residual.
El concepto de “cirugía blanda” fue introducido inicialmente por Lehnhardt20, e incorporó un rango de pautas enfocadas en minimizar el trauma coclear, lo cual incluía abrir el scala tympani lo más tarde posible, evitar succión del perilinfa, el uso de lubricantes tal como Healon® y la inserción lenta de la guía de electrodos. El objetivo original de cirugía blanda era de minimizar el daño a la cóclea en general y particularmente, el sustrato neural, con la esperanza de lograr una estimulación eléctrica más efectiva. Sin embargo, la mayoría de estos principios son igualmente válidos para la conservación auditiva (células ciliadas). Además, los cirujanos que intentan conservar audición frecuentemente tratan de evitar la perforación del endeosteum y hoy es común el uso de corticoides perioperatorias oral y/o intravenoso21.
Cuando se utiliza cirugía blanda, se ha informado de algún nivel de conservación auditiva en los receptores de un implante coclear convencional con audición medible con la mayoría de los tipos de electrodos actualmente disponibles, así demostrando que la pérdida de audición residual no es una consecuencia inevitable de un implante coclear. Por ejemplo, Fraysse et al.22 reportaron un promedio de deterioro del umbral de baja frecuencia de 23dB después de un mes en 12 receptores del dispositivo Nucleus CI24 con electrodo Contour Advance, al usar un protocolo de cirugía blanda. Obholzer & Gibson23 reportaron la conservación de audición residual en 58 de 81 pacientes con el dispositivo Nucleus CI24 (con banda derecha y guía de electrodos Contour) luego del control correspondiente a los 6 meses. El promedio de deterioro del umbral a 500Hz era 15dB en aquellas personas con audición conservada.
Conservación auditiva reportada para tipos de electrodos específicosCuando la conservación auditiva es un objetivo específico, tal como en candidatos para EEA, la mayoría de los estudios clínicos han utilizado guías de electrodos diseñados específicamente para la conservación auditiva. Estas guías son derechas, flexibles y relativamente delgadas y están diseñadas para yacer en el borde externo del scala tympani. Una cantidad significativa de estudios han cuantificado el grado de conservación auditiva logrado con tipos de electrodos específicos. Sin embargo, hacer comparaciones entre los distintos estudios es difícil debido a los múltiples métodos para reportar. Algunos estudios han reportado la proporción de sujetos con umbrales de baja frecuencia postoperatorio dentro de 10dB de los niveles pre-implante (frecuentemente llamado “conservación auditiva total”), o dentro de 20 o 30dB (“conservación auditiva parcial”). Otros estudios han informado que el umbral de baja frecuencia medio y mediana cambian post implante. Además, se han reportado resultados en una amplia gama de tiempos de seguimiento, impidiendo aún más cualquier comparación. Finalmente, los resultados de conservación auditiva con dispositivos específicos pueden están influenciados por variaciones en la técnica quirúrgica y/o características de los pacientes.
Las pruebas para los dispositivos Cochlear Hybrid vienen principalmente de una serie de estudios clínicos multicéntricos. El dispositivo Hybrid S8 más corto fue evaluado en un ensayo clínico en Estado Unidos reportado por Gantz et al.12,24. 87 adultos fueron implantados con la guía de electrodos de 10mm en el oído más débil, con umbrales de bajo frecuencia (125–500Hz) preoperatorios de 60dB HL o mejor. En la activación inicial, dos sujetos (1.3%) habían perdido toda su audición, y en los sujetos restantes, el promedio de los umbrales de baja frecuencia disminuyeron en promedio 14.8dB. Durante los 12 meses subsiguientes, 14 sujetos más perdieron su audición funcional (umbrales de baja frecuencia >90dB HL), pero hubo poco cambio en los umbrales de los sujetos restantes. A los 12 meses post activación, 80% de los sujetos retuvieron audición funcional de baja frecuencia y pudieron utilizar EEA.
Lenarz et al.16 informaron sobre un estudio multicéntrico de European Hybrid L24, lo cual incluyó 66 adultos con pérdida auditiva de alta frecuencia severa a profunda y con umbrales <60dB HL en frecuencias menor a 500Hz. En la activación inicial, 89% de los sujetos demostraron conservación auditiva de baja frecuencia dentro de 30dB de los niveles preoperatorios, y en un 61% de los sujetos, los umbrales disminuyeron menos que en un 10dB. A los 12 meses, estas proporciones fueron 74% y 43% respectivamente, indicando aún más pérdida auditiva en algunos sujetos. El 88% de los sujetos mantuvieron un nivel de audición suficiente para poder utilizar EEA a los 12 meses. Los resultados del ensayo clínico multicéntrico en Estados Unidos fueron reportados por Roland et al.25 y se evaluó 50 adultos con características preoperatorias similares a aquellos sujetos en el estudio europeo. El 66% de los sujetos mantuvieron audición acústica funcional luego de 6 meses, y la proporción de sujetos con cambios en los umbrales de <10dB y <30dB fueron 25% y 56% respectivamente.
El mayor grupo de receptores de la guía relativamente nueva de electrodos Cochlear Slim Straight (SS) han sido implantados por Skarzynski y sus colegas. Skarzynski et al.26 reportaron resultados de conservación auditiva en 35 adultos separados en tres grupos según umbrales preoperatorios a 500Hz. Los grupos A, B y C tuvieron umbrales a 500Hz de <50dB HL, 50-80dB HL y >80dB HL respectivamente. Para el grupo total, el aumento de umbral promedio para frecuencias bajas fue 10dB y 15dB a un mes y un año post operación respectivamente, y tres sujetos (9%) perdieron completamente su audición residual. Al año, 38% de los sujetos tenía umbrales a 500Hz dentro de 10dB de los niveles preoperatorios y el 79% tenía umbrales dentro de 30dB. La Figura 4 muestra el promedio preoperatorio y los umbrales postoperatorios a los 12 meses para los Grupos A y B (i.e. los sujetos que eran los típicos candidatos para EEA). En cada panel, el trazado superior indica la diferencia entre los umbrales pre-y postoperatorios.
MEDIANA DE UMBRALES PRE Y POSTOPERATORIO PARA DOS GRUPOS DE RECEPTORES DE ELECTRODOS COCHLEAR SLIM STRAIGHT
El n era 11 y 13 en grupos A and B respectivamente. Redibujado de Skarzynski et al.26.
El mismo grupo informó posteriormente los resultados en 19 niños implantados con el Nucleus CI42227. En este estudio, la conservación auditiva fue expresada como un porcentaje general (todas las frecuencias audiométricas mezcladas) comparando umbrales pre-y postoperatorios y tomando en cuenta los límites de output audiométricos (por ejemplo, los umbrales pre-y post operatorios de 60 y 75dB HL respectivamente, con un límite de output de 120dB HL, indicaría un 75% de conservación auditiva). Los autores sugirieron que una conservación de >75% puede ser considerada “completa” en términos de implementación práctica de EEA. El promedio de conservación auditiva registrada era 75% y 67% al año y dos años postoperatorio respectivamente (comparado con 97% y 94% en los oídos sin implante). Todos los sujetos mantuvieron audición suficiente para hacer uso de EEA a los 24 meses con la excepción de 4 sujetos que tenían muy malos niveles de audición preoperatorios.
Varios otros estudios han reportado sobre la conservación auditiva con el electrodo SS en grupos más pequeños, generalmente con resultados similares. Lenarz28 informó de conservación dentro de 15dB de los umbrales preoperatorios en el 48% de los 29 sujetos implantados con el dispositivo CI422 luego de 6 meses. El promedio de los umbrales de baja frecuencia preoperatorios fueron 63dB HL y el aumento promedio pre-postoperatorio en umbrales fue 15dB a 250Hz y 25dB a 500Hz. Friedmann et al.21 reportaron un aumento de 21.5dB en umbrales de baja frecuencia en la activación inicial en un grupo de 12 receptores de CI422, con un deterioro de 8.5dB adicionales a los 12 meses.
Estos estudios han incluido una variedad de técnicas quirúrgicas, tipos de pacientes y tiempos de seguimientos, sin embargo, se puede concluir que la audición de baja frecuencia a largo plazo es generalmente conservada dentro de 15–25dB de niveles preoperatorios al usar una guía SS, con la gran mayoría de los receptores aptos para utilizar EEA. Resultados de conservación auditiva similares han sido reportados para la guía MED-EL FLEXEAS de 24mm.29,30. Sin embargo, el uso de la guía MED-EL FLEXSOFT con el largo total de 31mm en sujetos con audición preoperatoria funcional ha demostrado ser asociado con una menor conservación auditiva y un mayor índice de pérdida auditiva total31,32.
FACTORES PREDICTIVOS DE BUENA CONSERVACIÓN AUDITIVAEstudios realizados sobre tipos de electrodos específicos han implantado una variedad de tipos de receptores y han usado múltiples técnicas quirúrgicas, y es probable que algunos de estos factores hayan contribuido hacia la variabilidad de los resultados observados. Varios artículos de crítica recientes han intentado identificar los factores predictivos de la conservación auditiva exitosa analizando los resultados de una gran cantidad de estudios. Sin embargo, mientras que algunos factores han emergido, es probablemente razonable estipular que la influencia reportada de muchos factores actualmente se mantiene inconsistente.
Santa María et al.33, Kopelovich et al.34 y Causon et al.35 analizaron por separado una amplia gama de características de receptores y técnicas quirúrgicas, y buscaron correlaciones por meta-análisis o análisis de regresión multivariado de conservación auditiva. La meta-análisis de Santa María et al.33 sugirió mejores resultados para:
- (i)
inserción cocleostomía (en vez de RW).
- (ii)
un método de timpanometría posterior (en vez de suprameatal).
- (iii)
tiempo de inserción de >30s.
- (iv)
uso de corticoides sistémicos postoperatorio.
Parámetros de electrodos no fueron predictivos de resultados. Causon et al.35 extrajo la conservación promedio de audición de baja frecuencia reportada para 110 pacientes en 12 estudios. Este análisis identificó que el uso de corticoides, especialmente cuando era administrado intraoperativamente, era predictivo de mejores resultados, pero también reportó mejores resultados de inserciones RW. Además, electrodos perimodiolares generaron peores resultados y la conservación auditiva estaba correlacionada de manera inversa con el ángulo de inserción. Respecto a las variables de los pacientes, la pérdida auditiva estable pareció ser predictiva de una mejor conservación auditiva más que pérdidas progresivas. Kopelovich et al.34 analizaron las variables de los pacientes del ensayo clínico de la Federación de Drogas y Alimentos en el Cochlear Hybrid S (85 sujetos). La conservación auditiva de frecuencia baja a un año post implante fue claramente superior en sujetos implantados a una edad más joven (dentro de un rango de 17 a 84 años) y fue significativamente superior en mujeres. Se constató que pacientes con pérdida auditiva producto de un exceso de ruido padecían de una mayor nivel de pérdida auditiva que aquellas personas con otras etiologías, aunque la etiología era desconocida en el 31% de los sujetos.
La administración de corticoides se ha convertido común en cirugías de conservación auditiva pero la vía y tiempo varía. La eficacia de corticoides preoperatorios (generalmente dexametasona, prednisona o triamcinolona) fue recientemente analizado por Kuthubutheen et al.36, quienes indicaron que, aunque la administración sistémica en varios momentos entre la inducción y cocleostomía ha llegado a ser habitual, la eficacia de un tratamiento con corticoides a corto plazo no está bien establecido por los estudios clínicos, aunque las pruebas de los estudios clínicos en animales son más fuerte. La concentración de corticoides intracoclear puede ser aumentado por administración local a la ventana redonda durante la cirugía, y existen pruebas que esto puede disminuir pérdida auditiva producto de la cirugía37. También existen pruebas que exposición extendida puede ser efectivo; Sweeney et al.38 reportaron mejor conservación auditiva en pacientes a quienes se les administró un protocolo de 2 semanas de corticoides (prednisona) con eliminación gradual, comenzando 3 días antes de la cirugía, aunque este estudio fue retrospectivo y no aleatorio. Estudios en la administración de corticoides postoperatorios a largo plazo, utilizando guisas de electrodos liberados de fármacos39 o vía bombas osmóticas40 muestran resultados alentadores en la reducción de fibrosis intracoclear y pérdida auditiva, aunque estos métodos actualmente se mantienen en una fase experimental.
RESULTADOS FUNCIONALES POR ESTIMULACIÓN ELECTRO AUDITIVO (EEA)Para poder satisfacer el criterio general de candidatos (comprensión de habla preoperatorio) junto con las indicaciones audiométricas de EEA, los candidatos potenciales de EEA comúnmente tienen pérdida auditiva más o menos simétrica. Cuando existe una diferencia significativa entre los oídos, generalmente se selecciona el oído más débil para el implante para poder evitar el riesgo de perder la audición natural en el oído con más capacidad auditiva. Por lo tanto, los usuarios de EEA pueden, generalmente, utilizar información de frecuencia baja de ambos oídos junto con la señal eléctrica en el oído implantado. Si hay pérdida auditiva en el oído implantado, los receptores de un implante coclear aún pueden beneficiarse de un estímulo “bimodal”, debido a que la combinación de estimulación acústica y eléctrica ha demostrado ser efectiva cuando el input acústico es del lado con implante o sin implante.
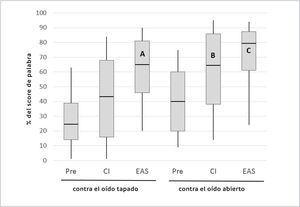
El estudio europeo multicéntrico del European Hybrid L, reportado por Lenarz et al.16 entregó una ilustración clara de las contribuciones individuales de estos inputs debido a que muchos de los sujetos fueron puestos a prueba con los oídos taponados por separado. Los 61 individuos que participaron en el estudio eran adultos sordos postlocutivos con umbrales auditivos de <60dB HL en frecuencias menores a 500Hz y >80dB HL en frecuencias mayores a 1500Hz. A un año post implante, 74% de los sujetos mantuvieron umbrales a 500Hz dentro de 30dB de los niveles preoperatorios. La señal eléctrica del implante coclear fue programada de tal manera como para no solapar, con el límite de filtro más bajo fijado cerca a la frecuencia donde los umbrales auditivos justo excedían 80dB HL41. La Figura 5 muestra el rendimiento de reconocimiento monosílabo a los 12 meses postoperatorio para 54 sujetos con la información completa (incluyendo cualquiera con una pérdida significativa de audición residual).
RECONOCIMIENTO MONOSILÁBICA EN SILENCIO EN UN GRUPO DE 54 USUARIOS DE HYBRID L ANTES DE LA OPERACIÓN Y A LOS 12 MESES PARA LAS CONDICIONES IMPLANTE COCLEAR SOLO Y EEA
Los cuadrados representan los percentiles 25/75 y whiskers representan los percentiles 10/90; las líneas horizontales indican los valores de la mediana. Todos los puntajes de oído implantado representan el rendimiento con el oído opuesto taponeado. Redibujado de Lenarz et al.16.
Se puede hacer varias observaciones importantes de la información en la Figura 5. Primero, para el oído implantado aislado (el oído opuesto está con un tapón) el rendimiento en la modalidad de audición (EEA) en Hybrid fue significativamente más alto que aquello obtenido utilizando solamente la señal eléctrica o la condición preoperatoria (solo acústico), demostrando una combinación sinérgica efectiva de input eléctrica y acústica. Segundo, las barras A y B muestran una mejora del rendimiento del implante coclear por si solo al agregar input acústico desde los lados ipsilateral o contralateral respectivamente; rendimiento aproximadamente equivalente es evidente para las dos condiciones. También es importante destacar que B (el oído implantado taponado) indica el rango de rendimiento que se lograría en cualquier sujeto que pierde completamente la audición residual en el oído implantado. Tercero, la barra C muestra una posible mejora adicional en rendimiento cuando el input acústico de ambos lados está disponible (aunque esto no fue estadísticamente significativo en esta serie). Lenarz et al.16 también entregaron datos para escuchar en listening in noise performance en un grupo más pequeño de sujetos, lo cual mostró patrones muy similares a aquellos demostrados para monosílabas en silencio.
Skarzynski y sus colegas han reportado extensamente sobre los resultados de implantes en sujetos con un rango de distintos niveles de audición de baja frecuencia19,26. Ellos clasificaron los potenciales receptores de un implante coclear según el nivel de los umbrales de bajo frecuencia preoperatorios. De este modo, los sujetos con “complemento eléctrico” (Grupo A) tuvieron umbrales a 500Hz mayores a 50dB HL y no siempre requirieron amplificación acústica. Los sujetos “EEA” (Grupo B) tuvieron umbrales a 500 de 50–80dB y se anticipó que utilizarían amplificación acústica y estimulación eléctrica en el oído implantado. Los sujetos con “estimulación eléctrica” (Grupo C) tuvieron umbrales a 500Hz fuera del rango que podría beneficiar de amplificación (>80dB HL), i.e. candidatos para implante coclear convencionales.
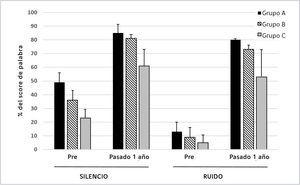
En una serie con 35 sujetos implantados con el Cochlear CI422 (con guía de electrodos Slim Straight), este centro utilizó una inserción parcial (20–23mm) para los sujetos del Grupo A y B y una inserción completa de 25mm para los sujetos del Grupo C26. Los resultados para los sujetos del Grupo C (n=11) fueron comparables con aquellos obtenidos en candidatos para implante coclear convencional con otras guías de electrodos de largo completo. De los dos grupos de usuarios potenciales de estimulación electro acústica, hubieron 11 y 13 sujetos en los Grupos A y B respectivamente. La Figura 6 muestra los puntajes al año para los tres grupos evaluados con palabras monosilábicas en silencio y con ruido simulando palabras (relación señal-ruido 10dB). El beneficio adicional de input acústico es evidente por los puntajes significativamente más altos en los Grupos A y B en relación a aquellos de los sujetos en el Grupo C. Una mayor mejora post implante es evidente con ruido comparado con en silencio para los tres grupos.
PROMEDIO DE PUNTAJES MONOSILÁBICAS EN SILENCIO A 1 AÑO POST IMPLANTE Y 10DB DE RUIDO SNR PARA TRES GRUPOS DE SUJETOS IMPLANTADOS CON EL COCHLEAR CI422
Las barras de errores muestran desviaciones típicas. Ver texto para mayor detalle. (de Skarzynski et al.26 con permiso).
Tal como se estipuló en la sección anterior, existen pruebas de un mayor riesgo de una pérdida importante de audición residual con guías de electrodos más largos durante la cirugía o en los meses o años posteriores. El uso de guías más cortas tiende a conservar la audición levemente más, sin embargo, una guía muy corta puede no proporcionar un rendimiento de implante coclear equivalente a la de guías más largas. Cuando pérdida auditiva funcional sucede, el usuario de un implante coclear solo tiene acceso a información entregada de manera eléctrica al oído implantado. Existen reportes de una pequeña cantidad de receptores del dispositivo Cochlear Hybrid S de 10mm que perdieron su audición residual y recibieron beneficios limitados solo con el implante coclear. Algunos de estos sujetos fueron implantados nuevamente con guías Contour estándar, con mejores resultados en ambos escenarios, solo con el implante y “con la mejor condición de ayuda”14,42.
Friedmann et al.21) evaluó los efectos funcionales de la pérdida de audición residual en un grupo de receptores de Cochlear CI422 y Hybrid L. La pérdida promedio del umbral de baja frecuencia posterior a la cirugía fue 21.5dB y 16.5dB en los receptores de CI422 y Hybrid L respectivamente, lo cual aumentó a 30dB y 22dB después de 12 meses. Siete usuarios de CI422 quienes perdieron su audición residual mostraron un rendimiento bimodal y del implante coclear solo significativamente superior a aquello obtenido por tres usuarios de Hybrid L que también perdieron su audición. Por lo tanto, los autores concluyeron que existe un cierto grado de contrapartida en la elección del largo del electrodo en términos de conservación de audición probable y los resultados si se pierde la audición residual. Sin embargo, los estudios realizados por Lenarz et al.16) y Skarzynksi et al.26 demostraron ambos que la condición bimodal para los sujetos utilizando el CI422 junto con audición residual en el oído sin implante (oído implantado bloqueado) proporcionó un rendimiento notablemente mejor en relación a la condición preoperatoria. Estos hallazgos sugieren que la guía Slim Straight de los dispositivos CI422 y CI522 proporcionan una combinación efectiva de conservación auditiva y rendimiento solo del implante coclear en usuarios potenciales de EEA junto con ofrecer una opción efectiva para candidatos de implante coclear convencionales.
CONCLUSIONES- 1.
Los individuos con pérdida auditiva de frecuencia alta muy empinada pueden generalmente oír a personas hablar pero no logran entender lo que se están diciendo. Los audífonos acústicos de compresión de frecuencia o convencionales han demostrado ser relativamente inefectivos para entregar una señal auditiva útil cuando la pérdida auditiva media-alta es severa o profunda.
- 2.
Los posibles receptores de un implante coclear con umbrales audiométricos de baja frecuencia (hasta 500Hz) mayores a aproximadamente 70-80dB HL son candidatos para la estimulación electro acústica (EEA), por el cual un implante coclear es implantada en la espira basal de la cóclea para poder proporcionar información de la frecuencia media-alta; y amplificación acústica es entregada para estimular audición de baja frecuencia residual. Tales candidatos generalmente son implantados en el oído más débil cuando existe audición preoperatoria funcional.
- 3.
Un rango de guías de electrodos para implante coclear flexibles y delgados han demostrado conservar audición residual dentro de niveles proporcionales con EEA en la mayoría de los receptores. La guía Cochlear Slim-Straight, de acuerdo a su uso en los dispositivos CI422 y CI522, entrega un buen rendimiento de conservación auditiva y a su vez proporciona altos niveles de rendimiento solo por el implante coclear incluso si la audición residual se pierde.
- 4.
Estudios clínicos han mostrado sistemáticamente una combinación sinérgica de información de frecuencia media-alta entregada de manera eléctrica por un implante coclear con frecuencias bajas entregados acústicamente, proporcionando un rendimiento superior a aquello obtenido solo por un implante coclear. La mejora observada de reconocimiento del habla solo por el implante coclear por frecuencias bajas acústicas ha demostrado ser efectivo cuando es entregado al lado ipsilateral o contralateral del implante.
- 5.
Los nuevos procesadores de sonido externos integrados, tal como la serie Cochlear CP900, tienen la capacidad de entregar señales acústicas y eléctricas desde un solo dispositivo, proporcionando mayor conveniencia para el usuario y un mejor proceso de ajuste integrado.
Herbert Mauch es empleado de Cochlear Latinoamérica y Paul Boyd es asesor para Cochlear Europe.