Las oclusiones venosas retínales constituyen una importante causa de deterioro de la agudeza visual. Su evolución y manejo mediante fotocoagulación retinal con láser se encuentra bien documentada por importantes estudios clínicos. Actualmente se ha sumado el uso de agentes antiangiogénicos para el tratamiento de sus complicaciones, en especial del Edema macular secundario. Se analizan cuadros clínicos, complicaciones y manejo de la Oclusión de Rama Venosa Retinal y de la Oclusión de Vena Central de la Retina resaltando el uso de terapia intravítrea con Triamcinolona.
The retinal vein occlusion constitute an important cause of deterioration of visual acuity. Their evolution and management through retinal photocoagulation wuith laser, is well documented by important clinical studies.
At present the use of antiangiogenics agents for the treatment of its complications has been added, and especially secondary macular edema. Clinical cases are analysed as well as complications and handling of the Branch Retinal Vein Occlusion and the Central Retinal Vein occlusion.
The use of Triamcinolone and Ranibizumab is highlighted.
Después de la Retinopatía Diabética, las Oclusiones Venosas Retinales (OVR) constituyen la segunda enfermedad vascular retinal más frecuente.
Su prevalencia en la población mayor de 48 años se ha estimado en alrededor de 1,6% (1), siendo su incidencia acumulativa a 15 años alrededor de 1,8% para la Oclusión de Rama Venosa Retinal y 0,5% para la Oclusión de Vena Central de la Retina (2).
Ambos cuadros clínicos cuentan con una historia natural bien delineada por los estudios clínicos Branch Vein Occlusion Study (BVOS) y Central Vein Occlusion Study (CVOS). En los últimos años se han publicado trabajos que muestran resultados del manejo de las complicaciones derivadas de las OVR, especialmente del Edema macular, haciendo énfasis en el uso de terapia antiangiogénica intravítrea.
Trombosis de rama venosa retinalPatogeniaCaracterísticamente la obstrucción se produce a nivel de un cruce arteriovenoso, donde existe una predisposición anatómica local determinada por la presencia de una adventicia común entre la rama arteriolar y la rama venosa subyacente además de cambios arterioscleróticos secundarios a Hipertensión arterial sistémica. Se genera constricción de la vena, alteración del flujo venoso con eventual daño endotelial y oclusión vascular venosa por trombosis (3, 4).
En casos en que la obstrucción no se relaciona con un cruce arteriovenoso se debe sospechar cuadros inflamatorios como vasculitis retinales o retinocoroiditis.
Cuadro ClínicoLa Oclusión de Rama Venosa Retinal (ORVR) suele presentarse alrededor de la sexta década de la vida. El grado de compromiso visual está en directa relación con el área y la ubicación del territorio afectado por la alteración del drenaje venoso, pudiendo ser asintomática e incluso presentarse como entopsias derivadas de hemorragia vítrea secundaria a neovascularización retinal.
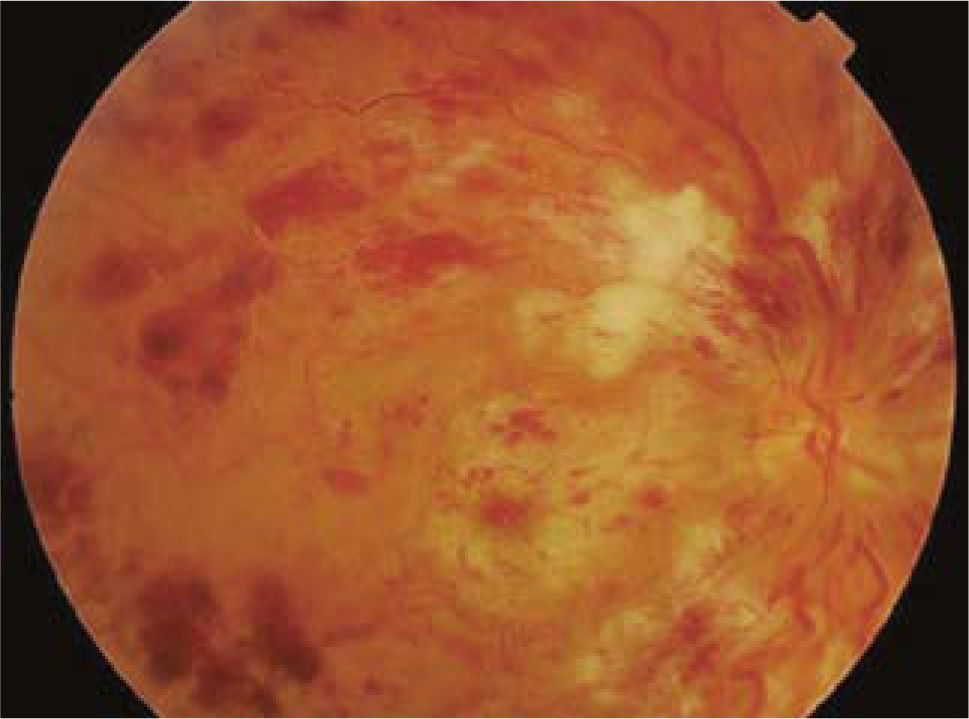
Al examen oftalmoscópico en la etapa aguda destaca la distribución segmentaria de los hallazgos: hemorragias intrarretinianas, tortuosidad y dilatación venosa, manchas algodonosas, edema retinal y eventualmente edema macular (Figura 1). Más tardíamente se pueden encontrar vasos en hilo de plata, desarrollo de vasos colaterales, neovasos y hemorragia vítrea.
Cabe mencionar que con el paso del tiempo esta apariencia característica varía lo que puede llevar a confusión diagnóstica.
Exámenes complementariosLa Angiografía con Fluoresceína entrega valiosa información para el manejo y pronóstico del cuadro. Determina la extensión de la isquemia retinal, estado de la red capilar perifoveal, presencia de isquemia o edema macular, desarrollo de colaterales y presencia de neovasos.
La Tomografía de Coherencia Óptica es útil en la evaluación y seguimiento del edema macular secundario, aunque al igual que en otros cuadros que cursan con EM la mejoría anatómica no necesariamente se asocia a una mejoría funcional (5, 6).
Complicaciones y ManejoLas principales complicaciones secundarias a ORVR están relacionadas con isquemia retinal con desarrollo de neovascularización y maculopatía por isquemia o edema macular.
1- NeovascularizaciónLa presencia de isquemia retinal extensa (mayor a 5 áreas discales) se relaciona con desarrollo de neovasos retinales o papilares en alrededor de un 41%.
En el Branch Vein Occlusion Study (BVOS) se estableció que la fotocoagulación retinal preventiva en casos con un área retinal afectada igual o mayor a 5 áreas discales, reduce la aparición de neovasos de un 22% a un 12%.
Con la fotocoagulación láser de la retina isquémica en presencia de neovasos, se obtiene una reducción del riesgo de hemorragia vítrea de un 61% a 29%. Al ser el beneficio visual más significativo, se recomienda esperar la aparición de neovasos para realizar la fotocoagulación retinal (7).
2- Edema macularEl edema macular frecuentemente es causa de baja de agudeza visual en ORVR, es el resultado del aumento de la presión hidrostática y del incremento de la permeabilidad vascular derivada de la producción de mediadores químicos por parte de la retina isquémica, dentro de estos mediadores destaca el Vascular Endothelial Growth Factor (VEGF), proteína de señal relacionada con la angiogénesis, vasodilatación y potente determinante de aumento de permeabilidad vascular.
El Branch Vein Occlusion Study (BVOS) demostró la utilidad de la foto-coagulación macular en rejilla en casos que cumplieron con los criterios de selección, obteniéndose una ganancia mayor o igual a 2 líneas de agudeza visual en el 65% de los pacientes tratados en comparación a 37% en los no tratados. Al tercer año de seguimiento un 60% de los tratados presentaban agudeza visual ≥20/40 comparado con 34% en el grupo de pacientes no tratados (8).
A partir del año 2002 se han reportado trabajos utilizando Triamcinolona mediante inyección intravítrea (9, 10). Este fármaco además de su efecto antiinflamatorio y neuroprotector, tiene la capacidad de inhibir la expresión del VEGF. Su utilidad en el tratamiento del edema macular secundario a ORVR fue investigado en el estudio Standard Care v/s Corticosteroid for Retinal Occlusion Study (SCORE) donde se comparan 3 grupos de pacientes: inyecciones intravítreas mensuales de 1mg, 4mg y manejo Standard basado en el BVOS. A los 12 meses no existe diferencia entre los tres grupos en cuanto a ganancia, promedio de cambio y pérdida de agudeza visual, siendo los tres tratamientos mejores que la evolución natural de la enfermedad destacando que el tratamiento Standard posee un mejor perfil de seguridad (11).
Más recientemente se ha utilizado con éxito la terapia intravitrea anti-VEGF con anticuerpos monoclonales como el Bevacizumab (Avastin®) (12, 13, 14, 15) o fragmentos Fab de anticuerpo como el Ranibizumab (Lucentis®), agentes que al parecer poseen una actividad similar en cuanto a inhibición del VEGF, pero que aún no han sido aprobados por la FDA para su uso en edema macular secundario a TRVR. El estudio Ranibizuma B for the treatment of macular edema following Branch retinal Vein Occlusion(16) (BRAVO) recientemente publicado compara Ranibizumab en dosis de 0,3mg y 0,5mg con placebo con posibilidad de iniciar terapia convencional si se alcanzaban los criterios BVOS. Los grupos con Ranibizumab lograron mejorías de agudeza visual desde el séptimo día. Los grupos de 0,3mg y 0,5mg lograron una mejoría de tres líneas a los 6 meses en un 55.2% y 61.1% respectivamente versus un 28.8% en el grupo de tratamiento convencional.
El uso de terapia anti – VEGF aparece como un valioso recurso en el tratamiento del edema macular secundario a TRVR, con un alto perfil de seguridad pero aún falta el resultado a largo plazo y la frecuencia óptima de las inyecciones. El futuro del tratamiento del edema macular en TRVR parece estar en el uso de terapias mixtas, mezclando el uso de láser con antiangiogénicos como lo dejan entrever los estudios en curso.
Oclusion de vena central de la retinaPatogeniaLos estudios histológicos sugieren que la Oclusión de la Vena Central de la Retina (TVCR) es la consecuencia de la obstrucción trombótica de la vena central de la retina a nivel de la lámina cribosa y/o posterior a ella. En algunos casos los cambios arterioscleróticos de la arteria central de la retina pueden ocasionar compresión de la vena causando turbulencia con eventual daño endotelial y formación de trombo.
Cuadro ClínicoAlrededor de un 90% de los pacientes son mayores de 50 años al momento de inicio del cuadro, el que se manifiesta por una disminución brusca de visión, sin dolor y sin ojo rojo. Se han determinado factores de riesgo y condiciones asociadas como: Hipertensión arterial sistémica, aterosclerosis, Diabetes mellitus, Glaucoma de ángulo abierto (17). También se ha implicado a enfermedades que cursan con alteraciones de la coagulación o hiperviscosidad sanguínea. De presentarse en pacientes jóvenes siempre se deben descartar patologías predisponentes en particular las trombofilias.
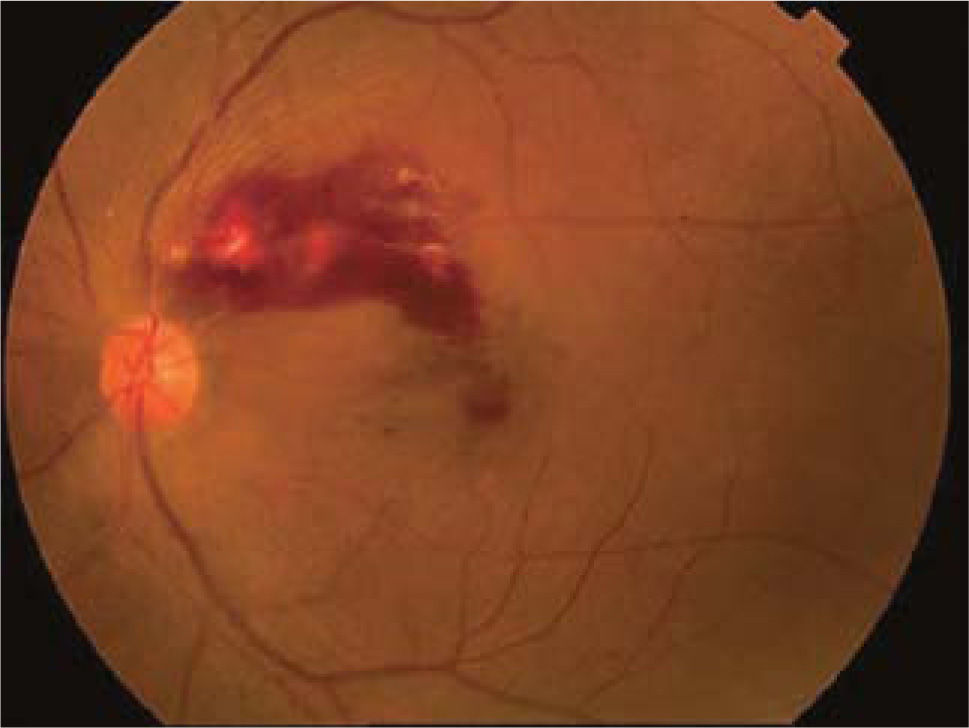
Al examen oftalmoscópico se observan hemorragias retinales en llama y redondas, dilatación y tortuosidad vascular en los cuatro cuadrantes, manchas algodonosas y un grado variable de edema de papila y edema macular (Figura 2).
ClasificaciónEn base a características clínicas y principalmente a la angiografía retinal con fluoresceína, la OVCR se puede clasificar en las formas no isquémica o perfundida, y la forma isquémica o no prefundida, esta última se caracteriza por la presencia de al menos 10 áreas papilares de no perfusión capilar retinal, lo que clínicamente se puede correlacionar con baja de visión importante, escotoma central denso, defecto pupilar aferente, hemorragias retinales abundantes. En general el pronóstico de la forma isquémica en muy malo dada su tendencia a cursar con isquemia macular, desarrollo de neovascularización y glaucoma neovascular.
Evolución y ManejoLas complicaciones más relevantes de la OVCR son la Neovascularización y el Edema macular.
1-NeovascularizaciónEs más frecuente la aparición de neovascularización del iris (rubeosis iridis) que neovascularización retinal. En el caso de la forma isquémica, se puede observar neovasos hasta en un 60% de los casos, lo que habitualmente ocurre dentro de los primeros 3 a 5 meses desde el inicio de los síntomas. El desarrollo de neovasos puede determinar glaucoma neovascular (18).
En el Central Vein Occlusion Study (CVOS) se evaluó la utilidad de la panfotocoagulación retinal con láser en la prevención y tratamiento de la neovascularización del iris y del ángulo iridocorneal. En este estudio no se encontró diferencia estadísticamente significativa en la aparición de neovascularización del iris y del ángulo iridocorneal entre el grupo tratado en forma preventiva y el grupo no tratado. Además se observó que al desarrollarse neovascularización del iris, ésta desaparece antes de un mes postratamiento en un 56% comparado con un 22% del grupo de pacientes tratados en forma profiláctica antes de la aparición de neovasos y que fueron retratados. Por lo tanto la recomendación es un seguimiento cuidadoso y realizar panfotocoagulación retinal al evidenciarse aparición de rubeosis iridis y/o neovasos en al ángulo iridocorneal (19, 20).
2-Edema macularEl aumento de presión hidrostática sumado a la liberación de mediadores químicos por la retina hipóxica tiene como resultado la aparición de Edema macular (EM) que junto a la isquemia macular son determinantes importantes de baja de agudeza visual (REF). De forma similar que lo observado en Trombosis de Rama Venosa Retinal, dentro de los mediadores químicos reconocidos destaca el Vascular Endotelial Growth Factor (VEGF) como responsable del aumento de permeabilidad vascular retinal (21, 22).
Aunque existe disminución del EM angiográfico, el estudio CVOS no observó diferencia en cuanto a mejoría de agudeza visual entre el grupo que fue tratado con fotocoagulación macular en rejilla respecto al grupo que no recibió tratamiento, por lo que no se recomienda como tratamiento de la pérdida visual secundaria a EM (23).
En la última década, al igual que lo que ha ocurrido en el manejo del EM secundario a ORVR, se ha desarrollado el uso de terapia intravítrea con agentes destinados principalmente a bloquear la expresión de mediadores relacionados con el aumento de permeabilidad vascular y vasodilatación, especialmente el VEGF.
El uso de Triamcinolona intravitreo fue evaluado en el estudio Standard Care v/s Corticosteroid for Retinal Occlusion Study (SCORE): a 12 meses se observó una ganancia de 15 o más letras ETDRS en 26,5% y 26,6% (grupos tratados con 1mg y 4mg respectivamente), comparado con 6,8% del grupo sometido al manejo Standard: observación. El promedio de inyecciones durante los 12 meses fue alrededor de 2 para ambos grupos. No existió diferencia relevante en cuanto a complicaciones entre el tratamiento Standard y el grupo tratado con inyecciones de 1mg. (24).
Por lo tanto se puede considerar el uso de Triamcinolona intravítrea en dosis de 1mg en el tratamiento del EM secundario a TVCR.
Desde la primera descripción de su uso intravítreo en casos de EM secundario a OVCR (25), el Bevacizumab (Avastin®) ha sido ampliamente utilizado, existiendo numerosos reportes destacando su efectividad (26, 27, 28, 29, 30), pero también el carácter transitorio de ésta. Actualmente no se ha establecido de manera consistente el esquema de administración más apropiado, siendo necesarios estudios bien diseñados para aclarar su forma de uso.
Por otra parte el estudio Central Retinal Vein Oclussion Study (31) (CRUISE) recientemente publicado evaluó el uso de Ranibizumab (Lucentis®) intravitreo en casos de EM secundario a OVCR para lo cual se compararon dosis mensuales de 0,3mg y 0,5mg y placebo.
Este estudió demostró que el porcentaje de ganancia de tres líneas a seis meses plazo fue de 46,7% y 46,9% en los grupos tratados versus 16,9% en el grupo placebo.
Estos estudios demuestran la gran utilidad de los antiangiogénicos y corticoides en el tratamiento de la OVCR con un buen perfil de seguridad. Queda aún abierta la pregunta sobre la duración del tratamiento y la frecuencia ideal de las inyecciones.
El conocimiento de los mecanismos involucrados en la aparición de las complicaciones de las OVR ofrece un interesante campo de investigación, debido a esto se espera el desarrollo de estudios bien diseñados que orienten un uso seguro y efectivo de las alternativas actualmente disponibles.
El autor declara no tener conflictos de interés, en relación a este artículo.