La complejidad y extensión de las lesiones traumáticas del miembro inferior son muy variables, incluyendo dehiscencias de abordajes quirúrgicos en lesiones cerradas, fracturas expuestas, avulsiones y amputaciones. El aporte de la cirugía plástica en estos pacientes radica especialmente en la reconstrucción mediante la movilización local o a distancia de tejidos vitales bien irrigados. La microcirugía es una herramienta fundamental para lograr reconstrucciones complejas con un diseño versátil, así los colgajos libres otorgan coberturas bien vascularizadas y se adaptan a requerimientos tan diversos. El éxito final de una reconstrucción debe ser evaluado en cuanto a la reinserción del paciente a sus actividades de vida diaria y a su calidad de vida. La coordinación y trabajo con los distintos profesionales necesarios en este proceso permite aproximarse a este objetivo. Revisaremos en este artículo las estrategias de reconstrucción en trauma de extremidad inferior y las técnicas de reconstrucción microquirúrgica más utilizadas.
The complexity and extent of traumatic lower limb injuries are quite variable, including dehiscence of surgical incisions in blunt injuries, open fractures, amputations and avulsion injuries. The role of plastic surgery in these patients lies mainly in reconstruction by local or distant well-vascularized tissue transfer. Microsurgery is an essential tool in complex reconstructions allowing a versatile design. Thus, free flaps provide stable coverage in diverse complexity cases. The ultimate success of reconstruction should be evaluated by reintegration of patients to their activities and quality of life. The coordination and work with the various professionals required in this process can approach this goal. We will review reconstruction strategies in lower limb trauma and the most used microsurgical reconstruction techniques.
La reconstrucción en situaciones de déficit de cobertura cutánea y de partes blandas ha representado un desafío desde los orígenes de la cirugía plástica. Según Sir Harold Gillies, uno de los padres de la cirugía plástica moderna, el desafío de la cirugía reconstructiva es la batalla constante entre el aporte de tejidos bien vascularizados, por una parte y la belleza por otra, es decir el aspecto estético tanto de la reconstrucción como de las zonas dadoras. De esta manera uno de sus principios fue reconstruir “like with like”, es decir, aportar tejidos similares a los que se encuentran en un defecto. Las variables que a menudo son consideradas en la toma de decisiones frente a un defecto cutáneo son:
- -
El tamaño y profundidad de la lesión
- -
Localización
- -
Las zonas dadoras disponibles
- -
Los recursos técnicos y habilidades adquiridas por el cirujano, recursos materiales
- -
Su disponibilidad, condición general del paciente y requerimientos específicos según el desempeño proyectado de una determinada reconstrucción.
Las diferentes opciones pueden ser ordenadas de manera lógica mediante el esquema de escalera reconstructiva, donde los diversos métodos son enumerados de menor a mayor complejidad.
El esquema clásico de escalera reconstructiva incluye:
- •
Cierre secundario
- •
Cierre primario
- •
Injertos
- •
Colgajos locales
- •
Colgajos regionales
- •
Colgajos a distancia
- •
Colgajos libres.
A esto debemos agregar métodos que se han incorporado a la reconstrucción de forma complementaria y en ocasiones reemplazando a las anteriormente mencionadas, como por ejemplo, expansión cutánea, coberturas transitorias biológicas (ej. heteroinjertos, Ez derm®), coberturas sintéticas (ej. Biobrane ®), sustitutos cutáneos y regeneradores dérmicos (ej. Integra®), y sistemas de presión negativas para el tratamiento de heridas (ej. VAC®, Renasys®). Este modelo escalonado permite tener un ordenamiento lógico de las opciones disponibles, pero no se recomienda como estrategia de reparación secuencial. De esta manera, el paradigma actual es el denominado ascensor reconstructivo, donde debemos considerar y efectuar la mejor opción disponible, directamente y sin pasar necesariamente por opciones más simples que no ofrezcan un óptimo resultado1. Así, en un defecto donde se requiere movilización de tejidos vitales distantes, especialmente si la lesión es extensa, o si no hay buenas opciones regionales, un colgajo libre será la primera opción. Incluso en casos de falla de un colgajo libre, en ocasiones la segunda mejor opción sigue siendo un segundo colgajo libre. En defectos postraumáticos de extremidades inferiores, la indicación de colgajos libres con técnicas de microcirugía se realiza principalmente en defectos de diversos tamaños en el tercio distal de la pierna, tobillo y pie. Si bien en defectos más proximales existen más opciones, de igual forma se requerirán colgajos libres cuando estos sean extensos, o en casos donde no hay adecuada disponibilidad de tejidos regionales2.
RECONSTRUCCIÓN DE PARTES BLANDAS EN TRAUMA DE EXTREMIDADES INFERIORESAlternativas de coberturas locales y regionalesLos defectos ubicados en el muslo habitualmente son cubiertos con tejidos locales, dada la gran disponibilidad de piel y musculatura en esa zona. En rodilla y tercio proximal de la pierna el colgajo gastrocnemius medial y en menor medida el lateral, son las opciones más utilizadas en defectos medianos. En tercio medio de la pierna el colgajo sóleo o hemisóleo a pedículo proximal, así como también el gastrocnemius extendido son muy útiles en diversos defectos localizados en la región medial, mientras en la región anterior el avance del músculo tibial anterior puede ser de utilidad en lesiones longitudinales. En el tercio distal de la pierna las opciones locales son pocas, destacándose entre otros el colgajo muscular hemisoleo a pedículo distal y el colgajo sural a pedículo distal. Este último permite cubrir lesiones medianas en tercio medio y distal de la pierna, tobillo y talón, pero en ocasiones su pedículo se encuentra en zona de trauma, lo que lo hace no viable. Además se reportan altos porcentajes de necrosis parciales y reoperaciones. A nivel del pie el colgajo muscular extensor digitorum brevis permite cobertura de defectos pequeños del tobillo y del pie, pudiendo ser elevado a pedículo proximal o distal, basado en a. tarsal lateral y pedia. En la planta del pie resultan de poca utilidad colgajos de musculatura intrínseca. El colgajo fasciocutáneo plantar medial (instep flap) puede otorgar cobertura con piel plantar en talón, tanto ipsilateral de forma pediculada, así como también contralateral como colgajo libre 3,4.
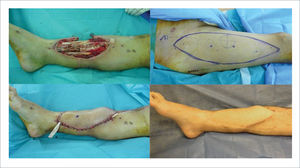
Colgajos perforantesEl desarrollo de los colgajos basados en perforantes significó un gran salto en la forma de enfrentar defectos de cobertura. Los estudios de irrigación de la piel de Salmón5, el mapeo de las perforantes que irrigan la piel y la sistematización de los angiosomas de Taylor y Palmer6, constituyen las bases anatómicas de los colgajos basados en perforantes. Así, los denominados colgajos perforantes consisten en segmentos de piel y tejido subcutáneo, que son movilizados basados en una o más perforantes. Las perforantes pueden tener distintos trayectos, ya sean directas, septocutáneas o musculocutáneas7. Mediante el mapeo de perforantes y la disección retrógrada es posible movilizar segmentos de tejidos con adecuada irrigación y de forma segura, preservando la musculatura subyacente. Los fenómenos hemodinámicos que ocurren al ligar las ramas colaterales o musculares de una perforante, favorecen un flujo sanguíneo abundante al colgajo, reclutando de esta manera vasos comunicantes entre angiosomas adyacentes (choke vessels), logrando perfundirlos de manera adecuada. Surge así el concepto de perforasoma, donde una perforante es capaz de irrigar el angiosoma correspondiente y el adyacente8. Así, en cualquier zona del cuerpo, una perforante de al menos 2mm puede ser utilizada como pedículo para una colgajo de estilo libre (free style), y mediante la disección retrógrada hasta un vaso de mayor calibre, podemos elevar un colgajo para ser transferido localmente o a distancia mediante microcirugía. El uso de los colgajos perforantes pediculados permite reparar defectos traumáticos en extremidades inferiores, de tamaño pequeño o mediano. El colgajo en hélice (propeller flap) constituye un ingenioso método de movilización de colgajos perforantes pediculados. Descrito por Hyakusoku9, el diseño del colgajo se realiza mediante el mapeo de una perforante cercana al defecto. La isla de piel es asimétrica respecto al eje de esta perforante, con una rama corta entre la perforante y el borde más cercano del defecto y una rama larga desde la perforante hacia proximal por una distancia 2cm superior a la distancia existente entre la perforante y el borde distal del defecto. Una vez identificada la perforante, se realiza disección retrógrada por al menos 2cm hasta la arteria y sus venas comitantes (ej. arteria peronea o tibial posterior), para luego elevar el colgajo. El colgajo se gira basado en su perforante (eje de la hélice), el defecto se cubre con la rama larga y la zona dadora se cubre parcialmente con la rama corta, procediendo al cierre primario de la porción proximal del defecto de zona dadora. Este colgajo se diseña habitualmente basado en perforantes de arteria tibial posterior y arteria peronea 10,11, dando solución a defectos pequeños y medianos de tercio distal de pierna y tobillo, con buenos resultados (Figura 1).
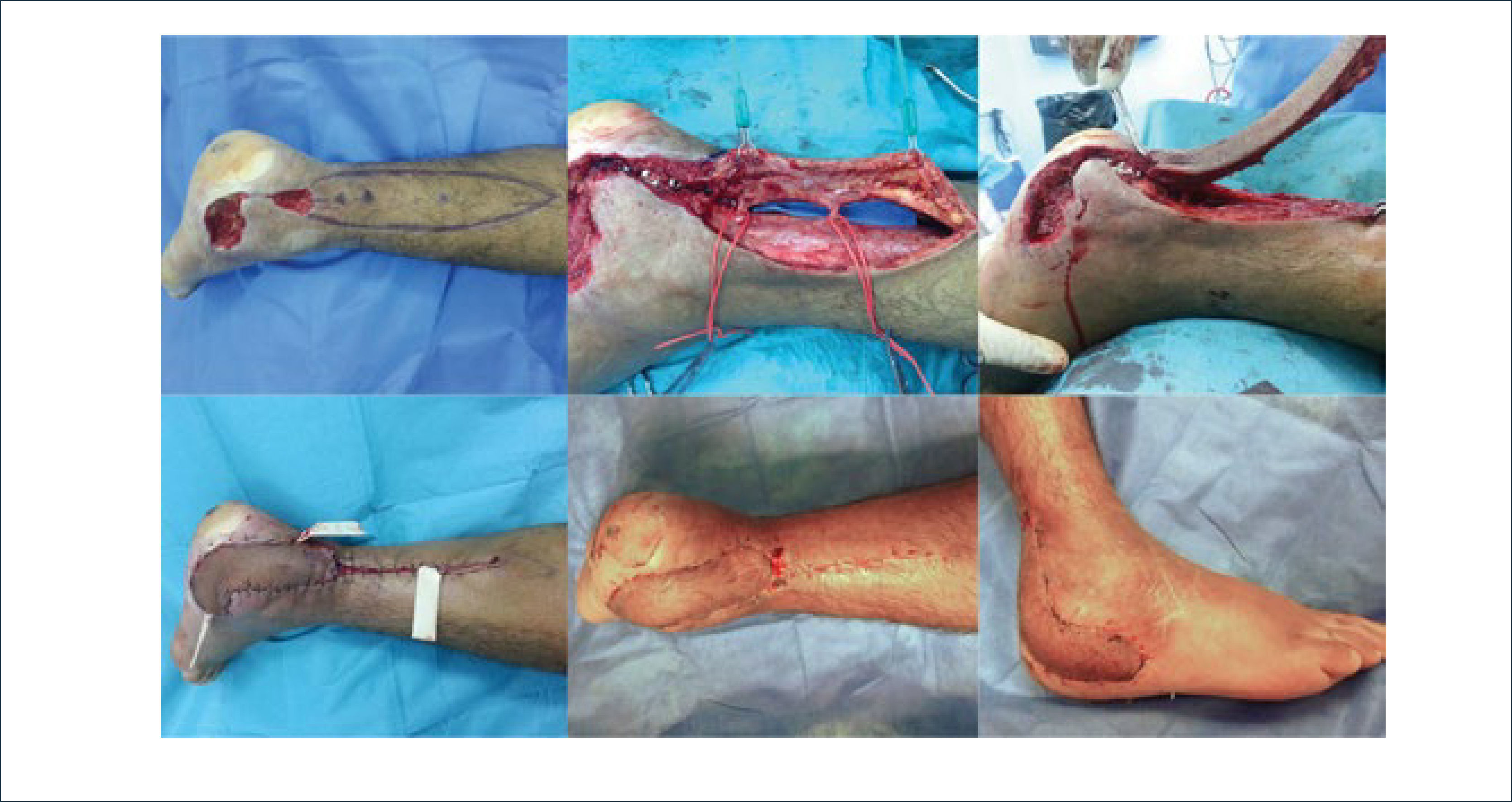
COLGAJO PERFORANTE DE ARTERIA PERONEA EN HÉLICE (PROPELLER FLAP)
Colgajo perforante de arteria peronea en hélice (propeller flap), para cobertura de defecto de tobillo y pie, por necrosis y dehiscencia de abordaje para reducción y osteosíntesis de fractura de calcáneo. Se realizó marcación con doppler de perforantes distales de arteria peronea, y diseño de isla de piel (arriba izquierda). Mediante abordaje anterior y disección subfascial se exponen perforantes mediante disección retrógrada (arriba centro). En este caso se escogió la perforante distal. Una vez completa disección de la perforante, se elevó la isla de piel (arriba derecha). Tras rotar en 180° la isla cutánea, con eje en la perforante, se cubrió el defecto, con cierre primario de la zona dadora (abajo izquierda). Evolución post operatoria visión posterior y lateral de tobillo derecho (abajo centro y derecha)
Defectos de extensión mayor son reparados de manera óptima con colgajos libres, ya sea musculares o fasciocutáneos. Las distintas opciones de colgajos musculares permiten adecuado relleno y cobertura de la mayoría de los defectos post traumáticos, tanto en pierna como en tobillo y pie. Luego de una fase inicial de remodelación espontánea, dada por la atrofia del músculo transportado, los colgajos musculares alcanzan un contorno muy favorable, lo que es especialmente relevante en lesiones del pie. El colgajo gracilis, muy útil en defectos de mediano tamaño, se destaca por una favorable zona dadora, sin secuela funcional, con una cicatriz poco visible y es muy útil en reparaciones funcionales. Limitado en cuanto al tamaño del colgajo, su pedículo mide no más de 5cm y sus vasos tienen un calibre a veces muy reducido (Figura 2). El recto abdominal es de fácil elevación, pedículo de buen calibre y longitud. Si bien puede ser elevado por cicatrices reducidas por abordaje similar a un Pfannenstiel, presenta secuelas importantes en zona dadora, caracterizada por debilidad de pared abdominal remanente. El colgajo latissimus dorsi permite cobertura de lesiones de gran tamaño gracias a su extensión. El pedículo es adecuado en longitud y calibre, pero requiere a menudo realizar el procedimiento de toma del colgajo en una posición diferente a la requerida para la microcirugía y el inset del colgajo. Estos cambios de posición no favorecen el trabajo a dos equipos y consumen tiempo quirúrgico. También es importante considerar que pacientes con traumatismos graves en sus extremidades inferiores, presentan siempre una etapa inicial de movilidad y carga limitada de sus extremidades lesionadas, por lo que necesitan hacer uso de bastones y elementos de descarga y para sus actividades se benefician de la indemnidad de sus extremidades superiores y musculatura de cintura escapular. A esto se suma la eventual posibilidad de una amputación, ya sea por reconstrucción fallida o por otra causa, lo que requerirá de especial manera el uso de musculatura de tronco y extremidades superiores. Actualmente, el caballo de batalla de la reconstrucción microquirúrgica de extremidades inferiores es el colgajo anterolateral de muslo, descrito por Song en 1984, basado en perforantes de la rama descendente de la arteria circunfleja femoral lateral12. Se realiza el diseño mediante el mapeo de perforantes de la región anterolateral del muslo, mediante doppler, identificación y disección retrógrada de la perforante y la rama descendente de la arteria circunfleja femoral lateral. Debe preservarse el nervio del vasto lateral. Un vez completada la disección de la perforante se realiza la elevación de la isla cutánea, sección del pedículo y transferencia a la zona receptora mediante microcirugía (Figura 3). Según la anatomía vascular pueden efectuarse variaciones del diseño, basándose en forma alternativa en perforantes de la rama ascendente o transversa (tensor de fascia lata), o en menor medida como colgajo anteromedial de muslo basado en perforantes que pueden originarse de la arteria femoral superficial, femoral profunda o circunfleja femoral lateral. Las perforantes del colgajo anterolateral de muslo pueden tener un trayecto septocutáneo (entre el recto femoral y el vasto lateral) o musculocutáneo (vasto lateral), siendo su disección más expedita en el primer caso. El colgajo anterolateral de muslo ofrece una gran versatilidad de diseño, tanto de área como de composición del colgajo (cutáneo, fasciocutáneo, miocutáneo, fascial) lo que permite adaptarnos a requerimientos de cobertura y de relleno de distintos defectos. Cuenta con la posibilidad de incluir más de una isla de piel, al incorporar más de una perforante del mismo eje vascular, lo que permite reparar defectos múltiples adyacentes13. Su pedículo vascular alcanza una longitud de hasta 10-12cm con vasos de calibre de 2-2,5mm, lo que permite realizar anastomosis microvasculares a una distancia aceptable de la zona de trauma y de manera segura. Se eleva en decúbito supino, permitiendo así trabajar en dos equipos de forma simultánea, inicialmente elevando el colgajo y preparando zona receptora y luego reparando la zona dadora mientras se realiza la microcirugía vascular y el posicionamiento del colgajo14. Este colgajo puede ser además adelgazado15, para adaptarse a contornos críticos, como el tobillo y pie, tanto en forma intraoperatoria, como en forma diferida mediante remodelación por liposucción. En casos con daño arterial en sitio receptor, el colgajo anterolateral de muslo puede elevarse con su perforante y la rama descendente de la arteria circunfleja femoral lateral, utilizando este segmento como puente vascular (flow-throw), ofreciendo así una opción de revascularización. Si se incorpora la rama cutánea femoral lateral del muslo, puede transferirse un colgajo inervado, lo que puede ser útil en lesiones plantares. Su limitación está dada por la complejidad de la disección y curva de aprendizaje. También debe considerarse contextura del paciente, ya que en pacientes obesos es un colgajo muy voluminoso. Su zona dadora puede ser desfavorable en mujeres, dada su visibilidad y en casos de colgajos muy extensos puede requerir injerto en la zona dadora.
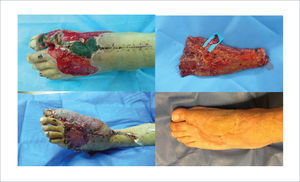
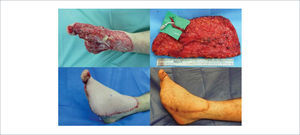
COLGAJO LIBRE GRACILIS PARA COBERTURA DE DEFECTO POST TRAUMÁTICO DE DORSO DE PIE
Presenta exposición ósea y articular en ortejo mayor (arriba izquierda). Colgajo gracilis en mesa operatoria, se destaca el pedículo con lamina azul por debajo (arriba derecha). Cobertura del defecto con colgajo libre gracilis con anastomosis a vasos pedios en forma termino terminal, y cobertura del músculo con injerto de piel parcial mallado (abajo izquierda). Resultado post operatorio con cobertura completa y de buen contorno (abajo derecha).
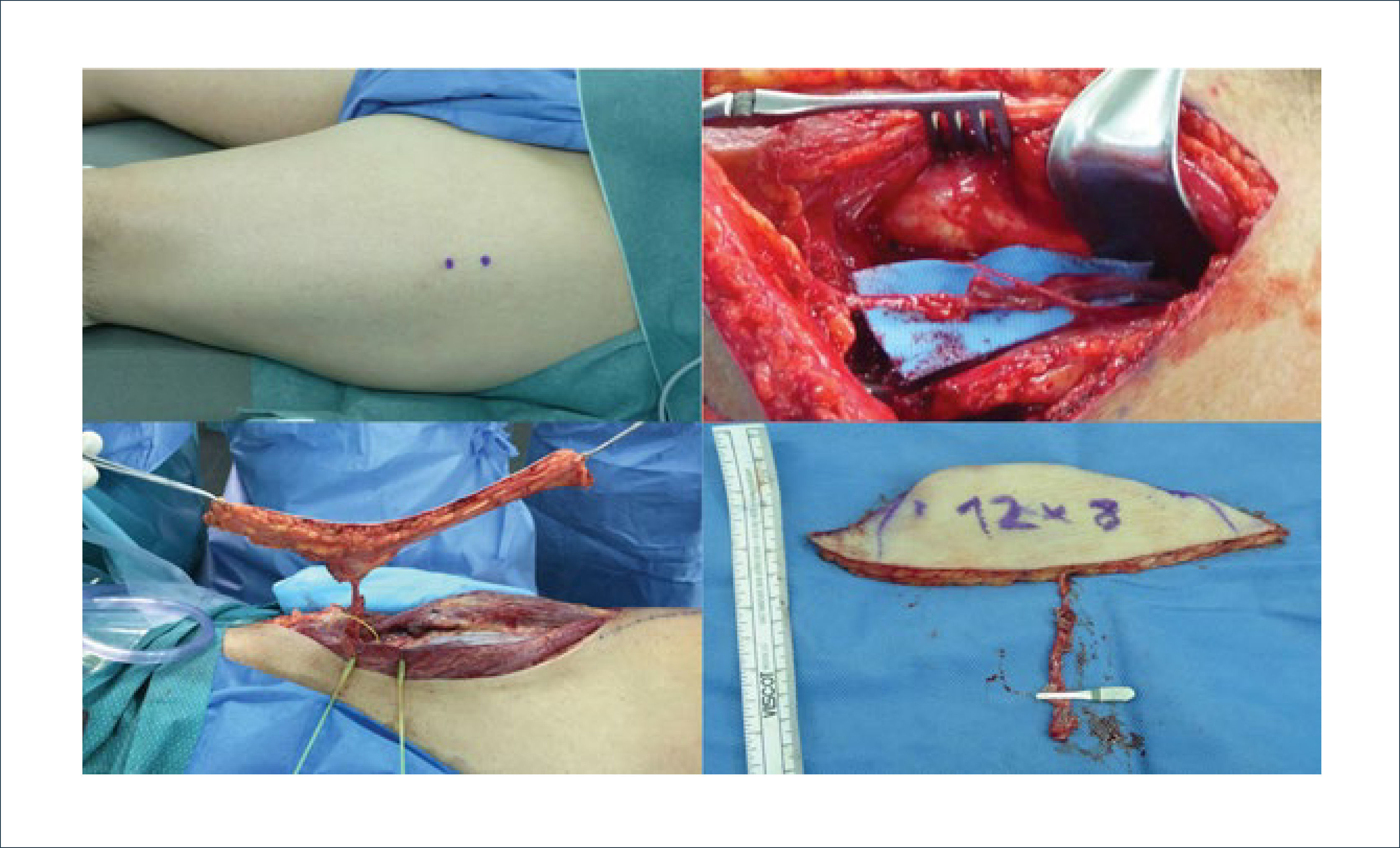
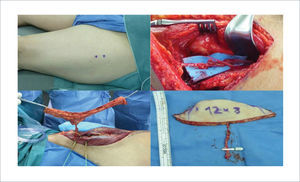
DISEÑO Y ELEVACIÓN DE COLGAJO LIBRE ANTEROLATERAL DE MUSLO
Marcación con doppler de perforantes anterolaterales del muslo izquierdo (arriba izquierda). Disección retrógrada de perforante y de rama descendente de arteria circunfleja femoral lateral, se observa el nervio del vasto lateral preservado y disecado sobre el pedículo vascular (arriba derecha). Isla de piel elevada pediculada en perforante (abajo izquierda). Colgajo en la mesa operatoria luego de la sección del pedículo, se destaca su largo pedículo vascular (abajo derecha).
El estudio de vasos receptores puede ser realizado con ecografía doppler color, que entrega información dinámica del flujo vascular arterial. La tomografía computada en fases arteriales (angiotac) entrega información limitada en el estudio de vasos receptores, ya que no es un estudio dinámico y con frecuencia los pacientes se encuentran con fijadores y/o osteosíntesis que interfieren con esta técnica y que hacen imposible utilizar otras como angio resonancia. En casos de presentar estas limitaciones, y especialmente en pacientes con antecedente o sospecha de daño vascular, debe considerarse una angiografía formal preoperatoria. Las tomografías computadas realizadas con protocolos especiales, destinados a contrastar los vasos perforantes (fases venosas iniciales), permiten una visión topográfica de las perforantes, definiendo con claridad su ubicación, trayecto y calibre. Esto ayuda a planificar de forma más predecible la localización de la zona dadora. A esto se puede agregar la marcación de perforantes por eco doppler color. El doppler sonido de confirmación de las perforantes marcadas es realizado por el cirujano durante la marcación preoperatoria. Si bien se pueden efectuar colgajos perforantes sin este mapeo preoperatorio, la predictibilidad de la técnica es mayor, y los tiempos quirúrgicos se acortan, al seleccionar la perforante óptima con anterioridad.
El diseño del colgajo debe considerar la forma del defecto y ubicación de los vasos receptores en relación al defecto. La anastomosis debe ser situada lo más alejado posible de la zona del trauma. Inicialmente se consideraba de mayor seguridad hacer anastomosis proximales al defecto, pero se ha demostrado que las anastomosis situadas distales al defecto son igualmente seguras. Es recomendable comenzar mediante la exploración de los vasos receptores previo a la elevación del colgajo. Si el estudio preoperatorio es favorable ambas tareas pueden ser simultáneas, con atención en seccionar el pedículo sólo una vez asegurada la disponibilidad de vasos receptores. En extremidad inferior, de preferencia se sugiere realizar anastomosis arteriales término-laterales, preservando así ejes vasculares. Las anastomosis venosas pueden ser efectuadas en forma manual o mediante el coupler venoso, un método con alta tasa de permeabilidad, probablemente menor tiempo quirúrgico y menor curva de aprendizaje16.
Habitualmente se utiliza heparinización local intraoperatoria, y antiagregantes plaquetarios en el postoperatorio, además de heparinas de bajo peso molecular en dosis profilácticas. La anticoagulación formal no ha demostrado reducir tasas de falla y aumenta las complicaciones hemorrágicas, por lo que se reserva para tratamiento de trombosis de vasos receptores, en casos de hallazgo intraoperatorio, o en trombosis de anastomosis microvascular durante o después de la cirugía. La monitorización postoperatoria se realiza mediante el control clínico del colgajo, evaluando su color, consistencia, temperatura y llene capilar. Dispositivos como el doppler implantable (Cook Swartz ®) permiten monitorear de forma continua el flujo arterial y/o venoso y se indica principalmente en los colgajos con mayor dificultad al control clínico, como colgajos musculares o colgajos que quedan sepultados (ej. Fíbula), siendo su principal limitación su alta tasa de falsos positivos, es decir, colgajos que pierden su señal de flujo y que se encuentran en buen estado17. La tasa de éxitos en centros de alto volumen es mayor al 95%, por lo que el costo efectividad de implementar un protocolo de monitorización debe considerar las tasas de fallas de cada centro.
SITUACIONES ESPECÍFICAS EN TRAUMA DE EXTREMIDADES INFERIORESFractura expuesta de piernaLa oportunidad de la reconstrucción ha sido uno de los elementos más debatidos respecto a las fracturas expuestas de tibia Gustilo IIIb. Las publicaciones de Byrd18, y posteriormente de Godina19 establecen las bases de la reconstrucción precoz. Godina revisó 532 colgajos libres en fracturas expuestas, clasificando los procedimientos de reconstrucción como inmediato (<72hrs), precoz (entre 3 y 90 días) y tardío (>3 meses). Reportó mejores resultados en reconstrucción inmediata, con menos fallas de colgajos, menos infecciones, re-operaciones y menor tiempo de consolidación de fracturas, al compararlo con pacientes sometidos a reconstrucción tardía. Destaca que el elemento más importante es un adecuado y completo desbridamiento de tejidos necróticos y desvitalizados, tanto de partes blandas como óseos. La mayor falla de reconstrucciones tardías la atribuye a la fibrosis presente en esas etapas. Otros autores promueven también un tratamiento multidisciplinario agresivo, mediante reducción abierta y osteosíntesis interna, con cobertura inmediata con colgajos y comunican buenos resultados con bajas tasas de infecciones y altas tasas de consolidación. Gopal y cols. revisaron ochenta pacientes consecutivos con ochenta y cuatro fracturas expuestas de tibia (Gustilo IIIb y IIIc), tratados con protocolo radical de debridamiento agresivo, estabilización ósea y cobertura precoz con colgajos en forma inmediata o dentro de las primeras 72 horas. Realizaron nueve colgajos pediculados y setenta y cinco colgajos libres, con una tasa de falla de 3,5%. Registraron cuatro amputaciones (5%). Los autores destacan que la fijación interna y cobertura inmediata se asoció a mejores resultados, comparado con uso de fijadores externos y cobertura diferida20. El impacto en calidad de vida de estos protocolos de tratamiento conjunto interdisciplinario, de traumatología y cirugía plástica, fue estudiado en el año 2004, mostrando buenos resultados en pacientes sometidos a salvataje de extremidades, comparable a lo reportado en pacientes amputados21. La gravedad de estas lesiones se asocia a una tasa de retorno al trabajo que fluctúa entre un 41-76% según series publicadas. Stannard revisó el concepto de reconstrucción inmediata bajo la perspectiva de disponibilidad de sistemas aspirativos de presión negativa, durante el período de delimitación de la lesión de partes blandas. Su uso se ha masificado en el tratamiento de estas lesiones en etapa inicial. El autor reporta una reducción de las tasas de infección en aquellas fracturas expuestas sometidas a cobertura en etapa subaguda, al comparar pacientes tratados con presión negativa versus curaciones tradicionales22. Si bien esta reducción es significativa, no existe comparación mediante trabajos prospectivos que permitan comparar los resultados de un protocolo de cobertura inmediata, con coberturas en etapa subaguda usando terapias de presión negativa como puente. Los dispositivos de presión negativa reducen el edema, mejoran la vascularización de las heridas y formación de tejido granulatorio, mecanismos que pueden mejorar las condiciones locales en espera de la cobertura definitiva23. La limitación más importante para construir protocolos de reconstrucción inmediata, están dadas por la gran contaminación inicial de algunas lesiones, el período requerido para delimitación de las zonas desvitalizadas, que puede tardar algunos días, lesiones múltiples, gravedad del paciente, y logística de organización para disponibilidad de pabellones y equipos quirúrgicos altamente calificados a toda hora. El uso de dispositivos de presión negativa han permitido optimizar el tratamiento de estas lesiones, entre el tratamiento inicial del trauma y la reconstrucción compleja diferida, con resultados comparables a los obtenidos con estrategias de reconstrucción inmediata, similares tasas de infección y de consolidación. La experiencia en lesiones de campos de batalla, en conflictos bélicos recientes, ha servido para explorar los límites de la reconstrucción subaguda, apoyada en terapias de presión negativa y desbridamientos seriados24. En la actualidad se considera aceptable realizar la cobertura y reconstrucción dentro de un plazo no mayor a 4-7 días, con colgajos que permitan prevenir las infecciones, reduciendo desecación y desvascularización ósea 25,26.
Estudios experimentales favorecieron el uso de colgajos musculares por sobre los colgajos fasciocutáneos tanto en fracturas expuestas, especialmente en casos de infección y osteomielitis. Sin embargo, en series clínicas actuales, donde se han incorporado los colgajos basados en perforantes, muestran resultados del todo similares al comparar colgajos musculares y colgajos fasciocutáneos libres. Y si consideramos las ventajas mencionadas de los colgajos perforantes, estos quedarían en una posición más favorable respecto a los primeros27. La variable más importante en el éxito de la reconstrucción de las fracturas expuestas de pierna Gustilo IIIb sigue siendo el momento de la cobertura, lo que requiere una estrecha coordinación y colaboración entre el traumatólogo y el cirujano plástico. La definición de protocolos es crucial para un adecuado tratamiento, ya sea con métodos de fijación interna y cobertura precoz, como mediante el uso de fijadores externos, cobertura secuencial y eventual paso a fijación interna en forma diferida una vez lograda la cobertura (Figura 4).
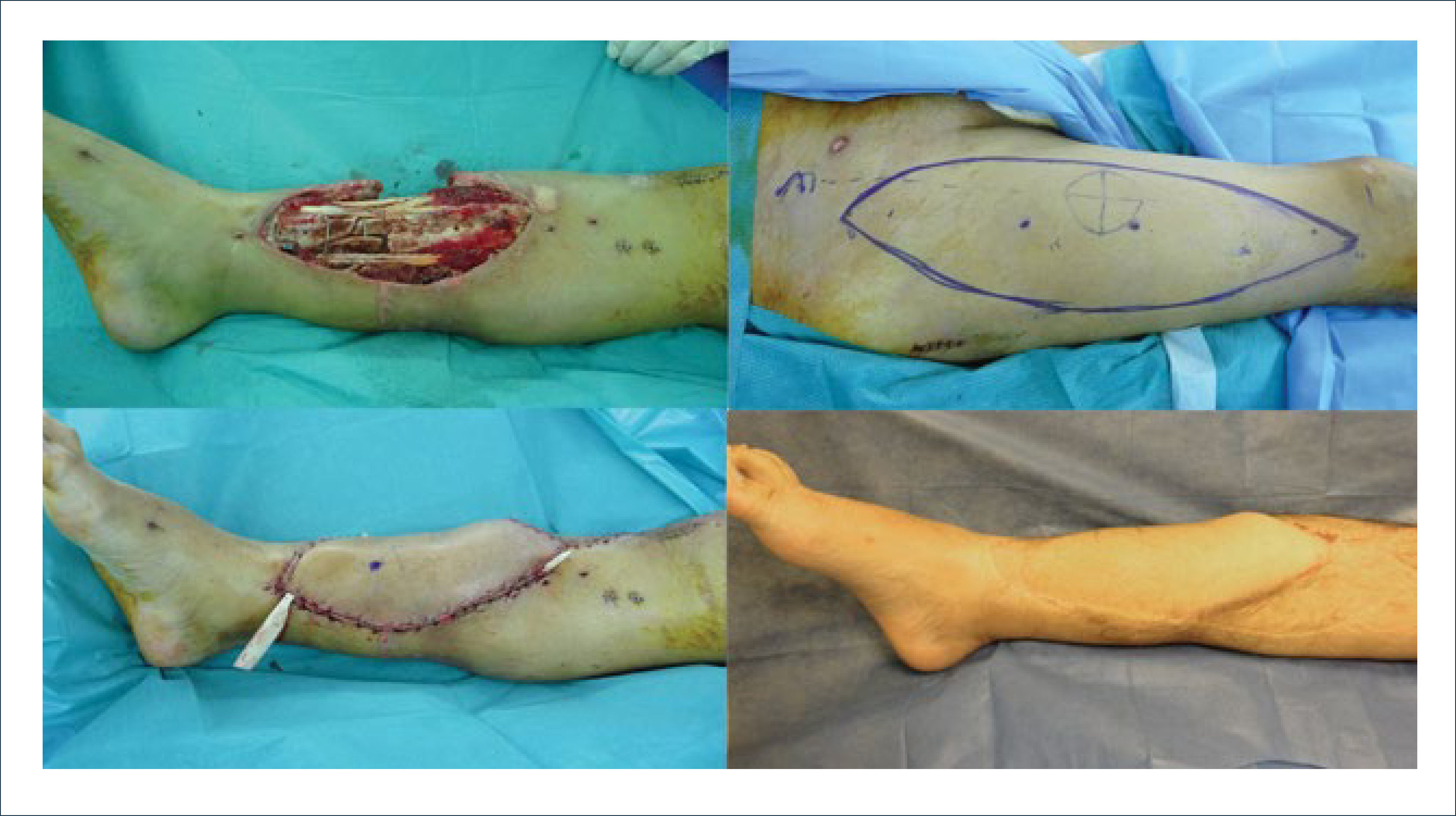
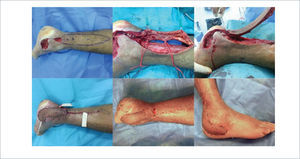
COBERTURA DE FRACTURA EXPUESTA DE PIERNA CON COLGAJO LIBRE ANTEROLATERAL DE MUSLO
Fractura expuesta de pierna derecha, con reducción y osteosíntesis interna (clavo endomedular), defecto de cobertura tercio distal (arriba izquierda). Diseño de colgajo anterolateral muslo derecho (arriba derecha). Cobertura del defecto con colgajo anterolateral de muslo pediculado en vasos tibiales anteriores (abajo izquierda). postoperatorio a los seis meses (abajo derecha).
Los colgajos libres deben ser diseñados en cuanto a sus dimensiones considerando el tamaño real del defecto, no el tamaño aparente. Esto es especialmente relevante en el caso de las articulaciones, donde el déficit de cobertura debe ser cuantificado con la posición de mayor exigencia y no en posición de reposo. La cobertura de lesiones anteriores de rodilla debe considerar los requerimientos en flexión, de esta forma se evitará coberturas complejas insuficientes, que se traducen en cicatrices inestables y restricciones de movilización. En el caso de defectos de cara posterior de rodilla debe evitarse colgajos muy abultados, ya que pueden restringir rangos articulares28. La cobertura de articulaciones con colgajos libres, a diferencia de colgajos locales, o de injertos, permite una movilización precoz de la articulación, lo que reduce el riesgo de rigidez articular. En tobillo, el requerimiento de un contorno apto para el uso de zapatos es crucial. Debemos preferir colgajos delgados, ya sea fasciocutáneos en pacientes delgados, o musculares en pacientes de contextura menos favorable para el uso de los primeros. Es importante considerar que, además de preservar la movilidad articular, es fundamental prevenir el desarrollo de equino. El uso de órtesis confeccionadas por terapeutas ocupacionales es de gran utilidad, pero su efectividad puede verse reducida por la limitaciones que encontrará el terapeuta para adaptar las fijaciones y soportes, según la extensión del daño de partes blandas y la localización del colgajo. En ciertos casos se requiere el uso de fijadores externos para mantener posicionamiento adecuado del tobillo y prevenir el equino. Este punto que debe ser considerado desde las etapas iniciales del trauma, ya que un retraso en la implementación de estas medidas puede llevar al desarrollo de un pie en equino, que requerirá eventualmente corrección quirúrgica, algo habitualmente prevenible.
Cobertura del pieEn términos generales, los defectos extensos del pié son reparados con colgajos libres tanto en el dorso como en la planta. Los defectos dorsales requieren coberturas delgadas con tolerancia al roce, mientras los defectos plantares requieren idealmente colgajos con alta adherencia a plano profundo, poco cizallamiento y tolerancia a la carga. Es recomendable tener especial cuidado en la planificación de cobertura de zonas de carga de la planta, tanto en talón como en antepie. En pacientes sometidos a reconstrucción plantar se desarrolla un cambio en el patrón de carga, redistribuyendo el apoyo a zonas de piel nativa y descargando zonas reconstruidas, de esta forma protegiendo estas áreas de riesgo de ulceración. Defectos plantares masivos no permiten esta adaptación, y el riesgo de ulceración es alto. Se han utilizado diversos colgajos en reconstrucción de talón y se han comparado los resultados obtenidos con colgajos musculares versus fasciocutáneos, sin demostrar claras ventajas de uno respecto al otro29. Si es posible, debe intentarse reparación con piel nativa (glabrous skin flaps), siendo la región plantar medial la única zona dadora disponible. En caso de no disponer de esta zona, o si se privilegia preservar la planta del pie sano contralateral, puede usarse colgajos libres musculares o fasciocutáneos. Los colgajos musculares forman un plano de adherencia fibroso que lo protege de las fuerzas de cizalla y su contorno es adecuado. Requieren injertos de piel parcial y no pueden ser neurotizados. Por otra parte, los colgajos fasciocutáneos permiten diseños versátiles y pueden ser inervados. Desafortunadamente el cizallamiento que se produce causa ulceraciones. No ha sido claramente establecido que la neurotización reduzca este riesgo, aunque sí se asocia a un período de rehabilitación más breve (Figura 5).
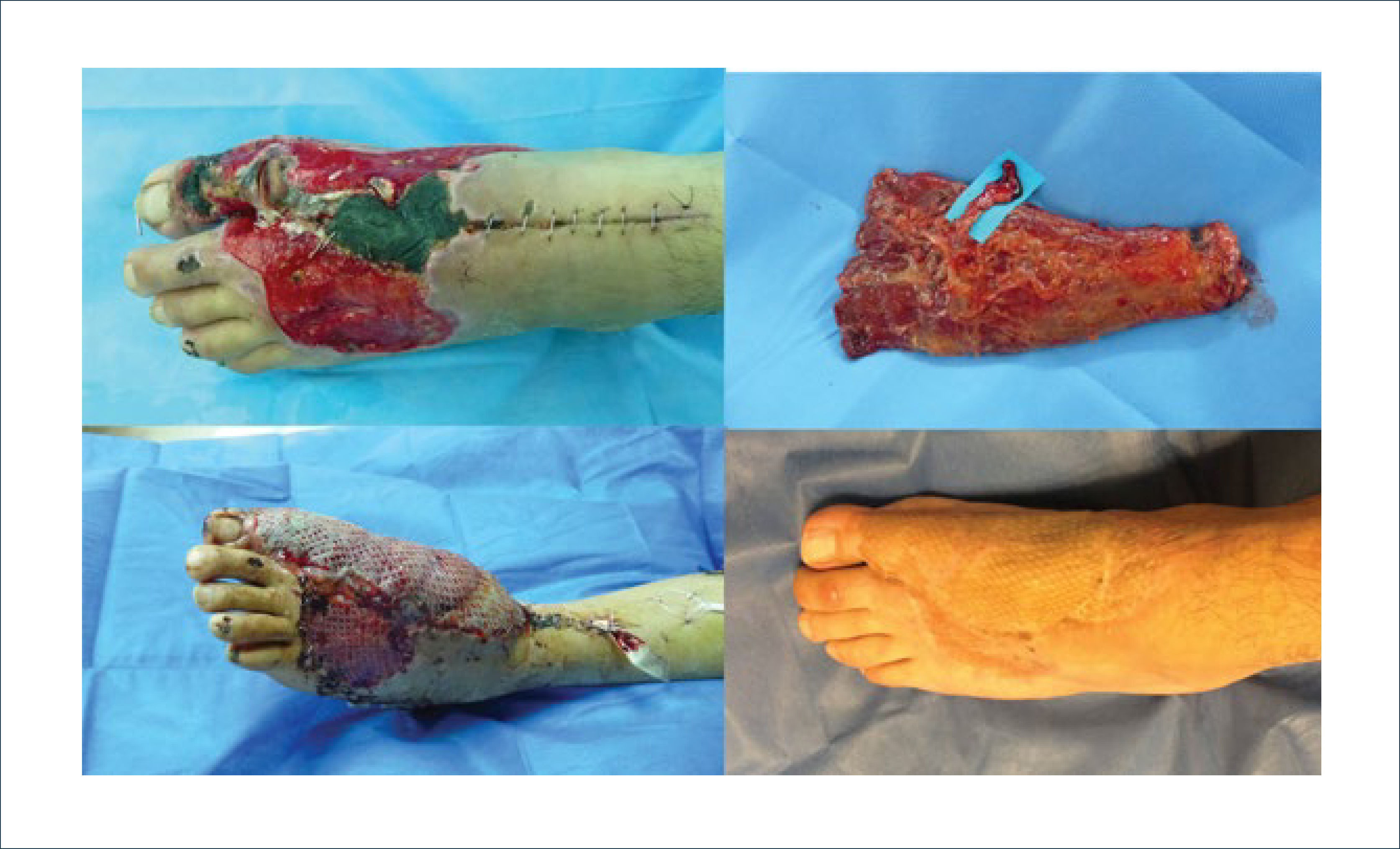
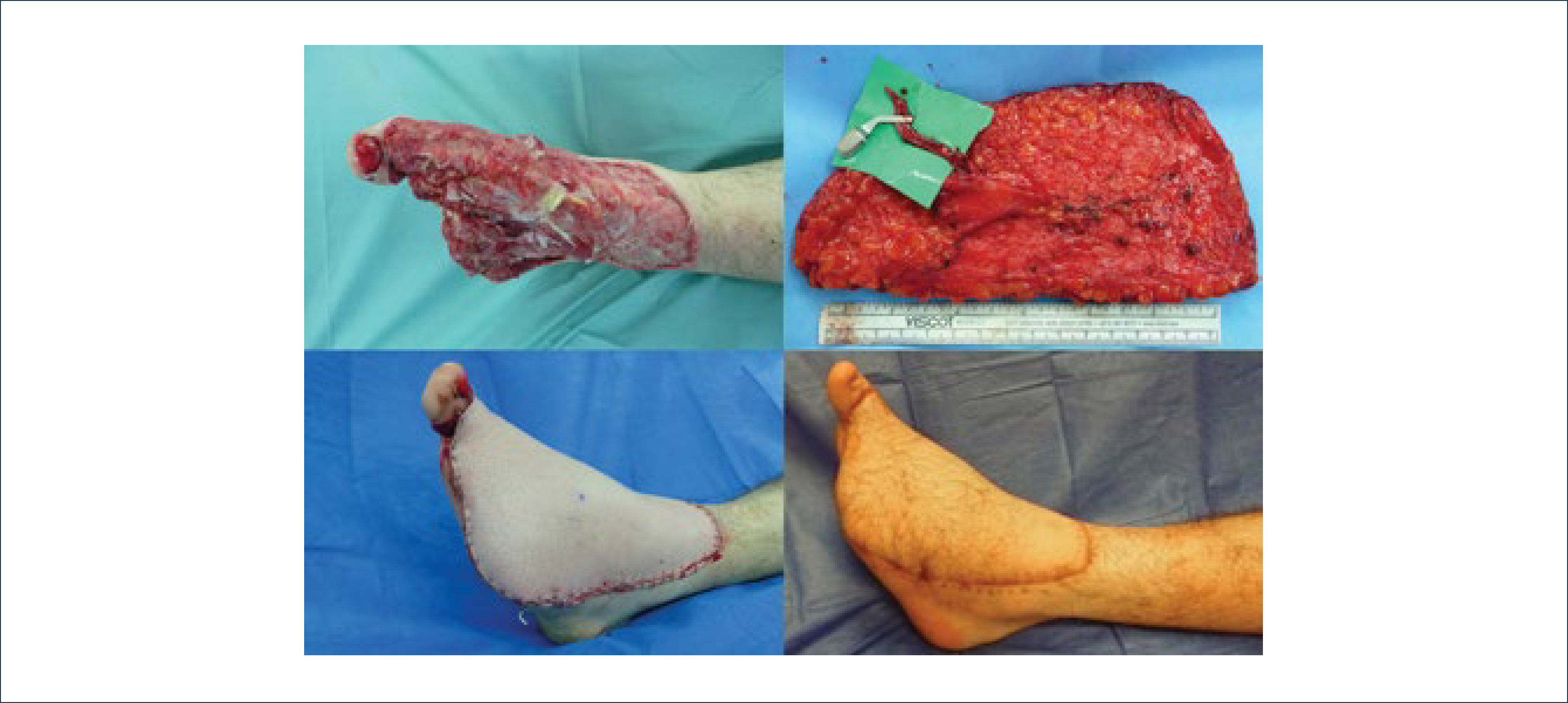
DESFORRAMIENTO Y AMPUTACIÓN TRAUMÁTICA DE ORTEJOS. COBERTURA CON COLGAJO LIBRE ANTEROLATERAL DE MUSLO ADELGAZADO
Defecto de cobertura extenso del dorso del pie izquierdo con exposición de muñones de amputación de ortejos (arriba izquierda). Colgajo anterolateral de muslo adelgazado, disección suprafascial, con fondo de color verde señalando pedículo vascular (arriba derecha). Intraoperatorio con cobertura completa del defecto mediante colgajo libre anastomosado a vasos pedios (abajo izquierda). Postoperatorio a los nueve meses (abajo derecha).
La ostemielitis crónica se presenta habitualmente como falta de consolidación y fístulas crónicas recurrentes. Las imágenes apoyan el diagnóstico, especialmente la tomografía computada y resonancia magnética. Los estudios microbiológicos e histológicos confirman el diagnóstico. El tratamiento es complejo y la tasa de recurrencia es alta. Es fundamental un completo desbridamiento de todos los focos de hueso desvitalizado, pudiendo requerirse resecciones segmentarias, uso de espaciadores de cemento con antibióticos, aseos seriados, antibióticos parenterales por períodos prolongados y aporte de coberturas con adecuado manejo del espacio muerto. Las opciones de reconstrucción ósea son numerosa y los protocolos varían en distintas instituciones. Los injertos óseos se utilizan en defectos de hasta 3cm. Defectos de mayor tamaño pueden ser tratados mediante técnicas de transporte óseo, descrito por Ilizarov30. Estas técnicas permiten reconstruir un hueso de calidad similar a la tibia nativa, con adecuada resistencia y biomecánica. Pueden requerir tiempos prolongados de tratamiento, con riesgos bajos de infecciones locales en sitios de inserción del fijador y desviaciones del eje. En casos de mayor déficit óseo debe considerarse la reconstrucción con aporte de tejidos compuestos, mediantes colgajos libres óseos, los cuales pueden además incorporar tejidos para cobertura31–33. El más utilizado es el colgajo libre de fíbula, el que puede ser sometido a osteotomías para configuraciones en doble barra, lo que permite una mayor resistencia del constructo, dado que la fractura es una de sus potenciales complicaciones, cuando se utiliza en fémur o tibia. Su zona dadora tiene pocas complicaciones. Otras opciones son el colgajo de cresta ilíaca y de escápula, los que tienen menores dimensiones que la fíbula, con las consecuentes limitaciones en su indicación.
DESAFÍOS Y PROYECCIÓN FUTURA: REIMPLANTE Y TRANSPLANTELos reimplantes de extremidades inferiores tienen una indicación controversial, dados los disímiles resultados reportados, influenciados por el nivel de amputación y el potencial de regeneración nerviosa34. Cavadas y cols. Reportaron trece reimplantes de extremidades inferiores bajo rodilla con sobrevida de todos los segmentos reimplantados, los cuales requirieron además colgajos libres para cobertura en zonas que sufrieron necrosis, sin amputaciones requeridas ni ulceras plantares en el seguimiento35. En casos donde el reimplante completo del segmento amputado no sea posible, debe considerarse el uso de tejidos a partir del segmentos amputado (spare parts surgery), que pueden ser útiles para lograr mayor longitud y coberturas en muñones remanentes36.
En el caso de las extremidades inferiores gravemente lesionadas, los resultados obtenidos en casos de amputaciones y salvatajes son difíciles de comparar. Si bien los pacientes con extremidades gravemente lesionadas prefieren habitualmente intentar un salvataje, en este proceso se requieren múltiples procedimientos quirúrgicos de variada complejidad, con eventuales secuelas. Tanto en casos de salvataje como de amputación, los resultados psicológicos y funcionales si bien son similares entre sí, son pobres al compararlos con condiciones basales. Estos resultados dejan en evidencia la necesidad de buscar mejores alternativas. El trasplante de tejidos compuestos ha experimentado un gran auge en los últimos años, lo que invita a considerar el trasplante de extremidad inferior en pacientes amputados, en la búsqueda de un restablecimiento tanto estético como funcional de la extremidad. Teóricamente, comparado con otros alotrasplantes de tejidos compuestos, técnicamente puede ser más sencillo por las características de las estructuras anatómicas que deben ser anastomosadas. La recuperación motora y sensitiva es posible, y el aspecto estético sería más favorable que una extremidad con secuelas o amputada. Entre sus limitaciones debe considerarse los efectos de la inmunosupresión y las limitaciones de indicación en pacientes amputados por patologías vasculares y tumorales37. El primer caso de alotrasplante de extremidad inferior fue publicado el 2006 en siameses isquiopagos de tres meses de edad, a partir del gemelo inviable a su hermana viable, por lo que no se requirió inmunosupresión. A seis años de seguimiento la paciente logró adecuados rangos de movilidad de cadera y rodilla, con limitaciones en movilidad del tobillo, sensibilidad en toda la extremidad trasplantada, pero menor que el lado normal. Pudo caminar y correr en distancias cortas38. El segundo reporte fue el 2010, con trasplante bilateral transfemoral en un hombre de 21 años. A los tres años de seguimiento, el paciente recuperó flexión y extensión de rodilla y algo de movilidad de tobillo, con recuperación progresiva de la sensibilidad, siendo capaz de caminar en barras paralelas39. Presentó un episodio de rechazo agudo y posteriormente desarrolló un linfoma del sistema nervioso central40.
CONCLUSIÓNLa microcirugía ofrece múltiples opciones de reconstrucción de lesiones traumáticas de extremidades inferiores. El aporte de tejidos bien vascularizados es crucial en la reparación de lesiones extensas en trauma, tanto de partes blandas como a nivel óseo. Los pacientes deben ser informados oportunamente de los riesgos y beneficios de las estrategias de reconstrucción que se planteen. La versatilidad de la microcirugía, especialmente de los colgajos basados en perforantes, constituyen una herramienta disponible y segura en la reconstrucción de defectos complejos de las extremidades. El rol del cirujano plástico, con experiencia en procedimientos de microcirugía reconstructiva, es fundamental en el tratamiento de estos pacientes, en estrecha coordinación con traumatólogos y apoyados por numerosos profesionales de otras áreas.
El autor declara no tener conflictos de interés, en relación a este artículo.
Las imágenes de este artículo han sido autorizadas por el paciente o sus padres para su publicación.