La disfagia es la alteración de la seguridad y eficacia del proceso deglutorio que dificulta el correcto paso del alimento/saliva desde la boca hacia el estómago, lo que aumenta la probabilidad de desnutrición, deshidratación y aspiración pulmonar con un consiguiente empeoramiento del pronóstico[1]. Los cambios en el acto de tragar relacionados con la edad se llaman presbifagia[6], un cuadro altamente prevalente afectando entre 13-30% de las personas mayores autovalentes, e incrementando considerablemente, en contexto de hospitalización, al 30-47% por causas adicionales[7]: mecánicas, neurológicas o iatrogénicas, que potencian las complicaciones o desestabilizan el equilibrio deglutorio.
Recientemente la disfagia se considera un síndrome geriátrico[6], lo que conlleva desafíos para el equipo multidisciplinario respecto de prevenir y disminuir efectos adversos[8]. El conflicto principal, es que para el equipo hospitalario resulta un desafío detectar a personas mayores con riesgo aspirativo, por lo que no son identificados a tiempo[6–8]. El objetivo de este artículo es exponer un esquema multidisciplinario de detección de riesgo aspirativo en contexto de hospitalización de la “Unidad Especializada de Cuidado en persona Mayor” (UCAM) de Clínica Las Condes, para lo cual, primero se revisa literatura asociada a disfagia, clasificación reciente, consecuencias, métodos de evaluación recomendados y condiciones específicas, asociadas a riesgo aspirativo y segundo, se definen dos vías junto con Geriatría, Enfermería y Nutrición: 1) Se definen criterios de derivación fonoaudiológica oportunos para evaluación clínica de la deglución, y 2) Método precoz de pesquizaje y evaluación multidisciplinario de disfagia orofaríngea y riesgo aspiratorio.
Dysphagia is the alteration of the safety and efficacy of the swallowing process that prevents the correct transit of food/saliva from the mouth to the stomach, which increases malnutrition, dehydration and pulmonary aspiration and patient's bad prognosis[1]. The changes in the act of swallowing related to age are called presbyophagy[6]. A highly prevalent affect of self-worthy elderly people (between 13-30%), and increasing considerably in hospitalization context (30-47%) for additional causes[7]: mechanical, neurological or iatrogenic, which increases complications or destabilizes swallowing balance. Recently dysphagia it is considered a geriatric syndrome[6], that challenges the multidisciplinary team regarding prevention and reduction of adverse effects related to hospitalization units of elderly people[8]. One of the main tasks of the healthcare team is the early detection of elderly people with aspiration risk. The objective of this article is present a multidisciplinary protocol of EP with dysphagia in the context of hospitalization in the “Specialized care unit for the elderly” (SCUE) of Clínica Las Condes. Initially, literature associated with oropharyngeal dysphagia (OD), recent classification, consequences, recommended evaluation methods and specific conditions associated with were reviewed. Accordingly, two routes are defined with SCUE’team, Speech language pathologist, Geriatrics, Nursing and Nutrition. 1) opportune referral criteria of Speech language pathologist for clinical swallowing evaluation and 2) Early multidisciplinary screening and evaluation method of OD and aspiration risk.
Para comprender el rol del equipo hospitalario en la prevención de aspiración pulmonar y disminución de neumonía en personas mayores, se presentará una revisión de literatura respecto del concepto de disfagia, sus clasificaciones, los cambios deglutorios asociados a la edad y las condiciones del contexto hospitalario y personal que desequilibran el sistema deglutorio aumentando el riesgo aspirativo.
También, se presenta una propuesta multidisciplinaria de detección temprana de los trastornos de la deglución con derivación directa a fonoaudiología y una segunda vía de tamizaje con la participación del equipo hospitalario no experto.
2CONCEPTO Y CLASIFICACIÓN DE DISFAGIACualquier alteración en el proceso de deglución puede definirse como disfagia[1]. Las personas con deficiencias anatómicas o fisiológicas en la cavidad oral, faringe, laringe y esófago pueden mostrar signos y síntomas de disfagia, la que contribuye a cambios negativos en el estado de salud, en particular, un mayor riesgo de desnutrición y complicaciones respiratorias,mayormente aspiración pulmonar[1,2].
Está clasificada como una condición digestiva en la Clasificación Internacional de Enfermedades (CIE) promovida por World Health[3,4], las organizaciones ICD-9 (787.2) y ICD-10 (R13).
Para comprender los trastornos de la deglución, se describen los tipos de clasificaciones en la Tabla 1.
Clasificación de tipos de disfagia
| Clasificación | Subtipo | Descripción |
|---|---|---|
| Según causa | Disfagia Neurogénica (DN) | Originada por alteración neurológica como por ejemplo Accidente Cerebrovascular, Traumatismo Encéfalo Craneano, tumores Sistema nervioso central, entre otras[2]. |
| Disfagia Mecánica (DM) | Es causada por defecto o alteraciones anatómicas tales como tumores de vía aérea, divertículo de Zenker o estenosis[2,3]. | |
| Disfagia Iatrogénica (DI) | Producida por algún efecto colateral de algún procedimiento o intervención como Traqueostomía, intubación orotraqueal, ventilación mecánica, radiación, sedación, medicamentos neurolépticos o antidepresivos, entre otras[2,4]. | |
| Según etapa de la deglución afectada | Disfagia Orofaríngea (DO) | Afecta etapas preoral, oral y faríngea, e implica una dificultad real o percibida para formar o mover un bolo de manera segura desde la cavidad oral hasta la apertura del esfinter cricofaringeo[3]. |
| Disfagia Esofágica (DE) | Afecta la etapa esofágica, que inicia cuando se abre el esfínter esofágico superior (cricofaringeo) para transportar el contenido alimenticio desde esófago con movimientos peristálticos hasta el estómago[2,3]. | |
| Según cambios fisiológicos propios la edad | Presbifagia (PF) | Afectan en mayor o menor medida todas las fases de la deglución por modificaciones producto de los procesos fisiológicos propios del envejecimiento. Existen cambios en eficacia de la deglución pero la seguridad no se ve comprometida inicialmente[6]. |
| Implican una disminución natural de la reserva funcional, que pueden o no estar asociados a deterioro funcional, fragilidad, sarcopenia, otras condiciones geriátricas u otros cambios anatómicos, fisiológicos, psicológicos y funcionales del proceso deglutorio[5,6]. |
En la DO es reportada entre un 13-30% e incrementa con la edad, afectando a 13% de personas mayores de 65 años; 16% en el grupo entre 70–79 años y 33% en mayores a 80 años[7].
3.2Prevalencia en persona mayor hospitalizadaLa DO en PM hospitalizada, es altamente prevalente con reportes entre 30-47%[6,7]. La incidencia anual de neumonía varía en cada centro, pero estudios informan que es mayor en PM con DO (40%) en comparación a los que no la presentan (21,8%)[7]y que es un factor de riesgo significativo para los reingresos hospitalarios en pacientes de 65 años o más[8].
Incluso en PM que no tienen dificultades en la deglución, ciertas condiciones propias del envejecimiento aumentan la prevalencia de aspiración pulmonar en la hospitalización[7,8].
La DO está más asociada con la edad, la capacidad funcional, la fragilidad, la polimedicación y la multimorbilidad[6]. La DO es más prevalente en pacientes ancianos hospitalizados con deterioro cognitivo o funcional[7].
El síndrome de fragilidad se ha asociado a mayor prevalencia (47%) en ancianos con DO entre las PM hospitalizados[6].
La sarcopenia o pérdida de masa muscular de los músculos esqueléticos generalizados y los músculos de la deglución están asociados a DO por la edad[9].
3.3Estudios ChilenosNo existen actualmente datos de prevalencia o incidencia de DO en el adulto mayor en Chile, sin embargo, según los datos del último censo 2017, la población en Chile alcanza a las 17.574.003, siendo el 51% mujeres y 48,9% hombres[10]. Por otro lado, según la encuesta CASEN 2017[11], las personas mayores de 60 años chilenas representan el 19,3% de la población, equivalente a 3.439.599.
Si consideramos los datos generales de DO revisados entre sujetos de 60 a 80 años, con valores entre 13-33%[7], podríamos considerar una estimación actual entre 447.147 y 1.135.067 adultos mayores chilenos con DO.
4CONSECUENCIAS EN personas mayores CON Disfagia OrofaringeaLas dos consecuencias más fuertemente demostradas son:
complicaciones respiratorias y efectos nutricionales[12].
- -
Las complicaciones respiratorias causadas por la pérdida de seguridad de la deglución. Es importante distinguir entre la aspiración pulmonar, que implica el paso del contenido alimenticio por debajo del nivel de las cuerdas vocales hasta el pulmón y la llamada neumonía aspirativa, infección pulmonar con evidencia radiológica de condensación generalmente en el lóbulo superior derecho. Diferentes revisiones de literatura indican que la DO tiene mal pronóstico para las PM con neumonía, se asocian con una mayor mortalidad a corto y largo plazo, aumento de estada hospitalaria y desnutrición[6,7,12].
- -
La desnutrición y deshidratación, es causada por la pérdida de la eficacia de la deglución[13]. Ésta se asocia con un aumento de la mortalidad, la duración de la estancia hospitalaria con un consecuente incremento de costos, restricciones para rehabilitar y mal estado funcional [5,14,15]. Cuando la ingesta oral no es posible, existen vías de alimentación alternativas, ya sea sondas nasoenterales o vías parenterales[1].
Por otro lado, existen consecuencias psicológicas frecuentes, tales como, ansiedad, miedo a la alimentación, vergüenza y frustración, con mayor riesgo de desarrollar depresión e impactar la calidad de vida.
Finalmente, la DO puede resultar en efectos secundarios, tales como, reducir estamina, mayor probabilidad de úlceras por presión, reducción de la recuperación física y reducción de la cicatrización de heridas[16].
5DEFINICIÓN DE PRESBIFAGIA EN LA persona mayorLos cambios relacionados con la edad en el acto de tragar se resumen bajo el término presbifagia.
Actualmente, consensos internacionales[5,6] coinciden en considerarla como síndrome geriátrico, ya que cumple con la definición de éste: Es altamente prevalente, su causa es multifactorial, está asociada a comorbilidades múltiples, pronóstico desfavorable; y necesita un enfoque multidimensional para ser tratada.
La Sociedad Europea de Disfagia describe que la presbifagia presenta cambios en la eficacia de la deglución, pero la seguridad no se ve comprometida[12], sin embargo, en PM la diferencia entre deglución fisiológica o patológica es difícil de establecer y a medida que avanza la edad, se mezclan otros factores de riesgo se puede comprometer también la seguridad[6,12].
Existe también la llamada disfagia sarcopénica, caracterizada por pérdida de masa y fuerza muscular de los músculos deglutorios con alteraciones en todas las etapas de la deglución. Si bien no está aceptada internacionalmente, tiene criterios diagnósticos establecidos: presencia de disfagia; presencia de sarcopenia generalizada; imagenología consistente con pérdida de masa muscular deglutoria; exclusión de otras causas de disfagia. La principal causa de disfagia es la sarcopenia[9].
6PRESBIFAGIA Y CAMBIOS DEGLUTORIOS ASOCIADOS AL ENVEJECIMIENTOEl proceso natural de envejecimiento facilita los cambios fisiológicos en la función de la deglución, produce cambios en la anatomía de cabeza y el cuello, así como en mecanismos neuronales y musculares, con consiguiente pérdida de reserva funcional que puede afectar la deglución[17]. También, hay factores que precipitan dificultades en la alimentación[19].
6.1Factores fisiológicosLa reducción en la masa muscular y la elasticidad del tejido conectivo dan como resultado la pérdida de fuerza y el rango de movimiento[20]. Estos cambios pueden afectar negativamente el transito efectivo y eficiente del bolo por el tracto aerodigestivo superior[21]. Con el tiempo, estos cambios sutiles pero acumulativos pueden contribuir a una mayor frecuencia de penetración de alimento/líquido en la vía respiratoria y mayor residuo oral o faringeo posterior a la deglución[17]. Existe una disminución de la sensibilidad y alteraciones de receptores orales. Si hay presencia de sarcopenia en los músculos masticatorios, y grupos de la musculatura esquelética habrá una pérdida de masa y fuerza muscular especialmente en el músculo intrínseco de la lengua y genihiodeo, también, los músculos de la mímica, masticatorios, suprahioídeos, infrahioídeos, palatinos, faríngeos y esofágicos. Una vez que ocurre atrofia lingual, hay desarrollo de malnutrición secundaria, lo que perpetúa el cuadro. Esto es debido a que los músculos deglutorios están conformados mayoritariamente por fibras musculares tipo II, afectadas en mayor medida por la malnutrición y la sarcopenia comparadas con las fibras tipo I[9].
6.2Factores neurológicosCambios neurológicos propios del envejecimiento producen diferencias en el proceso deglutorio. Las lesiones periventriculares de la materia blanca y la atrofia cerebral se asocian generalmente con una mayor duración de la deglución, dificultad en el inicio y un tiempo de respuesta prolongado, con mayor afectación de las etapas voluntarias o cognitivas[17]. También, existe un deterioro sensorial y un retraso en la conducción de la sinapsis en las entradas aferentes al sistema nervioso central lo que produce respuestas reflejas más enlentecidas y débiles[5] (Tabla 2).
Función deglutoria afectada en cada etapa de la deglución y la cambios fisiológicos asociados a las personas mayores por causa del envejecimiento
| Etapa | Función deglutoria afectada en PM | Cambios Fisiológicos |
|---|---|---|
| PRE ORAL | Existe una alteración en la percepción del gusto, la temperatura y la sensación táctil en muchos adultos mayores[22]. Sequedad oral. | Los umbrales de discriminación sensorial en la cavidad oral y la laringofaringe aumentan con la edad[23]. |
| Existe dificultad en formación cohesiva del bolo y en la activación de la fase voluntaria con la respuesta oportuna de la secuencia masticatoria[6]. | Hay una interrupción de los circuitos de retroalimentación sensorial-cortical-motor[17]. | |
| La pérdida de fuerza orolingual produce dificultades en trituración, por lo que la preparación oral de los alimentos requiere más tiempo[2,24] | La reducción de masa muscular y elasticidad del tejido conectivo orolingual producen pérdida de fuerza[24] y el rango de movimiento[25]. | |
| ORAL | Se reduce la presión lingual y, por lo tanto, disminuye la velocidad de tránsito del bolo[21,24]. La fase oral entonces es de mayor tiempo. | Se asocia a la disminución de la fuerza muscular, la densidad y sensibilidad del receptor sensorial[21,24]. |
| Aunque las personas mayores logran alcanzar las presiones necesarias para deglutir (a pesar de una reducción en la fuerza máxima de la lengua), son más lentas[25].El material transita más lentamente en la cavidad oral, hacia la faringe[17,24]. | Las personas mayores sanas demuestran una presión isométrica (es decir, estática) de la lengua significativamente reducida en comparación con sus homólogos más jóvenes, sin embargo, la presión máxima lingual durante la deglución (dinámica) permanece normal en magnitud[24,25]. | |
| FARINGEA | Hay un retardo en el inicio de la fase faríngea[21]. Activación retardada del reflejo de deglución[17]. Las respuestas faringolaríngeas, como la unión glosopalatal, el cierre velofaríngeo, y el cierre del vestíbulo laríngeo se retrasa significativamente[5,26]. | Atribuida al deterioro de la sensibilidad, una disminución en el número de neuronas en el cerebro y un retraso en la conducción de la sinapsis en las entradas aferentes al sistema nervioso central[18,21]. |
| El cierre laríngeo es más lento y no alcanza a realizarse durante la deglución, con su consiguiente penetración y aumento de residuos faríngeos[26]. | Los eventos orales voluntarios se “desacoplan” de la respuesta faríngea del tronco cerebral[26]. | |
| La penetración del bolo en cuerdas vocales ocurre con mayor frecuencia, en un nivel más profundo y más grave y fallan los mecanismos de tos[18]. | En condiciones de perturbaciones del sistema, las PM tienen menos posibilidades de compensar, por la reducción de la reserva relacionada con la edad[18]. | |
| ESOFÁGICA | Se puede observar estasis intraesofágica (retención de bolo), con potencial riesgo de fluir hacia la traquea o provocar reflujo faringoesofágico[27,28]. | Provocado por la disminución de la motilidad esofágica[18]. Potenciado por una desincronización la apertura del esfínter esofágico superior[28]. |
| Aumenta el riesgo de esofagitis[18,22]. | Potenciada por la disminución de saliva, que en condiciones normales protege al esófago de la inflamación en presencia de reflujo ácido (ya que el bicarbonato en la saliva sirve como un mecanismo neutralizador)[22]. |
Existen cambios que aumentan la susceptibilidad a la presbifagia y puede actuar como un factor precipitante[15]. Se describen como tal, reducción de la producción de saliva, con alteraciones en su densidad y viscosidad (menos humedad oral) con el deterioro de etapas preparatorias y oral[12,18], disminución del estado dental, de la sensibilidad oral y faríngea, reducción de la función olfativa y gustativa (sabor), y de la capacidad compensatoria deglutoria. En la figura 1 se resumen los factores asociados a presbifagia en personas mayores.
Factores asociados a presbifagia en personas mayores[15]. Nota: Indica una función disminuida. Autorizado por Wirth R, Dziewas R, Beck AM.
Bajo la perspectiva de la American Speech-Language- Hearing Association (ASHA)[29] la presbifagia puede exponer a las PM a mayor riesgo de desarrollar neumonía pulmonar. Sin embargo, la evidencia sugiere que los efectos secundarios de otras enfermedades son los responsables de interrumpir la ingesta normal de alimentos y líquidos. Existe evidencia de que la DO y aspiración pumonar están asociados a mayor riesgo de neumonía aspirativa, por lo tanto, es importante considerar, la patología de base subyacente, el motivo de ingreso, y condiciones asociadas a la DO[6–8] (Tabla 3).
Condiciones asociadas a personas mayores hospitalizadas que aumentan el riesgo de aspiración pulmonar por disfagia orofaríngea
| Condición | Subtipo | Descripción |
|---|---|---|
| Compromiso Neurológico | Demencia (D) | Revisiones sistemáticas de disfagia orofaríngea (DO) en demencia31 concluyen que la prevalencia varía de acuerdo al tipo de cuadro entre 13 a 57%. Por ejemplo, en enfermedad de Alzheimer se observa en las primeras etapas, mientras que en demencia frontotemporal en las últimas. Así mismo, las enfermedades progresivas con parkinsonismo (degenerción corticobasal, paralisis supranuclear progresiva, entre otras) tienden a presentar disfagia y disartria en etapas medias de la enfermedad. Se presentan con cambios conductuales de alimentación o alteración de deglución, o ambas31. Estas dificultades pueden estar relacionadas con el deterioro cognitivo, déficits motores como debilidad o apraxia, pérdida de apetito o saciedad (debido a los cambios en la función límbica o hipotalámica), y/o evitación de alimentos, o DO per se, dada por la dificultad en la etapa oral o faríngea. Como resultado, los pacientes con demencia pueden experimentar pérdida de peso y una mayor dependencia para la alimentación[30,31]. |
| E.Parkinson | En enfermedad de Parkinson existe entre el 52-82% de asociación Disfagia Neurogénica (DN) y hay registros de aspiración en el 50% de los pacientes con DN5,6. La latencia promedio desde los primeros síntomas de E. Parkinson hasta la disfagia severa es de 130 meses. Los predictores más útiles de disfagia relevante en la E. Parkinson son el babeo, pérdida de peso o índice de masa corporal y demencia asociada. Los hallazgos en E. Parkinson con DN, describen alteraciones en la etapa oral con movimientos repetitivos de la lengua o signo de rolling, mayor residuo oral, escape posterior prematuro y deglución gradual. En la etapa faríngea existen residuos en valleculas y senos piriformes, déficit somatosensorial, reducción de degluciones espontáneas (48 frente a 71 por hora). Finalmente en la etapa esofágica, podemos encontrar hipomotilidad, espasmos y contracciones múltiples[15]. | |
| Accidente cerebro vascular (ACV) | Es la segunda causa más común de muerte y discapacidad en adultos en todo el mundo32; La DO es una secuela común (27% y 64%) con reportes de Neumonia de 35% según los subtipos14,33 y puede llevar a resultados de salud adversos que van desde la hospitalización hasta la muerte[33,34]. Existe asociación positiva entre DO y la neumonía aspiratoria en PM con ACV de: región insular o frontal izquierda (apraxia deglutoria), Hemisferio derecho (control cortical de fases voluntarias), tronco cerebral (núcleos tracto solitario y ambiguo), lesiones cerebelosas y lesiones bihemisfericas (por daño funcional)[1,33]. Las alteraciones pueden comprometer todas las etapas de la deglución. Pueden haber tanto alteraciones cognitivas como apraxias con dificultad en el inicio de la deglución, o alteraciones neuromusculares con reducción de la motilidad orolingual, ausencia o enlentecimiento del reflejo faríngeo, disminución de elevación laríngea y reducción de la sensibilidad con la abolición del reflejo de tos[12,35]. | |
| Estado de conciencia y confusión | Somnolencia, estupor, sedación y/o agitación | Cualquier alteración del estado de alerta disminuye el control de las etapas voluntarias de la deglución a la vez de producir actos hiporesponsivas de los reflejos involucrados[7,12]. |
| Delirium o estado confusional agudo | Por cualquier causa, ya sea iniciado súbitamente, inducido por medicamentos u otras intervenciones médicas, el estado de variabilidad atencional, desorientación y confusión producen una alteración transitoria de la deglución[18]. Las etapas voluntarias de la deglución, pre oral y oral se afectan mayormente, con dificultad para iniciar el acto deglutorio, formar el bolo cohesivo, realizar el movimiento anteroposterior de la lengua y dar inicio a la etapa faríngea. También, la falta de seguimiento de instrucciones y el desorden conductual predisponen al adulto mayor frágil con protección límite de vía aérea para desarrollar aspiración franca[1,18]. | |
| Causas Iatrogénicas | Intubación orotraqueal, traqueostomía sondas de alimentación. Tiempo prolongados ventilación mecánica. | Pueden producir alteraciones mecánicas o funcionales en la deglución, aumentar su tiempo hospitalario con mayor posibilidad de desarrollar polineuropatía del paciente crítico y alterar el proceso deglutorio[2,12,13]. Se reduce la sensibilidad laringea, con alteración del mecanismo de la tos, menor presión subglótica y en algunos casos alteraciones anatómicas a nivel laríngeotraqueal, como paresia de cuerdas vocales, estenosis, fistulas, entre otros, lo que incrementa el riesgo de aspiración pulmonar[2]. En el caso de traquestomia e intubación, restricción mecánica de la laringe. |
| Causas oncológicas | Tumores cerebrales. Enfermedad de cabeza y cuello | Los tumores o lesiones de cabeza y cuello, carcinoma, infecciones complejas, afecciones tiroideas y diabetes se asocian con disfagia a mayor edad18. Además, algunas cirugías de médula espinal, intervenciones que afecte el nervio laríngeo recurrente pueden provocar disfagia orofaríngea, ya que pueden dañar directamente la anatomía o función de los mecanismos deglutorios15. Los tumores de sistema nervioso central, especialmente a nivel de Bulbo raquídeo o bihemisféricos se asocian a disfagia orofaríngea, ya que ahí están los centros reflejos de la deglución. Regímenes de quimioterapia y radioterapia pueden causar lesiones orofaríngea, xerostomía, mucositis, debilidad muscular, entre otros[2,18]. |
| Sindromes Geriátricos | Adicionalmente las hospitalizaciones prolongadas y el consiguiente período de inmovilidad y posible ayuno aceleran la atrofia muscular por desuso, lo que aumenta la sarcopenia, fragilidad y altera la capacidad funcional y por consiguiente potencian las alteraciones deglutorias al disminuírse la reserva funcional[6.9]. |
La identificación temprana de DO evita resultados adversos de salud, sin embargo, no hay consenso universal sobre la mejor herramienta de screening o evaluación clínica de la deglución para identificación y reducción de aspiración asociada a DO[6,34–36]; más bien, los objetivos y planes son individualizados para ajustarse a escenarios clínicos con un esfuerzo del equipo multidisciplinario[29].
La escalada elegida por el equipo según las recomendaciones son[12–29]:
- a.
Evaluación de screening o tamizaje: Detectan riesgo de aspiración pulmonar asociada a DO y pueden reducir la necesidad de evaluación clínica de la deglución o instrumentales[2–34].
- b.
Evaluación clínica de la deglución: Se realiza por fonoaudiología, para establecer el diagnóstico clínico, considerando si es segura, es decir, si esta ingesta no produce aspiración pulmonar o complicaciones respiratorias[5,6,12], y si es eficaz, es decir, si la persona mayor es capaz de tener una óptima hidratación y nutrición.
- c.
Evaluación instrumental: Son métodos objetivos, pero a la vez más costosos, como la videofluoroscopia o la evaluación fibroscópica de deglución, entre otros[34,36].
De acuerdo a la revisión anterior, el equipo de la Unidad especializada de persona mayor, compuesta por fonoaudiólogos, geriatras, enfermeras, nutricionistas y médicos familiares ha convenido la utilización de instrumentos sistemáticos en la escalada de pesquizaje, que se presentan en la Tabla 4.
Tabla 4.Descripción de método de evaluación de disfagia orofaríngea y consenso interno a utilizar en unidad especializada de pacientes mayores
Tipo Item Descripción Pruebas screening ¿Quién lo realiza? Profesional no experto. Enfermera, Nutricionista u otros profesionales de la salud con sospecha clínica capacitados[34,36]. Método Cuestionarios: Algunas alternativas, son los cuestionarios que se basan en los síntomas de riesgo de disfagia orofaringea (DO) autoinformados. Una de las más utilizados según consenso de autores6,12,34 y traducida al castellano es el Eating Assessment Tool 10 (EAT-10)37.Es un instrumento analógico verbal y unidimensional para el despistaje de la disfagia, cuyos resultados sugieren puntaje de corte > 3 sugerente de disfagia (sensibilidad 89% y especificidad 82%).Cabe mencionar que la utilización del EAT-10 fue implementada en Clínica Las Condes en el 2015 considerando los valores de dicha validación al Castellano. En Chile, se publicó la validación local a fines del 2018, sin embargo, se mantendrán los valores iniciales para homogeneizar nuestra recogida de datos. Pruebas clínicas: Existe evidencia de nivel 2 de que la introducción del cribado de deglución puede reducir la incidencia de neumonía30. Revisiones de literatura6, coinciden en recomendar el Toronto Bedside Swallowing Screening Test (TOR-BSST) desarrollado por Martino, el test de volumen-viscosidad (V-VST) desarrollado por Clavé y el 3-oz wáter swallow Test (WST) de Burke. No existe hasta el momento consenso internacional para recomendar una sobre otra[29,30]. Consenso equipo En el proceso de screening el equipo ha optado por WST38, que originalmente consideraba dar 90ml de agua al paciente. Fue elegida ya que, su outcome fue aspiración (no DO a diferencia de TOR-BSST), requiere materiales de rápida disposición, es de breve duración, el equipo está familiarizado con aquel test y tiene índices de sensibilidad de 97%, y especificidad de 49%. Hay muchas variaciones del WST, pero la recomendación en PM es administrar 60 ml29. Cuando hay al menos uno de los siguientes signos: escape de líquido por boca, Tos, carraspera, estridor respiratorio o baja en saturación de oxigeno mayor a 3%, la prueba se considera positiva[6,38]. Evaluación clínica de la deglución ¿Quién lo realiza? El Fonoaudiólogo[6,29,39]. Método La ASHA y otras revisiones6, 12, 29 reconocen ausencia de consenso respecto de algún instrumento clínico recomendado para PM, pero sugiere basarse en un historial cuidadoso, diferenciando la presbifagia de la DO y esofágica, identificando la causa subyacente, determinando el grado de riesgo de aspiración pulmonar, aspiración silenciosa, definiendo las capacidades y deficiencias del paciente, y el grado en que las deficiencias pueden mejorarse con la terapia[29]. Consenso equipo Se evaluará clínicamente los antecedentes aportados por el equipo, síndromes o factores de riesgo asociados, estado nutricional, preferencias del paciente y la familia[29,39]. Evaluación indirecta: que considera el estado general del paciente, vigilia, capacidad para seguir instrucciones simples, grado de cooperación, higiene y salud oral, examen orofacial, funcionamiento de pares craneales que intervienen en la deglución, presencia de retención de saliva o secreciones en cavidad oral o faríngea, signología de posible aspiración y monitoreo de parámetros hemodinámicos al evaluar la deglución de saliva[2,15,30]. Evaluación Directa: Si el paciente tiene deglución voluntaria, logra carraspeo y esta vigil se procede a evaluar con consistencias semisólidas, líquidas y sólidas (en ese orden) y valorar las etapas preparatoria, oral y faríngea, la presencia de reflejo de deglución, tiempo de desencadenamiento, elevación laríngea, tolerancia a volúmenes y capacidad de tomar medicamentos en el régimen real de la PM, según lo recomendado especialmente en PM con deterioro cognitivo[39,40]. Evaluación instrumental ¿Quién lo realiza? Otorrinolaringólogo (ORL)[41], Radiólogo[41]. Método Evaluación fibroscópica de deglución (FEES) por ORL es la más frecuente, por ser portátil y permitir evaluar al paciente al lado de la cama. Es segura, objetiva y bien tolerada. Usa un nasofibroscopío introducido por las narinas y situada en la entrada del vestíbulo y colorante azul para teñir las consistencias a evaluar y evaluar la etapa preparatoria, oral y faríngea. La ventaja es que permite ver daño estructural o mecánico y evaluar sensibilidad durante la deglución[41]. La Videofluoroscopia (VFC) es realizada por el radiólogo. Es una evaluación dinámica, objetiva y no invasiva que utiliza un medio de contraste (sulfato de bario) para ver todas las etapas de la deglución mediante radiación. Se puede hacer en posición lateral y anteroposterior[41]. Consenso equipo La evaluación de disfagia de deglución es requerida cuando clínicamente hay sospecha de aspiración silente, daño estructural o mecánico faringo.laríngeo, por alteraciones sensibilidad o mecanismo de protección de vía aérea, por lenta recuperación de DO, signos clínicos inconsistentes con evolución, baja seguridad de vía respiratoria y objetivar manejo de secreciones. Es una evaluación invasiva y más costosa, pero segura, bien tolerada y útil para el diagnóstico y tratamiento de la DO[2,6,41]. La videofluroscopia es solicitada principalmente por sospechas de disfunción cricofaríngea, compromiso en etapa esofágica o en casos más complejos para evaluación dinámica de todo el proceso deglutorio, siempre y cuando el paciente pueda trasladarse. En ambos casos no se indicará cuando el paciente esté medicamente inestable para tolerar el procedimiento, cuando no pueda participar (por ejemplo, dificultades cognitivas, nivel inapropiado de alerta) y/o cuando el juicio clínico indica que la evaluación instrumental no cambiaría el manejo clínico del paciente[41]. - d.
Evaluación geriátrica en persona mayor hospitalizada.
Debido a la complejidad de las condiciones de las personas mayores, se recomienda una evaluación geriátrica integral (VGI): un proceso de diagnóstico multidimensional e interdisciplinario para determinar la capacidad médica, psicológica y funcional de una persona mayor para desarrollar un plan coordinado e integrado de tratamiento y seguimiento a largo plazo[42]. La valoración geriátrica integral en pacientes mayores hospitalizados, tiene efectos positivos en la reducción de la mortalidad o la tasa de institucionalización y la mejora de la función física[42].
8.1Pesquizaje, evaluación y diagnóstico multidisciplinario de DO en PM hospitalizadaLa evaluación del riesgo de aspiración pulmonar, debe ser multidisciplinario, que debe incluir al menos médico geriatra, enfermeras, fonoaudiólogos, apoyo de evaluación instrumental cuando sea necesario y nutricionistas. También se pueden considerar otros profesionales según sea el caso[5]. La familia y el paciente deben ser incorporadas en la toma de decisiones[42].
Los objetivos del equipo multidisciplinario para manejar a la PM con DO incluyen[5]:
- •
Identificar tempranamente a la persona mayor con DO.
- •
Diagnosticar cualquier etiología médica o quirúrgica para la DO que pueda responder a un tratamiento específico.
- •
Caracterizar eventos biomecánicos específicos responsables de DO.
- •
Diseñar un conjunto de estrategias terapéuticas para proporcionar a los pacientes una deglución segura y eficaz vía oral, u opción de vía alternativa de alimentación[5,6].
Para equipos de salud, es un desafío reconocer a PM con riesgo de aspiración pulmonar, por lo que, se han planteado dos vías de pesquizaje:
- •
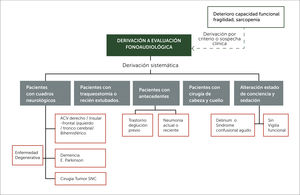
En la primera, se realiza una evaluación clínica de deglución por fonoaudiólogo derivada por geriatra o médico a cargo, guiados por los correspondientes criterios de derivación consensuados por el equipo basado en la literatura. También es válido derivar si los anteriores están ausentes, pero existe sospecha clínica. Al realizar la evaluación clínica de deglución y compartir información con equipo multidisciplinario, paciente y familia se procede a recomendar alimentos, líquidos y/o medicamentos (Figura 2).
Figura 2.Criterios de derivación directa a fonoaudiología para evaluación clínica de la deglución en unidad de hospitalización especializada de pacientes mayores. Nota: La derivación sistemática significa que siempre deben ser derivados a evaluación clínica de la deglución; y la derivación por criterio o sospecha clínica, dependerá de cada médico y antecedentes.
- •
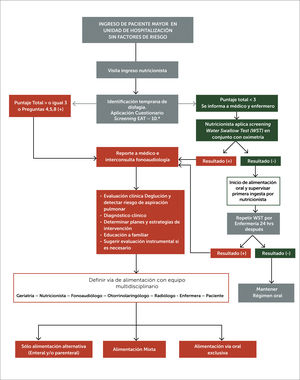
La segunda vía es para pacientes sin factores de riesgos/síntomas claros de DO y riesgo de aspiración pulmonar, que deben ser pesquisados por el equipo de salud cuando están hospitalizados. Se debe seguir el esquema elaborado, pero también se considera válida la sospecha clínica de cualquier integrante al reconocer signos clínicos propios de DO, estar en presencia de síndromes geriátricos de riesgo o notar cambios en la condición clínica del paciente[12]. En este caso se informa a enfermería para que repita el Water swallow test.
En el algoritmo de la figura 3, se muestra el flujograma desde el ingreso del paciente a la unidad, su escalada para pesquizaje precoz de disfagia de parte del equipo hospitalario hasta la definición de la vía de alimentación.
9DECISIÓN DE VÍA DE ALIMENTACIÓNLa decisión de iniciar la alimentación alternativa es éticamente compleja, especialmente en pacientes con compromiso cognitivo, ya que hace reflexionar sobre la vida en la demencia avanzada, y si debe prolongarse artificialmente o bien, dejarla seguir el transcurso natural del fin de vida[31–43].
Existe una tendencia a pensar que en PM la alimentación enteral se puede recomendar cuando la DO es transitoria y de buen pronóstico[44]. El mayor conflicto surge en los cuadros progresivos, en los que no existe evidencia clara respecto si la sonda de alimentación proporciona beneficios en términos de supervivencia, riesgo de mortalidad, calidad de vida, parámetros nutricionales y físicos en las personas con demencia[43].
Diferentes discusiones de expertos intentan tomar posición del tema, pero la evidencia es insuficiente para llegar a consensos (Tabla 5).
Resumen de conclusiones y/o consensos de diferentes grupos respecto a la decisión de vía de alimentación en demencia
| Conclusión | Referencia |
| Respecto de vías enterales de alimentación en Demencia avanzada, no se encontraron pruebas concluyentes de que la alimentación enteral por sonda proporcione algún beneficio en términos de tiempo de supervivencia, riesgo de mortalidad, calidad de vida, parámetros nutricionales, funcionamiento físico y mejoría o reducción de la incidencia de úlceras por presión. Tampoco encontraron evaluaciones sobre el efecto en la calidad de vida, la funcionalidad física o los síntomas conductuales o psiquiátricos de la demencia. Hubo poca información sobre los eventos adversos para estos procedimientos invasivos[43]. | The Cochrane Collaboration.Published by JohnWiley&Sons, Ltd.Review, 2010[43]. |
| En contexto de demencia aconsejan que la alimentación enteral solo se debe considerar cuando la disfagia es transitoria y no se debe usar generalmente con personas con demencia grave[44].NICE recomienda que la alimentación por sonda no se use normalmente para personas que viven con demencia severa. Se puede evaluar si los problemas de deglución son tratables. Esta evaluación ayudará al profesional de salud a explicar los posibles beneficios y desventajas de la alimentación por sonda y las ayudas alternativas. | National Institute for Health and Care Excellence (NICE).London, 2018[44]. |
| Aunque algunos investigadores sugieren que la gastrostomía endoscópica percutánea se debe considerar en personas con demencia moderada – severa cuando hay desnutrición y aspiración, existe el consenso de que la ingesta oral modificada, debe ser el objetivo principal del tratamiento para personas mayores con problemas de alimentación oral[45]. | Royal College of Physicians, British Society of Gastroenterology.London: 2010[45]. |
| El uso de tubos de gastrostomía endoscópica percutánea en la demencia avanzada no mostró beneficios con respecto a la supervivencia, la mejoría en la calidad de vida o la reducción de la neumonía por aspiración[31]. | Archives of Gerontology and GeriatricsKannayiram Et al.2013[31]. |
| Se recomienda la “Alimentación por comodidad únicamente” (o por confort), como opción válida cuando la ingesta oral no es suficiente para mantener la vida, y la persona no desea prolongar la vida con hidratación artificial. Las investigaciones al final de la vida sugieren que a medida que los residentes comen y beben menos, no sufren hambre ni sed[46]. | Registered Nurses’Asociation of Ontario. RNAO. Best Practice Guideline, 2011[46]. |
La decisión debería ser tomada de manera multidisciplinaria caso a caso, según los antecedentes médicos, pronóstico de enfermedad de base, la evaluación de riesgo de DO y aspiración pulmonar, el estado nutricional, las preferencias del paciente y la familia[44,45].
En el consenso interno de Clínica Las Condes, la ingesta oral modificada es la preferencia en PM con dificultades en la alimentación oral, sin embargo, cuando no es posible ¿Qué sucede si el paciente se niega al tratamiento? Hay dos dilemas éticos importantes en el paciente que puede, pero se niega a comer, y el otro, el paciente que está en riesgo pero insiste en comer una dieta no modificada. El equipo debe recordar dos aspectos fundamentales, primero, que debemos informar y explicar las medidas terapéuticas que le permitan disminuir efectos adversos para que eventualmente se adhiera, y segundo, que el paciente tiene derecho a rechazar el tratamiento, para lo cual se debe tener claro la capacidad del paciente para tomar decisiones[6,44.] Finalmente, la alimentación por confort[46] es una alternativa siempre y cuando sea debidamente evaluado por el equipo para dar recomendaciones dirigidas.
10TRATAMIENTO DE LA PM CON disfagia orofaríngeaDurante la hospitalización hay que considerar el componente multifactorial de la DO, las comorbilidades presentes y el enfoque multidimensional para ser tratada[6]. El objetivo del tratamiento de la PM con DO tiene por objetivo reducir el riesgo de aspiración pulmonar, restablecer la eficacia y seguridad del proceso deglutorio (cuando es posible), mantener el estado nutricional, minimizar el impacto en la calidad de vida y educar al paciente y familiar[5,18]. Para lo anterior, el fonoaudiólogo utiliza un conjunto de medidas con el equipo de rehabilitación.
10.1a. Reducir el riesgo de aspiraciónEl manejo fonoaudiólogico en la PM hospitalizada considera fuertemente el concepto de intervenciones Mínimo–Masivas (IMM) que tienen como objetivo tratar con medidas simples y económicas la alta prevalencia de DO en PM[47]. Éstas son aproximaciones terapéuticas basadas en la evidencia y proponen un abordaje precoz con las siguientes recomendaciones:
- •
Evaluación de la DO con una herramienta clínica y la posterior adaptación de líquidos y texturas para mejorar la seguridad.
- •
Mejorar el estado nutricional de los pacientes a través de la triple adaptación dietética propuesta por la AMDA The Society for Post-Acute and Long-Term Care Medicine.
- •
Evaluación y tratamiento de la salud e higiene oral para impedir la colonización de agentes patógenos en la cavidad oral.
El fonoaudiólogo junto a la evaluación instrumental (cuando sea necesario) integra la experiencia clínica individual con la mejor evidencia externa disponible[30,39] para utilizar tratamientos específicos. Aún faltan datos para determinar la efectividad de éstos[48]. Se sabe que los tratamientos tradicionales para la DO son costo-efectivos, logran disminuir la frecuencia de neumonía aspiratoria y el tratamiento varía según cada centro[5].
Cuando la DO es severa se utiliza régimen cero vía oral, inicialmente con intervención del fonoaudiólogo, para reactivar el proceso deglutorio, en la medida de lo posible. Se realiza estimulación, no nutritiva con mínimo sabor, incremento sensorial y facilitaciones para estimular los mecanismos neuromusculares y deglutorios, posteriormente ingesta terapéutica (sólo por fonoaudiología) aumentando progresivamente los volúmenes/consistencias y, finalmente cuando ya es seguro y eficaz, el entrenamiento a entorno para asistir/supervisar la alimentación hasta lograr independencia[29,39].
Según el tipo de colaboración y objetivo, se utilizan diferentes estrategias terapéuticas[49].
Maniobras deglutorias: Requieren colaboración del paciente y son utilizadas para reestablecer alteraciones biomecánica y fisiología deglutoria[5,49].
Técnicas compensatorias: Incluyen modificación en volumen y viscosidad de los alimentos y cambios posturales que tienen potencialidad de cambiar momentáneamente las dimensiones de la faringe, cambiar la dirección del bolo y reducir penetración a la vía aérea. Son fáciles de realizar y no generan fatiga en el paciente.
Técnicas de facilitación[29,39]: Producen cambios transitorios en el circuito deglutorio que favorecen el proceso deglutorio. No son duraderos. Estas serán utilizadas en PM según patología de base, pronóstico y fisiopatología deglutoria (Tabla 6).
Estrategias de tratamiento de la deglución de PM con disfunción orofaríngea
| Subtipo | Descripción |
|---|---|
| Maniobras deglutorias | |
| Maniobra supraglótica y super supraglótica | Tiene como objetivo el cierre de las cuerdas vocales antes y durante la deglución para proteger la vía aérea[2]. |
| Deglución con esfuerzo | Esta maniobra pretende mejorar la fuerza de propulsión del bolo durante la deglución y aumentar la fuerza de contracción de la musculatura deglutoria [2]. |
| Maniobra de Mendelsohn | Mejora la elevación laríngea y el tiempo de elevación, además permite una mayor apertura del esfínter esofágico superior[2]. |
| Maniobra de Masako | Es realizada para compensar la reducción del contacto de la base de la lengua con la pared posterior de la faringe[5]. |
| Programa de ejercicios y entrenamiento funcional | Mejora la fuerza, rango de movimiento y velocidad de las estructuras orales y faríngeas implicadas en la deglución con el objetivo de mejorar la fisiología deglutoria conllevando a un aumento en la sensibilidad faringolaríngea y tonicidad[29,39].Los ejercicios linguales progresivos (8 semanas) mejoraron las presiones isométricas y el volumen de la lengua, sugiriendo que este enfoque ayudaría a prevenir la disfunción orofaríngea (DO) debido a la sarcopenia (evidencia científica nivel B)[30].Ejercicios para mejorar la función labial, lo que mejora la formación y homogeneidad del bolo en la cavidad oral producen mejoras en la etapa oral[39].Otras técnicas adicionales de rehabilitación de la deglución, como el entrenamiento de la fuerza muscular espiratoria, aumenta la fuerza de los músculos suprahiodeos, mejora la presión espiratoria y, por lo tanto, la protección de la vía aérea (speech). |
| Técnicas compensatorias | |
| Postura | Se recomienda que la PM se alimente en posición 90° y realizar reposo posterior a la ingesta al menos entre 45-90° por 30 minutos[1]. |
| Chin Down | Se utiliza cuando hay retraso en el reflejo deglutorio, escape posterior precoz, entre otros. Acorta la distancia entre el hiodes y la laringe, favoreciendo el cierre de la vía aérea.No es adecuada para todos los pacientes. La flexión extrema puede hacer que las vías respiratorias sean propensas al colapso, y está contraindicada para PM con constrictores faríngeos débiles. La técnica afloja los constrictores y aumenta el riesgo de aspiración en esta población[39]. |
| Extensión de cabeza | Se utiliza por mal transito oral y/o propulsión lingual, pero con indemnidad en la fase faríngea. Favorece el paso del bolo hacía la faringe por gravedad[1]. |
| Rotación de cabeza | Se utiliza en debilidad unilateral. Se rota la cabeza hacia el lado enfermo. Direcciona el alimento por la musculatura sana, produce un peristaltismo y presión negativa eficiente con reducción de residuos faríngeos[2]. |
| Doble deglución | Se utiliza para reducción los residuos post deglución en cavidad oral y faríngea. Se solicita una segunda deglución previo a una nueva inspiración[2]. |
| Cambios en el volumen y la viscosidad | El uso de espesantes es una técnica comúnmente usada, disminuyendo la frecuencia de penetración laríngea y aspiración a vía aérea. A mayor viscosidad es más segura la deglución y disminuye el riesgo de aspiración, pero también disminuye el agrado y el confort con éstos alimentos[47].El conflicto es el bajo confort y agrado por el cambio de sabor y viscosidad que generan, provocando que la tolerancia al uso de espesantes varíe entre el 48% y 56%[47].Existe una falta de consenso. En este contexto The Society for Post Acute and Long Term Care Medicine (AMDA) ha propuesto una triple adaptación dietética que determina las texturas y espesor de los alimentos, contenido proteico/calórico y las propiedades organolépticas de los alimentos[47]. |
| Técnicas de facilitación | |
| Aumento del input sensorial | Se utilizan en momento previo a la ingesta deglutoria, para mejorar la latencia del disparo del reflejo deglutorio utilizando la estimulación de aferencias deglutorias[2,30].Las estrategia para aumento del input sensorial son la estimulación térmica de la lengua y de los pilares anteriores de la faringe, el uso de sabores ácidos y temperaturas frías5, estimulación del gusto con combinación de sabores ácido, amargo, dulce o salado, estimulación táctil en zonas intra y extra oral con masajes y toque con los dedos, estimulación de la salivación a través de los olores y la visión. |
| Nuevos recursos | |
| Se utilizan cuando se requiere aumento de input sensorial de la via aferente deglutoria[49].Presentan evidencia cuestionable39. Están basados en la estimulación periférica como la electroestimulación neuromuscular5, 49 y la estimulación química o farmacológica a través de la Capsaicina o Piperina que actúan como moléculas agonistas del receptor de membrana TRPV1 permitiendo un aumento en la estimulación sensorial de la vía aferente deglutoria[12].El taping además logra la estimulación del tegumento específico con respectiva activación de la corteza sensorial y aumento de propiocepción[39]. | |
| Apoyo médico | |
| Toxina Botulínica | Se utiliza cuando hay alteración del esfínter esofágico superior (en ocasiones se resecciona el músculo cricofaringeo)[5].Manejo de sialorrea o de paciente hipersecretor[41]. |
El fonoaudiólogo trabaja estrechamente con nutricionistas, ajustándose a las preferencias del paciente, con modificaciones de volumen y viscosidad de alimentos, controles de ingesta calórico proteicos diarios por parte de nutricionistas, progresión en consistencias evaluadas por fonoaudiólogo y en ocasiones algunas estrategias avaladas por guías internacionales, como “Protocolo de agua libre”[50], que producen una mejor ingesta de líquidos (aumento del 10% de los requerimientos) mejoras en calidad de vida, sin aumento de efectos adversos (aspiración o neumonía) con el uso juicioso del protocolo junto con estricta higiene oral. Este protocolo permite que las PM con DO especialmente seleccionadas, a las que normalmente se le recomiende solo líquidos espesados, también tengan acceso al agua no espesada. El agua es lo único permitido; por ser el fluido más seguro (ph neutro) en caso de aspiración, otros como café, té, jugo están prohibidos. No se permite el agua en las comidas o para medicamentos orales. La higiene oral es requisito clave[50].
10.4d. Minimizar el impacto en la calidad de vida y educar al paciente y familiar[5,18].10.4.1Adaptaciones instrumentalesEl fonoaudiólogo trabaja con terapia ocupacional para lograr la mayor satisfacción e independencia funcional. La eliminación de distractores, adaptaciones ambientales y las ayudas técnicas para comer y beber ayudan a dirigir y controlar el bolo de alimento o líquidos y a mantener las compensaciones durante la alimentación; algunas opciones son las tazas modificadas con escotadura, bombillas que evitan la elevación de cabeza, cucharas de menor tamaño (de te) o individuales especiales que llamen la atención del paciente, entre otros[18]. Estas estrategias deben ser implementadas entre el equipo, paciente y familia[18].
10.4.2Ejercicio físico y recuperación motoraEn periodos largos de hospitalización, para prevenir la pérdida de masa muscular y posible disfagia sarcopénica, se debe incluir una combinación de entrenamiento deglutorio, nutrición y de recuperación motora que repercute directamente en la musculatura deglutoria[16]. El apoyo con el kinesiólogo es fundamental, ya que el papel del ejercicio físico es recomendado no únicamente por el incremento de la masa muscular, sino también porque genera una reducción de la inflamación e infiltración muscular grasa, e incrementa la presencia de células satélites musculares[9].
10.4.3EducaciónLuego de incorporar todos los ajustes, el paciente, familia y cuidador debe recibir todas las recomendaciones de alimentación segura, adaptaciones instrumentales, objetivos nutricionales e higiene oral. Junto con ello alertar sobre los signos de neumonía aspirativa y adaptaciones en el hogar[6,29,39].
11ConclusiónEl artículo trata de informar respecto a la DO en PM y las condiciones que potencian el riesgo aspirativo en la hospitalización, tales como compromiso neurológico, estado de conciencia y confusión, causas iatrogénicas (tubo endotraqueal, sonda enteral, traquestomia, ventilación mecánica), causas oncológicas y algunas síndromes geriátricos asociados a DO como fragilidad, sarcopenia, multimorbilidad y polimedación, lo que le permite al profesional no experto en deglución, tener mayores herramientas para la detección precoz de riesgo aspirativo.
Se expone el consenso interno de pesquizaje de riesgo aspirativo en PM con el objetivo de disminuir efectos adversos y se incorpora al equipo de salud mediante dos vías:
- 1)
A cargo del médico y/o enfermera que deben conocer los criterios de derivación a fonoaudiología para evaluación clínica de la deglución.
- 2)
Un método de tamizaje multidisciplinario cuando no hay signos claros de riesgo (aplicado a todos los pacientes de la unidad), el cual, incluye la escalada recomendada[6,12,30] combinando pruebas de tamizajes con cuestionarios aplicados sistemáticamente por nutricionista, seguido de evaluación de screening realizados por nutricionista y enfermera, evaluación clínica de la deglución por fonoaudiólogo y por ORL o radiólogo en conjunto con la valoración geriátrico integral aplicada por geriatra.
Esto permite involucrar al equipo en la prevención y toma de decisiones compartida en la cual, los profesionales comunican resultados de la valoración clínica, opciones de tratamiento y los pacientes informan sobre sus preferencias.
Declaración de conflicto de intereses
Los autores declaran no tener conflictos de intereses.












![Factores asociados a presbifagia en personas mayores[15]. Nota: Indica una función disminuida. Autorizado por Wirth R, Dziewas R, Beck AM. Factores asociados a presbifagia en personas mayores[15]. Nota: Indica una función disminuida. Autorizado por Wirth R, Dziewas R, Beck AM.](https://static.elsevier.es/multimedia/07168640/0000003100000001/v1_202002011451/S0716864019301117/v1_202002011451/es/main.assets/thumbnail/gr1.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)