A partir de la década de los 80, las enfermedades raras han ido adquiriendo un lugar prioritario en los programas de salud y en la opinión pública. Se definen como aquellas que tienen una prevalencia menor a 1:2.000 individuos. En general son enfermedades crónicas, invalidantes y en más de un 80% de origen genético. Se estima que existen entre 7.000 y 8.000 enfermedades raras y que afectan al 6-8% de la población. Dada la baja prevalencia específica de cada afección, hay muy poco conocimiento de parte de la comunidad médica en relación a su diagnóstico y manejo. En este artículo se discute la importancia del diagnóstico de precisión, para su adecuado manejo y asesoramiento genético, también se muestra la importancia del trabajo en redes en las enfermedades de baja prevalencia y se destaca el rol fundamental de las agrupaciones de padres y familiares en promover políticas de salud para los afectados.
From the early 80's rare diseases had achieved a priority role in national health programs and in public opinion. Rare diseases are define as the ones who have a prevalence lower than 1:2000 habs. Generally, they are chronic and life threatening diseases and more than 80% of them are from genetic origin. It is estimated that there are between 7,000 and 8,000 different rare diseases affecting 6-8% of world population. Due to the low prevalence of each disease, there are very poor knowledge in the medical community about their diagnosis and management. In this review we discuss about the importance of the precise molecular diagnosis for the best treatment and genetic counselling; we also showed the importance of working in network in these diseases of low prevalence and we discuss about the fundamental role of parents associations in promoting public health politics for affected people.
Desde la década de los 80, las enfermedades raras han empezado a tener un lugar destacado en los programas de salud y en la opinión pública de los países desarrollados. Las enfermedades raras son condiciones de morbilidad caracterizadas por su baja prevalencia, pero también son condiciones poco conocidas, poco estudiadas y en general muchas de ellas sin tratamiento específico. Se les conoce también como “enfermedades huérfanas” por ser poco “atractivas” como foco de investigación o estudios clínicos.
Si bien no existe una definición única para el término “Enfermedad Rara”, todas las definiciones se basan en la frecuencia con que se presentan y algunas incluyen además elementos como la gravedad de las manifestaciones y/o la disponibilidad de tratamiento. Las definiciones utilizadas en la literatura médica y los diferentes programas nacionales de salud fluctúan entre prevalencias de 1:1000 a 1:200.000 habs.
En Estados Unidos, el Acta de Enfermedades Raras de 2002, define una enfermedad rara estrictamente de acuerdo a su prevalencia y específicamente dice que se refiere a cualquier enfermedad o condición que afecte a menos de 200.000 personas en los Estados Unidos, lo que equivale a alrededor de 1:500 personas 1. Esta definición es similar a la realizada en el Acta de Drogas Huérfanas de 1983, una ley federal escrita para estimular la investigación en enfermedades raras y su tratamiento 2.
En Japón, la definición legal señala que una enfermedad rara es aquella que afecta a menos de 50.000 pacientes, lo que equivale a 1:2.500 personas 3.
La Unión Europea (UE) define como enfermedad rara a aquella, de origen genético o adquirido, con peligro de muerte o invalidez crónica y cuya prevalencia en la población general sea inferior a 1 en 2.000 individuos. Se excluyen de esta definición enfermedades que son estadísticamente raras, pero que no producen compromiso vital ni son crónicamente debilitantes 4.
PrevalenciaEl impacto de las enfermedades raras en la morbimortalidad es más evidente si se considera su prevalencia (número de personas afectadas por la enfermedad) que la incidencia (número de casos nuevos diagnosticados por año). El Global Gene Project, estima que existen más de 300 millones de personas en el mundo afectadas por una enfermedad rara 5.
La Organización Europea para la Enfermedades Raras (EURODIS) estima que existen entre 6.000 y 8.000 enfermedades raras y que entre el 6 y el 8% de la población de la Comunidad Europea sufre de alguna de estas afecciones 6. Por otra parte, la prevalencia de las enfermedades raras puede variar en diferentes poblaciones, de manera que puede ser rara en algunas y más frecuente en otras; esto se ve con especial frecuencia en las enfermedades raras de origen genético en las que puede haber efecto de un gen fundador en una población específica.
Por otra parte, dado que las enfermedades raras no constituyen un grupo nosológico reconocido si no que son un grupo heterogéneo con un factor común que es la baja prevalencia, es obvio que este grupo puede incluir un número no especificado de patologías que serán definidas como raras de acuerdo al valor de corte estimado como frecuencia en la población.
En Chile, para una población de 17 millones de habitantes, y considerando la frecuencia de 6-8% determinada por la Comunidad Europea, debiéramos esperar más de 1.000.000 de afectados.
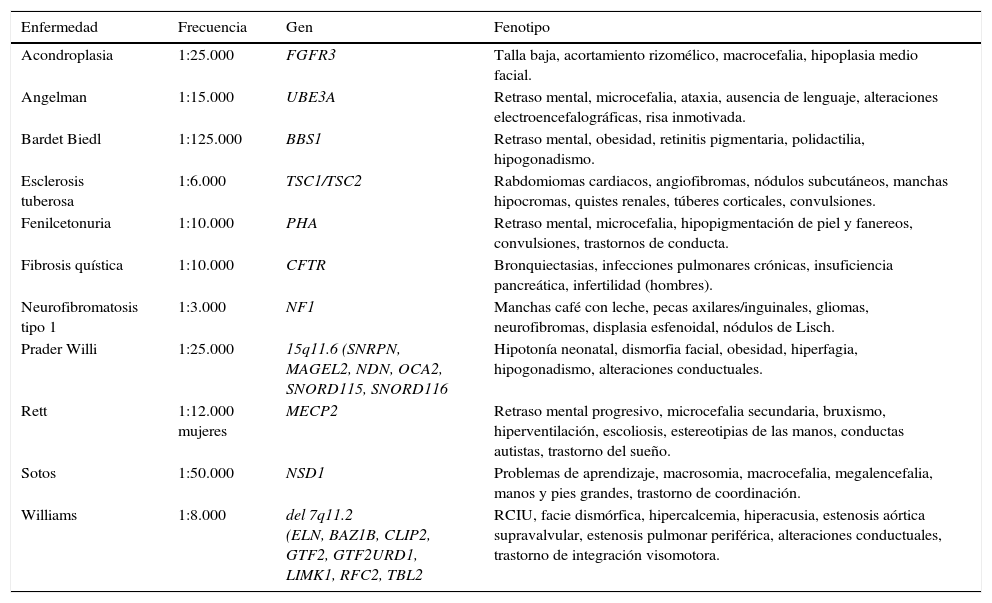
En la Tabla 1 se muestran algunas de las enfermedades raras de mayor prevalencia y algunas de sus características fenotípicas y bases moleculares.
. Algunas enfermedades raras “frecuentes”
| Enfermedad | Frecuencia | Gen | Fenotipo |
|---|---|---|---|
| Acondroplasia | 1:25.000 | FGFR3 | Talla baja, acortamiento rizomélico, macrocefalia, hipoplasia medio facial. |
| Angelman | 1:15.000 | UBE3A | Retraso mental, microcefalia, ataxia, ausencia de lenguaje, alteraciones electroencefalográficas, risa inmotivada. |
| Bardet Biedl | 1:125.000 | BBS1 | Retraso mental, obesidad, retinitis pigmentaria, polidactilia, hipogonadismo. |
| Esclerosis tuberosa | 1:6.000 | TSC1/TSC2 | Rabdomiomas cardiacos, angiofibromas, nódulos subcutáneos, manchas hipocromas, quistes renales, túberes corticales, convulsiones. |
| Fenilcetonuria | 1:10.000 | PHA | Retraso mental, microcefalia, hipopigmentación de piel y fanereos, convulsiones, trastornos de conducta. |
| Fibrosis quística | 1:10.000 | CFTR | Bronquiectasias, infecciones pulmonares crónicas, insuficiencia pancreática, infertilidad (hombres). |
| Neurofibromatosis tipo 1 | 1:3.000 | NF1 | Manchas café con leche, pecas axilares/inguinales, gliomas, neurofibromas, displasia esfenoidal, nódulos de Lisch. |
| Prader Willi | 1:25.000 | 15q11.6 (SNRPN, MAGEL2, NDN, OCA2, SNORD115, SNORD116 | Hipotonía neonatal, dismorfia facial, obesidad, hiperfagia, hipogonadismo, alteraciones conductuales. |
| Rett | 1:12.000 mujeres | MECP2 | Retraso mental progresivo, microcefalia secundaria, bruxismo, hiperventilación, escoliosis, estereotipias de las manos, conductas autistas, trastorno del sueño. |
| Sotos | 1:50.000 | NSD1 | Problemas de aprendizaje, macrosomia, macrocefalia, megalencefalia, manos y pies grandes, trastorno de coordinación. |
| Williams | 1:8.000 | del 7q11.2 (ELN, BAZ1B, CLIP2, GTF2, GTF2URD1, LIMK1, RFC2, TBL2 | RCIU, facie dismórfica, hipercalcemia, hiperacusia, estenosis aórtica supravalvular, estenosis pulmonar periférica, alteraciones conductuales, trastorno de integración visomotora. |
Se estima que alrededor de 80% de las enfermedades raras son de origen genético y con menos frecuencia son el resultado de enfermedades infecciosas, inmunológicas, degenerativas o proliferativas; y además un número muy minoritario de ellas, no más de 400, disponen de tratamiento 7. Esto determina que la gran mayoría sean enfermedades crónicas e incurables; de hecho se considera que las enfermedades raras son responsables de un 25% de las enfermedades crónicas 8.
Desde el punto de vista del manejo médico, las enfermedades raras se caracterizan por el gran número y la diversidad de afecciones y síntomas, que no solo varían de afección en afección, si no que también pueden variar dentro de la misma afección. La misma condición puede presentarse con manifestaciones clínicas muy diferentes entre una persona afectada y otra. Además, para muchas afecciones, existe también una gran variedad de subtipos dentro de la misma enfermedad. Las enfermedades raras pueden afectar a los pacientes tanto en su capacidad física como en sus habilidades mentales, conducta y capacidad sensorial, pudiendo además coexistir diferentes discapacidades en un mismo individuo.
Estas enfermedades representan afecciones graves y debilitantes para el 65% de los afectados. Sus manifestaciones comienzan tempranamente en la vida, estimándose que hasta en dos tercios de los pacientes los síntomas comienzan antes de los dos años de vida, aunque pueden aparecer a lo largo de toda la vida. Más de la mitad de los pacientes afectados presenta durante su vida deficiencia motora, sensorial o intelectual, con dolor crónico reconocible hasta en el 20% de los afectados y 30% de los afectados por enfermedades raras fallece antes de los cinco años 6.
La baja prevalencia individual de las enfermedades raras determina un menor conocimiento de ellas por parte del equipo médico, lo que produce diagnósticos más tardíos y poco específicos; esto se asocia a mayores costos y perjudica aún más la calidad de vida de los pacientes y sus familias, quienes habitualmente deben consultar varias opiniones de especialistas antes de llegar a un diagnóstico preciso. Estudios realizados en Estados Unidos reportan que pacientes con estas afecciones pueden visitar entre 6 y 13 médicos antes de lograr un diagnóstico definitivo y la demora en su diagnóstico frecuentemente es mayor a cinco años desde el inicio de los síntomas 9. El diagnóstico etiológico, certero y precoz, es fundamental para el adecuado manejo, para la prevención de complicaciones y para el asesoramiento preconcepcional de las familias en riesgo.
Si bien no todas las patologías poco frecuentes son congénitas (manifestaciones desde el nacimiento), la mayoría de ellas (75-80%) como se mencionó, son de origen genético y pueden ser heredadas, lo que sin duda aumenta su impacto e implica la necesidad de entregar asesoramiento genético al afectado y a su familia.
El tener una enfermedad poco frecuente, además de las circunstancias específicas de cada patología, implica para los afectados otros problemas: desconocimiento acerca del origen de la enfermedad, desconcierto y desorientación en el momento del diagnóstico; muchas veces rechazo social y pérdida de la autoestima; desinformación sobre cuidados, posibles complicaciones, tratamientos y ayudas técnicas que puedan facilitar su vida; aislamiento y falta de contacto con otras personas afectadas; desinformación sobre especialistas o centros médicos de referencia; falta de protocolos de estudio y seguimiento; falta de ayuda económica; falta de reconocimiento en políticas y sistemas de salud; falta de medicamentos específicos para tratar la enfermedad; también se debe considerar la falta de cobertura legal para fomentar la investigación sobre genética, ensayos clínicos y nuevos tratamientos.
Por otra parte, estas patologías afectan varios sistemas y su manejo implica la participación de distintos especialistas. Sin embargo, son pocos los centros que ofrecen atención integral y multidisciplinaria de manera coordinada. Las atenciones médicas suelen ser frecuentes y los exámenes numerosos cuando los pacientes están en busca de diagnóstico. Este alto costo se suma a la necesidad de tratamientos específicos, cuidados especiales y rehabilitación programada que la gran mayoría de ellos requiere durante toda su vida. Estas prestaciones en nuestro medio no se encuentran organizadas en paquetes o programas y muchas de ellas carecen de cobertura por parte de los seguros de salud habituales, lo que determina abandono de tratamientos y falta de seguimiento. A pesar del gran número de pacientes diagnosticados al año con este tipo de enfermedades, el número escaso de pacientes portadores de enfermedades específicas ha hecho difícil en nuestro país y en el mundo, el logro de beneficios o compensaciones gubernamentales. Son múltiples las asociaciones de familiares que se agrupan en torno a pacientes con un diagnóstico puntual y que reclaman la atención del Estado. Históricamente, ellos han conseguido logros parciales. En Chile específicamente las agrupaciones de pacientes y familiares han sido clave para conseguir la categoría GES (Garantías Explicitas en Salud) para la Enfermedad de Gaucher y su tratamiento (incidencia 1 por 60.000 nacidos vivos) o el plan piloto para diagnóstico y tratamiento de la Tirosinemia (incidencia 1 en 100.000 nacidos vivos); es evidente que ambos ejemplos corresponden a soluciones puntuales o transitorias, que no resuelven el problema global de los pacientes con enfermedades raras.
DiagnósticoEl manejo y el asesoramiento genético de pacientes afectados de enfermedades raras requieren de un diagnóstico etiológico certero. Este diagnóstico de precisión, la gran mayoría de las veces se basa en un estudio molecular, ya sea del gen específico asociado a la enfermedad en cuestión, o de paneles que incluyen los diferentes genes que eventualmente puedan ser responsables de un determinado fenotipo y que permitan identificar con exactitud la alteración molecular subyacente.
Como se ha señalado, las enfermedades raras son patologías muy heterogéneas que involucran diferentes órganos y sistemas, y de esta forma se relacionan con todas las especialidades y subespecialidades médicas. Si se considera que estas enfermedades se relacionan con múltiples genes y con múltiples mutaciones responsables de la afección, y también con otras mutaciones y polimorfismos que regulan su expresión, es posible entender la gran complejidad, desde el punto de vista tecnológico, asociada al estudio de las alteraciones moleculares responsables de las diferentes patologías.
El enfrentamiento diagnóstico desde el punto de vista molecular en las enfermedades raras parte por la identificación de las mutaciones patogénicas más frecuentes, mediante secuenciación Sanger, del gen preferentemente asociado a la enfermedad en cuestión, Si se encuentra la mutación, se confirma el diagnóstico; si no se encuentra, se debe continuar con la secuenciación de las otras mutaciones del mismo gen y según sea necesario, con las secuenciación de otros genes que hayan sido asociados a la enfermedad en estudio.
Los avances tecnológicos en biología molecular permiten que día a día aumente la disponibilidad de estudios moleculares tendientes a lograr diagnósticos de precisión en las diferentes patologías humanas. Como lo hemos señalado, este diagnóstico de precisión es la base de la medicina personalizada y esto es de especial importancia en las enfermedades de baja prevalencia.
Un detalle de los estudios moleculares disponibles, de las técnicas de estudio, su utilidad específica y su disponibilidad a nivel clínico se presentará en otro de los artículos de esta revista.
Asesoramiento genéticoSe considera el asesoramiento genético como un proceso de comunicación que pretende entregar al individuo y a las familias que tienen una enfermedad genética o que están a riesgo de tenerla, información en relación con la afección. Información que permitirá a las personas en riesgo, decidir sus alternativas reproductivas. Se trata de un proceso complejo que involucra una gran cantidad de variables que comprometen al individuo afectado, su familia y la afección propiamente tal.
La Academia Americana de Medicina ha definido al asesoramiento genético como: El proceso de comunicación entre un paciente (consultante) y un médico (consejero o asesor) que trata de los múltiples problemas humanos asociados al riesgo de ocurrencia y recurrencia de una enfermedad genética en una familia.
Dado que alrededor del 80% de las enfermedades raras son de origen genético, el asesoramiento genético es un punto de importancia mayor en el manejo de estos pacientes y sus familias. También en esto, es fundamental el diagnóstico de precisión, ya que conocer la alteración molecular responsable de la afección permitirá identificar a otros individuos en riesgo de presentar la enfermedad en cada una de las familias de los pacientes afectados, determinando las alternativas reproductivas para la familia y colaborando en la resolución de los problemas asociados al hecho de tener o estar en riesgo de tener una enfermedad rara (agrupaciones de padres, asistencia social, instituciones de apoyo, obtención de extremidades protésicas, dietas especiales, entre otros).
La importancia del trabajo en redesSi bien por definición, las enfermedades raras son aquellas con una prevalencia menor a 1:2.000 individuos, en general se trata de afecciones con prevalencias aún menores y que en algunas patologías pueden llegar a ser inferiores a 1:1.000.000. Considerando esto, es fácil entender que para tener una casuística que permita conocer el fenotipo de la afección, su evolución, variaciones y complicaciones, es necesario el registro y análisis a través de redes que permitan aumentar el número de casos evaluados 10.
Por ejemplo, en Chile, con una tasa de natalidad de 250.000 recién nacidos por año, si quisiéramos tener una serie de 100 casos para evaluar una patología con una frecuencia de 1:50.000, se requeriría 20 años de registro acucioso que nos asegure además que todos los casos nuevos han sido diagnosticados, para lograrlo 11. De aquí la importancia de sistemas de registro en red como el ECLAMC (Estudio Colaborativo Latinoamericano de Malformaciones Congénitas) que agrupa a 35 hospitales de Chile, Argentina, Bolivia, Brasil, Perú, Venezuela y Colombia 12 o el International Clearinghouse for Birth Defects Surveillance and Research que incluye 43 programas de registro de 36 países con un total de 4.000.000 de nacimientos por año 13. Sólo a través de estas redes que permiten análisis colaborativos, es posible concentrar un número de casos suficiente que permita conocer la evolución natural de la afección y eventualmente desarrollar estudios tendientes a encontrar alternativas terapéuticas. Es sabido que los pacientes afectados por enfermedades raras sufren un doble castigo: presentar una enfermedad severa y ser insuficientemente reconocidos, diagnosticados y tratados.
En general, existe un alto porcentaje de sub diagnóstico debido a la baja sospecha clínica. Como cada una de estas enfermedades por separado es muy infrecuente, un médico general rara vez evaluará más de un paciente con la misma afección durante todo el ejercicio de su profesión. Es un hecho que el diagnóstico precoz mejora el pronóstico de pacientes portadores de enfermedades raras, más aún, un porcentaje importante de estas enfermedades son susceptibles de ser diagnosticadas en etapa prenatal, lo que permite en algunos casos el tratamiento in útero, y en todos, preparar a la familia y al equipo médico para el manejo adecuado en el periodo neonatal.
Las agrupaciones de pacientes y familiasEs indudable que las agrupaciones de pacientes, padres y familiares han ido adquiriendo un rol fundamental en el enfrentamiento de la comunidad con las autoridades de salud. Esto es especialmente evidente en el caso de las enfermedades raras. La baja prevalencia los obliga a unir fuerzas y a empoderarse para enfrentar los diferentes desafíos asociados a vivir con alguna de estas afecciones.
El Banco Mundial define como empoderamiento “el proceso de aumentar la capacidad de un individuo o de grupos de individuos de elegir y de transformar las elecciones en acciones y resultados” 14. La Organización Mundial de la Salud ha descrito el empoderamiento como un “prerrequisito para la salud” y como “una asociación proactiva y una estrategia de autocuidado del paciente tendiente a mejorar los resultados de salud y la calidad de vida de los enfermos crónicos” 15.
Definidas así, las agrupaciones de pacientes, padres y familiares son una necesidad para los pacientes con enfermedades raras. Esto porque sus afecciones son crónicas, difíciles de manejar y tan infrecuentes que son imperativos los esfuerzos coordinados para lograr cambios y ser escuchados y considerados por los investigadores, la comunidad médica y los encargados de las políticas de salud 16. Las organizaciones de pacientes tienen roles a diferentes niveles, desde el financiamiento de la investigación hasta los aspectos regulatorios de la comercialización de medicamentos, incluyendo la producción de material educativo confiable, el diseño de políticas públicas y el estudio de proyectos. En Estados Unidos, el concepto de enfermedades raras y drogas huérfanas fue establecido en 1983 (2) por una coalición de agrupaciones de pacientes que incluyó a la comunidad académica, las agencias estatales reguladoras y la industria farmacéutica. Posteriormente, otros países han ido desarrollando entidades similares. En Chile, durante los últimos años se ha ido incrementando el interés por este tipo de afecciones y en general por las afecciones con alto costo y está próximo a legislarse en relación a su manejo 17.
En resumenMás allá de la gran diversidad de afecciones, los pacientes con enfermedades raras y sus familias están confrontados a un gran número de dificultades similares, las que surgen directamente de la baja frecuencia de estas afecciones:
- •
Falta de acceso a un diagnóstico correcto: el periodo entre el inicio de los síntomas y el diagnóstico certero involucra un retraso inaceptable y de alto riesgo; así como un diagnóstico equívoco puede determinar tratamientos inadecuados.
- •
Falta de información: tanto en relación a la enfermedad en sí, como en relación a lugares donde obtener apoyo, incluyendo el no ser referidos a profesionales calificados.
- •
Falta de conocimiento científico: esto se traduce en dificultades para el desarrollo de herramientas terapéuticas, falta de definición de estrategias terapéuticas y en déficit de productos terapéuticos ya sea medicamentos o accesorios médicos.
- •
Consecuencias sociales: el vivir con una enfermedad rara tiene implicancias en todos los ámbitos: escolaridad, trabajo, actividades de recreación, vida afectiva. Puede ser causa de estigmatización, aislamiento, exclusión de actividades sociales, discriminación en la suscripción de seguros (de salud, de viaje, de vida) y a menudo una reducción de las oportunidades laborales.
- •
Falta de cuidados de salud adecuados y de calidad: los pacientes con enfermedades raras requieren, además de los cuidados médicos, apoyo en múltiples esferas con profesionales expertos que incluyen: kinesiólogos, terapeutas ocupacionales, psicólogos, nutricionistas, fonoaudiólogos, etc. Los pacientes pueden vivir por muchos años en condiciones precarias sin atención médica competente, incluyendo las terapias de rehabilitación. Muchas veces permanecen excluidos de los sistemas de salud aun después de establecido el diagnóstico.
- •
Alto costo de los pocos medicamentos existentes: el gasto adicional de afrontar la enfermedad, en términos humanos y de ayudas técnicas, combinado con la falta de beneficios sociales y de reembolso, produce un empobrecimiento global de la familia y aumenta dramáticamente la inequidad de accesos a los cuidados generales requeridos por los pacientes con enfermedades raras.
- •
Inequidad en la disponibilidad de tratamiento y cuidado: los tratamientos innovadores están a menudo disponibles en forma desigual, debido al alto costo, la poca disponibilidad de reembolso, la falta de experiencia de los médicos tratantes y la falta de recomendaciones de tratamientos de consenso.
Orphanet es una organización europea, que se define como un portal para las enfermedades raras y las drogas huérfanas. En su página web entrega información en relación a las diferentes enfermedades raras descritas, los genes involucrados en cada una, disponibilidad de herramientas diagnósticas y manejo de emergencias; también dispone de un catálogo de drogas huérfanas, un directorio de laboratorios que disponen de diagnóstico molecular y un directorio de centros expertos 18. En relación a las propuestas concretas para mejorar la situación de estos pacientes y su familias, ellos proponen:
Implementar un enfrentamiento completo para las enfermedades raras.
Desarrollar políticas de salud pública adecuadas.
Aumentar la cooperación internacional en la investigación científica.
Aumentar y compartir el conocimiento científico de todas las enfermedades raras, no solo de las más “frecuentes”.
Desarrollar nuevos procedimientos diagnósticos y terapéuticos.
Lograr una concientización pública en relación con las enfermedades raras.
Facilitar el trabajo en redes de los grupos de pacientes para que puedan compartir sus experiencias.
Apoyar a los pacientes más aislados y a sus familias para crear nuevas agrupaciones o comunidades de pacientes.
Entregar información completa y de calidad, a toda la comunidad de pacientes con enfermedades raras.
La autora declara no tener conflictos de interés, en relación a este artículo.